Атомы металлов могут превратиться только в положительно заряженные ионы
Обновлено: 17.05.2024
Теорию ионной связи предложил в 1916г. немецкий ученый В. Коссель. Эта теория объясняет образование связей между атомами типичных металлов и атомамитипичных неметаллов:CsF, CsCl, NaCl, KF, KCl, Na2O и др.
Согласно этой теории, при образовании ионной связи атомы типичных металлов отдают электроны, а атомы типичных неметаллов принимают электроны.
В результате этих процессов атомы металлов превращаются в положительно заряженные частицы, которые называются положительными ионами или катионами; а атомы неметаллов превращаются в отрицательные ионы — анионы. Заряд катиона равен числу отданных электронов.
Атомы металлов отдают электроны внешнего слоя, а образующиеся ионы имеют завершенные электронные структуры (предвнешнего электронного слоя).
Величина отрицательного заряда аниона равна числу принятых электронов.
Атомы неметаллов принимают такое количество электронов, какое им необходимо для завершения электронного октета (внешнего электронного слоя).
Например: общая схема образования молекулы NaCl из атомов Na и С1: Na°-le = Na +1 Образование ионов
Na +1 + Сl - = Nа + Сl -
Na°+ Сl°= Nа + Сl - Соединение ионов
· Связь между ионами называется ионной связью.
Соединения, которые состоят из ионов, называются ионными соединениями.
Алгебраическая сумма зарядов всех ионов в молекуле ионного соединения должна быть равна нулю,потому что любая молекула является электронейтральной частицей.
Резкой границы между ионной и ковалентнои связями не существует. Ионную связь можно рассматривать как крайний случай полярной ковалентнои связи, при образовании которой общая электронная пара полностьюсмещается к атому с большей электроотрицательностью.
Атомы большинства типичных металлов на внешнем электронном слое имеют небольшое число электронов (как правило, от 1 до 3); эти электроны называются валентными. В атомах металлов прочность связи валентных электронов с ядром невысокая, то есть атомы обладают низкой энергией ионизации. Это обусловливает легкость потери валентных электронов ч превращения атомов металла в положительно заряженные ионы (катионы):
В кристаллической структуре металла валентные электроны обладают способностью легко перемещаться от одного атома к другому, что приводит к обобществлению электронов всеми соседними атомами. Упрощенно строение кристалла металла представляется следующим образом: в узлах кристаллической решетки находятся ионы Ме п+ и атомы Ме°, а между ними относительно свободно перемещаются валентные электроны, осуществляя связь между всеми атомами и ионами металла (рис. 3). Это особый тип химической связи, называемой металлической.
· Металлическая связь — связь между атомами и ионами металлов в кристаллической решетке, осуществляемая обобществленными валентными электронами.
Благодаря этому типу химической связи металлы обладают определенным комплексом физических и химических свойств, отличающим их от неметаллов.
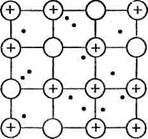
Рис. 3. Схема кристаллической решетки металлов.
Прочность металлической связи обеспечивает устойчивость кристаллической решетки и пластичность металлов (способность подвергаться разнообразной обработке без разрушения). Свободное передвижение валентных электронов позволяет металлам хорошо проводить электрический ток и тепло. Способность отражать световые волны (т.е. металлический блеск) также объясняется строением кристаллической решетки металла.
Таким образом, наиболее характерными физическими свойствами металлов в зависимости от наличия металлической связи являются:
■металлический блеск и непрозрачность;
■пластичность, ковкость, плавкость;
■высокие электро- и теплопроводность; и склонность к образованию сплавов.
Верны ли следующие суждения о закономерностях изменения свойств атомов в периодической системе?
Верны ли следующие суждения о закономерностях изменения свойств атомов в периодической системе?
А. - В пределах периода с уменьшением зарядов атомных ядер металлические свойства усиливаются.
Б. - В пределах главной подгруппы с уменьшением зарядов атомных ядер радиус атома увеличивается.
1) Верно только А.
2) Верны оба суждения.
3) Верно только Б.
4) Оба суждения неверны.

Верно только первое.

Какие из утверждений являются верными?
Какие из утверждений являются верными?
А) С увеличением заряда ядра атома радиус атомов галогенов увеличивается ; Б) С уменьшением заряда ядра атома электроотрицательность галогенов увеличивается.
1) верно только А 2) верно только Б 3) оба утверждения верны 4) оба утверждения неверны.
Верны ли следующие суждения о свойствах веществ?
Верны ли следующие суждения о свойствах веществ?
А. Уксусная кислота – слабая кислота.
Б. При окислении альдегидов получаются карбоновые кислоты.
1) верно только суждение А 2) верно только суждение Б
3) оба суждения верны 4) оба суждения неверны.

Верны ли следующие суждения о строении атомов элементов металлов?
Верны ли следующие суждения о строении атомов элементов металлов?
А. Во внешнем электронном слое атомов большинства химических элементов металлов находится небольшое количество электроннов.
Б. Атомы металлов имеют сравнительно большие радиусы * верно только А верно только Б оба суждения верны оба суждения неверны.

1. Верны ли следующие суждения?
1. Верны ли следующие суждения?
А. Радиус атомов элементов 2 - го периода с увеличением заряда ядра не изменяется.
Б. Радиус атомов элементов 2 - го периода с увеличением заряда ядра увеличивается.
1) верно только А 2) верно только Б 3) верны оба суждения 4) оба суждения не верны.
Вещества, которые взаимодействуют с кальцием : 1)СО2 2)Н2 3)HCl 4)H2O 5)O2 6)NaOH.

Верны ли следущие суждения о свойствах элементов подгруппы кислорода?
Верны ли следущие суждения о свойствах элементов подгруппы кислорода?
А . При взаимодейсвтии с фосфором кислород проявляет восстановительные свойства.
Б. Минимальная степень окисления атомов 6А группы равна - 2.
Верны ли суждения о металлах?
Верны ли суждения о металлах?
А. в пределах одного периода с увеличением порядковых номеров элементов их металлические свойства усиливаются
Атомы металлов могут превратиться только в положительно заряженные ионы.
Верны ли следующие суждения о неметаллах : А?
Верны ли следующие суждения о неметаллах : А.
В периоде с увеличением зарядов атомных ядер происходит усиление неметаллических свойств элементов.
Б. В главной подгруппе с увеличением зарядов атомных ядер происходит ослабление кислотных свойств гидроксидов.
Верны ли следующие суждения?
Верны ли следующие суждения?
А) Химический элемент - это совокупность атомов с одинаковым зарядом ядра
Б) Изотопы - этоатомы одного элемента, имеющие разные массовые числа.
А) верно только А, б) верно только Б,
в) верны оба суждения, г) оба суждения неверны.

Верны ли следующие суждения о свойствах жиров?
Верны ли следующие суждения о свойствах жиров?
1 – Жиры подвергаются гидролизу 2 – Жиры окисляются кислородом А) верно только 1 Б) верно только 2 В) верны оба суждения Г) оба суждения неверны.
Я про алюминийАлюминий – легкий, прочный и пластичный металл. Это один из самых востребованных металлов, и по темпам роста потребления он давно и с большим отрывом оставил позади сталь, никель, медь и цинк. Алюминий без преувеличений можно назвать ..

Тому що рН показує ступінь концентрації катіонів гідрогену у воді, що є дуже важливим для косметики.

1. дано N(NH3) = 4. 816 * 10 ^ 23 - - - - - - - - - - - - - - - - - - - - - - - - - - - - - V(NH3) - ? N(NH3) / N(A) = V(NH3) / Vm V(NH3) = N(NH3) * Vm / N(A) = 4. 816 * 10 ^ 23 * 22. 4 / 6. 02 * 10 ^ 23 = 15. 58 L ответ 15. 58 л 2) дано m(O2)..

Соотвественно правильным ответом будет являться : 4) KCl ; 5) AgCl ; 6) NH4Cl.
Дано W(O) = 47 % - - - - - - - - - - - - - - - - E - ? Е - это неизвестный элемент W(O) = Ar(O) * n / M(X2O3) * 100% 47% = 16 * 3 / 2x + 48 * 100% 94x + 2256 = 4800 X = 27 - это алюминий Al2O3 ответ алюминий.

Напиши нормально не понятно или сфоткай.
В SO3 32 / (32 + 3 * 16) = 0, 4 или 40 %.
Реакции есть на фотографии.
4HCl + MnO2 = MnCl2 + Cl2 + 2H2O соляная кислота отдаёт в свободном виде половину имеющегося хлора. M(Cl общ. ) = 1000 * 0, 365 * 0, 9726 = 355 г масса выделившегося хлора = 355 / 2 = 177, 5 г.
Типы химической реакции соединение, разложение замещение.
© 2000-2022. При полном или частичном использовании материалов ссылка обязательна. 16+
Сайт защищён технологией reCAPTCHA, к которой применяются Политика конфиденциальности и Условия использования от Google.
А - нет они ослабевают
Б - да все металлы имеют положительный заряд.
Какое утверждение верно а) все металлы пластичны б) при увеличение порядкового номера элемента в периоде металлические свойства элементов увеличиваются?
Какое утверждение верно а) все металлы пластичны б) при увеличение порядкового номера элемента в периоде металлические свойства элементов увеличиваются.
1. в периодах с увеличением порядкового номера металлические свойства (восстановительные) свойства ?
1. в периодах с увеличением порядкового номера металлические свойства (восстановительные) свойства .
, а неметаллические (окислительные) - .
Число электронных слоев в пределах периода у всех элементов .
; 2. в группах с увеличением порядкового номера элемента металлические свойства(восстановительные) .
, потому что : - число электронов на внешнем электроном уровне .
) ; - число электронных слоев .
Верны ли следующие высказывания?
Верны ли следующие высказывания?
А. В периоде с увеличением порядкового номера элемента основные свойства гидроксидов усиливаются.
Б. В периоде с увеличением порядкового номера элемента основные свойства гидроксидов ослабевают.
1) верно только А 3) верно только Б 2) верны оба суждения 4) оба суждения не верны.
Как изменяется металлические и неметаллические свойства атомов элементов в периодах с увеличением порядкового номера?
Как изменяется металлические и неметаллические свойства атомов элементов в периодах с увеличением порядкового номера?
Как изменяется металлические и неметаллические свойства атомов элементов в группах с увеличением порядкового номера?
В главной подгруппе неметаллические свойства атомов элементов с увеличением порядкового номера усиливается В главной подгруппе неметаллические свойства атомов элементов с увеличением порядкового номер?
В главной подгруппе неметаллические свойства атомов элементов с увеличением порядкового номера усиливается В главной подгруппе неметаллические свойства атомов элементов с увеличением порядкового номера ослабевает Какой из них правильный?
Помогите решить А?
Помогите решить А.
В периоде металлические свойства атомов элементов с увеличением порядкового номера усиливаются.
Б. В периоде металлические свойства атомов элементов с увеличением порядкового номера ослабевают.
1) верно только А 3) верно только Б 2) верны оба суждения 4) оба суждения не верны .
Соединениями с ионной связью являются : 1) NH3 3) BaCl2 5) ZnS 2) CO2 4) Al I3 6) O2.
Как изменяются свойства атомов элементов в периодах увеличение порядкового номера?
Как изменяются свойства атомов элементов в периодах увеличение порядкового номера.
Верны ли следующие утверждения В : А)периоде окислительные свойства атомов элементов с увеличением порядкового номера усиливаются Б)в периоде окислительные свойства атомов элементов с увеличением поря?
Верны ли следующие утверждения В : А)периоде окислительные свойства атомов элементов с увеличением порядкового номера усиливаются Б)
в периоде окислительные свойства атомов элементов с увеличением порядкового номера ослабевают.
Срочно, до 40 балловВерны ли следующие высказывания?
Срочно, до 40 баллов
А. В периоде металлические свойства атомов элементов с увеличением порядкового номера усиливаются.
А. В главной подгруппе неметаллические свойства атомов элементов с увеличением порядкового номера усиливаются.
Б. В главной подгруппе неметаллические свойства атомов элементов с увеличением порядкового номера ослабевают.
Верны ли следующие суждения о свойствах этилового спирта?
Верны ли следующие суждения о свойствах этилового спирта?
1 – Этанол взаимодействует с гидроксидом натрия 2 – Этанол имеет гидроксильную функциональную группу А) верно только 1 Б) верно только 2 В) верны оба суждения Г) оба суждения неверны.
Читайте также:
