Белок и тяжелые металлы
Обновлено: 04.10.2024
Введение.
Молоко является ценным пищевым продуктом, так как содержит много ценного по составу и легкоусвояемого белка, важного для нашего организма. Эти сложные молекулы, состоящие из более простых аминокислот, оказались универсальны, из-за чего заняли очень важную роль в жизни организмов: белки являются составляющими клеток, их незаменимой частью, давая им различные и специфичные свойства, дополнительно контролируя всё живое. Такие свойства белок приобретает из-за наличия структур – вторичной, третичной, четвертичной. Данные структуры белковой молекулы непрочные и могут быть легко разрушены воздействием извне. Такое разрушение структуры называется денатурацией.
Денатурация не нарушает порядок аминокислот, но меняет глобальную структуру белка, нарушая стандартную работу белка, изменяя изначальные свойства. Так, белки перестают растворяться, теряют гидрофильность, слипаются в комки. Причин денатурации достаточно много: от изменения температуры, до чрезмерного излучения и концентрации некоторых веществ, например, кислот, солей тяжёлых металлов. Тема денатурации и ее скорости меня очень заинтересовала и я решил сделать учебный проект.
Целями моего проекта можно назвать изучение процесса денатурации белков молока и предположение механизмов воздействия вещества, которое является причиной денатурации белков в каждом отдельном случае.
Для достижения этих целей, я поставил следующие задачи:
· найти в литературе и изучить информацию об особенности белков молока;
· изучить процесс денатурации и его визуальные проявления;
· изучить вещества, вызывающие денатурацию белков, и влияние их концентрации на скорость денатурации (в некоторых случаях);
· предположить механизм воздействия вещества, которое является причиной денатурации белков в каждом отдельном случае;
· проанализировать полученные результаты, сделать выводы.
В качестве объектов исследования я взял пищевое молоко и вещества, способные к денатурации (соли тяжёлых металлов, спирты, кислоты, щелочи), а в качестве предмета исследования – скорость и глубину денатурации белков в зависимости от концентрации и особенностей вещества.
Краткий обзор теоретических сведений о строении и свойствах белков молока.
Белки представляют основу структурных элементов клеток и тканей, состоящие из альфа-аминокислот, соединённых в цепочку пептидной связью. В живых организмах аминокислотный состав белков определяется генетическим кодом, при синтезе в большинстве случаев используется 20 аминокислот. Кроме того, аминокислотные остатки в составе белка часто подвергаются посттрансляционным модификациям, которые могут возникать и до того, как белок начинает выполнять свою функцию, и во время его функционирования в клетке. Часто в живых организмах несколько молекул разных белков образуют сложные комплексы, например фотосинтетический комплекс.
В молоке содержится в среднем 3,5% белков. Наибольшая доля принадлежит казеину (2-4%), содержание молочного альбумина 0,5-1%, молочного глобулина 0,1%, присутствуют также белки оболочек жировых шариков (до 0,01 %).
Как правило, белки достаточно стабильны в тех условиях, в которых они в норме функционируют в организме. Резкое изменение этих условий приводит к денатурации белка.
Денатурацией белка называют любые изменения в его биологической активности и/или физико-химических свойствах, связанные с потерей четвертичной, третичной или вторичной структуры. (рис. 1).
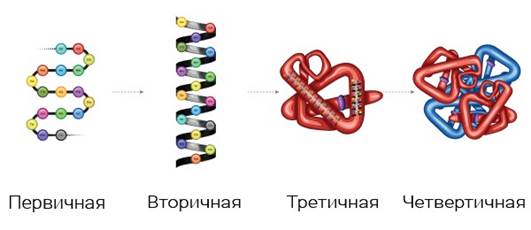
Рис. 1. Структуры белка
Под первичной структурой понимают последовательность аминокислотных остатков в полипептидной цепи. Вторичная структура – упорядоченное свертывание полипептидной цепи в спираль (имеет вид растянутой пружины). Третичная структура – укладка полипептидных цепей в глобулы, возникающая в результате возникновения химических связей (водородных, ионных, дисульфидных) и установления гидрофобных взаимодействий между радикалами аминокислотных остатков.
Четвертичная структура характерна для сложных белков, молекулы которых образованы двумя и более глобулами.
Утрата белковой молекулой своей природной структуры называется денатурацией. Она может возникнуть при воздействии температуры, химических веществ, при нагревании и облучении. Таким образом, денатурация белка может быть вызвана различными относительно мягкими воздействиями, приводящими к нарушению в его молекулах слабых взаимодействий — водородных, ионных связей и гидрофобных контактов, а также к разрыву дисульфидных связей, стабилизирующих нативную структуру белка. При этом нарушаются вторичная, третичная и четвертичная структуры белковых молекул, но не нарушаются ковалентные связи в полипептидной цепи, следовательно, не нарушается первичная структура белка.
В зависимости от природы денатурирующего агента, выделяют:
· механическую (сильное перемешивание или встряхивание),
· физическую (нагревание, охлаждение, облучение, обработка ультразвуком)
· химическую (кислоты и щёлочи, поверхностно-активные вещества, мочевина) денатурацию.
К нарушению различных связей в большинстве белков приводит прежде всего их нагревание до температуры выше 50°С, а также ультрафиолетовое и другие виды высокоэнергетического облучения, что обусловлено усилением колебаний атомов полипептидной цепи. Денатурацию белка способны вызвать даже механические воздействия, например сильное взбалтывание раствора белка.
Денатурация белков также может происходить вследствие какого- либо химического воздействия, например в присутствии некоторых органических растворителей (спирта, ацетона и др.), мочевины, ионов тяжелых металлов и др., а также в условиях экстремальных значений pH среды.
Визуально денатурация выглядит, например, как образование хлопьев, осадка или побеление жидкого и почти прозрачного яичного белка при жарке яиц. В молоке это проявляется уплотнением раствора и образованием комков от свёртывания белков, в том числе хорошо видимых на стенках стеклянной посуды и посредством стеклянной палочки. Этим свойством мы и будем пользоваться для определения влияния различных веществ на степень денатурации белка.
Краткий обзор факторов, влияющих на скорость денатурации
Основными факторами денатурации белков являются:
2. Специфичное воздействие спиртов;
3. Специфичное воздействие ионов тяжёлых металлов;
4. Изменение температуры (рассматриваться не будет)
5. Излучение и ионизация (рассматриваться не будет), и некоторые другие.
Данные факторы делятся на группы механического, физического и химического воздействия, а так как мой проект по химии, то я буду изучать только химическое воздействие.
Основным химическим фактором, значимым для денатурации белковых молекул, является изменение pH (кислотности). Это значит, что в воде, которая окружает белковые молекулы, возрастает (среда становится сильно кислой) или падает (среда становится сильно щелочной) концентрация ионов H+. Такие изменения в концентрации ионов закономерно изменяют заряд белковых молекул, возникает ионизация кислотных и основных групп. Из-за этого меняется их конфигурация в пространстве, рвутся водородные связи и утрачивается третичная и даже вторичная структуры. Данные изменения происходят достаточно быстро. Кислоты также достаточно активные вещества (окислители), поэтому могут также непосредственно разрывать связи между атомами в достаточно большой молекуле белка.
Щёлочи же в свою очередь легче (менее заметно) влияют на заряды белковых молекул, из-за чего белки практически денатурируют медленнее, они сворачиваются значительно мягче, чем при добавлении кислот.
Органические растворители — спирты, фенолы и другие — также нарушают в белках систему водородных связей в результате конкуренции с функциональными группами белков за их образование. Кроме этого, органические растворители вследствие установления контактов с неполярными радикалами остатков аминокислот нарушают в белках гидрофобные взаимодействия. Высокие концентрации мочевины или органических растворителей вызывают нарушение структуры воды, что также приводит к ослаблению в белковых молекулах гидрофобных взаимодействий. Таким образом, спирт и мочевина осаждает белки из раствора практически сразу же. Белок уплотняется, становятся заметны изменения физических и химических свойств.
Органические вещества, которые не растворяются в воде (гидрофобные молекулы), как правило, не имеют полярности в молекуле (или заряда) и не оказывают влияния на молекулы белка.
Ионы тяжелых металлов в свою очередь тоже имеют заряд и могут присоединяться к белкам, образуя альбуминаты. Однако, из-за большего радиуса чем у лёгких металлов, они меняют электрическое поле белка, заставляя тех образовать так называемые «кластеры» (слипание комков белка). Из-за этого молекулы больше не могут отталкиваться друг от друга, а наоборот притягиваются, что и позволяет им объединяться в довольно большие соединения (сгустки), нарушается растворимость белковых молекул. Степень и скорость денатурации определяется концентрацией ионов тяжелых металлов и степенью диссоциации их солей: малая концентрация солей тяжелых металлов вызывает гелификацию (уплотнение) белков на поверхности, большая концентрация вызывает необратимые глубокие изменения белковых молекул.
Также, некоторые тяжёлые металлы образуют прочную связь с тиольными группами, что также нарушает работу белковых молекул, делает молекулы более тяжелыми, нерастворимыми.
План проведения эксперимента.
Все исследования в рамках данного проекта осуществлялись в школьной лаборатории с соблюдением правил техники безопасности при работе с едкими веществами (кислотами, щелочами), с веществами, являющимися ядами. Опыты с летучими (сильно пахнущими) веществами, а также с концентрированными кислотами проводились с использованием вытяжного шкафа.
План проведения исследования:
1. Для исследования брали по 30 мл молока, 3,2% жирности. Молоко наливали в различные химические стаканы. Подписывали (нумеровали) емкости.
2. В каждую порцию молока наливали по 20 мл растворов различных химических веществ, в том числе:
2.1 10% растворы солей тяжёлых металлов (FeCl3, CuCl2, Pb(CH3COO)2, CdSO4, ZnSO4, BaCl2) и для сравнения 10% растворы солей более легких металлов (Na2CO3, NaCl, Na2S, Na2SO4, CaCl2, NH4Cl, MnSO4, CoSO4, NiSO4, CrCl2)
2.2 98%-100% растворы спиртов (этанол, бутанол) и других органических веществ (гептан, гексан, толуол, глицерин, гликоль).
2.3 концентрированные кислоты 98% растворы серной и азотной кислот, 70% раствор уксусной кислоты, разбавленные кислоты 25%, 10%, 1% растворы кислот (уксусная, серная и азотная кислоты)
2.4. 10% растворы щелочей (KOH, NaOH).
3. Оценивали: степень денатурации сразу после добавления веществ, через 2 часа и через сутки после смешивания. Оценку проводили по характеру сгустка (размешивание стеклянной палочкой), характеру комков и следов на стенках химического стакана, изменению цвета (в некоторых образцах), наличию отделяемой воды (выпадение осадка).
4. Фотографировали полученный результат.
5. Описывали результаты в таблице, формулировали выводы.
Описание результатов по исследованию молока.
Действие на молоко различных кислот, в том числе серной, уксусной, азотной. Результаты представлены в таблице 1. Действие на молоко различных спиртов и иных органических соединений. Результаты представлены в таблице 2. Действие на молоко различных солей. Результаты представлены в таблице 3. Действие на молоко растворов щелочей: гидроксида натрия NaOH, гидроксида калия KOH и гидроксида кальция Ca(OH)2. Результаты представлены в таблице 4.
Воздействие техногенной трансформации экосистем на аккумуляцию тяжелых металлов, содержание белка и липидов в яйцах natrix natrix ( Reptilia, Squamata) Текст научной статьи по специальности «Биологические науки»
Наведено результати досліджень вмісту білку, ліпідів і семи важких металів у яйцях звичайного вужа Natrix natrix (Linnaeus, 1758). Показано, що під впливом техногенної трансформації середовища кількість поживних речовин у яйцях вужів знижується, а вміст важких металів (за виключенням заліза) збільшується. Отримані дані можна використати як індикаторні для оцінки стану популяцій та біогеоценозів.
Похожие темы научных работ по биологическим наукам , автор научной работы — Гассо В. Я.
Микробные пейзажи почвы пойменной липо–ясеневой дубравы под влиянием экскреций лося Alces Alces ( Mammalia, Artiodactyla) при загрязнении почвы кадмием
Значение трофометаболической деятельности млекопитающих в процессе самоочистки почв при антропогенном загрязнении
ГИГИЕНИЧЕСКИЕ АСПЕКТЫ СОДЕРЖАНИЯ СОЕДИНЕНИЙ ТЯЖЕЛЫХ МЕТАЛЛОВ В ПОЧВЕ И ВОДЕ: СОСТОЯНИЕ ПРОБЛЕМЫ, ПЕРСПЕКТИВЫ ДАЛЬНЕЙШИХ ИССЛЕДОВАНИЙ (обзор)
Текст научной работы на тему «Воздействие техногенной трансформации экосистем на аккумуляцию тяжелых металлов, содержание белка и липидов в яйцах natrix natrix ( Reptilia, Squamata)»
ным естественным процессом. Нанесение определенного ущерба млекопитающими всходам и молодой поросли компенсируется средообразующей деятельностью млекопитающих, значительно повышающей эффективность лесовозобновления.
1. Абатуров Б. Д. Биопродукционный процесс в наземных экосистемах. - М.: Наука, 1979. -128 с.
2. Абатуров Б. Д. Особенности трофических взаимодействий млекопитающих в экосистемах пастбищ // Фитофаги в растительном сообществе. - М.: Наука, 1980. - С. 31-42.
3. Абатуров Б. Д. Млекопитающие как компонент экосистемы. - М.: Наука, 1984. - 286 с.
4. Бельгард А. Л. Степное лесоведение. - М.: Лесная промышленность, 1971. - 336 с.
5. Булахов В. Л., Губкин А. А., Мясоедова О. М. Изучение трофики и трофических связей позвоночных животных. - Д.: ДГУ. - 68 с.
6. Воронов А. Г. Методы исследования воздействия позвоночных на растительный покров и почвы // Вопросы экологии. - К., 1962. - Т. 4. - С. 96-98.
7. Новиков Г. А. Полевые исследования по экологии наземных позвоночных. - М.: Наука, 1964. - 502 с.
8. Пахомов А. Е. Биогеоценотическая роль млекопитающих в почвообразовательных процессах степных лесов Украины. - Д.: ДГУ, 1998. - Кн. 2. - 216 с.
9. Свириденко П. А. Питание мышевидных грызунов и их значение в проблеме возобновления леса // Зоол. журнал. - 1940. - Т. 19, № 4. - С. 680-703.
10. Смирнов В. С., Токмакова С. Г. Изменения фитоценоза под влиянием мышевидных грызунов // Тр. Свердловского ин-та экологии растений и животных. - Свердловск, 1971. -Вып. 4. - С. 49-50.
11. Сукачев В. Н. Основные понятия о биогеоценозах и общее направление их изучения // Программа и методика биогеоценотических исследований. - М.: Наука, 1966. - С. 5-21.
12. Формозов А. Н., Воронов А. Г. Деятельность грызунов на пастбищах и сенокосах Западного Казахстана // Ученые записки МГУ. - М.: МГУ, 1939. - Вып. 20. - С. 3-122.
Надійшла до редколегії 02.04.03.
Днепропетровский национальный университет
ВОЗДЕЙСТВИЕ ТЕХНОГЕННОЙ ТРАНСФОРМАЦИИ ЭКОСИСТЕМ НА АККУМУЛЯЦИЮ ТЯЖЕЛЫХ МЕТАЛЛОВ, СОДЕРЖАНИЕ БЕЛКА И ЛИПИДОВ В ЯЙЦАХ NATRIXNATRIX(REPTILIA, SQUAMATA)
Естественные экосистемы под влиянием человеческой деятельности претерпевают значительную трансформацию, выражающуюся в деградации ландшафта, раз-
© Гассо В. Я., 2003 146
рушении мест обитания, снижении биологического разнообразия, патологических и адаптивных физиолого-биохимических реакциях выживших видов и систем на различных уровнях организации.
Техногенное загрязнение среды часто оказывает большее влияние на химическую гетерогенность биосферы, чем естественный биогеохимический круговорот. К числу экотоксикантов, составляющих так называемую «грязную дюжину», относят также и тяжелые металлы: свинец, ртуть, кадмий и другие [7]. Учитывая, что тяжелые металлы входят в состав ферментов, гормонов, пигментов, витаминов, они влияют на связь РНК и ДНК с белками, на синтез протеинов, передачу наследственной информации и многие другие процессы. Изменение их нормального содержания в организме животных приводит к серьезным патологиям [2; 5].
Исследование физиолого-биохимических параметров репродукции представляет интерес для понимания процессов, лежащих в основе адаптации животных к изменяющимся условиям среды, вызванным антропическими факторами, даст возможность прогнозировать состояние их популяций в условиях техногенного стресса. Кроме того, эти параметры, наиболее зависящие от уровня техногенной нагрузки, могут служить биоиндикаторами трансформации экосистем.
Пресмыкающиеся остаются наименее изученным в отношении влияния химического загрязнения среды классом хордовых. К тому же, большая часть работ в этой области посвящена исследованию накопления органических загрязнителей в организме черепах и крокодилов [12; 13; 15]. Вместе с тем, большое внимание в научной среде уделяется разработке системы индикаторов и биомаркеров, не требующих умерщвления животных [14].
Материал и методы исследований
Материал, представленный в данной работе, был собран в 1991-1996 гг. Беременных самок обыкновенного ужа Natrix natrix (Linnaeus, 1758) отлавливали вручную на территории Днепровско-Орельского природного заповедника и на участке поступления промышленных сточных вод металлургических и химических предприятий г. Днепродзержинска в устье р. Коноплянка (полуостров Гречаный). В условиях лаборатории от самок были получены яйца, в которых было проанализировано содержание белка, общих липидов и тяжелых металлов: железа, меди, марганца, цинка, никеля, свинца и кадмия.
Количество белка определялось спектрофотометрическим методом с использованием биуретового реактива [6], основанным на образовании окрашенного в фиолетовый цвет комплекса пептидных связей с ионами двухвалентной меди в щелочной среде. Для этого к 4 мл щелочного раствора, содержащего пробу белка (концентрация щелочи 3 %) добавляют 0,2 мл раствора Бенедикта. Раствор фотометрируют на двухлучевом спектрофотометре «Спекорд М-40» при длине волны 330 нм, предварительно приготовив стандартный раствор белка (яичный альбумин). Количественное определение общих липидов проводилось по методу Кабара [3]. Липиды экстрагировали смесью хлороформ-метанол в соотношении 2 : 1. К 0,1 мл пробы добавляли 3 мл концентрированной H2SO4 и выдерживали на водяной бане 15 мин при температуре +100°С. Интенсивность поглощения растворов при длине волны 350 нм определяли спектрофотометрически после охлаждения. Полученные данные выражаем в процентах от влажной массы (в.м.).
Для определения содержания тяжелых металлов яйца ужей взвешивались с точностью до 0,001 г. Далее они маркировались и помещались в сушильный шкаф, где высушивались при температуре +105°С до абсолютно сухого веса. В дальнейшем,
навеска помещалась в муфельную печь в предварительно взвешенном тигле на 48 часов при постепенном повышении температуры до +450°С до полного озоления. Зола растиралась в ступке, помещалась в тефлоновый стакан и смачивалась несколькими каплями дистиллированной воды. Затем прибавляли по 5 мл концентрированной азотной кислоты, и проба перемешивалась. После охлаждения содержимое стакана помещали в кварцевый тигель, который ставили на песчаную баню. Жидкость упаривали до образования влажных солей. Затем прибавляли 10-15 мл азотной кислоты (1 : 100) и вновь нагревали на песчаной бане до растворения солей. После этого пробу фильтровали через плотный фильтр (синяя лента) в мерную колбу объемом 25 мл. Содержание тяжелых металлов определяли атомно-абсорбционным спектрофотометрическим анализом [8] на спектрофотометре ААS-30 (Саг1 Zeiss, Германия). Концентрация обнаружения для кадмия составила 0,5-Ы0-4 мкг/мл, марганца - 0,63,0 пг, меди - 4-40 пг, свинца - 4-20 пг [4].
Результаты и их обсуждение
Ранее нами было проведено исследование яиц другого вида пресмыкающихся -прыткой ящерицы Lacerta agilis Linnaeus, 1758 [1]. Полученные данные свидетельствуют о значительном накоплении тяжелых металлов в яйцах ящериц с загрязненной промышленными выбросами территории. Проведенные исследования яиц обыкновенного ужа показали, что у животных, обитающих в различных по степени химического загрязнения биогеоценозах, они отличаются по исследуемым биохимическим показателям (табл. 1). Так, яйца ужей из Днепровско-Орельского заповедника содержат в 1,7 раза больше белка и в 1,4 раза больше липидов, чем яйца этих змей из зоны промышленного загрязнения.
Такое значительное снижение содержания важнейших питательных веществ в яйце может стать причиной последующих патологий на относительно поздних стадиях развития эмбриона в условиях комплексного химического загрязнения среды. Очевидно, что выявление фактов патологий эмбриогенеза требует специальных дополнительных исследований.
Содержание белка, липидов и тяжелых металлов в яйцах обыкновенного ужа из различных мест обитания (п=27)
Показатель1 Днепровско-Орельский природный заповедник Зона промышленного загрязнения
Белок 16,4±1,6 9,7±2,3
Липиды 4,0±0,3 2,8±0,6
Железо 72,6±4,6 68,6±5,1
Марганец 2,1±0,2 3,0±0,5
Цинк 37,0±2,7 66,7±5,2
Никель 5,3±0,6 12,9±2,4
Свинец 1,9±0,2 10,1±1,2
Примечание: 1 содержание белка и липидов указано в % от влажной массы, а металлов - в мг/кг сухого веса.
Исследование накопления тяжелых металлов показало, что только количество железа в яйцах достоверно не отличается у змей из заповедника и зоны химического загрязнения. Для остальных металлов прослеживается закономерность повышенного
содержания в пробах с загрязненной территории. Марганца в яйцах ужей из биогеоценозов, подверженных комплексному химическому загрязнению больше в 1,4 раза, меди - в 1,8, цинка - в 1,8, никеля - в 2,4, свинца - в 5,3 раза. Что касается кадмия, то его во многих пробах из заповедника не зафиксировано. По-видимому, его количество в этих пробах находится за пределом обнаружения используемого прибора. В яйцах ужей из зоны промышленного загрязнения содержание кадмия составило 2,7 мг/кг с.в.
Бюргер и Гохфильд [9; 11] предположили, что одним из возможных путей экскреции избытка металлов у самок птиц и пресмыкающихся является их выведение с откладываемыми яйцами. По-видимому, это действительно так, но при этом необходимо учитывать популяционный эффект возможного тератогенного действия избытка токсикантов.
В перспективе, если удастся обнаружить корреляцию между содержанием металлов в скорлупе и содержимом яиц, возможно целесообразно использовать для индикации состояния среды только скорлупу, оставшуюся после вылупления животных (особенно в лабораторных уловиях). В исследованиях яиц черепах Trachemys scripta, проведенных Бюргером и Гиббонсом [10], такой корреляции обнаружено не было. Однако, необходимы дополнительные исследования других видов для уточнения этого факта.
Таким образом, в яйцах ужа обыкновенного в условиях зоны промышленного загрязнения тяжелые металлы аккумулируются в больших количествах по сравнению с малотрансформированными местообитаниями. Этот процесс сопровождается снижением содержания основных питательных веществ в яйце. Повышенные концентрации тяжелых металлов в формирующихся яйцах может оказывать негативный тератогенный эффект на развивающиеся эмбрионы, снижать их жизнестойкость как до, так и после рождения. В то же время, яйца пресмыкающихся могут оказаться приемлемым объектом для индикации уровня загрязнения окружающей среды и оценки токсической нагрузки на развивающийся эмбрион.
2. Карнаухов А. И., Безнис А. Т. Бионеорганическая химия. - К.: Вища школа, 1992. - 223 с.
3. Кучеренко Н. Е., Васильева А. Н. Липиды. - К.: Вища школа, 1985. - 228 с.
4. Морозов Н. П., Петухов С. А. Определение содержания микроэлементов группы тяжелых и переходных металлов в рыбах // Типовые методики исследования продуктивности видов рыб в пределах их ареалов. - Вильнюс, 1978. - Ч. 3. - С. 53-63.
5. Некоторые вопросы токсичности ионов металлов / Под ред. Х. Зигель, А. Зигель. - М.: Мир, 1993. - 368 с.
6. Практикум по биохимиии. - М.: МГУ, 1979. - С. 90-91.
7. Соколов В. Е., Бочаров Б. В., Криволуцкий Д. А. Экотоксикология и проблемы защиты окружающей среды от загрязнений // Экотоксикология и охрана природы. - М.: Наука, 1988. - С. 4-19.
8. Хавезов И., Цалев Д. Атомно'-адсорбционный анализ. - Л.: Химия, 1983. - 144 с.
9. Burger J. Heavy metals in avian eggshels: another excretion method // J. Toxicol. Environ. Health. - 1994. - Vol. 41. - P. 207-220.
10. Burger J., Gibbons W. Trace elements in egg contents and egg shells of slider turtles (Trache-mys scripta) from the Savannah River Site // Arch. Environ. Contam. Toxicol. - 1998. - Vol. 34. -P. 382-386.
11. Burger J., Gochfeld M. Cadmium and lead in common terns (Aves: Sterna hirundo): relationship between levels in parents and eggs // Environ. Monit. Assess. - 1991. - Vol. 16. - P. 253-258.
12. Environmental contamination and developmental abnormalities in eggs and hatchlings of the common snapping turtle (Chelydra serpentina serpentina) from the Great Lakes-St. Lawrence River basin (1989-1991) / C. A. Bishop, P. Ng, K. E. Pettit et al. // Environ. Pollut. - 1998. -Vol. 101. - P. 143-156.
13. Metals and metalloids in tissues of American alligators in three Florida lakes / J. Burger, M. Gochfeld, A. A. Rooney et al. // Arch. Environ. Contam. Toxicol. - 2000. - Vol. 38. -P. 501-508.
14. Nondestructive indices of trace element exposure in squamate reptiles / W. A. Hopkins, J. H. Roe, J. W. Snodgrass et al. // Environ. Pollut. - 2001. - Vol. 115. - P. 1-7.
15. Temporal and geographic variation of organochlorine residues in eggs of the common snapping turtle (Chelydra serpentina serpentina) (1981-1991) and comparisons to trends in the herring gull (Larus argentatus) in the Great Lakes basin in Ontario, Canada // C. A. Bishop, P. Ng, R. J. Norstrom et al. // Arch. Environ. Contam. Toxicol. - 1996. - Vol. 31. - P. 512-524.
Надійшла до редколегії 10.04.03.
МИКРОБНЫЕ ПЕЙЗАЖИ ПОЧВЫ ПОЙМЕННОЙ ЛИПО-ЯСЕНЕВОЙ ДУБРАВЫ ПОД ВЛИЯНИЕМ ЭКСКРЕЦИЙ ЛОСЯ ALCES ALCES (MAMMALIA, ARTIODACTYLA) ПРИ ЗАГРЯЗНЕНИИ ПОЧВЫ КАДМИЕМ
Наведено дані щодо впливу екскрецій лося на просторову структуру і таксономічний склад мікробоценозу в умовах забруднення ґрунту кадмієм. Підтверджено, що екскреторна діяльність ссавців є важливим природним екологічним чинником, що сприяє відновленню та розвитку мікрофлори в умовах забруднення.
Экскреторная деятельность млекопитающих - наиболее распространенное и масштабное явление в природных системах. Экскреторный опад представляет собой источник поступления органического вещества и является катализатором интенсификации биохимических процессов в почве. В пойменных дубравах величина экскреторного опада млекопитающих составляет 93,1 кг/га, за счет фитофагов выделяется 61,3 % опада [9]. Наибольшее количество данных накоплено по количеству экскреторного опада, производимого лосями. В степных лесах Украины лось рассеивает 3,0-9,8 кг/га экскреций [3]. Экскреции млекопитающих, являясь катализаторами деструкционного процесса, ускоряют разложение лесной подстилки [2].
Экскреции улучшают физико-химические свойства почвы: повышается пороз-ность и влажность почвы, увеличивается содержание минеральных, органических
Белок и тяжелые металлы






В результате активного воздействия цивилизации на окружающую среду степень ее загрязнения возрастает с каждым годом. Главной причиной ухудшения экологической обстановки можно считать колоссальное потребление и переработку минеральных ресурсов, являющихся источником металлов, необходимых для производства.
Особенно опасным является все возрастающее загрязнение природных источников воды токсическими веществами, включающими ионы тяжелых металлов (ТМ). Поскольку человек за год выпивает примерно две тонны питьевой воды, то даже малые концентрации этих веществ, которые накапливаются в организме человека, могут привести к различным тяжелым заболеваниям, включающим онкологические и сердечно-сосудистые патологии.
В условиях активной антропогенной деятельности загрязнение окружающей среды тяжелыми металлами стало особенно опасным потому, что не существует надежных механизмов самоочищения среды (период полувыведения из почвы цинка — до 500 лет, свинца — до нескольких тысяч лет). Попадая в окружающую среду с газовыми выбросами, твердыми отходами и сточными водами предприятий, удобрениями и пестицидами, ТМ загрязняют почвенный покров, воды и воздух, причем из водной и воздушной среды прямыми или косвенными путями попадают в почву. Особенно опасны загрязнения изотопами металлов, которые, как показала Чернобыльская катастрофа, могут быть радиоактивными.
Главными источниками поступления в биосферу большинства металлов являются предприятия теплоэнергетики, поскольку в угле и нефти присутствуют все металлы. Количество ртути, кадмия, кобальта, мышьяка в атмосферных выбросах при сжигании угля, нефти, торфа и другого горючего может в 3-8 раз превышать количество добываемых металлов.
Для пригородных и сельских районов характерно поступление ТМ в окружающую среду в составе сточных вод и отходов. Существенным источником загрязнения почвы является применение удобрений из шламов, полученных из промышленных и канализационных очистных сооружений. Даже обычные моющие средства могут быть источником ионов цинка и селена.
Кроме того, к основным источникам токсических загрязнений необходимо отнести и автотранспорт. Автомобили кроме оксидов азота, углерода и серы выбрасывают в атмосферу соли свинца. Содержание свинца в организме жителей США, например, в настоящее время приближается к предельно допустимой концентрации (ПДК).
Физический механизм воздействия тяжелых металлов на живые организмы
До недавнего времени было непонятно, почему сравнительно малые концентрации тяжелых металлов вызывают тяжелые отравления.
Последние годы в работах, проводимых на физическом факультете, было обнаружено новое физическое явление — образование надмолекулярных структур — дипольных белковых кластеров в растворах различных белков и ферментов, содержащих ионы тяжелых металлов. Принято называть тяжелыми металлами те элементы, атомный вес которых превышает 40.
Образование белковых нано структур было изучено нами в растворах различных протеинов, содержащих ионы тяжелых щелочных металлов — цезий, рубидий, а также медь, кадмий, свинец, европий и др. различными оптическими методами (рассеяние света, фотонно-корреляционная спектроскопия и поляризация флуоресценции).
Как показали эти исследования, особую роль играет взаимодействие белков и ферментов с таким важным для жизнедеятельности организма элементом, как калий. Оказалось, что наличие в растворах белков ионов калия K + также приводит к возникновению дипольных нанокластеров.
Таблица. Металлы и их ионные радиусы
| МЕТАЛЛ | Na+ | K+ | Cs+ | Rb+ | Cd+ | Pb 2+ | Eu 3+ | Сe+ |
| ВЕЛИЧИНА ИОННОГО РАДИУСА | 0,87 A | 1,33 A | 1,67 A | 1,47 A | 1,14 A | 1,2 A | 0,95 A | 1,27 A |
Было выявлено, что на процесс кластерообразования влияет величина ионного радиуса металла. В случаях, когда в растворах белков имеются малые ионы типа Na+, образование дипольных кластеров не наблюдается, поскольку ион натрия находится у поверхности белка в окружении молекул воды и не может соединиться непосредственно с противоположным зарядом на белке.
Ионы с большим радиусом (смотри таблицу), такие как Cs+, Rb+, Cd+, Ce+, Pb 2+ , Eu 3+ а также К+, не могут удерживать на своей поверхности воду, т.к. энергия взаимодействия заряд иона — дипольная молекула воды обратно пропорциональна четвертой степени ионного радиуса и может быть сравнима с тепловой энергией. Поэтому такие ионы присоединяются к отрицательным зарядам на поверхности белка непосредственно без водной оболочки (рис.1).
Когда концентрация перечисленных выше ионов увеличивается, наступает момент электрической разрядки поверхности белка. При этом вместо кулоновского отталкивания между макромолекулами белка возникает диполь-дипольное притяжение. Этот процесс возможен только для белков и ферментов, поскольку только у них наблюдаются гигантские дипольные моменты, достигающие величины в тысячу D (дебай).
Смена характера межмолекулярного взаимодействия приводит к появлению в растворах белков надмолекулярных наноструктур — дипольных белковых кластеров, масса которых растет в области изоэлектрической точки белка с ростом концентрации тяжелых ионов.

Рис.1. Схема возможного процесса образования дипольной белковой наноструктуры
Роль калия и натрия в жизнедеятельности организма очень важна. Электрические свойства (потенциал покоя — потенциал действия) большинства клеток определяются этими двумя ионами, а также ионом кальция Ca+, поэтому они называются потенциало — образующими. Как известно, натрий содержится в крови, в плазматической жидкости межклеточного пространства, в то время как калий в организме человека, в основном, находится внутри клеток. Так внутри мышечных клеток калия почти в 50 раз больше, чем в межклеточном пространстве. Для поддержания такой концентрационной неравновесности затрачивается большая энергия. С помощью молекулярных «машин» — Атфаз — натрий из клеток выкачивается, и в клетки закачивается калий. При патологическом состоянии у человека может происходить разрушение клеточных мембран (лизис клеток). В этом случае выходящий из клеток калий нарушает процесс синтеза белков и ферментов и приводит к кластеризации макромолекул.
Безусловный интерес представляют собой исследования свойств водных растворов основных белков крови (альбумина и гамма-глобулина), а также белков являющихся основными структурными элементами тканей живых организмов, к которым относится фибриллярный белок — коллаген.
В наших работах с помощью методов статического и динамического рассеяния света (фотонно-корреляционной спектроскопии) было показано, что размер ионного радиуса металла влияет на межмолекулярные взаимодействия и подвижность молекул коллагена в растворе. Воздействие ионов калия, имеющих больший ионный радиус по сравнению с ионами натрия, аналогично воздействию ионов тяжелых металлов, т.к. приводит к агрегации молекул коллагена вблизи изоэлектрической точки (pH 6). Это проявляется в уменьшении примерно в два раза величины коэффициента трансляционной подвижности, при этом масса рассеивающих частиц увеличивается на порядок.
Рост массы частиц в растворах белков при воздействии ионов металлов с большими ионными радиусами было подтверждено также с помощью метода поляризации флуоресценции.
Следует отметить, что по данным наших экспериментов начало кластерообразования в растворах альбумина, содержащих ионы свинца, меди, кадмия и др., соответствуют значениям ПДК для этих металлов.
В 2009 году в дипломной работе Т.Н. Тихоновой с помощью атомно-силового микроскопа (АСМ) были впервые получены изображения молекул основных белков сыворотки крови — альбумина и гамма-глобулина, а также изображения белковых кластеров, которые образуются в растворах при добавлении ионов с большими ионными радиусами.
В качестве примера на фотографиях показаны снимки молекул альбумина и белковых агрегатов в растворах альбумина с ионами калия и европия.
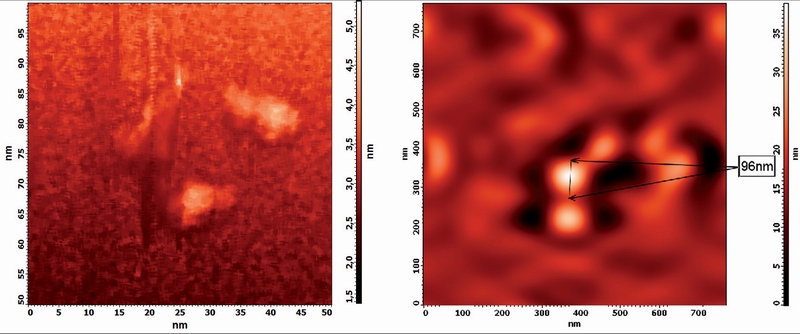
Рис.2. Строение молекулы альбумина, отснятой на АСМ
Рис.3. 2D-изображение частиц образующихся в растворе альбумина при добавлении KCl, полученного с помощью АСМ
Данная фотография, полученная с помощью АСМ, дает представление о размере молекулы альбумина (~10 нм).
Как можно видеть, размер частицы увеличился почти на порядок.
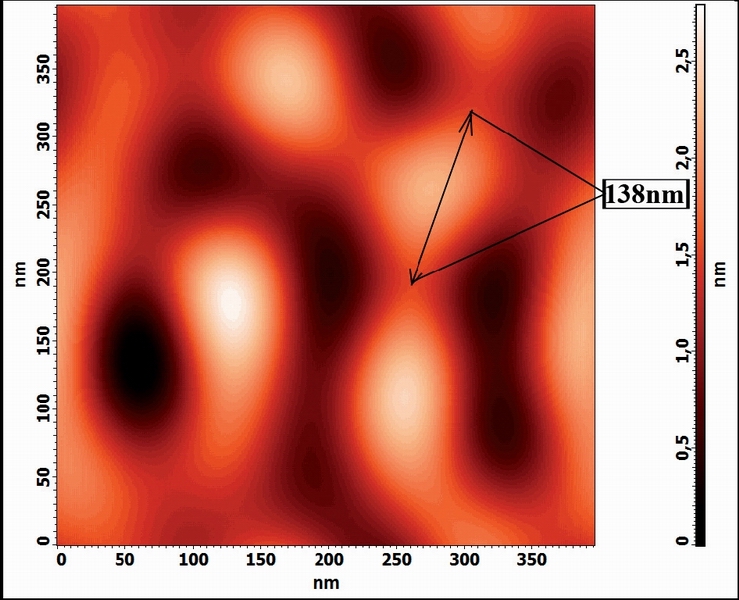
Рис. 4. 2D-изображение белковых кластеров в растворе альбумина, содержащем соль Eu(NO3)3
На фотографии (рис 4.), полученной с помощью АСМ, показано изображение частиц, образующихся в растворе альбумина при добавлении соли Eu(NO3)3 .
Таким образом, нами обнаружен и объяснен механизм образования наноразмерных дипольных кластеров в растворах белков, содержащих ионы тяжелых металлов и калия.
Можно предполагать, что образование белковых кластеров в крови человека под действием ТМ, приводит к нарушениям как транспортной, так и иммунной функций основных белков крови.
Возникает вопрос, каким способом можно обезопасить человека от отравления тяжелыми металлами.
Наиболее эффективным методом очистки от ТМ может служить сорбция металлических ионов на пористых средах, например на активированном угле. Подобные фильтры применяются во всех современных системах очистки водопроводной воды.
Г.П. Петрова, Ю.М. Петрусевич, И.А. Сергеева,
Т.Н. Тихонова, К.В. Федорова,
(кафедра молекулярной физики,
кафедра медицинской физики)
Литература
1. G.P. Petrova, Yu.M.Petrusevich, A.N.Evseevicheva.// Gen. Phys. and Biophys. 1998, V.17(2), C. 97
2. Петрова Г.П., Петрусевич Ю.М. // Биомед. радиоэлектроника. 2000, №3, С. 41.
3. Петрова Г.П., Петрусевич Ю.М., Тен Д.И. // Квант. Электроника. 2002, 32, №10, С. 897.
4. И.А. Сергеева, Н.В. Сокол, М.С. Иванова, Г.П. Петрова, Ю.М. Петрусевич// ВМУ. Серия 3 Физика. Астрономия. 2009, №4, С. 85
Исследовательская работа "Влияние антропогенных загрязнений на активность белков" (11 класс)
Актуальность. В условиях интенсивного антропогенного загрязнения окружающей среды, вопрос о влиянии загрязняющих веществ на живые организмы, является крайне актуальным. К отрицательным относят все виды воздействия на биосферу, создаваемых человеком и угнетающих природу. Небывалые по мощности и разнообразию негативные антропогенные воздействия, особенно резко стали проявляться во второй половине 20 века. Под их влиянием естественная биота экосистем перестала служить гарантом устойчивости биосферы.
Источниками антропогенного загрязнения, наиболее опасного для популяций любых организмов, являются промышленные предприятия (химические, металлургические, целлюлозно-бумажные, строительных материалов и др.), транспорт, теплоэнергетика, сельскохозяйственное производство. Количество загрязнителей (поллютантов) постоянно растёт по мере развития новых технологических процессов. Суммарный выброс в окружающую среду загрязнителей в России составил 41,8млн.т [3]. Специалисты считают, что в локальном и глобальном масштабах «приоритетными» являются следующие загрязнители: диоксид серы, канцерогенные вещества (бензпирен), нефтепродукты, хлорорганические пестициды, оксид углерода, оксиды азота. К особо опасным загрязнителям относят радиоактивные элементы, диоксины и тяжёлые металлы (ртуть, медь, кобальт, свинец, кадмий).
В то же время многие металлы играют важную роль в жизнедеятельности человека. Они участвуют в структурировании белков, нуклеиновых кислот, активных центров ферментов, активизируют биологические реакции, участвуют в ионной проницаемости клеточных мембран. Но при избыточном поступлении в организм, металлы вызывают глубокую денатурацию белков, образуя нерастворимые соли комплексного характера по анионным центрам радикалов аминокислот. При этом подавляется действие большинства ферментов, поскольку именно радикалы аминокислот участвуют в формировании их активных центров.
Цель работы: выявить влияние аналогов антропогенных загрязнителей на активность растительных и животных белков.
Ознакомиться по литературным источникам с вопросом о негативном влиянии на организм тяжёлых металлов и органических веществ.
Ознакомиться с методикой проведения экологического эксперимента, позволяющего выявить:
а) влияние тяжёлых металлов на активность растительных и животных
б) влияние органических веществ на структуру белков.
3. Определить концентрацию токсикантов, которая вызывает денатурацию
Проанализировать полученные результаты и сделать выводы.
Объект исследования: растительные и животные белки;
Предмет исследования: активность белков;
Проблемный вопрос: какие причины вызывают разрушение белков и приводят к потере активности?
Гипотеза: если воздействовать аналогами антропогенных загрязнений на животные и растительные белки, то они теряют активность и разрушаются.
Методы исследования: эксперимент, анализ литературных источников.
Глава 1. Обзор литературных источников
1.1 Экологические последствия загрязнения атмосферы
Загрязнение атмосферного воздуха воздействует на здоровье человека и окружающую природную среду различными способами – от прямой и немедленной угрозы до медленного и постепенного разрушения различных систем жизнеобеспечения организма. Во многих случаях загрязнение воздушной среды нарушает компоненты экосистемы до такой степени, что регуляторные процессы не в состоянии вернуть их в первоначальное состояние.
Физиологическое воздействие на организм человека главных загрязнителей (поллютантов) чревато самыми серьёзными последствиями. Так, диоксид серы, соединяясь с влагой, образует серную кислоту, которая разрушает лёгочную ткань человека и животных.
Пыль, содержащая диоксид кремния, вызывает тяжёлое заболевание лёгких – силикоз. Оксиды азота раздражают и разъедают слизистые оболочки глаз и лёгких, участвуют в образовании ядовитых туманов. Если они содержатся в воздухе совместно с диоксидом серы, то возникает эффект синергизма, т.е. усиление токсичности всей газовой смеси.
Широко известно действие на организм человека оксида углерода: при отравлении возможен летальный исход. Благодаря низкой концентрации СО в атмосфере он не вызывает массовых отравлений, хотя и опасен страдающим сердечно-сосудистыми заболеваниями [1].
Среди взвешенных твёрдых частиц наиболее опасны частицы размером менее 5 мкм, которые способны проникать в лимфатические узлы, задерживаться в альвеолах лёгких, засорять слизистые оболочки.
Весьма неблагоприятные последствия, которые могут сказываться на огромном интервале времени, связаны и с незначительными по объёму выбросами, как свинец, фосфор, кадмий, кобальт. Они угнетают кроветворную систему, вызывают онкологические заболевания, снижают иммунитет.
Последствия воздействия на организм человека вредных веществ, содержащихся в выхлопных газах автомобилей, весьма серьёзны и имеют широкий диапозон действия: от кашля до летального исхода. Тяжёлые последствия в организме живых существ вызывает ядовитая смесь дыма, тумана и пыли – смог. Смог особенно опасен для людей, страдающих лёгочными заболеваниями [1].
Антропогенные выбросы загрязняющих веществ в больших концентрациях и в течении длительного времени наносят большой вред не только человеку, но и остальной биоте. Известны случаи массового отравления диких животных, особенно птиц и насекомых, при выбросах вредных загрязняющих веществ большой концентрации.
Что касается растений, то выбросы вредных веществ действуют на их зелёные части, попадая через устьица в ткани, разрушая хлорофилл и структуру клеток, а также попадая из почвы через корни. Особенно опасен для растений диоксид серы, под действием которого прекращается фотосинтез и гибнут многие деревья, особенно хвойные: ель, сосна, пихта, кедр [3].
Глобальное загрязнение атмосферы приводит к нарушению озонового слоя и кислотным дождям. «Озоновые дыры» - это значительные пространства в озоновом слое атмосферы на высоте 20-25 км с заметно пониженным содержанием озона (до 50%).
Истощение озонового слоя признано всеми как серьёзная угроза глобальной экологической безопасности. Оно ослабляет способность атмосферы защищать всё живое от жёсткого ультрафиолетового излучения («УФ - радиация»), энергии одного фотона которого достаточно, чтобы разрушить большинство органических молекул. Поэтому в районах с пониженным содержанием озона многочисленны солнечные ожоги, увеличивается количество заболеваний раком кожи.
Антропогенное происхождение «озоновых дыр» связано с повышенным содержанием хлорфторуглеродов (фреонов). Фреоны широко применятся в промышленном производстве и в быту (хлорагрегаты, растворители, распылители, аэрозоли.) В атмосфере фреоны распадаются с выделением оксида хлора, губительно действующего на молекулы озона.
Основными поставщиками фреонов являются США(30,85%), Япония (12,42%), Великобритания (8,65%), Россия (8%) (по данным «Гринпис»).
«Кислотные дожди» образуются при промышленных выбросах в атмосферу диоксида серы и оксидов азота. Соединяясь с атмосферной влагой, диоксид серы и оксид углерода образуют разбавленную серную и азотную кислоты. В результате дождь и снег оказываются подкисленными (рН ниже 5,6) [2].
Суммарные мировые антропогенные выбросы диоксида серы и оксидов азота ежегодно составляют более 255млн т. Закисление природной среды негативно отражается на состоянии экосистем. Под действие кислотных дождей из почвы выщелачиваются не только питательные вещества, но и токсичные металлы6 свинец, кадмий, алюминий и др. Далее они сами и их токсичные соединения усваиваются растениями и почвенными организмами, что ведёт к весьма негативным последствиям [3].
Воздействие кислотных дождей снижает устойчивость лесов к засухам, болезням, природным загрязнениям, что приводит к их деградации как природных экосистем. 50 млн га леса в европейских странах страдают от действия загрязняющих веществ. Гибнут хвойные леса в на Северных Аппалачах, в Баварии. Отмечены случаи поражения хвойных и лиственных лесов в Сибири, Карелии, что свидетельствует о неблагополучном состоянии окружающей среды. В районе г. Норильска и на Северном Урале огромные площади тайги и лесотундры стали почти безжизненными из-за выбросов серы Норильским горно-химическим комбинатом [3].
1.2 Влияние тяжёлых металлов на здоровье человека
Загрязнение окружающей среды тяжёлыми металлами, а особенно свинцом, приобрело огромные масштабы в связи с содержанием в бензине антидетонаторной добавки – тетраэтилсвинца. Вместе с выхлопными газами автомобилей он выбрасывается в атмосферу. Ежегодно мировой парк автотранспорта выбрасывает в воздух свыше 0,4 млн.т свинца [3]. Вследствие этого за последние десятилетия уровень свинца в крови людей увеличился в несколько раз. Накопление свинца в организме приводит к раковым заболеваниям, так как, в несколько раз усиливает действие канцерогенных веществ (диоксины, полициклические углеводороды). В этом проявляется взаимодействие различных ксенобиотиков в окружающей среде либо в организме, с образованием ещё более ядовитых веществ. Масштабы отравления медью наиболее опасны в промышленных медедобывающих районах, где на 1т добытой меди приходится 2т пыли, содержащей 15% меди, 60% - оксидов железа, по 4% мышьяка, ртути, свинца. При избытке меди в организме происходит угнетение многих ферментов, разрушаются железосодержащие белки (гемоглобин, ферритин и др.) в результате замещения железа на медь. Вследствие отравления медью возникает глобинонурия, желтуха, накапливается метгемоглобин (потемнение крови). Избыток ионов меди в организме вызывает заболевания нервной системы, печени, гастриты, язвенную болезнь желудка. В то же время, медь, как и железо, играет важную роль в процессе кроветворения и поддержания нормального состава крови. Недостаток меди в почве может привести к заболеванию животных анемией, а у растений вызвать задержку образования хлорофилла, понизить содержание в них витаминов. Токсичность ртути, свинца и других тяжёлых металлов усиливается в результате их преобразования в окружающей среде в алкильные производные [5].
Метил и фенил-ртуть очень легко проникают в организм. Таким образом, тяжёлые металлы, попавшие в окружающую среду, пагубно влияют на здоровье человека, разрушают белки, в том числе и ферменты, вызывая тяжёлые заболевания.
Несмотря на то, что дефицит лития в организме человека приводит к психическим расстройствам, при повышенной концентрации он очень токсичен. Так избыток лития вызывает общую заторможенность, нарушение дыхания и сердечного ритма, слабость, сонливость, потерю аппетита, жажду, расстройство зрения, а также дерматит лица и рук.
Бериллий принадлежит к числу наиболее токсичных металлов. ПДК бериллия составляет 0,001мг/м, а ртути - 0,01. Бериллий и его соединения обладают аллергическим и канцерогенным действием, раздражают кожу и слизистые оболочки, вызывают дерматозы, конъюктивиты, фарингит, заболевания лёгких и бронхов – трахеобронхит, пневмонию и опухоли лёгких. Заболевания могут возникнуть через 10-15 лет после прекращения контакта с бериллием [1].
Цинк менее токсичен, чем другие металлы, но его избыток в организме может привести к понижению кальция в крови и костной ткани. Присутствие цинка в производственных помещениях в виде пыли вызывает заболевания дыхательных путей, называемое «литейной лихорадкой». С другой стороны цинк - важный микроэлемент. Он входит в состав инсулина, (гормон поджелудочной железы), участвует в переносе углекислого газа кровью позвоночных, стимулирует рост растений [1].
Никель относится к металлам с умеренной токсичностью. ПДК никеля в питьевой воде составляет 0,1мг/л. Аллергическое действие металлического никеля проявляется только при продолжительном контакте кожи человека с декоративными никелевыми покрытиями (корпуса и браслеты часов, оправы очков). В то же время, летучий тетракарбонил никеля – одно из самых ядовитых веществ, известных человеку. ПДК никеля в воздухе производственных помещений 0,0005мг/м. В своё время это соединение состояло в списках отравляющих боевых веществ ряда стран [4].
Кадмий в организме человека в основном накапливается в почках и печени, причём его повреждающее действие наступает, когда концентрация этого химического элемента в почках достигает 200мкг/г живой массы. Попадая с неочищенными стоками промышленных предприятий в водоёмы, растворённый кадмий осаждается и накапливается в донных отложениях. Особенно аккумулируют в своих организмах кадмий водоросли, моллюски и ракообразные. Употребление в пищу этих организмов приводит к заболеваю «итай – итай». В Японии эта болезнь известна с 1955г, когда сточные воды концерна «Мицуй», содержащие кадмий попали в оросительную систему рисовых полей. Это отравление вызвало у людей апатию, повреждение почек, размягчение костей, отмечалось немало смертельных случаев. У японцев, употребляющих в пищу значительное количество риса, содержание кадмия в почках колеблется от 65 до 115 мкг/г, тогда как у европейцев и американцев – от 10 до 30 мкг/г.Источниками кадмия являются газовые выбросы промышленных предприятий, сжигание угля на ТЭС, производство минеральных удобрений, красителей, катализаторов. Усвоение вводно-пищевого кадмия – на уровне 5%, а воздушного – до 80%. К характерным « кадмиевым» болезням горожан относятся: гипертония, ишемическая болезнь сердца, почечная недостаточность. У курящих (табак сильно аккумулирует соли кадмия из почвы) или занятых на производстве с использованием кадмия к раку лёгких добавляется эмфизема лёгких, а для некурящих – бронхиты, фарингиты [1].
Глава 2. Методика исследования и результаты
Прекрасную модель для исследований представляют белки, выделенные из семян бобовых растений и белок куриных яиц. В определённых условиях они длительное время сохраняют свои биологические свойства. В растворах белки вступают во взаимодействие со многими веществами (металлами, спиртами, фенолами и др.) [4].
Оборудование и реактивы: набор химических стеклянных пробирок, 1-2 куриных яйца, 5%, 2,5%, 1,25% растворы солей: сульфата меди, хлорида меди, сульфата натрия, хлорида калия, ацетата натрия, ацетата свинца (или свинцовая примочка), 40% раствор формалина, этиловый спирт, растительный белок (горох), пипетка, фильтровальная бумага.
Приготовление растворов белков
У куриного яйца отделить белок от желтка в мерный стаканчик, размешать его стеклянной палочкой в дистиллированной воде в соотношении 1:10. Затем профильтровать.
Зерновой горох перемолоть в муку, развести в соотношении : 10г. гороховой муки на 50мл 10% раствора хлористого натрия или хлористого калия. Профильтровать.
Опыт №1 Воздействие на белки солей металлов
В 6 пробирок наливаем 1,0-1,5мл раствора белка и медленно по каплям из пипетки при встряхивании приливать растворы сульфата меди и сульфата калия (1 и 2 пробирки), хлорида меди и хлорида натрия (3 и 4 пробирки), ацетата свинца и ацетата натрия (5 и 6 пробирки). В 1, 3, 5 пробирках образуются хлопьевидные осадки в результате образования малорастворимых соединений: с солями меди - голубого цвета, с солью свинца – белого цвета. В остальных пробирках изменений не происходит [4].
Читайте также:
