Добавка на коррозию металла
Обновлено: 16.05.2024
Что такое коррозия металла, и во что она может в короткие сроки превратить металлические изделия или детали — знают, наверное, все. Особенно красноречиво, по всей видимости, не выбирая выражений, многое могут рассказать о ней автолюбители. Ведь без должного ухода, без специальной обработки, особенно в условиях массированного применения противогололедных химических смесей на наших дорогах, стальные корпуса автомобилей буквально за пару лет способны превратиться в ржавое решето. Только средства защиты металлов от коррозии способны «переломить ситуацию».
Евгений Афанасьев
Обновлено: 22.04.2020
Немало проблем доставляется коррозия и в строительстве. Страдают металлические постройки гаражи, ангары и т.п., заборы, несущие детали каркасных конструкций, кровля. Не щадит этот «безжалостный противник» сантехнику и приборы бытового предназначения, особенно контактирующие с водой.
С коррозионными процессами непросто, но все же можно и обязательно нужно бороться. И очень хорошо, что человек создал для этих целей специальное «вооружение» — имеется в виду довольно широкий ассортимент разнообразных средств. Вот о них и пойдет речь: средства защиты металлов от коррозии — разновидности, способы применения, рейтинг наиболее эффективных составов.
Способы борьбы с коррозией
Коррозия металлов – это деструктивный, разрушающий кристаллическую решетку, окислительно-восстановительный химический процесс. Вызывается он чаще всего высокой химической активностью самих металлов – многие помнят из школьного курса химии «линейку» активности элементов. Активизироваться может при создании неблагоприятных условий, например, высокой влажности и опущенной температуре, в агрессивной солевой, кислотной или щелочной среде.
Чаще всего приходится сталкиваться с коррозией черных металлов, то есть – различных сортов стали и чугуна, применяемых буквально повсеместно, во всех сферах деятельности человека. Процесс начинает выдавать себя появлением на металлической поверхности пятен или разводов рыжего цвета.

Если с коррозией не бороться, она способна показать свою крайне разрушительную силу – металлические изделия быстро приходят в негодность.
Если не предпринять никаких шагов, то очаг начинает разрастаться, захватывая все новые площади. Причем иногда это происходит незаметно для глаз. Так, многие участки механизмов, приборов и т.п. — попросту скрыты из поля зрения, и увидеть их можно только при полной разборке узла или всего устройства. А иные очаги коррозии могут до поры скрываться под слоем краски, и только кода процесс зайдет очень далеко – поваляться сначала в виде вздутий, а потом – и прорывов ржавчины наружу.
Однако подобная методика, если и может быть применена, то с исключительной осторожностью, и только в качестве предварительного этапа, перед нанесением специальных составов. Только механическая очистка является весьма малоэффективным средством.

Точечные проявления коррозии, проступившие через слой краски
Особенно сложно удалить этим способом мелкие точечные очаги ржавчины, так как они в процессе чистки забиваются мелкодисперсной коррозийной пылью, и их становится практически не видно. Но беда как раз в том, что они никуда не деваются, и обязательно в дальнейшем проявят себя, даже после окрашивания. Поэтому обработка химическимисредствами — более надежна.
Кроме того, если ржавчиной поражен тонкий металл, то во время очистки, под давлением щёток или абразивного материала, он может повредиться вплоть до сквозной дырки.
Разновидности средств зашиты от коррозии
Существует несколько разновидностей составов, предназначенных для борьбы с коррозией. Это преобразователи ржавчины, специальные грунтовки и антикоррозийные покрытия:
- Одними из наиболее часто используемых и эффективных средств являются так называемые преобразователи ржавчины. Эти составы способны на химическом уровне не только удалить, но преобразовать образовавшиеся продукты коррозии в защитную, достаточно прочную пленку, своеобразную грунтовку поверхности. Подобные составы экономны в расходовании и отлично выполняют возложенные на них функции.
В продажу преобразователи поступают в жидкой форме (растворы или суспензии), и можно выбрать оптимальную форму применения, в зависимости от расположения поврежденного участка – будет ли это нанесение кисточкой, или более удобным видится применение распылителя.
Преобразователи подходят для обработки любых металлических деталей, но при условии, что толщина пораженного слоя не будет превышать 15÷20 мкм. Глубже состав не проникнет — он просто закроет поврежденный участок фосфатной пленкой, а оставшийся под ней очаг коррозии продолжит разъедать металл.
- Грунтовки по металлу не менее популярны, чем преобразователи ржавчины. В продаже можно найти разные варианты этих химических средств — это пассирующие, фосфатирующие, протекторные, изолирующие, а также преобразующие (то есть во многом сходные с упомянутыми выше преобразователям) и другие.
- Еще одной группой материалов для защиты металла от ржавчины являются специальные антикоррозийные покрытия, применяемые в комплексе с другими названными выше материалами.
Удаление ржавчины с металлических поверхностей
Если мы говорим об автомобилях, то коррозия чаще всего проявляется на кузове машины. Понятно, что любой автовладелец заинтересован в «здоровье» своего «питомца», и регулярные обновления антикоррозионной защиты – полностью на совести хозяина. Но бывает и так , что коррозия находит лазейки, или в силу каких-то обстоятельств на защитном слое появляются уязвимые участки.
При обнаружении малейших признаков поражения необходимо сразу же принимать меры, иначе очаг активного окисления будет не только расширяться, но и уходить вглубь металла. Если же металлический лист будет проеден ржавчиной насквозь, то тогда придется использовать другие, более дорогостояще способы ремонта.
Здесь нужно действовать быстро: если спохватиться вовремя, то еще можно вернуть поврежденному участку первоначальный внешний вид(при условии правильно подобранного оттенка краски).

Удаление ржавчины с кузова автомобиля — нанесение преобразователя с помощью кисточки
Любое из выбранных средств от ржавчины должно использоваться в установленной последовательности. Только в этом случае можно добиться необходимого эффекта:
- Первым шагом поврежденный участок необходимо аккуратно очистить от рыхлой ржавчины, применив металлическую щетку, а затем наждачную бумагу нужной зернистости.
- Далее, поверхность обрабатывается преобразователем ржавчины;
- Следующим шагом обработанная зона промывается несколько раз (если это оговорено в инструкции преобразователя ржавчины, так как иногда этого делать не требуется.)
- После этого производится просушка металлической поверхности ветошью или же с помощью строительного фена;
- По готовности поверхности – переходят к покрасочным работам.
При очистке может обнаружиться, что ржавчина уже сделала в металле сквозное отверстие. Если оно совсем небольшое, то его можно попробовать заделать шпаклевкой с применением стеклоткани. В случае если отверстие достигло значительных размеров, без приваривания заплатки не обойтись, а для этого потребуется специальное оборудование и, естественно¸ устойчивые навыки по проведению подобных ремонтно-восстановительных работ. Чтобы не доводить дело до такого, следует внимательно следить за состоянием антикоррозионной защиты автомобиля, что пресечь начало процесса коррозии металла на ранней стадии.

Зачистка поврежденного коррозией участка
Восстановление поврежденного коррозией участка с использованием преобразователя и грунта производится в примерно такой последовательности:
- Очистка металла от рыхлых слоев ржавчин.
- Обезжиривание очищенного участка.
- Обработка преобразователем ржавчины.
- При необходимости далее идет этап шпаклевки, а после ее высыхания — шлифовки.
- Затем поверхность снова обезжиривается.
- Следующий этап — это нанесение защитного грунта одним или двумя слоями.
- Далее идет два-три слоя адгезионной грунтовки;
- После этого отремонтированное место окрашивается в несколько слоев.
- Сверху краски наносится специальный лак.
Выполняя все работы с применением антикоррозионных химических средств, необходимо соблюдать правила техники безопасности. Обязательным условием считается использование защитных средств —резиновых перчаток, очков и респиратора. При необходимости следует закрыть окружающую поврежденный участок поверхность металла, чтобы исключить вероятность попадания и преобразователя и грунтовки, и финишных лакокрасочных материалов.
Надо сразу сказать, что полное восстановление сильно пораженного участка с его последующей финишной покраской – задача довольно сложная, и не всем поддающаяся. То есть при сомнениях в получении приемлемого результата лучше все же обратиться к специалистам. Это недёшево, и поэтому оптимальный выход – постараться не доводить свою технику до состояния, требующего такого вмешательства. То есть пресекать появление и развитие пораженных коррозией участков, как говорится, «в зародыше». Средств для этого — немало.
Далее будет представлен рейтинг лучших составов, способных эффективно бороться с коррозийным процессом, возникшим на поверхности и в скрытых полостях автомобиля.
Какой лучше выбрать состав?
В продаже (и в хозяйственных и в магазинах автозапчастей, автохимии и косметики, и в хозяйственных) представлено большое количество продукции отечественных и зарубежных производителей. Интересный факт, что пользователи особенно выделяют составы, изготовленные компаниями России и США. Отлично показывают себя и продукты многих европейских брендов.

Преобразователи ржавчины различного типа
Качество и эффективность работы представленной продукции проверено практикой применения — все они при соблюдении технологии использования дают ожидаемый результат. Поэтому их охотно используют и работники ремонтных служб, и домашние мастера.
Приятно удивляет и то, что потребители поставили на первое место отечественные составы. Скорее всего, потому, что они разрабатывались с учетом российских климатических и дорожных условий.
Газовая коррозия в технологических средах
В металлургии, химической промышленности множество процессов или их определенных стадий протекает в условиях повышенных температур и давлений. При низких температурах (100 – 200 °С) большинство газов и их смесей не представляет опасности. При повышенных температурах (выше 200 – 300 °С) и давлениях химическая активность газов сильно возрастает, и они начинают оказывать вредное влияние на металлы и сплавы.
При температуре выше 200 °С вредное воздействие оказывает хлор, а выше 300 °С – хлористый водород (HCl). С повышением температуры до 500 °С пары серы, диоксид серы (оксид серы (IV), сернистый ангидрид, сернистый газ, SO2) и диоксид азота (оксид азота (IV), бурый газ, NO2) также становятся химически активными.
Поведение газов и их смесей необходимо хорошо изучить, т.к. в условиях металлургического либо химического производства вышеописанные ситуации встречаются достаточно часто.
В технологических средах часто встречаются следующие случаи газовой коррозии: водородная коррозия, обезуглероживание стали, сернистая коррозия, карбонильная коррозия, разрушение в среде хлора и хлористого водорода.
Водородная коррозия
Водородная коррозия – вид коррозионного разрушения, который наблюдается, в основном, в технологических средах, содержащих водород, при воздействии повышенных температур и давлений. Очень часто водородная коррозия наблюдается при гидрировании нефти и угля, синтезе метанола и аммиака и т.п.
При воздействии водорода металл может подвергаться двум видам разрушения: водородная коррозия и водородная хрупкость. Зачастую эти два вида протекают одновременно.
Водородная коррозия происходит вследствии химического взаимодействия водорода среды и карбидной составляющей стали. При повышенных температурах и давлениях водород, попадая на поверхность стального изделия, диссоциирует. Образовавшиеся атомы H2 очень подвижны, их диаметр составляет 0,1 нм. Атомы водорода диффундируют вглубь металла, растворяясь в нем. Некоторая часть вступает в реакцию с углеродом:
При остывании металла, водород переходит в газообразное состояние, создавая достаточно высокое внутреннее давление. Это охрупчивает металл. На поверхности появляются трещины, вздутия. Прочность стали сильно уменьшается.
Обычно водородная коррозия появляется из-за нескольких причин:
- повышение внутреннего давления при образовании в порах CH4 и в результате – растрескивание по границам зерен;
- обезуглероживание стали, которое происходит из-за восстановления водородом цементита (Fe3C входит в состав сталей):
- водород проникает вглубь стали, образуя хрупкий твердый раствор водорода в Fe.
У водородной коррозии есть, так называемый, инкубационный период, при котором какие-либо внешние признаки разрушения отсутствуют. В среднем этот период может составлять около 1000 часов (зависит от условий).
Расчеты по термодинамике показывают, что при повышенном давлении и температуре около 350 – 600 °С цементит почти полностью разрушается.
Реакция, при которой образуется СН4 (метан) может протекать в сторону уменьшения объема, т.е. она обратимая. При повышении температуры равновесие реакции сдвигается вправо. Поэтому на нефтехимических производствах температуру поддерживают до 200 °С, при давлении около 50 МПа.
Скорость протекания водородной коррозии зависит не только от рабочих давлений и температур, но и от глубины обезуглероживания стали.
Обезуглероживание стали (декарбюризация)
Обезуглероживание стали (декарбюризация) - процесс обеднения поверхностного слоя металла углеродом. Наблюдается при температурах свыше 650 °С.
Чаще всего процесс обезуглероживания стали протекает в окислительных атмосферах (O2, H2O, CO), но может происходить и в атмосфере водорода. Кислород окисляет сначала углерод, а потом только железо. Обезуглероживание стали проходит интенсивнее с увеличением в газовой среде количества углекислого газа, влаги и кислорода. Если газовая среда содержит больше угарного газа и метана – скорость декарбюризации уменьшается.
Процесс восстановления цементита Fe3C является основой процесса обезуглероживания стали:
При температуре выше 650 °С атомы углерода более подвижны, чем атомы основного металла (железа), коэффициент диффузии атомов углерода также превышает коэффициент диффузии атомов Fe. Обезуглероживание стали протекает тогда, когда углерод диффундирует быстрее, чем окисляется железо.
Обезуглероживание сопутствует очень многим технологическим процессам, таким, как разнообразные реакции горения, окислительного крекинга и др. Сталь, подвергшаяся декарбюризации, теряет свою прочность и твердость, тем самым ухудшается ее качество, сокращается срок службы готовых изделий.
Декарбюризация (обезуглероживание стали) наблюдается после образования пленки оксидов на поверхности металла. С утолщением пленки окалина образуется медленнее, при этом обезуглероженный слой утолщается (может уходить на несколько миллиметров вглубь основного металла).
Для уменьшения степени обезуглероживания в сталь вводятся добавки вольфрама и алюминия. Незначительное влияние оказывают хром, марганец и кобальт.
Сернистая коррозия (коррозия в среде серы)
Различные соединения серы оказывают большое влияние на высокотемпературную газовою коррозию. Самым вредным и опасным среди таких соединений является сероводород (даже более чем сернистый ангидрид).
Сернистый ангидрид (SO2) выделяется в результате многих технологических процессов. Под воздействием этого соединения при температуре свыше 300 °С образуется на поверхности черных металлов слоистая окалина, которая состоит из FeS, FeO и Fe3O4.
Очень негативное влияние оказывает сернистый газ на чугун. При температурах выше 400 °С детали из чугуна окисляются изнутри, идет увеличение объема до 10%. Сильно уменьшается прочность чугунных изделий, наблюдается коробление, появляются поверхностные трещины и деталь разрушается. Это явление получило название «рост чугуна». Максимальное повреждение наблюдается при температуре около 700 °С.
Карбонильная коррозия
Карбонильная коррозия часто наблюдается в технологических средах, а именно, в случаях, когда при повышенном давлении и температуре протекают процессы с участием углерода (II). Карбонильная коррозия наблюдается при конверсии окиси углерода и метана, получении бутилового и метилового спиртов и т.д.
Оксид углерода при нормальном давлении и температуре по отношению к металлам инертен. Но при повышенных значениях температуры и давления CO реагирует с большинством металлов. В результате такого взаимодействия образуются карбонилы. Например, процесс образования карбонила железа описывается реакцией:
С оксидом углерода железо может образовать три вида карбонилов: Fe(CO)5 (пентакарбонил), Fe(CO)4 (тетракарбонил) и Fe(CO)9 (нонакарбонил). При повышении температуры все эти соединения разлагаются, т.к. не обладают достаточной устойчивостью. Наибольшей стойкостью, среди вышеперечисленных карбонилов железа, обладает пентакарбонил, который почти полностью диссоциирует на CO и Fe уже при температуре выше 140°С. Оксид углерода может образовывать подобные соединения со многими металлами.
Карбонильная коррозия протекает только в верхних слоях. Разрыхление и разрушение поверхностного слоя металла в глубину может достигать до 5 мм. Глубже структура не меняется.
При высоких температурах (до 700°С) и давлениях (до 35 МПа) для защиты от карбонильной коррозии металлов можно применять хромоникелевые стали, в состав которых входит около 20% Ni и 23% Cr, хромистые с содержание хрома 30%, а также марганцевые бронзы. Менее легированные стали (например, Х18Н9) можно использовать в случаях, когда давление и температура несколько ниже 700°С.
Карбонильная коррозия наблюдается также при синтезе мочевины. В качестве исходного сырья для получения CO(NH2)2 используется углекислый газ и NH3. Сам процесс протекает при давлении в 20 МПа и температуре 175 - 190°С. Для изготовления аппаратов, в которых протекают основные процессы синтеза, нержавеющие хромистые стали абсолютно не подходят. Самой высокой стойкостью к карбонильной коррозии в данных условиях обладает хромоникелевая сталь, в состав которой входит медь и молибден, а также некоторые молибденовые стали. Для повышения коррозионной устойчивости основных агрегатов, в которых проходит синтез мочевины, необходима очистка газов от сероводорода, а также обязательное введение в систему O2 в количестве 0,5-1 об.% от содержания углекислого газа.
Коррозия в среде хлористого водорода и хлора
В среде газообразного хлора и хлористого водорода металлы ведут себя не так, как в других агрессивных средах. Дело в том, что при воздействии хлористого водорода и газообразного хлора на поверхности металла образуются хлористые соли. Эти соединения обладают низкой температурой плавления, а в некоторых случаях, при сильном повышении температуры, они возгоняются (Т возгонки AlCl3 - 192°С). Почти все аналогичные процессы проходят с выделением тепла (положительный тепловой эффект). В результате нагрева хлориды, которые образовались на поверхности металла, плавятся и разлагаются (нарушается их структура).
Хлоридные пленки не обладают высокими защитными свойствами.
В атмосфере сухого хлора при низких температурах очень многие металлы обладают хорошей устойчивостью. Но при нагревании металл начинает реагировать с хлором и происходит воспламенение (протекает экзотермическая реакция). Температура, при которой происходит воспламенение, во многом определяется природой металла и зависит от величины теплового эффекта.
Температуры воспламенения некоторых металлов в среде сухого хлора:
- свинец – 90 – 100°С;
- железо и сталь – около 150°С;
- титан – около 20°С;
- никель – около 500°С;
Многие сплавы и металлы при комнатной температуре обладают удовлетворительной стойкостью и в среде хлористого водорода. Но с повышением температуры постепенно идет снижение стойкости. У каждого металла существует своя максимальная температура, при которой он еще относительно стойкий.
Если не считать благородных металлов, то в среде сухого хлора наибольшей стойкостью обладает никель и сплавы на его основе. Платина в среде хлористого водорода и хлора устойчива до температуры 1200°С.
На хромоникелевых сплавах (сталях) и самом никеле образуются поверхностные пленки, которые обладают нормальными защитными свойствами и малой летучестью.
народный самодельный незасыхающий антикор(автоконсервант) внутренних полостей.Консервационные масла. Ингибиторы коррозии в маслах.

Статья устарела и потеряла нить.Прочитав её вы потратите драгоценное время.
>>>сразу в начале статьи выводы:
состав аналога раст-стопа для самопального приготовления в условиях кризиса
1.Любой доступный МАСЛОРАСТВОРИМЫЙ ингибитор коррозии или из подручных:
например: Нитрит Натрия, разбавленный в воде(пассиватор (даёт плёнку), Бура(флюс для пайки),растворимая в воде или уротропин(сухой спирт), разбавленный в глицерине.
Ингибитор коррозии основной элемент смеси.Всего надо 1%-5% ингибитора в смеси, не более.
2. Поливинилбутираль (PVB) (для адгезии).Растворим в спирте.(опционно, но не обязательно)
3.Основа масло, олифа, трансмиссионка(без противозадирных присадок, т.е. не ) итд
например Трансмиссионка atf 220 1:1 как Раст стоп А
4.Загуститель(Пластификатор)-пушсало, опционно,т.е. для скрытых полостей не надо
5.Керосин или аналог для лучшего растекания и обезвоживания влажной поверхности(опционно)
Сам я уже потом купил на пробу самый дешёвый в Ашане в баллоне за 100 рублей
Дешевле не было. Так что вопрос темы крайне спорный, но я свой опыт и знания приобрёл.
Вывод:растстоп для скрытых полостей: трансмиссионка+масляный или маслорастворимый ингибитор коррозии
конец полезной информации
-----------------------------------------------------------------------------
----------------------------------------------------------------------
Дальше много лишних для мозга буков, которые читать трудно в силу обилия информации и не обязательно в виду отсутствия нити повествования.Но познавательно…Без обид, хорошо?будет лишнее время,читайте.
Из цикла: ударим смекалкой и рукоблудием по импортозамещателям или что делать если негде купить оригинал или если его уже конкретно начали бодяжить.
-------------
-------------
Вот начало той статьи и прочих умствований которые вам читать уже не обязательно:
Статья тяжёлая и спорная.Отнеситесь с юмором.Я пишу её для себя и друзей любителей
Кому лень читать мой бред про "самопальный ингибитор коррозии", сообщество серьёзных антикорщиков тут .
В статье прозвучит состав для самоделок или готовые, крайне не дорогие растворы отечественного производителя из смежный областей, пригодных для задач автолюбителя…
Для написания статьи были использованы печатные материалы времён СССР, открытая информация с рекламных сайтов, выводы химиков с форумов, отзывы и опыт практиков.И миллионы прочитанных постов о практике применения антикоров на форумах, сканы которых в комментах
Статья ни в коей мере не ставит целью убедить в том что качественный импортный или иной антикор это плохо, просто хотел разобраться в 2014-15 году в разгар кризиса что делать если доллар будет стоит 100 рублей и покупка нормального антикора станет для меня не возможной, разобраться с тем как сделать его самому.
-------------------------------------------
Мовиль и Пушсало итд, это всего лишь разной плотности носитель для ингибиторов коррозии.
Но как ни странно, для многих старорежимных автолюбителей было шоком, что ингибиторы в их любимом ПУШСАЛЕ по ГОСТу не положены! Поэтому и родилась мысль написать для себя любимого по теме и собрать в комментах кучу противоречивой инфы. Солянка собранных данных шокировала и затянула с головой .
Статья ограничена жидкими незасыхающимии антикорами для замедления развития ржавчины в скрытых полостях…
Итак:
Раст стоп и аналоги в основном своем компоненте — это масляный раствор масляного ингибитора коррозии
Например Нитрит натрия, это пассиваторный (создающий плёнку) ингибитор коррозии.Присутствующий в куче недорогих консервирующих смазок отечественного производства.Нитрит Натрия согласно книге советского сержанта,разбавленный в воде служит пассиватором системы охлаждения при консервации машин на хранение.
Водный раствор нитрита натрия заливался в систему охлаждения и потом сливался, для повторного использования в следующей машине.Вот так просто в СССР водой и копеешной добавкой предохраняли металл системы охлаждения от ржи.
Раст стоп или любой иной незасыхающий антикор для внутренних полостей, это:
Масло+церезин(парафин)+масляный ингибитор+тиксотропная добавка (ЗАГУСТИТЕЛЬ), повышающая пластичность(например загуститель аэросил, но не только аэросил, он же «кремния диоксид коллоидный» )).
В раст стоп и аналогичные добавляют ароматизатор или отдушку.Разбавьте растворителем по вкусу, но не забывайте что процент ингибитора при разбавлении снижается!
В качестве подручных средств, как ингибитора коррозии можно использовать уротропин, бура, нитрит натрия и прочие примерно 1%-5% …
1 Ингибитор коррозии Нитрит натрия, водорастворимый ингибитор коррозии.Он же (Пищевая добавка E250 или NaNo2)., сочетается с маслами лучше всего.Применяя для него эмульгаторы и водные коллоидные системы — эмульсионные масла!(*)
2 Ингибитор коррозии БУРА, оно же флюс для пайки, оно же Консервант Е285 (Тетраборат натрия), разводить водой(*)
3 Ингибитор коррозии Уротропин(сухой спирт), оно же консервант(Е239), разбавленный в глицерине.
Глицерин брать в аптеке.
>>!>>Жирное с мокрым мешается ТАК: берём эмульгатор, т.е. любое мыло, можно стиральный порошок и смешивая масло в воде получаем Эмульсию.
Трансмиссионка должна мешаться с пушсалом без дополнительных средств.
Лайфхак из СССР:
Готовый густой аналог раст-стопа- "АМС-3" (смазка подводных лодок и погружных морских механизмов, обладает высокой липкостью и водостойкостью в агрессивной среде), разбавить это растворителем сольвентом или даже бензином.
Смазка с ингибиторами + растворитель.ТО же самое или почти тоже самое что и Раст-Стоп или аналоги.
Всё это в период кризиса можно купить за копейки, если импортозамещатели пролоббируют закон против импорта.
Нитрит натрия NaNo2 (пищевая добавка Е250) используется в пищевой промышленности в качестве фиксатора цвета и консерванта в мясных и рыбных продуктах.
А уротропин добавляют в красную икру как консервант(Е239).Приятного аппетита.Или пользуют как антисептик и лекарство от всех хворей.
Т.е .с основным компонентом для гаражного коктейля даже в жуткий кризис проблем не будет.
Без основного компонента ингибитора, всё что вы купите для днища-не более чем брачная ночь без невесты.
Можно конечно купить на рынке импортозаместительный аналог в красивой упаковке с кучей фраз про нано и про совершенную формулу, но как показала практика качество товара в кризис не падает только у упаковки, а что внутри никто из продавцов гарантировать не может.Вот тут отличные примеры на тему подделок . Так что доверяй, но проверяй+соблюдай инструкцию по нанесению.
Смешав свою "амальгаму" лично можно ждать каких то результатов.Особенно если нет денег на качественный импортный состав, нанесённый по правильной технологии прилежными опытными руками специалиста в дорогом сервисе.
>>>>Перед употреблением можно пройтись по ржавчине ОРГАНИЧЕСКИМ .т.е. бескислотным преобразователем, той же конторы "Ифхан 58 ПР" ( на основе таннинов, спиливает 300 мкм ржи в отличии от 150мк чем у кислотников).
Минусы этой группы ингибиторов:на открытой поверхности, например на днище нужно раз в год обновлять раствор.
Минусы и антиреклама:
При влаге под давлением и песке- сей фирменный, разработанный для канадской армии "антикор" стирается как тушь с лица заплаканной фотомодели
так же есть аналог раст стопа ингибитор Krown Т40,который полный аналог Rust-Stop.Он как и раст стоп идеален для скрытых полостей, но так же возможен как сезонно обновляемый антикор днища по ржавчине с ингибитором коррозии.
В сети интернет пользователи раст стоп мешают с литолом, пушсалом, мовилем, нигролом и остаются довольны.Ругаются только сварщики, которые потом вынуждены варить проржавевшие под покрытием днища буквально по кипящему маслу(о чём есть комменты)
Мешают растворы просто потому что в пуш сале, мовиле, консервационной смазке и раст стопе и прочих теоретически есть именно те самые ингибиторы и пассиваторы коррозии .Смысл мешанины предать удобоваримость методике нанесения, но после смеси массовая доля полезных активных веществ стремится к минимуму.
Конец лирического отступления
------------------------
Помните что именно Пассиваторы (нитрит натрия итд) создают на поверхности плёнку, в отличии от ингибиторов(уротропин), которые работают только влажными.
------------------------
Замедляющий коррозию состав содержит три основных компонента:
* Ингибитор – который предназначен для остановки реакции коррозии. Молекулы ингибитора эффективно покрывают поверхность металла и образуют водонепроницаемый слой, а также увеличивают адгезию пленки к поверхности.
* Пленкообразователь – который создает барьер на поверхности металла от механического воздействия. Пленкообразователь может формировать масляную, восковую или твердую пленку.
* Третий компонент содержит специальные химические вещества, такие как обезвоживатель и активаторы поверхности(ПАВ).
--------------------------
Всё это не сохнет в полостях, не отваливается как мастика слоями от днища(
Можно покрывать прямо по ржавчине (раст стоп в рекламных материалах расширяется на плоскости, в том числе и вверх по поверхности(капните отработкой на вертикальную железяку и эффект будет таким же), но смывается потоком воды и пескоструем (см.видео выше).Зато за час можно покрыть днище и испачкав шевелюру сделать на какое то время свою голову нержавеющей.
теперь о самодеятельности:
Из всего собранного материала хочется обратить внимание юного и не очень читателя на уротропин (сухой спирт) он не только ингибитор коррозии, но и частый компонент преобразователя ржавчины, что делает его при его цене и доступности очень любопытным кандидатом на попадание в масла для скрытых полостей.Его нужно 1% не менее и для достаточной эффективности более 5% совсем не обязательно.Что совсем не дорого.Но работает он ДО момента высыхание жижи.В отличии от NaNo2, который даёт плёнку и остаётся ею на поверхности после высыхания раствора.
уротропин можно в глицерине например растворить (растворимость уротропина в глицерине: 20,5 г/100г (20°C)), а потом глицериновый раствор уже мешать с маслом, пуш салом и т.д.Или изопропиловом спирте, однако уротропин не даёт защитной плёнки и работает только находясь в растворе
->>>>
В общем все секреты раскрыты.Если таможня победит или вырастит курс бакса, а покупать палёные бутылки неизвестно с чем вам не позволит логика.Вы сможете смешать NaNo2 хоть с олифой, хоть с отработкой(бойтесь металлической стружки!).Хоть с мовилем, хоть с пушсалом. С чем больше всего нравится.Хоть с пластилином в консервной банке на костре.И теперь это точно будет работать.
Напомню, что изначально незасыхающий раствор масла с ингибиторами и тиксотропными (вязкостными) добавками был придуман для скрытых полостей.Там всё ясно, там нет песка и влага без давления.А уже потом маркетологи решили втюхать это в качестве антикора для днища и в ход пошли презентации, отзывы фокус групп и прочие авторитетные заключения типа : зуб даю, мамой клянусь и ты чо, мне не веришь?
Субстанция что мы мешаем для себя любимого должна быть активной как по форме, так и по содержанию
Т.е. и наполнитель и содержимое должны все время быть активны, а не как мастика которая засохла и под ней ржавеет или мовиль(производства нонейм), который отвалится после засыхания кусками засохшей плёнки.
ничего не буду утверждать, хотелось бы услышать мнение всемогущих пользователей
Как Это сделать самому?
Кто нибудь делал?
вот тут с 5й минуты отзыв о качественном растворе ML от российского производителя.
PS: ниже небольшой конспект на тему что я нашёл для себя любимого по теме, собирая копипасты по форумам.В том числе отзывы о качественных антикорах разных марок.
Изобретение антикора. часть 2

С тех пор я много чего изучил нового, что то освежил в памяти и после всего еще не ходил смотреть на результаты )))) По сути я шел уже проверенным путем… Понятно, что придумать что то новое в этой области сложно, остается только уложить все в голове. Не уверен, что дочитаете до конца, но ладно… Цель — понять из чего сейчас делают антикоры и как нас обманывают и чему верить… Скажу сразу — речь не про то, как растворить пушсало в отработке(в прошлый раз про это много писали и думали), все намного серьезнее…
Итак, основные моменты и вопросы:
1. Нас интересует процесс защиты от коррозии внутренних полостей автомобиля. Что там внутри? Вода, земля, какие то противогололедные реагенты, мертвые мухи и кислород воздуха. Среда может быть как кислой, так и щелочной. Для нас важна ситуация, при которой рН2. Что происходит процессе коррозии, какие основные элементы принимают участие в этом процессе? Железо, окисляясь переходит в раствор, за счет этого кислород восстанавливается и также переходит в раствор(вместо кислорода может не плохо вступать во взаимодействие и обычный углекислый газ, образуя HCO3(-)) )))) (Если интересны подробности — погуглите "анодное растворение железа, анодная коррозия и т.д. — я и так боюсь, что до конца люди просто откажутся читать, видя такое большое количество сложной информации") Из вышесказанного и того, что говорили на уроках химии следует, что необходим еще некий электролит — вода с растворенными в ней солями… Т.е. чтобы химическая реакция шла, необходимо, чтобы ионы железа кто то сольватировал и переводил в раствор, унося из зоны реакции, перемещая равновесие в сторону прямой химической реакции. В раствор Fe(2+) могут "уносить" самые разные анионы, Сl(-), SO4 (2-) и т.д.
3. По какой причине внутренние полости вообще ржавеют, — они же обработаны с завода и т.д? И почему сильнее всего ржавеют всякие швы, т.е. места, в которых кислорода мало, а в соответствии с п.2 нам необходим кислород? Я думаю, что во время эксплуатации кузов испытывает знакопеременные нагрузки, деформируется и это приводит к микротрещинам защитного покрытия. Таким образом железо и кислород начинают взаимодействовать в соответствии с п.2 Процесс растрескивания защитного покрытия я обнаружил на своем автомобиле внутри задней арки — прям по сварочному шву.(задняя верхняя часть арки — проверьте у себя).
Отсюда уже видно, что чудес не бывает и все сводится к защите поверхности металла (ну или удалению кислорода, аналогично — в случае коррозии из за взаимодействия металла с кислотой надо или защищать поверхность, или удалять кислоту ))) . Удалить кислород, закачивая в пороги азот — хорошая идея, но наверно это не наш метод… Аналогично и с проблемой удаления электролита. Как нам защитить поверхность металла, которая находится внутри и неизвестно где? Понятно как — разбрызгать что то максимально полно и при этом оно должно проникать в эти микротрещины (могут быть еще дефекты с завода и просто голые участки металла внутри порогов, но это мы не будем рассматривать, а если у Вас этот самый случай — просто сожгите свой автомобиль и купите себе Jeep! )) ) Говоря сухим научным языком — нам необходим анодный ингибитор в избытке! На катодные процессы (восстановление кислорода и еще чего попало) мы влиять не можем. Так же не рассматриваем влияние сероводорода на коррозию наших кузовов. Надеюсь, что он не оказывает, иначе опа (((( Очень опасная в этом смысле штука… — у него есть одна особенность, из за которой он выступает "катализатором" коррозии, но тут не будем это рассматривать. (Надеюсь, что у нас в порогах нет источника сероводорода в виде разлагающихся белковых структур.)
Но разбрызгать по поверхности — еще не значит защитить ее… Необходимо что то, что сцепляется с железом лучше, чем электролит…Тогда, приклеившись к поверхности железа, наше соединение не позволит идти электрохимической реакции. Не будем долго ломать голову, ученые все сделали до нас, это практически любые химические соединения, содержащие азот, серу и т.д. Хорошим соединением в этом смысле является бензотриазол[1,2,3].(Так же хорошие результаты были получены и при использовании аналогичных гетероциклических соединений, например имидазолинов [4], триэтаноламин[5] и т.д.) Но есть нюанс — это порошок по вполне понятным причинам. И по тем же причинам понятно, что в воде он слоборастворим, но хорошо растворим во всяких: бензол, толуол и т.д.
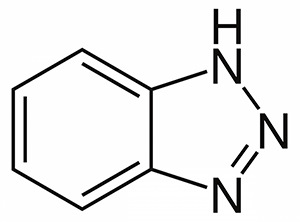
По известным причинам [6] с уменьшением рН(увеличение кислотности среды) защитные свойства бензотриазола уменьшаются. Это необходимо помнить при использовании ингибитора.
Так же к пассивации железа приводят и соли жирных кислот — карбоксилаты. К примеру карбоксилат натрия. Они точно так же адсорбируется на поверхности железа, защищая его от коррозии. [7,8]
Следует так же упомянуть про синергизм — т.е. если мы применяем смесь каких либо ингибиторов, то результирующее действие может быть сильнее, чем действие каждого ингибитора по отдельности. (Только учтите, что могут, а не обязаны! — для этого проводятся отдельные исследования, к примеру в работе [9] рассказывается что смесь фенилантранилата натрия и фенилундеканоата натрия в мольном соотношении 3:1 проявляет значительно более сильные ингибирующие свойства, чем скажем олеат натрия или нитрит натрия (известный неорганических ингибитор — его не рассматриваем(как и фосфаты), там слишком все просто а развитие всегда двигалось и двигается в сторону органической химии)) Можете погуглить — есть масса патентов, в которых рассказывается про изобретение новых ингибиторов, в которых совместно с бензотриазолом используется соль олеиновой кислоты, вот пример [10] (удивительно, в патенте приведенв именно олеиновая кислота, а не ее соль, что было бы логично, видимо при этих концентрациях и просто сам бензотриазол не плохо работает! )
Изучая различные литературные источники я наткнулся на интересную таблицу (см.ниже) В ней ученые обрабатывали пластины металла в различных ингибиторах, а затем помещали в среду со 100% влажностью и вдобавок коденсировали на них воду и смотрели кто сколько продержится. Вот результаты испытаний:
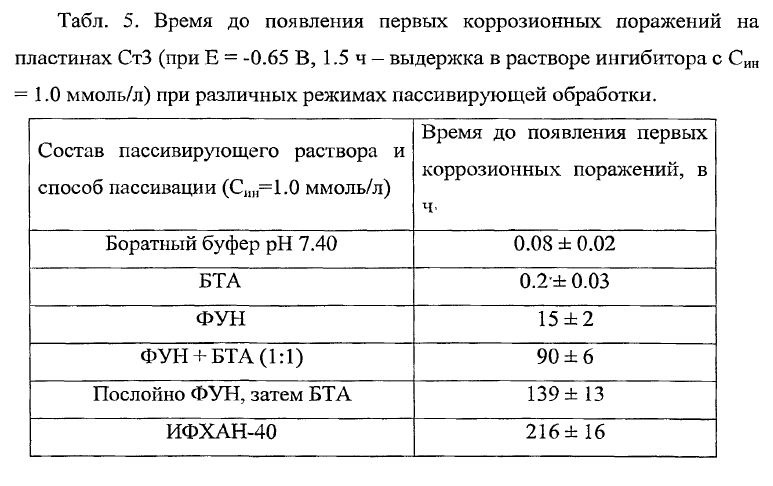
Видно, что сам по себе бензотриазол не очень хорош — смывается зараза (по этойпричине я в лес не ходил смотреть — что у меня получилось…)
Сокращения, которые есть в таблице:
БТА — бензотриазол
ФАН — фенилантранилат натрия (карбоксилат, соль жирной кислоты, у которой на конце фенил крутится)
ФУН — фенилундеканоат натрия (тоже карбоксилат, соль жирной кислоты, у которой на конце фенил крутится)
Видно, что попытки БТА (давайте так его называть) удержаться на поверхности металла честно говоря не очень успешны… Видимо, его гидрофобность оставляет желать лучшего… Но есть и другой вывод — для повышения эффективности ингибитора необходимо сконцентрироваться на создании нанослоев органических
ингибиторов коррозии. Именно это мы и наблюдаем при последовательной обработки сначала карбоксилатом, а затем БТА. Механизм расписывать не буду — он интересный и неоднозначный, но и так не особо уверен, что до сюда люди дочитали (((
ИФХАН-40 — это судя по всему выпускаемый ингибитор коррозии, но на сайте производителя ничего не нашел про ифханы, в базах патентов тоже ничего нет. Но в какую сторону двигаться — уже понятно…
Таблица — размещенная выше имеет смысл только для очищенного чистого железа в лабораторных условиях. В жизни мы будем иметь дело с уже окисленным металлом и тут ситуация немного другая:
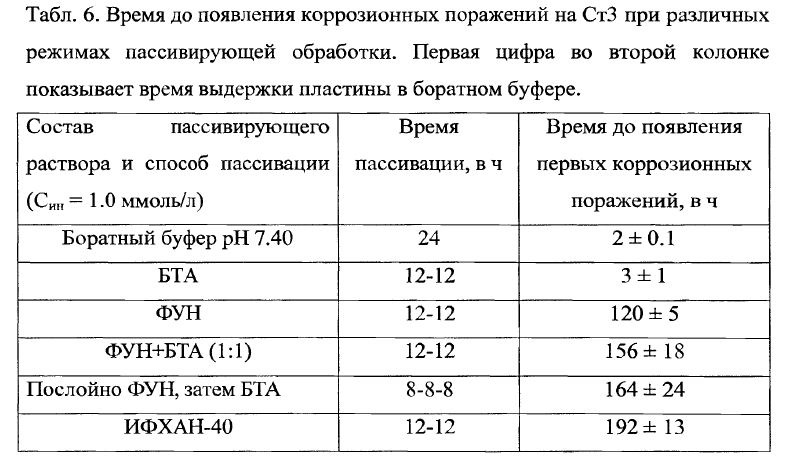
Видно, что последовательное нанесение веществ уже не так критично(ФУН+БТА).
То, что ИФХАН-40 оказался на высоте, скорее всего обусловлено дополнительными компонентами, которые входят в его состав (триэтаноламин к примеру, возможно, что еще что-то)…
К сожалению у меня пока нет полярографа или какого то аналогичного оборудования, позволяющего определять величину перенапряжения электрода, — это один из способов определения хороший у нас получился ингибитор или не очень… Но в скором времени, возможно, что такое оборудование у меня появится и можно будет продолжить изучение вопроса…
Так, с коррозией, вызванной кислородом воздуха мы разобрались — тут в общем все понятно, бензотриазол + карбоксилаты, можно добавить замещенных аминов (диэтиламин, триэтиламин). Теперь давайте посмотрим — что делать в случае кислотной коррозии?
Хороший опыт борьбы с этим видом коррозии выработан у нефтянников — добываемая нефть содержит кислоты, которые как раз и вызывают такую коррозию. Что же они придумали? А много чего [11] С механизмом действия все в принципе понятно: Ингибиторы кислотной коррозии тормозят процесс разрушения металла за счет увеличения поляризуемости анодного, катодного либо обоих электродных процессов. Ну катодный процесс мы откинем — я все еще не уверен, что можем на него влиять… Увеличение поляризуемости говорит о том, что оторвать электрон от железа стало труднее, а значит оно уже так легко не переходит в раствор… Единого строгого описания механизма действия в литературе я не нашел, но можно предположить, что анодное ингибирующее действие объясняется тем, что миграция электронов происходит скорее от железа к положительно заряженному ингибитору, чем к катодным участкам поверхности и на этом процесс останавливается )))))
В качестве таких веществ выступают катапины:
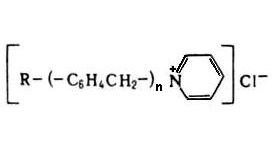
Пеназолин(ПАВ-466) — это разновидность имидазолинов(к примеру бензиламмонийимидазолинхлорид).
В промышленности известен ингибитор КИ-1, который состоит из водного раствора катапина (25%) и уротропина (25%), так вот если его добавить к серной кислоте и опустить туда ржавую железную деталь, то железо растворяться не будет, а вот все оксиды растворятся… Вот как это работает!
Интересный факт: соединение додецилдиметилбензиламмонийхлорид(и диоктадецилдиметиламмонийхлорид), т.е. алифатическое-четвертичное производное аммония, запатентованны компанией Эссо и эффективны для сырой нефти при концентрации 0,001%. Эти материалы эффективны в кислых скважинах даже при значении рН от 2 до 5.(Очень кислые среды)
Короче, мы видим с Вами все те же азот содержащие соединения…
Очень хорошее описание процессов ингибирования кислотной коррозии я встретил вот в этой книге [12] Всю пересказывать не буду, там много внимания уделяется высокотемпературным ингибиторам(рабочие температуры за 100С) на основе ацетиленовых производных, просто отмечу ряд моментов. С повышением температуры эффективность ингибиторов как правило повышается, затем после примерно 80 градусов резко падает. Для нас это в принципе пофигу, нам важны более низкие температуры, дожди и тому подобные капризы природы.
Ну и на последок — что выпускает наша промышленность и что не рекламируется так, как растстор, краун и т.д.:
Росоил-700
Состав:
Олеиновая кислота
Борная кислота
Диэтаноламин
Триэтаноламин
Бензотриазол
Окисленный петролатум
Индустриальное масло
Применяется для защиты листового металлопроката в условиях тропиков, сроком до 6-ти месяцев(пишу по памяти, могу ошибаться)
Как видите — все в пределах нашей теории, только надо заменить олеиновую кислоту на ее соль и получим то, что нам необходимо — антикор для скрытых полостей. Окисленный петролатум — это для вязкости, зачем борная кислота, пока не понятно, но уверен, что для того, чтобы не развивались микроорганизмы…
Тадам! встречайте, выглядит, как г@вно и упаковка оттуда же, но походу должно реально работать… Я таким вещам доверяю больше, чем растопам, клонам мовилей, солидолам, динитролам и т.д.

PS: Кстати, я вот все писал про эффективность действия ингибиторов и т.д., но не рассказал — а как все таки проверяют это самое действие. Рассказываю — есть методика на испытания: ГОСТ 9.054-75 (может есть и новее, я особо не искал, но что то читал про дополнительную проверку сероводородом (имеет значение для нефтедобывающих производств)), которая включает 6 методов ухреначить подопытную железяку… )))
Литература.
1. Cotton J.B. US Pat. 933979 On. 14.08.1963
2. Aiken J.K. Copper Corrosion and its Consequences // Products Finishing. -1959.-V. 12.-№10-P. 90-92
3. Кузнецов Ю.И., Казанский JI.П. Физико-химические аспекты защиты металлов ингибиторами коррозии класса азолов // Успехи химии. 2008. — Т. 77. — № 3. — С. 227-242
4. М.Д. Плотникова, М.И. Пантелеева, А.Б. Шеин Антикоррозионная защита малоуглеродистой стали ингибиторами серии «Флэк» // Вестник ТГУ, т.18, вып.5, 2013, С. 2309-2313
5. А.Р. Фархутдинова, Н.И. Мукатдисов, А.А. Елпидинский, А.А. Гречухина Составы ингибиторов коррозии для различных сред // Вестник Казанского технологического университета. 2013. Т. 16. № 4. С. 272-276
6. М.О.Агафонкина Ингибирование коррозии черных и цветных металлов в нейтральных средах 1,2,3-бензотриазолом и его композициями с солями карбоновых кислот // Диссертация. Институт Физической Химии и Электрохимии им. А.Н. Фрумкина РАН. 2011
7. Шмелева Н.К., Баранник В.П. Замедление коррозии стали в воде присадками солей одно- и двухосновных органических кислот // Журнал прикладной химии. 1963. — Т. 36. — С. 813-817
8. Лубенский А.П., Подобаев Н.И., Новиков В.Е. Электрохимическое растворение железа в нейтральных растворах солей карбоновых кислот // Защита металлов. 1972. — Т. 8. — № 5. — С. 570-571
9. Mohai M. XPS MultiQuant. Copyright © 1999-2005
10. В.Ю. Шолом, А.М. Казаков, Н.В. Савельева, А.Н. Абрамов // Консервационное масло "росойл-700". Патент на изобретение №: 2232794
11. Г.Р. Хайдарова Ингибиторы коррозии для защиты нефтепромыслового оборудования // Современные проблемы науки и образования. 2014. № 6. С. 286.
12. Е.С. Иванов Ингибиторы коррозии металлов в кислых средах. Металлургия. 1986г
12 лучших преобразователей ржавчины
Любая железная поверхность, даже будь это нержавейка, чугун, цветной металл или сплав, подвержена разрушению коррозией. В нашем обзоре представлены самые эффективные, безопасные и приемлемые по цене преобразователи ржавчины.
Не забудьте подписаться на наш канал в Telegram.

Какой преобразователь ржавчины лучше купить
На прилавках магазинов в изобилии продаются преобразователи в форме аэрозолей, жидкостей и геля. Но принцип действия любого преобразователя ржавчины зависит от основного химического вещества.
Большинство модификаторов изготовлено на основе кислот – ортофосфорной или оксикарбоновой. Некоторые содержат одновременно несколько компонентов. Такие средства превращают оксид железа в инертную соль, легко счищаемую с поверхности. Главный минус этой группы – необходимость смывать раствор после применения, во избежание излишнего разъедания ею металла. Подобные преобразователи эффективно справляются с ржавчиной на любой стадии, безопасны как для толстого, так и для тонкого железа. Работать с ними можно даже при минусовой температуре.
Кислотная химия широко применяется для обработки кузовов автомобилей, бытовых приборов и строительных конструкций из металла.
Нейтральные преобразователи на основе растительных танинов и специальных присадок также эффективно нейтрализуют коррозию. Отсутствие в составе таких средств опасных кислот позволяет очищать более деликатные поверхности черных и цветных металлов, сплавов. Ними обрабатывают внутренние узлы авто, готовят железо к бетонированию и покрытию мастикой. Нейтральные преобразователи не нуждаются в смывке, а за счет добавок проникают в глубокие слои ржавчины (150 мкм и более).
Самыми современными средствами в борьбе с коррозией считаются преобразователи ржавчины в грунт. Большинство составов этого вида изготовлены на основе оксида цинка или марганца, дубильной кислоты и органических полимеров. Вступая в химическую реакцию с кислородом, перечисленные вещества разрушают ржавчину и образуют на поверхности твердый защитный слой, предотвращающий ее появление в будущем.
Важное условие – перед нанесением необходимо тщательно зачистить поврежденный участок наждачкой. Такими растворами часто обрабатывают днище и колесные арки кузова, что делает их устойчивыми к проникновению влаги и химических реагентов.
Лучшие преобразователи ржавчины в жидком виде
Среди всех форм выпуска преобразователи в жидком виде представлены наиболее широко. Средства наносятся кистью, тряпкой или ручным пульверизатором, за счет чего можно экономно обработать обширную площадь поверхности. Жидкий раствор легко затекает в самые маленькие щели, добираясь до всех очагов коррозии. Кроме того, подобные модификаторы обходятся гораздо дешевле гелей или аэрозолей.
Читайте также:

