Электроны и дырки в металлах
Обновлено: 17.06.2024
1.2.1. Энергетические зоны. Свободные носители зарядов: электроны и дырки.
Известно, что первичными и единственными носителями заряда являются электроны и протоны. В вакууме и газах электроны и протоны могут быть свободными, в твердых телах и жидкостях электроны и протоны связаны с атомами и их заряды нейтрализуют друг друга.
Полупроводниковые кристаллы образуются из атомов, расположенных в определенном порядке. Естественно возникает вопрос, если в атоме электроны связаны с ядром, то откуда в состоящем из атомов кристалле берутся свободные заряды, способные перемещаться по кристаллу создавая электрический ток. Действительно, если представить атом как изолированный шарик, то тело полученное из миллиардов уложенных в правильном порядке шариков все равно останется изолятором, поскольку в нем способные переносить заряд не появятся. Для того, чтобы объяснить как в металлах и полупроводниках появляются свободные электроны необходимо использовать закономерности микромира. Впервые эти закономерности были использованы Бором для объяснения электронной структуры атома. Работы бора стимулировали работы по квантовой механике, которая в настоящее время используется для объяснения поведения электронов в атомах, молекулах и твердых телах.
Согласно современным представлениям атомы состоят из положительно заряженных ядер вокруг которых распложены заполненные электронами оболочки. При этом каждому электрону соответствует строго определенный уровень, на котором не может находиться более двух электронов с разными значениями спина, характеризующего вращение электрона. В магнитном поле этот уровень расщепляется на два близко расположенных уровня.
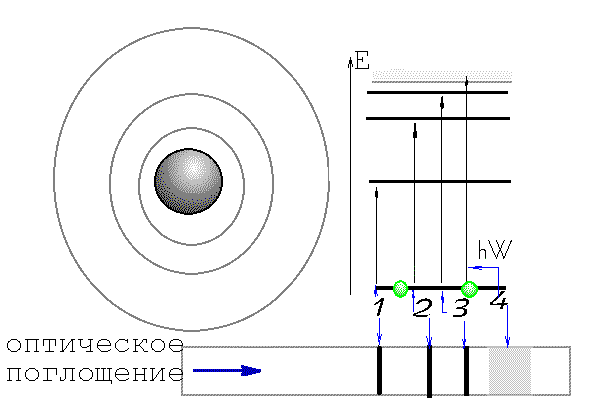
Согласно законам квантовой механики, электроны могут находиться только в строго определенных энергетических состояниях. Изменение энергии электрона возможно при поглощении или испускании кванта электромагнитного излучения с энергией, равной разности значений энергий на начальном и конечном уровне. Поэтому оптические спектры поглощения (или излучения) атомов, соответствующие электронным переходам на свободные дискретные уровни, так же должны быть дискретны, что и наблюдается в экспериментах (рис. 1.5.)

Рис. 1.5. Диаграмма, иллюстрирующая энергетический спектр электронов в атоме (модель Бора) и ожидаемый спектр поглощения.
Электронные оболочки принято обозначать буквами и числами (N). Число N называют главным квантовым. Отсчет его значения осуществляется от уровня, ближайшей к ядру N = 1, 2, 3, 4 и т.д., оболочки имеют соответствующие буквенные обозначения: K, L, M, N, и т.д.
На каждой оболочке может находиться несколько электронов, причем каждому из них соответствует свой энергетический уровень, со своим пространственным распределением заряда, который часто называют орбиталью. Энергетические уровни электронов (орбитали) внутри оболочки (с одним числом N) принято обозначать буквами: s (нижний уровень), p, d, f и т.д. Причем чем выше энергия оболочки (больше N), тем большее число электронов может на ней находиться, или другими словами ей соответствует большее число орбиталей. Так первой оболочке соответствует один уровень - орбиталь 1s, т.е. на этой оболочке могут находиться только два электрона с разными спинами. Соответственно конфигурацию с одной оболочкой имеют только два атома – водорода и гелия.
Второй оболочке соответствуют три уровня: одна орбиталь 2s и три орбитали 2p, т.е. в этой оболочке могут находиться шесть электронов.
Третей оболочке соответствуют девять уровней: одна орбиталь 3s, три орбитали 3p, пять орбиталей 3d, т.е. в этой оболочке могут находиться до 18 электронов.
При увеличении числа электронов в атоме, заполнение оболочек происходит по определенным правилам:
первыми заполняются низшие по энергии орбитали ;
на любой орбитали может находиться не более двух электронов с противоположными значениями спина (принцип запрета Паули);
заполнение орбиталей одной оболочки начинается одиночными электронами с параллельными спинами, пары начинают образовываться только после того как каждая орбиталь имеет по одному электрону (правило Гунда).
Именно на основе правил заполнения оболочек построена периодическая таблица элементов Д.И. Менделеева. Один ряд таблицы соответствует элементам, в которых происходит заполнение внешней (валентной) оболочки, переход от одной ячейке к другой в пределах ряда соответствует добавлению одного электрона.
При сближении двух атомов , например водорода, их орбитали начинают перекрываться и возможно возникновение связи между ними. Существует правило, согласно которому число орбиталей у молекулы равно сумме чисел орбиталей у атомов, при этом взаимодействие атомов приводит к тому, что уровни у молекулы расщепляются, при этом чем меньше расстояние между атомами, тем сильнее это расщепление.
На рис. 1.6. показана схема расщепления уровней для пяти атомов при уменьшении расстояния между ними. Как видно из графиков при образовании между атомами связей валентные электроны формируют разрешенные для электронов зоны, причем число состояний в этих зонах тем больше, чем больше взаимодействующих атомов. В кристаллах число атомов более чем 10 22 см -3 , примерно такое же количество уровней в зонах. При этом расстояние между уровнями становится чрезвычайно малым, что позволяет считать, что энергия в разрешенной зоне изменяется непрерывно. Тогда электрон, попавший в незанятую зону можно рассматривать как классический, считая, что под действием электрического поля он набирает непрерывно энергию, а не квантами, т.е. ведет себя как классическая частица.

Рис. 1.6. Энергетическое расщепление 1s и 2s уровней для пяти атомов в зависимости от расстояния между ними
При образовании кристаллов образуемые валентными электронами зоны могут быть частично заполненными, свободными или полностью заполненными электронами. При этом если между заполненными и свободными состояниями запрещенная зона отсутствует, то материал является проводником, если существует небольшая запрещенная зона, то это полупроводник, если запрещенная зона большая и электроны за счет тепловой энергии в нее не попадают, то это изолятор. Рисунок 1.7. иллюстрирует возможные конфигурации зон.
Для проводников разрешенная зона частично заполнена электронами, поэтому даже при приложении внешнего напряжения они способны набирать энергию и перемещаться по кристаллу. Такая структура зон характерна для металлов. Уровень F, разделяющий заполненную электронами и незаполненную часть зоны называют уровнем Ферми. Формально его определяют как уровень вероятность заполнения которого электронами равна 1/2.

Рис. 1.7. Возможная структура энергетических зон, создаваемых валентными электронами в кристаллах
Для полупроводников и диэлектриков структура зон такова, что нижняя разрешенная зона полностью заполнена валентными электронами, поэтому ее называют валентной. Потолок валентной зоны обозначают Ev. В ней электроны перемещаться под действием поля (и соответственно набирать энергию) не могут, поскольку все энергетические уровни заняты, а согласно принципу Паули электрон не может переходить с занятого состояния на занятое. Поэтому электроны в полностью заполненной валентной зоны не участвуют в создании электропроводности. Верхняя зона в полупроводниках и диэлектриках в отсутствии внешнего возбуждения свободна от электронов и если каким либо образом туда забросить электрон, то под действием электрического поля он может создавать электропроводность, поэтому эту зону называют зоной проводимости. Дно зоны проводимости принято обозначать Ec. Между зоной проводимости и валентной зоной находится запрещенная зона Eg, в которой согласно законам квантовой механики электроны находиться не могут (подобно тому как электроны в атоме не могут иметь энергии не соответствующие энергиям электронных оболочек). Для ширины запрещенной зоны можно записать:
В полупроводниках в отличие от изоляторов ширина запрещенной зоны меньше, это сказывается в том что при нагреве материала в зону проводимости полупроводника попадает за счет тепловой энергии значительно больше электронов, чем в зону проводимости изолятора и проводимость полупроводника может быть на несколько порядков выше чем проводимость изолятора, однако граница между полупроводником и изолятором условная.
Поскольку в отсутствии внешнего возбуждения валентная зона полностью заполнена (вероятность нахождения электрона на Ev = 1), зона проводимости полностью свободна (вероятность нахождения электрона на Eс = 0), то формально уровень Ферми с вероятностью заполнения ½ должен был бы находиться в запрещенной зоне. Расчеты показывают, что действительно в беспримесных бездефектных полупроводниках и диэлектриках (их принято называть собственными) он лежит вблизи середины запрещенной зоны. Однако электроны там находится не могут, поскольку там нет разрешенных энергетических уровней.
Основные элементарные полупроводники относятся к четвертой группе таблицы Менделеева, они имеют на внешней оболочке 4 электрона. Соответственно эти электроны находятся в S (1 электрон) и p (3 электрона). При образовании кристалла внешние электроны взаимодействуют и образуются полностью заполненная оболочка с восьмью электронами, как это показано на диаграмме рис. 1.7.

Рис. 1.7. Схематическое представление бездефектного кристалла кремния.
Элементы четвертой групп используют четыре электрона находящихся в s и p орбиталях, но в разных электронных оболочках (N изменяется от 2 для С до 6 для Pb). При взаимодействии образуется гибридная sp 3 орбиталь) в ее образовании участвует одна s орбиталь и 3p – орбитали). Эта орбиталь состоит из гибридизированных четырех орбиталей каждая из которых с учетом спина может принять четыре электрона и таким образом образуется заполненная внешняя оболочка с восьмью электронами. При этом атом может образовывать химические связи с четырьмя соседями, т.е. является четырежды координированными. Все связи эквивалентны и образуют тетраэдрическую решетку (тетраэдр – фигура с четырьмя одинаковыми поверхностями). Схема образования гибридной sp 3 орбитали показана на рис. 1.8.
Тетраэдрическая структура свойственна кристаллам алмаза. Такие известные полупроводники как Si и Ge имеют структуру типа алмаза, это и понятно, поскольку у них внешние электроны находятся на sp 3 орбиталях.

Рис. 1.8. Схема образования гибридной sp 3 орбитали и соответственно тетраэдрической структуры кристалла (типа алмаза).
На рис. 1.9 показана схема образования энергетических зон и sp 3 орбиталей для кристаллов других элементов четвертой группы периодической системы элементов Д.И. Менделеева. Как видно из рисунка все зоны формируются на основе s и p состояний, но принадлежащих к разным оболочкам (различно значение главного квантового числа N). Так для углерода валентная оболочка формируется из 2s и 2p состояний соответственно структура алмаза определяется гибридными 2sp 3 состояниями. Для Si валентная оболочка формируется из 3s и 3p состояний атома Si, соответственно структура кристаллической решетки создается 3sp 3 орбиталями, является тетраэдрической и аналогична структуре алмаза. В Ge в образовании химических связей участвую 4s и 4p электроны, Sn 5s и 5p электроны и т.д. При этом для образовавшаяся sp 3 оказывается полностью заполненной, верхняя полностью свободной, т.е. имеет место энергетическая структура соответствующая полупроводникам и диэлектрикам с валентной зоной и зоной проводимости. Следует обратить внимание на тот факт, что по мере роста числа N , движении по группе таблицы Менделеева сверху вниз, ширина запрещенной зоны уменьшается и для свинца обе зоны перекрываются, т.е. для этого материала реализуется зонная структура, характерная для проводника.

Рис. 1.9. Схема образования зон элементарных полупроводников четвертой группы периодической системы элементов.
Следует отметить, что sp 3 гибридизация может происходить не только для кристаллов элементарных полупроводников, но и для полупроводниковых соединения. Необходимым для этого условием является то, чтобы электроны внешней оболочки исходных компонентов принадлежали к s и p оболочкам и чтобы суммарное число на внешней оболочки соединения равнялось 8 (тогда нижняя зона оказывается полностью заполненной). Последнее условие будет выполняться для соединений элементов первой и седьмой групп, второй и шестой, третьей и пятой, т.е. для соединений A 1 B 7 , A 2 B 6 , A 3 B 5 . Действительно большинство из этих соединений является полупроводниками, причем для них так же выполняется правило, что с увеличением номера электронной оболочки атомов из которых образуется соединение ширина запрещенной зоны уменьшается.
В качестве примера рассмотрим такое несколько полупроводниковых соединений. Примеры из группы A 3 B 5 : GaAs: Eg = 1.43эВ (при Т=300К), атомы компонентов имеют электронную конфигурацию внешних оболочек – 3s 2 4p 1 (Ga), 4p 3 (As); InSb: Eg=0.18 эВ (при Т=300К), электронная конфигурация валентной оболочки – 4s 2 4p 1 (In), 5p 3 (Sb).
При уходе электрона в зону проводимости он делокализуется и может перемещаться по зоне от одного атома к другому. Он становится электроном проводимости и может создавать электрический ток. Обычно говорят: появился свободный носитель заряда, хотя на самом деле электрон не покидал кристалл, у него только появилась возможность перемещаться из одного места кристалла в другое.
На месте откуда ушел электрон условие электронейтральности нарушается и возникает положительно заряженная вакансия электрона, которую принято называть дыркой (положительный заряд обусловлен не скомпенсированным зарядом ядра).
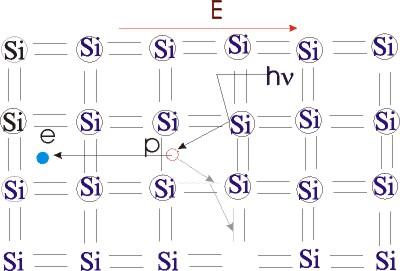
На место откуда ушел электрон может переместиться соседний электрон, что приведет к перемещению положительно заряженной дырки. Таким образом перемещение валентных электронов заполняющих свободное электронное состояние (запрет Паули снят) приводит к перемещению вакансии в которой нарушено условие компенсации заряда, т.е. дырки. Вместо того, чтобы рассматривать движение валентных электронов, которых в валентной зоне чрезвычайно много рассматривают перемещение положительно заряженных дырок, которых мало и которые так же как электроны могут переносить заряд. Этот процесс поясняет рис. 1.10.
На рисунке 1.10 показан кристалл, в котором каким либо внешним возбуждением, например квантом света с hν > Eg один из электронов переброшен в зону проводимости (стал свободным), т.е. у одного из атомов была разорвана одна из валентных связей. Тогда в кристалле помимо не связанного с атомом электрона возник положительно заряженный ион. Способность под действием поля перемещаться самого иона очень мала, поэтому ее учитывать не следует. Поскольку в кристалле атомы расположены близко друг от друга к этому иону может притянуться электрон от соседнего атома. В этом случае положительная дырка возникает у соседнего атома откуда ушел валентный электрон и т.д. Для совершенного, не имеющего примесей и дефектов, кристалла концентрация электронов будет равна концентрации дырок. Это собственная концентрация носителей заряда ni = pi, значок i означает концентрацию носителей для собственного полупроводника (intrinsic –собственный). Для произведения концентраций электронов и дырок можно записать:
Следует отметить, то это соотношение выполняется не только для полупроводников с собственной проводимостью, но и для легированных кристаллов, в которых концентрация электронов не равна концентрации дырок.

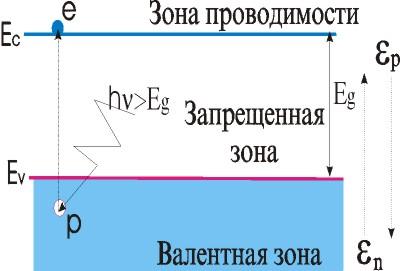
Рис. 1.10. Схематическое изображение возникновения электрона и дырки при поглощении света
Направление движения дырки отложено направлению движения электрона. Каждый электрон находящийся в валентной связи характеризуется своим уровнем. Все уровни валентных электронов расположены очень близко и образуют валентную зону, поэтому перемещение дырки можно рассматривать как непрерывный процесс, аналогичный движению классической свободной частицы. Аналогично поскольку в зоне проводимости энергетические уровни расположены очень близко, зависимость энергии от импульса можно считать непрерывной и соответственно движение электрона можно в первом приближении рассматривать как движение классической свободной частицы. Таким образом разгоняемый (говорят разогреваемый) электрическим полем электрон в твердом теле на энергетической диаграмме перемещается от дна зоны проводимости к ее потолку. Аналогично дырка разогреваемая полем перемещается от потолка валентной зоны к ее дну (для нее отсчет энергии идет относительно электрона в другую сторону). Поведение электрона и дырки, как квазиклассических частиц нарушается в тот момент когда они достигают высокоэнергетической границы энергетической зоны. Для свободного классического электрона таких границ нет и теоретически его можно разгонять вплоть до скорости свет. Электрон в твердом теле достигший потолка зоны проводимости должен упруго от нее отразится и пойти в обратном направлении, достигнув дна зоны проводимости он отражается от него и идет вверх и т.д. Таким образом если бы удавалось разогреть электронный (или дырочный) газ в твердом теле до энергий порядка ширины разрешенной зоны, то должны были бы возникнуть мощные высокочастотные колебания. Однако осуществить такой разогрев не удается, поскольку горячие носители начинают взаимодействовать с решеткой, отдавая ей часть своей энергии, поэтому как для электронов, так и для дырок существует некоторое предельное значение скорости (насыщение скорости в электрическом поле) близкое к тепловой скорости электронов в твердом теле (10 6 – 10 7 см/c)

Рис. 1.11. Энергетическая диаграмма , поясняющая возникновение электрона и дырки в совершенном кристалле.
Таким образом в качестве носителей заряда в любой среде могут выступать способные перемещаться под действием электрического поля электроны - n, дырки - p, положительно и отрицательно заряженные ионы- ip и in . Для концентрации заряда в единице объема можно записать:
N = n + p + in + ip, (1.6)
Если (in + ip ) >> (n + p), то это материалы с ионной проводимостью, что типично для диэлектриков.
Если (n + p ) >> (in + ip), то это материалы с электронной проводимостью, это типично для полупроводников и металлов.
Зонная теория твердых тел
Квантовая физика описывает состояния электронов в атоме согласно схеме из четырех квантовых чисел. Квантовые числа описывают допустимые состояния, которые электроны могут принимать в атоме. Используя аналогию с амфитеатром, квантовые числа описывают, сколько доступно рядов и мест. Отдельные электроны могут быть описаны комбинацией квантовых чисел, как зритель в амфитеатре, занимающий конкретные ряд и место.
Как и зрители в амфитеатре, перемещающиеся между рядами и сиденьями, электроны могут изменять свое состояние, учитывая наличие доступных мест, которые они могут занять, и доступной энергии. Уровень оболочки тесно связан с количеством энергии, которой обладает электрон: «прыжки» между уровнями оболочек (и даже подоболочек) требуют передачи энергии. Если электрон перемещается на оболочку более высокого порядка, то требуется передача дополнительной энергии электрону от внешнего источника. Используя аналогию с амфитеатром, человеку необходимо больше энергии, чтобы перейти на более высокий ряд сидений, так как ему необходимо подняться на большую высоту, противодействуя силе тяжести. И наоборот, электрон «перепрыгивающий» на более низкую оболочку отдает часть своей энергии, как человек, прыгающий вниз на нижний ряд сидений; излишки энергии выделяются в виде тепла или звука.
Не все «прыжки» равнозначны. Прыжки между разными оболочками требуют существенного обмена энергией, а прыжки между подоболочками или орбиталями требуют обменов меньшим количеством энергии.
Когда атомы объединяются в вещество, наиболее удаленные оболочки, подоболочки и орбитали сливаются, обеспечивая большее количество доступных энергетических уровней, доступных электронам. Когда большое количество атомов расположены близко друг к другу, эти доступные энергетические уровни образуют почти непрерывную зону, в которой электроны могут перемещаться, как показано на рисунке ниже.
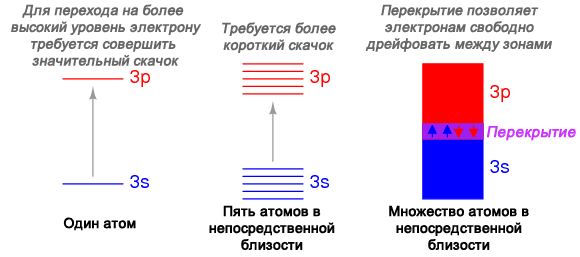
Перекрытие электронных зон в элементах металлов.
Ширина этих зон и их близость к существующим электронам определяют, как будут подвижны эти электроны при воздействии электрического поля. В металлических веществах пустое перекрытие зон и зоны, содержащие электроны, означают, что электроны одного атома могут перейти к тому, что обычно было состоянием более высокого уровня, под воздействием небольшого количества дополнительной энергии (или вовсе без нее). Таким образом, внешние электроны или, как говорят, «свободные» готовы перемещаться по мановению электрического поля.
Перекрытие зон происходит не во всех веществах, независимо от того, сколько атомов близки друг к другу. В некоторых веществах остается значительный разрыв между верхней зоной, содержащей электроны (так называемой валентной зоной) и следующей зоной, которая пуста (так называемой зоной проводимости). Смотрите рисунок ниже. В результате валентные электроны «связаны» с их атомами и не могут стать подвижными в веществе без значительного количества прикладываемой энергии. Эти вещества называются диэлектриками.
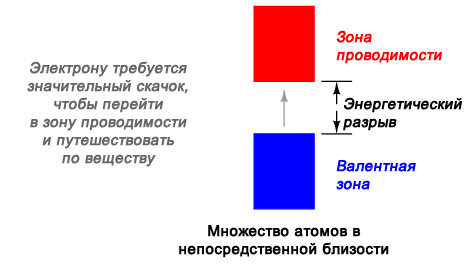
Разделение электронных зон в изолирующих материалах.
Материалы, которые попадают в категорию полупроводников, обладают узким разрывом между валентной зоной и зоной проводимости. Таким образом, количество энергии, необходимой для перемещения валентного электрона в зону проводимости, где он станет подвижным, весьма мало (рисунок ниже).
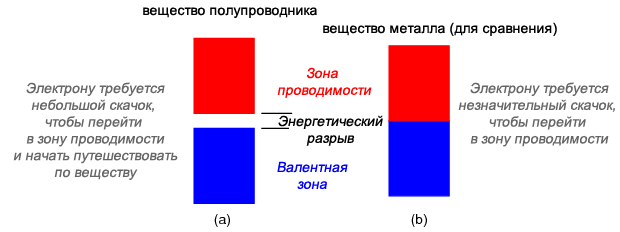
Разделение электронных зон в полупроводниковых материалах,
(a) множество близко расположенных атомов полупроводника все еще приводит к значительной запрещенной зоне,
(b) множество близко расположенных атомов металла для сравнения.
При низких температурах небольшая тепловая энергия способна выдавить валентные электроны от запрещенной зоны, и полупроводниковый материал начинает действовать больше как диэлектрик. При высоких температурах количества окружающей тепловой энергии становится достаточно, чтобы заставить электроны преодолеть разрыв, и материал увеличивает свою электрическую проводимость.
Трудно предсказать проводящие свойства вещества, исследуя конфигурации электронов его атомов. Хотя лучшие металлические проводники электричества (серебро, медь, золото) все обладают внешней s-подоболочкой с одним электроном, необязательно, что есть связь между проводимостью и количеством валентных электронов:
| Элемент | Удельное сопротивление (ρ), Ом·мм 2 /м при 20°C | Конфигурация электронов |
|---|---|---|
| Серебро (Ag) | 0,0162 | 4d 10 5s 1 |
| Медь (Cu) | 0,018 | 3d 10 4s 1 |
| Золото (Au) | 0,023 | 5d 10 6s 1 |
| Алюминий (Al) | 0,0295 | 3p 1 |
| Вольфрам (W) | 0,055 | 5d 4 6s 2 |
| Молибден (Mo) | 0,054 | 4d 5 5s 1 |
| Цинк (Zn) | 0,059 | 3d 10 4s 2 |
| Никель (Ni) | 0,087 | 3d 8 4s 2 |
| Железо (Fe) | 0,098 | 3d 6 4s 2 |
| Платина (Pt) | 0,107 | 5d 9 6s 1 |
Конфигурации электронных зон, создаваемых соединениями различных элементов, с трудом можно связать с электронными конфигурациями их составных элементов.
Итоги
Для удаления электрона из валентной зоны в более высокую свободную зону (зону проводимости) требуется энергия. Большая энергия требуется для перемещения между оболочками, меньшая – между подоболочками.
Валентная зона и зона проводимости в металлах перекрываются, и для перемещения электрона требуется малое количество энергии. Металлы являются отличными проводниками.
Большой разрыв между валентной зоной и зоной проводимости в диэлектрике требует большого количества энергии, чтобы перенести электрон из валентной зоны. Таким образом, диэлектрики не проводят электрический ток.
Полупроводники обладают небольшим разрывом между валентной зоной и зоной проводимости. Чистые полупроводники не являются ни хорошими диэлектриками, ни хорошими проводниками.
Электроны и «дырки»
Чистые полупроводники являются относительно хорошими диэлектриками по сравнению с металлами, хотя и не настолько хорошими, как настоящий диэлектрик, например, стекло. Чтобы быть полезным в полупроводниковых применениях, собственный полупроводник (чистый нелегированный полупроводник) должен иметь не более одного атома примеси на 10 миллиардов атомов полупроводника. Это аналогично крупинке соли в железнодорожном вагоне сахара. Нечистые, или грязные полупроводники являются значительно более проводящими, хотя и такими хорошими, как металлы. Почему так происходит? Чтобы ответить на этот вопрос, мы должны рассмотреть электронную структуру этих материалов на рисунке ниже.
Рисунок ниже (a) показывает 4 электрона в валентной оболочке полупроводника, образующих ковалентные связи с четырьмя другими атомами. Это плоская, более простая для рисования, версия рисунка, приведенного ранее. Все электроны атома связаны в четырех ковалентных связях, в парах общих электронов. Электроны не могут свободно перемещаться по кристаллической решетке. Таким образом, собственные, чистые, полупроводники являются относительно хорошими диэлектриками по сравнению с металлами.
(b) Тем не менее, тепловая энергия может создать несколько пар электрон-дырка, что в результате даст слабую проводимость.
Тепловая энергия иногда может освобождать электрон из кристаллической решетки, как показано на рисунке выше (b). Этому электрону становится доступно передвижение по кристаллической решетке. Когда электрон освобождается, он оставляет в кристаллической решетке пустое место с положительным зарядом, известное как дырка. Эта дырка не прикреплена к решетке и может свободно по ней перемещаться. Свободные электрон и дырка вносят свой вклад в движение электронов по кристаллической решетке. То есть, электрон свободен, пока он не попадает в дырку. Это явление называется рекомбинацией. При воздействии на полупроводник внешним электрическим полем электроны и дырки разводятся в противоположных направлениях. Увеличение температуры увеличит и количество электронов и дырок, что в свою очередь уменьшит сопротивление. Это противоположно поведению металлов, у которых сопротивление увеличивается с ростом температуры за счет увеличения столкновений электронов с кристаллической решеткой. Количество электронов и дырок в собственном полупроводнике одинаково. Тем не менее, оба носителя при воздействии внешнего поля необязательно будут двигаться с одинаковой скоростью. Другими словами, подвижность у электронов и дырок неодинакова.
Чистые полупроводники, сами по себе, не особенно полезны. Хотя полупроводники и должны быть в большой степени очищены от примесей для создания отправной точки перед добавлением определенных примесей.
В материал полупроводника, с долей содержания примесей 1 к 10 миллиардам, для увеличения количества носителей могут добавляться определенные примеси в соотношении примерно 1 часть на 10 миллионов. Добавление в полупроводник необходимой примеси известно, как легирование. Легирование увеличивает проводимость полупроводника, и, таким образом, он становится более сопоставим с металлом, а не с диэлектриком.
Можно увеличить количество отрицательно заряженных носителей в кристаллической решетке полупроводника путем легирования таким электронным донором, как фосфор. Электронные доноры, также известные, как примеси N-типа, включают в себя элементы группы VA (группы 15 по IUPAC) периодической таблицы: азот, фосфор, мышьяк и сурьма. Азот и фосфор являются примесью N-типа для алмаза. Фосфор, мышьяк и сурьма используются совместно с кремнием.
Кристаллическая решетка на рисунке ниже (b) содержит атомы, содержащие четыре электрона во внешней оболочке, формирующих ковалентные связи с соседними атомами. Эта кристаллическая решетка ожидаема. Добавление атома фосфора с пятью электронами во внешней оболочке вводит в решетку дополнительный электрон по сравнению с атомом кремния. Пятивалентная примесь образует четыре ковалентные связи с четырьмя атомами кремния с помощью четырех из пяти электронов, встраиваясь в решетку с одним электроном в запасе. Обратите внимание, что этот лишний электрон не сильно привязан к решетке, как электроны обычных атомов Si. Будучи не привязанным к узлу фосфора в кристаллической решетке, он свободен для перемещения по ней. Так как мы легировали одну часть фосфора на 10 миллионов атомов кремния, то по сравнению с многочисленными атомами кремния было создано лишь несколько свободных электронов. Тем не менее, по сравнению с немногочисленными парами электрон-дырка в собственном полупроводнике, в этом случае было создано достаточно много электронов.
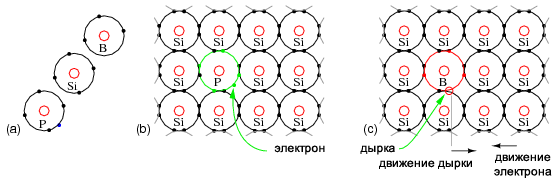
(a) Конфигурация электронов внешней оболочки донора N-типа фосфора, кремния (для сравнения) и акцептора P-типа бора.
(b) Примесь донора N-типа создает свободный электрон.
(c) Примесь акцептора P-типа создает дырку, положительно заряженный носитель.
Кроме того, можно вводить примеси, у которых, по сравнению с кремнием, не хватает электрона, то есть, которые имеют три электрона в валентной оболочке, по сравнению с кремнием с четырьмя валентными электронами. На рисунке выше (c) они оставляют пустое место, известное как дырка, положительно заряженный носитель. Атом бора пытается связаться с четырьмя атомами кремния, но в валентной зоне имеет только три электрона. В попытке сформировать четыре ковалентные связи три его электрона двигаются вокруг, пытаясь образовать четыре связи. Это заставляет двигаться появляющуюся дырку. Кроме того, трехвалентный атом может занимать электрон от соседнего (или более отдаленного) атома кремния, чтобы сформировать четыре ковалентные связи. Однако это оставляет атом кремния с нехваткой одного электрона. Другими словами, дырка перемещается к соседнему (или более отдаленному) атому кремния. Дырки располагаются в валентной зоне, уровнем ниже зоны проводимости. Легирование электронным акцептором, атомом, который может принять электрон, создает дефицит электронов и избыток дырок. Так как дырки являются носителями положительного заряда, примесь электронного акцептора также известна, как примесь P-типа. Легирующая примесь P-типа оставляет полупроводник с избытком дырок, носителей положительного заряда. Элементы P-типа из группы IIIA (группы 13 по IUPAC) периодической таблицы включают в себя: бор, алюминий, галлий и индий. Бор используется в качестве легирующей примеси P-типа для полупроводников кремний и алмаз, в то время как индий используется с германием.
Подобно «шарику в трубе» передвижение электронов (рисунок ниже) зависит от движения дырок и движения электронов. Шарик представляет собой электроны в проводнике, в трубе. Движение электронов слева направо в проводнике или полупроводнике N-типа объясняется входом электрона в трубу слева, заставляя выйти электрон справа. Передвижение электронов в полупроводнике N-типа происходит в зоне проводимости. Сравните это с движением дырок в валентной зоне.
(a) Электроны двигаются вправо в зоне проводимости.
(b) Дырки двигаются вправо в валентной зоне, в то время как электроны двигаются влево.
Чтобы дырка вошла в левой части рисунка выше (b), электрон должен быть удален. При перемещении дырки слева направо электрон должен двигаться справа налево. Первый электрон выбрасывается из левого конца трубы, чтобы дырка могла двигаться вправо в трубу. Электрон двигается в направлении, противоположном движению положительных дырок. Чтобы дырка двигалась дальше вправо, электроны должны перемещаться влево, заполняя дырку. Дырка – это отсутствие электрона в валентной зоне за счет легирования P-типа. Она имеет локальный положительный заряд. Чтобы переместить дырку в заданном направлении, валентные электроны двигаются в противоположном направлении.
Поток электронов в полупроводнике N-типа аналогичен движению электронов в металлическом проводе. Атомы примеси N-типа дадут электроны, доступные для передвижения. Эти электроны из-за легирующей примеси известны, как основные носители, так как они находятся в большинстве, по сравнению с немногочисленными тепловыми дырками. Если к пластине полупроводника N-типа приложить электрическое поле (рисунок ниже (a)), электроны перейдут в отрицательный (левый) конец пластины, пройдут кристаллическую решетку и выйдут справа к клемме (+) батареи.
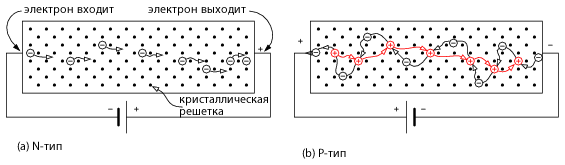
(a) Полупроводник N-типа с электронами, перемещающимися через кристаллическую решетку слева направо.
(b) Полупроводник P-типа с дырками, перемещающимися слева направо, что соответствует движению электронов в противоположном направлении.
Объяснить протекание тока в полупроводнике P-типа немного сложнее. Примесь P-типа, акцептор электронов, придает локальным областям положительный заряд, известный как дырки. Эти дырки и являются основными носителями в полупроводнике P-типа. Хотя дырки и образуются в местах трехвалентных атомов примеси, они могут перемещаться по пластине полупроводника. Обратите внимание, что включение батареи на рисунке выше (b) противоположно включению на рисунке (a). Положительный вывод батареи подключен к левому концу пластины P-типа. Поток электронов выходит из отрицательного вывода батареи и через пластину P-типа возвращается к положительному выводу батареи. Электрон покидает положительный (левый) конец пластины полупроводника, чтобы положительный вывод батареи оставил дырку в полупроводнике, которая может двигаться вправо. Дырки проходят через кристаллическую решетку слева направо. В отрицательном конце пластины электрон из батареи соединяется с дыркой, нейтрализуя её. Это дает возможность другой дырке в положительном конце пластины двигаться вправо. Имейте в виду, что когда дырки перемещаются слева направо, это на самом деле электроны двигаются в противоположном направлении, что и делает видимым движение дырок.
Элементы, используемые для производства полупроводников, приведены на рисунке ниже. Полупроводниковый материал германий из группы IVA (14 по IUPAC) сейчас используется довольно ограничено. Полупроводники на основе кремния составляют около 90% всего промышленного производства полупроводников. Полупроводники на основе алмаза сейчас широко исследуются и обладают значительным потенциалом. Составные полупроводники включают в себя кремний-германий (тонкие слои на пластинах Si), карбид кремния и соединения групп III-V, например, арсенид галлия. Полупроводниковые соединения групп III-VI включают в себя AlN, GaN, InN, AlP, AlAs, AlSb, GaP, GaAs, GaSb, InP, InAs, InSb, AlxGa1-xAs и InxGa1-xAs. Столбцы II и VI периодической таблицы, не показанные на рисунке, также формируют составные полупроводники.
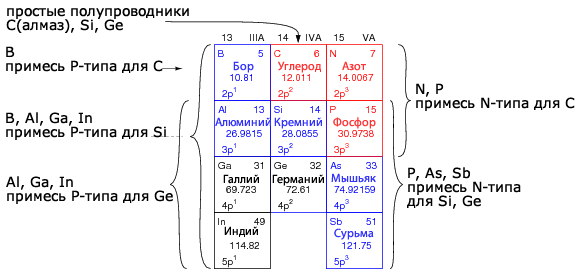
Группа IIIA – примеси P-типа, группа IV – основные полупроводниковые материалы, и группа VA – примеси N-типа.
Основной причиной включения групп IIIA и VA на рисунок выше является возможность показать примеси, используемые с группой полупроводников IVA. Элементы группы IIIA являются акцепторами, примесями P-типа, которые принимают электроны, оставляя дырки (положительные носители) в кристаллической решетке. Бор является примесью P-типа для алмаза и самой распространенной примесью для кремниевых полупроводников. Индий является примесью P-типа для германия.
Элементы группы VA являются донорами, примесями N-типа, дающими свободный электрон. Азот и фосфор подходят в качестве примеси N-типа для алмаза. Фосфор и мышьяк являются наиболее используемыми примесями N-типа для кремния, хотя может использоваться и сурьма.
Собственные полупроводники, максимальная доля примеси в которых составляет 1 на 10 миллиардов, являются плохими проводниками.
Полупроводник N-типа легируется пятивалентной примесью, чтобы создать свободные электроны. Такой материал является проводящим. Электрон в нем является основным носителем.
Полупроводник P-типа, легированный трехвалентной примесью, имеет множество свободных дырок. Это носители положительного заряда. Материал P-типа является проводящим. Дырки в нем являются основными носителями.
Большинство полупроводников основаны на элементах из группы IVA периодической таблицы. Причем кремний является наиболее распространенным, германий устарел, а углерод (алмаз) в настоящее время исследуется.
Широко используются и составные полупроводники, такие как карбид кремния (группа IVA) и арсенид галлия (группа III-V).
Электрический ток в металлах: подробное объяснение
Электрический ток в металлах представляет собой упорядоченное движение свободных электронов. Более подробно об этом читайте далее в нашей статье.
Важно знать
Как известно, электрический ток – это упорядоченный поток носителей электрического заряда. Носители – это заряженные частицы, способные свободно перемещаться во всем объеме тела.
В случае металлов этими частицами являются электроны, которые высвобождаются при образовании связи между атомами металла.
Известно, что металлы в твердом состоянии имеют кристаллическую структуру. Частицы в кристаллах расположены в определенном порядке, образуя пространственную решетку (кристалл).
Наконец, кристаллическая решетка металла образована положительными ионами, погруженными в “облако” хаотически движущихся так называемых свободных электронов, также называемых электронами проводимости. В зависимости от валентности атомов металла, один атом может освободить от одного до трех электронов при образовании металлических связей. Число таких высвобожденных электронов непосредственно переводится в число носителей заряда. Это является одним из факторов, влияющих на способность металла проводить электрический ток.
Доказательством того, что ток в металлах вызывается электронами, послужили эксперименты наших отечественных физиков Леонида Исааковича Мандельштама и Николая Дмитриевича Папалекси, а также американских физиков Бальфура Стюарта и Роберта Толмана.
Способность металла проводить электрический ток может быть описана физической величиной, называемой удельным электрическим сопротивлением. Эта физическая величина обозначается греческой буквой ρ (читается как “ро”). Единицей измерения удельного сопротивления является Ом · м, т.е. произведение Ом на метр. Удельное сопротивление – это константа, которая характеризует материал и имеет различные значения для разных материалов. Например, удельное сопротивление меди составляет 1.72*10 -8 Ом · м. Это означает, что электрическое сопротивление медного проводника длиной 1 метр и площадью поперечного сечения 1 м равно 1.72*10 -8 Ом . В целом, чем ниже удельное сопротивление материала, тем лучше он проводит электрический ток.
В таблице ниже приведены некоторые примеры удельного сопротивления часто используемых металлов.
| Металл | Удельное сопротивление (Ом · м) |
| Серебро | 1.59*10 -8 |
| Медь | 1.72*10 -8 |
| Алюминий | 2.82*10 -8 |
| Вольфрам | 5.6*10 -8 |
| Железо | 10*10 -8 |
Удельное электрическое сопротивление может быть связано с микроскопическими свойствами материала. В частности, он зависит от концентрации носителей заряда и их подвижности.
Движение свободных электронов в металлах не является полностью “свободным”, поскольку во время их движении они взаимодействуют с другими электронами, и прежде всего с ионами кристаллической решетки. Специфика этого движения описывается так называемой классической моделью проводимости.
Основные предположения и выводы этой модели представлены в большом упрощении ниже.
Классическая модель проводимости
Без внешнего электрического поля электроны совершают тепловые хаотические движения, сталкиваясь друг с другом, а также сталкиваясь с ионами кристаллической решетки. В результате такого движения среднее положение электронов практически не меняется (см. рис. 1.).

Рис. 1. Пример траектории электрона во время его хаотического теплового движения в металле
Из-за квантовых эффектов, и в частности из-за принципа запрета Паули, который не позволяет всем электронам занимать самое низкое энергетическое состояние, средняя скорость электронов в металлах, связанная с их хаотическим тепловым движением, больше, чем скорость частиц в классическом идеальном газе той же температуры. Она составляет порядка 10 м/с.
Если электрическое напряжение U приложено к концам проводника длиной L в нем появится электрическое поле с напряженностью E = U / L
Под действием этого внешнего поля, согласно второму закону динамики, электроны ускоряются: a = F / m,
где F = e*E – сила, с которой электрическое поле действует на электрон с зарядом e. Таким образом, ускорение электрона составляет: a = e*E / m .
Ускоренное движение электрона длится лишь довольно короткое время, пока он не столкнется с ионом
кристаллической решетки. В результате такого столкновения электрон теряет практически всю свою кинетическую энергию. Однако замедленный электрон не остается в состоянии покоя – он снова ускоряется под действием электрического поля, снова сталкивается с одним из ионов из ионы кристаллической решетки и т.д. Этот эффект добавляет к скорости тепловых движений дополнительную направленную среднюю скорость u, которая из-за отрицательного заряда электрона имеет направление, противоположное напряженности внешнего электрического поля. Эта скорость называется средней скоростью дрейфа (рис. 2).

Рис. 2. Дрейф электрона под действием внешнего электрического поля
В проводнике начинает течь электрический ток с силой тока I (см. рисунок 3).

Рис. 3. Дрейфующие электроны сталкиваются с ионами кристаллической решетки
Предполагая, что движение электрона равномерно ускоряется между столкновениями с ионами решетки, с ускорением a = e*E / m , и предполагая, что в результате столкновения электрон передает всю свою кинетическую энергию кристаллической решетке, мы можем вычислить скорость, которую развивает электрон в своем свободном движении: v = a*τ . В этой формуле τ – средний интервал времени между последующими столкновениями дрейфующего электрона с ионами кристаллической решетки.
Поскольку при равномерно ускоренном движении без начальной скорости средняя скорость является средним арифметическим начальной (равной нулю) и конечной скоростью, то получаем: u = v / 2 = e*E*τ / 2*m .
Из полученной формулы следует, что скорость дрейфа, помимо внешнего электрического поля, определяется средним интервалом времени между столкновениями электронов с ионами решетки. Этот параметр зависит от многих факторов (включая температуру, кристаллическую структуру металла, дефекты кристаллической структуры, примеси) и, как выясняется, существенно влияет на электрическое сопротивление материала.
Средняя дрейфовая скорость электронов составляет порядка 10 -4 м/с. Она очень мала по сравнению со скоростью теплового движения, которая составляет порядка 10 6 м/с.
Классическая теория проводимости достаточно хорошо описывает явление электропроводности в металлах. Однако эта теория не может объяснить экспериментально наблюдаемую зависимость электрического сопротивления от температуры.
Причина упомянутой неудачи классической теории проводимости заключается в том, что она не учитывает влияние ионов решетки на движение электронов между столкновениями. Более близкие к реальности результаты дает квантовая теория проводимости, которая описывает электроны как частицы, подверженные квантовой статистике, движущиеся в периодическом электрическом поле, создаваемом положительными ионами решетки.
Выводы простым языком
Отрицательный заряд всех свободных электронов по абсолютному значению равен положительному заряду всех ионов решётки. Поэтому в обычных условиях металл электрически нейтрален. Свободные электроны в нём движутся беспорядочно. Но если в металле создать электрическое поле, то свободные электроны начнут двигаться направленно под действием электрических сил. Возникнет электрический ток. Беспорядочное движение электронов при этом сохраняется, подобно тому как сохраняется беспорядочное движение в стайке мошкары, когда под действием ветра она перемещается в одном направлении.
« Скорость движения самих электронов в проводнике под действием электрического поля невелика – несколько миллиметров в секунду, а иногда и ещё меньше. Но как только в проводнике возникает электрическое поле, оно с огромной скоростью, близкой к скорости света в вакууме (300 000 км/c), распространяетcя по всей длине проводника. »
Перышкин А. В. Физика 8. – М.: Дрофа, 2010
Как пример, электрический сигнал, посланный, например, по проводам из Москвы во Владивосток (s = 8000 км), приходит туда примерно через 0,03 с.
Одновременно с распространением электрического поля все электроны начинают двигаться в одном направлении по всей длине проводника. Так, например, когда цепь электрической лампы замкнута, электроны в спирали лампы также движутся упорядоченно.
Сравнение электрического тока с потоком воды в водопроводной системе и распространения электрического поля с распространением давления воды поможет нам понять это. Когда вода поднимается в резервуар для воды, давление (напор) воды очень быстро распространяется по всей системе водоснабжения. Когда мы включаем кран, вода уже находится под давлением и сразу же начинает течь. Но вода, которая была в кране, течет, а вода из башни достигает крана гораздо позже, потому что вода движется с меньшей скоростью, чем распространяется давление.
Когда говорят о скорости распространения электрического тока в проводнике, то имеют в виду скорость распространения по проводнику электрического поля.
Лекция 2
Электронные оболочки принято обозначать буквами и числами (N). ЧислоNназывают главным квантовым. Отсчет его значения осуществляется от уровня, ближайшей к ядруN= 1, 2, 3, 4 и т.д., оболочки имеют соответствующие буквенные обозначения:K,L,M,N, и т.д.
На каждой оболочке может находиться несколько электронов, причем каждому из них соответствует свой энергетический уровень, со своим пространственным распределением заряда, который часто называют орбиталью. Энергетические уровни электронов (орбитали) внутри оболочки (с одним числом N) принято обозначать буквами:s(нижний уровень),p,d,fи т.д. Причем чем выше энергия оболочки (большеN), тем большее число электронов может на ней находиться, или другими словами ей соответствует большее число орбиталей. Так первой оболочке соответствует один уровень - орбиталь 1s, т.е. на этой оболочке могут находиться только два электрона с разными спинами. Соответственно конфигурацию с одной оболочкой имеют только два атома – водорода и гелия.
Второй оболочке соответствуют три уровня: одна орбиталь 2sи три орбитали 2p, т.е. в этой оболочке могут находиться шесть электронов.
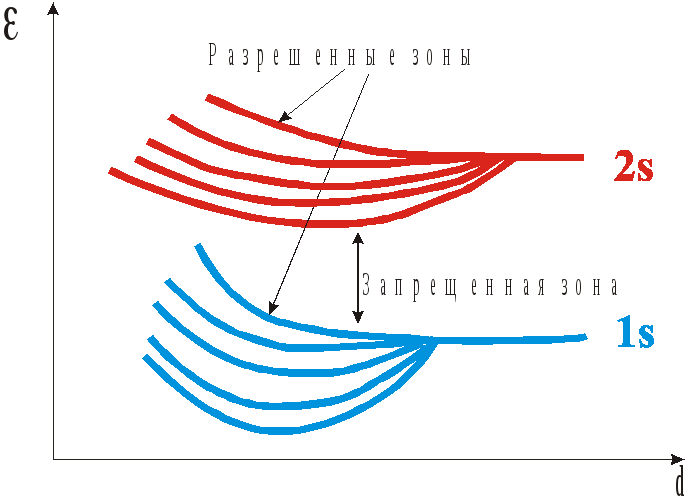
Рис. 1.6. Энергетическое расщепление 1sи 2sуровней для пяти атомов в зависимости от расстояния между ними
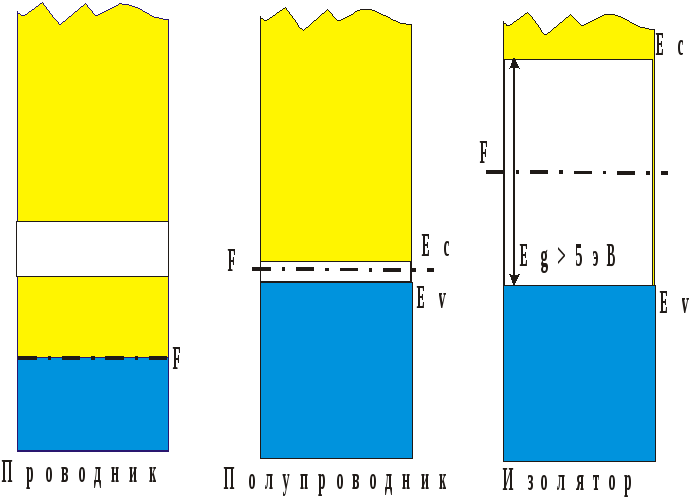
Для полупроводников и диэлектриков структура зон такова, что нижняя разрешенная зона полностью заполнена валентными электронами, поэтому ее называют валентной. Потолок валентной зоны обозначают Ev. В ней электроны перемещаться под действием поля (и соответственно набирать энергию) не могут, поскольку все энергетические уровни заняты, а согласно принципу Паули электрон не может переходить с занятого состояния на занятое. Поэтому электроны в полностью заполненной валентной зоны не участвуют в создании электропроводности. Верхняя зона в полупроводниках и диэлектриках в отсутствии внешнего возбуждения свободна от электронов и если каким либо образом туда забросить электрон, то под действием электрического поля он может создавать электропроводность, поэтому эту зону называют зоной проводимости. Дно зоны проводимости принято обозначатьEc. Между зоной проводимости и валентной зоной находится запрещенная зонаEg, в которой согласно законам квантовой механики электроны находиться не могут (подобно тому как электроны в атоме не могут иметь энергии не соответствующие энергиям электронных оболочек). Для ширины запрещенной зоны можно записать:
Поскольку в отсутствии внешнего возбуждения валентная зона полностью заполнена (вероятность нахождения электрона на Ev= 1), зона проводимости полностью свободна (вероятность нахождения электрона наEс = 0), то формально уровень Ферми с вероятностью заполнения ½ должен был бы находиться в запрещенной зоне. Расчеты показывают, что действительно в беспримесных бездефектных полупроводниках и диэлектриках (их принято называть собственными) он лежит вблизи середины запрещенной зоны. Однако электроны там находится не могут, поскольку там нет разрешенных энергетических уровней.
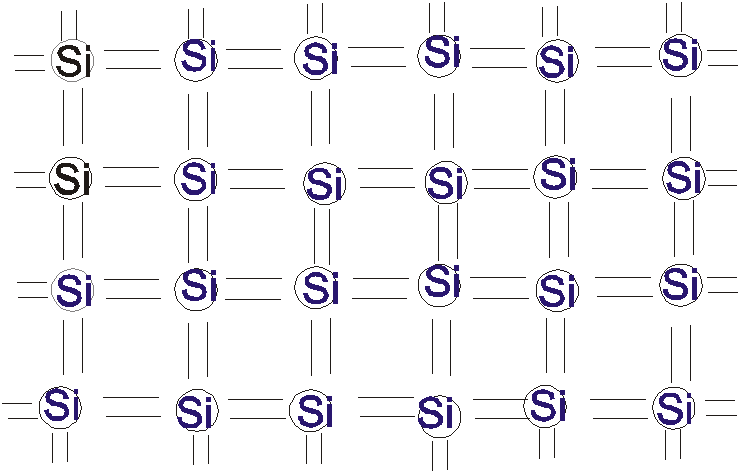
Основные элементарные полупроводники относятся к четвертой группе таблицы Менделеева, они имеют на внешней оболочке 4 электрона. Соответственно эти электроны находятся в S(1 электрон) иp(3 электрона). При образовании кристалла внешние электроны взаимодействуют и образуются полностью заполненная оболочка с восьмью электронами, как это показано на диаграмме рис. 1.7.
Элементы четвертой групп используют четыре электрона находящихся в sиpорбиталях, но в разных электронных оболочках (Nизменяется от 2 для С до 6 дляPb). При взаимодействии образуется гибриднаяsp 3 орбиталь) в ее образовании участвует однаsорбиталь и 3p– орбитали). Эта орбиталь состоит из гибридизированных четырех орбиталей каждая из которых с учетом спина может принять четыре электрона и таким образом образуется заполненная внешняя оболочка с восьмью электронами. При этом атом может образовывать химические связи с четырьмя соседями, т.е. является четырежды координированными. Все связи эквивалентны и образуют тетраэдрическую решетку (тетраэдр – фигура с четырьмя одинаковыми поверхностями). Схема образования гибриднойsp 3 орбитали показана на рис. 1.8.

Тетраэдрическая структура свойственна кристаллам алмаза. Такие известные полупроводники как SiиGeимеют структуру типа алмаза, это и понятно, поскольку у них внешние электроны находятся наsp 3 орбиталях.
На рис. 1.9 показана схема образования энергетических зон и sp 3 орбиталей для кристаллов других элементов четвертой группы периодической системы элементов Д.И. Менделеева. Как видно из рисунка все зоны формируются на основеsиpсостояний, но принадлежащих к разным оболочкам (различно значение главного квантового числаN). Так для углерода валентная оболочка формируется из 2sи 2pсостояний соответственно структура алмаза определяется гибридными 2sp 3 состояниями. ДляSiвалентная оболочка формируется из 3sи 3pсостояний атомаSi, соответственно структура кристаллической решетки создается 3sp 3 орбиталями, является тетраэдрической и аналогична структуре алмаза. ВGeв образовании химических связей участвую 4sи 4pэлектроны,Sn5sи 5pэлектроны и т.д. При этом для образовавшаясяsp 3 оказывается полностью заполненной, верхняя полностью свободной, т.е. имеет место энергетическая структура соответствующая полупроводникам и диэлектрикам с валентной зоной и зоной проводимости. Следует обратить внимание на тот факт, что по мере роста числаN, движении по группе таблицы Менделеева сверху вниз, ширина запрещенной зоны уменьшается и для свинца обе зоны перекрываются, т.е. для этого материала реализуется зонная структура, характерная для проводника.
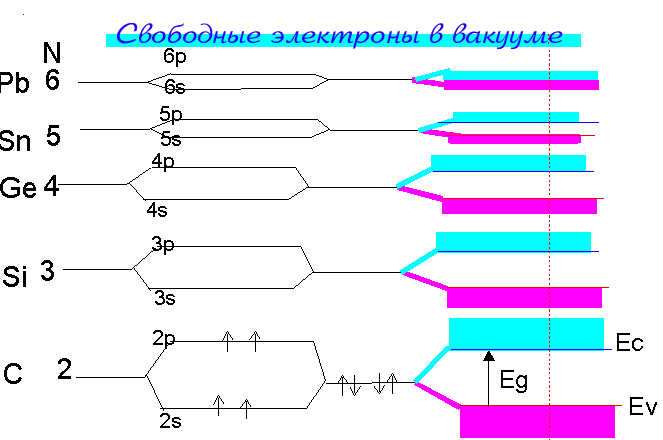
Следует отметить, что sp 3 гибридизация может происходить не только для кристаллов элементарных полупроводников, но и для полупроводниковых соединения. Необходимым для этого условием является то, чтобы электроны внешней оболочки исходных компонентов принадлежали кsиpоболочкам и чтобы суммарное число на внешней оболочки соединения равнялось 8 (тогда нижняя зона оказывается полностью заполненной). Последнее условие будет выполняться для соединений элементов первой и седьмой групп, второй и шестой, третьей и пятой, т.е. для соединенийA 1 B 7 ,A 2 B 6 ,A 3 B 5 . Действительно большинство из этих соединений является полупроводниками, причем для них так же выполняется правило, что с увеличением номера электронной оболочки атомов из которых образуется соединение ширина запрещенной зоны уменьшается.
В качестве примера рассмотрим такое несколько полупроводниковых соединений. Примеры из группы A 3 B 5 :GaAs:Eg= 1.43эВ (при Т=300К), атомы компонентов имеют электронную конфигурацию внешних оболочек – 3s 2 4p 1 (Ga), 4p 3 (As);InSb:Eg=0.18 эВ (при Т=300К), электронная конфигурация валентной оболочки – 4s 2 4p 1 (In), 5p 3 (Sb).
На рисунке 1.10 показан кристалл, в котором каким либо внешним возбуждением, например квантом света с hν>Egодин из электронов переброшен в зону проводимости (стал свободным), т.е. у одного из атомов была разорвана одна из валентных связей. Тогда в кристалле помимо не связанного с атомом электрона возник положительно заряженный ион. Способность под действием поля перемещаться самого иона очень мала, поэтому ее учитывать не следует. Поскольку в кристалле атомы расположены близко друг от друга к этому иону может притянуться электрон от соседнего атома. В этом случае положительная дырка возникает у соседнего атома откуда ушел валентный электрон и т.д. Для совершенного, не имеющего примесей и дефектов, кристалла концентрация электронов будет равна концентрации дырок. Этособственная концентрация носителей заряда ni=pi, значокiозначает концентрацию носителей для собственного полупроводника (intrinsic–собственный). Для произведения концентраций электронов и дырок можно записать:
Читайте также:
