Энергетические зоны в металлах
Обновлено: 04.10.2024
а. Твердотельные лазеры на люминесцирующих средах с оптической накачкой. Это рубиновые и лазеры на стеклах, активированные неодимом. Работают в импульсном режиме.
б. Газоразрядные лазеры низкого давления на смесях He-Ne, He-Xe, непрерывного действия, генерируют излучение высокой монохроматичности и направленности.
в. Полупроводниковые лазеры с инжекционной накачкой через р-n переход. (Подробнее см. параграф 16). Миниатюрны, могут работать в импульсном и непрерывном режимах.
г. Газоразрядные лазеры высокого давления (N2-CO2, CO). Мощность – десятки кВт. Могут работать в непрерывном и импульсном режимах.
К настоящему времени разработаны так же газоразрядные аргоновые лазеры непрерывного действия, генерирующие зелёный луч, жидкостные лазеры на красителях, химические лазеры на смеси газов, работающие за счёт энергии химической реакции, и др.
1. Современная квантовая теория твердого тела (ТТ) рассматривает ТТ как систему частиц, в которой действуют кулоновские электрические силы. Магнитное взаимодействие между атомами в кристаллической решетке ТТ гораздо слабее, чем электрическое. Это позволяет часто им пренебрегать.
Точное решение уравнения Шредингера для многочастичной системы, каковой является кристалл, упирается в непреодолимые математические трудности. Ситуация напоминает проблему решения системы уравнений движения молекул, например, в объеме газа. В молекулярной физике выход найден во введении средних характеристик движения молекул и таких интегральных специфических параметров, как давление и температура.
В физике твердого тела задача решается с помощью приближенных методов. Например, в теории металлов вместо многих электронов рассматривается один электрон, движущийся в постоянном периодическом поле кристаллической решётки.
2. Энергетические зоны. Одинаковые атомы, бесконечно удаленные друг от друга, имеют одинаковые энергетические уровни. Если эти атомы постепенно сближать, то их электронные облака перекрываются. Энергетические уровни такой системы связанных общими электронами атомов расщепляются. Возникают энергетические полосы или зоны.
Любой монокристалл можно рассматривать как одну большую молекулу. Если постепенно наращивать кристалл, то каждый последующий атом будет создавать дополнительное расщепление энергетических уровней. Ширина полос определяется расстоянием между атомами. Поэтому каждый последующий атом не делает полосы шире. Он лишь увеличивает число энергетических уровней в постоянной по ширине полосе. Сильнее всего расщепляются внешние уровни. Чем ниже уровень, тем слабее он расщепляется (рис.82).
Сравним величину энергетических ступеней в полосе с энергией теплового движения. В качестве примера рассмотрим кристалл натрия. Допустим, полоса образуется расщеплением уровня 4s и ширина этой полосы не больше разности энергий между уровнями 3s и 5s. Как видно из рис.44, это составляет около 4 эВ.
Допустим, кристалл натрия имеет объем 1 см 3 . При плотности натрия r » 10 3 кгçм 3 масса m кристалла составляет 1 г = 10 -3 кг. Число атомов в таком кристалле N = (mçM)·Na = (10 -3 ç0,023)·6·10 23 » 10 23 .
Число энергетических уровней в каждой энергетической зоне кристалла по крайней мере не меньше числа атомов N. Будем полагать, что оно равно N. Тогда расстояние между уровнями в полосе 4s кристалла натрия составляет 4 эВç10 23 » 6·10 -42 Дж.
Энергия теплового движения даже при температуре 1 К составляет величину порядка kТ = 1,38·10 -23 Дж. Она примерно на 20 порядков превосходит ширину энергетических ступеней в полосе. Поэтому в кристаллах при Т > 0 К, электроны в энергетических полосах при наличии свободных уровней могут перепрыгивать на них в пределах полос за счет энергии теплового движения.
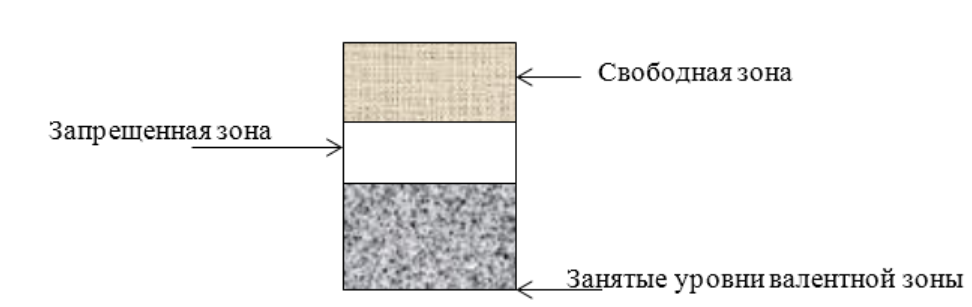
Различают разрешенные зоны, то есть зоны – полосы, состоящие из разрешенных уровней, на каждом из которых могут находиться электроны (не более одного электрона на каждом уровне в разрешённой зоне), и запрещенные энергетические зоны, то есть области, где нет разрешённых уровней, и где электроны находиться не могут.
3. Проводники, диэлектрики и полупроводники. Энергетическую зону, возникшую из того уровня, на котором находятся валентные электроны в основном (не возбужденном) состоянии атома, называют валентной зоной. В зависимости от степени заполнения валентной зоны электронами и ширины выше расположенной запрещенной зоны возможны три случая (рис.83).
а. Проводники (рис.83-а). Рассмотрим в качестве примера натрий. В изолированном и невозбужденном атоме натрия в 3s-состоянии находится один валентный электрон. Максимально возможное число электронов в 3s-состоянии равно двум. При объединении атомов натрия в кристалл уровни расщепляются, но соотношение между заполненными и свободными вакансиями сохраняется. В результате в кристалле натрия образуется валентная зона, заполненная электронами при температуре абсолютного нуля наполовину. Поэтому достаточно сообщить электронам, находящимся на верхних уровнях, ничтожную энергию порядка 10 -42 Дж, чтобы они приобрели возможность перехода на более высокие уровни. Эта возможность реализуется при любых температурах, отличных от абсолютного нуля. В результате электроны могут ускоряться электрическим полем и приобретать скорость направленного движения. Это металлы (Au, Cu, Ag, Na, K, Li. ). Валентную зону в металлах называют зоной проводимости.
Электрическая проводимость в кристаллах оказывается возможной потому, что валентные и более высокие разрешенные зоны соседних атомов в кристаллах перекрываются. Валентные электроны в кристаллической решетке металлов обобществляются между всеми атомами. В результате возникает зона проводимости, пронизывающая весь кристалл.
б. Диэлектрики (рис.83-б). В них при температуре абсолютного нуля Т = 0 электроны заполняют валентную зону полностью. В кристалле существуют зоны двух типов: до конца заполненные и совсем пустые. Такой кристалл при Т = 0 не проводит электрический ток и является диэлектриком (изолятором). При наложении на кристалл диэлектрика внешнего электрического поля (с напряженностью не большей напряженности пробоя кристалла), валентные электроны в таких кристаллах остаются на своих местах, ибо нет близко расположенных свободных уровней, на которые они могли бы перейти.
в. Полупроводники (рис.83-в). Кристалл с заполненной валентной зоной при нагревании ведет себя по-разному в зависимости от ширины запрещенной зоны Еg. Кристаллы с широкой запрещенной зоной являются диэлектриками вплоть до высоких температур. Твердых диэлектриков одноэлементного состава сравнительно мало. Это сера S, алмаз C, кристаллический азот N и др. Их диэлектрические свойства сохраняются вплоть до температур фазовых переходов. У алмаза, например, температура превращения алмаз®углерод составляет 1400°С. Более распространенными высокотемпературными диэлектриками являются оксиды SiO2 (кварц), TiO2 (рутил), Al2O3 (глинозем) и др. Обычно к диэлектрикам относят кристаллы с шириной запрещенной зоны Еg > 3 эВ. Например, у алмаза Еg = 5,2 эВ, у глинозема Еg = 7 эВ. Если ширина запрещенной зоны невелика, так что при нагревании кристалла до нескольких сот кельвин тепловой энергии оказывается достаточно для перехода электронов из валентной в свободную зону, то диэлектрик превращается в проводник. Свободная зона при переходе в нее электронов становится зоной проводимости. Такие кристаллы с малой шириной запрещенной зоны называются полупроводниками. При низких температурах они приближаются к диэлектрикам, при высоких – к проводникам. У типичных полупроводников Еg » 1 эВ. Например, у германия Ge Еg = 0,66 эВ, у кремния Si Еg = 1,08 эВ, у арсенида галлия GaAs Еg = 1,43 эВ, у антимонида индия InSb Еg = 0,17 эВ.
Резкой границы между диэлектриками и полупроводниками нет, и в реальных диэлектриках при Т > 0 в зоне проводимости всегда есть некоторое количество электронов. Оно тем больше, чем меньше ширина запрещенной зоны и чем выше температура.
Это число может составлять 10 12 ¸10 15 элçсм 3 , что много меньше количества электронов в зоне проводимости металлов (10 20 ¸10 23 элçсм 3 ). Концентрация электронов в зоне проводимости возбужденных полупроводников заключена между этими границами и составляет 10 18 ¸10 19 элçсм 3 .
4. Поверхность Ферми. Сравним распределение электронов проводимости в металлах с распределением Максвелла-Больцмана молекул идеального газа при Т = 0.
Классический газ при Т = 0 должен прекратить свое существование, поскольку энергия его частиц обращается в нуль, = 3кТç2 = 0. Следовательно, обращается в нуль и скорость движения частиц.
С электронами проводимости дело обстоит иначе. При Т ® 0 энергия электронов проводимости в кристалле не может стремиться к нулю, так как иначе все электроны перейдут в одинаковое состояние с нулевой энергией. Но это запрещено принципом Паули. При Т = 0 электроны проводимости располагаются на энергетической лесенке, начиная с самой нижней ступеньки и плотно заполняя все разрешенные энергетические уровни и состояния так, что на каждом из них находится по одному электрону.
Функция плотности q(Е) распределения разрешённых уровней электронов проводимости в металле объёмом V по энергиям Е имеет вид: q(Е) =. (12.1)
График функции q(Е) показан на рис.84. Верхний из заполненных при Т = 0 К уровней зоны проводимости металла называют уровнем Ферми, а его энергию – энергией Ферми Еф. Величина Еф при Т = 0 определяется выражением: Еф=, (12.2) где n – концентрация свободных электронов в металле. У одновалентных щелочных металлов концентрация свободных электронов равна концентрации узлов решётки.
В пространстве импульсов, откладывая по осям проекции px, py, pz импульсов частиц, можно получить наглядную геометрическую картину распределения частиц по энергиям. Так, распределение Максвелла-Больцмана для идеального газа при Т > 0 К выглядит в таком представлении как центрально – симметричная туманность с увеличивающейся к центру концентрацией частиц (рис.85). Чем больше энергия частиц, тем дальше они от центра. При Т ® 0 К туманность стягивается в центральную точку. С ростом температуры туманность увеличивается в размерах.
В отличие от классического газа изоэнергетические поверхности электронов в зоне проводимости металлов образуют в импульсном пространстве более сложную форму. Поверхность, соответствующую уровню Ферми, называют поверхностью Ферми. Вид этой поверхности существенно сказывается на многих электрических, магнитных и других свойствах металлов. Это позволяет построить поверхность Ферми по экспериментальным данным.
У одновалентных (щелочных) металлов поверхность Ферми имеет форму сферы (рис.86). У двухвалентных, например, бериллий Ве, поверхность Ферми имеет более сложную форму. Дело в том, что 2s-уровень в атоме бериллия заполнен полностью. При объединении атомов Ве в кристалл в валентной зоне не образуется вакансий, все уровни по-прежнему заняты. Но при объединении атомов Ве в кристалл следующая 3s-зона уширяется настолько, что “наезжает” на 2s-зону. В результате у электронов появляется возможность переходить при тепловом возбуждении в 3s-зону, превращая ее в зону проводимости.
На рис.87 показаны поверхности Ферми для некоторых металлов.
С ростом температуры кривая распределения электронов по энергиям смазывается на графике g(Е) вправо (рис.88), а поверхность Ферми разрыхляется тем сильнее, чем выше температура. При этом распределение электронов приближается к классическому. Критерием поведения любого газа является температура вырождения Т0 = , 12.3)
При Т < Т0 газ называется вырожденным, его поведение описывается законами квантовой механики. Например, для электронов проводимости в металлах n » 10 29 м -3 , m » 10 -30 кг. Отсюда, температура вырождения электронного газа Т0 = = 8,5·10 3 К. Следовательно, при всех температурах существования кристаллических проводников электроны проводимости в металлах представляют собой вырожденный газ (Ферми-газ), подчиняющийся квантовым законам.
Если Т > Т0, то газ невырожден, по своим свойствам он приближается к классическому. Например, у гелия He m = 6,7·10 -27 кг, при нормальных условиях n = 2,7·10 25 м -3 . Отсюда
Примененный здесь критерий температуры вырождения Т0 не учитывает возможность фазовых переходов в реальных газах. Он лишь определяет температурную границу использования квантовой или классической статистик для описания конкретной системы частиц.
5. Парадокс теплоемкости металлов. Как известно из курса молекулярной физики, для твердых кристаллических диэлектриков справедлив закон Дюлонга и Пти (1819 г.), согласно которому молярная теплоемкость всех твердых кристаллических веществ одинакова для всех веществ, практически не зависит от температуры и равна 3R.
Классическая теория так объясняет этот опытный закон. Каждый атом – узел кристаллической решетки можно уподобить упругому осциллятору, способному колебаться в 3-х взаимно перпендикулярных направлениях. Полагая осцилляторы гармоническими с непрерывно изменяющейся энергией, можно постулировать, что на каждое направление приходиться в среднем kTç2 кинетической и kTç2 потенциальной энергии осциллятора. Средняя энергия осциллятора составляет в этом случае . (12.4)
Один моль содержит число Авогадро NA атомов. Внутренняя энергия одного моля U=NA=3kNA·T=3RT. Изохорная молярная теплоемкость . (12.5)
Сложнее оказалось объяснить теплоемкость металлов. В начале 20 века еще в доквантовую эпоху Друде и Лоренц построили электронную теорию проводимости металлов. В основу теории было положено предположение, что валентные электроны атомов металлов связаны со своими атомами настолько слабо, что могут легко перемещаться от одного атома к другому лишь за счет энергии теплового движения. Такую совокупность обобществленных валентных электронов они рассматривали как идеальный газ, подчиняющийся распределению Максвелла – Больцмана (см. Электричество, §9).
Теория Друде – Лоренца просто и наглядно объяснила эмпирические законы Ома и Джоуля – Ленца. Но она оказалась не в состоянии объяснить закон Дюлонга и Пти у металлов. Действительно, если в объеме кристалла наряду с атомами – узлами есть электронный газ, то теплоемкость кристалла должна складываться из теплоемкости этих двух систем частиц, находящихся в тепловом равновесии.
Пусть на каждый атом приходиться Z валентных электронов. Тогда на 1 моль узлов приходится Z молей электронного газа. Молярная теплоемкость узлов – осцилляторов равна 3R, теплоемкость Z молей идеального газа равна (3Rç2)·Z. Суммарная теплоемкость CV = 3R + 3ZRç2. При Z = 1 CV = 4,5R. У натрия, калия, лития и других одновалентных металлов молярная теплоемкость должна быть 1,5 раза больше, чем постулирует закон Дюлонга и Пти. Но опыт показывает, что CV металлов, как и диэлектриков, ближе к 3R. В этом суть парадокса теплоемкости.
Квантовая теория объясняет этот парадокс. Средняя энергия электронов на заполненных уровнях зоны проводимости составляет около 3 эВ = 4,8·10 -19 Дж. Средняя энергия теплового движения при комнатной температуре kT » 1ç40 Эв. Поэтому тепловой энергии недостаточно для перевода всех электронов на верхние свободные уровни.
Вклад в теплоемкость вносят лишь самые верхние электроны проводимости вблизи поверхности Ферми, которые имеют сверху свободные энергетические уровни с относительно малой шириной энергетического перехода (рис.89). Поэтому-то вклад электронов в теплоемкость кристаллической решетки мал и составляет всего около 1%.
Особенности зонной структуры диэлектриков, полупроводников и металлов
Зонная теория - это квантовая механическая теория, которая рассматривает движение электронов в твердом теле.
Зонная теория твердого тела
Согласно теории, свободные электроны могут обладать любой энергией. Электроны в атомах твердого тела могут иметь только определенные дискретные значения энергии. Другими словами, спектр энергии электронов в атомах состоит из разрешенных и запрещенных энергетических зон.
Положения зонной теории
Итак, согласно постулатам Бора, электрон в отдельном атоме может находится на одной из нескольких энергетических орбиталей. Иначе говоря, иметь лишь определенные дискретные значения энергии. Когда атомы образуют молекулу, количество орбиталей расщепляется пропорционально числу атомов в молекуле.
При увеличении количества молекул до макроскопического тела количество орбиталей становится очень большим, а разница между соответствующими им энергиям - очень маленькой. Орбитали сливаются, образуя энергетические зоны.
Валентная зона - в диэлектриках и полупроводниках наивысшая энергетическая зона, которая заполнена полностью при температуре 0 К. Зона проводимости - следующая за валентной зона. В металлах зоной проводимости называется наивысшая разрешённая зона, в которой находятся электроны при температуре 0 К.
Зонная теория объясняет различие в электрических свойствах материалов: проводников, полупроводников, диэлектриков. Можно выделить следующие причины различий:
- Ширина запрещенных энергетических зон
- Разница в заполнении разрешенных энергетических зон электронами.
Зонная структура диэлектриков
Вещество является диэлектриком, когда валентная зона заполнена полностью, в высших зонах нет электронов, также отсутствует перекрытие зон. Такое вещество не проводит ток. Ширина между зонами у диэлектриков условно составляет более 2 электронвольт.
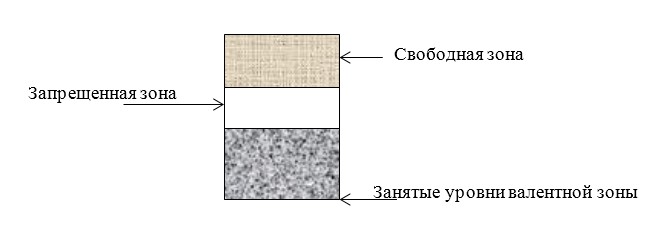
Зонная структура полупроводников
Вещество является полупроводником, если валентная зона разделена с соседними зонами узкой (менее 2 электронвольт) запрещающей зоной. Отметим, что такое вещество при температуре, близкой к абсолютному нулю, является диэлектриков. Однако при росте температуры электроны из верхней занятой зоны перескакивают в вакантную зону проводимости, и вещество становится электропроводным. Проводимость растет вместе с температурой и концентрацией электронов в зоне проводимости. Соответственно, в заполненной зоне, из которой электроны переходят в зону проводимости, растет концентрация дырок.
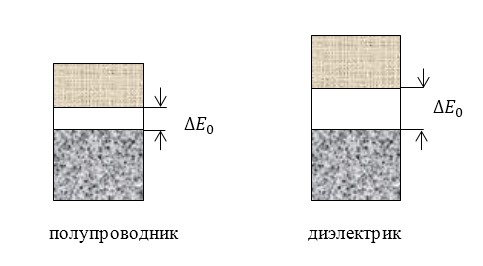
Разделение веществ на полупроводники и диэлектрики весьма условно. Вещества с шириной запрещённой зоны более 3—4 эВ и менее 4—5 эВ совмещают свойства диэлектриков и полупроводников.
Зонная структура проводников (металлов)
В металлах валентная зона занята не полностью, и при воздействия на проводник разности потенциалов электроны могут свободно перемещаться из точек с меньшим потенциалом в точку с большим потенциалом.
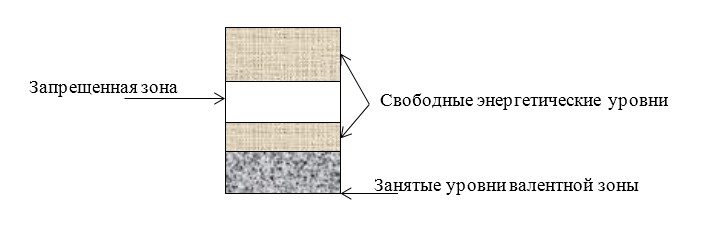
Также в проводниках зона проводимости пересекается с валентной зоной. Получившаяся зона пересечения заполнена не полностью.
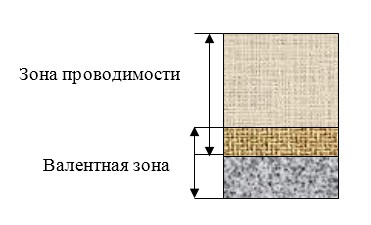
Почему проводимость металлов не растет с увеличением валентности?
Валентность - это способность атома вещества образовать определенное число химических связей. Проще говоря, способность "прикрепить" к себе другой атом.
Однако электропроводность зависит не от количества валентных электронов на один атом, а от числа электронов в валентной зоне, для которых существуют свободные энергетические уровни. Так, у двухвалентных металлов число электронов, которые могут перейти под действием внешнего поля в свободное состояние меньше, чем у одновалентных. Таким образом, электропроводность двухвалентных металлов меньше, чем одновалентных.
Зонная теория твердых тел
Основываясь лишь на модели электронного газа невозможно объяснить тот факт, что одни вещества представляют собой проводники, вторые полупроводники, а третьи изоляторы. Стоит принимать во внимание взаимодействие между атомами и электронами. Предположим, что кристаллическая решетка металла или полупроводника сформирована как результат сближения атомов. Связь с атомными ядрами валентных электронов атомов металлов проявляет себя гораздо слабее, чем связь с подобными электронами полупроводников. При условии сближения атомов электроны приходят во взаимодействие. В результате валентные электроны разрывают свою связь с атомами металла, что делает их свободными, обладающими возможностью перемещаться по всему металлу.
В полупроводниках, по причине существенно более сильной связи электронов с ядрами атомов, для того, чтобы разорвать связь валентного электрона нужно сообщить ему так называемую энергию ионизации.
Для разных полупроводников величина энергии ионизации может колебаться от 0 , 1 до 2 э В , в то же время средняя кинетическая энергия теплового движения атома близка к 0 , 04 э В . Количество атомов, энергия которых выше или эквивалентна энергии ионизации, относительно невелико. Соответственно, свободных электронов в полупроводниках не много. С увеличением температуры, число атомов с энергией ионизации повышается, а это значит, что растет и электрическая проводимость полупроводника.
За процессом ионизации всегда идет сопровождение в виде обратного процесса, а именно рекомбинация. В условиях состояния равновесия среднее число актов ионизации эквивалентно количеству актов рекомбинации.
Понятие о зонной теории
Квантовая теория электропроводности твердых тел основывается на так называемой зонной теории твердых тел, которая заключается в изучении энергетического спектра электронов.
Данный спектр подразделяется на разделенные запрещенными промежутками зоны. В случае, если в верхней зоне, где определяется присутствие электронов, они не заполняют каждое из квантовых состояний (в пределах зоны может быть проведено перераспределение энергии и импульса), то данное вещество представляет собой проводник. Подобная зона носит название зоны проводимости, вещество — проводника электрического тока, тип проводимости такого вещества является электронным.
Если в зоне проводимости находится большое количество электронов и свободных квантовых состояний, то значение электропроводности велико. Электроны в условиях зоны проводимости при прохождении электрического тока определяются как носители заряда. Процесс движения подобных электронов может быть описан с помощью законов квантовой механики. Если проводить сравнение с общим количеством электронов, то число таких электронов может считаться малым.
Энергетические уровни
Энергетические уровни валентного электрона в одном изолированном атоме могут быть представлены таким образом, как это проиллюстрировано на рисунке 1 . Снизу вверх по вертикали на рисунке 1 откладываются: величины полной энергии электрона, а также отмечаются минимальная энергия электронов проводимости E c с наибольшим значением энергии связанных электронов E v . Вероятные значения энергий электронов заполняют собой некоторую область или же так называемую зону энергии W ≥ E c . Такая зона представляет собой зону проводимости. Энергии электронов связи формируют другую зону с W ≤ E v . Приведенная зона носит название зоны валентных электронов или, другими словами, валентной зоны. Данные зоны разделены энергетическим промежутком с шириной, определяемой с помощью следующего выражения: E g = E c − E v .
Такой энергетический промежуток представляет собой зону запрещенных энергий. В условиях отсутствующих примесных атомов, а также дефектов решетки, стационарные движения электронов с энергией внутри запрещенной зоны не представляются возможными.
Процесс разрыва химической связи, который провоцирует возникновение электрона проводимости и положительной дырки, носит название электронного перехода.
Валентная зона — зона проводимости (смотрите рисунок 1 цифра 1 ).
Обратный процесс определяется как рекомбинация электрона проводимости и положительной дырки (электронный переход 2 , рисунок 1 ). В условиях существования атомов примеси вероятно возникновение дискретных разрешенных уровней энергии как ,например, уровень E d , проиллюстрированный на рисунке 1 . Данные уровни могут существовать не во всем объеме кристалла, а лишь в местах нахождения атомов примеси (такие уровни определяются как локальные). Каждый из локальных уровней производит энергию электрона, в случае его нахождения на примесном атоме. Локальные электронные уровни дают возможность дополнительных электронных переходов. Как пример, ионизация донора с образованием электрона проводимости проиллюстрирована на рисунке 1 в виде электронного перехода 3 . Роль обратного ему процесса захвата электрона на атом донора играет электронный переход 4 из зоны проводимости на незаполненный уровень донора.
Образование энергетических зон
Из решения задачи о движении электрона в поле периодического потенциала можно сделать вывод, что имеет место система зон разрешённых энергий (рисунок 2 ). Каждая из зон ограничивается снизу некоторой энергией W m i n или, другими словами, дном зоны, а сверху так называемым потолком зоны W m a x . Данные зоны разделены полосами запрещенных энергий. Ширина разрешенных зон в условиях увеличения энергии возрастает. Возможно перекрытие друг друга широкими зонами, такое явление провоцирует образование единой сложной зоны. Предположим, что существует N изолированных атомов, которые никоим образом не взаимодействуют. В каждом из таких атомов энергия электронов может претерпевать изменения только в виде скачка, таким образом, она характеризуется совокупностью резких, дискретных уровней энергии. В данной системе невзаимодействующих атомов роль каждого атомного энергетического уровня играет N совпадающих уровней энергии. Сократим расстояние между атомами до формирования кристаллической решетки. Атомы начинают взаимодействовать друг с другом, а уровни энергии изменяются. Ранее совпадающие N уровней энергии начинают разниться. Подобная система несовпадающих уровней энергии носит название разрешенной зоны энергий.
Выходит, что энергетические зоны возникают в качестве результата расщепления дискретных уровней энергии электрона в атомах, вызванного действием атомов решетки. Количество энергетических уровней в каждой из зон крайне большое (порядка числа атомов в кристалле), энергетические уровни расположены довольно близко. Таким образом, в некоторых случаях можно принять, что внутри зон энергия электрона претерпевает непрерывные изменения (как это происходит в классической теории). Однако тот факт, что количество уровней конечно, имеет принципиальное значение. Совокупность энергетических уровней, на которые расщепляется кратный уровень, представляет собой так называемую энергетическую зону или, другими словами, зону кристалла. Зона,возникающая как результат расщепления N -кратного вырожденного основного уровня, носит название основной зоны, все остальные зоны определяются как зоны возбуждения.
Энергетические зоны не могут быть отождествлены с пространственными зонами, областями пространства, в которых находится электрон.
В рамках зонной теории принимается тот факт, что электрон движется в постоянном электрическом поле, которое формируется ионами и остальными электронами. Ионы обладают сравнительно большими массами и считаются неподвижными. Электроны учитываются суммарно. Они определяются в виде отрицательно заряженной жидкости, которая заполняет пустующее пространство между ионами. В подобной модели роль электронов заключается в компенсации заряда ионов. Электрическое поле модели периодично в пространстве, место периодов занимают пространственные периоды решетки. Задание сводится к задаче о движении одного электрона в постоянном периодическом поле. Решение данной задачи в квантовой механике приводит к зонной структуре энергетических уровней.
Дайте описание зонных структур металлов, диэлектриков и полупроводников.
Решение
Электрические свойства тел зависимы от ширины запрещенной энергетической зоны и различий в заполнении разрешенных зон. Существование в разрешенной зоне свободных энергетических уровней является необходимым условием возникновения проводимости. На данный уровень поле сторонних сил может перенести электрон. Зону, которая является пустой или же заполнена лишь частично определяется как зона проводимости. В свою очередь, зона, заполненная электронами полностью, носит название валентной. Металлы, диэлектрики и полупроводники отличаются в области степени заполнения валентной зоны электронами, а также шириной запретной зоны. У металлов зона проводимости является частично заполненной и обладает свободными верхними уровнями. При условии T = 0 валентные электроны попарно заполняют нижние уровни валентной зоны. Локализованным на верхних уровнях электронам для того, чтобы перевести их на более высокие уровни достаточно подвести энергию 10 - 23 - 10 - 22 э В . У диэлектриков первая, являющаяся незаполненной зона, отделена от целиком заполненной нижней зоны с помощью широкой запрещенной зоны. Чтобы перевести электрон в свободную зону необходимо сообщить энергию большую или же эквивалентную ширине запретной зоны. Ширина запрещенной зоны диэлектриков является равной нескольким электрон вольтам. Тепловое движение не имеет возможности перевести в свободную зону большое количество электронов. У кристаллических полупроводников ширина запрещенной зоны между полностью заполненной валентной зоной и первой незаполненной зоной довольно мала. Если ширина запретной зоны эквивалентна нескольким десятым э В , энергии теплового движения хватает для того, чтобы перевести электроны в свободную зону проводимости. При этом вероятен переход электрона внутри валентной зоны на освободившиеся уровни.
Перечислите основные предположения зонной теории.
В качестве основных предположений зонной теории можно привести следующие:
Понятие о зонной теории твердых тел. Расщепление энергетических уровней и образование зон. Энергетические зоны металлов, полупроводников и изоляторов
В основе зонной теории твердых тел лежат представления квантовой теории о том, что атом может находиться только в состояниях с определенной энергией. В основном стационарном (не изменяющемся со временем) состоянии атом имеет минимальную энергию и не излучает ее. При получении энергии атом переходит в возбужденное стационарное состояние (с другим распределением электронов) «время жизни» в котором достаточно мало, а при возвращении в основное состояние энергия излучается.
Тогда, если не учитывать ядерной и других видов энергии, энергия простейшего атома водорода представляется как энергия взаимодействия электрона с ядром. Для атома водорода есть только определенный набор энергий, который представляют в виде набора энергетических уровней или энергетического спектра (рис.197) , который отражает энергию электрона в различных состояниях.
С точки зрения физики твердое тело – кристаллическая структура, в которой каждый электрон может взаимодействовать с различными атомами, и, следовательно, находясь в определенном состоянии в «своем» атоме, иметь различную энергию взаимодействия с другими атомами, поэтому говорят, что каждый энергетический уровень « расщепляется» (рис.198).
Совокупность близко расположенных энергетических уровней, образовавшихся в результате расщепления некоторого энергетического уровня изолированного атома, называется энергетической зоной или просто зоной. Расстояние между соседними уровнями зоны порядка 10 -22 эВ, т.е. так мало, что, для многих явлений соответствует классическому представлению о возможности любой энергии для электрона.
Промежутки между энергетическими зонами называются запрещенными зонами, поскольку электрон не может иметь соответствующую энергию.
Электроны распределяются по уровням и зонам в соответствии с принципом Паули: в любой системе в каждом квантовом состоянии не может быть больше одной частицы. Соответственно на одном уровне может быть только два электрона с различными спинами, а в зоне – лишь определенное количество электронов.
При температурах близких к абсолютному нулю заполняются все нижние зоны, чтобы система имела минимальную энергию. При повышении температуры часть электронов переходит на более высокие энергетические уровни, поскольку нагревание на 1К соответствует энергии порядка 10 -4 эВ. Энергетическая зона с минимальной энергией называется основной.
Ток в металлах – это направленное движение электронов. В квантовой механике движение электронов – это переход из одного энергетического состояния в другое, которое должно быть свободным.
Если зона полностью заполнена, то переходы электронов в ней невозможны, а возможен, только при получении достаточной энергии, переход в следующую зону.
Полностью заполненная зона называется валентной, а частично заполненная или полностью свободная – зоной проводимости.
Если валентная зона полностью заполнена, а зона проводимости полностью свободна, то в зависимости от ширины запрещенной зоны кристалл относят к диэлектрикам или полупроводникам
Для диэлектриков ширина запрещенной зоны несколько эВ, т.е. энергия теплового движения при всех реальных температурах недостаточна для перехода электронов в зону проводимости.
При ширине запрещенной зоны меньше 1 эВ, при повышении температуры, возможен переход электронов в зону проводимости и такие кристаллы относят к полупроводникам.
Зонная теория твердого тела
При объединении атомов в кристалл значение энергии атома изменяется по отношению к изолированному атому: появляется диэлектрическая проницаемость , ядра кристаллической решетки создают потенциальное поле . Рассмотрим кристаллическую решетку с периодом аn.
Электрон, находящийся на орбитали атома, связан со «своим» ядром, вероятность его перемещения по кристаллу под воздействием температуры или внешнего электрического поля мала. Говорят, что такой «квазисвязанный» электрон находится в «потенциальной яме». Под влиянием внешних факторов (света, температуры и т.д.) электрон может увеличить свою кинетическую энергию и перейти на следующий энергетический уровень, вплоть до полного освобождения от влияния «своего» ядра.
| а | 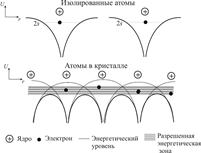 б |
 в | |
| Рис. 1.1 |
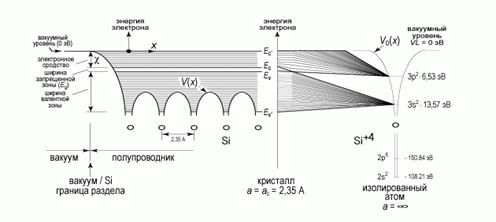
При сближении атомов потенциальные кривые частично налагаются друг на друга (штриховая линия рис. 1.1,б) и дают результирующий потенциальный рельеф (сплошные линии) с пониженными потенциальными барьерами между атомами. Говорят, что валентные электроны обобществляются, и каждый электрон теперь принадлежит всему кристаллу.
До тех пор, пока электрон будет находиться в кристалле, он будет не совсем свободен, то есть находиться в периодическом поле всей решетки кристалла. Другими словами даже «свободный» электрон будет принадлежать всем образующим кристалл атомам. При этом электрон получает возможность беспрепятственно перемещаться по кристаллу от атома к атому без изменения энергии.
Как видно из рис. 1.1, потенциальная энергия =, где (x, y,z) - радиус-вектор данной точки пространства, - вектор кристаллической решетки. При повышении энергии электрона возрастает вероятность его туннелирования через потенциальный барьер (для туннелирования в квантовой механике не обязательно, чтобы энергия электрона стала больше максимума потенциальной ямы). С другой стороны, даже «свободный» электрон под влиянием потенциального поля может изменить свою траекторию, то есть потерять (рассеять) часть своей кинетической энергии в направлении . Говорят, что такой «квазисвободный» электрон движется в периодическом поле кристаллической решетки.
Каждый энергетический уровень изолированного атома в кристалле расщепляется в зону.
| Рис. 1.2. Зонная диаграмма |
Энергетические зоны в общем случае разделены запрещенными для электронов энергетическимизазорами (щелями), называемыми запрещенными зонами Eg (g – от gap – промежуток, щель). С ростом энергии (главного квантового числа) ширина энергетических зон увеличивается, а ширина запрещенных зон уменьшается.
Оценим среднее расстояние между соседними уровнями энергии в разрешенной зоне. Пусть постоянная решетки а=0,4 нм, то есть а 3 =64·10 -24 см 3 . Количество элементарных ячеек в объеме V=1 см 3 равно числу состояний в зоне:. При ширине зоны 1 эВ среднее расстояние между ее уровнями ~ 10 -22 эВ, то есть энергетическую зону можно считать квазинепрерывной.
На любом энергетическом уровне в разрешенной зоне в соответствии с принципом Паули могут находиться не более двух электронов с противоположно направленными спинами.
Число квантовых состояний в зоне равно общему числу мест на уровнях изолированных атомов, из которых образовалась эта зона, таким образом, на N уровнях могут находиться не более 2N электронов.
Рассмотрим последнюю полностью или частично заполненную зону, сформированную из валентных электронов и следующую за ней, то есть зону энергий, соответствующую энергиям электронов, разорвавших связь с атомами, но не покинувших кристалл.
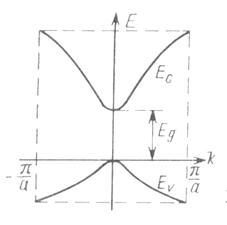
В каждой энергетической зоне энергия электрона является функцией его квазиимпульса (волнового вектора): =. На рис.1.3 для двух смежных зон представлены простейшие зависимости E(k), характерные для кубического кристалла. Вблизи экстремумов мы получаем параболическое изменение энергии.
 | |
| Рис. 1.3. Энергетическая диаграмма | Упрощенная энергетическая диаграмма |
Верхняя зона называется зоной проводимости, поскольку зона имеет множество свободных состояний, попавшие в неё электроны могут перемещаться под действием внешних полей, изменяя свое положение и энергию, т.е. создавая токи проводимости.
Нижняя зона – валентная. Электрон попасть в зону проводимости из валентной зоны может, только преодолев запрещенную зону величиной Eg. Энергетический уровень, соответствующий дну зоны проводимости принято обозначать Ec. Энергетический уровень, соответствующий потолку валентной зоны обозначают Ev.
В зависимости от положения экстремумов энергетических зон различают прямозонные и непрямозонные полупроводники (рис. 1.4).
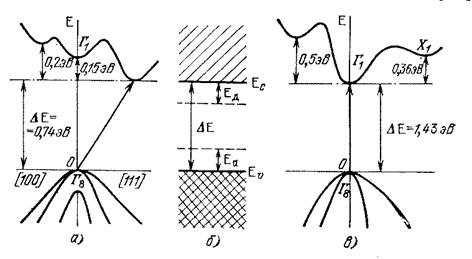 |
| Рис. 1.4. Зонная диаграмма |
Ширина запрещенной зоны Eg - одна из важнейших характеристик вещества и может принимать как положительные (для диэлектриков и полупроводников), так и отрицательные значения. В последнем случае дно зоны проводимости будет находиться при энергиях меньших, чем потолок валентной зоны. На рис.1.5 приведена схема энергетических зон для полупроводников, диэлектриков и металлов.
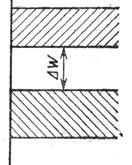 | 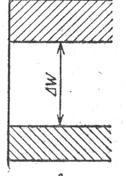 |  |
| Рис. 1.5. |
Полупроводники и диэлектрики отличаются только шириной запрещенной зоны. Так, у диэлектриков ширина запрещенной зоны, как правило, больше 4 эВ. При комнатной температуре тепловой энергии недостаточно для заброса электронов из валентной зоны в зону проводимости. Для металлов характерно отсутствие запрещенной зоны.
При воздействии на кристалл температуры и давления изменяются расстояния между атомами, области перекрытия волновых функций. Это вызывает изменение ширины энергетических и запрещенных зон.
| , | (1.17) |
| Рис. 1.6. Температурная зависимость Eg для кремния |
Значения близки к единице, - температурный коэффициент изменения ширины запрещенной зоны.
Значения , и для основных полупроводников, применяемых в микроэлектронике приведены в табл. 1.1.
Значение Eg и для некоторых полупроводников
| Полупроводники | Ge | Si | GaAs |
| Eg(T=300K), эВ | 0,66 | 1,11 | 1,43 |
| (T=0K), эВ | 0,74 | 1,166 | 1,52 |
| , эВ·К -1 | -2,4·10 -4 | -3,9·10 -4 | -4,3·10 -4 |
Для свободного электрона мы записывали =.Отличие свободного электрона, от электрона, находящегося в кристалле в его эффективной массе, определяемой как:
Вторая производная характеризует степень крутизны зависимости E(k), чем круче эта зависимость, тем меньше масса электрона. Эффективная масса электрона в кристалле зависит от его энергии и является характеристикой материала.
Читайте также:
