Гидрид щелочного металла с водой
Обновлено: 21.09.2024
У атомов ЩМ на внешнем электронном уровне находится только один электрон на s-подуровне, легко отрывающийся при протекании химических реакций. При этом из нейтрального атома ЩМ образуется положительно заряженная частица – катион с зарядом +1:
Семейство ЩМ является наиболее активным среди прочих групп металлов в связи с чем в природе обнаружить их в свободной форме, т.е. в виде простых веществ невозможно.
Простые вещества щелочные металлы являются крайне сильными восстановителями.
Взаимодействие щелочных металлов с неметаллами
с кислородом
Щелочные металлы реагируют с кислородом уже при комнатной температуре, в связи с чем их требуется хранить под слоем какого-либо углеводородного растворителя, такого как, например, керосина.
Взаимодействие ЩМ с кислородом приводит к разным продуктам. С образованием оксида, с киcлородом реагирует только литий:
Натрий в аналогичной ситуации образует с кислородом пероксид натрия Na2O2:
а калий, рубидий и цезий – преимущественно надпероксиды (супероксиды), общей формулы MeO2:
с галогенами
Щелочные металлы активно реагируют с галогенами, образуя галогениды щелочных металлов, имеющих ионное строение:
2Li + Br2 = 2LiBr бромид лития
2Na + I2 = 2NaI иодид натрия
2K + Cl2 = 2KCl хлорид калия
с азотом
Литий реагирует с азотом уже при обычной температуре, с остальными же ЩМ азот реагирует при нагревании. Во всех случаях образуются нитриды щелочных металлов:
с фосфором
Щелочные металлы реагируют с фосфором при нагревании, образуя фосфиды:
3Na + P = Na3Р фосфид натрия
3K + P = K3Р фосфид калия
с водородом
Нагревание щелочных металлов в атмосфере водорода приводит к образованию гидридов щелочных металлов, содержащих водород в редкой степени окисления – минус 1:
Н2 + 2K = 2KН -1 гидрид калия
Н2 + 2Rb = 2RbН гидрид рубидия
с серой
Взаимодействие ЩМ с серой протекает при нагревании с образованием сульфидов:
S + 2Na = Na2S сульфид натрия
Взаимодействие щелочных металлов со сложными веществами
с водой
Все ЩМ активно реагируют с водой с образованием газообразного водорода и щелочи, из-за чего данные металлы и получили соответствующее название:
2HOH + 2Na = 2NaOH + H2↑
2K + 2HOH = 2KOH + H2↑
Литий реагирует с водой довольно спокойно, натрий и калий самовоспламеняются в процессе реакции, а рубидий, цезий и франций реагируют с водой с мощным взрывом.
с галогенпроизводными углеводородов (реакция Вюрца):
со спиртами и фенолами
ЩМ реагируют со спиртами и фенолами, замещая водород в гидроксильной группе органического вещества:
Щелочные металлы. Химия щелочных металлов и их соединений

Щелочные металлы расположены в главной подгруппе первой группы периодической системы химических элементов Д.И. Менделеева (или просто в 1 группе в длиннопериодной форме ПСХЭ). Это литий Li, натрий Na, калий K, цезий Cs, рубидий Rb и франций Fr.
Электронное строение щелочных металлов и основные свойства
Электронная конфигурация внешнего энергетического уровня щелочных металлов: ns 1 , на внешнем энергетическом уровне находится 1 s-электрон. Следовательно, типичная степень окисления щелочных металлов в соединениях +1.
Рассмотрим некоторые закономерности изменения свойств щелочных металлов.
В ряду Li-Na-K-Rb-Cs-Fr, в соответствии с Периодическим законом, увеличивается атомный радиус , усиливаются металлические свойства , ослабевают неметаллические свойства , уменьшается электроотрица-тельность .

Физические свойства
Все щелочные металлы — вещества мягкие, серебристого цвета. Свежесрезанная поверхность их обладает характерным блеском.

Кристаллическая решетка щелочных металлов в твёрдом состоянии — металлическая. Следовательно, щелочные металлы обладают высокой тепло- и электропроводимостью. Кипят и плавятся при низких температурах. Они имеют также небольшую плотность.

Нахождение в природе
Как правило, щелочные металлы в природе присутствуют в виде минеральных солей: хлоридов, бромидов, йодидов, карбонатов, нитратов и др. Основные минералы , в которых присутствуют щелочные металлы:
Поваренная соль, каменная соль, галит — NaCl — хлорид натрия

Сильвин KCl — хлорид калия

Сильвинит NaCl · KCl

Глауберова соль Na2SO4⋅10Н2О – декагидрат сульфата натрия

Едкое кали KOH — гидроксид калия
Поташ K2CO3 – карбонат калия
Поллуцит — алюмосиликат сложного состава с высоким содержанием цезия:

Способы получения
Литий получают в промышленности электролизом расплава хлорида лития в смеси с KCl или BaCl2 (эти соли служат для понижения температуры плавления смеси):
2LiCl = 2Li + Cl2
Натрий получают электролизом расплава хлорида натрия с добавками хлорида кальция:
2NaCl (расплав) → 2Na + Cl2
Электролитом обычно служит смесь NaCl с NaF и КСl (что позволяет проводить процесс при 610–650°С).
Калий получают также электролизом расплавов солей или расплава гидроксида калия. Также распространены методы термохимического восстановления: восстановление калия из расплавов хлоридов или гидроксидов. В качестве восстановителей используют пары натрия, карбид кальция, алюминий, кремний:
KCl + Na = K↑ + NaCl
KOH + Na = K↑ + NaOH
Цезий можно получить нагреванием смеси хлорида цезия и специально подготовленного кальция:
Са + 2CsCl → 2Cs + CaCl2
В промышленности используют преимущественно физико-химические методы выделения чистого цезия: многократную ректификацию в вакууме.
Качественные реакции
Качественная реакция на щелочные металлы — окрашивание пламени солями щелочных металлов .

Цвет пламени:
Li — карминно-красный
Na — жѐлтый
K — фиолетовый
Rb — буро-красный
Cs — фиолетово-красный
Химические свойства
1. Щелочные металлы — сильные восстановители . Поэтому они реагируют почти со всеми неметаллами .
1.1. Щелочные металлы легко реагируют с галогенами с образованием галогенидов:
2K + I2 = 2KI
1.2. Щелочные металлы реагируют с серой с образованием сульфидов:
2Na + S = Na2S
1.3. Щелочные металлы активно реагируют с фосфором и водородом (очень активно). При этом образуются бинарные соединения — фосфиды и гидриды:
3K + P = K3P
2Na + H2 = 2NaH
1.4. С азотом литий реагирует при комнатной температуре с образованием нитрида:
Остальные щелочные металлы реагируют с азотом при нагревании.
1.5. Щелочные металлы реагируют с углеродом с образованием карбидов, преимущественно ацетиленидов:
1.6. При взаимодействии с кислородом каждый щелочной металл проявляет свою индивидуальность: при горении на воздухе литий образует оксид, натрий – преимущественно пероксид, калий и остальные металлы – надпероксид.
Цезий самовозгорается на воздухе, поэтому его хранят в запаянных ампулах. Видеоопыт самовозгорания цезия на воздухе можно посмотреть здесь.
2. Щелочные металлы активно взаимодействуют со сложными веществами:
2.1. Щелочные металлы бурно (со взрывом) реагируют с водой . Взаимодействие щелочных металлов с водой приводит к образованию щелочи и водорода. Литий реагирует бурно, но без взрыва.
Например , калий реагирует с водой очень бурно:
2K 0 + H2 + O = 2 K + OH + H2 0

Видеоопыт: взаимодействие щелочных металлов с водой можно посмотреть здесь.
2.2. Щелочные металлы взаимодействуют с минеральными кислотами (с соляной, фосфорной и разбавленной серной кислотой) со взрывом. При этом образуются соль и водород.
Например , натрий бурно реагирует с соляной кислотой :
2Na + 2HCl = 2NaCl + H2↑
2.3. При взаимодействии щелочных металлов с концентрированной серной кислотой выделяется сероводород.
Например , при взаимодействии натрия с концентрированной серной кислотой образуется сульфат натрия, сероводород и вода:
2.4. Щелочные металлы реагируют с азотной кислотой. При взаимодействии с концентрированной азотной кислотой образуется оксид азота (I):
С разбавленной азотной кислотой образуется молекулярный азот:
При взаимодействии щелочных металлов с очень разбавленной азотной кислотой образуется нитрат аммония:
2.5. Щелочные металлы могут реагировать даже с веществами, которые проявляют очень слабые кислотные свойства . Например, с аммиаком, ацетиленом (и прочими терминальными алкинами), спиртами , фенолом и органическими кислотами .
Например , при взаимодействии лития с аммиаком образуются амиды и водород:
Ацетилен с натрием образует ацетиленид натрия и также водород:
Н ─ C ≡ С ─ Н + 2Na → Na ─ C≡C ─ Na + H2
Фенол с натрием реагирует с образованием фенолята натрия и водорода:
Метанол с натрием образуют метилат натрия и водород:
Уксусная кислота с литием образует ацетат лития и водород:
2СH3COOH + 2Li → 2CH3COOLi + H2↑
Щелочные металлы реагируют с галогеналканами (реакция Вюрца).
Например , хлорметан с натрием образует этан и хлорид натрия:
2.6. В расплаве щелочные металлы могут взаимодействовать с некоторыми солями . Обратите внимание! В растворе щелочные металлы будут взаимодействовать с водой, а не с солями других металлов.
Например , натрий взаимодействует в расплаве с хлоридом алюминия :
3Na + AlCl3 → 3NaCl + Al
Оксиды щелочных металлов
Оксиды щелочных металлов (кроме лития) можно получить только к освенными методами : взаимодействием натрия с окислителями в расплаве:
1. О ксид натрия можно получить взаимодействием натрия с нитратом натрия в расплаве:
2. Взаимодействием натрия с пероксидом натрия :
3. Взаимодействием натрия с расплавом щелочи :
2Na + 2NaOН → 2Na2O + Н2↑
4. Оксид лития можно получить разложением гидроксида лития :
2LiOН → Li2O + Н2O
Химические свойства
Оксиды щелочных металлов — типичные основные оксиды . Вступают в реакции с кислотными и амфотерными оксидами, кислотами, водой.
1. Оксиды щелочных металлов взаимодействуют с кислотными и амфотерными оксидами :
Например , оксид натрия взаимодействует с оксидом фосфора (V):
Оксид натрия взаимодействует с амфотерным оксидом алюминия:
2. Оксиды щелочных металлов взаимодействуют с кислотами с образованием средних и кислых солей (с многоосновными кислотами).
Например , оксид калия взаимодействует с соляной кислотой с образованием хлорида калия и воды:
K2O + 2HCl → 2KCl + H2O
3. Оксиды щелочных металлов активно взаимодействуют с водой с образованием щелочей.
Например , оксид лития взаимодействует с водой с образованием гидроксида лития:
Li2O + H2O → 2LiOH
4. Оксиды щелочных металлов окисляются кислородом (кроме оксида лития): оксид натрия — до пероксида, оксиды калия, рубидия и цезия – до надпероксида.
Пероксиды щелочных металлов
Свойства пероксидов очень похожи на свойства оксидов. Однако пероксиды щелочных металлов, в отличие от оксидов, содержат атомы кислорода со степенью окисления -1. Поэтому они могут могут проявлять как окислительные , так и восстановительные свойства.
1. Пероксиды щелочных металлов взаимодействуют с водой . При этом на холоде протекает обменная реакция, образуются щелочь и пероксид водорода:
При нагревании пероксиды диспропорционируют в воде, образуются щелочь и кислород:
2. Пероксиды диспропорционируют при взаимодействии с кислотными оксидами .
Например , пероксид натрия реагирует с углекислым газом с образованием карбоната натрия и кислорода:
3. При взаимодействии с минеральными кислотами на холоде пероксиды вступают в обменную реакцию. При этом образуются соль и перекись водорода:
При нагревании пероксиды, опять-таки, диспропорционируют:
4. Пероксиды щелочных металлов разлагаются при нагревании, с образованием оксида и кислорода:
5. При взаимодействии с восстановителями пероксиды проявляют окислительные свойства.
Например , пероксид натрия с угарным газом реагирует с образованием карбоната натрия:
Пероксид натрия с сернистым газом также вступает в ОВР с образованием сульфата натрия:
6. При взаимодействии с сильными окислителями пероксиды проявляют свойства восстановителей и окисляются, как правило, до молекулярного кислорода.
Например , при взаимодействии с подкисленным раствором перманганата калия пероксид натрия образует соль и молекулярный кислород:
Гидроксиды щелочных металлов (щелочи)
1. Щелочи получают электролизом растворов хлоридов щелочных метал-лов:
2NaCl + 2H2O → 2NaOH + H2 + Cl2
2. При взаимодействии щелочных металлов, их оксидов, пероксидов, гидридов и некоторых других бинарных соединений с водой также образуются щелочи.
Например , натрий, оксид натрия, гидрид натрия и пероксид натрия при растворении в воде образуют щелочи:
2Na + 2H2O → 2NaOH + H2
Na2O + H2O → 2NaOH
2NaH + 2H2O → 2NaOH + H2
3. Некоторые соли щелочных металлов (карбонаты, сульфаты и др.) при взаимодействии с гидроксидами кальция и бария также образуют щелочи.
Например , карбонат калия с гидроксидом кальция образует карбонат кальция и гидроксид калия:
1. Гидроксиды щелочных металлов реагируют со всеми кислотами (и сильными, и слабыми, и растворимыми, и нерастворимыми). При этом образуются средние или кислые соли, в зависимости от соотношения реагентов.
Например , гидроксид калия с фосфорной кислотой реагирует с образованием фосфатов, гидрофосфатов или дигидрофосфатов:
2. Гидроксиды щелочных металлов реагируют с кислотными оксидами . При этом образуются средние или кислые соли, в зависимости от соотношения реагентов.
Например , гидроксид натрия с углекислым газом реагирует с образованием карбонатов или гидрокарбонатов:
Необычно ведет себя оксид азота (IV) при взаимодействии с щелочами. Дело в том, что этому оксиду соответствуют две кислоты — азотная (HNO3) и азотистая (HNO2). «Своей» одной кислоты у него нет. Поэтому при взаимодействии оксида азота (IV) с щелочами образуются две соли- нитрит и нитрат:
А вот в присутствии окислителя, например, молекулярного кислорода, образуется только одна соль — нитрат, т.к. азот +4 только повышает степень окисления:
3. Гидроксиды щелочных металлов реагируют с амфотерными оксидами и гидроксидами . При этом в расплаве образуются средние соли, а в растворе комплексные соли.
Например , гидроксид натрия с оксидом алюминия реагирует в расплаве с образованием алюминатов:
в растворе образуется комплексная соль — тетрагидроксоалюминат:
Еще пример : гидроксид натрия с гидроксидом алюминия в расплаве образут также комплексную соль:
4. Щелочи также взаимодействуют с кислыми солями. При этом образуются средние соли, или менее кислые соли.
Например : гидроксид калия реагирует с гидрокарбонатом калия с образованием карбоната калия:
5. Щелочи взаимодействуют с простыми веществами-неметаллами (кроме инертных газов, азота, кислорода, водорода и углерода).
При этом кремний окисляется щелочами до силиката и водорода:
Фтор окисляет щелочи. При этом выделяется молекулярный кислород:
Другие галогены, сера и фосфор — диспропорционируют в щелочах:
Сера взаимодействует с щелочами только при нагревании:
6. Щелочи взаимодействуют с амфотерными металлами , кроме железа и хрома . При этом в расплаве образуются соль и водород:
В растворе образуются комплексная соль и водород:
2NaOH + 2Al + 6Н2О = 2Na[Al(OH)4] + 3Н2
7. Гидроксиды щелочных металлов вступают в обменные реакции с растворимыми солями .
С щелочами взаимодействуют соли тяжелых металлов.
Например , хлорид меди (II) реагирует с гидроксидом натрия с образованием хлорида натрия и осадка гидроксида меди (II):
2NaOH + CuCl2 = Cu(OH)2↓+ 2NaCl
Также с щелочами взаимодействуют соли аммония.
Например , при взаимодействии хлорида аммония и гидроксида натрия образуются хлорид натрия, аммиак и вода:
NH4Cl + NaOH = NH3 + H2O + NaCl
8. Гидроксиды всех щелочных металлов плавятся без разложения , гидроксид лития разлагается при нагревании до температуры 600°С:
2LiOH → Li2O + H2O
9. Все гидроксиды щелочных металлов проявляют свойства сильных оснований . В воде практически нацело диссоциируют , образуя щелочную среду и меняя окраску индикаторов.
NaOH ↔ Na + + OH —
10. Гидроксиды щелочных металлов в расплаве подвергаются электролизу . При этом на катоде восстанавливаются сами металлы, а на аноде выделяется молекулярный кислород:
4NaOH → 4Na + O2 + 2H2O
Соли щелочных металлов
Нитраты и нитриты щелочных металлов
Нитраты щелочных металлов при нагревании разлагаются на нитриты и кислород. Исключение — нитрат лития. Он разлагается на оксид лития, оксид азота (IV) и кислород.
Например , нитрат натрия разлагается при нагревании на нитрит натрия и молекулярный кислород:
Нитраты щелочных металлов в реакциях могут выступать в качестве окислителей.
Нитриты щелочных металлов могут быть окислителями или восстановителями.
В щелочной среде нитраты и нитриты — очень мощные окислители.
Например , нитрат натрия с цинком в щелочной среде восстанавливается до аммиака:
Сильные окислители окисляют нитриты до нитратов.
Например , перманганат калия в кислой среде окисляет нитрит натрия до нитрата натрия:
ГИДРИДЫ
ГИДРИДЫ, соединения водорода с металлами или менее электроотрицательными, чем водород, неметаллами. Иногда к гидридам относят соед. всех хим. элементов с водородом. Различают простые, или бинарные, гидриды, комплексные (см., напр., Алюмогидриды, Борогидриды металлов)и гидриды интерметаллич. соединений. Для большинства переходных металлов известны также комплексные соед., содержащие атом Н наряду с др. лигандами в координац. сфере металла-комплексообразователя.
Простые гидриды. Известны для всех элементов, кроме благородных газов, платиновых металлов (исключение -Pd), Ag, Au, Cd, Hg, In, Tl. В зависимости от природы связи элемента (Э) с водородом подразделяются на ковалентные, ионные (солеобразные) и металлоподобные (металлические), однако эта классификация условна, т. к. между разл. типами простых гидридов резких границ нет.
К ковалентным относят гидриды неметаллов, Al, Be, Sn, Sb. Гидриды SiH4, GeH4, SnH4, PH3, AsH3, SbH3, H2S, H2Se, H2Te (см. табл. 1) и низшие бороводороды-газы. Ковалентные гидриды обладают высокой реакц. способностью. Эффективный положит. заряд атома Э в молекуле возрастает в пределах одной группы периодич. системы с увеличением его порядкового номера. Элементы Si и Ge образуют высшие гидриды общей ф-лы ЭnН2n + 2 (п 2 и Н2. Все эти гидриды раств. в неполярных или малополярных орг. р-рителях. Ковалентные гидриды-сильные восстановители. Легко вступают в обменные р-ции, напр. с галогенидами металлов. При 100-300 °С (H2S ок. 400 °С) разлагаются практически необратимо до Э и Н2.
Гидриды подгруппы фосфора получают р-цией ЭС13 с Li[AlH4] в эфире при 25 °С; SiH4 и GeH4-взаимод. Мg2Э с водой или с В2Н6 в жидком NH3; H2S, H2Se и Н2Те-кислотным гидролизом сульфидов, селенидов или теллуридов металлов (H2S-также взаимод. Н, и S). Все упомянутые гидриды, особенно AsH3 и РН3, высокотоксичны. Гидриды Ge, Si, As используют для получения полупроводниковых материалов. См. также Мышьяка гидрид, Сероводород, Силаны, Фосфины.
К ионным относят гидриды щелочных и щел.-зем. металлов (кроме Mg). Эти соед.-структурные аналоги соответствующих галогенидов. Представляют собой кристаллы, к-рые в расплавл. состоянии проводят электрич. ток, причем Н2 выделяется на аноде. Не раств. в орг. р-рителях, хорошо раств. в расплавах галогенидов щелочных металлов. Обладают высокой хим. активностью, бурно реагируют с О2 и влагой воздуха. Взаимод. с водой (напр., МН + Н2О -> МОН + Н2) сопровождается выделением тепла. В эфире, диглиме, ТГФ легко (особенно LiH и NaH) реагируют с галогенидами или гидридами В и А1, образуя соотв. борогидриды М[ВН4]n и алюмогидриды М[А1Н4]n. При 700-800°С восстанавливают оксиды до металлов. С СО2 дают соли муравьиной к-ты. Взаимод. с N2, напр. 3СаН2 + + N2->Ca3N2 + ЗН2.
Получают ионные гидриды обычно взаимод. Н2 с расплавом соответствующего металла под давлением. Их используют в кач-ве сильных восстановителей (напр., для получения металлов из их оксидов или галогенидов, удаления окалины с пов-стей изделий из стали и тугоплавких металлов). Многие гидриды-источники Н2, перспективное ракетное топливо. Дейтериды и тритиегидриды - возможное горючее для ядерных реакторов. См. также Лития гидрид.
Гидрид Mg по св-вам и природе хим. связи занимает промежут. положение между ковалентными и ионными гидридами; кристаллы с решеткой типа ТiO2; при высоких давлениях ( ~ 7 МПа) претерпевает полиморфные превращения. С водой и водными р-рами к-т и щелочей MgH2 взаимод. с выделением Н2, однако менее энергично, чем гидриды щелочных и др. щел.-зем. металлов. М. б. получен взаимод. Mg с Н2 при 200-250 °С и давлении 10 МПа (скорость р-ции мала) либо обменной р-цией MgHal2 с МН или М [А1Н4], где М—Li, Na, в среде орг. р-рителя. Легко образуется при гидрировании сплавов Mg, содержащих небольшие добавки РЗЭ и переходных металлов, при 150-180°С и 1-5 МПа, причем р-ция обратима. В связи с этим такие сплавы-перспективные хим. аккумуляторы Н2 для нужд малой энергетики, металлургии и хим. технологии.
К металлоподобным относят гидриды переходных металлов и РЗЭ. Формально такие соед. могут рассматриваться как фазы внедрения водорода в металл. Их образованию всегда предшествует адсорбция Н2 на пов-сти металла.
Адсорбированная молекула диссоциирует на атомы Н, в результате диффузии к-рых в кристаллич. решетку происходит образование т.н. 2 в , как правило, стехиометрич. состава (МН3 для металлов III гр., МН2 для IV гр. и ванадия). Взаимод. Н2 с указанными металлами (кроме Pd) всегда сопровождается перестройкой кристаллич. решетки. Для описания природы хим. связи водорода с металлич. матрицей используют представление о типе связи, промежуточном между ионной и металлической; электроны водорода в большей или меньшей степени участвуют в формировании зоны проводимости гидридов. По-видимому, вклад ионной составляющей связи М + —Н - Наиб. велик для EuH2, YbH2 и тригидридов лантаноидов и минимален для PdH0,6, а также для гидридов Mn, Fe, Co, Ni, существующих при высоких давлениях Н2 и содержащих менее одного атома Н на атом металла.
Металлоподобные гидриды (см. табл. 2)-светло- и темно-серые кристаллы с металлич. блеском, устойчивые на воздухе при комнатной т-ре. С О2, водой и водяным паром реагируют медленно. М.б. получены взаимод. металла с Н2 при обычной т-ре или при нагр.; напр., TiH2 и LaH3 синтезируют при 150-200 °С. Получение гидридов стехиометрич. состава в большинстве случаев сопряжено со значит. трудностями из-за высокой чувствительности гидрироваиия к наличию примесей в металле и особенно О2 и водяных паров в Н2. Металлоподобные гидриды ограниченно применяют в кач-ве источников Н2 высокой чистоты (используемых, напр., в топливных элементах) и для поглощения Н2 из газовых смесей. Гидриды Pd-катализаторы гидрирования, изомеризации, орто- и парапревращения Н2.
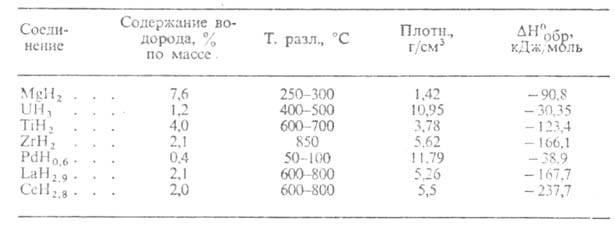
Табл. 2.-СВОЙСТВА МЕТАЛЛОПОДОБНЫХ ГИДРИДОВ
Гидриды интерметаллических соединений. Содержат обычно атомы РЗЭ, Mg, Ca, Ti, Al, Fe, Co, Ni, Си. Легко образуются при взаимод. интерметаллидов даже с техн. Н2 (содержащим до 1-2% примесей О2 и водяного пара) при 25-200°С и давлениях Н2 0,1-1 МПа; скорость поглощения Н2 очень велика. Р-ции характеризуются малыми тепловыми эффектами (20-30 кДж на 1 моль Н2, для индивидуальных металлов-100-120 кДж) и не приводят к значит. изменениям в структуре исходной металлич. матрицы; в большинстве случаев происходит лишь увеличение ее объема на 10-30%. Для гидридов этого типа характерна высокая подвижность водорода и большая хим. активность (о св-вах см. также табл. 3).
Данная р-ция характерна для соед., образованных РЗЭ и Mg, а также РЗЭ и Fe, Ni или Со. Так, гидрид РЗЭ, образующийся при гидрогенолизе интерметаллида, содержащего Mg, катализирует как гидрирование Mg, так и дегидрирование MgH2 при 150-180°С: МН2 + nMg + (n + 0,5) Н2 МН3 + nMgH2
Благодаря высокому содержанию Н2, возможности значит. смещения равновесия в ту или др. сторону посредством небольших изменений т-ры и давления Н2, способности поглощать Н2 при низких т-рах и устойчивости к действию О2 и влаги воздуха, гидриды интерметаллич. соединений м.б. использованы как хим. аккумуляторы слабосвязанного водорода. Перспективно их применение как источников топлива для автономных энергосистем, напр. автомобильного транспорта (см. Водородная энергетика), а также для получения высокодисперсных металлич. порошков и катализаторов гетерог. гидрирования.

Табл. 3.-СВОЙСТВА ГИДРИДОВ ИНТЕРМЕТАЛЛИЧЕСКИХ СОЕДИНЕНИЙ
===
Исп. литература для статьи «ГИДРИДЫ» : Гидриды металлов, пер. с англ., М., 1973; Девятых ГГ., Зорин А. Д., Летучие неорганические гидриды особой чистоты, М., 1974; Антонова А. М., Морозова Р. А., Препаративная химия гидридов. К., 1976; Водород в металлах, пер. с англ., т. 2, М., 1981. К.Н. Семененко.
Гидриды
Гидр и ды, соединения водорода с другими элементами. В зависимости от характера связи водорода различают три типа гидридов: ионные, металлические и ковалентные.
К ионным (солеобразным) гидридам относятся гидриды щелочных и щёлочноземельных металлов. Это белые кристаллические вещества, устойчивые в обычных условиях и лишь при нагревании разлагающиеся без плавления на металл и водород (кроме LiH, плавящегося при 680°С). Водой энергично разлагаются с выделением водорода. Получаются при взаимодействии металлов с водородом при 200—600°С. LiH и NaH применяются в органическом синтезе как восстановители и конденсирующие агенты. CaH2 — для высушивания и определения воды в органических растворителях, при получении порошков металлов из окислов, а также водорода. Раствором NaH в расплавленной щёлочи снимают окалину с металлических изделий. Ионное строение имеют и двойные гидриды — борогидриды МеВН4 и алюмогидриды MeA1H4 (см. Алюминия гидрид), широко используемые в органическом синтезе в качестве эффективных восстановителей.
Гидриды переходных металлов принадлежат к типу металлических, т.к. по характеру химических связи они сходны с металлами. Эти гидриды в большинстве случаев являются соединениями переменного состава, и приводимые ниже формулы дают лишь предельное содержание в них водорода. Многие металлы способны поглощать значительное количество водорода с образованием твёрдых растворов, сохраняющих кристаллическую структуру данного металла. Напротив, истинные гидриды имеют структуру иную, чем исходный металл. Для металлов III группы периодической системы (подгруппа Sc и лантаноиды) характерно образование двух типов гидридов — MeH2 и MeH3. Металлы IV группы (подгруппа Ti) образуют гидриды MeH2, а металлы V группы (подгруппа ванадия) — MeH. Гидриды металлов этих групп — хрупкие твёрдые вещества серого или чёрного цвета, получаются при действии водорода на мелкораздробленные металлы при повышенных температурах. Металлы VI, VII и VIII групп (кроме палладия) при поглощении водорода не дают определённых химических соединений.
Гидриды переходных металлов служат катализаторами различных химических реакций. Способность металлов образовывать гидриды используется в высоковакуумной технике для связывания водорода. В результате образования гидридов, например при действии паров воды на раскалённый металл и при электролитическом выделении металлов, ухудшается качество металлов (появляется т. н. водородная хрупкость).
Гидриды переходных металлов I и II групп периодической системы, а также гидриды III группы (подгруппа A1) не образуются при взаимодействии металла с водородом. Они получаются, например, при восстановлении соединений этих металлов алюмогидридом лития LiAlH в эфирном растворе. Все они при нагревании легко разлагаются на металл и водород.
Ковалентные гидриды образуются неметаллами IV, V, VI и VII групп периодической системы, а также бором. Кроме простейших соединений этого типа (метана CH4, силана SiH4 и т.п.), являющихся газами, известны гидриды с большим числом атомов элемента, соединённых друг с другом в виде цепей, например силаны SinH2n+2. Простейший гидрид бора ВН3 не существует, бороводороды имеют сложное строение. Гидриды элементов первых периодов очень стабильны, гидриды тяжёлых элементов крайне неустойчивы. Многие гидриды (B2H6, SiH4, PH3) легко воспламеняются на воздухе. B2H6 и SiH4 разлагаются водой с выделением водорода. Гидриды элементов V, VI и VII групп водой не разлагаются. Известны многочисленные производные ковалентных гидридов, в которых часть атомов водорода замещена на атомы галогена или металла, а также на алкильные и др. группы. Ковалентные гидриды получают непосредственным взаимодействием элементов, разложением металлических соединений водой или кислотами, восстановлением галогенидов и др. соединений гидридами, борогидридами и алюмогидридами щелочных металлов. Термическое разложение гидридов служит одним из методов получения особо чистых элементов (например, кремния, германия).
Лит.: Херд Д., Введение в химию гидридов, пер. с англ., М., 1955; Жигач А. Ф., Стасиневич Д. С., Химия гидридов, Л., 1969; Михеева В. И., Гидриды переходных металлов, М., 1960; Маккей К., Водородные соединения металлов, пер. с англ., М., 1968; Галактионова Н. А., Водород в металлах, 2 изд., М., 1967.
Гидриды - свойства, формулы и применение водородных соединений
Соединения водорода с другими элементами, в которых он выступает как более электроотрицательный элемент, называют гидридами. Но часто так именуют любые химические вещества, образованные водородом с другими элементами. Водород — элемент не из редких, вещества, образованные его взаимодействием с другими элементами, в природе встречаются часто. Человек имеет с ними дело постоянно. Самый знакомый — Н2О, вода, или гидрид кислорода.
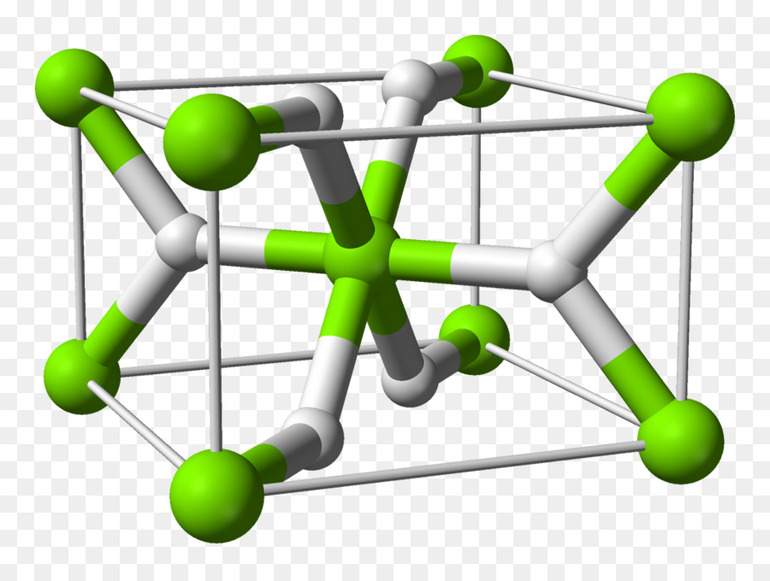
Типы и классификация
Вещества, созданные водородом с металлами и неметаллами многобразны. В зависимости от характера полученного соединения, выделяют:
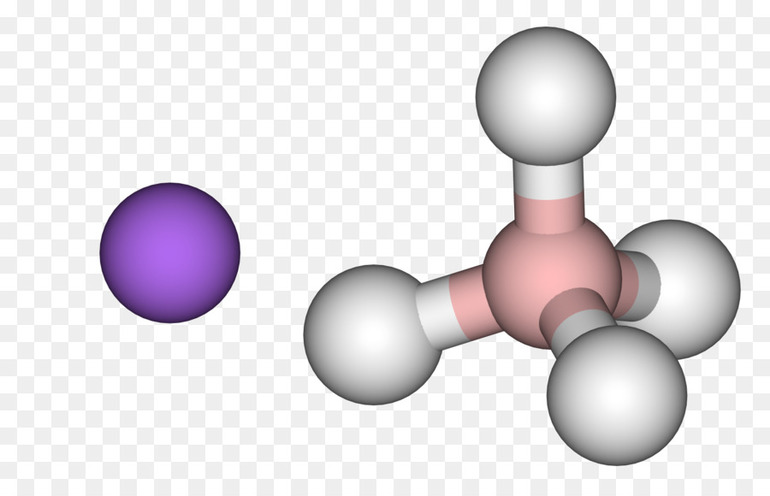
- Простые гидриды — бинарные, в них только 2 элемента, они встречаются чаще всего.
- Со многими переходными металлами (элементы р-подгруппы) водород образует ко́мплексные соединения. Ко́мплексные гидриды металлов (к примеру, боро- или алюмогидриды) вместо атома водорода, имеют алюмогруппу (AlH4) или борогруппу (BH4). Из них натрийборогидрид Na (BH4) и литийалюмогидрид Li (AlH4), будучи сильными восстановителями, нашли применение в лабораторной практике. Кроме этого, Na (BH4) используют для отбеливания бумаги.
- И также есть гидриды интерметаллидов (пример: TiAl или Ti3Al, алюминид титана), в кристаллических решётках которых водород просто растворяется, аккумулируется.
У разных химических элементов строение атомов и молекул отличается. Соответственно, связи в образованных гидридах тоже неодинаковы. Классификация по виду связи определяет полученные вещества, как:
- металлоподобные;
- ионные (солеобразные);
- ковалентные.
Бинарные соединения самые распространённые, есть у всех элементов. Исключения здесь металлы платиновой группы (платиноиды), Au, Ag, Hg, Ti, Cd, In, а также благородные газы. Между этими веществами нет чётко выраженных границ, деление по характеру связи для них немного условно.
Металлические гидриды
К металлическим принадлежат соединения водорода с переходными металлами и редкоземельными элементами. Это, скорее, раствор неметалла в металле, с внедрением атомов в кристаллическую решётку. Характерно для них следующее:

- В основном такие гидриды являются бертоллидами, состав их зависит от способа получения, непостоянен, законам постоянных и кратных отношений не подчиняется.
- В формулах для них указывают предельное содержание водорода.
- В отличие от прочих, они сохраняют исходную металлическую решётку.
- Их вид и физические свойства соответствуют металлам, с которыми они образованы.
- Имеют характе́рный металлический блеск, взаимодействуют с H2O (в жидком или газообразном состоянии), кислородом, при нормальных условиях, но медленно.
- Как и металлы, обладают значительной теплопроводностью и проводимостью.
- При нагревании распадаются на водород и исходный металл.
Образуются в процессе адсорбции водорода на металлической поверхности, диссоциации H2 и диффузного проникновения атомов в металлическую решётку. Поглощение обратимо, но химические связи весьма крепкие.
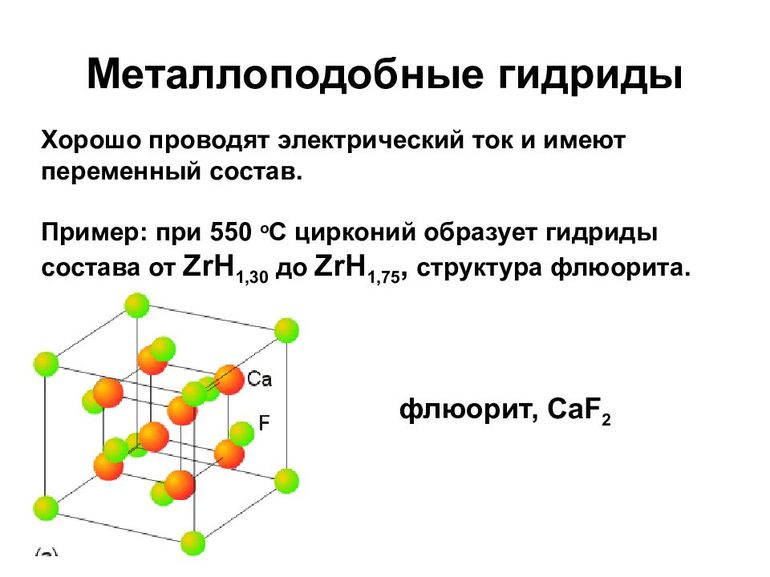
От металлоподобных, через гидриды меди (CuH, водородистая медь), цинка, ZnH2, водородистый цинк и им подобных, осуществляется переход к полимерам.
Это химические вещества со сложной структурой, в которой присутствуют цепи и полиэдры. Твёрдые, устойчивые, с кристаллическим строением (полимерные гидриды лёгких металлов стабильнее всего), данные соединения распадаются при нагреве на составляющие элементы.
От них, через гидриды бора и галлия — к водородным соединениям с неметаллами. В них водород имеет степень окисления +1.
Соединения с ионным типом связи
Их образует водород с металлами 1А и 2А групп, кроме Mg, а также с Al. Они отчасти показывают свойства соответствующих галогенидов, откуда и появилось второе наименование — солеобразные.
Это химические соединения, такие как гидрид натрия (NaH), кальция (CaH2), лития, с формулой LiH, другие. Для них характерно:
- Получают при высокой температуре и под давлением.
- В этих соединениях, проявляющих, как правило, щелочные свойства, у водорода степень окисления -1. С металлами 1А и 2А групп, такими, как Na, Li, Be, K, Rb, Sr он выступает окислителем, подобно галогенам. Например, гидрид натрия, с химической формулой NaH — в этом соединении ион водорода имеет отрицательный заряд.
- Это кристаллические вещества белого цвета, с ионной решёткой, структура подобна строению соответствующего галогенида.
- При нормальных условиях устойчивы.
- Распад на металл и водород при нагреве, минуя этап плавления (исключением является LiH, его температура плавления 688 градусов Цельсия).
- В расплаве — хорошие проводники, при этом на аноде будет выделяться H2.
- Вспыхивают при растирании на воздухе.
- Все являются сильными восстановителями. Применяются для получения чистых металлов из солей и оксидов, для удаления окалины, коррозии.
- Реагируют с оксидом углерода, формируют соли муравьиной кислоты (формиаты).
- Как и соли, могут участвовать в обменных реакциях, гидролизе.
Солеобразными бывают не только бинарные (простые) соединения водорода. Дигидриды, образуемые добавлением групп бора (BH4) или алюминия (AlH4) к металлу, также имеют ионный тип связи.
Окислительная активность водорода небольшая по сравнению с галогенами. Дополнительный электрон он отдаёт с трудом, при нагреве (реакция проходит с поглощением тепла). Это и обусловливает различие между свойствами ионных гидридов и галогенидов.
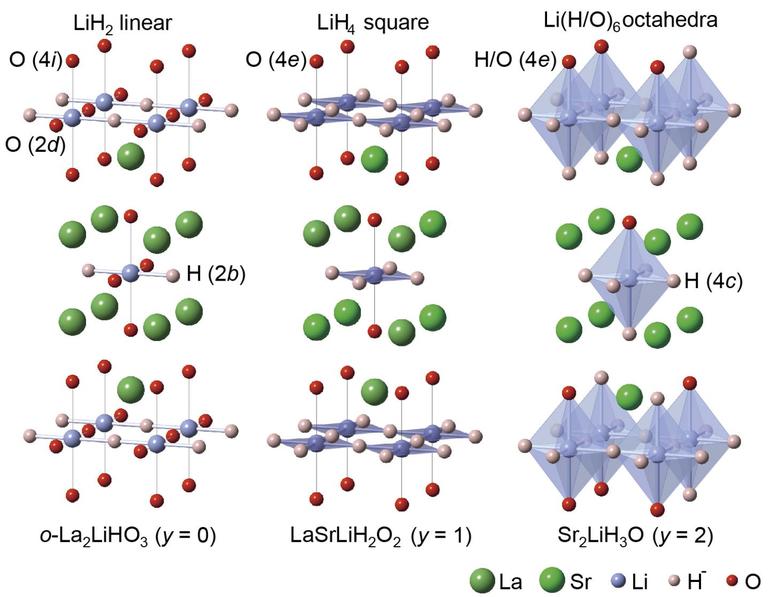
По химической природе такие соединения ведут себя как основные. Ионные гидриды обладают высокой химической активностью. Они бурно реагируют с кислородом и H2O в парообразном состоянии.
Но выраженный ионный характер — свойство, проявляемое соединениями кальция, натрия, щелочных и щёлочноземельных элементов. На них проще всего и нагляднее можно показать химию взаимодействий этих веществ:
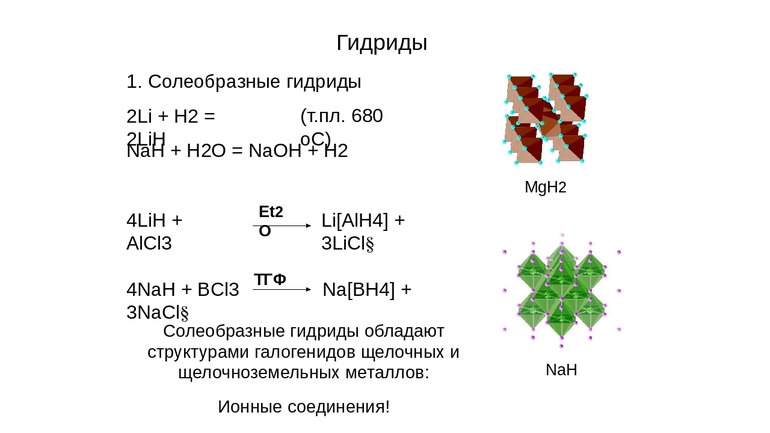
- С водой: 2NaH + H2O = 2NaOH + H2O.
- С кислородом: NaH + O2 = NaO + H2O.
- Реакция разложения: CaH2 = Ca + H2.
- С оксидами углерода: NaH + CO2 = NaCOOH.
- Кремния: 4NaH + 3SiO2 = 2Na2SiO3 + Si + 2H2.
- Металлов: 4NaH + Fe3O4 = 4NaOH + 3Fe.
- Восстановление: 2NaH + 2SO2 = Na2SO4 + H2S.
- С аммиаком: NaH + NH3 = NaNH2 + H2.
- С кислотами: 2NaH + H2SO4 = Na2SO4 + 2H2.
- Со спиртами: KH + HO-R = KOR + H2.
По свойствам и природе связи промежуточное положение между ионными и ковалентными занимает гидрид магния, с формулой MgH2.
Соли и оксиды калия, кальция, меди и других щелочных и щёлочноземельных металлов образуют с гидридом кислорода (водой) ещё один вид соединений — дигидраты. Это соли серной кислоты (сульфаты), галогениды, оксиды плюс 2 присоединённых молекулы H2O. Формула алебастра — Ca5O4 плюс 2H2O, гипс — CaSO4 плюс 2H2O, в природе они не редкость.
Гидросульфид натрия, NaHS, образует не только дигидрат, NaHS плюс 2H2O, но и тригидрат, с присоединением 3H2O.
Когда связь ковалентна
Это соединения, в которых степень окисления водорода +1, как правило, газы, летучие жидкости. Их водород даёт с неметаллами, а также с германием, алюминием, бериллием, оловом, мышьяком, сурьмой — элементами 4, 5, 6 и 7 групп периодической системы. И также ковалентную связь имеют соединения водорода и бора.
Это могут быть вещества простые, бинарные, такие как метан (CH4), силан (формула SiH4). Сложные тоже имеются, с длинными цепями, многоатомные молекулы — они образуются водородом с кремнием, бором, германием.
Многие из них неустойчивы, так гидрид олова (SnH4) распадается уже при комнатной температуре, а гидрид свинца недолго существует и при отрицательных температурах. Самый простой гидрид бора не существует в природных условиях вообще.
Отличительные свойства:

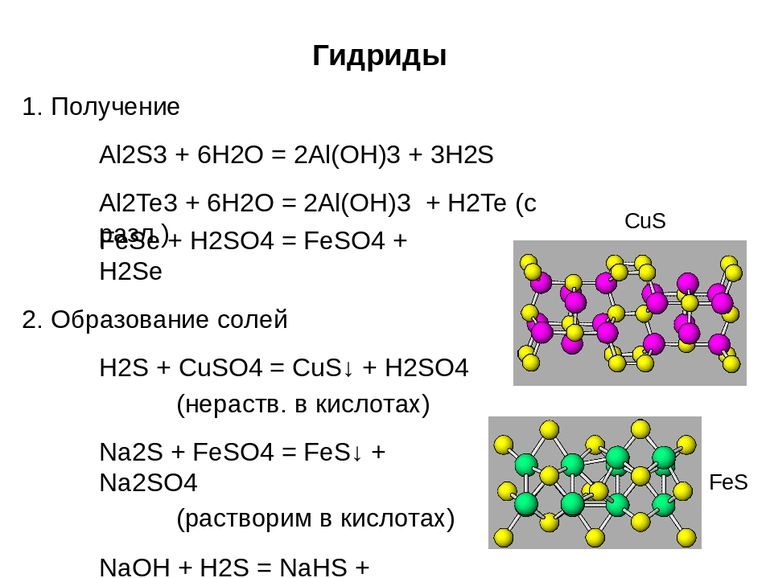
- Все сильные восстановители, степень окисления водорода +1.
- Проявляют кислотные, а также амфотерные свойства.
- Агрегатное состояние — газ или летучая жидкость, исключения тут гидрид кислорода (вода), азота, фтороводород (плавиковая кислота), те, в которых молекулы полярны и возникает водородная связь. Последние существуют, как нелетучая жидкость или в твёрдом состоянии.
- Электронодефицитные виды, получаемые с элементами главной подгруппы 3 группы, например, гидрид алюминия AlH3 или бериллия, химическая формула BeH2, очень активны и образуют многоатомные, длинные полимерные цепи, с больши́м весом. Такие полимеры — твёрдые вещества.
- При нагреве легко и практически необратимо, разлагаются на элемент и водород H2. Требуется температура от 100 до 300 градусов по Цельсию (для гидрида серы H2S — порядка 400 градусов).
- Чаще всего они имеют высокую токсичность.
- Характерна высокая химическая активность, реакционная способность.
- Получить можно непосредственным взаимодействием элементов, разложением металлических соединений водой, кислотой, восстановлением галогенидов гидридами бора, алюминия, щелочных металлов.
- Высшие гидриды германия, кремния, с общей химической формулой EnH2n+2 — это полимеры, их стабильность тем ниже, чем больше атомный вес и количество атомов элемента.
- Принадлежащие к s-подгруппе хорошо растворяются в воде и проявляют кислотные свойства. Прочие — в незначительной мере, свойства у них основные. Все хорошо растворимы в неполярных органических растворителях.
- При взаимодействии с водой (H2O), выделяется чистый водород (H2) и оксид, с общей химической формулой EO2.
Тяжёлые элементы дают соединения с небольшой устойчивостью.
За счёт водородных связей и способности к донорно-акцепторному взаимодействию, вода (H2O), плавиковая кислота (HF), аммиака (NH3), а частично HCl и H2S, хорошие растворители.
Интерметаллические соединения
Химические вещества, образованные двумя или более металлов, такие как FeTi, Ca2Ru, Mg2Ni — это интерметаллические соединения. Они хорошо поглощают водород и соединяясь с ним дают гидриды-интерметаллиды.
Содержат атомы железа, магния, меди, кальция, титана, алюминия, редкоземельные элементы. Их легко получить даже с H2 нехимическим (для технических нужд, до 2% примесей). Применяют для хранения водорода и аккумуляторных батарей.

У гидридов много областей применения. Особенно широко используют NaH. С его помощью удаляют термическую окалину с металлов, производят добавки, повышающие октановое число бензина, катализаторы полимеризации. Он необходим при производстве красителей, моющих средств, в качестве мощного восстановителя применяется в металлургии.
В органической химии комплексные водородные соединения применяют уже более 50 лет, для получения особо чистых химических элементов. В химии алкалоидов также широко используют комплексные гидриды металлов. Без них не обходится производство металлокерамики, дегазаторов, многих фармакологических средств.
Азот с водородом образует аммиак, кислород — воду, сера даёт сероводород, в природе постоянно идёт синтез подобных веществ. С миром химии человек пересекается постоянно. Поэтому знания о наиболее распространёных веществах принесут пользу каждому.
Читайте также:
