H металл или неметалл
Обновлено: 18.05.2024
Водород - первый элемент периодической системы элементов; обозначается символом H. Простое вещество водород H2 (легкий водород, дипротий) - легкий бесцветный газ без запаха и вкуса; обладает, в особенности при повышенных температурах, сильным восстановительным действием.
Природный водород содержит изотоп 1 H (протий) с примесью стабильного изотопа 2 H (дейтерий D, преобладает) и радиоактивного изотопа 3 H (тритий T, следы).
Физические свойства
| Молярная масса | H2 2,016 г/моль |
| Температура плавления, tпл. | -259,34 °C |
| Температура кипения, tкип. | -252,87 °C |
| Плотность, ρ | 0,082 г/дм 3 |
Неметалл. Бесцветный трудносжижаемый газ. Очень мало растворяется в воде, лучше - в органических растворителях. Хемосорбируется металлами (Fe, Ni, Pt, Pd).
Методы получения
Выпускающийся в стальных баллонах водород получают электролизом или из водяного газа.
Электролитический водород представляет собой газ 99,7-99,8%-ной чистоты, который в виде примеси содержит только воздух - и, в частности, кислород - в количестве, меньшем 0,1%. Этот газ пропускают при 400°С через трубку, наполненную восстановленным оксидом меди (в виде проволоки), или, по методу Мейера и Ронге, через башню с «активной медью», или при 30—50°С через колонку с восстановленным катализатором BTS фирмы BASF. Далее водород высушивают хлоридом кальция и пентаоксидом фосфора. Такой водород можно применять для большинства лабораторных целей, так как присутствие незначительного количества азота (около 0,2%) редко служит помехой.
Водород, полученный из водяного газа, содержит заметные количества примесей оксида углерода, диоксида углерода, кислорода и азота, а иногда также AsH3 и Fe(CO)5. Для поглощения диоксида углерода применяют гидроксид калия или натронную известь; AsH3 поглощают насыщенным раствором перманганата калия в присутствии избытка твердого KMnO4. Для удаления кислорода газ пропускают, как это описано выше, над нагретой медью или раскаленным докрасна платинированным асбестом, причем одновременно происходит термическое разложение Fe(CO)5. Оксид углерода удаляется при пропускании газа через восстановленный BTS-катализатор, а также путем вымораживания жидким азотом. Вообще для получения очень чистого водорода следует по возможности исходить из электролитического водорода.
- Способ 1. Нагревание палладия, насыщенного водородом (см. ниже);
- Способ 2. Диффузия через палладий или сплав палладия с серебром (см. ниже);
- Способ 3. Диффузия через никель (см. ниже);
- Способ 4. Разложение гидрида урана(III);
- Способ 5. Разложение гидрида титана;
- Способ 6. Электролиз без доступа воздуха.
Нагревание палладия, насыщенного водородом
Губку палладия, полученную путем восстановления дихлорида палладия в растворе, тщательно промывают горячей водой и после высушивания сильно прокаливают в пламени паяльной горелки. Еще в горячем состоянии губку помещают в нагретую трубку с присоединенным к ней манометром и медленно охлаждают в вакууме. Затем при комнатной температуре через трубку пропускают поток тщательно очищенного и высушенного водорода. Поглощение палладием водорода сопровождается слабым раскаливанием. Путем последующего нагревания до 200°C поглощенный водород можно снова выделить, причем при слабом отсасывании ею насосом получается равномерный поток очень чистого газа. Количество выделившегося водорода составляет при нормальных условиях около 100 мл/г палладия.
Диффузия через палладий или сплав палладия с серебром
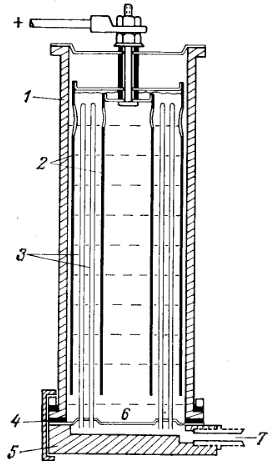
Рис. Разрез электролизера для получения водорода высокой чистоты путем электролиза поды с последующей диффузией через сплав палладий-серебро.
1 - стеклянный цилиндр (диаметр 10 см);
2 - концентрические платиновые аноды;
3 - диффузионные трубки из сплава палладий-серебро (100 штук), нижние концы которых закреплены путем припайки золотом к платиновой пластине 4;
5 - тефлоновое уплотнение;
6 - основание в виде стальной плиты;
7 - трубка для отвода водорода высокой чистоты.
Метод диффузии при повышенной температуре через металлический палладий или его сплавы с серебром в основном используется в технике для непрерывного получения больших количеств очень чистого водорода. Получение водорода в лабораторных условиях удобно осуществлять в приборе для электролиза и диффузии, устройство которого показано на рис. Прибор заполняется разбавленной серной кислотой и работает при температуре 70°С и плотности тока 2 А/см 2 . Между двумя анодами из платины находятся 100 трубок из сплава палладия с серебром (25% Ag), служащие катодами. Наружный диаметр трубок равен 1,6 мм при толщине стенок 7,6·10 -2 мм. Прибор работает на постоянном токе (выпрямитель) и дает 2 л водорода в минуту при содержании примесей менее 1 млн -1 . Прибор прост в эксплуатации, поскольку не требует дополнительного подогрева, и для его заправки необходима только дистиллированная вода.
Диффузия через никель
Очистку поступающего в продажу водорода проводят в приборе, схема/ которого показана на рис. 98. Прибор позволяет получить поток очень чистого водорода при атмосферном давлении. Пять цельнотянутых никелевых трубок диаметром 2 мм, с толщиной стенок 0,1 мм и длиной 5 м, изогнутых в виде спиралей, одним концом впаиваются в латунную головку, оканчивающуюся нормальным шлифом. Для того чтобы трубки было легче вставлять в головку, их в течение 2 ч нагревают до 1000°С в атмосфере водорода, после чего их можно легко гнуть руками. Другие концы трубок запаивают наглухо. Никелевые спирали помещают в кварцевую трубку диаметром 35 мм и длиной 1 м. Латунные головки приклеивают на пиценне.
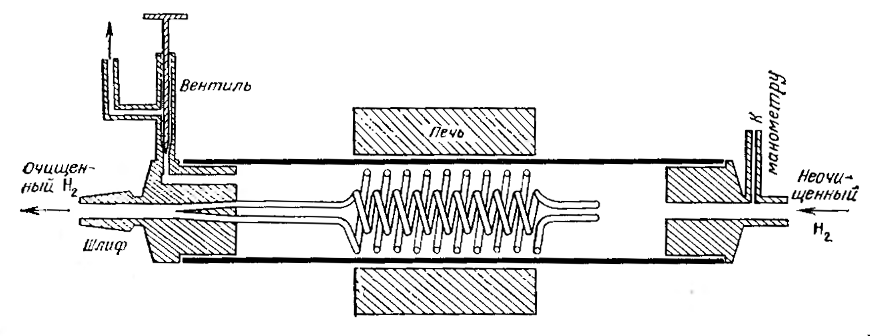
В головке с нормальным шлифом имеется игольчатый вентиль, служащий для тонкой регулировки избыточного давления и выжигания примесей, накапливающихся в кварцевой трубке. В головке на другом конце кварцевой трубки подсоединен ртутный манометр. Нагревание кварцевой трубки производят только в ее центре так, чтобы места припаивания никелевых трубок не нагревались. В зависимости от режима работы прибора его производительность (мл/мин) изменяется следующим образом:
| Температура, °C | Избыточное давление, мм рт. ст. | |||
| 15 | 20 | 25 | 30 | |
| 750 | 20 | 27 | 34 | 41 |
| 815 | 27 | 36 | 43 | 52 |
| 860 | 34 | 45 | 55 | 68 |
| 900 | 41 | 54 | 68 | 84 |
Скорость подачи газа пропорциональна величине избыточного давления, тогда как зависимость от температуры не является линейной. Путем изменения давления скорость подачи может быть практически моментально отрегулирована до нужного уровня. При наличии хорошего вентиля на баллоне с водородом аппаратура работает без сбоев. Продолжительность непрерывной работы составляет не менее 250 ч. Перед каждым новым опытом следует убедиться в герметичности аппаратуры.
Химические свойства
Сильный восстановитель. При повышенных температурах, реагирует с металлами, неметаллами, оксидами металлов. Особенно высока восстановительная способность у атомного водорода H 0 . образующегося при термическом разложении молекулярного водорода H 2 или в результате реакций непосредственно в зоне проведения восстановительного процесса.
кстати, а водород это метал или неметал (в метастабильном-твердом- состоянии)?
В обычном твердом состоянии водород - это неметалл, поскольку электричества не проводит.
Однако есть сведения о том, что при ОЧЕНЬ высоком давлении его можно все-таки перевести в проводящее состояние, т. е. сделать "металлом"
За последние четверть века после изобретения алмазных наковален исследователи системно изучили свойства твердого водорода вплоть до
давления 2 млн. атм. (последний рекорд 3.75 млн. атм. ) Теперь ученые знают, что даже при этих давлениях существуют, по крайней мере, три фазы металлического водорода, причём каждая из них совершает переход диэлектрик - металл при своём значении давления. Одна при 1.6 млн. атм. , когда другие фазы ещё остаются диэлектриками. Последние теоретические данные позволяют надеяться, что весь водород перейдёт в металлическую фазу при 4 млн. атм. ( при 0 гр. К)
Опять же остается открытым вопрос, распадается ли при этом водород на атомы или остается в молекулярном состоянии. Уже известно, что «коллеги» водорода по свойствам бром и йод становятся проводниками при высоком давлении именно в процессе плавления, то есть в атомарном виде. С другой стороны, есть данные, что в статических экспериментах при достигнутых давлениях водород находится в основном в виде молекул.
Гораздо более продуктивный способ получения высоких давлений взрывной метод, когда экспериментаторы ударяют по ячейке с образцом металлическими пластинами или струей газа, ускоренными до гиперзвуковых скоростей. Сейчас существуют установки однократного ударного сжатия, в которых водород можно сжимать до 10 млн. атм.
В момент удара, когда давление достигает миллионов атмосфер, водород неизбежно нагревается до тысяч градусов Кельвина и переходит в жидкое состояние. Ученые пытаются придумать, как уменьшить температуры в эксперименте, но пока это все равно тысячи градусов. Более того, через микросекунды, когда заканчивается действие ударной волны, водород опять становится газом, поэтому померить что-то очень сложно.
Но, решая проблему атомной бомбы, ученые научились с этим справляться. В динамических экспериментах измеряют плотность водорода, просвечивая образец рентгеновским излучением, либо судят о том, что происходит, по сигналам от оптических и электрических датчиков. Таким образом давление в таких опытах величина расчетная.
Последний рекорд 15 млн. атм. Больших давлений удалось достичь ученым из Ливерморской национальной лаборатории (США) , а в России исследователям из Всесоюзного научно-исследовательского института экспериментальной физики (г. Саров) и Института проблем химической физики РАН (г. Черноголовка) .
Измеряя сопротивление в динамических экспериментах, исследователи видели, что водород становится проводником, с проводимостью почти как у жидких металлов. Но эта проводимость все-таки слабо зависела от температуры, что свидетельствует, что водород еще не металл. Ученые характеризуют состояние водорода, которое они наблюдают в динамических экспериментах, как «неупорядоченная проводящая среда» (неупорядоченная так как температуры слишком высоки) или «плотная низкотемпературная неидеальная плазма» , а появляющийся эффект проводимости «ионизация давлением»
При сверхвысоких давлениях - металл (там есть свои вопросы в эксперименте, но теоретически должен быть металл)
При не очень высоких - молекулярный кристалл H2 и потому изолятор
Метастабильных (при нормальном давлении) фаз экспериментально не обнаружено.

Сплошные линии - металлические фазы в разных вариантах ТЕОРИИ
пунктирная - молекулярный водород (эксперимент)
Классификация неорганических веществ
Химические вещества можно разделить на две группы: простые и сложные.
Простые вещества состоят из атомов одного элемента (О2, P4).
Сложные вещества состоят из атомов двух и более элементов (CaO, H3PO4).
Простые вещества можно разделить на металлы и неметаллы.
Металлы – это простые вещества, в которых атомы соединены между собой металлической химической связью. Металлы стремятся отдавать электроны и характеризуются металлическими свойствами (металлический блеск, высокая электро- и теплопроводность, пластичность и др.).
Неметаллы – это простые вещества, в которых атомы соединены ковалентными (или межмолекулярными) связями. Неметаллы стремятся принимать или притягивать электроны. Неметаллические свойства – это способность принимать или притягивать электроны.
Все элементы в Периодической системе химических элементов (ПСХЭ) расположены либо в главной подгруппе, либо в побочной. В различных формах короткопериодной ПСХЭ главные и побочные подгруппы расположены по-разному. Есть простой способ, который позволит вам быстро и надежно определять, к какой подгруппе относится элемент. Дело в том, что все элементы второго периода расположены в главной подгруппе. Те элементы, которые расположены в ячейке точно под элементами второго периода (справа или слева), относятся к главной подгруппе. Остальные — к побочной.
Например , в таблице Менделеева, которая используется на ЕГЭ по химии, элемент номер 31, галлий, расположен в ячейке справа, точно под соответствующим ему элементом второго периода, бором. Следовательно, галлий относится к главной подгруппе. А вот скандий, элемент номер 21, расположен в ячейке слева. Следовательно, скандий относится к побочной подгруппе.
Неметаллы расположены в главных подгруппах, в правом верхнем угле ПСХЭ. К металлам относятся все элементы побочных подгрупп и элементы главных подгрупп, расположенные в левой нижней части ПСХЭ. Разделяют металлы и неметаллы обычно, проводя условную линию от бериллия до астата. На рисунке показано точное разделение на металлы и неметаллы. Закрашены цветом неметаллы.

Основные классы сложных веществ — это оксиды, гидроксиды, соли.

Оксиды — это сложные вещества, которые состоят из атомов двух элементов, один из которых кислород, имеющий степень окисления -2.
В зависимости от второго элемента оксиды проявляют разные химические свойства. Некоторым оксидам соответствуют гидроксиды (солеобразующие оксиды), а некоторым нет (несолеобразующие).
Солеобразующие оксиды делят на основные, амфотерные и кислотные.
Основные оксиды — это оксиды, которые проявляют характерные основные свойства. К ним относят оксиды, образованные атомами металлов со степенью окисления +1 и +2 . Например, оксид лития Li2O, оксид железа (II) FeO.
Амфотерные оксиды — это оксиды, которые проявляют и основные, и кислотные свойства. Это оксиды металлов со степенью окисления +3 и +4 , а также четыре оксида со степенью окисления +2: ZnO, PbO, SnO и BeO .
Несолеобразующие оксиды не проявляют характерных основных или кислотных свойств, им не соответствуют гидроксиды. К несолеобразующим относят четыре оксида: CO, NO, N2O и SiO .
Встречаются и оксиды, похожие на соли, т.е. солеобразные (двойные).
Двойные оксиды — это некоторые оксиды, образованные элементом с разными степенями окисления. Например , магнетит (магнитный железняк) FeO·Fe2O3.
Алгоритм определения типа оксида: сначала определяем, какой элемент образует оксид – металл или неметалл . Если это металл, то определяем степень окисления, затем определяем тип оксида. Если это неметалл, то оксид кислотный (если это не исключение).
Гидроксиды — это сложные вещества, в составе которых есть группа Э-O-H. К гидроксидам относятся основания, амфотерные гидроксиды, и кислородсодержащие кислоты.
Солеобразующим оксидам соответствуют гидроксиды:
основному оксиду соответствует гидроксид основание ,
кислотному оксиду соответствует гидроксид кислота ,
амфотерному оксиду соответствует амфотерный гидроксид .
Например , оксид хрома (II) CrO — основный, ему соответствует гидроксид основание. Формулу гидроксида легко получить, просто добавив к металлу гидроксидную группу OH: Cr(OH)2.
Оксид хрома (VI) — кислотный, ему соответствует гидроксид кислота H2CrO4, и кислотный остаток хромат-ион CrO4 2- .
Если все индексы кратны 2, то мы делим все индексы на 2.
Например : N2O5 + H2O → H2N2O6, делим на 2, получаем HNO3. Так получаем мета-формулу кислоты. Если мы добавим еще одну молекулу воды, то получим орто-формулу кислоты.
Например : оксид P2O5, мета-форма: HPO3. Добавляем воду, орто-форма: H3PO4. Орто-форма устойчива у фосфора и мышьяка.
Оксид хрома (III) — Cr2O3 — амфотерный, ему соответствует амфотерный гидроксид, который может выступать и как основание, и как кислота: Cr(OH)3 = HCrO2, кислотный остаток хромит: CrO2 — .
Взаимосвязь оксидов и гидроксидов:
Основания (основные гидроксиды) — это сложные вещества, которые при диссоциации в водных растворах в качестве анионов (отрицательных ионов) образуют только гидроксид-ионы OH — .
Основания можно разделить на растворимые в воде ( щелочи ), нерастворимые в воде, и разлагающиеся в воде .

К разлагающимся в воде (неустойчивым) основаниям относят гидроксид аммония, гидроксид серебра (I), гидроксид меди (I). В водном растворе такие соединения практически необратимо распадаются:
2AgOH → Ag2O + H2O
2CuOH → Cu2O + H2O
Основания с одной группой ОН – однокислотные (например, NaOH ) , с двумя – двухкислотные (Ca(OH)2) и с тремя – трехкислотные (Fe(OH)3) .

Кислоты – это сложные вещества, которые при диссоциации в водных растворах образуют в качестве катионов только ионы гидроксония H3O + (H + ). Кислоты состоят из водорода H + и кислотного остатка.
По числу атомов водорода, которые можно заместить на металлы: одноосновные (HNO3), двухосновные (H2SO4), трехосновные (H3PO4) и т.д.

По содержанию атомов кислорода кислоты бывают бескислородные ( например , соляная кислота HCl) и кислородсодержащие ( например , серная кислота H2SO4).

Кислоты также можно разделить на сильные и слабые.
Сильные кислоты. К ним относятся:
- Бескислородные кислоты: HCl, HBr, HI . Остальные бескислородные кислоты, как правило, слабые.
- Некоторые высшие кислородсодержащие кислоты: H2SO4, HNO3, HClO4 и др.
Слабые кислоты . К ним относятся:
Определить, сильная кислота перед вами, или слабая, позволяет простой прием. Мы вычитаем из числа атомов O в кислоте число атомов H. Если получаем число 2 или 3, то кислота сильная. Если 1 или 0 — то кислота слабая.
Например : HClO: 1-1 = 0, следовательно, кислота слабая.
Соли – сложные вещества, состоящие из катиона металла (или металлоподобных катионов, например, иона аммония NH4 + ) и аниона кислотного остатка. Также солями называют вещества, которые могут быть получены при взаимодействии кислот и оснований с выделением воды.
Если рассматривать соли, как продукты взаимодействия кислоты и основания, то соли делят на средние , кислые и основные .
Средние соли – продукты полного замещения катионов водорода в кислоте на катионы металла ( например , Na2CO3, K3PO4).
Кислые соли – продукты неполного замещения катионов водорода в кислоте на катионы металлов ( например , NaHCO3, K2HPO4).
Основные соли – продукты неполного замещения гидроксогрупп основания на анионы кислотных остатков кислоты ( например , малахит (CuOH)2CO3).
По числу катионов и анионов соли разделяют на:
Простые соли – состоящие из катиона одного типа и аниона одного типа ( например , хлорид кальция CaCl2).
Двойные соли – это соли, состоящие из двух или более разных катионов и аниона одного типа ( например , алюмокалиевые квасцы – KAl(SO4)2).
Смешанные соли – это соли, состоящие из катиона одного типа и двух или более анионов разного типа ( например , хлорид-гипохлорит кальция Ca(OCl)Cl).
По структурным особенностям выделяют также гидратные соли и комплексные соли.
Гидратные соли (кристаллогидраты) – это такие соли, в состав которых входят молекулы кристаллизационной воды ( например , декагидрат сульфата натрия Na2SO4·10 H2O).
Комплексные соли – это соли, содержащие комплексный катион или комплексный анион (K3[Fe(CN)6], [Cu(NH3)4]Cl2).

Помимо основных классов неорганических соединений, существуют и другие.
Например , бинарные соединения элементов с водородом.
Водородные соединения – это сложные вещества, состоящие из двух элементов, один из которых водород. Водород образует солеобразные гидриды и летучие водородные соединения.
Солеобразные гидриды ЭНх – это соединения металлов IA, IIA групп и алюминия с водородом. Степень окисления водорода равна -1. Например , гидрид натрия NaH.
Летучие водородные соединения НхЭ – это соединения неметаллов с водородом, в которых степень окисления водорода равна +1. Например , аммиак NH3, фосфин PH3.

Тренировочный тест «Классификация неорганических веществ» 10 вопросов, при каждом прохождении новые.
Металлы и неметаллы
Наш мир наполняют различные простые вещества – металлы или неметаллы. При существовании 120 химических элементов, Вселенную наполняют более 400 простых веществ. Этот парадокс связан с понятием аллотропии – явлением образования одним химическим элементом двух и более простых веществ. Например, атом кислорода может формировать молекулярный кислород О2 и озон О3.
План урока:
Физические свойства металлов
Металлы – химические элементы, атомы которых в процессе реакции стремятся отдавать электроны. Они обладают металлической кристаллической решеткой и общими физическими свойствами. На данный момент известно более 87 металлов.
Для металлов характерен ряд свойств:
- твердость (кроме ртути, которая представляет собой жидкость);
- металлический блеск;
- проводимость электрического тока и тепла;
- пластичность.
Металлы при ударах не разрушаются, а меняют форму. С этой особенностью связано то, что из них производят проволоку, металлические листы и др. Развитие бронзового и железного века связано с производством товаров из металлов.
Физические свойства неметаллов
Неметаллы – химические элементы, атомы которых стремятся принять чужие электроны. Для них характерны атомные и молекулярные кристаллические решетки. Для атомов неметаллов не характерны общие физические свойства. На данный момент существует 22 неметалла.
Для неметаллов характерен ряд свойств:
- хрупкость (неметаллы нельзя ковать);
- отсутствие блеска;
- непроводимость электрического тока и тепла.
Расположение металлов и неметаллов в периодической таблице Д.И. Менделеева
Определить, является простое вещество металлом или неметаллом, можно с помощью периодической таблицы Менделеева. Металлы располагаются ниже диагонали «водород-бор- кремний-мышьяк-теллур-астат», а неметаллы выше.
Красные ячейки – неметаллы, синие – металлы
Элементы, расположенные вблизи диагонали, обладают смешанными свойствами: проявляют как металлические, так и неметаллические свойства. Они называются полуметаллами.
Красные ячейки – полуметаллы
Полуметаллы имеют ковалентную кристаллическую решетку при наличии металлической проводимости (электропроводности). Валентных электронов у них либо недостаточно для образования полноценной ковалентной связи, либо они не удерживаются достаточно прочно из-за больших размеров атома. Поэтому связь в ковалентных кристаллах этих элементов имеет частично металлический характер.
Закономерности в таблице Д.И. Менделеева
Каждый атом состоит из протонов, нейтронов и электронов. Протоны и нейтроны находятся в ядре, который несет положительный заряд. Вокруг ядра движутся отрицательно заряженные электроны. Атомный номер указывает на количество протонов.
Чем больше заряд ядра, тем сильнее к нему притягиваются электроны. Т.о., атому сложнее отдавать электроны. Поэтому в периоде слева направо, с увеличением порядкового номера металлические свойства ослабевают, а неметаллические – усиливаются.
Неметаллы стремятся принять электроны от других атомов. Период в таблице указывает на количество электронных уровней. По мере увеличения числа орбиталей электроны отдаляются от ядра и атому сложнее удерживать электроны на последних уровнях. Т.о., в группе сверху вниз количество орбиталей возрастает, поэтому металлические свойства усиливаются, а неметаллические – уменьшаются.
Способы получения металлов
Большую часть металлов получают из оксидов при нагревании.
Металлы, имеющие на внешнем уровне один-два электрона, получают с помощью электролиза расплавов.
Химические свойства металлов
Все металлы проявляют восстановительные свойства. Легкость в отдачи внешнего электрона применяется в фотоэлементах. Степень активности определяется рядом активности. У самых активных на внешнем уровне располагается по одному электрону.
Общие химические свойства металлов выражаются в реакциях со следующими соединениями.
Активные металлы реагируют с галогенами и кислородом. С азотом взаимодействуют только литий, кальций и магний. Большинство металлов при взаимодействии с кислородом образуют оксиды, а наиболее активные металлы – пероксиды (N2O2).
2 Ca + MnO2 → 2 CaO + Mn(нагревание)
Водород в кислотах вытесняют только те металлы, которые в ряду напряжений стоят до водорода.
Более активные металлы вытесняют из соединений менее активные.
- Химические свойства щелочных и щелочно-земельных металлов (реакции с водой)
2 Na + 2 H2O → 2 NaOH + H2
Способы получения неметаллов
Неметаллы синтезируют из природных соединений с помощью электролиза.
2 KCl → 2 K + Cl2
Также неметаллы получают в результате окислительно-восстановительных реакций.
SiO2 + 2 Mg → 2 MgO + Si
Химические свойства неметаллов
Неметаллы проявляют окислительные свойства. Самый активный неметалл – фтор. Он бурно реагирует со всеми веществами, а некоторые реакции сопровождаются горением и взрывом. В атмосфере фтора горят даже вода и платина. Фтор окисляет кислород и образует фторид кислорода OF2.
Неметаллы вступают в реакции со следующими веществами.
3 F + 2 Al → 2 AlF3 (нагревание)
S + Fe →FeS (нагревание)
Меньшей активностью обладают такие неметаллы как бор, графит, алмаз. Они могут проявлять восстановительные свойства.
2 C + MnO2 → Mn + 2 CO
Коррозия металла
Коррозия – это процесс разрушения металлов или металлических конструкций под действием кислорода, воды и вредных примесей. Не все металлы подвергаются коррозии. Их стойкость зависит от ряда факторов.
- На благородных металлах не образуется коррозия.
- На поверхности алюминия, титана, цинке, хрома и никеля есть оксидная пленка, которая предотвращает процессы коррозии.
Различают несколько видов коррозии – химическую и электрохимическую.
Химическая коррозия
Химическая коррозия сопровождается химическими реакциями. Она образуется под действием газов.
Электрохимическая коррозия
Электрохимическая коррозия – процесс разрушения металлов или металлических конструкций, который сопровождается электрохимическими реакциями. В большинстве металлов находятся примеси. В процессе коррозии электродами могут служить не только металлы, но и его примеси.
Например, в железе могут находиться примеси олова. В этом случае на аноде электроны переносятся от олова к железу и металлы растворяются, т.е. железо подвергаются коррозии. На катоде восстанавливается водород из воды или растворенного кислорода. Электрохимическая коррозия может сопровождаться следующими процессами.
Анод: Fe 2+ - 2e → Fe 0
Катод: 2H + + 2e → H2
Способы защиты от коррозии
В промышленности популярны различные методы защиты металлов от коррозии.
Покрытия защищают поверхности от действия окислителей. Ими служат различные вещества:
- покрытие менее активным металлом (железо покрывают оловом);
- краски, лаки, смазки.
- Создание специальных сплавов
Физические свойства сплавов и чистых металлов отличаются. Поэтому для повышения стойкости в сплав необходимо добавить дополнительные металлы.
Биологическая роль металлов и неметаллов
В организмах содержится множество различных металлов и неметаллов. Различных химических элементов в организме может не хватать, поэтому приходится потреблять их извне.Химические элементы можно разделить на две большие группы – макроэлементы и микроэлементы.
К макроэлементам относятся вещества, содержание которых в организме превышает 0,005 %. Эта группа включает водород, углерод, кислород, азот, натрий, магний, фосфор, сера, хлор, калий, кальций.Микроэлементы – элементы, содержание которых не превышает 0,005%. К ним относятся железо, медь, селен, йод, хром, цинк, фтор, марганец, кобальт, молибден, кремний, бром, ванадий, бор. Каждый макро- и микроэлемент в организме выполняет определенную функцию.
Применение металлов и неметаллов
В синтезе химических препаратов и лекарств применяются чистые металлы и неметаллы. В органической химии металлы используются в качестве катализаторов, а также при получении металлорганических соединений. Неметаллы служат исходным сырьем для получения чистых кислот и других химических соединений.
Читайте также:
