Из чего делают железо и металл
Обновлено: 04.10.2024
Железо и сталь — важнейшие металлы. Сталь получают из железа. Из нее делают множество предметов — от нефтяных вышек до канцелярских скрепок. Наряду с 80 чистыми металлами людям известно немало сплавов — смесей металлов, качества которых отличаются от качеств чистых металлов. Башенные краны, мосты, другие сооружения делают из стали, содержащей до 0,2% углерода. Углерод делает сталь прочнее, причем она сохраняет ковкость. Сталь покрывают краской для защиты от коррозии.
Железо и сталь
Железо — это элемент. Его добывают из руды — соединения железа с кислородом. Большая часть добытого железа идет на производство стали, сплава железа с углеродом. Наиболее распространенные железные руды: магнетит(вверху) и гематит(внизу). Железо добывается из руды в доменных печах. Этот процесс называется плавкой. В печи через слой железной руды, известняка и кокса продувают очень горячий воздух. Кокс представляет собой почти чистый углерод, его получают нагреванием угля. Углерод кокса соединяется с кислородом, образуя моноксид углерода, который затем «вытягивает» кислород из руды, оставляя чистое железо, и образует диоксид углерода. Это пример реакций восстановления. Руда, кокс и известняк поступают в печь. Известняк реагирует с имеющимися в руде примесями, образуя шлак. Внутри печи раскаленный воздух реагирует с углеродом. Образуется моноксид углерода. При этом температура в печи повышается до 2000°С. Затем оксид углерода реагирует с кислородом руды, восстанавливая ее до железа. Расплавленный шлак вытекает из нижней части печи. Его используют в строительстве дорог. В конце расплавленное железо выводится наружу. Доменная печь непрерывно функционирует 10 лет, пока её стенки не начнут разрушаться. Высота доменной печи 30 метров, толщина её стен 3 метра.
Железо, получаемое из руды, содержит углерод (около 4%) и другие примеси, в частности серу. Примеси делают железо хрупким, поэтому большую его часть перерабатывают в сталь. При этом из железа удаляются примеси. В стальных скрепках около 0,08% углерода. Инструменты делают из стали, содержащей хром, ванадий и до 1% углерода. Сталь получают при воздействии на расплавленное железо кислорода. Часто в железо добавляют небольшое количество стального лома. Кислород реагирует с углеродом, содержащимся в железе, при этом образуется моноксид углерода, используемый как топливо. После очистки в стали остается не более 0.04% углерода; его количество зависит от марки стали. Сталь получают также путем переплавки стального лома в дуговой электропечи. Для получения стали расплавленное железо и стальной лом заливают в печь, называемую конвертером. В конвертер под высоким давлением закачивается почти чистый кислород. При его реакции с углеродом получается моноксид углерода (см. так же статью «Химические реакции«). Другой способ получения стали — переплавка стального лома в дуговой электропечи. Мощный электрический ток (см. статью «Электричество«) расплавляет лом. Расплавленный шлак вытекает из нижней части печи. Его используют в строительстве дорог.
Сплавы
Сплавом называется смесь двух или более металлов или металла и иного вещества. Так, латунь — это сплав меди и цинка. Латунь прочнее меди, ее легко обрабатывать, и она не подвержена коррозии. В чистых металлах атомы «упакованы» в тесные ряды (рис. слева). Ряды могут скользить относительно друг друга, что делает металл мягким. При резких сдвигах рядов металл ломается. В сплаве другие атомы укрепляют металл (см. рис. справа), т.к. сдвиг рядов уже невозможен. Поэтому сплавы прочнее чистых металлов.
Многие металлы сами по себе чересчур мягкие, чтобы их можно было использовать, зато их сплавы могут выдерживать большое давление и высокие температуры (см. статью «Тепло и температура«). Сталь — это сплав железа и углерода, неметалла. Добавляя небольшие количества других металлов, можно получить разновидности стали. Ножи и вилки делают из нержавеющей стали — сплава стали, хрома и никеля. Сплавы стали с марганцем чрезвычайно прочны и используются в промышленности для изготовления режущих инструментов. Алюминиево-магниевые сплавы легки, прочны и не подвержены коррозии. Из них делают велосипеды и самолеты (см. статью «Полет«).
Важнейшие металлы и сплавы
Алюминий. Очень легкий серебристо-белый металл, не подверженный коррозии. Его получают из бокситов путем электролиза. Из алюминия делают электропровода, самолеты, корабли (см. статью «Плавучесть«), автомобили, банки для напитков, фольгу для приготовления пищи. Алюминиевые банки для напитков очень легкие и прочные.
Латунь. Ковкий сплав меди и цинка. Из латуни делают украшения, орнаменты, музыкальные инструменты, винты, кнопки для одежды.
Бронза. Известный с древнейших времен ковкий, не подверженный коррозии сплав меди и олова.
Хром. Твердый серый металл. Используется в производстве нержавеющей стали. Хромом покрывают металлические изделия в защитных целях и для придания им зеркального блеска.
Медь. Ковкий красноватый металл. Из меди делают электропровода, резервуары для горячей воды. Медь входит в состав латуни, бронзы, мельхиора.
Мельхиор. Сплав меди и никеля. Из него делают почти все «серебряные» монеты.
Золото. Мягкий неактивный ярко-желтый металл. Используется в электронике и в ювелирном деле.
Железо. Ковкий серебристо-белый ферромагнетик. Добывается в основном из руды в доменных печах. Используется в инженерных конструкциях, а также в производстве стали и сплавов. В нашей крови тоже есть железо.
Свинец. Тяжелый ковкий ядовитый синевато-белый металл. Добывается из минерала галенита. Из свинца делают электрические батареи, крыши и экраны, защищающие от рентгеновских лучей.
Ртуть. Тяжелый серебристо-белый ядовитый жидкий металл. Используется в термометрах, входит в состав зубной амальгамы и взрывчатых веществ.
Платина. Ковкий серебристо-белый неактивный металл. Используется в качестве катализатора, а также в электронике и в производстве ювелирных изделий. Платина не вступает в реакции. Из нее делают украшения.
Плутоний. Радиоактивный металл. Образуется в ядерных реакторах при бомбардировке урана и используется в производстве ядерного оружия (см. статью «Ядерная энергия и радиоактивность«).
Калий. Легкий серебристый металл. Очень химически активен. Калиевые соединения входят в состав удобрений.
Припой. Сплав олова и свинца. Плавится при сравнительно низкой температуре. Используется для спайки проводов в электронике.
Сталь. Сплав железа с углеродом. Широко применяется в промышленности. Нержавеющая сталь — сплав стали с хромом — не подвержена коррозии и используется в авиакосмической индустрии (см. статью «Ракеты и космические аппараты«).
Титан. Прочный белый ковкий металл, не подверженный коррозии. Из титановых сплавов делают космические аппараты, самолеты, велосипеды.
Вольфрам. Твердый серовато-белый металл. Из него изготавливают нити ламп накаливания и детали электронных приборов. Из стали с Нить вольфрамом делают накаливания режущие инструменты.
Уран. Серебристо-белый радиоактивный металл, источник ядерной энергии. Применяется при создании ядерного оружия.
Ванадий. Твердый ядовитый белый металл. Придает прочность стальным сплавам. Используется как катализатор при производстве серной кислоты.
Переработка металлов
Переработка — это повторное использование сырья, способ сохранить природные ресурсы. Металлы легко поддаются переработке, т.к. их можно переплавить и получить металл такого же качества, как и тот, что получается непосредственно из руды. Переплавлять сталь и алюминий несложно и выгодно. Медь, олово, свинец также подвергаются переплавке. Железные и стальные предметы можно извлечь из кучи отходов при помощи сильного магнита. Большую часть стали для переработки добывают из старых автомобилей и станков, но часть ее получают из фабричных металлических опилок и даже бытовых отходов. Стальной лом смешивают с расплавленным железом и получают новую сталь.
Алюминий — не ферромагнетик, но алюминиевые отходы можно отделить от железного лома при помощи электромагнита. Больше половины банок для напитков делают из алюминия, полученного путем переработки. Чтобы узнать, сделана банка из стали или алюминия, возьми магнит. К стальной банке он прилипнет, а к алюминиевой — нет. Переработка металлолома требует значительно меньше энергии, чем получение металла из руды, и отходов при переработке меньше. Теоретически металл можно перерабатывать сколько угодно раз. Для переработки алюминиевых банок необходимо в 20 раз меньше энергии, чем для производства нового алюминия.
Выплавка стали: технология, способы, сырье

Железную руду получают привычным способом: открытой или подземной добычей и последующей транспортировкой для первоначальной подготовки, где материал измельчается, промывается и перерабатывается.
Руду засыпают в доменную печь и подвергают струйной обработке горячим воздухом и теплом, который превращает ее в расплавленное железо. Далее оно извлекается из нижней части печи в формы, известные как свиньи, где происходит остывание для получения чугуна. Он превращается в кованое железо или перерабатывается в сталь несколькими способами.

Что такое сталь?
Вначале было железо. Оно является одним из наиболее распространенных металлов в земной коре. Его можно встретить почти везде, в сочетании со многими другими элементами, в виде руды. В Европе начало работы с железом датируется 1700 г. до н.э.
В 1786 году французские ученые Бертолле, Мондж и Вандермонде точно определили, что разница между железом, чугуном и сталью обусловлена различным содержанием углерода. Тем не менее сталь, изготовленная из железа, быстро стала самым важным металлом промышленной революции. В начале XX века мировое производство стали составило 28 миллионов тонн - это в шесть раз больше, чем в 1880 году. К началу Первой мировой войны ее производство составляло 85 миллионов тонн. В течение нескольких десятилетий она практически заменила железо.
Содержание углерода влияет на характеристики металла. Существует два основных вида стали: легированная и нелегированная. Сплав стали относится к химическим элементам, отличным от углерода, добавленного к железу. Таким образом, для создания нержавеющей стали используется сплав 17 % хрома и 8 % никеля.
В настоящее время существует более 3000 каталогизированных марок (химических составов), не считая тех, которые созданы для удовлетворения индивидуальных потребностей. Все они способствуют превращению стали в наиболее подходящий материал для решения задач будущего.

Сырье для выплавки стали: первичное и вторичное
Выплавка данного металла с использованием многих компонентов – самый распространенный способ добычи. Шихтовые материалы могут быть как первично используемые, так и вторично. Основной состав шихты, как правило, составляет 55 % чугуна и 45 % оставшегося металлолома. Ферросплавы, переделанный чугун и технически чистые металлы используются как основной элемент сплава, ко вторичным, как правило, относят все виды черного металла.
Железная руда является самым важным и основным сырьем в черной металлургии. Для производства тонны чугуна требуется около 1,5 тонны этого материала. Для производства одной тонны чугуна используется около 450 тонн кокса. Многие металлургические заводы применяют даже древесный уголь.
Вода - важное сырье для черной металлургии. Она в основном используется для закалки кокса, охлаждения доменных печей, производства пара в дверях угольной печи, работы гидравлического оборудования и удаления сточных вод. Для производства тонны стали требуется около 4 тонн воздуха. Флюс используется в доменной печи для извлечения загрязнений из плавильной руды. Известняк и доломит объединяются с экстрагированными примесями с образованием шлака.
Как дутьевые, так и стальные печи, облицованы огнеупорами. Они используются для облицовочных печей, предназначенных для плавки железной руды. Диоксид кремния или песок используется для формования. Для производства стали различных марок применяют цветные металлы: алюминий, хром, кобальт, медь, свинец, марганец, молибден, никель, олово, вольфрам, цинк, ванадий и др. Среди всех этих ферросплавов марганец широко используется в выплавке стали.
Железные отходы, полученные из демонтированных конструкций заводов, механизмов, старых транспортных средств и т. д., перерабатываются и широко используются в этой отрасли.

Чугун для стали
Выплавку стали с использованием чугуна производят гораздо чаще, чем с другими материалами. Чугун - это термин, который обычно относится к серому железу, однако он также идентифицирован с большой группой ферросплавов. Углерод составляет примерно от 2,1 до 4 мас.%, тогда как кремний составляет обычно от 1 до 3 мас.% в сплаве.
Выплавка чугуна и стали проходит при температуре плавления между 1150 и 1200 градусов, что примерно на 300 градусов ниже, чем температура плавления чистого железа. Чугун также демонстрирует хорошую текучесть, отличную обрабатываемость, устойчивость к деформации, окислению и отливке.
Сталь также является сплавом железа с переменным содержанием углерода. Содержание углерода в стали составляет от 0,2 до 2,1 мас.%, И это наиболее экономичный легирующий материал для железа. Выплавка стали из чугуна полезна для различных инженерных и конструкционных целей.

Железная руда для стали
Процесс выплавки стали начинается с переработки железной руды. Породу, содержащую железную руду, измельчают. Руду добывают с использованием магнитных роликов. Мелкозернистая железная руда перерабатывается в крупнозернистые комки для использования в доменной печи. Уголь очищается от примесей в коксовой печи, что дает почти чистую форму углерода. Затем смесь железной руды и угля нагревают для получения расплавленного железа или чугуна, из которого производится сталь.
В основной кислородной печи расплавленная железная руда является основным сырьем и смешивается с различными количествами стального лома и сплавов для производства различных марок стали. В электродуговой печи переработанный стальной лом расплавляется непосредственно в новую сталь. Около 12% стали изготовлено из переработанного материала.

Технология выплавки
Плавление - процесс, посредством которого металл получают либо в виде элемента, либо как простое соединение из его руды путем нагревания выше температуры плавления обычно в присутствии окислителей, таких как воздух, или восстановителей, таких как кокс.
В технологии выплавки стали металл, который сочетается с кислородом, например оксидом железа, нагревается до высокой температуры, и оксид образуется в сочетании с углеродом в топливе, выходящим как монооксид углерода или диоксид углерода.
Другие примеси, все вместе называемые жилами, удаляются добавлением потока, с которым они объединяются, образуя шлак.
В современных плавках стали используется отражательная печь. Концентрированная руда и поток (обычно известняк) загружаются в верхнюю часть, а расплавленный штейн (соединение меди, железа, серы и шлака) вытягивается снизу. Вторая термообработка в конвертерной печи необходима для удаления железа из матовой поверхности.

Кислородно-конвекторный способ
Кислородно-конвертерный процесс является ведущим процессом сталеплавильного производства в мире. Мировое производство конвертерной стали в 2003 году составило 964,8 млн тонн или 63,3 % от общего производства. Производство конвертера является источником загрязнения окружающей природной среды. Основными проблемами этого являются снижение выбросов, сбросов и уменьшение отходов. Суть их заключается в использовании вторичных энергетических и материальных ресурсов.
Экзотермическое тепло генерируется реакциями окисления во время продувки.
Основной процесс выплавки стали с использованием собственных запасов:
- Расплавленный чугун (иногда называемый горячим металлом) из доменной печи выливается в большой огнеупорный футерованный контейнер, называемый ковшом.
- Металл в ковше направляется непосредственно для основного производства стали или стадии предварительной обработки.
- Высокочистый кислород под давлением 700-1000 килопаскалей вводится со сверхзвуковой скоростью на поверхность ванны железа через охлаждаемую водой фурму, которая подвешена в сосуде и удерживается в нескольких футах над ванной.
Решение о предварительной обработке зависит от качества горячего металла и требуемого конечного качества стали. Самые первые конвертеры со съемным дном, которые могут быть отсоединены и отремонтированы, все еще используются. Были изменены копья, используемые для дутья. Для предотвращения заклинивания фурмы во время продувки применялись щелевые манжеты с длинным сужающимся медным наконечником. Кончики наконечника после сгорания сжигают CO, образующийся при выдувании в CO2, и обеспечивают дополнительное тепло. Для отвода шлака используются дротики, огнеупорные шарики и шлаковые детекторы.

Кислородно-конвекторный способ: достоинства и недостатки
Не требует затрат на оборудование по очищению от газа, так как пылеобразование, т. е. испарение железа, снижено в 3 раза. За счет снижения выхода железа наблюдается рост выхода жидкой стали в 1,5 - 2,5 %. Преимуществом стало и то, что интенсивность продувки в таком способе увеличивается, что дает возможность повысить производительности конвертера на 18 %. Качество стали выше, потому что температура в зоне продувки снижена, что приводит к уменьшению образования азота.
Недостатки данного способа выплавки стали привели к снижению спроса на потребление, так как повышается уровень потребления кислорода на 7 % из-за большого расхода на сжигание топлива. Наблюдается повышенное содержание водорода в переработанном металле, из-за чего приходится некоторое время после окончания процесса вести продувку при помощи кислорода. Среди всех способов кислородно-конвертерный обладает самым повышенным шлакообразованием, причиной является невозможность следить за процессом окисления внутри оборудования.

Мартеновский способ
Мартеновский способ на протяжении большей части 20-го века составлял основную часть обработки всей стали, изготовленной в мире. Уильям Сименс в 1860-х годах искал средства повышения температуры в металлургической печи, воскресив старое предложение об использовании отработанного тепла, выделяемого печью. Он нагревал кирпич до высокой температуры, затем использовал тот же путь для ввода воздуха в печь. Предварительно нагретый воздух значительно увеличивал температуру пламени.
Природный газ или распыленные тяжелые масла используются в качестве топлива; воздух и топливо нагреваются до сгорания. Печь загружается жидким доменным чугуном и стальным ломом вместе с железной рудой, известняком, доломитом и флюсами.
Сама печь изготовлена из высокоогнеупорных материалов, таких как магнезитовый кирпич для очагов. Вес мартеновских печей достигает 600 тонн, и их обычно устанавливают группами, так что массивное вспомогательное оборудование, необходимое для зарядки печей и обработки жидкой стали, может быть эффективно использовано.
Хотя мартеновский процесс практически полностью заменен в большинстве промышленно развитых стран основным кислородным процессом и электродуговой печью, им изготавливают около 1/6 всей стали, произведенной во всем мире.

Достоинства и недостатки данного способа
К преимуществам относят простоту использования и легкость в получении легированной стали с примесью различных добавок, которые придают материалу различные специализированные свойства. Необходимые добавки и сплавы добавляют непосредственно перед окончанием выплавки.
К недостаткам можно отнести сниженную экономичность, по сравнению с кислородно-конверторным способом. Также качество стали более низкое, по сравнению с остальными методами выплавки металла.

Электросталеплавильный способ
Современный способ выплавки стали с использованием собственных запасов представляет собой печь, которая нагревает заряженный материал с помощью электрической дуги. Промышленные дуговые печи имеют размеры от небольших единиц грузоподъемностью около одной тонны (используются в литейных цехах для производства чугунных изделий) до 400 тонн единиц, применяемых для вторичной металлургии.
Дуговые печи, используемые в исследовательских лабораториях, могут иметь емкость всего несколько десятков граммов. Промышленные температуры электрической дуговой печи могут составлять до 1800 °C (3,272 °F), в то время как лабораторные установки могут превышать 3000 °C (5432 °F).
Дуговые печи отличаются от индукционных тем, что зарядный материал непосредственно подвергается воздействию электрической дуги, а ток в выводах проходит через заряженный материал. Электрическая дуговая печь используется для производства стали, состоит из огнеупорной футеровки, обычно водоохлаждаемой, больших размеров, покрыта раздвижной крышей.
Печь в основном разделена на три секции:
- Оболочка, состоящая из боковых стенок и нижней стальной чаши.
- Очаг состоит из огнеупора, который вытягивает нижнюю чашу.
- Крыша с огнеупорной футеровкой или водяным охлаждением может быть выполнена в виде секции шара или в виде усеченного конуса (коническая секция).

Достоинства и недостатки способа
Данный способ занимает лидирующие позиции в области производства стали. Метод выплавки стали применяется для создания высококачественного металла, который либо совсем лишен, либо содержит незначительное количество нежелательных примесей, таких как сера, фосфор и кислород.
Главным плюсом метода является использование электроэнергии для нагревания, благодаря чему можно легко контролировать температуру плавления и достичь невероятной скорости нагревания металла. Автоматизированная работа станет приятным дополнением к прекрасной возможности качественной переработки различного металлического лома.
Как получают и из чего делают железо (сталь)?
Железо и стали на его основе используются повсеместно в промышленности и обыденной жизни человека. Однако мало кто знает, из чего делают железо, вернее, как его добывают и преобразовывают в сплав стали.
Популярное заблуждение
Для начала определимся с понятиями, поскольку люди часто путаются и не совсем понимают, что такое железо вообще. Это химический элемент и простое вещество, которое в чистом виде не встречается и не используется. А вот сталь – это сплав на основе железа. Она богата на различные химические элементы, а также содержит углерод в своем составе, который необходим для придания прочности и твердости.

Следовательно, не совсем правильно рассуждать о том, из чего делают железо, так как оно представляет собой химический элемент, который есть в природе. Человек из него делает сталь, которая в дальнейшем может использоваться для изготовления чего-либо: подшипников, кузовов автомобилей, дверей и т. д. Невозможно перечислить все предметы, которые из нее производятся. Итак, ниже мы не будем разбирать, из чего делают железо. Вместо этого поговорим о преобразовании этого элемента в сталь.
Добыча
В России и мире существует множество карьеров, где добывают железную руду. Это огромные и тяжелые камни, которые достаточно сложно достать из карьера, так как они являются частью одной большой горной породы. Непосредственно на карьерах в горную породу закладывают взрывчатку и взрывают ее, после чего огромные куски камней разлетаются в разные стороны. Затем их собирают, грузят на большие самосвалы (типа БелАЗ) и везут на перерабатывающий завод. Из этой горной породы и будет добываться железо.

Иногда, если руда находится на поверхности, то ее вовсе необязательно подрывать. Ее достаточно расколоть на куски любым другим способом, погрузить на самосвал и увезти.
Производство
Итак, теперь мы понимаем, из чего делают железо. Горная порода является сырьем для его добычи. Ее отвозят на перерабатывающее предприятие, загружают в доменную печь и нагревают до температуры 1400-1500 градусов. Эта температура должна держаться в течение определенного времени. Содержащееся в составе горной породы железо плавится и приобретает жидкую форму. Затем его остается разлить в специальные формы. Образовавшиеся шлаки при этом отделяют, а само железо получается чистым. Затем агломерат подают в бункерные чаши, где он продувается потоком воздуха и охлаждается водой.

Есть и другой способ получения железа: горную породу дробят и подают на специальный магнитный сепаратор. Так как железо имеет способность намагничиваться, то минералы остаются на сепараторе, а вся пустая порода вымывается. Конечно, чтобы железо превратить в металл и придать ему твердую форму, его необходимо легировать с помощью другого компонента – углерода. Его доля в составе очень мала, однако именно благодаря нему металл становится высокопрочным.
Стоит отметить, что в зависимости от объема добавляемого в состав углерода сталь может получаться разной. В частности, она может быть более или менее мягкой. Есть, например, специальная машиностроительная сталь, при изготовлении которой к железу добавляют всего 0,75 % углерода и марганец.

Теперь вы знаете, из чего делают железо и как его преобразовывают в сталь. Конечно, способы описаны весьма поверхностно, но суть они передают. Нужно запомнить, что из горной породы делают железо, из чего далее могут получать сталь.
Производители
На сегодняшний день в разных странах есть крупные месторождения железной руды, которые являются базой для производства мировых запасов стали. В частности, на Россию и Бразилию приходится 18 % мирового производства стали, на Австралию – 14 %, Украину – 11 %. Самыми крупными экспортерами является Индия, Бразилия, Австралия. Отметим, что цены на металл постоянно меняются. Так, в 2011 году стоимость одной тонны металла составляла 180 долларов США, а к 2016 году была зафиксирована цена в 35 долларов США за тонну.
Заключение
Теперь вы знаете, из чего состоит железо (имеется в виду металл) и как его производят. Применение этого материала распространено во всем мире, и его значение практически невозможно переоценить, так как используется он в промышленных и бытовых отраслях. К тому же экономика некоторых стран построена на базе изготовления металла и его последующего экспорта.
Мы рассмотрели, из чего состоит сплав. Железо в его составе смешивается с углеродом, и подобная смесь является основной для изготовления большинства известных металлов.
Железо

Железо — ковкий металл серебристо-белого цвета с высокой химической реакционной способностью: железо быстро корродирует при высоких температурах или при высокой влажности на воздухе. В чистом кислороде железо горит, а в мелкодисперсном состоянии самовозгорается и на воздухе. Обозначается символом Fe (лат. Ferrum). Один из самых распространённых в земной коре металлов (второе место после алюминия).
Смотрите так же:
СТРУКТУРА

Две модификации кристаллической решетки железа
Для железа установлено несколько полиморфных модификаций, из которых высокотемпературная модификация – γ-Fe(выше 906°) образует решетку гранецентрированного куба типа Сu (а0 = 3,63), а низкотемпературная – α-Fe-решетку центрированного куба типа α-Fe (a0 = 2,86).
В зависимости от температуры нагрева железо может находиться в трех модификациях, характеризующихся различным строением кристаллической решетки:
- В интервале температур от самых низких до 910°С —а-феррит (альфа-феррит), имеющий строение кристаллической решетки в виде центрированного куба;
- В интервале температур от 910 до 1390°С — аустенит, кристаллическая решетка которого имеет строение гранецентрированного куба;
- В интервале температур от 1390 до 1535°С (температура плавления) — д-феррит (дельта-феррит). Кристаллическая решетка д-феррита такая же, как и а-феррита. Различие между ними только в иных (для д-феррита больших) расстояниях между атомами.
При охлаждении жидкого железа первичные кристаллы (центры кристаллизации) возникают одновременно во многих точках охлаждаемого объема. При последующем охлаждении вокруг каждого центра надстраиваются новые кристаллические ячейки, пока не будет исчерпан весь запас жидкого металла.
В результате получается зернистое строение металла. Каждое зерно имеет кристаллическую решетку с определенным направлением его осей.
При последующем охлаждении твердого железа при переходах д-феррита в аустенит и аустенита в а-феррит могут возникать новые центры кристаллизации с соответствующим изменением величины зерна
СВОЙСТВА

В чистом виде при нормальных условиях это твердое вещество. Оно обладает серебристо-серым цветом и ярко выраженным металлическим блеском. Механические свойства железа включают в себя уровень твердости по шкале Мооса. Она равна четырем (средняя). Железо обладает хорошей электропроводностью и теплопроводностью. Последнюю особенность можно ощутить, дотронувшись до железного предмета в холодном помещении. Так как этот материал быстро проводит тепло, он за короткий промежуток времени забирает большую его часть из вашей кожи, и поэтому вы ощущаете холод.
Дотронувшись, к примеру, до дерева, можно отметить, что его теплопроводность намного ниже. Физические свойства железа — это и его температуры плавления и кипения. Первая составляет 1539 градусов по шкале Цельсия, вторая — 2860 градусов по Цельсию. Можно сделать вывод, что характерные свойства железа — хорошая пластичность и легкоплавкость. Но и это еще далеко не все. Также в физические свойства железа входит и его ферромагнитность. Что это такое? Железо, магнитные свойства которого мы можем наблюдать на практических примерах каждый день, – единственный металл, обладающий такой уникальной отличительной чертой. Это объясняется тем, что данный материал способен намагничиваться под действием магнитного поля. А по прекращении действия последнего железо, магнитные свойства которого только что сформировались, еще надолго само остается магнитом. Такой феномен можно объяснить тем, что в структуре данного металла присутствует множество свободных электронов, которые способны передвигаться.
ЗАПАСЫ И ДОБЫЧА
Железо — один из самых распространённых элементов в Солнечной системе, особенно на планетах земной группы, в частности, на Земле. Значительная часть железа планет земной группы находится в ядрах планет, где его содержание, по оценкам, около 90 %. Содержание железа в земной коре составляет 5 %, а в мантии около 12 %.

В земной коре железо распространено достаточно широко — на его долю приходится около 4,1 % массы земной коры (4-е место среди всех элементов, 2-е среди металлов). В мантии и земной коре железо сосредоточено главным образом в силикатах, при этом его содержание значительно в основных и ультраосновных породах, и мало — в кислых и средних породах.
Известно большое число руд и минералов, содержащих железо. Наибольшее практическое значение имеют красный железняк (гематит, Fe2O3; содержит до 70 % Fe), магнитный железняк (магнетит, FeFe2O4, Fe3O4; содержит 72,4 % Fe), бурый железняк или лимонит (гётит и гидрогётит, соответственно FeOOH и FeOOH·nH2O). Гётит и гидрогётит чаще всего встречаются в корах выветривания, образуя так называемые «железные шляпы», мощность которых достигает несколько сотен метров. Также они могут иметь осадочное происхождение, выпадая из коллоидных растворов в озёрах или прибрежных зонах морей. При этом образуются оолитовые, или бобовые, железные руды. В них часто встречается вивианит Fe3(PO4)2·8H2O, образующий чёрные удлинённые кристаллы и радиально-лучистые агрегаты.
Содержание железа в морской воде – 1·10 −5 -1·10 −8 %
В промышленности железо получают из железной руды, в основном из гематита (Fe2O3) и магнетита (FeO·Fe2O3).
Существуют различные способы извлечения железа из руд. Наиболее распространённым является доменный процесс.
Первый этап производства — восстановление железа углеродом в доменной печи при температуре 2000 °C. В доменной печи углерод в виде кокса, железная руда в виде агломерата или окатышей и флюс (например, известняк) подаются сверху, а снизу их встречает поток нагнетаемого горячего воздуха.
Кроме доменного процесса, распространён процесс прямого получения железа. В этом случае предварительно измельчённую руду смешивают с особой глиной, формируя окатыши. Окатыши обжигают, и обрабатывают в шахтной печи горячими продуктами конверсии метана, которые содержат водород. Водород легко восстанавливает железо, при этом не происходит загрязнения железа такими примесями, как сера и фосфор, которые являются обычными примесями в каменном угле. Железо получается в твёрдом виде, и в дальнейшем переплавляется в электрических печах. Химически чистое железо получается электролизом растворов его солей.
ПРОИСХОЖДЕНИЕ

ПРИМЕНЕНИЕ

Кольцо из железа
Железо — один из самых используемых металлов, на него приходится до 95 % мирового металлургического производства.
Железо является основным компонентом сталей и чугунов — важнейших конструкционных материалов.
Железо может входить в состав сплавов на основе других металлов — например, никелевых.
Магнитная окись железа (магнетит) — важный материал в производстве устройств долговременной компьютерной памяти: жёстких дисков, дискет и т. п.
Ультрадисперсный порошок магнетита используется во многих чёрно-белых лазерных принтерах в смеси с полимерными гранулами в качестве тонера. Здесь одновременно используется чёрный цвет магнетита и его способность прилипать к намагниченному валику переноса.
Уникальные ферромагнитные свойства ряда сплавов на основе железа способствуют их широкому применению в электротехнике для магнитопроводов трансформаторов и электродвигателей.
Хлорид железа(III) (хлорное железо) используется в радиолюбительской практике для травления печатных плат.
Семиводный сульфат железа (железный купорос) в смеси с медным купоросом используется для борьбы с вредными грибками в садоводстве и строительстве.
Железо применяется в качестве анода в железо-никелевых аккумуляторах, железо-воздушных аккумуляторах.
Водные растворы хлоридов двухвалентного и трёхвалентного железа, а также его сульфатов используются в качестве коагулянтов в процессах очистки природных и сточных вод на водоподготовке промышленных предприятий.

Железо — ковкий металл серебристо-белого цвета с высокой химической реакционной способностью: железо быстро корродирует при высоких температурах или при высокой влажности на воздухе. В чистом кислороде железо горит, а в мелкодисперсном состоянии самовозгорается и на воздухе. Обозначается символом Fe (лат. Ferrum). Один из самых распространённых в земной коре металлов (второе место после алюминия).
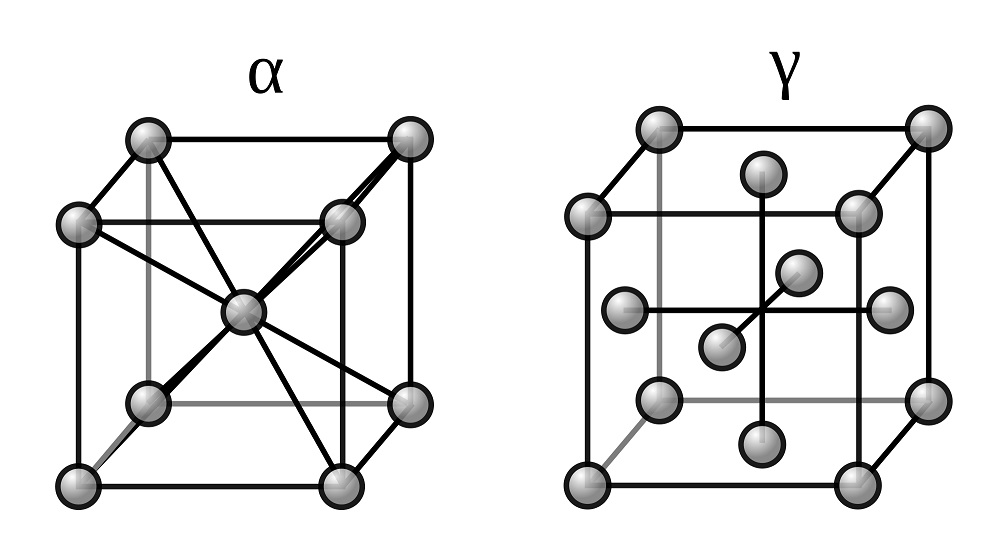
Для железа установлено несколько полиморфных модификаций, из которых высокотемпературная модификация — γ-Fe (выше 906°) образует решетку гранецентрированного куба типа Сu (а0 = 3,63), а низкотемпературная — α-Fe-решетку центрированного куба типа α-Fe (a0 = 2,86).
В зависимости от температуры нагрева железо может находиться в трех модификациях, характеризующихся различным строением кристаллической решетки:
В интервале температур от самых низких до 910°С — а-феррит (альфа-феррит), имеющий строение кристаллической решетки в виде центрированного куба;
В интервале температур от 910 до 1390°С — аустенит, кристаллическая решетка которого имеет строение гранецентрированного куба;
В интервале температур от 1390 до 1535°С (температура плавления) — д-феррит (дельта-феррит). Кристаллическая решетка д-феррита такая же, как и а-феррита. Различие между ними только в иных (для д-феррита больших) расстояниях между атомами.
При охлаждении жидкого железа первичные кристаллы (центры кристаллизации) возникают одновременно во многих точках охлаждаемого объема. При последующем охлаждении вокруг каждого центра надстраиваются новые кристаллические ячейки, пока не будет исчерпан весь запас жидкого металла.
В результате получается зернистое строение металла. Каждое зерно имеет кристаллическую решетку с определенным направлением его осей.
При последующем охлаждении твердого железа при переходах д-феррита в аустенит и аустенита в а-феррит могут возникать новые центры кристаллизации с соответствующим изменением величины зерна.
В чистом виде при нормальных условиях это твердое вещество. Оно обладает серебристо-серым цветом и ярко выраженным металлическим блеском. Механические свойства железа включают в себя уровень твердости по шкале Мооса. Она равна четырем (средняя). Железо обладает хорошей электропроводностью и теплопроводностью. Последнюю особенность можно ощутить, дотронувшись до железного предмета в холодном помещении. Так как этот материал быстро проводит тепло, он за короткий промежуток времени забирает большую его часть из вашей кожи, и поэтому вы ощущаете холод.
Дотронувшись, к примеру, до дерева, можно отметить, что его теплопроводность намного ниже. Физические свойства железа — это и его температуры плавления и кипения. Первая составляет 1539 градусов по шкале Цельсия, вторая — 2860 градусов по Цельсию. Можно сделать вывод, что характерные свойства железа — хорошая пластичность и легкоплавкость. Но и это еще далеко не все. Также в физические свойства железа входит и его ферромагнитность. Что это такое? Железо, магнитные свойства которого мы можем наблюдать на практических примерах каждый день, — единственный металл, обладающий такой уникальной отличительной чертой. Это объясняется тем, что данный материал способен намагничиваться под действием магнитного поля. А по прекращении действия последнего железо, магнитные свойства которого только что сформировались, еще надолго само остается магнитом. Такой феномен можно объяснить тем, что в структуре данного металла присутствует множество свободных электронов, которые способны передвигаться.
Железо — один из самых распространённых элементов в Солнечной системе, особенно на планетах земной группы, в частности, на Земле. Значительная часть железа планет земной группы находится в ядрах планет, где его содержание, по оценкам, около 90%. Содержание железа в земной коре составляет 5%, а в мантии около 12%.
В земной коре железо распространено достаточно широко — на его долю приходится около 4,1% массы земной коры (4-е место среди всех элементов, 2-е среди металлов). В мантии и земной коре железо сосредоточено главным образом в силикатах, при этом его содержание значительно в основных и ультраосновных породах, и мало — в кислых и средних породах.

Известно большое число руд и минералов, содержащих железо. Наибольшее практическое значение имеют красный железняк (гематит, Fe2O3; содержит до 70% Fe), магнитный железняк (магнетит, FeFe2O4, Fe3O4; содержит 72,4% Fe), бурый железняк или лимонит (гётит и гидрогётит, соответственно FeOOH и FeOOH·nH2O). Гётит и гидрогётит чаще всего встречаются в корах выветривания, образуя так называемые «железные шляпы», мощность которых достигает несколько сотен метров. Также они могут иметь осадочное происхождение, выпадая из коллоидных растворов в озёрах или прибрежных зонах морей. При этом образуются оолитовые, или бобовые, железные руды. В них часто встречается вивианит Fe3(PO4)2·8H2O, образующий чёрные удлинённые кристаллы и радиально-лучистые агрегаты.
Содержание железа в морской воде — 1·10−5-1·10−8%
В промышленности железо получают из железной руды, в основном из гематита (Fe2O3) и магнетита (FeO·Fe2O3).
Существуют различные способы извлечения железа из руд. Наиболее распространённым является доменный процесс.
Первый этап производства — восстановление железа углеродом в доменной печи при температуре 2000 °C. В доменной печи углерод в виде кокса, железная руда в виде агломерата или окатышей и флюс (например, известняк) подаются сверху, а снизу их встречает поток нагнетаемого горячего воздуха.

Кроме доменного процесса, распространён процесс прямого получения железа. В этом случае предварительно измельчённую руду смешивают с особой глиной, формируя окатыши. Окатыши обжигают, и обрабатывают в шахтной печи горячими продуктами конверсии метана, которые содержат водород. Водород легко восстанавливает железо, при этом не происходит загрязнения железа такими примесями, как сера и фосфор, которые являются обычными примесями в каменном угле. Железо получается в твёрдом виде, и в дальнейшем переплавляется в электрических печах. Химически чистое железо получается электролизом растворов его солей.
Почти чистое железо найдено в лунном грунте, что связывают как с падениями метеоритов, так и с магматическими процессами. Наконец, два класса метеоритов — железокаменные и железные содержат природные сплавы железа в качестве породообразующего компонента.
Железо — один из самых используемых металлов, на него приходится до 95% мирового металлургического производства.

Железо является основным компонентом сталей и чугунов — важнейших конструкционных материалов.
Железо может входить в состав сплавов на основе других металлов — например, никелевых.
Магнитная окись железа (магнетит) — важный материал в производстве устройств долговременной компьютерной памяти: жёстких дисков, дискет и т. п.
Ультрадисперсный порошок магнетита используется во многих чёрно-белых лазерных принтерах в смеси с полимерными гранулами в качестве тонера. Здесь одновременно используется чёрный цвет магнетита и его способность прилипать к намагниченному валику переноса.
Уникальные ферромагнитные свойства ряда сплавов на основе железа способствуют их широкому применению в электротехнике для магнитопроводов трансформаторов и электродвигателей.
Хлорид железа(III) (хлорное железо) используется в радиолюбительской практике для травления печатных плат.
Семиводный сульфат железа (железный купорос) в смеси с медным купоросом используется для борьбы с вредными грибками в садоводстве и строительстве.
Железо применяется в качестве анода в железо-никелевых аккумуляторах, железо-воздушных аккумуляторах.
Водные растворы хлоридов двухвалентного и трёхвалентного железа, а также его сульфатов используются в качестве коагулянтов в процессах очистки природных и сточных вод на водоподготовке промышленных предприятий.
Железо (англ. Iron) — Fe
Молекулярный вес – 55.85 г/моль
Происхождение названия – возможно англо-саксонского происхождения
IMA статус – действителен, описан впервые до 1959 (до IMA)
ФИЗИЧЕСКИЕ СВОЙСТВА
Цвет минерала – железно-черный
Цвет черты – серый
Прозрачность – непрозрачный
Блеск – металлический
Спайность – несовершенная по
Твердость (шкала Мооса) – 4,5
Излом – в зазубринах
Прочность – ковкий
Плотность (измеренная) – 7.3 — 7.87 г/см³
Радиоактивность (GRapi) – 0
Магнетизм – ферромагнетик
ОПТИЧЕСКИЕ СВОЙСТВА
Тип – изотропный
Цвет в отраженном свете – белый
Люминесценция в ультрафиолетовом излучении – не флюоресцентный
КРИСТАЛЛОГРАФИЧЕСКИЕ СВОЙСТВА
Точечная группа – m3m (4/m 3 2/m) — изометрический — гексаоктаэдральный
Пространственная группа – Im3m (I4/m 3 2/m)
Сингония – кубическая
Параметры ячейки – a = 2.8664Å
Двойникование – (111) также в пластинчатых массах
Морфология – в маленьких пузырьках
Читайте также:
