Кадмий ряд активности металлов
Обновлено: 20.09.2024
Электрохимический ряд активности (ряд напряжений, ряд стандартных электродных потенциалов) металлов — последовательность, в которой металлы расположены в порядке увеличения их стандартных электрохимических потенциалов φ 0 , отвечающих полуреакции восстановления катиона металла Me n+ : Me n+ + nē → Me
Ряд напряжений характеризует сравнительную активность металлов в окислительно-восстановительные реакциях в водных растворах.
Содержание
История
Последовательность расположения металлов в порядке изменения их химической активности в общих чертах была известна уже алхимикам [1] . Процессы взаимного вытеснения металлов из растворов и их поверхностное осаждение (например, вытеснение серебра и меди из растворов их солей железом) рассматривались как проявление трансмутации элементов.
Поздние алхимики вплотную подошли к пониманию химической стороны взаимного осаждения металлов из их растворов. Так, Ангелус Сала в работе «Anatomia Vitrioli» (1613) пришёл к выводу, что продукты химических реакций состоят из тех же «компонентов», которые содержались в исходных веществах. Впоследствии Роберт Бойль предложил гипотезу о причинах, по которым один металл вытесняет другой из раствора на основе корпускулярных представлений [2] .
В 1793 году Алессандро Вольта, конструируя гальванический элемент («Вольтов столб»), установил относительную активность известных тогда металлов: Zn, Pb, Sn, Fe, Cu, Ag, Au. «Сила» гальванического элемента оказывалась тем больше, чем дальше стояли друг от друга металлы в этом ряду («ряд напряжений»). Однако Вольта не связал этот ряд с химическими свойствами металлов.
В 1798 году Иоганн Вильгельм Риттер указал, что ряд Вольта эквивалентен ряду окисления металлов (т. е. последовательности уменьшения их сродства с кислородом). Таким образом, Риттер высказал гипотезу о возникновении электрического тока вследствие протекания химической реакции [3] .
В эпоху становления классической химии способность элементов вытеснять друг друга из соединений стала важным аспектом понимания реакционной способности. Й. Берцелиус на основе электрохимической теории сродства построил классификацию элементов, разделив их на «металлоиды» (сейчас применяется термин «неметаллы») и «металлы» и поставив между ними водород.
Не отрицая значительных заслуг Бекетова в становлении современных представлений об ряде активности металлов, следует считать ошибочным бытующее в отечественной популярной и учебной литературе представление о нём как единственном создателе этого ряда. [5] [6] .
Многочисленные экспериментальные данные, полученные в конце XIX века, опровергали гипотезу Бекетова. Так, Уильям Одлинг описал множество случаев «обращения активности». Например, медь вытесняет олово из концентрированного подкисленного раствора SnCl2 и свинец — из кислого раствора PbCl2; она же способна к растворению в концентрированной соляной кислоте с выделением водорода. Медь, олово и свинец находятся в ряду правее кадмия, однако могут вытеснять его из кипящего слабо подкисленного раствора CdCl2.
Бурное развитие теоретической и экспериментальной физической химии указывало на иную причину различий химической активности металлов. С развитием современных представлений электрохимии (главным образом в работах Вальтера Нернста) стало ясно, что эта последовательность соответствует «ряду напряжений» – расположению металлов по значению стандартных электродных потенциалов. Таким образом, вместо качественной характеристики — «склонности» металла и его иона к тем или иным реакциям — Нерст ввёл точную количественную величину, характеризующую способность каждого металла переходить в раствор в виде ионов, а также восстанавливаться из ионов до металла на электроде, а соответствующий ряд получил название ряда стандартных электродных потенциалов.
Теоретические основы
Значения электрохимических потенциалов являются функцией многих переменных и поэтому обнаруживают сложную зависимость от положения металлов в периодической системе. Так, окислительный потенциал катионов растёт с увеличением энергии атомизации металла, с увеличением суммарного потенциала ионизации его атомов и с уменьшением энергии гидратации его катионов.
В самом общем виде ясно, что металлы, находящиеся в начале периодов характеризуются низкими значениями электрохимических потенциалов и занимают места в левой части ряда напряжений. При этом чередование (щелочных и щёлочноземельных металлов отражает явление диагонального сходства. Металлы, расположенные ближе к серединам периодов, характеризуются большими значениями потенциалов и занимают места в правой половине ряда. Последовательное увеличение электрохимического потенциала (от −3,395 В у пары Eu 2+ /Eu [источник не указан 228 дней] до +1,691 В у пары Au + /Au) отражает уменьшение восстановительной активности металлов (свойство отдавать электроны) и усиление окислительной способности их катионов (свойство присоединять электроны). Таким образом, самым сильным восстановителем является металлический европий, а самым сильным окислителем — катионы золота Au + .
В ряд напряжений традиционно включается водород, поскольку практическое измерение электрохимических потенциалов металлов производится с использованием стандартного водородного электрода.
Практическое использование ряда напряжений
Ряд напряжений используется на практике для сравнительной оценки химической активности металлов в реакциях с водными растворами солей и кислот и для оценки катодных и анодных процессов при электролизе:
Кадмий

Мягкий ковкий серебристо-серый металл
Ка́дмий / Cadmium (Cd), 48
1,69 (шкала Полинга)
Ка́дмий — элемент побочной подгруппы второй группы, пятого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 48. Обозначается символом Cd (лат. Cadmium ). Простое вещество кадмий (CAS-номер: 7440-43-9) при нормальных условиях — мягкий ковкий тягучий переходный металл серебристо-белого цвета. Устойчив в сухом воздухе, во влажном на его поверхности образуется плёнка оксида, препятствующая дальнейшему окислению металла.
История открытия
Открыт немецким профессором Ф. Штромейером в 1817. Провизоры Магдебурга при изучении оксида цинка ZnO заподозрили в нём примесь мышьяка. Штромейер выделил из ZnO коричнево-бурый оксид, восстановил его водородом и получил серебристо-белый металл, который получил название кадмий.
Происхождение названия
Штромейер назвал кадмий по греческому названию руды, из которой в Германии добывали цинк, — καδμεία. В свою очередь, руда получила своё название в честь Кадма, героя древнегреческой мифологии.
Нахождение в природе
Среднее содержание кадмия в земной коре 130 мг/т, в морской воде 0,11 мкг/л. Кадмий относится к редким, рассеянным элементам: он содержится в виде изоморфной примеси во многих минералах и всегда в минералах цинка. Известно всего лишь 6 кадмиевых минералов. Весьма редкими минералами кадмия являются гринокит CdS (77,8% Cd), хоулиит (то же), отавит CdCO3, монтемпонит CdO (87,5% Cd), кадмоселит CdSe (47% Cd), ксантохроит CdS(H2O)х (77,2% Cd). Основная масса кадмия рассеяна в большом числе минералов (более 50), преимущественно в сульфидах цинка, свинца, меди, железа, марганца и ртути. Максимальная концентрация отмечена в минералах цинка и прежде всего в сфалерите (до 5%). В большинстве же случаев содержание кадмия в сфалерите не превышает 0,4 – 0,6%. В других сульфидах, например, в станине содержание кадмия 0,003 – 0,2%, в галените 0,005 – 0,02%, в халькопирите 0,006 – 0,12%; из этих сульфидов кадмий обычно не извлекается.
Кадмий не образует самостоятельных месторождений, а входит в состав руд месторождений других металлов. Относительно высоко содержание кадмия в рудах среднетемпературных свинцово-цинковых и частично медно-колчеданных месторождений.
Получение
Единственный минерал, который представляет интерес в получении кадмия — гринокит, так называемая «кадмиевая обманка». Его добывают вместе со сфалеритом при разработке цинковых руд. В ходе переработки кадмий концентрируется в побочных продуктах процесса, откуда его потом извлекают. В настоящее время производится около 20000 тонн кадмия в год. [2]
Физические свойства
Кадмий — серебристо-белый мягкий металл с гексагональной решёткой. Если кадмиевую палочку изгибать, то можно услышать слабый треск — это трутся друг о друга микрокристаллы металла (так же трещит и пруток олова).
Химические свойства
Кадмий расположен в одной группе периодической системы с цинком и ртутью, занимая промежуточное место между ними, поэтому некоторые химические свойства этих элементов сходны. Так, сульфиды и оксиды этих элементов практически нерастворимы в воде. С углеродом кадмий не взаимодействует и карбидов не образует [3] .
Применение
Сплавы
Кадмий используется как компонент твёрдых припоев (сплавов на основе серебра, меди, цинка) для снижения их температуры плавления. Около 10 % производимого кадмия — компонент ювелирных и легкоплавких сплавов. Сплав кадмия с золотом имеет зеленоватый цвет [4] [5] .
Защитные покрытия
40 % производимого кадмия используется для нанесения антикоррозионных покрытий на металлы.
Химические источники тока
Около 20 % кадмия идет на изготовление кадмиевых электродов, применяемых в аккумуляторах (никель-кадмиевых и серебряно-кадмиевых), нормальных элементах Вестона, в резервных батареях (свинцово-кадмиевый элемент, ртутно-кадмиевый элемент) и др.
Пигменты
Около 20 % кадмия используется для производства неорганических красящих веществ (сульфиды и селениды, смешанные соли, например, сульфид кадмия — кадмий лимонный).
Цена на кадмий на август 2011 года составила примерно 3$ за 1 кг. [6]
Другие сферы применения
- Сульфид кадмия применяется для производства плёночных солнечных батарей с КПД около 10—16 %, а также как очень хороший термоэлектрический материал.
- Кадмий используется как компонент полупроводниковых материалов и люминофоров.
- Кадмий очень хорошо захватывает тепловые нейтроны и служит для изготовления регулирующих стержней для атомных реакторов и в качестве защиты от нейтронов. Иногда эти свойства используются в экспериментальных моделях противоопухолевой терапии (нейтрон-захватная терапия)
- Фтороборат кадмия — важный флюс, применяемый для пайки алюминия и других металлов.
- Теплопроводность кадмия вблизи абсолютного нуля наивысшая среди всех металлов, поэтому кадмий иногда применяется для криогенной техники.
Физиологическое действие
Соединения кадмия ядовиты. Особенно опасным случаем является вдыхание паров его оксида (CdO) [7] . Вдыхание в течение 1 минуты воздуха с содержанием 2,5 г/м 3 окиси кадмия, или 30 секунд при концентрации 5 г/м 3 является смертельным. [8] Кадмий является канцерогеном [9] .
В качестве первой помощи при остром кадмиевом отравлении рекомендуется свежий воздух, полный покой, предотвращение охлаждения. При раздражении дыхательных путей — тёплое молоко с содой, ингаляции 2 %-ным раствором NaHCO3. При упорном кашле — кодеин, дионин, горчичники на грудную клетку, необходима врачебная помощь. Противоядием при отравлении, вызванном приёмом внутрь кадмиевых солей, служит альбумин с карбонатом натрия. [8]
Острая токсичность
Пары кадмия, все его соединения токсичны, что связано, в частности, с его способностью связывать серосодержащие ферменты и аминокислоты.
Симптомы острого отравления солями кадмия — рвота и судороги.
Хроническая токсичность
Кадмий — кумулятивный яд (способен накапливаться в организме).
Санитарно-экологические нормативы
В питьевой воде ПДК для кадмия 0,001 мг/дм³ (СанПиН 2.1.4.1074-01).
Механизм токсического действия
Механизм токсического действия кадмия заключается, по-видимому, в связывании карбоксильных, аминных и особенно сульфгидрильных групп белковых молекул, в результате чего угнетается активность ферментных систем [8] . Растворимые соединения кадмия после всасывания в кровь поражают центральную нервную систему, печень и почки, нарушают фосфорно-кальциевый обмен. Хроническое отравление приводит к анемии и разрушению костей.
Кадмий в норме в небольших количествах присутствуют в организме здорового человека. Кадмий легко накапливается в быстроразмножающихся клетках (например в опухолевых или половых). Он связывается с цитоплазматическим и ядерным материалом клеток и повреждает их. Он изменяет активность многих гормонов и ферментов. Это обусловлено его способностью связывать сульфгидрильные (-SH) группы.
Изотопы
Из восьми природных изотопов кадмия шесть стабильны, для двух изотопов обнаружена слабая радиоактивность. Это 113 Cd (изотопная распространённость 12,22 %, бета-распад с периодом полураспада 7,7·10 15 лет) и 116 Cd (изотопная распространённость 7,49 %, двойной бета-распад с периодом полураспада 3,0·10 19 лет).
Примечания
Ссылки
- Химические элементы
- Соединения кадмия
- Металлы
- Высокоопасные вещества
- Радиоактивные элементы
- Кадмий
Wikimedia Foundation . 2010 .
Полезное
Смотреть что такое "Кадмий" в других словарях:
КАДМИЙ — (лат. cadmium). Тягучий металл, похожий цветом на олово. Словарь иностранных слов, вошедших в состав русского языка. Чудинов А.Н., 1910. КАДМИЙ лат. cadmium, от kadmeia gea, кадмиева земля. Металл, похожий на олово. Объяснение 25000 иностранных… … Словарь иностранных слов русского языка
КАДМИЙ — КАДМИЙ, Cadmium, хим. элемент, симв. Cd, атомного веса 112,41, порядковый номер 48. Содержится в малых количествах в большинстве цинковых руд и при добывании цинка получается в качестве побочного продукта; может быть также получен… … Большая медицинская энциклопедия
КАДМИЙ — см. КАДМИЙ (Cd). Содержится веточных водах многих промышленных предприятий, особенно свинцово цинковых и металлообрабатывающих заводов, использующих гальванопокрытие. Он присутствует в фосфорных удобрениях. В воде растворяются сернокислый,… … Болезни рыб: Справочник
Кадмий — (Cd) серебристо белый металл. Применяется в ядерной энергетике и гальваностегии, входит в состав сплавов, используется для приготовления типографских клише, припоев, сварочных электродов, при производстве полупроводников; является компонентом… … Российская энциклопедия по охране труда
КАДМИЙ — (Cadmium), Cd, химический элемент II группы периодической системы, атомный номер 48, атомная масса 112,41; металл, tпл 321,1шC. Кадмий используют для нанесения антикоррозийных покрытий на металлы, изготовления электродов, получения пигментов,… … Современная энциклопедия
КАДМИЙ — (символ Cd), серебристо белый металл из второй группы периодической таблицы. Впервые выделен в 1817 г. Содержится в гриноките (в форме сульфида), но в основном его получают в качестве побочного продукта при извлечении цинка и свинца. Легко куется … Научно-технический энциклопедический словарь
Кадмий — Cd (от греч. kadmeia цинковая руда * a. cadmium; н. Kadmium; ф. cadmium; и. cadmio), хим. элемент II группы периодич. системы Mенделеева, ат.н. 48, ат. м. 112,41. B природе встречаются 8 стабильных изотопов 106Cd (1,225%) 108Cd (0,875%),… … Геологическая энциклопедия
КАДМИЙ — муж. металл (одно из химических начал или неразлагаемых стихий), встречаемый в цинковой руде. Кадмиевый, к кадмию относящийся. К адмистый, содержащий в себе кадмий. Толковый словарь Даля. В.И. Даль. 1863 1866 … Толковый словарь Даля
Кадмий — (Cadmium), Cd, химический элемент II группы периодической системы, атомный номер 48, атомная масса 112,41; металл, tпл 321,1°C. Кадмий используют для нанесения антикоррозийных покрытий на металлы, изготовления электродов, получения пигментов,… … Иллюстрированный энциклопедический словарь
КАДМИЙ — хим. элемент, символ Cd (лат. Cadmium), ат. н. 48, ат. м. 112,41; серебристо белый блестящий мягкий металл, плотность 8650 кг/м3, tпл = 320,9°С. Кадмий редкий и рассеянный элемент, ядовит, обычно встречается в рудах вместе с цинком, на который… … Большая политехническая энциклопедия
КАДМИЙ — (лат. Cadmium) Cd, химический элемент II группы периодической системы, атомный номер 48, атомная масса 112,41. Название от греческого kadmeia цинковая руда. Серебристый металл с синеватым отливом, мягкий и легкоплавкий; плотность 8,65 г/см³,… … Большой Энциклопедический словарь
Кадмий — элемент двенадцатой группы (в устаревшей классификации — побочной подгруппы второй группы), пятого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 48. Обозначается символом Cd (лат. Cadmium ). Простое вещество кадмий при нормальных условиях — мягкий ковкий тягучий переходный металл серебристо-белого цвета. Устойчив в сухом воздухе, во влажном на его поверхности образуется плёнка оксида, препятствующая дальнейшему окислению металла. Кадмий и его соединения ядовиты.
- 1 История открытия
- 2 Происхождение названия
- 3 Нахождение в природе
- 4 Нахождение в продуктах
- 5 Получение
- 6 Физические свойства
- 7 Химические свойства
- 7.1 Сплавы
- 7.2 Защитные покрытия
- 7.3 Химические источники тока
- 7.4 Пигменты
- 7.5 Цена
- 7.6 Другие сферы применения
- 7.7 Ограничение применения
- 8.1 Механизм токсического действия
![Кадмий слиток]()
Открыт немецким профессором Ф. Штромейером в 1817 году. Провизоры Магдебурга при изучении оксида цинка ZnO заподозрили в нём примесь мышьяка. Штромейер выделил из ZnO коричнево-бурый оксид, восстановил его водородом и получил серебристо-белый металл, который получил название кадмий.
Среднее содержание кадмия в земной коре — 130 мг/т, в морской воде — 0,11 мкг/л. Кадмий относится к редким, рассеянным элементам: он содержится в виде изоморфной примеси во многих минералах и всегда в минералах цинка. Известно всего лишь 6 кадмиевых минералов. Весьма редкими минералами кадмия являются гринокит CdS (77,8 % Cd), хоулиит (то же), отавит CdCO3, монтепонит CdO (87,5 % Cd), кадмоселит CdSe (47 % Cd), ксантохроит CdS(H2O)х (77,2 % Cd). Основная масса кадмия рассеяна в большом числе минералов (более 50), преимущественно в сульфидах цинка, свинца, меди, железа, марганца и ртути. Максимальная концентрация отмечена в минералах цинка и, прежде всего, в сфалерите (до 5 %). В большинстве же случаев содержание кадмия в сфалерите не превышает 0,4—0,6 %. В других сульфидах, например, в станине содержание кадмия — 0,003—0,2 %, в галените — 0,005—0,02 %, в халькопирите — 0,006—0,12 %; из этих сульфидов кадмий обычно не извлекается.
Почва содержит 0,06 мг/кг, глина — 0,3 мг/кг.
Нахождение в продуктах
ПДК кадмия в воде согласно СанПиН 2.1.4.1074-01 «Питьевая вода. Гигиенические требования к качеству воды централизованных систем питьевого водоснабжения. Контроль качества. Гигиенические требования к обеспечению безопасности систем горячего водоснабжения» — 1 мкг/л
Ископаемый уголь, древесный уголь, ПЭТ тара, древесные гранулы пеллеты (до 0,5 мг/кг), рыба (0,2 мг/кг), какао-порошок (0,5 мг/кг), почки животных (1 мг/кг), рис (0,06 мг/кг), сигарета (0,002 мг/кг), пшеничный хлеб (0,03 мг/кг), маргарин (0,042 мг/кг), говядина/свинина (0,016 мг/кг), креветки (1,2 мг/кг)
Единственный минерал, который представляет интерес в получении кадмия — гринокит, так называемая «кадмиевая обманка». Его добывают вместе со сфалеритом при разработке цинковых руд. В ходе переработки кадмий концентрируется в побочных продуктах процесса, откуда его потом извлекают. В настоящее время производится около 20000 тонн кадмия в год.
Кадмий — серебристо-белый мягкий металл с гексагональной решёткой. Температура плавления — 321 °C, температура кипения — 770 °C. Если кадмиевую палочку изгибать, то можно услышать слабый треск — это трутся друг о друга микрокристаллы металла (так же трещит и пруток олова); любые примеси в металле уничтожают этот эффект. Кадмий твёрже олова, но мягче цинка — его можно резать ножом. При нагревании выше 80 °C кадмий теряет упругость до такой степени, что его можно истолочь в порошок.
![Кадмий слиток]()
Кадмий расположен в одной группе периодической системы с цинком и ртутью, занимая промежуточное место между ними, поэтому некоторые химические свойства этих элементов сходны. На воздухе кадмий устойчив и не утрачивает металлического блеска. Вступает в реакцию с кислородом лишь при нагревании до 350 °C с образованием оксида кадмия CdO . Сульфиды и оксиды этих элементов практически нерастворимы в воде. С углеродом кадмий не взаимодействует и карбидов не образует. Вступает в реакции с кислотами-неокислителями выделяя водород: Cd + H2SO4(20%) ⟶ CdSO4 + H2
Кадмий используется как компонент твёрдых припоев (сплавов на основе серебра, меди, цинка) для снижения их температуры плавления. Около 10 % производимого кадмия — компонент ювелирных и легкоплавких сплавов. Сплав кадмия с золотом имеет зеленоватый цвет.
40 % производимого кадмия используется для нанесения антикоррозионных покрытий на металлы. Кадмирование стальных деталей даёт большую устойчивость против коррозии, особенно в морской воде.
Кадмирование — это электролитическая процедура нанесения кадмиевых покрытий на поверхность металлоизделий. Кадмием покрывают высокоуглеродистые, инструментальные и нержавеющие стали, а кадмирование хлористо-аммонийное наносят на высокопрочные стали.
Около 20 % кадмия идёт на изготовление кадмиевых электродов, применяемых в аккумуляторах (никель-кадмиевых и серебряно-кадмиевых), нормальных элементах Вестона, в резервных батареях (свинцово-кадмиевый элемент, ртутно-кадмиевый элемент) и др.
Цена на кадмий в августе 2011 года составила примерно $3 за 1 кг.
- Сульфид кадмия применяется для производства плёночных солнечных батарей с КПД около 10—16 %, а также как очень хороший термоэлектрический материал.
- Кадмий используется как компонент полупроводниковых материалов и люминофоров.
- Кадмий очень хорошо захватывает тепловые нейтроны (среднее сечение радиационного захвата тепловых нейтронов изотопом 114 Cd составляет 20600 барн). Поэтому кадмий служит для изготовления регулирующих стержней для атомных реакторов и в качестве защиты от нейтронов. Иногда эти свойства используются в экспериментальных моделях противоопухолевой терапии (нейтрон-захватная терапия).
- Фтороборат кадмия — важный флюс, применяемый для пайки алюминия и других металлов.
- Теплопроводность кадмия вблизи абсолютного нуля — наивысшая среди всех металлов, поэтому кадмий иногда применяется для криогенной техники.
- Экранирование гамма-спектрометров от естественного радиационного фона: «свинцовый домик», в котором располагается спектрометрический датчик, выстилается изнутри медным и кадмиевым слоями для экранирования паразитного излучения свинца, искажающего гамма-спектр измеряемого вещества.
Ограничение применения
В 2016 году принят Технический регламент Евразийского экономического союза «Об ограничении применения опасных веществ в изделиях электротехники и радиоэлектроники» (ТР ЕАЭС 037/2016), по которому содержание кадмия в изделиях электротехники и радиоэлектроники не должно превышать 0,01 % по весу однородного материала (Приложение N 2). В Европе действует аналогичная норма (Директива 2002/95/EC).
![]()
Кадмий и все его соединения ядовиты. Особенно опасным случаем является вдыхание паров его оксида (CdO). Вдыхание в течение 1 минуты воздуха с содержанием 2,5 г/м 3 оксида кадмия, или 30 секунд при концентрации 5 г/м 3 является смертельным. Кадмий является канцерогеном.
В качестве первой помощи при остром кадмиевом отравлении рекомендуется свежий воздух, полный покой, предотвращение охлаждения. При раздражении дыхательных путей — тёплое молоко с содой, ингаляции 2%-ным раствором NaHCO3. При упорном кашле — кодеин, дионин, горчичники на грудную клетку, необходима врачебная помощь. Противоядием при отравлении, вызванном приёмом внутрь кадмиевых солей, служит альбумин с карбонатом натрия.
Симптомы острого отравления кадмием — рвота и судороги.
Механизм токсического действия кадмия заключается, по-видимому, в связывании карбоксильных, аминных и особенно сульфгидрильных групп белковых молекул, в результате чего угнетается активность ферментных систем. Растворимые соединения кадмия после всасывания в кровь поражают центральную нервную систему, печень и почки, нарушают фосфорно-кальциевый обмен. Хроническое отравление приводит к анемии и разрушению костей.
Кадмий в норме в небольших количествах присутствуют в организме здорового человека. Кадмий легко накапливается в быстроразмножающихся клетках (например, в опухолевых или половых). Он связывается с цитоплазматическим и ядерным материалом клеток и повреждает их. Он изменяет активность многих гормонов и ферментов. Это обусловлено его способностью связывать сульфгидрильные (-SH) группы.
![Кадмий слиток]()
Из восьми природных изотопов кадмия шесть стабильны, для двух изотопов обнаружена слабая радиоактивность. Это 113 Cd (изотопная распространённость 12,22 %, бета-распад с периодом полураспада 7,7⋅10 15 лет) и 116 Cd (изотопная распространённость 7,49 %, двойной бета-распад с периодом полураспада 3,0⋅10 19 лет).
- Кадмий (Cd)
- Азид кадмия (Cd(N3)2) Тринитрид кадмия
- Амид кадмия (Cd(NH2)2)
- Антимонид кадмия (CdSb) Кадмий сурмянистый
- Ацетат кадмия (Cd(C2H5O2)2) Кадмий уксуснокислый
- Бензоат кадмия (Cd(C7H5O2)2) Кадмий бензойнокислый
- Бромат кадмия (Cd(BrO3)2) Кадмий бромноватокислый
- Бромид кадмия (CdBr2) Кадмий бромистый
- Бромид-триарсенид дикадмия (Cd2As3Br)
- Вольфрамат кадмия (CdWO4) Кадмий вольфрамовокислый
- Гидрид кадмия ((CdH2)n) Кадмий водородистый
- Гидроксид кадмия (Cd(OH)2) Гидроокись кадмия
- Гидроксохлорид кадмия (Cd(OH)Cl)
- Диарсенид кадмия (CdAs2) Мышьяковистый кадмий
- Диарсенид трикадмия (Cd3As2)
- Дигидрофосфат кадмия (Cd(H2PO4)2) Кадмий фосфорнокислый кислый
- Дитизонат кадмия (Cd(C13H11N4S)2)
- Дифенилкадмий (Cd(C6H5)2)
- Дифосфид кадмия (CdP2) Кадмий фосфористый
- Дифосфид трикадмия (Cd3P2) Фосфористый кадмий
- Дихлорид-диоксид трикадмия (Cd3O2Cl2)
- Диэтилкадмий (Cd(C2H5)2)
- Йодат кадмия (Cd(IO3)2) Кадмий йодноватокислый
- Йодид кадмия (CdI2) Кадмий йодистый
- Карбонат кадмия (CdCO3) Кадмий углекислый
- Лактат кадмия (Cd(C3H5O3)2) Кадмий молочнокислый
- Метасиликат кадмия (CdSiO3) Кадмий кремнекислый
- Молибдат кадмия (CdMoO4) Кадмий молибденовокислый
- Ниобат кадмия (Cd2Nb2O7) Кадмий ниобиевокислый
- Нитрат кадмия (Cd(NO3)2) Кадмий азотнокислый
- Нитрид кадмия (Cd3N2) Кадмий азотистый
- Оксалат кадмия (CdC2O4) Кадмий щавелевокислый
- Оксид кадмия I (Cd2O)
- Оксид кадмия (CdO) Кадмий окись
- Оксинат кадмия (Cd(C9H6NO)2)
- Ортосиликат кадмия (Cd2SiO4) Кадмий кремниекислый
- Перманганат кадмия (Cd(MnO4)2) Кадмий марганцовокислый
- Пероксид кадмия (CdO2) Перекись кадмия
- Перхлорат кадмия (Cd(ClO4)2) Кадмий хлорнокислый
- Пирофосфат кадмия (Cd2P2O7) Кадмий фосфорнокислый пиро
- Салицилат кадмия (Cd(C7H5O3)2) Кадмий салициловокислый
- Селенат кадмия (CdSeO4) Кадмий селеновокислый
- Селенид кадмия (CdSe) Кадмий селенистый
- Стеарат кадмия (Cd(C18H35O2)2) Кадмий стеариновокислый
- Сукцинат кадмия (CdC4H4O4) Кадмий янтарнокислый
- Сульфат кадмия (CdSO4) Кадмий сернокислый
- Сульфид кадмия (CdS) Кадмий сернистый
- Сульфит кадмия (CdSO3) Кадмий сернистокислый
- Тартрат кадмия (CdC4H4O6) Кадмий виннокислый
- Теллурид кадмия (CdTe) Кадмий теллуристый
- Теллурит кадмия (CdTeO3) Кадмий теллуристокислый
- Тетрафосфид кадмия (CdP4)
- Тетрафтороборат кадмия (Cd[BF4]2)
- Тиоцианат кадмия (Cd(SCN)2) Кадмий роданистый
- Титанат кадмия (CdTiO3) Кадмий титановокислый
- Трихлорид-фосфид трикадмия (Cd3PCl3)
- Формиат кадмия (Cd(HCO2)2) Кадмий муравьинокислый
- Фосфат кадмия (Cd3(PO4)2) Кадмий фосфорнокислый
- Фторид кадмия (CdF2) Кадмий фтористый
- Хлорат кадмия (Cd(ClO3)2) Кадмий хлорноватокислый
- Хлорид кадмия (CdCl2) Кадмий хлористый
- Хромат кадмия (CdCrO4) Кадмий хромовокислый
- Цианид кадмия (Cd(CN)2) Кадмий цианистый
Eu, Sm, Li, Cs, Rb, K, Ra, Ba, Sr, Ca, Na, Ac, La, Ce, Pr, Nd, Pm, Gd, Tb, Mg, Y, Dy, Am, Ho, Er, Tm, Lu, Sc, Pu,
Th, Np, U, Hf, Be, Al, Ti, Zr, Yb, Mn, V, Nb, Pa, Cr, Zn, Ga, Fe, Cd, In, Tl, Co, Ni, Te, Mo, Sn, Pb, H2,
W, Sb, Bi, Ge, Re, Cu, Tc, Te, Rh, Po, Hg, Ag, Pd, Os, Ir, Pt, AuРяд активности металлов
![Ряд активности металлов]()
Химия
Что же из себя представляет ряд активности металлов давайте разбираться. Металлы — группа химических элементов, обладающих сходными свойствами. Среди них — электропроводность, пластичность, температурная зависимость сопротивления. По виду металлы можно отличить по характерному блеску, который так и назвали — металлический. Но химические свойства элементов отличаются в зависимости от строения их молекул и кристаллической решетки. Особенно ярко отличия проявляются по отношению взаимодействия с кислотами и щелочами. Всего на данный момент насчитывается 96 металлов. Общие свойства металлов показаны в таблице:
![ряд реактивности металлов]()
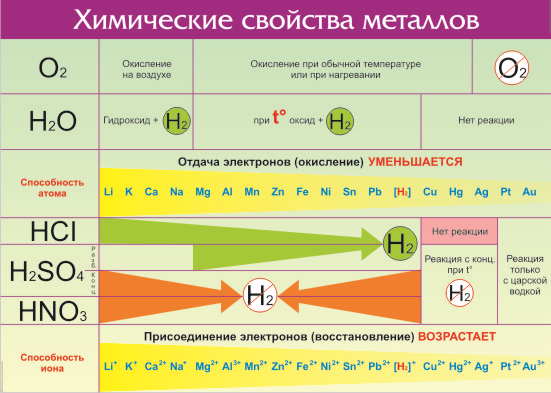
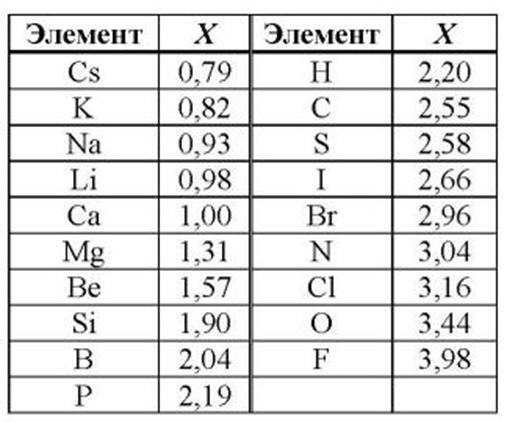
Все металлы в той или иной степени являются восстановителями, то есть, отдают электроны при течении окислительно-восстановительных реакций. Таблица электроотрицательности металлов показывает, какой металл является наиболее активным восстановителем. Если цифра напротив элемента больше 2, то это окислитель с характерными свойствами и выходит из ряда металлов, проявляя типичные свойства неметалла.
![Таблица электроотрицательности металлов]()
Электрохимический ряд активности металлов показывает, какие из металлов более активные, какие менее. Расположение элементов в горизонтальном ряду слева направо показывает направление снижения восстановительной способности и возрастание окислительной.
Восстановительная способность — свойство отдавать электроны в химических реакциях с водными растворами солей и щелочей.
Окислительная способность — свойство присоединять электроны в реакциях с теми же веществами.
![электрохимический ряд напряжений металлов]()
Металлы в правой стороне более слабые восстановители, они вытесняются при реакциях с солевыми растворами металлами, расположенными левее. Пример реакции — Zn + Cu 2+ → Zn 2+ + Cu, которая протекает только в одном направлении. Цинк вытесняет медь, реагируя с водным раствором любой соли меди. Цинковая пластинка, при этом, растворяется, а медная восстанавливается.
Такую последовательность элементов еще называют ряд напряженности металлов, или ряд Бекетова. На всех вариантах записи ряда можно заметить, что последовательность металлов разделена знаком водорода (гидрогена), который металлом никак не является. Это своеобразный маркер, показывающий, что стоящие левее металлы вытесняют водород из водных растворов кислот, не обладающих окислительными свойствами. Некоторые металлы, например, литий, кальций, барий и остальные, стоящи до алюминия, вытесняют водород и при реакции с водой.
2Al +3H2SO4 = Al2(SO4)3 + 3H2↑
Fe + 2HCl = FeCl2 + H2↑
Стоящие правее знака водорода металлы с кислотами-неокислителями не взаимодействуют при нормальных условиях.
Шкала активности металлов широко используется для практических целей, например, в гальванике. Если электроды сделаны из разных металлов, то разрушаться будет тот, который стоит левее. Чем больше промежуток между металлами в ряду, тем активнее проходит процесс коррозии.
Например, метод оцинковки позволяет защитить железо именно потому, что цинк находится левее железа в ряду активности. Пока он не разрушится, то ржавчина на железе не появится. При электролизе, расположенные за водородом металлы осаживаются на катоде, а самые активные, занимающее места до алюминия, выделить из солевых растворов в не получится при нормальных температуре и давлении.
Малоактивные металлы, так называемые переходные элементы с электроотрицательностью в пределах 1,5 – 2. Это:
- Ртуть;
- Олово;
- Серебро;
- Никель;
- Рений;
- Медь;
- Марганец и еще несколько элементов.
К металлам средней активности относятся элементы с числом электроотрицательности от 1 до 1,5. В эту группу входят такие известные элементы, как магний, плутоний, неодим, кальций. Остальные элементы обладают высокой химической активностью. Лидирует в этом списке Франций, который практически не встречается в чистом виде. Из более известных можно назвать калий и натрий, которые приходится хранить в керосине, чтобы они не взаимодействовали с водой и воздухом. Если извлечь их из керосина, то металлы практически мгновенно сгорают.
Реакции кальция и натрия с водой при комнатной температуре выглядят так:
2Na + 2H2O = 2NaOH + H2↑
Сa + 2H2O = Сa(OH)2 + H2↑Стоящие в ряду электронапряжения металлов правее элементы тоже взаимодействуют с водой, но реакция протекает при более высокой температуре с образованием оксида и водорода.
3Fe + 4H2O = Fe3O4 + 4H2↑
Если вступает в реакцию металл и неметалл, то электрический ряд напряжений металлов тоже дает возможность заранее узнать, в каком направлении будет протекать реакция. Скорость реакции зависит как от восстановительной активности металла, так и от окислительных свойств неметалла. Стоящие до водорода металлы реагируют с кислородом уже при комнатной температуре, некоторые — достаточно бурно, например, литий и кальций.
4Li + O2 = 2Li2O
2Ca + O2 = 2CaO.
При таком взаимодействии образуются оксиды. Менее активные металлы, например железо, реагируют с кислородом спокойнее, а некоторые, например, золото и серебро, платина не окисляются вовсе, благодаря чему получили определение благородных.
С хлором реагируют практически все активные металлы с выделением теплоты.
2Fe + 3Cl2 = 2FeCl3
Также выделяется теплота при реакции активных металлов с серой, но начинается она при нагревании. После начала реакции нагрев не нужен — образовавшегося тепла достаточно для поддержания реакции.
2Al + 3S = Al2S3
Внимательно изучив ряд металлов, несложно определить тип реакции при контакте с другими элементами в зависимости от места в последовательности. Также легко назвать основные характеристики металла, как химического элемента, и возможность его использования на практике.
Руководство по материалам электротехники для всех. Часть 12. Финальная
![]()
Последняя часть руководства. Внутри бонусные главы, немного новых фотографий, и главное — pdf с руководством которое можно скачать и поделиться с другом.
Доработки (доступны в pdf версии):— Добавлены фото деструкции оптического поликарбоната, добавлены фото кварцевого стекла, фото проводящих углеродных композиций в конструкции ПДУ.
— Доработан раздел с изолентами, пришлось подождать посылок, но оно того стоило — теперь это самое полное описание изоляционных лент (добавлена полиэфирная, мастичная, тканевая и другие виды лент).
— Добавлена глава про электрические соединения — с ответом на вопрос почему нельзя.
— Ну и много мелких правок согласно комментариям.Название я сменил, просто из соображений «легко запомнить-легко гуглить».
Электрические соединения
Популярная шутка говорит о том, что электротехника — это наука о контактах. И две основные неисправности — нет контакта там где он должен быть, и есть контакт там где его быть не должно.
На обложке этого руководства изображена скрутка двух проводов — медного и алюминиевого. Некоторых читателей такое зрелище возмутило, и не без оснований — так делать нельзя. Если попытаться разобраться в причинах этого «нельзя», то можно найти множество дискуссий на эту тему, практически в каждой из которых можно найти довод «всегда так делал, на даче такая скрутка работает уже 100500 лет». К сожалению, понимания причин запрета такой подход не привносит.
В чем же проблема соединить в контакт два произвольных металла? Дело в том, что в силу некоторых причин (о которых ниже) некоторые металлы образуют надежный контакт и работают практически безотказно, а некоторые образуют контакт, который тоже работает, но менее надежен и чаще приносит проблемы. Нужно понимать, что «чаще» не означает, что если вы сделали такое соединение, то оно откажет завтра с вероятностью 100%. Нет, вероятность отказа станет не 0,0001%, а к примеру 0,01%. Все такая же малая, но вас бы не устроила в 100 раз большая вероятность пожара?
Опыт эксплуатации различной техники привел инженеров к выводу, что определенные комбинации металлов обеспечивают приемлемую надежность контакта, а некоторые слишком низкую. Еще раз стоит отметить, что на надежность контакта сильно влияют условия эксплуатации, если соединение находится при постоянной температуре в сухом месте, то оно может быть вполне надежным, даже если пара металлов нежелательная.
Ряд электрохимической активности металлов
Первая причина нарушения контакта которую мы рассмотрим — электрохимическая коррозия. Некоторые из вас помнят со школы ряд активности металлов (неполный):
Li K Ba Sr Ca Na Mg Al Mn Cr Zn Fe Cd Co Ni Sn Pb H Sb Bi Cu Hg Ag Pd Pt Au
Металл Электрохимический потенциал, Вольт Литий (Li) -3,0401 Калий (K) -2,931 Барий (Ba) -2,905 Стронций (Sr) -2,899 Кальций (Ca) -2,868 Натрий (Na) -2,71 Магний (Mg) -2,372 Алюминий (Al) -1,700 Марганец (Mn) -1,185 Хром (Cr) -0,852 Цинк (Zn) -0,763 Железо (Fe) -0,441 Кадмий (Cd) -0,404 Кобальт (Co) -0,28 Никель (Ni) -0,234 Олово (Sn) -0,141 Свинец (Pb) -0,126 Водород (H) 0 Сурьма (Sb) +0,240 Висмут (Bi) +0,317 Медь (Cu) +0,338 Ртуть (Hg) +0,7973 Серебро (Ag) +0,799 Палладий (Pd) +0,98 Платина (Pt) +0,963 Золото (Au) +1,691
Для инженера этот ряд говорит следующее: В присутствии электролита (вода, влажность воздуха) в паре металлов будет разрушаться тот металл, что в ряду напряженности левее. Чем дальше друг от друга металлы в ряду, тем интенсивнее будет протекать коррозия. На базе
этого явления построена электрохимическая защита металлов, например оцинковка стали. При наличии воды, первым делом разрушается цинковое покрытие, и только после того как оно разрушилось начинается коррозия стали.В случае электрических контактов, нам важнее не то, какой металл разрушится в паре, они нужны оба, а то, насколько интенсивно будет протекать процесс коррозии. И в этом плане потенциал создаваемый парой алюминий-медь 2,038 В очень большой, его достаточно чтобы разорвать молекулу воды в процессе электролиза! Но если разделить эти два металла стальной оцинкованной пластинкой, то образуется две пары: цинк-алюминий с потенциалом 0,937 В, и цинк-медь, с потенциалом 1,101 В. Это уже не такие большие потенциалы, поэтому процесс коррозии будет протекать медленнее.
Принимая во внимание, что основными металлами для изготовления проводников являются медь и алюминий, то заучивать таблицу и считать потенциалы не требуется, важно только помнить, что непосредственно соединять медь и алюминий в электрический контакт работающий на воздухе нельзя.
Тепловое расширение
Все тела при нагревании расширяются, и металлы не исключение. Для любого материала есть характеристика, такая как «коэффициент теплового расширения тел», который показывает, во сколько раз увеличится размер тела, при нагреве на 1 градус Цельсия. (В различных диапазонах температур значение теплового коэффициента расширения может различаться, кроме того для некоторых анизотропных материалов коэффициент может различаться в разных плоскостях. Для упрощения не будем учитывать эту разницу, воспользовавшись усредненными значениями) Вот небольшая табличка:
Материал Тепловой коэффициент расширения α, (1/К) Алюминий Медь Сталь Стекло Стекло термостойкое (боросиликатное) Стекло кварцевое Инвар (сплав) Платина
Из этой таблички видно, что соединение из двух материалов при нагревании будет расширяться по разному, провоцируя внутренние напряжения и деформации. Иногда это полезное свойство — оно используется в биметаллических пластинках в терморегуляторах, такие пластинки при нагреве изгибаются и разрывают контакт. Но в деле создания надежного электрического соединения такая разница в величине теплового расширения может ослабить контакт. Если соединение не обладает упругими свойствами, то спустя нескольких циклов нагрева и охлаждения, можно обнаружить что вместо плотного тугого контакта проводник болтается.Если соединения разных материалов не избежать, то нужно помнить, что такое соединение потенциально может ослабнуть при изменениях температуры, и должно быть обслуживаемым и контролируемым. Замуровать соединение медного и алюминиевого проводника в стенке под слоем штукатурки — плохая идея.
Ползучесть
Некоторые материалы склонны проявлять явление «ползучести», когда к примеру проводник под небольшой механической нагрузкой, не достаточной для пластической деформации, тем не менее деформируется со временем. Величина этого явления зависит от нагрузки и от температуры, характеризуясь очень малой величиной. Пройдут тысячи часов, прежде чем размер тела изменится на доли процента. Тем не менее это явление достаточно важно в обеспечении надежного контакта. Ползучесть, наряду с тепловым расширением вносит вклад в то, что затянутая клемма спустя годы ослабевает и провод в ней болтается.
К сожалению алюминий (чистый) обладает значительно более интенсивной ползучестью, чем медь, что делает электрические контакты с его участием менее надежными и требующими регулярного обслуживания. Это стоит помнить при ремонте и обслуживании проводки из алюминиевого кабеля времен СССР. Производители современных алюминиевых кабелей легируют алюминий в токопроводящей жиле, добиваясь уменьшения ползучести до значений, сопоставимых с медью, пускай и ценой небольшого снижения электропроводности.
Так как же все-таки соединять провода?
Вопрос сложный тем, что ответ зависит от условий работы соединения и однозначно универсального способа нет.
Но про пару алюминий-медь было сказано столько плохого, что я просто обязан дать ответ на вопрос «как их соединять?».
Первый вариант — классический, при помощи стальной пластинки исключая непосредственный контакт меди и алюминия. Стальная пластинка предотвратит интенсивную электрохимическую коррозию (но не избавит от нее совсем), обеспечит приемлемое усилие на площади контакта проводников. Но такое соединение требует регламентных работ по обслуживанию: 1–2 раза в год необходимо проверять усилие затяжки проводников.
Второй вариант. Специализированные пружинные клеммы для алюминиевого проводника. (например клеммники WAGO серии 2273 с пастой). В такой клемме зачищенный проводник всё время прижимается пружинным контактом, предотвращая его ослабление вследствие ползучести.
Паста внутри клеммника предотвращает доступ влаги и воздуха к поверхности алюминия, препятствуя окислению проводника. (Важно отметить, клеммы должны быть качественные, а сечение проводника номинальным. Самолично наблюдал сгоревшие соединения выполненные клеммами, купленными в ближайшем киоске (вероятно поддельными).)Третий вариант — Медно-алюминиевые гильзы. Этот вид соединения актуален для силовых линий на большие токи с сечением от 10 кв. мм. Медно-алюминиевые гильзы предназначены под опрессовку специальным инструментом. Соединенные в толще металлы обеспечивают надежный контакт большой площади, влага и электрохимическая коррозия могут лишь повредить нежную поверхность гильзы, не нарушив контакт в толще.
И помните, любое силовое электрическое соединение (тем более из разных металлов) должно быть доступно для обслуживания! Замурованная в стену скрутка — залог того, что вас будет вспоминать ремонтная бригада в различных матерных выражениях.
Заключение
Так как установка при написании данного пособия была на минимум брехни, я писал о том, что сам пощупал, использовал, с чем работал. Некоторые темы я не раскрыл, в силу малого опыта (или малого количества собранного материала) в этих областях, но их стоило бы раскрыть. Переписывать бездумно то, что описано в специализированной литературе я не стал, зачем искажать источник? Поэтому, если вы можете что-то рассказать по теме — я буду рад включить ваш текст в руководство.
Данное руководство распространяется свободно, вы можете скачать самую последнюю вер-
сию у меня в блоге совершенно бесплатно. Если вам понравилась моя работа, я буду рад услышать от вас пожелания и предложения, а также замечания и указания на допущенные ошибки.Где скачать?
→ Руководство на GitHub вместе с исходником текста и фотографиями. Там же pdf с книгой.
→ Домашняя страничка руководства на моем сайте.
Если вы захотите бумажный экземпляр к себе на полку, то его можно приобрести (технология печати по требованию). Это не реклама — я выставил руководство по себестоимости — не заработаю ни копейки. К сожалению в бумажном виде иллюстрации будут черно-белые.
Благодарности
Выражаю признательность Алексею Gall Галахову за ценные дополнения руководства и помощь в верстке руководства.
Talion_amur за предоставленный образец ртутного счетчика времени наработки.
Спасибо всем кто написал комментарии, они дали ценную обратную связь.
Пользуясь случаем хочу передать привет Meklon DIHALT Milfgard lozga superhimik tnenergy BarsMonster — я с удовольствием читаю ваши посты и старался держать планку не ниже.
Ссылки на части руководства:
1: Проводники: Серебро, Медь, Алюминий.
2: Проводники: Железо, Золото, Никель, Вольфрам, Ртуть.
3: Проводники: Углерод, нихромы, термостабильные сплавы, припои, прозрачные проводники.
4: Неорганические диэлектрики: Фарфор, стекло, слюда, керамики, асбест, элегаз и вода.
5: Органические полусинтетические диэлектрики: Бумага, щелк, парафин, масло и дерево.
6: Синтетические диэлектрики на базе фенолформальдегидных смол: карболит (бакелит), гетинакс, текстолит.
7: Диэлектрики: Стеклотекстолит (FR-4), лакоткань, резина и эбонит.
8: Пластики: полиэтилен, полипропилен и полистирол.
9: Пластики: политетрафторэтилен, поливинилхлорид, полиэтилентерефталат и силиконы.
10: Пластики: полиамиды, полиимиды, полиметилметакрилат и поликарбонат. История использования пластиков.
11: Изоляционные ленты и трубки.Так получилось, что у меня параллельно собирается материалы по нескольким темам, какая тема интереснее?
Читайте также: