Какие металлы могут вытеснить медь из растворов ее солей
Обновлено: 17.05.2024
Общая характеристика переходных элементов-металлов
К переходным элементам относятся такие, которые расположены в побочных подгруппах больших периодов периодической системы Д.И. Менделеева. К ним принадлежат d– и f–элементы. Название «переходные» связано с тем, что переходные элементы расположены между s– и р–элементами.
Мы рассмотрим три металла: железо, хром и медь.
Железо — металл VIIIB-группы четвёртого периода. Его особенностью, как и особенностью других переходных металлов, является наличие валентных электронов как на внешнем (4s), так и на предвнешнем (3d) подуровнях.
Хром — металл VIB-группы четвёртого периода. Как и железо, это d-элемент, у которого валентные электроны находятся и на внешнем слое и на предвнешнем подуровне. Помимо этого, в атоме хрома в основном состоянии происходит провал электрона.
Железо и хром имеют идентичный набор степеней окисления, а также возможных оксидов и гидроксидов: 0, +2, +3, +6.
Медь — металл IB-группы четвёртого периода. Как и в случае других элементов побочных подгрупп, особенностью для неё является наличие валентных электронов как на внешнем (4s), так и на предвнешнем (3d) подуровнях. Как и у хрома, у меди в электронной конфигурации наблюдается провал электрона.
Степени окисления меди следующие:
- низшая степень окисления равна 0, как и у всех металлов;
- высшая равна +2;
- промежуточная равна +1.
Физические свойства
По физическим свойствам железо и хром — совершенно типичные металлы серебристо-белого цвета, которые не растворяются в воде, а на воздухе покрываются прочной оксидной плёнкой.
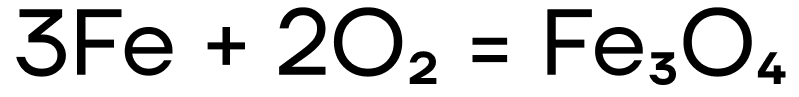
Особенностью железа является его быстрая коррозия (то есть окисление) кислородом во влажном воздухе, а особенностью хрома — высокая твёрдость: он является одним из самых твёрдых металлов.
Медь же — металл красного цвета, один из четырёх металлов, имеющих явную цветовую окраску, которая отлична от серой или серебристой.
Способы получения
Основным способом получения меди, хрома и железа является пирометаллургия, то есть различные реакции, происходящие при высоких температурах.
Химические свойства
- Взаимодействие с простыми веществами
Как и другие металлы, железо и хром способны взаимодействовать со своими противоположностями, неметаллами, с образованием различных бинарных соединений.
При этом неметаллы, являющиеся сильными окислителями, окисляют железо и хром до +3, а неметаллы, являющиеся слабыми окислителями, — только до +2.
Железо и хром не реагируют с водородом и азотом ввиду неактивности последних. При взаимодействии с кислородом железо ржавеет: образуется смесь оксидов железа, то есть железная окалина Fe3O4.
Медь способна также окисляться до разных степеней окисления в зависимости от силы окислителя или его избытка/недостатка.
Железо и хром являются металлами, стоящими в ряду активности до водорода, поэтому они могут вытеснять его из воды с образованием оксидов и вытесненного водорода.
Так как это металлы средней активности (стоящие в промежутке от алюминия до водорода) они реагируют с водой не при нормальных условиях, а при очень высокой температуре.
При взаимодействии с водой железо ржавеет: образуется железная окалина Fe3O4, как и в случае с кислородом.

Медь же находится в ряду активности после водорода, следовательно, она “слабее” водорода и не способна вытеснить такого сильного соперника.
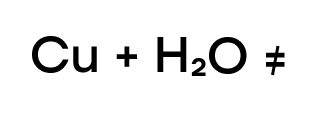
- Реакция с кислотами-неокислителями
Благодаря нахождению железа и хрома до водорода в ряду активности металлов они также способны вытеснять водород из растворов кислот-неокислителей.
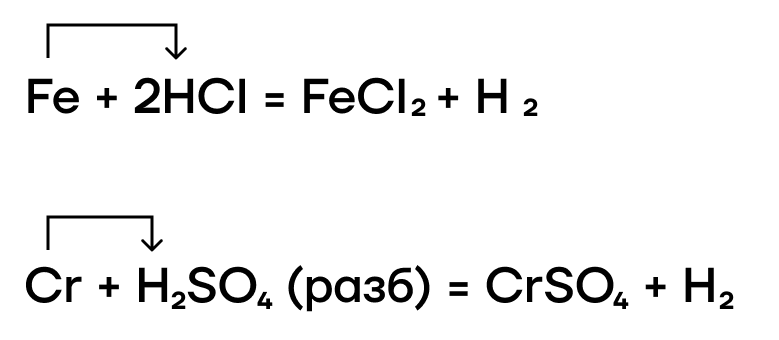
Так же, как и в случае с водой, медь не может вытеснить “качка”-водорода из таких кислот.
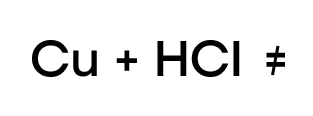
Как и прочие металлы, железо, хром и медь могут вытеснять менее активные металлы из растворов их солей.
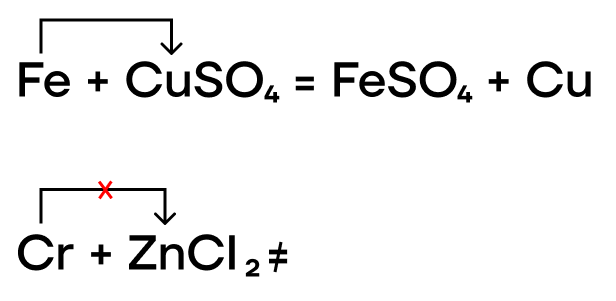
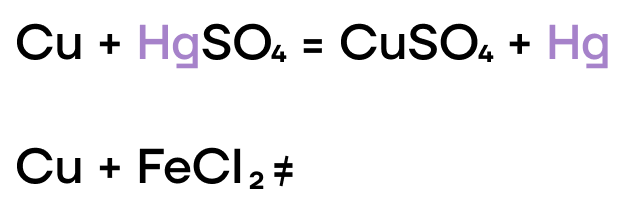
Из-за низких значений электроотрицательности, железо, хром и медь являются типичными восстановителями, а следовательно, способны реагировать с окислителями.
Ниже представлены различные способы повышения степеней окисления железа и хрома и основные реагенты, которые используются.
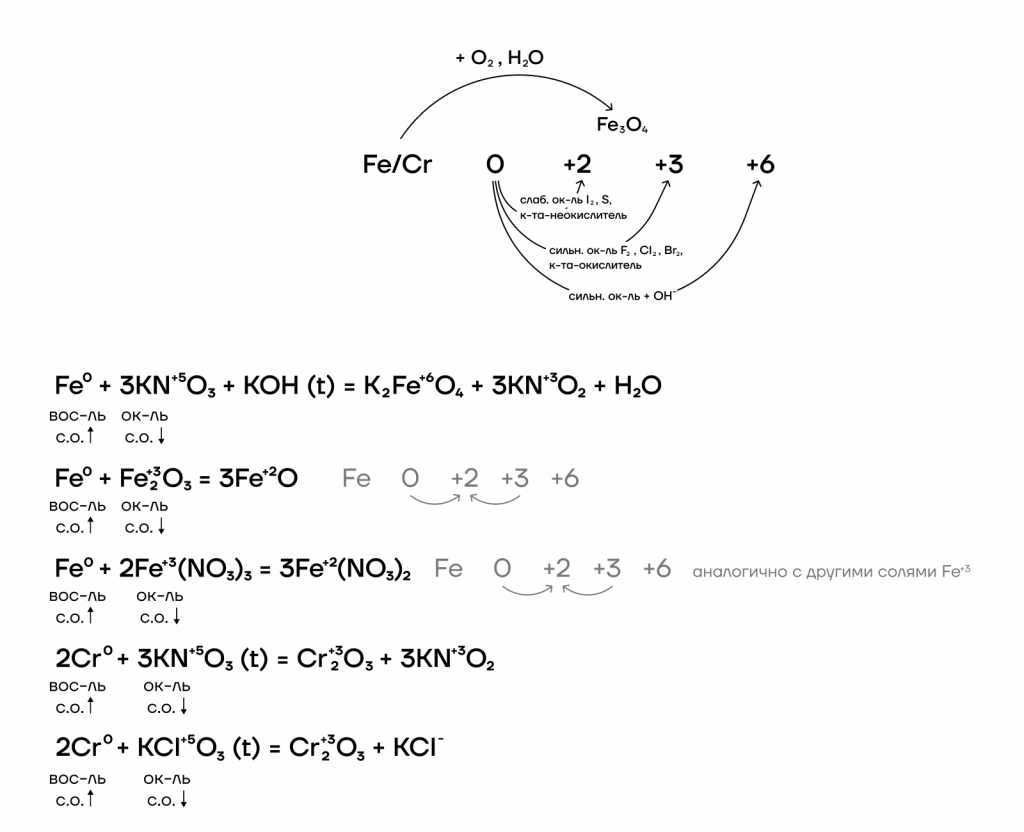
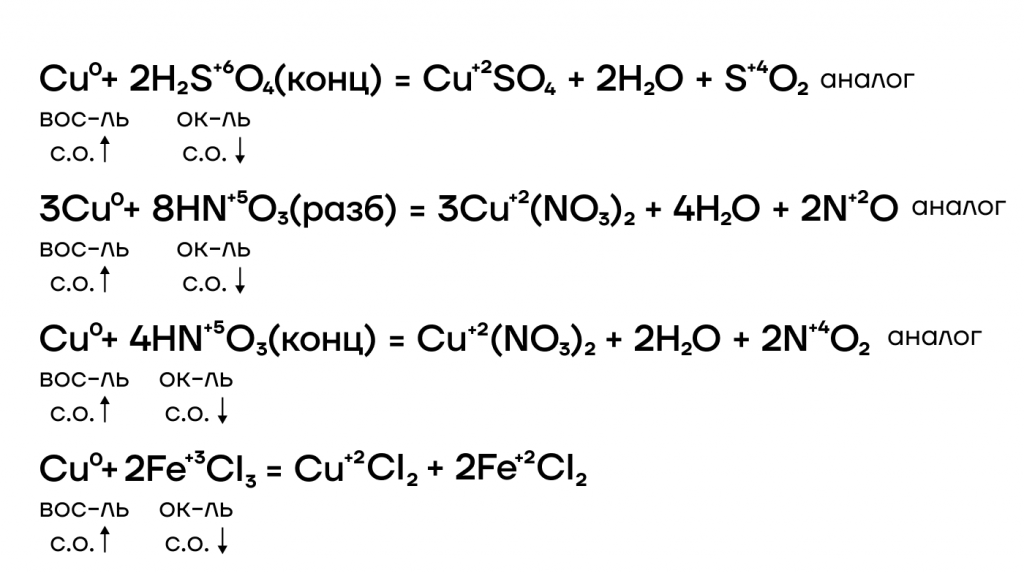
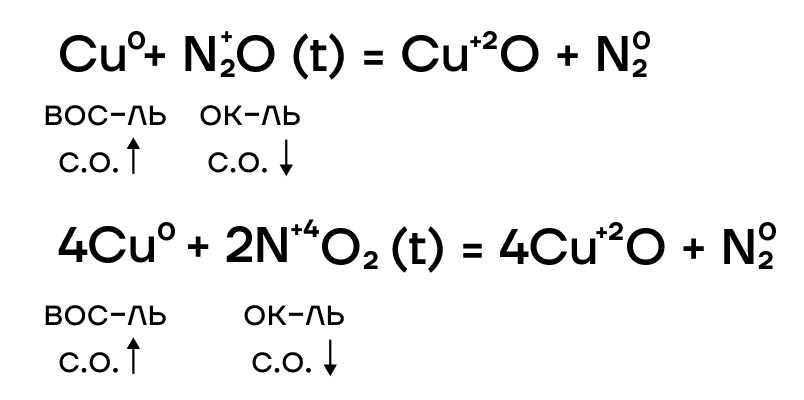
Фактчек
- Медь, железо и хром относятся к переходным металлам, то есть таким, которые расположены в побочных подгруппах больших периодов;
- Возможные степени окисления железа и хрома: 0, +2, +3, +6. Возможные степени окисления меди: 0, +1, +2.
Проверь себя
Задание 1.
У атома какого химического элемента не наблюдается «проскок» электрона?
Задание 2.
С какой солью будет реагировать медь?
- Хлорид натрия;
- Сульфат ртути(II);
- Хлорид железа(III);
- Фосфат кальция.
Задание 3.
Для какого металла характерна степень окисления +1?
Ответы: 1. — 3; 2. — 2; 3. — 4
Какие металлы могут вытеснить медь из растворов её солей?
Какие металлы могут вытеснить медь из растворов её солей.

Li, K, Ba, Ca, Na, Mg, Al, Mn, Zn, Cr, Fe, Co, Sn, Pb.
Все это можно узнать из электрического ряда напряжения металов.

Срочно помогите пожалуйста Какие из перечисленных металлов могут быть вытеснены из растворов их солей хромом?
Срочно помогите пожалуйста Какие из перечисленных металлов могут быть вытеснены из растворов их солей хромом?

Какая масса меди может быть вытеснена избытком магния из раствора хлорида меди (П) массой 268 г с массовой долей соли 10%?
Какая масса меди может быть вытеснена избытком магния из раствора хлорида меди (П) массой 268 г с массовой долей соли 10%?

Металл вытесняет из растворов солей другие (?
Металл вытесняет из растворов солей другие (.
), находящееся в ряду активности металлов (.
)его, а сам может быть вытеснен из растворов солей металлами, расположенными(.

Укажите, какими металлами может быть вытеснено серебро(Ag) из раствора соли?
Укажите, какими металлами может быть вытеснено серебро(Ag) из раствора соли?

Какие металлы получают электролизом раствора соли?
Какие металлы получают электролизом раствора соли?
Рассмотрите электролиз раствора сульфата меди(2).
Каким ещё способом можно получить медь?
Даны металлы : цинк, медь, железо - и растворы их солей?
Даны металлы : цинк, медь, железо - и растворы их солей.
Напишите уравнение осуществимых реакций между металлами и их солями.
ПОМОГИТЕ?
Определите какие металлы могут быть замещены медью в растворах солей.
Напишите уравнения таких реакций замещения.

Свинец из раствора его соли можно вытеснить каждым из двух металлов : 1) калий и алюминий, 2) барий и магний, 3) цинк и железо, 4) медь и олово?
Свинец из раствора его соли можно вытеснить каждым из двух металлов : 1) калий и алюминий, 2) барий и магний, 3) цинк и железо, 4) медь и олово.
Олово из раствора его соли можно вытеснить 1) Литий?
Олово из раствора его соли можно вытеснить 1) Литий.
Олово из раствора его соли можно вытеснить 1?
Олово из раствора его соли можно вытеснить 1.
Вопрос Какие металлы могут вытеснить медь из растворов её солей?, расположенный на этой странице сайта, относится к категории Химия и соответствует программе для 10 - 11 классов. Если ответ не удовлетворяет в полной мере, найдите с помощью автоматического поиска похожие вопросы, из этой же категории, или сформулируйте вопрос по-своему. Для этого ключевые фразы введите в строку поиска, нажав на кнопку, расположенную вверху страницы. Воспользуйтесь также подсказками посетителей, оставившими комментарии под вопросом.
Я про алюминийАлюминий – легкий, прочный и пластичный металл. Это один из самых востребованных металлов, и по темпам роста потребления он давно и с большим отрывом оставил позади сталь, никель, медь и цинк. Алюминий без преувеличений можно назвать ..
Тому що рН показує ступінь концентрації катіонів гідрогену у воді, що є дуже важливим для косметики.

1. дано N(NH3) = 4. 816 * 10 ^ 23 - - - - - - - - - - - - - - - - - - - - - - - - - - - - - V(NH3) - ? N(NH3) / N(A) = V(NH3) / Vm V(NH3) = N(NH3) * Vm / N(A) = 4. 816 * 10 ^ 23 * 22. 4 / 6. 02 * 10 ^ 23 = 15. 58 L ответ 15. 58 л 2) дано m(O2)..
Соотвественно правильным ответом будет являться : 4) KCl ; 5) AgCl ; 6) NH4Cl.
Дано W(O) = 47 % - - - - - - - - - - - - - - - - E - ? Е - это неизвестный элемент W(O) = Ar(O) * n / M(X2O3) * 100% 47% = 16 * 3 / 2x + 48 * 100% 94x + 2256 = 4800 X = 27 - это алюминий Al2O3 ответ алюминий.

Напиши нормально не понятно или сфоткай.

В SO3 32 / (32 + 3 * 16) = 0, 4 или 40 %.
Реакции есть на фотографии.
4HCl + MnO2 = MnCl2 + Cl2 + 2H2O соляная кислота отдаёт в свободном виде половину имеющегося хлора. M(Cl общ. ) = 1000 * 0, 365 * 0, 9726 = 355 г масса выделившегося хлора = 355 / 2 = 177, 5 г.
Типы химической реакции соединение, разложение замещение.
© 2000-2022. При полном или частичном использовании материалов ссылка обязательна. 16+
Сайт защищён технологией reCAPTCHA, к которой применяются Политика конфиденциальности и Условия использования от Google.
Медь из раствора сульфата меди (II) вытесняет все металлы ряда 1) Na, Cr, Zn 2) K, Fe, Cu 3) Fe, Zn, Al 4) Zn, Fe, Au?
Медь из раствора сульфата меди (II) вытесняет все металлы ряда 1) Na, Cr, Zn 2) K, Fe, Cu 3) Fe, Zn, Al 4) Zn, Fe, Au.
Медь из раствора сульфата меди (II) вытесняет все металлы , стоящие в ряду напряжений до меди, но начиная с магния, металлы которые активнее магния будут реагировать с водой, образуя щелочи.
Металлические свойства возрастают в ряду : 1) Zn - Mg - Na 2) Rb - Ca - Fe 3) Na - Mg - Al 4) K - Ca - Fe?
Металлические свойства возрастают в ряду : 1) Zn - Mg - Na 2) Rb - Ca - Fe 3) Na - Mg - Al 4) K - Ca - Fe.
Zn - ZnO - Zn(NO3)2 - Zn(OH)2 - ZnO - ZnFe - FeO - FeSO4 - Fe(OH) 2 - Fe(No3) 2Написать реакции цепочек?
Zn - ZnO - Zn(NO3)2 - Zn(OH)2 - ZnO - Zn
Fe - FeO - FeSO4 - Fe(OH) 2 - Fe(No3) 2
Написать реакции цепочек.
Назовите металл, который не может вытеснять медь из ее раствора : 1)Hg?
Назовите металл, который не может вытеснять медь из ее раствора : 1)Hg.
Какие элементы будут вытеснять марганец из раствора солей : K, Fe, Zn, Al, Ni?
Какие элементы будут вытеснять марганец из раствора солей : K, Fe, Zn, Al, Ni.
1. Металл, способный вытеснить водород из раствора кислоты : Ca Ag Hg ?
1. Металл, способный вытеснить водород из раствора кислоты : Ca Ag Hg ?
2. Из раствора соли сульфата меди2, медь не вытесняют : Zn Ca Fe Na Ag ?
3. Растворится ли образец смеси металлов Fe, Ag, Zn в растворе : H2SO4, KOH.
В паре Me - Fe быстрее разрушается Fe a) Fe - Zn b) Fe - Cu c) Fe - Cr d) Fe - Mg Желательно с объяснением : )?
В паре Me - Fe быстрее разрушается Fe a) Fe - Zn b) Fe - Cu c) Fe - Cr d) Fe - Mg Желательно с объяснением : ).
Випишете металлы из таблицы например Cu, Zn, Fe?
Випишете металлы из таблицы например Cu, Zn, Fe.
ПомооооооооооооогиииииииИИИИИИИИИИИТТТТТТТТТТТТТЕЕЕЕЕЕЕЕЕЕЕЕ?
В результате взаимодействия каких веществ с водой получится щелочь?
Na Zn CaH2 K K2O Fe MexOy + H2O→щелочь.
С какими металлами может быть Me?
Na Fe K Al Ca Zn Cu.
D - элементы Fe, Cr , Cu или ZN?
D - элементы Fe, Cr , Cu или ZN.
Следующие пары металлов, находящиеся в тесном контакте, погружены в раствор соляной кислоты?
Следующие пары металлов, находящиеся в тесном контакте, погружены в раствор соляной кислоты.
Укажите пару, где железо не будет разрушаться и почему : Fe / Cu, Fe / Al, Fe / Zn, Fe / Mg.
На странице вопроса Медь из раствора сульфата меди (II) вытесняет все металлы ряда 1) Na, Cr, Zn 2) K, Fe, Cu 3) Fe, Zn, Al 4) Zn, Fe, Au? из категории Химия вы найдете ответ для уровня учащихся 10 - 11 классов. Если полученный ответ не устраивает и нужно расшить круг поиска, используйте удобную поисковую систему сайта. Можно также ознакомиться с похожими вопросами и ответами других пользователей в этой же категории или создать новый вопрос. Возможно, вам будет полезной информация, оставленная пользователями в комментариях, где можно обсудить тему с помощью обратной связи.
Какие металлы могут вытеснить железо из растворов солей, а какие не могут?
Какие металлы могут вытеснить железо из растворов солей, а какие не могут?
Металлы, которые находятся слева в ряду активности, вытесняют металлы, которые находятся справа из растворров их солей.
След - но, все металлы, которые находятся слева, вытесняют железо.
НО! для реакций нельзя брать активные металлы, потому что они будут реагировать и с водой.
Zn + FeCl2 = ZnCl2 + Fe.
Приведите 2 примера к схеме соль + металл = новая соль + металл?
Приведите 2 примера к схеме соль + металл = новая соль + металл.
Какие вещества могут образовывать аллотропные видоизменения?
Какие вещества могут образовывать аллотропные видоизменения?
Приведите примеры где применяться.
Какие металлы могут быть вытеснены медь?
Какие металлы могут быть вытеснены медь.
Из водных растворов солей kcl, agno3, Hg(NO3)2, NiSo?
Записать уравнения протекающих реакций.
Омогите ответить : Какой из Ме - медь, цинк или ртуть могут вытеснить свинец из раствора его соли?
Омогите ответить : Какой из Ме - медь, цинк или ртуть могут вытеснить свинец из раствора его соли?
Ответ подтвердите уравнением реакции.
Какие вещества могут быть получены при взаимодействии кислоты с солью, кислоты с основанием, соли с солью?
Какие вещества могут быть получены при взаимодействии кислоты с солью, кислоты с основанием, соли с солью?
Приведите пример уравнения соответствующих реакций.
Какие кислоты могут образовывать кислые соли?
Какие кислоты могут образовывать кислые соли?
Приведите примеры кислых солей кислородсодержащих и бескислородных кислот.
Какие металлы не способны вытеснить серебро из раствора нитрата серебра?
Какие металлы не способны вытеснить серебро из раствора нитрата серебра.
2. Какие металлы могут быть замещены медью в растворах их солей?
2. Какие металлы могут быть замещены медью в растворах их солей?
Приведите два примера.
С какими металлами реагирует раствор кислоты и как?
С какими металлами реагирует раствор кислоты и как?
С какими металлами реагирует раствор солей и как?
Вы находитесь на странице вопроса Какие металлы могут вытеснить железо из растворов солей, а какие не могут? из категории Химия. Уровень сложности вопроса рассчитан на учащихся 5 - 9 классов. На странице можно узнать правильный ответ, сверить его со своим вариантом и обсудить возможные версии с другими пользователями сайта посредством обратной связи. Если ответ вызывает сомнения или покажется вам неполным, для проверки найдите ответы на аналогичные вопросы по теме в этой же категории, или создайте новый вопрос, используя ключевые слова: введите вопрос в поисковую строку, нажав кнопку в верхней части страницы.
Читайте также:
