Какие металлы можно расплавить на ладони
Обновлено: 04.10.2024
Плавится в руках металл галлий при температуре +29,8. А еще читала где -то, что индий-галлиевая эвтектика плавится при температуре +11.
Из металлов это галлий с температурой плавления +29,8 С и цезий с температурой плавления +28,5 С. Цезий из-за высокой химической активности плавят руками внутри ампулы с инертным газом.
Геродот и некоторые другие авторы древности писали о том, что первые монеты были отчеканены в малоазийском государстве Лидии. В наше время точно установлено, что древнейшие монеты появились именно там около 685 год до н. э. , при царе Ардисе. 2. Хорошая сохранность, высокая известность и принимаемость в любой точке гос-ва. Это было связанно с "узнаваемым" рисунком на монерте.
Это раньше оставляли зазоры и путь назывался звеньевым. Сейчас же все больше используется именно бесстыковой путь. Хотя и на бесстыковом пути могут встречаться стыковые зазоры - это в случае эксплуатации уравнительных пролетов, которые обеспечивают возможность снятия излишних напряжений. Уже давно практикуется сварка плетей длиной в перегон между станциями, в этом случае в рельсах нет никаких стыков, а возможность использования светофорной сигнализации обеспечивается ввариванием высокопрочных изостыков.
Конкретно насчет металла не подскажу, просто знаю, что раньше распределительные щиты изготавливали по ГОСТ 10985-80. (довольно объёмный документ, регламентировавший и тип материалов в том числе).
Сейчас производители "подсели" на ТУ 3431-001-18461115-2003.
P.S. Конечно, кому было в 2003г. новым ГОСТом заниматься?
В 2017 году, больше всего меди в мире добывалось в в Чили - 34% от мировой добычи меди. В США добывалось 9,1% от мировой добычи. В Перу -9%, в Австралии -6% и в России - 5% от мировой добычи меди.
Именно в Чили находится около 20% разведанных запасов меди в мире, в США находится 12,7% от разведанных мировых запасов. А по выплавке меди в 2017 году места распределились следующим образом: Чили, Китай, Перу, США, Австралия, Конго, Россия, Замбия, Канада. В Чили было выплавлено столько меди, сколько в Китае, Перу и США вместе взятых.
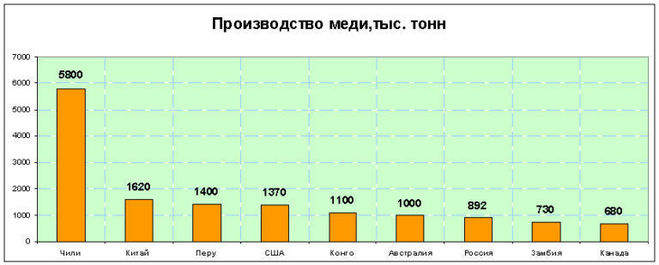
Это на фото карьер "Эскондида" в Чили, один из крупнейших в мире.

Химический элемент (металл) тантал был назван в честь героя древнегреческих мифов Тантала. Открытый А. Г. Экбергом в 1802 году новый химический элемент (металл) по свойствам почти полностью совпадал с танталом. Но это был другой элемент. А в 1844 г. из-за невероятной схожести нового элемента по свойствам с титаном, и чтобы отличить его от титана, немецкий химик Генрих Розе переименовал его в Ниобий, в дочери Титака – Ниобы.
Ниобий (Nb) это металл светло-серого цвета, относится к категории редких элементов и является компонентом тугоплавких сплавов. Втаблице Менделеева занимает 41 место.
12 физ. и хим. характеристик металла, что плавится в руках
Металл который плавится в руке: понятие легкоплавкости + характеристика галлия + разбор термодинамических свойств химического элемента + физические/химические свойства металла + его область применения.

Многие из нас видели в интернете фото металла, который плавится в руке. Единственный химический элемент в природе, который может безопасно для здоровья человека, провернуть подобный трюк – галлий.
В сегодняшней статье мы разберем отличительные свойства группы легкоплавких металлов + предоставим характеристику элемента, тающего в руках его владельца.
Понятие легкоплавких металлов/сплавов
Легкоплавкость – понятие растяжимое, особенно это актуально для промышленности. В химии легкоплавкими считаются элементы группы металлов + их сплавы, температура плавления которых ниже порога в 1000 градусов Цельсия.

Если температура плавления металла превышает 1 500 градусов Цельсия – его принято выделять в группу тугоплавких. Диаграмма выше четко дает понять, куда какой металл следует относить.
Обратите внимание: минимальная температура плавления у ртути — 39 градусов. Именно благодаря такому физическому свойству, мы можем наблюдать химический элемент в постоянно жидком состоянии.
Теперь пройдемся по легкоплавким сплавам. В своем большинстве – это сплавы эвтектического типа, пиковая температура плавления которых не превышает 232 градусов по Цельсию. В основе производства легкоплавких сплавов лежат легкоплавкие металлы – олово, висмут, таллий, галлий и другие.

Ученым удалось добиться -78 градусов в качестве минимальной температуры плавления для советского сплава, который состоит на 12% из натрия, 47% калия и 41% цезия. Недостаток сплава — реакция с водой. Ближайший конкурент – амальгама. Токсичный сплав из ртути с таллием, сохраняющий жидкое состояние до температуры -61 градус по Цельсию.
Область применения легкоплавких металлов/сплавов:
- энергетическая промышленность и машиностроение. Основное направление – создание тепловых носителей с жидкометаллического типа;
- литьевая промышленность;
- как основа для датчиков температуры, что актуально в системах пожарной безопасности;
- как основа для разработки термометров;
- как ремонтный материал в вакуумных технологиях;
- припои, предохранители и прочие мелочи в микроэлектронике;
- медицинское направление. То же протезирование;
- как металлическая смазка.
Низкая температура плавления является базовых свойством, которое требуется от легкоплавких металлов и сплавов. Вторичные параметры, которые берутся во внимание в различных областях использования – плотность, прочность на разрыв и инертность в химическом плане.
Галлий: металл, который плавится в руках
Поистине, занимательный химический элемент, который имеется в любом школьном кабинете химии. Благодаря демонстрационной наглядности, галлий считается лучшим вариантом донесения до умов учащихся тепловых свойств химических элементов.

Gallium (Ga) – металл, который плавится в руках при достижении температуры в 29.8 градуса по Цельсию . Учитывая стандартные 36.6 в организме человека, чтобы получить желаемый эффект, достаточно кусочек галлия положить на ладошку и наблюдать как тот медленно по ней растекается в разные стороны.
1) Общая информация по элементу
В периодической системе химических элементов галлий находится на 31 позиции. Его латинское обозначение – «Ga». Металл принадлежит к группе легких металлов, куда также входит алюминий, индий, олово, таллий, свинец и висмут.

Внешне, галлий представляет собой мягкий или хрупкий металл (в зависимости от температуры), имеющий белый + серебристый оттенки. Иногда можно заметить синеватые отблески на поверхности чистого вещества.

Великий Менделеев заранее знал о данном химическом элементе. Впервые он просчитал некоторые свойства галлия еще в 1871 году. Изначальное название, присвоенное химиком, звучало как «экаалюминий».
К предугаданным свойствам галлия Менделеевым относились:
- оксидный тип;
- варианты связи с хлором;
- медленная растворимость при соприкасании с щелочами/кислотами;
- галлий не будет реагировать с кислородом;
- возможность легкоплавкого металла образовывать основные соли;
- химический элемент будет открыт при использовании спектроскопии.
Непосредственное выделение металла в чистом виде пришлось на француза Буабодраном. Открытие приходится на 1875 год. Из-за малого долевого содержания галлия в руде (менее 0.2%), пришлось потратить пару месяцев на получение минимального запаса чистого вещества для полноценного исследования его физических/химических свойств.
| Физика галлия | Химия галлия |
|---|---|
| Наличие нескольких модификаций полиморфного типа. | Низкая химическая активность замедляет протекание химических реакций металла в твердом состоянии. |
| При нормальных условиях кристаллическая решетка имеет орторомбическую структуру. При повышении давления наблюдается образование 2 структур полиморфного типа с кубической и тетрагональной решетками. | На воздухе галлий покрывается оксидной пленкой, которая предохраняет его от дальнейших реакций окисления. |
| Плотность галлия – 5.9 грамма на сантиметр кубический, а в жидком состоянии плотность увеличивается до 6.1 грамма на сантиметр кубический. | В контакте с горячей водой, он вытесняет из нее водород, в результате чего образуется гидроксид галлия. |
| Сопротивление электричеству у галлия в твердом и жидком состояниях одинаковы и равны 0.5 на 10-8 Ом*см при температурном режиме в 0 градусов по Цельсию. | Вступает в реакцию с паром (выше 340 градусов) и образует метагаллиевую кислоту. |
| Вязкость галлия колеблется в зависимости от температурного режима. При температуре в 100 градусов – 1.6 сантипуаз, а при 1000 градусов С – 0.6 сантипуаз. | Может взаимодействовать с кислотами минерального типа – происходит выделение Н и образование солевых веществ. |
| Поверхностное натяжение составляет 0.74 ньютона на метр, а отражательный коэффициент от 71% до 76% при разной длине волн. | Галлий инертен по отношению к водороду, азоту, углероду и кремнию. |
В земной коре металл, который плавится в руках, встречается довольно часто. На 1 тонну земли приходится 19 грамм чистого вещества. В химическом аспекте, галлий – элемент рассеянного типа, располагающий двойной природой по геохимии. Хотя кларки вещества и большие, из-за его сильной склонности к изоморфизму, больших скоплений чистого галлия в природе не найти.

К основным минералам, где сравнительно высокое содержание галлия в чистом виде относят сфалерит (до 0.1%), биотит (до 0.1%) и натролит (до 0.1%). В остальных 10+ минералах, которые также применяются для добычи галлия, долевое содержание чистого вещества менее 0.1%. В морской воде галлий также присутствует, но его содержание крайне мало – всего 30 на 10-6 миллиграммов на литр жидкости.
2) Почему галлий – это металл, который плавится в руке?
Обратимся к тепловым свойствам металла, и полностью разберем их при различных уровнях, хотя ответ на вопрос очевиден уже из базового понятия, температуры плавления, которая приравнивается к 29 градусам по Цельсию.
Термодинамические свойства чистого галлия:
- металл переходит из твердого в жидкое состояние при достижении температуры в 29.8 С или 302 градуса Кельвина;
- металл закипает при достижении температуры в 2 448 градусов Кельвина;
- удельная теплота плавления чистого галлия составляет 5600 Джоулей на моль;
- удельная теплота по испарению составляет 270 000 джоулей на моль;
- молярная теплоемкость составляет 26 джоулей, деленных на Кельвины, перемноженные на моли.
Главными поставщиками галлия на мировой рынок являются государства из Юго-Запада Африки, Российская Федерация и большинство стран СНГ. Галлий – металл, который не только плавится в руке, но и вещество, способное менять плотность при смене температурного режима на основании данного свойства можно провести интересный опыт.

Эксперимент: переводим галлий в жидкое состояние, а далее загоняем его в маленький стеклянный пузырек. По мере охлаждения емкости, металл станет постепенно превращаться в твердую субстанцию. Постепенно образующиеся кристаллы начнут расширяться, за счет чего колба рано или поздно треснет.
Во избежание повреждений со стороны зрителей, демонстрация должна проходить в изолированном пространстве с защитной перегородкой. Если слишком резко переохладить колбу, осколки могут разлететься в разные стороны в радиусе нескольких десятков метров.
Обзор свойств и характеристик плавящегося в руке металла, галлия:
3) Получение галлия + области применения металла в промышленности/быту
В основе добычи чистого вещества лежит галлит – редкий минерал, который является смесью галлия и сульфида меди. Наиболее часто он встречается в совокупности с такими минералами как сфалерит и германит. Странный факт, но в залежах каменных углей иногда реально найти галлит в размере 1.5% от всего объема добычи, что делает такие месторождения крайне важными стратегическими запасами для промышленного производства галлия.
Основные методы получения металлического галлия – это переработка боксита, нефелина и некоторые типы полиметаллических руд/угля.
Алгоритм извлечения галлия из руд:
- Электролиз с участием щелочных жидкостей, которые в свою очередь являются промежуточным продуктом с переработки бокситов в глинозем технического применения.
- Получение концентрированных растворов по методу спекания или через процесс Байера. В первом случае получаем до 70 миллиграмм на литр, а во втором до 160 миллиграмм на литр концентрата.
- Дальнейшая очистка галлия путем карбонизации.
- Обогащенный осадок отправляют в емкость с известью, вследствие чего получаем раствор.
- При помощи электролиза раствора получаем черновой вариант металла.
- Черновой галлий прогоняют через водяной напор.
- Смесь фильтруют при помощи пористых пластинок и греют в вакууме, из-за чего из чернового металла удаляются примеси летучего типа.
- В зависимости от степени чистоты конечного продукта, используют химический, электрохимический, либо физический методы разложения.
Эталонный вариант чистки может предоставить галлий с чистотой в 99.9%. В данном случае используется метод электрохимического рафинирования и восстановление с помощью очищенного водорода.

В промышленном плане у галлия нет широкого распространения. Металл сравнительно дорогой для металлургии + его физические/химические свойства редко где могут пригодиться для массового использования.
Где применяется галлий:
- в соединениях с натрием металл применяют при создании лазеров полупроводникового типа с ультрафиолетовым и синим диапазонами;
- как присадка к германию/кремнию;
- как отражающий элемент для зеркал среднего качества. В чистом виде материал способен отражать порядка 89% света. Достоинства подобных изделий обусловливаются способностью металл к пропуску ультрафиолетовых лучей;
- как компонент в смазочных материалах. Клеи с добавкой жидкого галлия весьма популярны и сегодня;
- как замена ртути в кварцевых термометрах;
- оксид галлия – это стратегически важный объект в производстве лазерных материалов.
Иногда галлий применяют как компонент для светящихся красок, а соли на основе металла являются катализаторами в аналитической химии, медицине и органическом синтезе. Чтобы купить 1 килограмма металла, который плавится в руках, потребуется выложить от 250 до 400 американских долларов в зависимости от степени чистоты химического элемента.
Галлий – металл, который плавится в руках
Галлий – металл, который плавится в руке. Вещество имеет температуру плавления, что составляет 29,76 о С. Если поместить его в теплую ладонь, оно постепенно начинает переходить из твердого состояния в жидкую форму.
Краткий экскурс в историю

Как называется металл, который плавится в руке? Как уже было отмечено выше, такой материал известен под определением галлий. Его теоретическое существование предсказал в далеком 1870 году отечественный ученый, автор таблицы химических элементов – Дмитрий Менделеев. Основой к возникновению такого предположения стало изучение им свойств многочисленных металлов. На то время ни одному теоретику не могло прийти в голову, что металл, который плавится в руках, существует в реальности.
Возможность синтеза чрезвычайно легкоплавкого материала, появление которого предсказывал Менделеев, доказал французский ученый Эмиль Лекок де Буабодран. В 1875 году ему удалось выделить галлий из цинковой руды. Во время опытов с материалом ученый получил металл, который плавится в руках.
Известно, что Эмиль Буабодран испытывал значительные трудности с выделением нового элемента из цинковой руды. В ходе первых опытов ему удалось добыть всего лишь 0,1 грамма галлия. Однако даже этого оказалось достаточно, чтобы подтвердить удивительное свойство материала.
Где встречается галлий в природе

Галлий относится к элементам, которые не встречаются в виде залежей руд. Материал очень рассеян в земной коре. В природе он встречается в составе крайне редких минералов, таких как галлит и зенгеит. В ходе лабораторных опытов небольшое количество галлия можно выделить из руд цинка, алюминия, германия, железа. Иногда его находят в бокситах, залежах угля, прочих месторождениях полезных ископаемых.
Как получают галлий
В настоящее время ученые чаще всего синтезируют металл, который плавится в руках, из алюминиевых растворов, что добываются в ходе переработки глинозема. В результате удаления основной массы алюминия и проведения процедуры неоднократного концентрирования металлов получают щелочной раствор, в котором находится незначительная доля галлия. Выделяют такой материал из раствора путем электролиза.
Сферы применения

Галлий по сей день не нашел применения в промышленности. Виной всему широкое использование алюминия, который обладает схожими свойствами в твердом виде. Несмотря на это, галлий выглядит перспективным материалом, поскольку обладает отменными полупроводниковыми качествами. Такой металл потенциально может быть использован для производства элементов транзисторов, высокотемпературных выпрямителей тока, солнечных батарей. Галлий выглядит прекрасным решением для изготовления покрытий оптических зеркал, которые будут обладать высочайшей отражательной способностью.
Главным препятствием на пути к применению галлия в промышленных масштабах остается высокая стоимость его синтеза из руд и минералов. Цена за тонну такого металла на мировом рынке составляет более 1,2 миллиона долларов.
На сегодняшний день галлий нашел эффективное применение лишь в сфере медицины. Металл в жидкой форме применяется в целях замедления потери костной массы у людей, что страдают от онкологических недугов. Его используют для быстрой остановки кровотечений при наличии крайне глубоких ран на теле пострадавших. В последнем случае закупорка сосудов галлием не приводит к образованию тромбов.
Интересные опыты с галлием

Как уже отмечалось выше, галлий – металл, который плавится в руках. Поскольку температура, что требуется для перехода материала в жидкое состояние, составляет чуть больше 29 о С, его достаточно подержать в ладонях. Через некоторое время изначально твердый материал начнет плавиться буквально на глазах.
Довольно увлекательный эксперимент можно провести с затвердеванием галлия. Представленный металл имеет свойство расширяться в ходе затвердевания. Для проведения интересного опыта достаточно поместить жидкий галлий в стеклянный пузырек. Далее необходимо начать охлаждать емкость. Через некоторое время можно заметить, как в пузырьке станут образовываться кристаллы металла. Они будут иметь синеватый цвет, в отличие от серебристого оттенка, который характерен для материала в жидком состоянии. Если не прекращать охлаждение, кристаллизирующийся галлий в конечном итоге разорвет стеклянный пузырек.
В заключение
Вот мы и выяснили, какой металл плавится в руке. Сегодня галлий можно отыскать в продаже для проведения собственных опытов. Однако обращаться с материалом следует крайне осторожно. Твердый галлий является нетоксичным веществом. Однако продолжительный контакт с материалом в жидкой форме может привести к самым непредвиденным последствиям для здоровья, вплоть до остановки дыхания, паралича конечностей и вхождения человека в состояние комы.
Какой металл плавится на ладони?
Судя по всему, это галлий. Второе место по легкоплавкости после ртути - около 30 град. Цельсия. Галлиевые амальгамы обладают всеми достоинствами ртутных амальгам, но освобождены от ртутной ядовитости. Хотя вполне может быть какой-нибудь легкоплавкий сплав - их много известно - типа Вуда либо Розе, но конкретно у этих сплавов температура плавления гораздо выше человеческого тела.
Вот именно. Ладонь получит сильное обморожение, так что до плавления дело не дойдет. Цезий тоже теоретически можно "расплавить на ладони", но еще раньше ладонь получит сильнейший ожог.
Этот металл называется галлий. Температура плавки 29.8 градусов выше нуля. Галлий имеет малую токсичность. Ученые до сих пор не вывели летальную дозу для человека. Однако он очень дорогой, 1 кг. галлия стоит примерно от 600$ - 800$. При контакте галлия с кожей сверхмалые частицы остаются на руках. Внешне остается серый след. При остром отравлении наблюдается сначала острая возбужденность, далее заторможенность, нарушение координации движения, замедление и нарушение ритма дыхания. Все это кончается параличом нижних конечностей, а далее кома и смерть.
Кстати все фокусы со сгибанием ложек и вилок основаны именно на этом металле.
Вы наверное не в курсе, но человеческая кожа содержит на своей поверхности яд и сильнодействующие агрессивные вещества, для защиты организма от внешней биологически агрессивной среды. Огромные толпы вирусов, микробов и более взрослых "существ" постоянно пытаются пощупать кожу, в поисках малейшей лазейки внутрь организма, откуда вкусно пахнет теплым мясом. Именно защищаясь от них, кожа непрерывно трудится, выделяя пот, жир, сало и всё это ядовитое, соленое, горькое и агрессивное направлено против непрошеных гостей, желающих попасть в термостатируемое комфортное помещение с отборной пищей высшего сорта. Возьмите в руки стальную чистую пластинку и обратите внимание на оставленные вами отпечатки пальцев. Если пластинка не из нержавейки (да и из нержавейки тоже, только слабее), то вы можете увидеть, как агрессивные жидкости поверхности нашей кожи начинают бурно реагировать с железом, разъедая его, оставляя въевшийся в металл узор в виде этих отпечатков пальцев.
Вот поэтому, до всего, до чего могут дотянуться наши шаловливые конечности, или чего мы можем коснуться кожей, делается из качественных и устойчивых к агрессивным средам материалов, в том числе и металлов. Золото очень хороший метал, но очень дорогой и потому чаще идет на контакты в электронике. А вот латунь уже много дешевле. Потому и используют латунь для ручек, кранов и прочего. А пластмасса, увы, пока еще уступает латуни по долговечности.
Температура плавления металлов зависит от многих факторов:
- кристаллической фазы (у многих металлов их несколько с разными температурами плавления)
- от внешнего давления (обычно с увеличением давления температура плавления растет)
- от степени дисперсности металла (при увеличении дисперсности температура плавления падает)
- от чистоты металла (примеси и легирующие компоненты сплавов могут значительно менять температуру плавления металла, чаще всего в сторону снижения, хотя бывают и отрицательные эвтектики).
Ртуть, она плавится при -38 градусах Цельсия. В принципе, в жидком состоянии до +30 градусов Цельсия может существовать галлий, но в "ладонях" его не удержать, нужны специальные условия. При температурах ниже +36 градусов плавятся сплавы таких элементов, как натрий, калий, цезий. рубидий друг с другом.
На данный момент (февраль 2018 года) известно 118 химических элементов. И вероятность того, что в этом году (и даже в ближайшие годы!) будет открыт 119-й химический элемент, довольно мала. Названия последних четырех элементов были анонсированы пару лет назад, официально были рекомендованы комиссией по номенклатуре Международного союза теоретической и прикладной химии (ИЮПАК) в ноябре 2016 года и окончательно утверждены на конгрессе ИЮПАК в июле 2017 года.Это элементы нихоний (символ Nh), московий (символ Мс), "теннессин" (символ Ts) и оганессон (символ (Og). Мой скептицизм по поводу будущих открытий вызван теоретическими расчетами атома оганессона. Они показывают, что из-за очень большого заряда ядра у его электронов него нет привычных орбиталей! Вместо них присутствует "более или менее равномерно распределенное электронное облако". Хотя, конечно, ядру элемента от этого ни холодно ни жарко :)
К середине XIX века было уже открыто 63 химических элемента. И разными учеными делались попытки найти закономерности этого набора: Иоганн Вольфганг Дёберейнер ("закон триад", 1817 для кальция, стронция, бария, 1829 - , , ), Джон Ньюлендс ("закон октав", по аналогии с музыкой, 1865), Юлиус Лотар Мейер (1864, опубликовал таблицу 28 элементов - 6 столбцов по валентностям).
Д.И.Менделеев знал об этих исследованиях. Но в отличие от Ю.Л.Мейера он учел атомные веса элементов, о чем сначала сообщил ведущим химикам мира, а затем опубликовал свое открытие в статье "Соотношение свойств с атомным весом элементов". Гениальность прозрения Д.И.Менделеева заключалась в том, что он в своей "периодической системе" оставил несколько клеток пустыми! О чём до него никому в голову не приходило. И таким образом известные элементы "вписались" в закон Менделеева. Более того, он имел большую внутреннюю уверенность, что существуют ещё неоткрытые элементы, для которых он оставил пустые клетки. Как показала жизнь, он оказался прав. Первый вариант таблицы, описывающей периодический закон Д.И.Менделеева выглядел так:
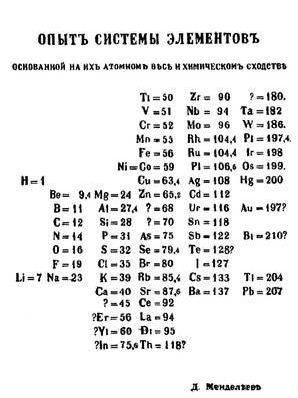
Вот так Менделеев создал Периодическую систему химических элементов.
Есть легенда, что Д.И.Менделеев увидел свою Периодическую таблицу во сне. Эту версию распространял профессор А.А.Иностранцев, желая позабавить своих студентов. Он рассказывал, якобы, что Д.И.Менделеев во сне отчетливо увидел свою таблицу, где элементы оказались расставлены, как нужно. А дальше уже студенты распространили эту байку, как и байку про "открытие водки 40%". Однако, основания для такой истории были. Д.И.Менделеев часто много работал, как говорится, "без сна и отдыха". Однажды его застал А.А.Иностранцев в крайне изможденном состоянии. А днем Д.И.Менделеев прилег отдохнуть и заснул. Когда он проснулся, он тут же на клочке бумаги записал итоговый вариант таблицы.
Сам же он к этой легенде относился скептически и говорил:
"Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово".
Какой металл может расплавляться в ладони?
Таких металлов науке известно четыре. Первое место среди этих четырёх по праву держит металл с названием Франций, далее следуют Цезий и Галллий и замыкает эту легкоплавкую четвёрку всем известная ртуть.
Ртуть - в ладони? Однако, не только опасно вдыхать пары ртути, но ртуть всасывается неповреждённой кожей - так и отравиться не долго. Ртуть - опасный яд.
Бесспорно токсичность ртути высока. Но никто и говорит о том, что нужно держать её в ладони. Речь идёт о температуре человеческой руки и металлах, которые при этой температуре имеют жидкое состояние.
Да, но исходный вопрос поставлен именно про ладонь: «Какой металл может расплавляться в ладони?», предположу даже, что имелась в виду человеческая ладонь, без защитных кремов и перчаток. :)
Возьмите немного ртути, в какой-нибудь сосуд. Например в крышку от пластиковой бутылки. Поставьте в морозилку часа на три. Потом достаньте замёрзший кусок и положите себе в ладонь, - ртуть расплавится. И довольно быстро. И за это время никакого вреда ни руке, ни всему организму не принесёт. Потом просто вымойте хорошо руки. Конечно ртуть это для человека яд, но на ладони кожа достаточно прочная и огрубевшая, чтобы не пропустить в организм этот яд за несколько минут его держания в ладони.
В целом, вы правы, но неприятная всё таки это процедура, ртуть начинает замерзать при –38,9°С, а прикосновение к металлу при минус сороковнике - чревато локальным обморожением и таки неприятно и опасно.
Согласен! Ртуть вообще сам по себе странный металл. И по своим свойствам, и по внешнему виду, и по поведению! Просто какая-то аномалия, а не металл! А к разным аномалиям всегда нужно относиться с особенной осторожностью!
Любой взрыв баллона страшен и опасен.
При взрыве газового баллона возможна не только ударная волна, но еще и пожар, который только увеличит нанесение ущерба, а также приведет к гибели находящихся рядом людей.
Но если учитывать давление, под которым находятся кислород (150 атм.) и пропан/бутан (16 атм.) в баллонах, то сильнее рванет кислородный баллон, там ведь давление в разы больше.
В общем если вы не специалист, то лучше возле кислородного баллона вообще не находиться, а с газовым баллоном надо быть осторожным при эксплуатации газовых приборов, работающих на сжиженном газе.
Читайте также:
