Какое действие тока используется при получении чистых металлов из растворов
Обновлено: 20.09.2024
Электролиз - принцип действия, назначение и применение
Сущность электролиза заключается в выделении из электролита при протекании через электролитическую ванну постоянного тока частиц вещества и осаждении их на погруженных в ванну электродах (электроэкстракция) или в переносе веществ с одного электрода через электролит на другой (электролитическое рафинирование). В обоих случаях цель процессов - получение возможно более чистых незагрязненных примесями веществ.
В отличие от электронной электропроводности металлов в электролитах (растворах солей, кислот и оснований в воде и в некоторых других растворителях, а также в расплавленных соединениях) наблюдается ионная электропроводность.
Электролиты являются проводниками второго рода. В этих растворах и расплавах имеет место электролитическая диссоциация - распад на положительно и отрицательно заряженные ионы.
Если в сосуд с электролитом - электролизер поместить электроды, присоединенные к электрическому источнику энергии, то в нем начнет протекать ионный ток, причем положительно заряженные ионы - катионы будут двигаться к катоду (это в основном металлы и водород), а отрицательно заряженные ионы - анионы (хлор, кислород) - к аноду.
У анода анионы отдают свой заряд и превращаются в нейтральные частицы, оседающие на электроде. У катода катионы отбирают электроны у электрода и также нейтрализуются, оседая на нем, причем выделяющиеся на электродах газы в виде пузырьков поднимаются кверху.
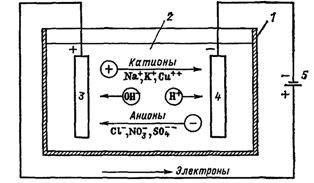
Рис. 1. Процессы, протекающие при электролизе. Схема электролизной ванны: 1 - ванна, 2 - электролит, 3 - анод, 4 - катод, 5 - источник питания
Электрический ток во внешней цепи представляет собой движение электронов от анода к катоду (рис. 1). При этом раствор обедняется, и для поддержания непрерывности процесса электролиза приходится его обогащать. Так осуществляют извлечение тех или иных веществ из электролита (электроэкстракцию).

Если же анод может растворяться в электролите по мере обеднения последнего, то частицы его, растворяясь в электролите, приобретают положительный заряд и направляются к катоду, на котором осаждаются, тем самым осуществляется перенос материала с анода на катод. Так как при этом процесс ведут так, чтобы содержащиеся в металле анода примеси не переносились на катод, такой процесс называется электролитическим рафинированием.
Если электрод поместить в раствор с ионами того же вещества, из которого он изготовлен, то при некотором потенциале между электродом и раствором не происходит ни растворения электрода, ни осаждения на нем вещества из раствора.
Такой потенциал называется нормальным потенциалом вещества. Если на электрод подать более отрицательный потенциал, то на нем начнется выделение вещества (катодный процесс), если же более положительный, то начнется его растворение (анодный процесс).
Значение нормальных потенциалов зависит от концентрации ионов и температуры. Принято считать нормальный потенциал водорода за нуль. В табл. 1 даны нормальные электродные потенциалы некоторых водных растворов веществ при +25° С.
Таблица 1. Нормальные электродные потенциалы при +25° С

Если в электролите имеются ионы разных металлов, то первыми на катоде выделяются ионы, имеющие меньший отрицательный нормальный потенциал (медь, серебро, свинец, никель), щелочноземельные металлы выделить труднее всего. Кроме того, в водных растворах всегда имеются ионы водорода, которые будут выделяться ранее, чем все металлы, имеющие отрицательный нормальный потенциал, поэтому при электролизе последних значительная или даже большая часть энергии затрачивается на выделение водорода.
Путем специальных мер можно воспрепятствовать в известных пределах выделению водорода, однако металлы с нормальным потенциалом меньше 1 В (например, магний, алюминий, щелочноземельные металлы) получить электролизом из водного раствора не удается. Их получают разложением расплавленных солей этих металлов.
Нормальные электродные потенциалы веществ, указанные в табл. 1, являются минимальными, при них начинается процесс электролиза, практически требуются большие значения потенциала для развития процесса.
Разность между действительным потенциалом электрода при электролизе и нормальным для него потенциалом называют перенапряжением. Оно увеличивает потери энергии при электролизе.
С другой стороны, увеличивая перенапряжение для ионов водорода, можно затруднить его выделение на катоде, что позволяет получить электролизом из водных растворов ряд таких более отрицательных по сравнению с водородом металлов, как свинец, олово, никель, кобальт, хром и даже цинк. Это достигается ведением процесса при повышенных плотностях тока на электродах, а также введением в электролит некоторых веществ.
Течение катодных и анодных реакций при электролизе определяется следующими двумя законами Фарадея.
1. Масса вещества m э, выделившегося при электролизе на катоде или перешедшего с анода в электролит, пропорциональна количеству прошедшего через электролит электричества I τ : m э = α / τ , здесь а - электрохимический эквивалент вещества, г/Кл.
2. Масса выделенного при электролизе вещества одним и тем же количеством электричества прямо пропорциональна атомной массе вещества А и обратно пропорциональна его валентности n : m э = А / 96480 n , здесь 96480 - число Фарадея, Кл х моль -1 .
Таким образом, электрохимический эквивалент вещества α = А / 96480 n представляет собой массу вещества в граммах, выделяемую единицей проходящего через электролитическую ванну количества электричества - кулоном (ампер-секундой).
Для меди А = 63,54, n = 2, α = 63,54/96480 -2 = 0,000329 г/Кл, для никеля α = 0,000304 г/Кл, для цинка α = 0,00034 г/Кл.

В действительности масса выделившегося вещества всегда меньше указанной, что объясняется рядом побочных процессов, проходящих в ванне (например, выделением водорода на катоде), утечками тока и короткими замыканиями между электродами.
Отношение массы фактически выделившегося вещества к массе его, которая должна была бы выделиться по закону Фарадея, носит название выхода вещества по току η1.
Следовательно, для реального процесса m э = η1 х ( А / 96480 n) х It
Естественно, всегда η1
Выход по току существенно зависит от плотности тока на электроде. С увеличением плотности тока на электроде выход по току растет и повышается эффективность процесса.
Напряжение U эл, которое необходимо подвести к электролизеру, состоит из: напряжения разложения Ер (разность потенциалов анодной и катодной реакций), суммы анодного и катодного перенапряжений падения напряжения в электролите Еп, падения напряжения в электролите U э = IR эп ( R эп - сопротивление электролита), падения напряжения в шинах, контактах, электродах U с = I ( R ш+ R к+ R э). Получаем: U эл = Ер + Еп + U э + U с.
Мощность, потребляемая при электролизе, равна: Рэл = IU эл = I (Ер + Еп + U э + U с)
Из этой мощности только первая составляющая расходуется на проведение реакций, остальные являются тепловыми потерями процесса. Лишь при электролизе расплавленных солей часть теплоты, выделяющейся в электролите IU э, используется полезно, так как расходуется на расплавление загружаемых в электролизер солей.
Эффективность работы электролизной ванны, может быть оценена массой вещества в граммах, выделяемого на 1 Дж затраченной электроэнергии. Эта величина носит название выхода вещества по энергии . Ее можно найти по выражению q э = (αη1)/ U эл100, здесь α - электрохимический эквивалент вещества, г/Кл, η1 - выход по току, U эл - напряжение на электролизере, В.
Телеграмм канал для тех, кто каждый день хочет узнавать новое и интересное: Школа для электрика
Если Вам понравилась эта статья, поделитесь ссылкой на неё в социальных сетях. Это сильно поможет развитию нашего сайта!
1. Электрический ток в металлах, полупроводниках, жидкостях и газах. Действия тока

Металлы в твёрдом состоянии имеют кристаллическое строение.
Модель металла — кристаллическая решётка (рис. 1 ) , в узлах которой частицы совершают хаотичное колебательное движение.
Отрицательными ионами называют атомы и молекулы, присоединившие к себе лишние электроны — приобретшие отрицательный заряд .
Положительными ионами называют атомы и молекулы, потерявшие электроны — приобретшие положительный заряд .
Положительные ионы располагаются в узлах кристаллической решётки. Свободные электроны движутся в пространстве между ними (рис. 2 ).
В невозбуждённом состоянии атом любого вещества имеет одинаковое количество электронов и протонов, поэтому суммарный их заряд равен нулю. Говорят, что атом электрически нейтрален .
Процесс электризации тела представляет собой приобретение или потерю этим телом электронов и ионов. Подвижными носителями зарядов в твёрдых металлов являются только электроны. При электризации металлических тел с одного на другое переходят только электроны.
Свободным называется электрон, оторвавшийся и не присоединившийся к другим молекулам и атомам, существующий как самостоятельная частица.
Электрический ток в металлах обусловлен наличием свободных подвижных электронов, совокупность которых называют электронным газом .
Электрически нейтральным будет называться вещество, в котором количество положительных зарядов равно количеству отрицательных зарядов.
Оказывается, скорость движения электронов в проводнике чрезвычайно мала, всего лишь несколько миллиметров в секунду. Почему же тогда лампочка загорается сразу после нажатия на выключатель? Все дело в том, при включении света в проводнике возникает электрическое поле (скорость его распространения около 300 000 км/с), которое заставляет
электроны двигаться в одном направлении по всей длине проводника.
Подтверждением того, что ток в металлах обусловлен движением электронов, явились многочисленные опыты, например, опыт Мандельштама и Папалекси (1916 г.). Цель опыта состояла в проверке того, есть ли масса у носителя электрического тока — электрона. Если масса у электрона есть, то он должен подчиняться законам механики, в частности, закону инерции. К примеру, если движущийся проводник резко затормозить, то электроны ещё некоторое время будут двигаться в том же направлении по инерции.
Для этой проверки исследователи вращали катушку с проходящим током, а затем резко останавливали её. Возникающий бросок тока регистрировали с помощью телефона.
По щелчку тока в телефонах Мандельштам и Папалекси установили, что электрон обладает массой. Но измерить эту массу они не смогли. Поэтому этот опыт — качественный. Позже американские физики Толмен и Стюарт, используя ту же идею вращения катушки, измерили массу электрона. Для этого они измеряли возникающий при торможении катушки заряд на её выводах.
Электрический ток может существовать не только в металлах, но и в других средах: в полупроводниках, газах и растворах электролитов. Носители электрических зарядов в разных средах разные.
Так, в растворах электролитов (солей, кислот и щелочей) носителями являются положительные и отрицательные ионы, в газах — положительные и отрицательные ионы, а также электроны. В полупроводниках носителями заряда являются электроны и дырки (дырка — придуманная частица для объяснения механизма проводимости, по сути — свободное место, не занятое электроном).

Полупроводники при низкой температуре не проводят электрический ток — являются диэлектриками. При воздействии на полупроводник светом, добавлением примесей или при нагревании появляются свободные носители зарядов, которые при своём направленном движении создают электрический ток. Полупроводник становится проводником.
Свойство полупроводников изменять электропроводность под воздействием света используется в фотосопротивлениях для создания сигнализации, при сортировке деталей.
В экстренных ситуациях они позволяют автоматически останавливать станки и конвейеры, предупреждая несчастные случаи.
При этом, если единственными носителями тока являются отрицательно заряженные частицы (например, электроны в металле), то направление тока противоположно направлению движения электронов: движение электронов показано зеленой стрелкой, а направление тока — красной стрелкой (рис. 4 ).

Используя это свойство, можно найти место обрыва фазового провода приборами, реагирующими на изменения в электромагнитном поле, к примеру, индикаторной отвёрткой с фазоискателем.
Магнитное действие тока используют в устройстве гальванометра. Для этой цели между полюсами магнита помещают легкую рамку с витками провода. При протекании тока она поворачивается, увлекая за собой стрелку (рис. 5 ).

Магнитное действие тока проявляется вне зависимости от агрегатного состояния вещества. При замыкании ключа можно наблюдать, как проволока, намотанная на гвоздь, начинает притягивать небольшие железные предметы. Это свойство широко используется в грузоподъёмных электромагнитах.
При прохождении электрического тока по проводнику в результате столкновений свободных электронов с его атомами и ионами проводник нагревается. Это явление проявляется в любых устройствах, имеющих нагревательный элемент: фен, плойка, электроплита, калорифер, стиральная машина, тостер, электровафельница и т.д. И даже спираль лампочки накаливания нагревается током до яркого накаливания. Под действием тока нагревается и провисает проволока.
Химическое действие тока применяется для покрытия одного металла слоем другого металла, например, при хромировании и никелировании.
Электрометаллургия
Электрометаллургия — Методы получения металлов, основанные на электролизе, т. е. выделении металлов из растворов или расплавов их соединений при пропускании через них постоянного электрического тока. Этот метод применяют главным образом для получения очень активных металлов – щелочных, щелочноземельных и алюминия, а также производства легированных сталей.
Содержание
Виды процессов
В электрометаллургии используются электротермические и электрохимические процессы. Электротермические процессы используются для выделения металлов из руд и концентратов, производства и рафинирования чёрных и цветных металлов и сплавов на их основе (Электротермия). В этих процессах электрическая энергия является источником технологического тепла. Электрохимические процессы распространены в производстве чёрных и цветных металлов на основе электролиза водных растворов и расплавленных сред (Электрохимия). За счёт электрической энергии осуществляется окислительно-восстановительные реакции на границах раздела фаз при прохождении тока через электролиты. Особое место в этих процессах занимает гальванотехника, в основе которой лежат электрохимические процессы оседания металлов на поверхность металлических и неметаллических изделий.
Электрохимические процессы охватывают плавку стали в дуговых и индукционных печах, спецэлектрометаллургию, рудовосстанавливающую плавку, включающую производство ферросплавов и штейнов, выплавку чугуна в шахтных электропечах, получения никеля, олова и других металлов.
Электродуговая плавка
Электросталь, предназначенная для дальнейшего передела, выплавляется главным образом в дуговых печах с основной футеровкой. Важные преимущества этих печей перед другими сталеплавильными агрегатами (возможность нагрева металла до высоких температур за счёт электрической дуги, обновляемая атмосфера в печи, меньший угар легирующих элементов, высокоосновные шлаки, обеспечивающие существенное снижение содержания серы) обусловили их использование для производства легированных высококачественных сталей — коррозионностойких, инструментальных (в том числе быстрорежущих), конструкционных, электротехнических, жаропрочных и т. д., а также сплавов на никелевой основе.
Мировая тенденция развития электродуговой плавки — увеличение ёмкости отдельного агрегата до 200—400 тонн, удельной мощности трансформатора до 500—600 и более кВА/т, специализация агрегатов (в одних — только расплавление, в других — рафинирование и легирование), высокий уровень автоматизации и использования ЭВМ для программного управления плавкой. В печах повышенной мощности экономически целесообразно плавить не только легированную, но и обычную углеродистую сталь. В развитых странах доля углеродистой стали от общего объёма электростали, выплавляемой в электропечах, составляет 50 % и более. В СССР в электропечах выплавлялось ~80 % легированного металла.
Для выплавки специальных сталей и сплавов приобретают распространение плазменно-дуговые печи с основным керамическим тиглем (ёмкостью до 30 т), оборудованные плазмотронами постоянного и переменного тока (Плазменная металлургия). Дуговые электропечи с кислотной футеровкой используют для плавки металла, предназначенного для стального литья. Кислотный процесс в целом более высокопродуктивный, чем основной, из-за кратковременности плавки, благодаря меньшей продолжительности окислительного и восстановительного периодов. Кислотная сталь дешевле основной вследствие меньшего расхода электроэнергии, электродов, лучшей стойкости футеровки, меньшим затратам окислителей и возможности осуществления кремневосстанавливающего процесса. Дуговые печи ёмкостью до 100 тонн широко используются также для плавки чугуна в чугуноплавильных цехах.
Индукционная плавка
Плавка стали в индукционной печи, осуществляемая в основном методом переплавки, сводится, как правило, к расплавлению шихты, раскислению металла и отпуску. Это обуславливает высокие требования к шихтовым материалам с содержанием вредных примесей (P, S). Выбор тигля (основной или кислый) обуславливается свойствами металла. Чтобы кремнезём футеровки не восстанавливались в процессе плавки, стали и сплавы с повышенным содержанием Mn, Ti, Al выплавляют в основном тигле. Существенный недостаток индукционной плавки — холодные шлаки, которые нагреваются только от металла. В ряде конструкций этот недостаток устраняется путём плазменного нагрева поверхности металл-шлак, что позволяет также значительно ускорить расплавление шихты. В вакуумных индукционных печах выплавляют чистые металлы, стали и сплавы соответствующего назначения (Вакуумная плавка). Ёмкость существующих печей составляет от нескольких килограмм до десятков тонн. Вакуумную индукционную плавку интенсифицируют продувкой инертными (Ar, Не) и активными (CO, CH4) газами, электромагнитным перемешиванием металла в тигле, продувкой металла шлакообразующими порошками.
Спецэлектрометаллургия
Спецэлектрометаллургия охватывает новые процессы плавки и рафинирования металлов и сплавов, которые получили развитие в 50—60-х гг. 20 столетия для удовлетворения потребностей современной техники (космической, реактивной, атомной, химического машиностроения и др.) в конструкционных материалах с высокими механическими свойствами, жаропрочностью, коррозионной стойкостью и т. д. Спецэлектрометаллургия включает вакуумную дуговую плавку, электроннолучевую плавку, электрошлаковую переплавку и плазменно-дуговую плавку. Этими методами переплавляют стали и сплавы ответственного назначения, тугоплавкие металлы — вольфрам, молибден, ниобий и их сплавы, высокореакционные металлы — титан, ванадий, цирконий, сплавы на их основе и др. Вакуумная дуговая плавка была предложена в 1905 году В. фон Больтоном (Германия); в промышленных масштабах этот метод впервые был использован для плавки титана В. Кроллом (США) в 1940 году. Метод электрошлакового переплава разработан в 1952—53 гг. в Институте электросварки им. Патона АН УССР. Для получения сталей и сплавов на никелевой основе особо ответственного назначения используют разные варианты дуплекс-процессов, наиважнейший из которых — объединение вакуумной индукционной плавки и вакуумно-дуговой переплавки. Особое место в спецэлектрометаллургии занимает вакуумная гарнисажная плавка, в которой источниками тепла служат электрическая дуга, электронный луч, плазма. В этих печах, используемых для высокоактивных и тугоплавких металлов (W, Мо и др. и сплавы на их основе), порция редкого металла в водоохлаждаемом тигле с гарнисажем используется для получения слитков и фасонных отливок.
Рудовосстанавливающая плавка
Рудовосстанавливающая плавка включает производство ферросплавов, продуктов цветной металлургии — медных и никелевых штейнов, свинца, цинка, титановых шлаков и др. Процесс заключается в восстановлении природных руд и концентратов углеродом, кремнием и другими восстановителями при высоких температурах, которые создаются главным образом за счёт мощной электрической дуги (Рудотермическая печь). Восстанавливающие процессы обычно являются непрерывными. По мере проплавления подготовленную шихту загружают в ванну, а полученные продукты периодически выпускают из электропечи. Мощность таких печей достигает 100 МВА. На некоторых предприятиях на основе рудовосстанавливающей плавки производится чугун в электродоменных печах или электродуговых бесшахтных печах.
Электрохимические процессы получения металлов
Г. Деви в 1807 впервые использовал электролиз для получения натрия и калия.
В конце 1970-х гг. методом электролиза были получены более 50 металлов, в частности медь, никель, алюминий, магний, калий, кальций. Различают 2 типа электролитических процессов. Первый связан с катодным оседанием металлов из растворов, полученных методами гидрометаллургии; в этом случае восстановлению (откладыванию) на катоде металла из раствора отвечает реакция электрохимического окисления аниона на нерастворимом аноде.
Второй тип процессов связан с электролитическим рафинированием металла из его сплава, из которого изготавливается растворимый анод. На первой стадии в результате электролитического растворения анода металл переводится в раствор, на второй стадии он оседает на катоде. Последовательность растворения металлов на аноде и осаждения на катоде определяется предел напряжения. Однако в реальных условиях потенциалы выделения металлов существенно зависят от величины перенапряжения водорода на соответствующем металле. В промышленных масштабах рафинируют цинк, марганец, никель, железо и другие металлы; алюминий, магний, калий и др. получают электролизом расплавленных солей при 700—1000 °C. Последний способ связан с бо́льшим потреблением электроэнергии (15—20 тыс. кВт•час/т) в сравнении с электролизом водных растворов (до 10 тыс. кВт•час/т).
История
В начале 19 века В. В. Петров обнаружил возможность получения при помощи электрической дуги чистых металлов из их оксидов (руд). Этот процесс восстановления металлов лежит в основе современной электрометаллургии. Первые дуговые электрические печи для восстановления из руд были построены в конце 1870 годов. Но электропечи расходуют очень много электроэнергии, поэтому их промышленное применение началось только тогда, когда стали строить мощные электростанции и была решена проблема передачи электрической энергии на расстояние.
§ 45.1. Получение металлов электролизом водных растворов солей
В § 45 вы познакомились с электрохимическим методом промышленного получения металлов, который основан на электролизе, — электрометаллургией.
У этого метода есть две разновидности. Первая — это проведение электролиза расплава соединений металлов. Особенности этого способа вы рассмотрели на примере электролиза расплава хлорида магния.
Вторая разновидность электрохимического метода, называемая гидроэлектрометаллургией, основана на электролизе водных растворов солей металлов. Преимущество этого метода, по сравнению с электролизом расплавов, заключается в том, что он не требует энергетических затрат на расплавление вещества. Ограничение электролитического метода извлечения металлов из водных растворов состоит в том, что он пригоден лишь для металлов, стоящих в ряду активности металлов правее алюминия.
Особенность проведения электролиза водных растворов солей заключается в том, что наряду с процессами восстановления ионов металла на катоде и окисления анионов соли на аноде протекает конкурирующий процесс электролиза молекул воды. В результате на катоде может выделяться водород, а на аноде — кислород.
Процессы на катоде:
2Н + + 2е – = Н2↑ при рН < 7;
Процессы на аноде:
2Н2О – 4е – = О2↑ + 4Н + при рН ≤ 7;
4ОН – – 4е – = О2↑ + 2Н2О при рН > 7.
Процессы на катоде
Способность металлов восстанавливаться на катоде при электролизе водного раствора солей определяется положением металла в ряду активности.
Катионы металлов в левой части ряда активности, заканчивая алюминием (Li + , Na + , K + , . Аl 3+ ), при электролизе не восстанавливаются. Вместо них восстанавливается водород из молекул воды:
Катионы металлов, расположенных в ряду активности правее водорода (Cu 2+ , Ag + , Hg 2+ , Pt 2+ , Au 3+ ), при электролизе восстанавливаются на катоде до металла:
Cu 2+ + 2е – = Cu 0 ;
Au 3+ + 3е – = Au 0 .
Этот процесс доминирует, но если электролит имеет сильно кислую среду, то одновременно с ионами металла могут восстанавливаться ионы водорода:
Катионы металлов, расположенных в ряду активности между алюминием и водородом (Mn 2+ , Zn 2+ , Сr 3+ , Fe 2+ , . Pb), при электролизе восстанавливаются на катоде одновременно с водородом из воды:
Ni 2+ + 2e – = Ni 0 ;
При электролизе водных растворов солей металлов следует учитывать возможность протекания процессов гидролиза, который ускоряется в результате образования гидроксид-ионов в электролите вблизи катода. В результате на поверхности катода могут образовываться нерастворимые основные соли и основания:
Электропроводность электрода уменьшается, и процесс электролиза замедляется или прекращается. Один из способов борьбы с таким явлением — подкисление электролитов.
Процессы на аноде
На аноде протекают процессы окисления компонентов электролита. В процессе окисления может участвовать и материал самого анода. Различают процессы электролиза в растворах с активным и инертным анодами.
Инертные аноды не окисляются под действием электрического тока и не реагируют с веществами раствора. При электролизе они служат лишь передатчиками электронов. Инертными являются электроды из графита, платины, платинированного титана.
К активным относятся аноды, изготовленные из Сu, Ag, Fe, Ni, Sn, Zn. Металл активных анодов в процессе электролиза разрушается и переходит в раствор в виде ионов. Активные аноды обычно применяют в промышленности при получении покрытий путём электрохимического восстановления металлов из растворов, поскольку растворение металлического анода в процессе электролиза восполняет убыль ионов восстанавливаемого металла из электролита. При этом они обеспечивают постоянство состава раствора, скорости процесса электролиза, состава и свойств получаемых металлических покрытий.
Рассмотрим подробнее процессы, протекающие при электролизе растворов на инертных анодах. Можно выделить следующие закономерности (табл. 31.1):
• в растворах бескислородных кислот и их солей (кроме HF и фторидов) на аноде окисляются анионы, например:
• в растворах кислородсодержащих кислот и их солей в случае максимальной степени окисления атомов неметалла в анионе ( , ) окисляются атомы кислорода в молекулах воды с выделением газообразного кислорода:
• в растворах кислородсодержащих кислот и их солей, в анионах которых содержатся атомы неметалла в промежуточной степени окисления ( , ), окисляются именно эти атомы в составе анионов, например:
Таблица 31.1. Способность к окислению на аноде анионов при электролизе водных растворов солей
В водном растворе не окисляются; окислению подвергаются молекулы воды с выделением кислорода:
В водном растворе легко окисляются, например:
В специально созданных условиях в водных растворах может идти процесс окисления и кислородсодержащих анионов с максимальной степенью окисления неметалла. Например, электролизом концентрированного раствора гидросульфата калия получают сильный окислитель — пероксодисульфат калия:
Примеры использования электролиза водных растворов солей металлов в промышленности и в лаборатории
При разработке условий электролиза следует учитывать, что продукты электролиза могут вступать в химические реакции с электродами и водными растворами или между собой.
Промышленный электролиз водного раствора NaCl. Процесс используют для получения водорода, хлора и каустической соды (NaOH). При этом на катоде выделяется водород:
а в растворе накапливается каустическая сода:
Если не разделить продукты электролиза, то между образовавшимися газами произойдёт химическая реакция.
В растворе также возможно взаимодействие хлора со щёлочью:
Cl2 + 2NaOH = NaClO + NaCl + H2O.
Для того чтобы между продуктами электролиза не происходило взаимодействие, катодное и анодное пространство разделяют мембраной (рис. 108.2).
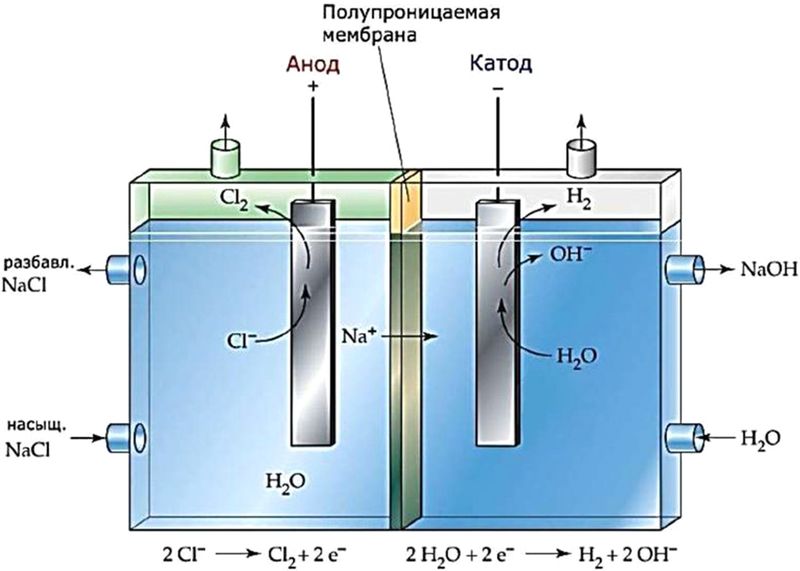
Рис. 108.2. Схема электролизёра с ионообменной мембраной для электролиза раствора хлорида натрия. Мембрана пропускает ионы Na + , но не пропускает ионы Cl – и OH –
С 2015 года в ОАО «Беларуськалий» функционирует цех мембранного электролиза. Продукцией цеха являются: водный раствор гидроксида калия (с массовой долей KOH 46−54 % ); твёрдый гидроксид калия (с массовой долей KOH 9 0−95 % ); соляная кислота (с массовой долей HCl 28−35 % ); гипохлорит натрия NaClO.
Электролиз растворов солей в лаборатории.
Для наглядности при рассмотрении особенностей электролиза водных растворов солей обратимся к химическому эксперименту.
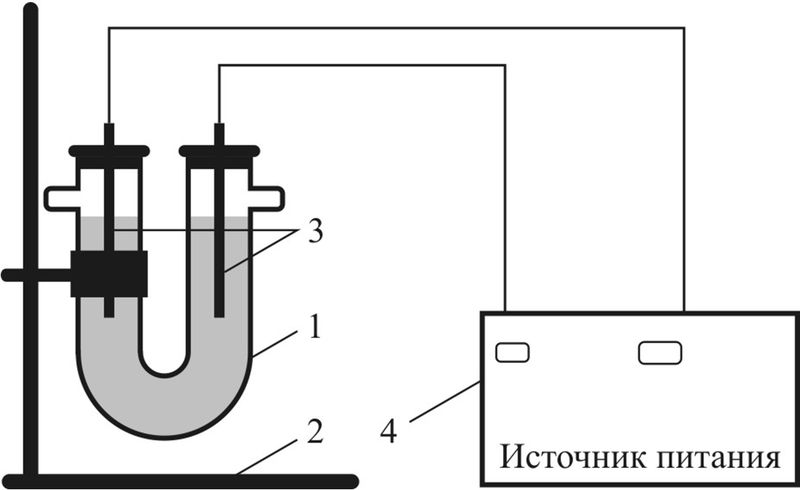
Рис. 108.3. Схема прибора для электролиза:
1 — U-образная трубка (электролизёр);
2 — штатив;
3 — электроды (графитовые стержни);
4 — источник питания постоянного тока
Опыт 1. Проведём электролиз водного раствора CuSO4. Для этого соберём прибор по схеме, представленной на рис. 108.3. В U-образную трубку нальём раствор сульфата меди(II) и опустим два графитовых стержня, закреплённых в резиновых пробках. Стержни с помощью проводов присоединим к источнику тока, на котором поддерживается напряжение постоянного тока до 12 В.
Рис. 108.4. Осаждённая медь на графитовом электроде после проведения электролиза раствора сульфата меди(II)
При пропускании электрического тока через раствор CuSO4 на стержне, присоединённом к положительному полюсу источника тока (анод), можно наблюдать выделение пузырьков газа (это кислород), а на стержне, присоединённом к отрицательному полюсу (катод), — появление красного налёта (это восстановленная медь) (рис. 108.4).
Объяснить наблюдаемое явление можно следующими процессами.
В растворе сульфата меди происходит диссоциация:
При подключении электродов к источнику тока в растворе электролита происходит направленное движение ионов к электродам, имеющим противоположные заряды.
На катоде происходит восстановление меди, которая образует красный налёт на электроде:
Сu 2+ + 2e – = Сu 0
На аноде (положительно заряженном электроде) происходит окисление молекул воды с выделением кислорода:
Суммарное уравнение процессов на электродах в молекулярной форме:
Опыт 2. Проведите электролиз водного раствора йодида калия.
Для проведения электролиза раствора KI воспользуемся установкой из примера 1 (рис. 108.3).
В U-образную трубку нальём раствор KI и пропустим через него электрический ток. Через 3–5 минут, отключив ток и достав электроды, в катодное пространство добавим 2−3 капли фенолфталеина, а в анодное пространство прильём крахмальный клейстер.

Рис. 108.5. Электролизёр после проведения электролиза раствора йодида калия и добавления раствора фенолфталеина (катодное пространство) и крахмального клейстера (анодное пространство)
Раствор в катодном пространстве окрашивается в малиновый цвет, что свидетельствует о щелочной среде. В анодном пространстве наблюдается выделение жёлто-бурого вещества, при добавлении к которому 2–3 капель крахмального клейстера происходит посинение раствора, что указывает на присутствие в растворе йода (рис. 108.5).
Таким образом, продуктами электролиза водного раствора йодида калия являются I2 и щёлочь.
Наблюдаемые явления свидетельствуют о протекании на электродах следующих реакций:
2Н2О + 2e – = Н2↑ + 2ОН – на катоде;
2I – – 2e – = I2 на аноде.
Суммарное уравнение процесса электролиза в молекулярной форме:
Электролиз с активными анодами в промышленности. Помимо электрохимического осаждения металлических покрытий и получения порошков металлов, этот метод применяют для извлечения металлов из растворов, а также для очистки (рафинирования) металлов от содержащихся в них примесей. Так получают чистое золото, медь и многие другие металлы.
Например, при очистке (рафинировании) меди исходный металл, содержащий нежелательные примеси, служит анодом. Анод погружают в раствор сульфата меди(II). При пропускании тока медь на аноде окисляется, её ионы переходят в раствор, перемещаются к катоду и на нём восстанавливаются. Примеси в этом процессе не участвуют из-за их малой концентрации, и поэтому на катоде образуется слой чистой меди.
Процессы электролиза с активными анодами используют для получения покрытий из оксидов металлов. Так, при проведении электролиза с анодом из алюминия его поверхность окисляется, покрываясь слоем оксида. Такой процесс специального наращивания оксида на поверхности металла называют электрохимическим оксидированием (или анодированием). Анодирование применяют для защиты металла от коррозии, придания его поверхности декоративного внешнего вида, повышенной твёрдости.
Методом электролиза растворов солей на поверхность различных изделий наносят покрытия из металлов и их сплавов, композитов с неметаллами, что придаёт изделиям нужные свойства (повышенная коррозионная стойкость, декоративная отделка, электропроводность и др.). К распространённым промышленным процессам относятся цинкование, никелирование, меднение, хромирование, оловянирование, золочение и серебрение.
В НИИ физико-химических проблем Белорусского государственного университета разработаны и внедрены в промышленность процессы электрохимического осаждения покрытий из сплавов металлов и композиционных покрытий металл — оксид металла, например: Ni—B , Ni—P , Ni—Sn , Au—Co , Сu—CuO—Cu2O , Ni — алмаз (алмаз в виде тонко измельчённого порошка). Такие покрытия более твёрдые, износо- и коррозионностойкие, чем покрытия из индивидуальных металлов, обладают декоративным внешним видом (рис. 108.6).
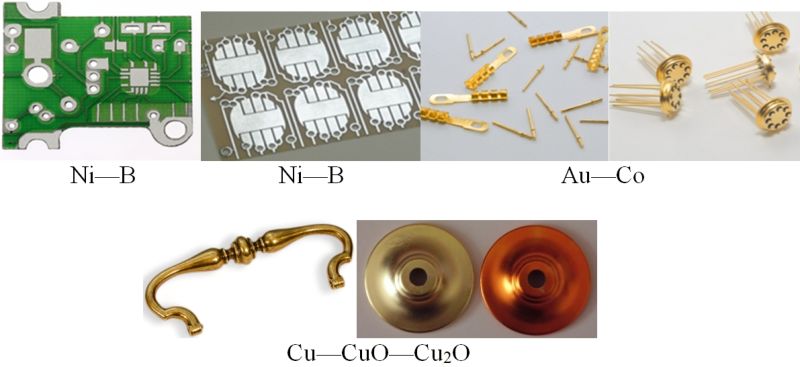
Рис. 108.6. Покрытия на часовых платах, платах кредитных карточек, корпусах транзисторов, фурнитурных изделиях
Электролиз водных растворов используется также в синтезе различных неорганических веществ, в обработке поверхностей металлов (азотирование, борирование, электрополировка, очистка), в очистке сточных вод (процессы электрокоагуляции, электроэкстракции, электрофлотации). Электролизом получают кислород и водород.
При электролизе водных растворов солей на катоде восстанавливаются катионы металлов, расположенных в ряду активности после водорода.
На катоде не восстанавливаются катионы металлов IA- и IIA-групп , расположенных в начале ряда активности, а также алюминий, вместо них восстанавливается водород из молекул воды.
На катоде одновременно с водородом из воды восстанавливаются катионы металлов, расположенных в ряду активности между алюминием и водородом.
На аноде в растворах солей бескислородных кислот окисляются анионы (кроме фторид-ионов).
На аноде в растворах солей кислородсодержащих кислот с максимальной степенью окисления неметалла ( , ) окисляются молекулы воды с выделением кислорода.
Вопросы, задания, задачи
1. Какие из веществ — каменная соль, сахар, медный купорос, глицерин, серная кислота — могут подвергнуться электролизу в водном растворе?
2. Объясните, почему алюминий нельзя получить электролизом водного раствора его хлорида.
3. Приведите уравнения реакций на электродах при электролизе водного раствора сульфата никеля(II).
4. Сравните продукты электролиза расплава и водного раствора хлоридов натрия, никеля(II) и меди(II). Приведите соответствующие уравнения химических реакций.
5. При электролизе водного раствора хлорида натрия без разделения электродных пространств можно получить гипохлорит натрия. Приведите возможные уравнения электродных процессов и химических реакций в растворе.
6. Продукцией цеха мембранного электролиза ОАО «Беларуськалий» являются водный раствор гидроксида калия и соляная кислота. Приведите уравнения реакций, которые лежат в основе получения этих веществ.
7. Как изменится концентрация катионов и анионов в водных растворах CuCl2, Na2SO4, KI, NaOH, HCl при электролизе? Приведите соответствующие уравнения реакций.
8. В качестве лабораторного способа дезинфекции воды используется электролиз водного раствора хлорида натрия в портативных электролизёрах. Объясните процессы, на которых основан этот способ дезинфекции воды.
9. Сырьём для получения цинка является руда, содержащая цинковую обманку (ZnS). Продукт её обжига растворяют в серной кислоте и после нескольких стадий очистки от примесей (Cu 2+ , Fe 2+ , Fe 3+ и др.) подвергают электролизу. Приведите уравнения химических реакций, иллюстрирующих все основные стадии получения цинка.
10. Оксид марганца(IV) получают электролизом раствора сульфата марганца(II) в присутствии серной кислоты. Предположите, какие процессы протекают на электродах и приведите уравнения соответствующих реакций.
Самоконтроль
1. При электролизе водных растворов солей восстанавливаются ионы:
- а) Li + ;
- б) Mg 2+ ;
- в) Ni 2+ ;
- г) Au 3+ .
2. При электролизе водных растворов солей не восстанавливаются ионы:
- а) K + ;
- б) Са 2+ ;
- в) Cu 2+ ;
- г) Ag + .
3. Продуктами электролиза водного раствора калийной соли являются:
4. На катоде могут протекать процессы:
- а) 2Н2О + 2e – = Н2↑ + 2ОН – ;
- б) 2Н2О – 4e – = О2↑ + 4Н + ;
- в) 2Н + + 2e – = Н2↑;
- г) Ni 2+ + 2e – = Ni 0 .
5. При электролизе водного раствора хлорида натрия выделился водород объёмом 2,24 дм 3 (н. у.). Число электронов, отданных при этом ионами хлора, равно:
Действия электрического тока: тепловое, химическое, магнитное, световое и механическое
Электрический ток в цепи всегда проявляется каким-нибудь своим действием. Это может быть как работа в определенной нагрузке, так и сопутствующее действие тока. Таким образом, по действию тока можно судить о его наличии или отсутствии в данной цепи: если нагрузка работает — ток есть. Если типичное сопутствующее току явление наблюдается — ток в цепи есть, и т. д.
Вообще, электрический ток способен вызывать различные действия: тепловое, химическое, магнитное (электромагнитное), световое или механическое, причем разного рода действия тока зачастую проявляются одновременно.
Об этих явлениях и действиях тока и пойдет речь в данной статье.

Тепловое действие электрического тока
При прохождении постоянного или переменного электрического тока по проводнику, проводник нагревается. Такими нагревающимися проводниками в разных условиях и приложениях могут выступать: металлы, электролиты, плазма, расплавы металлов, полупроводники, полуметаллы.


В простейшем случае, если, скажем, через нихромовую проволоку пропустить электрический ток, то она нагреется. Данное явление используется в нагревательных приборах: в электрочайниках, в кипятильниках, в обогревателях, электроплитках и т. д. В электродуговой сварке температура электрической дуги вообще доходит до 7000°С, и металл легко плавится, - это тоже тепловое действие тока.
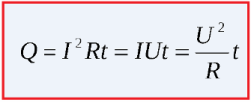

Явление выделения тепла при протекании электрического тока впервые наблюдал Джеймс Джоуль в 1841 году, а затем независимо Генрих Ленц в 1842 году. В настоящее время оно используется для преобразования электричества во внутреннюю энергию.
Выделяемое на участке цепи количество теплоты зависит от приложенного к этому участку напряжения, значения протекающего тока и от времени его протекания (Закон Джоуля — Ленца).
Преобразовав закон Ома для участка цепи, можно для вычисления количества теплоты использовать либо напряжение, либо силу тока, но тогда обязательно необходимо знать и сопротивление цепи, ведь именно оно ограничивает ток, и вызывает, по сути, нагрев. Или, зная ток и напряжение в цепи, можно так же легко найти количество выделяемой теплоты.
Это явление часто нежелательно, например, при передаче электроэнергии на расстояние. В этом случае высвобожденное тепло будет потрачено впустую.
В электронных устройствах эффект Джоуля-Ленца создает тепло внутри устройства и требует его отвода оттуда для стабильной работы устройства. Поэтому, например, компьютеры требуют охлаждения.
Преобразование электрической энергии в тепловую энергию (тепловые приборы, холодильники) имеет КПД более 90%.
Химическое действие электрического тока
Электролиты, содержащие ионы, под действием постоянного электрического тока подвергаются электролизу — это и есть химическое действие тока.
К положительному электроду (аноду) в процессе электролиза притягиваются отрицательные ионы (анионы), а к отрицательному электроду (катоду) — положительные ионы (катионы). То есть вещества, содержащиеся в электролите, в процессе электролиза выделяются на электродах источника тока.
Например, в раствор определенной кислоты, щелочи или соли погружают пару электродов, и при пропускании электрического тока по цепи на одном электроде создается положительный заряд, на другом — отрицательный. Ионы содержащиеся в растворе начинают откладываться на электроде с противоположным зарядом.
Скажем, при электролизе медного купороса (CuSO4), катионы меди Cu2+ с положительным зарядом движутся к отрицательно заряженному катоду, где они получают недостающий заряд, и становятся нейтральными атомами меди, оседая на поверхности электрода.
Гидроксильная группа -OH отдаст электроны на аноде, и в результате выделится кислород. Положительно заряженные катионы водорода H+ и отрицательно заряженные анионы SO42- останутся в растворе.
Химическое действие электрического тока используется в промышленности, например, для разложения воды на составляющие ее части (водород и кислород). Также электролиз позволяет получать некоторые металлы в чистом виде. С помощью электролиза покрывают тонким слоем определенного металла (никеля, хрома) поверхности — это нанесение гальванических покрытий и т.д.
В 1832 году Майкл Фарадей установил, что масса m вещества, выделившегося на электроде, прямо пропорциональна электрическому заряду q, прошедшему через электролит. Если через электролит пропускается в течение времени t постоянный ток I, то справедлив первый закон электролиза Фарадея:
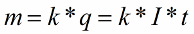
Здесь коэффициент пропорциональности k называется электрохимическим эквивалентом вещества. Он численно равен массе вещества, выделившегося при прохождении через электролит единичного электрического заряда, и зависит от химической природы вещества.
Гальванические элементы используют химическую реакцию, которая высвобождает энергию в виде электрического поля. При химической реакции молекула вновь образованного соединения имеет меньшую энергию, чем сумма энергий частей, из которых она образовалась.
Существует много видов гальванических элементов. Гальванические элементы относятся к первичным элементам — мы можем брать от них электрический ток, не «подав» его предварительно. Простейший гальванический элемент состоит из электролита и двух электродов. В качестве электролита используется серная кислота.
Положительный электрод изготовлен из меди, а отрицательный - из цинка. Когда серную кислоту разбавляют водой, молекулы воды освобождают прочную связь молекул кислоты, которая расщепляется на положительные и отрицательные ионы. Но существует баланс между зарядами, и электролит остается электрически нейтральным.
После погружения цинкового электрода в электролит цинк начинает растворяться, а его катионы заряжаются электролитом положительно. Цинковый электрод заряжается отрицательно и между положительным и отрицательным электродами появляется напряжение 1,05 В.
Если к выводам гальванического элемента подключить потребитель, то состояние равновесия нарушается, электроны переходят от цинкового электрода к медному электроду через потребителя, и создается электрический ток.
Магнитное действие электрическо го тока
При наличии электрического тока в любом проводнике (в твердом, жидком или газообразном) наблюдается магнитное поле вокруг проводника, то есть проводник с током приобретает магнитные свойства.
Так, если к проводнику, по которому течет ток, поднести магнит, например в виде магнитной стрелки компаса, то стрелка повернется перпендикулярно проводнику, а если намотать проводник на железный сердечник, и пропустить по проводнику постоянный ток, то сердечник станет электромагнитом.
В 1820 году Эрстед открыл магнитное действие тока на магнитную стрелку, а Ампер установил количественные закономерности магнитного взаимодействия проводников с током.
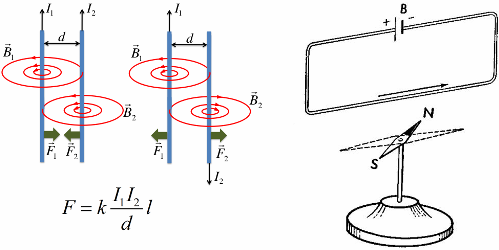
Магнитное поле всегда порождается током, то есть движущимися электрическими зарядами, в частности - заряженными частицами (электронами, ионами). Противоположно направленные токи взаимно отталкиваются, однонаправленные токи взаимно притягиваются.
Такое механическое взаимодействие происходит благодаря взаимодействию магнитных полей токов, то есть это, в первую очередь, — магнитное взаимодействие, а уж потом - механическое. Таким образом, магнитное взаимодействие токов первично.

В 1831 году, Фарадей установил, что изменяющееся магнитное поле от одного контура порождает ток в другом контуре: генерируемая ЭДС пропорциональна скорости изменения магнитного потока. Логично, что именно магнитное действие токов используется по сей день и во всех трансформаторах, а не только в электромагнитах ( например, в промышленных).
Световое действие электрического тока
Это действие тока используется в различных источниках света — источниках электромагнитного излучения в диапазоне длин волн примерно 380–780 нм (360–800 нм), которое мы можем наблюдать человеческим глазом в виде видимого света.
В простейшем виде световое действие электрического тока можно наблюдать в лампе накаливания, спираль которой разогревается проходящим через нее током до белого каления и излучает свет.
Для лампы накаливания на световую энергию приходится около 5% от подведенной электроэнергии, остальные 95% которой преобразуется в тепло.
Люминесцентные лампы более эффективно преобразуют энергию тока в свет — до 20% электроэнергии преобразуется в видимый свет благодаря люминофору, принимающему ультрафиолетовое излучение от электрического разряда в парах ртути или в инертном газе типа неона.
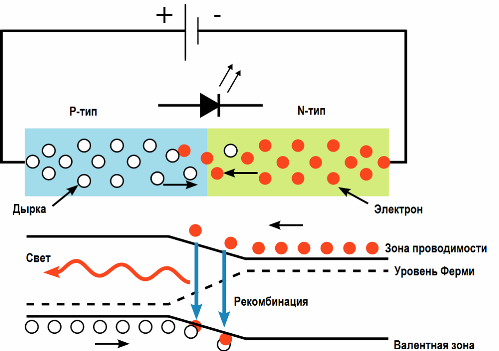
Более эффективно световое действие электрического тока реализуется в светодиодах. При пропускании электрического тока через p-n переход в прямом направлении, носители заряда — электроны и дырки — рекомбинируют с излучением фотонов (из-за перехода электронов с одного энергетического уровня на другой).
Лучшие излучатели света относятся к прямозонным полупроводникам (то есть к таким, в которых разрешены прямые оптические переходы зона-зона), например GaAs, InP, ZnSe или CdTe. Варьируя состав полупроводников, можно создавать светодиоды для всевозможных длин волн от ультрафиолета (GaN) до среднего инфракрасного диапазона (PbS). КПД светодиода как источника света доходит в среднем до 50%.
Механическое действие электрического тока
Как было отмечено выше, каждый проводник, по которому течет электрический ток, образует вокруг себя магнитное поле. Магнитные действия превращаются в движение, например, в электродвигателях, в магнитных подъемных устройствах, в магнитных вентилях, в реле и т. д.
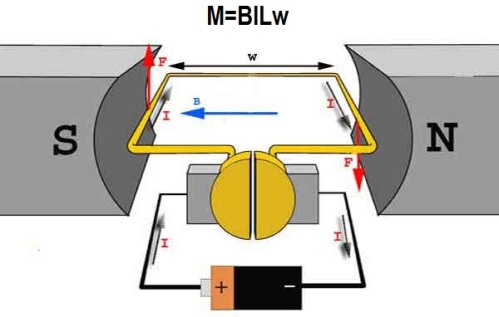
Механическое действие одного тока на другой описывает закон Ампера. Впервые этот закон был установлен Андре Мари Ампером в 1820 для постоянного тока. Из закона Ампера следует, что параллельные проводники с электрическими токами, текущими в одном направлении, притягиваются, а в противоположных — отталкиваются.
Законом Ампера называется также закон, определяющий силу, с которой магнитное поле действует на малый отрезок проводника с током. Сила, с которой магнитное поле действует на элемент проводника с током, находящегося в магнитном поле, прямо пропорциональна току в проводнике и векторному произведению элемента длины проводника на магнитную индукцию.
На этом принципе основана работа электродвигателей, где ротор играет роль рамки с током, ориентирующейся во внешнем магнитном поле статора вращающим моментом M.
Эффективность преобразования к механической энергии с помощью электродвигателя составляет более 90%.
Читайте также:
