Какую температуру держит рука человека на металле
Обновлено: 08.07.2024
Симптомы лейкемии не всегда заметны, но если вы знаете, на что нужно обратить внимание, вы можете вовремя их распознать.
Хотя при некоторых заболеваниях, таких как синусит, симптомы очень четкие, при лейкемии это может быть не так, потому что часто бывает, что человек не испытывает каких-либо заметных симптомов, которые могли бы выявить проблему. Общие симптомы лейкемии могут быть легко связаны с напряженным днем или стрессом, например, с ночным потоотделением или синяками, и по этой причине диагноз часто ставится поздно.
Однако если прислушаться к своему организму и обратить внимание на новые изменения, то можно вовремя их заметить и сразу обратиться к врачу. Вот несколько симптомов, которые означают, что срочно необходимо обследование.
Каковы симптомы лейкемии?
Симптомы будут различаться в зависимости от типа лейкемии, и некоторые из них часто встречаются у взрослых:
- хроническая усталость и слабость;
- лихорадка и жар;
- частые болезни;
- потеря веса;
- увеличение лимфатических узлов;
- из носа часто течет кровь;
- ночные поты;
- боль в костях;
- сыпь.
У вас не обязательно будут именно эти симптомы, но те, кто их замечает, могут принять их за что-то еще, особенно за хронический лейкоз, который прогрессирует медленнее и менее агрессивно, чем другие формы болезни.
Какие симптомы лейкемии указывают на необходимость срочного обращения к врачу?
Прежде всего, следует отметить, что важно обратиться к врачу, если у вас есть какие-либо вышеуказанные симптомы, а ниже немного более детальный обзор конкретных симптомов, связанных с лейкемией.
1. Синяки
Лейкоз — это рак крови, который возникает в спинном мозге, где вырабатываются красные и белые кровяные тельца и тромбоциты. У людей с лейкемией слишком много белых кровяных телец, которые играют важную роль в иммунитете, но во время этого заболевания они разрастаются и никак не помогают.
Необъяснимые синяки без предшествующих физических травм — один из многих симптомов лейкемии. Необычный синяк — результат низкого количества тромбоцитов или проблем со свертыванием крови. Синяки возникают спонтанно и могут быть где угодно на теле, но обычно появляются на конечностях — руках и ногах.
2. Вы постоянно болеете
Имеется в виду, что у вас появляется одна небольшая инфекция, которая не проходит, что бы ни прописал врач. В этом случае пора сделать общий анализ крови, который может показать отклонения в уровнях лейкоцитов, гемоглобина и тромбоцитов. Значения, которые сильно отклоняются от нормы, приводят к ослаблению иммунной системы, что может объяснить частые инфекции и ощущение, что вы всегда находитесь на грани гриппа. Этого, наряду с другими признаками, такими как усталость или синяки, должно быть достаточно, чтобы спланировать визит к врачу.
3. Вы постоянно уставшие и обессилившие
Это, вероятно, наиболее распространенные симптомы лейкемии, вызванные анемией (уменьшением объема красных кровяных телец). Эти симптомы со временем ухудшаются по мере прогрессирования болезни. При некоторых формах лейкемии большое количество лейкоцитов может сделать кровь более густой, а это означает, что поток через мелкие кровеносные сосуды в мозг замедляется. Эти проблемы могут вызвать усталость.
4. Увеличение лимфатических узлов
Если вы заметили безболезненное увеличение лимфатических узлов на шее, подмышках или паху во время принятия душа, это может быть легкий воспалительный процесс. Однако, если узелки остаются увеличенными или продолжают расти, возможно, это симптом лейкемии или лимфомы. Поскольку лейкемия также влияет на лимфатические узлы, которые помогают фильтровать кровь, если кровь поражена раковыми клетками, клетки могут накапливаться в узлах и, таким образом, расти.
5. Вам холодно, Вы бледны
Недостаток эритроцитов также может привести к анемии, которая вызывает бледность кожи, одышку и чувство постоянного холода.
6. Ваши кости болят
Боль в костях, похожая на ту, которую вы чувствуете при гриппе, бывает относительно редко, но, следовательно, это явный признак того, что вы страдаете лейкемией. Больные клетки образуются внутри костного мозга, поэтому, если вы испытываете легкую или сильную боль в костях, лучше немедленно обратиться за медицинской помощью. У очень бледных пациентов болезнь быстро прогрессирует. Такие пациенты обычно очень устают, потому что, если количество эритроцитов настолько низкое, что вызывает бледность, вероятно, даже самая короткая прогулка до туалета станет для вас проблемой.
7. Затрудненное дыхание
По мере нарастания слабости и утомляемости усиливаются и другие симптомы, одним из которых является одышка в результате анемии или, в гораздо более редких случаях, злокачественных новообразований грудной клетки. Возникают затруднения с дыханием, у человека легко перехватывает дыхание, а попытка переместиться из одного конца комнаты в другой может создать проблему.
8. Ночная потливость
Ночная потливость нередко бывает результатом инфекции, которая может быть связана с лейкемией. Если вы часто просыпаетесь на промокших от пота простынях, обратитесь к врачу.
9. У Вас странная сыпь
Проблемы с кожей указывают на болезнь, так как симптомы особенно заметны. Пятна, которые вы не можете не заметить из-за их размера, безболезненности и того, что они обычно расположены в области лодыжки, указывают на низкое количество тромбоцитов и являются одним из симптомов лейкемии. Чаще всего они возникают вокруг лодыжек, потому что в течение дня гравитация заставляет жидкость тела скапливаться у основания конечностей.
10. Вы часто болеете
Этот симптом часто возникает при клеточном лейкозе. У больных увеличена селезенка, а иногда наблюдаются такие симптомы, как тошнота, запор или диарея. Вы можете почувствовать большую массу в брюшной полости, там, где находится селезенка.
Гродненская областная детская клиническая больница
Заведующий 8 хирургическим отделением Хмеленко А.И.
Термические ожоги
Термические ожоги - это ожоги пламенем, горячим паром, горячей или горящей жидкостью, кипятком, от соприкосновения с раскаленными предметами, солнечные ожоги. Термические ожоги могут возникать в результате воздействия светового излучения, пламени, кипятка или другой горячей жидкости, пара, горячего воздуха или горячих предметов.
От ожога живые ткани погибают, прежде всего, вследствие непосредственного воздействия на них пламени, горячих предметов, пара, жидкостей, температура которых превышает 50 – 55°С. Но известно, что во время длительного воздействия на тело человека инфракрасного излучения термические ожоги могут возникать и при более низких температурах (43-44°С). При температуре 60-70°С возникает частичная денатурация тканевых белков, а при 100°С и выше - полная денатурация.
Глубина ожога зависит от температуры и продолжительности ее воздействия на тело. Чем выше температура и дольше экспозиция, тем глубже ожог. Известны молниеносные ожоги, которые бывают поверхностными, несмотря на очень высокую температуру, когда вредное воздействие длится доли секунды (взрыв атомной бомбы, газа в шахте и т.д.). Но не все участки тела одинаково чувствительны к высокой температуре. На шее, в промежности или паховых участках ожог будет глубже, чем на ладонях, подошвах, где грубый эпидермис надежнее защищает подчиненные слои кожи и ткани от повреждающего фактора.
Низкая теплопроводность кожи снижает температуру, и поэтому подавляющее большинство термических ожогов ограничивается ее поверхностным поражением. Однако очень нагретые твердые предметы (металл, песок, кирпич и т.д.) отдают так много теплоты, что возникают глубокие ожоги - первичное коагуляционное омертвение тканей. Коагуляционный некроз возникает также при действии на кожу пламени. Под влиянием горячих жидкостей и пара не возникает обезвоживание тканей, и поэтому образуется влажный колликвационный некроз.
Классификация термических ожогов по А.Вишневскому:
I степень - эритема кожи, II - наличие пузырей; III А степень - поверхностный некроз кожи, при котором возможна островковая эпителизация кожи; III Б степень - полный некроз всех слоев кожи; IV степень - некроз кожи и подлежащих тканей.
При термическом ожоге III А степени возникает коагуляция мальпигиевого и частично сосочкового слоя дермы. Эту степень ожога определяют после очистки ожоговой поверхности от пузырей и некротических тканей и появления мелких эпителиальных островков. Таким образом, ожоги III А степени, если не возникает нагноение, могут заживать самостоятельно за счет эпителиальных элементов дермы и придатков кожи. Поэтому ожоги III А степени относят к поверхностным ожогам.
Нагноение ожоговой поверхности ведет к вторичному некрозу эпителиальных островков под влиянием протеолитических ферментов раны приближает ее к ожогу III Б степени. Ожоги III Б степени характеризуются некрозом всех слоев кожи, который доходит до подкожной клетчатки, а IV степени - в более глубоких тканей.
Причины ожогов
Термические ожоги возникают в результате воздействия высокой температуры:
— открытый огонь поражает большую поверхность, вызывая ожоги преимущественно второй степени.
— горячая жидкость может вызывать небольшие по площади, но глубокие ожоги.
— ожог паром обычно происходит на большой площади, но не бывает глубоким.
— контакт с раскаленными предметами вызывает четко очерченный и глубокий ожог – вплоть до четвертой степени.
— химические ожоги возникают в результате контакта с опасными веществами: кислотами и щелочами. Особенно опасны ожоги, вызванные попаданиями этих веществ в дыхательные пути и пищеварительный тракт.
— электрические ожоги возникают в точках входа и выхода электрического заряда в тело. Они занимают небольшую площадь, но могут быть очень глубокими. Кроме того, при коротком замыкании электропроводки может произойти ожог вольтовой дугой. Он напоминает ожог открытым пламенем.
Первая помощь при легких бытовых ожогах:
- Охладите обожженное место прохладной проточной водой в течение нескольких минут. Не используйте сильный напор воды.
- Не используйте лед, снег, замороженные продукты для охлаждения ожога. Низкие температуры могут быстро вызвать обморожение, поскольку кожа в месте ожога уже повреждена и не выполняет свою защитную функцию.
- Ожоги первой степени или небольшие ожоги второй степени можно лечить при помощи сертифицированных мазей или спреев от ожогов. Запомните: подобные мази должны быть изготовлены строго на водной основе.
- Никогда не смазывайте ожоги маслом, салом или любым другим жиром, включая жирные кремы. Масляная пленка удерживает тепло внутри кожи и делает ожог более глубоким.
- Не вскрывайте самостоятельно волдыри, оставшиеся от ожога – так вы рискуете занести инфекцию. Ожоги склонны к воспалению и развитию нагноения чаще, чем другие травмы.
- Если ожог вызывает сильные боли, озноб или лихорадку – немедленно обратитесь к врачу.
Как предотвратить ожоги
Большинство ожогов можно предотвратить. Предотвратить ожоги у малышей помогут простые правила:
- Не позволяйте маленькому ребенку самостоятельно открывать краны в ванной и на кухне до тех пор, пока он не будет уметь смешивать горячую и холодную воду. Даже вода температурой 60°С может вызвать серьезный ожог всего за полминуты контакта с ней.
- Не переносите горячие жидкости и пищу над теми местами, где играет ребенок.
- Не открывайте духовку, если на кухне находится маленький ребенок.
- Во время пикника не позволяйте малышу приближаться к мангалу. Играйте с ребенком подальше от того места, где готовится шашлык.
- При готовке на плите включайте дальние конфорки и поверните кастрюли ручками внутрь. Это позволит и вам самим уберечься от случайного переворачивания горячей кастрюли или сковороды.
- Не откладывайте починку неисправных электрических розеток и вилок. Не используйте приборы с неисправной проводкой.
- Откажитесь от использования обогревателей с открытой спиралью.
- Не учите ребенка пользоваться зажигалками или спичками, пока не будете уверены, что он понимает их потенциальную опасность. Храните подобные предметы в тех местах, куда ребенок не может добраться.
- Никогда не приносите в дом, где есть маленькие дети, любые едкие жидкости. Бытовую химию убирайте на шкафы, а лучше – под замок.
- Не позволяйте детям запускать фейерверки – в том числе и играть с бенгальскими огнями, хлопушками или небольшими петардами.
Самое важное
Ожоги происходят под воздействием различных горячих предметов, жидкости, пара и даже едких химических веществ.
Если ожоги глубоки и велики по площади – немедленно вызывайте бригаду скорой помощи.
Никогда не смазывайте место ожога жиром и не прикладывайте лед к пораженной коже.

Повышенная температура тела является нормальной и даже желательной реакцией организма на болезнь. И температуру ниже 38,5 градусов сбивать не рекомендуется (за некоторым исключением). Но что делать, если температура высокая, а сбить ее не получается или же сбивается с большим трудом? Напомним некоторые нюансы, о которых забывают родители.
Обезвоживание (нехватка жидкости). Без воды препараты (любые, в том числе и жаропонижающие) плохо всасываются, медленнее распределяются по организму и, соответственно, действуют не так быстро, как должны. И не забываем, что снижение температуры связано с потерей тепла через кожу — потение, а если потеть «не чем», то и температура будет выше.
Вывод: ребенка поить обязательно! Питье должно быть не слишком сладким, не слишком кислым, без добавок и консервантов, немного теплым (близким к температуре тела). Можно давать воду — питьевую или кипяченую, (но не газированную!), морсы, отвар из шиповника или травяные чаи (внимание, детям с аллергией с осторожностью), компот из сухофруктов (изюм, курага), обычный чай (можно с лимоном или малиной), минеральную воду без газов.
Поим часто, можно небольшими порциями. Не нужно «вливать» в ребенка за один раз пол-литра чая или компота, лучше по пару глотков, но каждые 10-15 мин. Если ребенок отказывается пить из кружки, можно пробовать напоить из поильника, бутылочки для питья, из чайной ложки, из шприца без иглы.
Температура выше 38,5 и продолжает расти, ребенка напоить не получается — в больницу!
Сухой воздух и жара в комнате. Как говорит известный доктор Комаровский: «в комнате, где лежит больной ребенок, должно быть прохладно и влажно». Температура воздуха в идеале должна быть ближе к 19-20 градусам и влажность 40-60% .
Неподходящая одежда. Одежда должна быть свободной, не жаркой, из натуральных материалов. Если ребенок потеет, ее нужно чаще менять. Кутать температурящего ребенка в одеяло нельзя, так как нарушаются процессы терморегуляции.
Завышенные требования. Не стоит добиваться снижения температуры до 37, а то и 36.6 градусов, если у ребенка 39. Снижение до 38,5 градусов уже достаточно. Главное, чтобы улучшилось самочувствие ребенка.
Время. Температура не начнет снижаться мгновенно и даже через 2-5 минут. Препарату необходимо время для всасывания и распространения по организму, а это не менее часа. Только спустя час можно оценить эффективность жаропонижающего.
Неправильный выбор формы и/или дозы лекарства. Есть два типа жаропонижающих — с парацетамолом или ибупрофеном. А вот формы различны — свечи, таблетки, сиропы, раствор.
До года и в случае рвоты оптимально использовать ректальные свечи. Сироп подходит детям от 1 года до 4-5 лет.
Дозу лекарства необходимо рассчитывать на вес ребенка согласно инструкции к препарату, а ни в коем случае не «на глаз».
Разовая доза ПАРАЦЕТАМОЛА 15 мг/кг, интервал между приемами — 6 часов.
Разовая доза ИБУПРОФЕНА 10 мг/кг, интервал между приемами – 8 часов. В сутки принимать лекарство можно не более 3 раз.
Если жаропонижающий препарат не подействовал — температура не снизилась на 1 градус в течение часа, можно дать препарат с другим действующим веществом.
Какую температуру держит рука человека на металле
Выполнены 4 серии экспериментов на взрослых беспородных собаках. Изучена температурная реакция тканей в области имплантации разного типа титановых накостных пластин (без отверстий и с отверстиями) с гидроксиапатитным покрытием, изготовленных методом 3D печати. в зависимости от серии эксперимента, биоактивное покрытие было нанесено методом микродугового оксидирования (МДО) или высокочастотного магнетронного распыления (КФ ВЧМР). в течение первых двух недель после имплантации температура тканей повышалась, что не зависело от типа изделия и способа нанесения биоактивного покрытия. Через 3 недели эксперимента динамика температурной реакции зависела от типа имплантата, а способ нанесения покрытия не оказывал значимого влияния. Через 4 недели после имплантации значения изучаемого показателя во всех сериях нормализовались. Полученные данные будут использованы при оценке особенностей кровообращения в тканях области имплантации тестируемых изделий и учтены при анализе результатов гистологического исследования. Это позволит определить оптимальную пористость и топографию поверхности для накостных и внутрикостных имплантатов с биоактивным гидроксиапатитным покрытием, изготовленных из титановых сплавов с помощью аддитивных технологий.

1. Ахтямов И.Ф. Исследование взаимодействия биосовместимого покрытия из смеси нитридов металлов IV группы с тканями живого организма / И.Ф. Ахтямов, Э.Б. Гатина, Ф.Ф. Кадыров, М.Ф. Шаехов, Ф.В. Шакирова // Вестник Казанского технологического университета. – 2012. – Т.15(20). – С. 176–178.
2. Карлов А.В., Шахов В.П. Системы внешней фиксации и регуляторные механизмы оптимальной биомеханики. – Томск: СТТ, 2001. – C. 480.
3. Кобызев А.Е., Кононович Н.А., Краснов В.В. Температурная реакция тканей при сколиотической деформации поясничного отдела позвоночника и в условиях ее коррекции (экспериментальное исследование) // Успехи современного естествознания. – 2015. – № 9–3. – С. 429–433.
4. Некоторые аспекты применения термографии при реабилитации пациентов с нарушением функций опорно-двигательной и нервной систем / В.И. Виноградов, И.С. Веретенов, В.Н. Слезко, г. И. Пугач, В.А. Ланда, г. И. Большакова // Функциональная диагностика. – 2005. – № 3. – С. 72–78.
5. Попков А.В., Попков Д.А., Кононович Н.А., Горбач Е.Н., Твердохлебов С.И. Возможности остеогенной активности интрамедуллярных имплантатов в зависимости от технологии нанесения кальций-фосфатного покрытия (экспериментальное исследование) // Успехи современного естествознания. – 2015. – № 5. – С. 142–145.
6. Твердохлебов С.И., Игнатов В.П., Степанов И.Б., Сивин Д.О., Петлин Д.Г. Гибридный метод формирования биокомпозитов на поверхности имплантатов из нержавеющей стали // Биотехносфера. – 2012. – № 5–6 (23–24). – C. 63–69.
7. Barrere F., van der Valk C.M., Dalmeijer R.A. et al. Osteogenecity of octacalcium phosphate coatings applied on porous metal implants // J. Biomed. Mater. Res. – 2003. – Vol. 66A. – P. 779–788.
8. Helfet D.L. tt al. AO philosophy and principles of fracture managmentits evolution and evaluatijn. J. Bone Joint Surg. Am. 85– A:1156, 2003.
9. Tverdokhlebov S.I., Bolbasov E.N., Shesterikov E.V., Malchikhina A.I., Novikov V.A., Anissimov Y.G. Research of the surface properties of the thermoplastic copolymer of Vinilidene Fluoride and Tetrafluoroethylene modified with radio-frequency magnetron sputtering for medical application // Applied surface science – 2012 – Vol. 263 – pp. 187–194.
10. Yuan H., Van den Doel M., Li S.H. et al. A comparison of the osteoinductive potential of two calcium phosphate ceramics implanted intramuscularly in goats // J. Mater. Sci. Mater. Med. – 2002. – Vol. 13. – P. 1271–1275.
В настоящее время в медицине одним из актуальных направлений помощи больным с повреждениями и заболеваниями опорнодвигательного аппарата является поиск новых технологий, основанных на использовании имплантатов с биоактивным покрытием. Их основная цель – не только гарантировать успех лечения, но и осуществить это в очень короткие сроки [1, 2, 8].
Остеоиндуктивные и остеокондуктивные свойства используемых материалов зависят от химического состава поверхности (наличие биоактивных элементов), ее топографии и архитектоники (шероховатость, размер пор) [10].
Доказано, что металлические имплантаты, поверхность которых покрыта наночастицам фосфатов кальция, стимулируют остеогенную активность. при этом степень последней может зависеть от способа нанесения биоактивного слоя [5–7, 9].
Одним из критериев обоснования использования новых видов имплантационных материалов и изделий медицинского назначения являются результаты доклинических испытаний. Основная цель данного вида исследований заключается в определении биологического действия и местной реакции тканей на имплантацию.
В этом плане, одним из информативных является методов оценки местной температурной реакции, что косвенно может отражать особенности локального кровообращения, интенсивность воспалительной реакции и активность процессов костеобразования в целом. в клинической практике этот метод может использоваться в качестве дополнительного при диагностике, прогнозе течения и оценки качества проводимого лечения различных патологических состояний опорно-двигательной системы [3, 4].
Целью настоящего исследования являлось определение температурной реакции тканей в области имплантации накостных титановых пластин с биоактивным покрытием, нанесенным разными способами.
Материалы и методы исследования
Проведено пилотное исследование на взрослых (старше 1 года) беспородных собаках обоего пола. Животные были разделены на 4 серии в зависимости от вида имплантируемого изделия и способа нанесения биоактивного покрытия.
Во всех случаях в условиях операционной с медиальной поверхности диафиза большеберцовых костей моделировали повреждение надкостницы. Для этого выполняли продольный разрез параоссальных мягких тканей протяженностью 2,5 см. Надкостницу разрезали так же в продольном направлении и при помощи шпателя отслаивали от компактной кости. После этого на корковую пластинку устанавливали титановые накостные имплантаты, выполненные в виде пластин шириной 1,0 см, длиной 2,0 см и толщиной 1 мм. при этом пластины имели изгиб, повторяющий рельеф кости. Затем на надкостницу и мягкие ткани накладывали узловые швы. Все изделия были изготовлены с использованием аддитивных технологий (методом 3D печати).
Во всех сериях на поверхности имплантатов был слой биоактивного покрытия на основе гидроксиапатита.
В серии 1 использовали пластины без отверстий (n=3), а в качестве способа нанесения покрытия был применен метод микродугового оксидирования (КФ МДО). Данная технология позволяет формировать покрытия с развитой пористой поверхностью.
В серии 2 на пластины без отверстий (n=3) было нанесено покрытие методом высокочастотного магнетронного распыления (КФ ВЧМР). Оно позволяет формировать тонкие плотные, эластичные кальций-фосфатные покрытия с высокими адгезионными свойствами.
В серии 3 и 4 использовали пластины с отверстиями с покрытием нанесенным методом КФ МДО (n=3) и КФ ВЧМР (n=3) соответственно.
Температурную реакцию покровных тканей в области расположения имплантата регистрировали в периоды: перед операцией, через 7, 14, 21 и 28 суток после выполнения оперативного вмешательства. Для этого использовали реограф-полианализатор РГПА-6/12 «РЕАН-ПОЛИ» (НПКФ «МЕДИКОМ-МТД», Россия) и входящий в комплект принадлежностей, контактный температурный датчик термисторного типа – ДТ-3. Показания снимали с участков, освобожденных от шерстного покрова. в качестве физиологической нормы, которую принимали за 100%, использовали результаты, полученные перед операцией, а так же данные от 15 клинически здоровых (интактных) животных соответствующего возраста.
Дополнительно выполняли визуальную оценку состояния мягких тканей в проекции имплантации.
Исследования проводили в утренние часы перед первым кормлением. Температура воздуха в помещении во время проведения обследования составляла 28,6 ± 0,1°С.
При выборе основных периодов обследования руководствовались регламентирующими стандартами, относящимися к времени кратковременной имплантации биостабильных материалов, которое в норме составляет от 1 до 4 недель (по «ГОСТ Р ИСО 10993–6–2009. Национальный стандарт Российской Федерации. Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 6. Исследования местного действия после имплантации»).
Анализ количественных данных проводили методами описательной статистики. Результаты исследований обрабатывали методами непараметрической статистики (критерий Вилкоксона для независимых выборок). Различия показателей считали достоверными при р ? 0,05.
Эксперименты выполнены на базе вивария ФГБУ «РНЦ «ВТО» им. акад. Г.А. Илизарова» Минздрава России. Животные содержались в индивидуальных боксах (по одному). Получали одинаковые стандартные, сбалансированные по питательным веществам, корма и чистую питьевую воду.
До начала исследований было получено одобрение Комитета по этике ФГБУ «РНЦ «ВТО» им. акад. Г.А. Илизарова» на их выполнение.
Результаты исследования и их обсуждение
При визуальной оценке состояния мягких тканей в проекции имплантации тестируемых материалов определили, что процессы эпителизации раневых поверхностей в области швов протекали без особенностей. Признаков острого воспаления, гематомы и очагов некроза выявлено не было. Швы были сняты в общепринятые сроки (через 7–10 суток после оперативного вмешательства).
При изучении температурных данных выявили, что эти значения у интактных животных и экспериментальных собак в области планируемого оперативного вмешательства варьировали в диапазоне 30,06–33,76°С и в среднем составляли 31,43±1,1°С.
Во всех сериях опытов через 7 суток после операции регистрировали однонаправленные изменения локальной температуры тела в сторону увеличения, значения которой между собой достоверных различий не имели (р=0,8). Разница показателей по отношению к нормальным значениям составляла в среднем 2,78±0,5°С (p=0,002). Следует отметить, что в сериях 1 и 3, когда применяли накостные пластины с покрытием, нанесенным методом КФ МДО, температура тканей в зоне расположения имплантатов была выше на 0,75°С в сравнении с аналогичными значениями при использовании пластин покрытых методом КФ ВЧМР (серии 2 и 4).
К 14 суткам эксперимента температура тканей продолжала равномерно увеличиваться во всех сериях. Ее значения были достоверно выше нормы на 3,69±0,3°С (p=0,002) и составляли 35,12±0,3°С. в этот период, не смотря на отсутствие достоверных различий между сериями, температура тканей в сериях 1 и 2 (пластины без отверстий) была выше на 0,42°С чем в случаях, когда использовали имплантаты с отверстиями.
Через 21 сутки поле операции регистрировали наиболее выраженные различия изучаемого показателя между сериями в зависимости от типа изделия. Так, в сериях с пластинами без отверстий (1 и 2) температура в области расположения имплантата продолжала увеличиваться и составляла в среднем 35,29±0,3°С. Тогда как в сериях 3 и 4 – происходило ее резкое достоверное понижение до верхней границы нормы. у этих животных разница по отношению к предыдущему сроку обследования была в среднем 2,0°С.
Динамика локальной температуры тканей в периоде эксперимента представлена на рисунке.
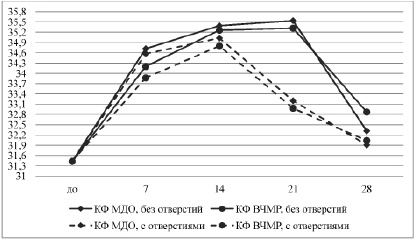
Динамика температурной реакции тканей в области расположения накостных имплантатов с биоактивным покрытием, изготовленных из титановых сплавов по аддитивным технологиям
Таким образом, в результате выполненного исследования была определена местная температурная реакция тканей на материалы, имплантируемые под поврежденную надкостницу большеберцовой кости собаки в периоды 1–4 недели эксперимента. в качестве тестируемых образцов использовали накостные пластины без отверстий и с отверстиями, изготовленные из титана по аддитивной технологии, методом 3D печати. Каждая из пластин была покрыта слоем гидроксиапатита, нанесенного по технологии микродугового оксидирования, либо высокочастотного магнетронного распыления.
Анализ полученных результатов показал, что в течение первых двух недель после операции температура тканей в области расположения имплантатов резко повышалась и ее динамика особо не зависела от типа тестируемого изделия, а также способа нанесения биоактивного покрытия. не смотря на то, что в этот период при использовании накостных пластин с покрытием, нанесенным методом КФ МДО, температурные значения были несколько выше, чем у изделий с покрытием КФ ВЧМР, мы считаем, что подобный эффект мог быть обусловлен в большей степени самой процедурой хирургического вмешательства.
Заключение
Полученные данные в последующем будут использованы как дополнительные, при оценке особенностей кровообращения в тканях области имплантации тестируемых изделий. Будут учитываться при анализе результатов гистологических исследований. Подобный комплексный подход позволит определить оптимальную пористость и топографию поверхности для накостных и внутрикостных имплантатов с биоактивным покрытием на основе гидроксиапатита, изготовленных из титановых сплавов с помощью аддитивных технологий.
Данное исследование выполнено при финансовой поддержке гранта РНФ «Установление закономерностей остеоинтеграции медицинских имплантатов на основе аддитивного производства с биоактивным покрытием», соглашение № 16–17–00176, в рамках задачи по выявлению оптимальной пористости и топографии поверхности для адгезии биоактивного покрытия на основе гидроксиапатита.
Читайте также:
