Медь к какой группе относится металлов
Обновлено: 20.05.2024
1. Химический элемент (Сu), ковкий металл желтого цвета с красноватым отливом (широко применяется в промышленности). Добыча меди. Надраить м. самовара. Изготовить из меди котелок.
2. собир. Изделия из этого металла. Вся м. в подвале позеленела. / О музыкальных инструментах из такого металла (преимущественно духовых). М. оркестра.
4. обычно чего. Красновато-желтый, цвета такого металла. Осенняя м. листьев. Любоваться медью заката.
(лат. Cuprum), химический элемент I группы периодической системы. Металл красного (в изломе розового) цвета, ковкий и мягкий; хороший проводник тепла и электричества (уступает только серебру); плотность 8,92 г/см 3 , tпл 1083,4°C. Химически малоактивна; в атмосфере, содержащей CO2, пары Н2O и др., покрывается патиной — зеленоватой плёнкой основного карбоната (ядовит). Из минералов важны борнит, халькопирит, халькозин, ковеллин, малахит; встречается также самородная медь. Главное применение — производство электрических проводов. Из меди изготовляют теплообменники, трубопроводы. Более 30% меди идёт на сплавы.МЕДЬ (лат. Cuprum), Cu (читается «купрум»), химический элемент с атомным номером 29, атомная масса 63,546. Латинское название меди происходит от названия острова Кипра (Cuprus), где в древности добывали медную руду; однозначного объяснения происхождения этого слова в русском языке нет.
Природная медь состоит из двух стабильных нуклидов (см. НУКЛИД) 63 Cu (69,09% по массе) и 65 Cu (30,91%). Конфигурация двух внешних электронных слоев нейтрального атома меди 3s 2 p 6 d 10 4s 1 . Образует соединения в степенях окисления +2 (валентность II) и +1 (валентность I), очень редко проявляет степени окисления +3 и +4.
В периодической системе Менделеева медь расположена в четвертом периоде и входит в группу IВ, к которой относятся такие благородные металлы, как серебро (см. СЕРЕБРО) и золото (см. ЗОЛОТО (химический элемент)) .
Радиус нейтрального атома меди 0,128 нм, радиус иона Cu + от 0,060 нм (координационное число 2) до 0,091 нм (координационное число 6), иона Cu 2+ — от 0,071 нм (координационное число 2) до 0,087 нм (координационное число 6). Энергии последовательной ионизации атома меди 7,726, 20,291, 36,8, 58,9 и 82,7 эВ. Сродство к электрону 1,8 эВ. Работа выхода электрона 4,36 эВ. По шкале Полинга электроотрицательность меди 1,9; медь принадлежит к числу переходных металлов. Стандартный электродный потенциал Cu/Cu 2+ 0,339 В. В ряду стандартных потенциалов медь расположена правее водорода и ни из воды, ни из кислот водорода не вытесняет.
Простое вещество медь — красивый розовато-красный пластичный металл.
Нахождение в природе
В земной коре содержание меди составляет около 5·10 -3 % по массе. Очень редко медь встречается в самородном виде (см. МЕДЬ САМОРОДНАЯ) (самый крупный самородок в 420 тонн найден в Северной Америке). Из руд наиболее широко распространены сульфидные руды: халькопирит (см. ХАЛЬКОПИРИТ) , или медный колчедан, CuFeS2 (30% меди), ковеллин (см. КОВЕЛЛИН) CuS (64,4% меди), халькозин (см. ХАЛЬКОЗИН) , или медный блеск, Cu2S (79,8% меди), борнит (см. БОРНИТ) Cu5FeS4.(52—65% меди). Существует также много и оксидных руд меди, например: куприт (см. КУПРИТ) Cu2O, (81,8% меди), малахит (см. МАЛАХИТ) CuCO3·Cu(OH)2 (57,4% меди) и другие. Известно 170 медьсодержащих минералов, из которых 17 используются в промышленных масштабах.
Различных руд меди много, а вот богатых месторождений на земном шаре мало, к тому же медные руды добывают уже многие сотни лет, так что некоторые месторождения полностью исчерпаны. Часто источником меди служат полиметаллические руды, в которых, кроме меди, присутствуют железо, цинк, свинец, и другие металлы. Как примеси медные руды обычно содержат рассеянные элементы (см. РАССЕЯННЫЕ ЭЛЕМЕНТЫ) (кадмий, селен, теллур, галий, германий и другие), а также серебро, а иногда и золото. Для промышленных разработок используют руды, в которых содержание меди составляет немногим более 1% по массе, а то и менее.
В морской воде содержится примерно 1·10 -8 % меди.
Получение
Промышленное получение меди — сложный многоступенчатый процесс. Добытую руду дробят, а для отделения пустой породы используют, как правило, флотационный метод обогащения. Полученный концентрат (содержит 18—45% меди по массе) подвергают обжигу в печи с воздушным дутьем. В результате обжига образуется огарок — твердое вещество, содержащее, кроме меди, также и примеси других металлов. Огарок плавят в отражательных печах или электропечах. После этой плавки, кроме шлака, образуется так называемый штейн (см. ШТЕЙН (в металлургии)) , в котором содержание меди составляет до 40—50%.
Далее штейн подвергают конвертированию — через расплавленный штейн продувают сжатый воздух, обогащенный кислородом. В штейн добавляют кварцевый флюс (песок SiO2). В процессе конвертирования содержащийся в штейне как нежелательная примесь сульфид железа FeS переходит в шлак и выделяется в виде сернистого газа SO2:
2FeS + 3O2 + 2SiO2 = 2FeSiO3 + 2SO2
Одновременно сульфид меди(I) Cu2S окисляется:
2Cu2S + 3О2 = 2Cu2О + 2SO2
Образовавшийся на этой стадии Cu2О далее реагирует с Cu2S:
2Cu2О + Cu2S = 6Cu + SО2
В результате возникает так называемая черновая медь, в которой содержание самой меди составляет уже 98,5—99,3% по массе. Далее черновую медь подвергают рафинированию. Рафинирование на первой стадии — огневое, оно заключается в том, что черновую медь расплавляют и через расплав пропускают кислород. Примеси более активных металлов, содержащихся в черновой меди, активно реагируют с кислородом и переходят в оксидные шлаки.
На заключительной стадии медь подвергают электрохимическому рафинированию в сернокислом растворе, при этом черновая медь служит анодом, а очищенная медь выделяется на катоде. При такой очистке примеси менее активных металлов, присутствовавшие в черновой меди, выпадают в осадок в виде шлама (см. ШЛАМ) , а примеси более активных металлов остаются в электролите. Чистота рафинированной (катодной) меди достигает 99,9% и более.
Физические и химические свойства
Кристаллическая решетка металлической меди кубическая гранецентрированная, параметр решетки а = 0,36150 нм. Плотность 8,92 г/см 3 , температура плавления 1083,4 °C, температура кипения 2567 °C. Медь среди всех других металлов обладает одной из самых высоких теплопроводностей и одним из самых низких электрических сопротивлений (при 20 °C удельное сопротивление 1,68·10 -3 Ом·м).
В сухой атмосфере медь практически не изменяется. Во влажном воздухе на поверхности меди в присутствии углекислого газа образуется зеленоватая пленка состава Cu(OH)2·CuCO3. Так как в воздухе всегда имеются следы сернистого газа и сероводорода, то в составе поверхностной пленки на металлической меди обычно имеются и сернистые соединения меди. Такая пленка, возникающая с течением времени на изделиях из меди и ее сплавов, называется патиной. Патина предохраняет металл от дальнейшего разрушения. Для создания на художественных предметах «налета старины» на них наносят слой меди, который затем специально патинируется.
При нагревании на воздухе медь тускнеет и в конце концов чернеет из-за образования на поверхности оксидного слоя. Сначала образуется оксид Cu2O, затем — оксид CuO.
Красновато-коричневый оксид меди(I) Cu2O при растворении в бромо- и иодоводородной кислотах образует, соответственно, бромид меди(I) CuBr и иодид меди(I) CuI. При взаимодействии Cu2O с разбавленной серной кислотой возникают медь и сульфат меди:
Cu2O + H2SO4 = Cu + CuSO4 + H2O.
При нагревании на воздухе или в кислороде Cu2O окисляется до CuO, при нагревании в токе водорода — восстанавливается до свободного металла.
Черный оксид меди (II) CuO, как и Cu2O, c водой не реагирует. При взаимодействии CuO с кислотами образуются соли меди (II):
CuO + H2SO4 = CuSO4 + H2O
При сплавлении со щелочами CuO образуются купраты, например:
CuO + 2NaOH = Na2CuO2 + H2O
Нагревание Cu2O в инертной атмосфере приводит к реакции диспропорционирования:
Cu2O = CuO + Cu.
Такие восстановители, как водород, метан, аммиак, оксид углерода (II) и другие восстанавливают CuO до свободной меди, например:
CuO +СО = Cu + СО2.
Кроме оксидов меди Cu2O и CuO, получен также темно-красный оксид меди (III) Cu2O3, обладающий сильными окислительными свойствами.
Медь реагирует с галогенами (см. ГАЛОГЕНЫ) , например, при нагревании хлор реагирует с медью с образованием темно-коричневого дихлорида CuCl2. Существуют также дифторид меди CuF2 и дибромид меди CuBr2, но дииодида меди нет. И CuCl2, и CuBr2 хорошо растворимы в воде, при этом ионы меди гидратируются и образуют голубые растворы.
При реакции CuCl2 с порошком металлической меди образуется бесцветный нерастворимый в воде хлорид меди (I) CuCl. Эта соль легко растворяется в концентрированной соляной кислоте, причем образуются комплексные анионы [CuCl2] - , [CuCl3] 2- и [СuCl4] 3- , например за счет процесса:
CuCl + НCl = H[CuCl2]
При сплавлении меди с серой образуетcя нерастворимый в воде сульфид Cu2S. Сульфид меди (II) CuS выпадает в осадок, например, при пропускании сероводорода через раствор соли меди (II):
H2S + CuSO4 = CuS + H2SO4
C водородом, азотом, графитом, кремнием медь не реагирует. При контакте с водородом медь становится хрупкой (так называемая «водородная болезнь» меди) из-за растворения водорода в этом металле.
В присутствии окислителей, прежде всего кислорода, медь может реагировать с соляной кислотой и разбавленной серной кислотой, но водород при этом не выделяется:
2Cu + 4HCl + O2 = 2CuCl2 + 2H2O.
С азотной кислотой различных концентраций медь реагирует довольно активно, при этом образуется нитрат меди (II) и выделяются различные оксиды азота. Например, с 30%-й азотной кислотой реакция меди протекает так:
3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO + 4H2O.
С концентрированной серной кислотой медь реагирует при сильном нагревании:
Cu + 2H2SO4 = CuSO4 + SO2+ 2H2O.
Практическое значение имеет способность меди реагировать с растворами солей железа (III), причем медь переходит в раствор, а железо (III) восстанавливается до железа (II):
2FeCl3 + Cu = CuCl2 + 2FeCl2
Этот процесс травления меди хлоридом железа (III) используют, в частности, при необходимости удалить в определенных местах слой напыленной на пластмассу меди.
Ионы меди Cu 2+ легко образуют комплексы с аммиаком, например, состава [Cu(NH3)] 2+ . При пропускании через аммиачные растворы солей меди ацетилена С2Н2 в осадок выпадает карбид (точнее, ацетиленид) меди CuC2.
Гидроксид меди Cu(OH)2 характеризуется преобладанием основных свойств. Он реагирует с кислотами с образованием соли и воды, например:
Сu(OH)2 + 2HNO3 = Cu(NO3)2 + 2H2O.
Но Сu(OH)2 реагирует и с концентрированными растворами щелочей, при этом образуются соответствующие купраты, например:
Сu(OH)2 + 2NaOH = Na2[Cu(OH)4]
Если в медноаммиачный раствор, полученный растворением Сu(OH)2 или основного сульфата меди в аммиаке, поместить целлюлозу, то наблюдается растворение целлюлозы и образуется раствор медноаммиачного комплекса целлюлозы. Из этого раствора можно изготовить медноаммиачные волокна, которые находят применение при производстве бельевого трикотажа и различных тканей.
Применение
Медь, как полагают, — первый металл, который человек научился обрабатывать и использовать для своих нужд. Найденные в верховьях реки Тигр изделия из меди датируются десятым тысячелетием до нашей эры. Позднее широкое применение сплавов меди определило материальную культуру бронзового века (см. БРОНЗОВЫЙ ВЕК) (конец 4 — начало 1 тысячелетия до нашей эры) и в дальнейшем сопровождало развитие цивилизации на всех этапах. Медь и ее использовались для изготовления посуды, утвари, украшений, различных художественных изделий. Особенно велика была роль бронзы (см. БРОНЗА) .
С 20 века главное применение меди обусловлено ее высокой электропроводимостью. Более половины добываемой меди используется в электротехнике для изготовления различных проводов, кабелей, токопроводящих частей электротехнической аппаратуры. Из-за высокой теплопроводности медь — незаменимый материал различных теплообменников и холодильной аппаратуры. Широко применяется медь в гальванотехнике — для нанесения медных покрытий, для получения тонкостенных изделий сложной формы, для изготовления клише в полиграфии и др.
Большое значение имеют медные сплавы — латуни (см. ЛАТУНЬ) (основная добавка цинк, Zn), бронзы (сплавы с разными элементами, главным образом металлами — оловом, алюминием, берилием, свинцом, кадмием и другими, кроме цинка и никеля) и медно-никелевые сплавы, в том числе мельхиор (см. МЕЛЬХИОР) и нейзильбер (см. НЕЙЗИЛЬБЕР) . В зависимости от марки (состава) сплавы используются в самых различных областях техники как конструкционные, антидикционные, стойкие к коррозии материалы, а также как материалы с заданной электро- и теплопроводностью Так называемые монетные сплавы (медь с алюминием и медь с никелем) применяют для чеканки монет — «меди» и «серебра»; но медь входит в состав и настоящих монетного серебра и монетного золота.
Биологическая роль
Медь присутствует во всех организмах и принадлежит к числу микроэлементов, необходимых для их нормального развития (см. Биогенные элементы (см. БИОГЕННЫЕ ЭЛЕМЕНТЫ) ). В растениях и животных содержание меди варьируется от 10 -15 до 10 -3 %. Мышечная ткань человека содержит 1·10 -3 % меди, костная ткань — (1—26) ·10 -4 %, в крови присутствует 1,01 мг/л меди. Всего в организме среднего человека (масса тела 70 кг) содержится 72 мг меди. Основная роль меди в тканях растений и животных — участие в ферментативном катализе. Медь служит активатором ряда реакций и входит в состав медьсодержащих ферментов, прежде всего оксидаз (см. ОКСИДАЗЫ) , катализирующих реакции биологического окисления. Медьсодержащий белок пластоцианин участвует в процессе фотосинтеза (см. ФОТОСИНТЕЗ) . Другой медьсодержащий белок, гемоцианин (см. ГЕМОЦИАНИН) , выполняет роль гемоглобина (см. ГЕМОГЛОБИН) у некоторых беспозвоночных. Так как медь токсична, в животном организме она находится в связанном состоянии. Значительная ее часть входит в состав образующегося в печени белка церулоплазмина, циркулирующего с током крови и деставляющего медь к местам синтеза других медьсодержащих белков. Церулоплазмин обладает также каталитической активностью и участвует в реакциях окисления. Медь необходима для осуществления различных функций организма — дыхания, кроветворения (стимулирует усвоение железа и синтез гемоглобина), обмена углеводов и минеральных веществ. Недостаток меди вызывает болезни как растений, так и животных и человека. С пищей человек ежедневно получает 0,5—6 мг меди.
Сульфат меди и другие соединения меди используют в сельском хозяйстве в качестве микроудобрений и для борьбы с различными вредителями растений. Однако при использовании соединений меди, при работах с ними нужно учитывать, что они ядовиты. Попадание солей меди в организм приводит к различным заболеваниям человека. ПДК для аэрозолей меди составляет 1 мг/м 3 , для питьевой воды содержание меди должно быть не выше 1,0 мг/л.
Энциклопедический словарь . 2009 .
Полезное
Смотреть что такое "медь" в других словарях:
медь — медь, и … Русский орфографический словарь
медь — медь/ … Морфемно-орфографический словарь
МЕДЬ — жен. в чистом, корольковом виде называется красною, а в сплаве с цинком желтою или зеленою. | Медные деньги; | медная посуда. Медь, в продаже, вообще бывает: штыковая, дощатая, листовая (или латунь), прутковая. Медь дороже серебра: серебро… … Толковый словарь Даля
МЕДЬ — (символ Сu), переходный элемент красно розового цвета. Красноватая медь встречается в виде самородков, а также в составе нескольких руд, в том числе, куприта (оксид меди) и халькопирита (сульфид меди). Руды извлекают из окружающей их породы и… … Научно-технический энциклопедический словарь
медь — cu, мягкий, ковкий и пластичный металл красного цвета; химический элемент i группы периодической системы; ат. н. 29, ат. масса 63.546. Плотность 8920 кг/мі, температура плавления 1083.4 °C. Латинское cuprum происходит от названия о. Кипр,… … Энциклопедия техники
МЕДЬ — МЕДЬ, меди, мн. нет, жен. 1. Металл красноватого цвета, наиболее вязкий после железа, ковкий, широко употребительный. Красная медь (чистая медь). Желтая медь (сплав меди с цинком). 2. Медные деньги (разг.). Сдали сдачи серебром и медью. Толковый… … Толковый словарь Ушакова
МЕДЬ — (симв. Си), хим. элемент, порядковый номер 29; атомный вес 63,57, уд. в. 8,93; t° пл. 1 083°; принадлежит к числу металлов. В природе М. встречается иногда в чистом виде (самородная М.), но чаще в виде соединений, образующих медные руды.… … Большая медицинская энциклопедия
медь — сущ., ж., употр. сравн. часто Морфология: (нет) чего? меди, чему? меди, (вижу) что? медь, чем? медью, о чём? о меди 1. Медь это металл красно жёлтого цвета, который часто используется для изготовления монет, проводов и других изделий. Добыча меди … Толковый словарь Дмитриева
МЕДЬ — см. МЕДЬ (Си) содержится в сточных водах рудообогатительных комбинатов, металлургических, машиностроительных и электротехнических предприятий. Сульфат, карбонат, хлорокись и арсенат меди применяют как альгициды, фунгициды и моллюскоциды. Медь… … Болезни рыб: Справочник
МЕДЬ — (Cuprum), Cu, химический элемент I группы периодической системы, атомный номер 29, атомная масса 63,546; розовато красный металл, tпл 1083,4шC. Содержание в земной коре (4,7 5,5)?10 3% по массе. Медь главный металл электротехники, ее используют… … Современная энциклопедия
Медь к какой группе относится металлов
МЕДЬ
Cu (cuprum),
химический элемент IB подгруппы (семейства монетных металлов - Cu, Ag, Au) периодической системы элементов. Известна и широко используется с древних времен (медный век, бронзовый век). Медь наряду с серебром и золотом используется для чеканки монет, применяется в произведениях искусства и в электротехнике. Медь получают из ее руд: куприта, содержащего оксид меди, малахита, содержащей основной карбонат меди, халькозина (медный блеск) и халькопирита (медный колчедан), содержащих сульфид меди. Мировым лидером по производству меди считается Чили, затем идут США, Россия, Казахстан, Канада, Замбия, Заир, Польша и Перу.
Свойства. Медь - мягкий, тяжелый, ковкий, тягучий, вязкий и достаточно прочный металл красновато-желтого цвета в отраженном свете и зеленый в проходящем (в очень тонком слое). Чистая медь очень хорошо проводит тепло и электрический ток, уступая в этом только серебру, но ее электрическая проводимость резко падает в присутствии примесей мышьяка, сурьмы, кремния и др. Расплавленная медь поглощает воздух и после затвердевания в отливке остаются пузырьки воздуха, затрудняющие обработку. В ряду напряжений медь стоит после водорода и при реакции с кислотами не вытесняет из них водород, поэтому медь широко используется в гальванических элементах. Медь устойчива к коррозии при обычной температуре в сухом воздухе, но при нагревании окисляется, образуя оксиды меди(I) и меди(II): Cu2O и CuO. При долговременной атмосферной коррозии постепенно образует основной карбонат, по составу аналогичный малахиту: 2Cu + O2 + CO2 + H2O = Cu2(OH)2CO3. С галогенами медь соединяется уже при комнатной температуре, легко взаимодействует с серой и селеном; с водородом, азотом и углеродом не реагирует даже при высокой температуре. В отсутствие кислорода медь не реагирует ни с хлороводородной (соляной) кислотой, ни с разбавленной серной, но растворяется в горячей концентрированной серной кислоте (Cu + 2H2SO4 (r) CuSO4 + SO2 + 2H2O) и хорошо в азотной, образуя нитрат меди и оксиды азота. СВОЙСТВА МЕДИ
Атомный номер 29 Атомная масса 63,54 Изотопы
Температура плавления, ° С 1083 Температура кипения, ° С 2567 Плотность, г/см3 8,92 Твердость (по Моосу) 2,5 Содержание в земной коре, % (масс.) 0,007 Степени окисления +1, +2
Применение. Большая часть мирового производства меди используется в электротехнической промышленности для изготовления проводов. Листовая медь широко применяется для изготовления кровли, желобов, водостоков. Из-за коррозионной стойкости в морской воде, и в частности к действию морских организмов и растений, она является прекрасным материалом для кораблей. Медь часто используют в химической, пищевой промышленности и промышленности ферментов, для изготовления чайников, перегонных аппаратов, емкостей, теплообменников и другой утвари. Благодаря своему блеску и красивому цвету медь широко используется в декоративных изделиях и произведениях искусства, а также в гальванопластике и гравировании. Медь входит в состав многочисленных сплавов, которых известно более 1000. Самые распространенные из них - латуни (сплавы с цинком), бронзы (сплавы с оловом), медно-никелевые сплавы (мельхиор, нейзильбер, манганин, копель и т.д.); одним из наиболее распространенных применений меди является ее использование в сплавах для чеканки монет. Медь принадлежит к числу микроэлементов, необходимых для нормальной жизнедеятельности растений. Ее вносят в почву с микроудобрениями. Она способствует росту растений, повышению устойчивости против засухи, холода и некоторых заболеваний.
Соединения. Электронное строение атома меди 1s22s22p63s23p63d104s1. Атом меди легко отдает внешний электрон, образуя соединения Cu(I). Не все электроны на 3d-оболочке прочно удерживаются ядром, поэтому многие элементы способны оттягивать два электрона от атома меди, образуя устойчивый ион Cu2+. Соединения Cu(II) наиболее распространены и более стабильны, а относительно малый радиус иона и высокий заряд ядра позволяют меди проявлять акцепторные свойства с образованием комплексных ионов, например [[CuCl4]]2-, имеющего координационную связь. Ионы меди координируют молекулы воды в растворе, образуя стабильный комплексный ион [[Cu(H2O)4]]2+, который и вызывает голубую окраску разбавленных водных растворов соединений меди. Медь образует много соединений в степени окисления +1 и +2, но известны и некоторые нестабильные соединения меди в степени окисления +3. Соединения в степени окисления +1 обычно плохо растворяются в воде, являются восстановителями, легко окисляются на воздухе и, как правило, менее практически ценны и реже используются по сравнению с соединениями, в которых медь находится в степени окисления +2.
Соединения меди(I). Cu2O - темнокрасный кристаллический порошок, применяемый для изготовления рубинового стекла, окрашивания фарфора, гальванопластики металлических поверхностей. Хлорид меди(I) CuCl - серовато-белый кристаллический порошок, используемый как инсектицид, для очистки ацетилена и денитрации искусственного шелка. Кислота HCuCl2 (с комплексным анионом) используется в газовом анализе для поглощения CO.
Соединения меди(II). Оксид CuO - черный порошок, активный окислитель, используемый при сжигании органических соединений в элементном анализе. CuO используется также для производства солей, окраски в зеленый или голубой цвет стекла, фарфора, глиняных изделий, для очистки нефти от серы и в медицине. Гидроксид Cu(OH)2 - голубовато-зеленый порошок - в горячих растворах превращается в черный оксид меди(II). Гидроксид меди(II) растворяется в растворе тартрата щелочного металла с образованием тартрата меди CuC4H4O6 (реактив Фелинга), применяемого для обнаружения и определения восстанавливающих сахаров. Гидроксид меди(II) используется также как фунгицид в составе бордоской жидкости для уничтожения или предотвращения развития патогенных грибов и бактерий на семенах и сельскохозяйственных растениях на полях и на фабриках производства кормов. Гидроксид тетрамминмеди(II) (комплексное соединение) темноголубого цвета используется в качественном анализе на медь, как растворитель для хлопка, шелка, полотна и в производстве искусственного шелка. Хлорид меди CuCl2.2H2O в виде голубовато-зеленых кристаллов поглощает влагу из влажного воздуха, может увлажнять сухой воздух и используется в производстве краски, стойких чернил и в текстильной промышленности. Сульфат меди CuSO4 - наиболее распространенное соединение меди - получают растворением оксида (гидроксида или карбоната) меди в серной кислоте или металла в конц. серной кислоте. В промышленности его получают обжигом сульфида с дальнейшим растворением оксида в серной кислоте. Безводный сульфат бесцветен, но, хорошо поглощая воду, образует голубой пентагидрат CuSO4.5H2O (медный купорос). Сульфат меди(II) используется в изготовлении электролитических покрытий, гальванопластике, для изготовления пигментов, инсектицидов, для консервирования и дубления кожи, пропитки шпал, в крашении хлопка и шелка и как вяжущее средство. Он ядовит для низших организмов, особенно для морских водорослей, и поэтому используется на станциях водоподготовки. Ацетат меди(II) Cu(CH3COO)3*H2O (ярь-медянка) применяется для приготовления зеленой масляной краски. Смешанный ацетат-арсенит меди(II) Cu(CH3COO)2*Cu3(AsO3)2 (парижская зелень) применяется для уничтожения вредителей растений. Все соли меди ядовиты, поэтому медную посуду лудят, т.е. покрывают внутри слоем олова, чтобы предотвратить возможность образования солей.
См. также
ЭЛЕМЕНТЫ ХИМИЧЕСКИЕ;
МЕДНАЯ ПРОМЫШЛЕННОСТЬ.
ЛИТЕРАТУРА
Смирнягин А.П. и др. Промышленные цветные металлы и сплавы. М., 1974 Подчайнова В.Н., Симонова Л.Н. Медь. М., 1990

Самородная медь размером около 4 см
Медь — минерал из класса самородных элементов. В природном минерале обнаруживаются Fe, Ag, Au, As и другие элементы в виде примеси или образующие с Cu твёрдые растворы. Простое вещество медь — это пластичный переходный металл золотисто-розового цвета (розового цвета при отсутствии оксидной плёнки). Один из первых металлов, широко освоенных человеком из-за сравнительной доступности для получения из руды и малой температуры плавления. Он входит в семёрку металлов, известных человеку с очень древних времён. Медь является необходимым элементом для всех высших растений и животных.
Смотрите так же:
СТРУКТУРА
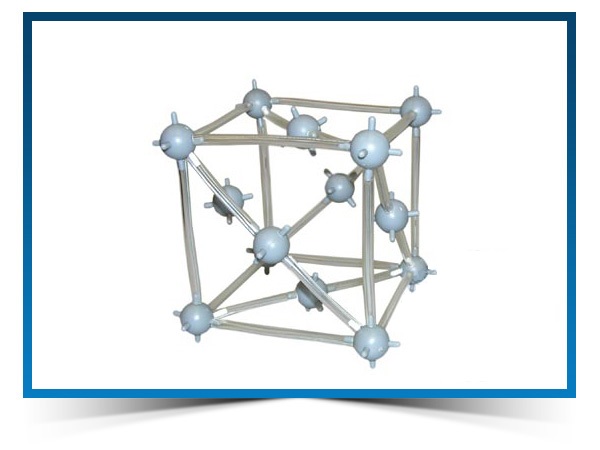
Кристаллическая структура меди
Кубическая сингония, гексаоктаэдрический вид симметрии m3m, кристаллическая структура – кубическая гранецентрированная решётка. Модель представляет собой куб из восьми атомов в углах и шести атомов , расположенных в центре граней (6 граней). Каждый атом данной кристаллической решетки имеет координационное число 12. Самородная медь встречается в виде пластинок, губчатых и сплошных масс, нитевидных и проволочных агрегатов, а также кристаллов, сложных двойников, скелетных кристаллов и дендритов. Поверхность часто покрыта плёнками “медной зелени” (малахит), “медной сини” (азурит), фосфатов меди и других продуктов её вторичного изменения.
СВОЙСТВА
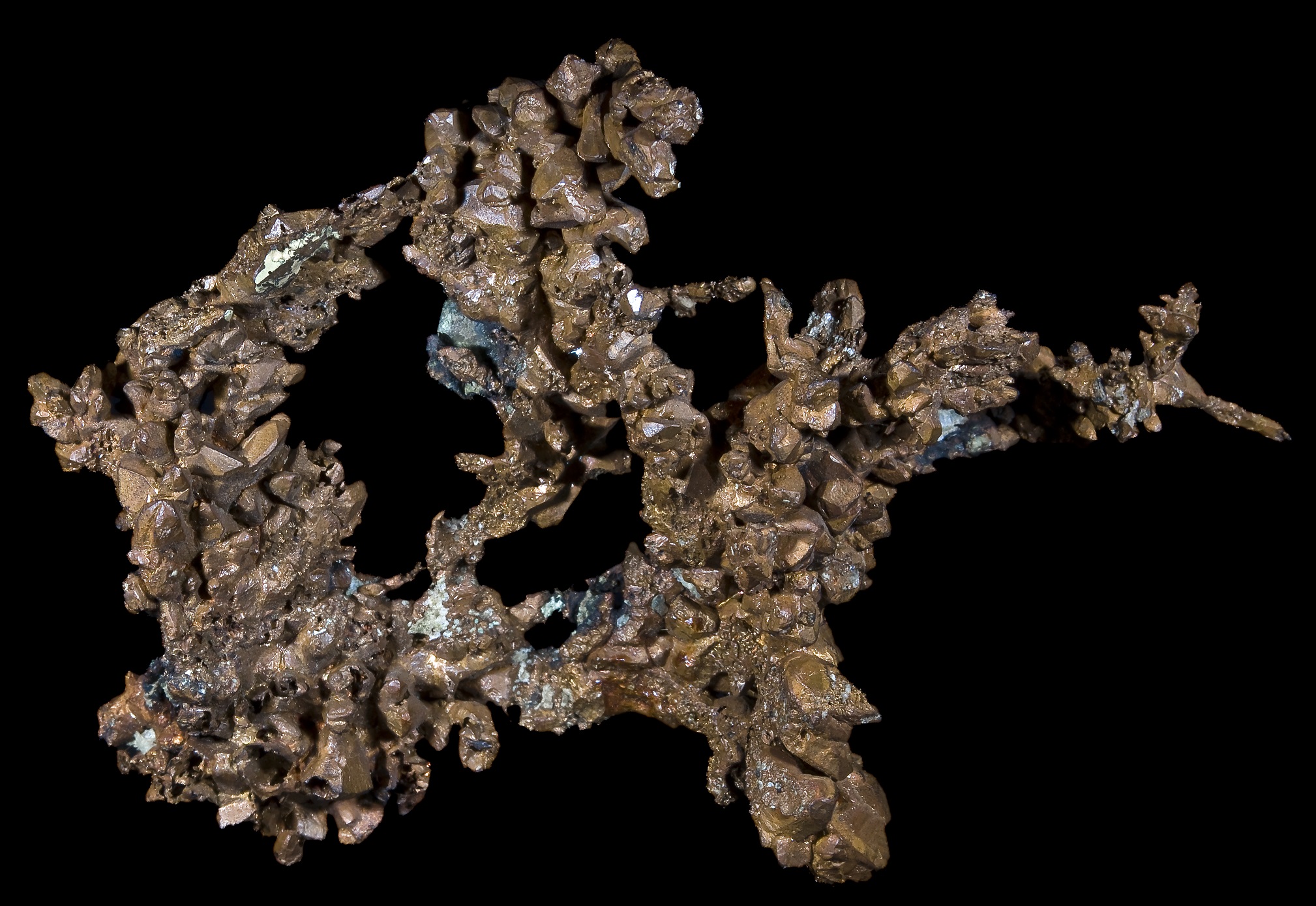
Кристаллы самородной меди, Верхнее озеро, округ Кинави, Мичиган, США. Размер 12 х 8,5 см
Медь — золотисто-розовый пластичный металл, на воздухе быстро покрывается оксидной плёнкой, которая придаёт ей характерный интенсивный желтовато-красный оттенок. Тонкие плёнки меди на просвет имеют зеленовато-голубой цвет.
Наряду с осмием, цезием и золотом, медь — один из четырёх металлов, имеющих явную цветовую окраску, отличную от серой или серебристой у прочих металлов. Этот цветовой оттенок объясняется наличием электронных переходов между заполненной третьей и полупустой четвёртой атомными орбиталями: энергетическая разница между ними соответствует длине волны оранжевого света. Тот же механизм отвечает за характерный цвет золота.
Медь обладает высокой тепло- и электропроводностью (занимает второе место по электропроводности среди металлов после серебра). Удельная электропроводность при 20 °C: 55,5-58 МСм/м. Медь имеет относительно большой температурный коэффициент сопротивления: 0,4 %/°С и в широком диапазоне температур слабо зависит от температуры. Медь является диамагнетиком.
Существует ряд сплавов меди: латуни — с цинком, бронзы — с оловом и другими элементами, мельхиор — с никелем и другие.
ЗАПАСЫ И ДОБЫЧА

Образец меди, 13,6 см. Полуостров Кинави, Мичиган, США
Среднее содержание меди в земной коре (кларк) — (4,7-5,5)·10 −3 % (по массе). В морской и речной воде содержание меди гораздо меньше: 3·10 −7 % и 10 −7 % (по массе) соответственно. Большая часть медной руды добывается открытым способом. Содержание меди в руде составляет от 0,3 до 1,0 %. Мировые запасы в 2000 году составляли, по оценке экспертов, 954 млн т, из них 687 млн т — подтверждённые запасы, на долю России приходилось 3,2 % общих и 3,1 % подтверждённых мировых запасов. Таким образом, при нынешних темпах потребления запасов меди хватит примерно на 60 лет.
Медь получают из медных руд и минералов. Основные методы получения меди — пирометаллургия, гидрометаллургия и электролиз. Пирометаллургический метод заключается в получении меди из сульфидных руд, например, халькопирита CuFeS2. Гидрометаллургический метод заключается в растворении минералов меди в разбавленной серной кислоте или в растворе аммиака; из полученных растворов медь вытесняют металлическим железом.
ПРОИСХОЖДЕНИЕ

Небольшой самородок меди
Обычно самородная медь образуется в зоне окисления некоторых медносульфидных месторождений в ассоциации с кальцитом, самородным серебром, купритом, малахитом, азуритом, брошантитом и другими минералами. Массы отдельных скоплений самородной меди достигают 400 тонн. Крупные промышленные месторождения самородной меди вместе с другими медьсодержащими минералами формируются при воздействии на вулканические породы (диабазы, мелафиры) гидротермальных растворов, вулканических паров и газов, обогащенных летучими соединениями меди (например, месторождение озера Верхнее, США).
Самородная медь встречается также в осадочных породах, преимущественно в медистых песчаниках и сланцах.
Наиболее известные месторождения самородной меди – Туринские рудники (Урал), Джезказганское (Казахстан), в США (на полуострове Кивино, в штатах Аризона и Юта).
ПРИМЕНЕНИЕ

Браслеты из меди
Из-за низкого удельного сопротивления, медь широко применяется в электротехнике для изготовления силовых кабелей, проводов или других проводников, например, при печатном монтаже. Медные провода, в свою очередь, также используются в обмотках энергосберегающих электроприводов и силовых трансформаторов.
Другое полезное качество меди — высокая теплопроводность. Это позволяет применять её в различных теплоотводных устройствах, теплообменниках, к числу которых относятся и широко известные радиаторы охлаждения, кондиционирования и отопления.
В разнообразных областях техники широко используются сплавы с использованием меди, самыми широко распространёнными из которых являются упоминавшиеся выше бронза и латунь. Оба сплава являются общими названиями для целого семейства материалов, в которые помимо олова и цинка могут входить никель, висмут и другие металлы.
В ювелирном деле часто используются сплавы меди с золотом для увеличения прочности изделий к деформациям и истиранию, так как чистое золото очень мягкий металл и нестойко к этим механическим воздействиям.
Прогнозируемым новым массовым применением меди обещает стать её применение в качестве бактерицидных поверхностей в лечебных учреждениях для снижения внутрибольничного бактериопереноса: дверей, ручек, водозапорной арматуры, перил, поручней кроватей, столешниц — всех поверхностей, к которым прикасается рука человека.
Медь – цветной металл планеты номер один
Медь не относится к благородным или редким элементам. Это самый распространенный цветной металл на Земле. Благодаря своим характеристикам в почете у промышленников и ювелиров. Предмет охоты сборщиков лома.

Что представляет собой
Медь – это розоватый металл с золотисто-металлическим блеском. Элемент №29 периодической системы Менделеева. Международное обозначение – Cu (Cuprum).
Чистый металл мягок, поэтому чаще используется с примесями. Пластичен: вытягивается до микронных диаметров.
На воздухе покрывается пленкой, обретая желтовато-красный оттенок. Тонкие пластинки на просвет зеленовато-голубые.
По официальной классификации причислен к тяжелым цветным металлам. В эту же группу входят свинец, цинк, олово, никель.
История
Медь – один из первых металлов, с которыми имело дело человечество. Этому способствовали преимущества: большая распространенность, доступность, относительно низкая температура плавления.
Достоинства меди люди оценили восемь тысячелетий назад.
Медный век начался сразу после каменного:
- Древнейшими признаны медные артефакты, откопанные на территории современной Турции. Это бусинки и декоративные накладки.
- Из металла делали режущий инструментарий и посуду.
- История открытия медных рудников на Руси начинается на Урале за две тысячи лет до новой эры. Затем были Кавказ, Алтай, Сибирь.
- Промышленная переработка с использованием бронзы началась в XIV веке. Из сплава отливали пушки и колокола.
Из бронзы отлиты Царь-колокол и Царь-пушка.
Предполагается, что металл назван по имени острова Кипр. Здесь еще в III веке до нашей эры обнаружились медные залежи, а население освоило выплавку меди.
Происхождение русскоязычного термина медь «Этимологический словарь русского языка» М.Фасмера увязывает с древненемецким корнем smid – кузнец, металл.
Запасы, добыча
Глобальные объемы медной руды оцениваются в миллиард тонн (разведанные). Наличие половины подтверждено. Ученые полагают, что земная кора таит еще три миллиарда тонн меденосной руды.

Самородная медь
Богатыми запасами располагают страны на всех континентах:
- Америка – Чили, Канада, США.
- Азия – Казахстан, Иран.
- Африка – ЮАР, Замбия, Заир.
На Россию приходится 3% мировых запасов. Месторождения сосредоточены на Урале. Основной добытчик – концерн «Норильский никель».
Руду добывают открытым либо закрытым способом, в зависимости от глубины залегания.
Ежегодный мировой объем добычи руды – 15-20 млн. тонн.
Физико-химические параметры
Медь – металл с типичными внешними признаками (блеск, гладкость) и структурой кристаллической решетки. Наделена высокой электро- и теплопроводностью. По этим физическим свойствам вторая после серебра.
| Название, символ, номер | Медь/Cuprum (Cu), 29 |
|---|---|
| Атомная масса (молярная масса) | 63,546(3)а. е. м. (г/моль) |
| Электронная конфигурация | [Ar] 3d10 4s1 |
| Радиус атома | 128 пм |
| Химические свойства | |
| Ковалентный радиус | 117 пм |
| Радиус иона | (+2e) 73 (+1e) 77 (K=6) пм |
| Электроотрицательность | 1,90 (шкала Полинга) |
| Электродный потенциал | +0,337 В/ +0,521 В |
| Степени окисления | 3, 2, 1, 0 |
| Энергия ионизации (первый электрон) | 745,0 (7,72) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
| Плотность (при н. у.) | 8,92 г/см³ |
| Температура плавления | 1356,55 K (1083,4 °С) |
| Температура кипения | 2567 °С |
| Уд. теплота плавления | 13,01 кДж/моль |
| Уд. теплота испарения | 304,6 кДж/моль |
| Молярная теплоёмкость | 24,44 Дж/(K·моль) |
| Молярный объём | 7,1 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | кубическая гранецентрированая |
| Параметры решётки | 3,615 Å |
| Температура Дебая | 315 K |
| Прочие характеристики | |
| Теплопроводность | (300 K) 401 Вт/(м·К) |
| Номер CAS | 7440-50-8 |
Главное химическое свойство металла, оцененное человеком, – нулевая коррозийность. Медь химически малоактивна, при стандартных условиях не окисляется.
Медь в природе
В природе выявлено два проявления элемента – самородки и компонент соединений с другими элементами.

Самородок меди
Чаще это соединения: оксиды, сульфиды, гидрокарбонаты. Самое распространенное сырье – медный колчедан.
Медь придает глубокие синие, голубые, зеленоватые оттенки малахиту, бирюзе, хризоколле, другим минералам ювелирно-декоративного сегмента.
Способы получения
Содержание металла в рудах не превышает 2%. Поэтому перед плавкой их обогащают. Существует два способа получения меди: пиро- и гидрометаллургический.
Пирометаллургический
Многоуровневый процесс, включающий следующие этапы:
- Обогащение. Руды обогащают методом флотации. Взвешенные в воде медные частички «цепляются» к воздушным пузырькам, которые увлекают их на поверхность. На выходе получается порошок-концентрат с 12-36% меди.
- Обжиг. Процедура показана бедным (9-24% меди) медным рудам и концентратам, сильно «загрязненным» серой. При прокаливании с кислородом доля серы падает вдвое.
- Плавка. Кусками руды или порошком-концентратом загружают печи шахтного либо отражательного типа при 1452°С. Получают медный штейн.
- Продувка. В конвертерах на него воздействуют сжатым воздухом. Сульфиды и железо окисляются, образуется почти чистая (98,51 – 99,51%) черновая медь плюс железо, другие ценные компоненты в следовых количествах.
- Рафинирование. Черновой продукт отправляют на рафинирование – пламенем, затем электролитом. Примеси удаляются с газами. После первого этапа металл очищается до 99,51%, после заключительного – до 99,96%.
Способ применяется к 9/10 добытого сырья.
Гидрометаллургический
Состоит в обработке сырья растворенной серной кислотой малой концентрации и выделении металлического медного продукта.
Метод оптимален для руд с минимальным процентом меди. Извлечения других компонентов не предусматривается.
Сплавы
Номенклатура сплавов меди с другими компонентами насчитывает десятки позиций.

Сплавы меди и их применение
Они применяются чаще чистого металла, поскольку уменьшают недостатки, присущие чистому металлу. То есть делают продукт прочнее, устойчивее, дешевле.
Медные соединения подразделяются на две группы:
Помимо этих главных легирующих компонентов, в составе соединения алюминий, никель, висмут, титан, серебро, золото, неметаллические элементы.
Сферы применения
Свойства металла обусловили его применение разными сферами. Главный потребитель – промышленный комплекс.

Промышленность
Металл и сплавы разбирают следующие отрасли:
- Электротехника, радиоэлектроника. Кабели (силовые, другие), провода. Обмотка в трансформаторах. Теплообменные устройства (радиаторы отопления, кондиционеры, кулеры компьютеров, тепловые трубки ноутбуков).
- Приборо-, машиностроение. Из сплавов меди с цинком, оловом, алюминием делают детали, узлы машин. Без нее невозможно создание гальванических элементов и батарей.
- Трубы. Для транспортировки пара, воды, газа. В энергетике, судостроении, для бытовых потребностей.
В Японии медные трубопроводы признаны сейсмоустойчивыми, что для этой страны жизненно важно.

Медные трубы
Строительство
Крыши из медного листа экологичны, их можно не красить, поскольку влага, погодные катаклизмы не страшны. Срок службы – до 100 лет.
Медицина
Медициной востребованы характеристики металла как антисептика и вяжущего средства.
Это компонент глазных капель и смесей для лечения ожогов.
Медные ручки дверей, другие поверхности – атрибут лечебных учреждений.
Соединения меди подавляют вирус свиного гриппа.
Ювелирное дело
Ювелиры используют сплавы на основе меди.

Кольцо из меди
Красное или розовое золото – это конгломерат благородного металла с медью.
Ее количество в составе определяет финальный оттенок:
Эти виды золота – самые любимые ювелирами. Медь делает изделия прочнее, попутно удешевляя стоимость.

Второй популярный ювелирный сплав – мельхиор (медь + никель).
Другие отрасли
- Оксид меди – основа купрата, используемого в сверхпроводниках.
- Латунь идет на изготовление гильз для винтовок и артиллерии.
- Из мельхиора чеканят монеты, создают интерьерные украшения, столовые приборы.
- Медь задействована при синтезе хлорофилла. Ее всегда добавляют в минеральные удобрения для растений.
Значение для человека
Медь заложена в организм человека изначально:
- Участвует в образовании красных кровяных телец, коллагена, эластина.
- Активирует работу эндокринной системы, замедляет старение организма.
- Ее дефицит чреват замедлением белкового обмена. Это влечет патологии в развитии скелета и составе крови.
Она есть во многих продуктах питания. Медью богаты говяжья печень, устрицы, кунжут, какао-порошок, черный перец, гречневая крупа. А также орехи (лесной, грецкий, кешью, арахис, миндаль).
Предостережение
В составе металла есть изотопы: два стабильных плюс два десятка нестабильных. Хотя период полураспада «долгожителя» – менее 2,5 суток, материал токсичен.
Поэтому применение меди контролируется.
В России на федеральном уровне (национальный стандарт, федеральный Свод Правил) регламентируется:
- Производство и использование медных водо- паро- и газопроводных труб.
- Количество меди в питьевой воде.
В 1 литре питьевой воды не должно быть больше 1 мг меди.
Избыток медных компонентов вызывает отравление организма. Для приготовления пищи медная посуда непригодна.
Карьер, в котором медную руду извлекали открытым способом, становится источником токсичных соединений.
Мировая цена меди устанавливается на Лондонской бирже металлов. Она зависит от спроса, определяемого состоянием экономики.

И колеблется соответственно:
- К началу 2008 года преодолена психологическая отметка $8000 за тонну.
- Через полгода было уже $+940, что стало рекордом за всю историю биржи.
- На начало 2011 года взята планка $10 000.
Затем произошел спад. На 2021 год тонна меди торгуется по $8057. Сказалось торможение экономики из-за пандемии коронавируса.
Цветные металлы – перечень и их полезные свойства
Эта группа металлов немногочисленна, но ценима промышленностью, медициной, эстетами. Цветные металлы не утилизируют даже после многих лет использования. Переработка дает им вторую жизнь и бережет природу.

Что считать цветным металлом
Первый уровень деления металлов – на чёрные и цветные.
С чёрными проблем нет: это железо и его сплавы(чугун, сталь).
Цветные ранжируют по-разному. Иногда таковыми считаются все металлы, кроме железа и его сплавов (в список включаются благородные, редкоземельные, радиоактивные).
У промышленников своя классификация. Цветные металлы – это бесжелезистые элементы определенного цветового оттенка (отсюда название группы).
Подразделяются на два вида:
В ряде стран такие металлы именуются не цветными, а нежелезными.
Сокращенное наименование сегмента цветных металлов – цветмет, черных – чермет.
Чермет и цветмет: в чем разница?
Первый фактор, по которому цветные металлы отличаются от черных, – отсутствие магнетизма . У чермета его создает железо.

Чтобы отличить черный металл от цветного, к образцу подносят магнит. Если притянется, – он из черного металла.
Другие характеристики цветмета:
- Пластичнее, легче черных.
- Благодаря отсутствию железа, цветмет устойчивее к коррозии.
- Премиальные механические характеристики при низких температурах. Однако медь, алюминий, магний утрачивают их при нагревании, разрушаясь даже от слабого удара.
- Взаимодействуют с газами (исключая инертные), растворяют их при нагреве.
- Высокая тепловодность, теплоемкость. Это свойство цветмета учитывают сварщики. Для работы требуется термоимпульс, без которого изделие быстро остывает. Поэтому перед сваркой детали (особенно из алюминия, меди, магния) разогревают.
- Прочнее, долговечнее. Неуязвимость к внешнему форс-мажору обеспечивает пленка-оксид на поверхности.
Однако агрессивные внешние факторы (особенно кислородно-влажная среда) влияют на структуру цветмета. Например, оцинкованные поверхности становятся белесоватыми.
У цветмета окисляется только поверхность, в отличие от черных металлов.
Добыча и обработка
Источник цветмета – рудное сырье. Способы добычи руды традиционны: из шахты либо карьера.
Сырьем занимается цветная металлургия. Это сегмент полного цикла.
Здесь выполняются следующие процессы:
- Обогащение (очистка руд цветных металлов от примесей).
- Плавка.
- Механическая обработка. Материал куют, прессуют, штампуют.
Различают металлургию легких и тяжелых металлов. В обоих видах это затратное, загрязняющее окружающую среду производство.
Второй способ получения сырья – переработка металлолома. Более рентабельный, экологически чистый метод.
По происхождению различают первичный (из руды) и вторичный (из лома) металл.
Классификация и сферы применения цветмета
По физическим свойствам цветмет подразделяется на тяжелые и легкие металлы. Сфера использования обоих видов обусловлена свойствами цветных металлов: износостойкостью, легкостью на фоне прочности, пластичностью, устойчивостью к коррозии.
Тяжелые цветные металлы
Данный вид цветмета включает пять названий.
Номер один в цветмете. Самый распространенный плюс повышенная пластичность, тепло- и электропроводность. Формирует сплавы почти со всеми металлами. Самые популярные – бронза (с оловом), латунь (с цинком), красное золото.
Золотистый с розоватостью цветмет – основа кабелей, проволоки, труб для термоагрегатов, боеприпасов, бытовых изделий, декора.
Свинец
Самый тяжелый из цветмета, плотный сизовато-серый.
Мягкий (1,5 из 10 по Моосу), режется вручную, царапается ногтем, легко прокатывается до фольги.

Тепло- и электропроводность ниже средних: у меди, например, на порядок больше. Плюс малая стойкость к вибрациям, беззащитность перед гниющей органической массой, растворами извести, бетона.
Идет на аккумуляторы, основу и покрытие проводов, кабелей, электроды, боеприпасы.
Свинец ставит щит радиации, но токсичен, отнесен к химически опасным веществам 1 класса.
Легкоплавкий цветмет со сменными свойствами: хрупок при обычной температуре, пластичен при нагреве. Равнодушен к ржавлению, разрушается кислотами либо щелочами.

Используется машиностроителями, металлургами как покрытие железа для предотвращения коррозии.
Олово
Серебристо-белый умеренно блестящий тяжелый металл.
Востребован как компонент сплавов для подшипников, припоев.

Расплавленное олово
Самый экологически чистый в «тяжелом» сегменте цветмета, поэтому используется не только промышленностью, но и в быту (например, как материал крышек для консервации).
Никель
Серебристо-белый с желтоватостью цветмет. Один из лучших катализаторов, обязательный компонент нержавеющих сталей, повышающий химическую стойкость.

Мелкий порошок никеля самовоспламеняется при комнатной температуре.
Востребован изготовителями щелочных аккумуляторов (в том числе для электромобилей) и емкостей для химически агрессивных веществ.
Легкие цветные металлы
Сегмент легких цветных металлов состоит из трех позиций.
Алюминий
Серебристый цветмет – суперпроводник электричества, пластичен. Механические параметры оставляют желать лучшего, поэтому добавляется к сплавам. Они прочны, легки, невосприимчивы к коррозии, большинству агрессивных сред, термовоздействию.

Используется как материал корпуса изделий авиа-, морских судов, электропроводов.
Титан
Блестящий серебристый с голубоватым отливом материал. Легок, прочен, устойчив к коррозии, вязок. Пластичен, хрупким становится при -80°C или большом проценте примесей.

Стержень, состоящий из титановых кристаллов высокой чистоты
По прочности цветмет сопоставим со сталью, но вполовину легче. Вдвое прочнее алюминия, однако массивнее всего наполовину. За это ценится строителями ракет, самолетов, судов, нефтяниками.

Заготовка титанового шпангоута истребителя F-15 до и после прессования на штамповочном прессе компании Alcoa усилием 45 тыс. тонн, май 1985
Титан совместим с тканями организма человека, благодаря чему используется пищепромом и как материал экзоскелета, зубных протезов, пирсинга.
Магний
Легкое красивое блестящее вещество.
Благодаря малой плотности цветмет хорошо обрабатывается, устойчив к жару, большинству горючих веществ.

Металлический магний
Однако требует осторожности. В нагретом воздухе сгорает с ярким свечением. Смесь порошка с марганцовкой, другими окислителями порождает взрыв.
Горящий магний затушить водой невозможно.
Вторичное использование цветмета
Использованный цветмет не утилизируют по многим причинам.
Переработка – дело выгодное
Первичное производство цветмета (из руд) – затратный, трудоемкий, экологически проблемный процесс. Поэтому закономерно стремление предприятий оптимизировать расходы. То есть перерабатывать цветной металлолом. Стоимость процесса впятеро дешевле переработки первичного сырья.
Вторичное использование лома цветмета выгодно: предприятие экономит деньги, попутно избегая штрафов за загрязнение окружающей среды.
Сдатчики цветмета тоже получают неплохие деньги. Поэтому на промышленных предприятиях отработана практика складирования такого металлолома для сдачи на пункт приема либо меткомбинат.
Какой лом берут на переработку
Металлолом подразделяют на два вида:
- Бытовой – корпус, детали отслужившей бытовой техники, гаджетов, кабели.
- Промышленный – не подлежащее ремонту оборудование, изношенные элементы конструкций, стружка, другие отходы, отбраковка производства.
Для переработки годится алюминиевый, медный, никелевый, свинцовый, цинковый, оловянный, титановый лом. Плюс сплавы (бронза, латунь), лом смешанного состава.
Этапы переработки
Поступивший цветмет проходит следующие стадии:
- Проверка на предмет радиации, взрывоопасности, наличия опасных химических компонентов.
- Сортировка по металлам.
- Измельчение.
- Прессовка.
- Упаковка.
- Отправка на металлургический комбинат.
Пункт приема металлического вторсырья (лома) есть в большинстве населенных пунктов. Диапазон принимаемых от организаций и граждан металлических отходов – от крупных конструкций до стружки и порошка любой массы.
Читайте также:
