Металл не растворяется в азотной кислоте
Обновлено: 09.05.2024
а) Хорошо растворяется в соляной кислоте. Медленно растворяется в концентрированной и разбавленной HNO3 н разбавленной Н2SO4.
б) Алюминий и его сплавы хорошо растворяются в концентрированных растворах едких щелочей (20—40% NaOH или KОН).
Бериллий
Хорошо растворяется в соляной и серной кислотах, а также в азотной кислоте при нагревании. Холодная азотная кислота пассивирует металл вследствие образования пленки окиси бериллия.
Растворяется в кислотах-окислителях: в концентрированных азотной и серной, а также в хлорной при нагревании до белого дыма. Сплавляется с едкими щелочами, образуя метабораты.
Ванадий
Растворяется на холоду в «царской водке» и в азотной кислоте. При нагревании растворяется в концентрированной серной и плавиковой кислотах. Сплавляется со щелочами, образуя соли ванадиевой кислоты (ванадаты). Нерастворим в разбавленных серной и соляной кислотах.
Висмут
Хорошо растворяется в разбавленной азотной кислоте, в смеси азотной и соляной кислот, в горячей концентрированной серной кислотах. Нерастворим в разбавленных соляной и серной кислотах.
Вольфрам
Нерастворим в серной и соляной кислотах. Концентрированная азотная кислота и «царская водка» окисляют вольфрам с поверхности, переводя его в нерастворимую вольфрамовую кислоту. Растворяется в смеси плавиковой и азотной кислот. Растворим в смесях кислот, содержащих фосфорную кислоту, вследствие образования комплексной вольфрамо-фосфорной кислоты H7[P(W2O7)6]*xH2O
Растворяется в насыщенном растворе щавелевой кислоты в присутствии перекиси водорода. Сплавляется со щелочами или Na2CO3 в присутствии окислителей (например, КСlO3) с образованием солей вольфрамовой кислоты.
Гафний
Германий
Хорошо растворяется в «царской водке», а также в щелочном растворе перекиси водорода. Кислоты на германий действуют слабо; в азотной кислоте образуется гидрат двуокиси германия.
Железо
Легко растворяется в азотной кислоте, разбавленной серной, а также в соляной кислоте. Чистейшее железо растворяется в азотной кислоте, но не растворяется в соляной.
Золото
Индий
Легко растворяется в соляной кислоте, медленно — в серной, с трудом в концентрированной азотной кислоте.
Кадмий
Растворяется в горячей разбавленной азотной кислоте. Плохо растворяется в разбавленной соляной и серной кислотах; растворение ускоряется в присутствии перекиси водорода.
Кобальт
Растворяется в разбавленной азотной кислоте, а также в разбавленной соляной и серной кислотах. Концентрированные серная и азотная кислоты пассивируют кобальт.
Лантан
Магний
Легко растворяется во всех разбавленных кислотах, в т. ч. и в уксусной. Растворяется в концентрированных растворах хлорида аммония.
Марганец
Растворяется в разбавленных азотной, соляной и серной кислотах с образованием солей двухвалентного марганца (Мn 2+ ). В концентрированной серной кислоте растворяется с выделением SO2
Легко растворяется в азотной кислоте. Нерастворима в соляной и в разбавленной серной кислотах. Концентрированная серная кислота растворяет медь при нагревании до паров Н2SO4. Соляная кислота растворяет медь в присутствии окислителей (например, Fe 3+ , Н2О2, НNО3 и т. д.).
Молибден
Легко растворяется в «царской водке» и в смеси плавиковой и азотной кислот. Растворяется в концентрированной серной кислоте при нагревании до паров Н2SO4. В разбавленной соляной кислоте растворяется при нагревании очень медлепно.
Сплавляется со щелочами в присутствии окислителей. Концентрированная азотная кислота пассивирует молибден.
Мышьяк
Растворяется в смеси азотной и соляной кислот, в концентрированной серной кислоте при нагревании до паров Н2SO4. Нерастворим в соляной и разбавленной серной кислотах.
Никель
Растворяется в разбавленной азотной кислоте. В концентрированной азотной кислоте пассивируется и не растворяется. Плохо растворяется в разбавленных соляной и серной кислотах.
Ниобий
Нерастворим в «царской водке» и концентрированной азотной кислоте. Растворяется в плавиковой кислоте с добавкой азотной кислоты. Концентрированная серная кислота с добавкой (NH4)2SO4 или К2SO4 растворяет ниобий при нагревании до паров Н2SO4. Сплавляется со щелочами, образуя солн-ниобаты.
Олово
Растворяется в соляной кислоте и в смеси соляной и азотной кислот. Растворяется в концентрированной серной кислоте при нагревании. В азотной кислоте образуется нерастворимый осадок метаоловянной кислоты H2SnO3
Платина
Рений
Растворяется в азотной кислоте с образованием раствора рениевой кислоты. Концентрированная серная кислота при нагревании медленно растворяет рений. Соляная и разбавленная серная кислоты очень медленно растворяют его.
Ртуть
Хорошо растворяется в азотной кислоте, а также в концентрированной серной при нагревании. Нерастворима в соляной кислоте и в разбавленной серной.
Свинец
Хорошо растворяется в разбавленной азотной кислоте. Соляная и серная кислоты растворяют свинец лишь при нагревании. Растворяется в уксусной кислоте.
Селен
Растворяется в азотной кислоте с образованием растворимой селенистой кислоты H2SeO3. Растворяется также в «царской водке».
Серебро
Легко растворяется в азотной кислоте; при нагревании растворяется в концентрированной серной кислоте. Нерастворимо в соляной, а также на холоду в серной кислотах.
Сурьма
Растворяется в концентрированной серной кислоте при нагревании до паров Н2SO4, в смеси азотной и соляной кислот, в смеси азотной кислоты с винной.
Таллий
Легко растворяется в азотной кислоте. В серной кислоте растворяется труднее, в соляной — плохо вследствие образования малорастворимого хлорида одновалентного таллия.
Тантал
Нерастворим в «царской водке» и в азотной кислоте. На него не действует плавиковая кислота (в отсутствие платины). Концентрированная серная кислота лишь при нагревании действует на металл. Растворяется в плавиковой кислоте с добавкой азотной. Металл сплавляется со щелочами, образуя танталаты.
Теллур
Растворяется в азотной кислоте с образованием растворимой теллуристой кислоты H2TeO3. Растворим в «царской водке», в концентрированной серной кислоте, в растворах NaOH и KCN.
Титан
Растворяется в разбавленной 1 : 1 соляной и разбавленной 1 : б серной кислотах с образованием солей трех валентного титана фиолетового цвета. Очень легко растворяется в разбавленной плавиковой кислоте и в смеси плавиковой и азотной кислот.
Азотная кислота пассивирует титан вследствие образования нерастворимой метатитановой кислоты. Такой пассивированный титан плохо растворяется в соляной и серной кислотах.
Торий
Легко растворяется в концентрированной соляной кислоте и в смеси соляной и азотной кислот. Одна азотная кислота пассивирует металл.
Растворяется в разбавленных серной и соляной кислотах, а также в хлорной кислоте. Азотная кислота на холоду пассивирует уран (при растворении образуется нитрат уранила UO2(NO3)2 ).
Легко растворяется в соляной и хлоркой кислотах, а также в разбавленной серной кислоте. В азотной кислоте хром с поверхности пассивируется, и дальнейшее растворение его протекает крайне медленно.
Церий
Цирконий
Растворяется в «царской водке» и плавиковой кислоте, а также в смеси плавиковой и азотной кислот. Медленно растворяется в серной и концентрированной соляной кислоте. Устойчив к действию 5%-ной соляпой кислоты даже при нагревапии.
Легко переводится в раствор мокрым сплавлением (на 10 мл концентрированной Н2SO4 добавляют 3 грамма K2SO4).
--> Растворимость металлов в различных жидкостях. Ртуть Хорошо растворяется в азотной кислоте, а также в концентрированной серной при нагревании. Нерастворима в соляной кислоте и в разбавленной серной. | растворимость, металл, химия, кислота
Металл не растворяется в азотной кислоте
ОТНОШЕНИЕ МЕТАЛЛОВ К КИСЛОТАМ
Чаще всего в химической практике используются такие сильные кислоты как серная H 2 SO 4 , соляная HCl и азотная HNO 3 . Далее рассмотрим отношение различных металлов к перечисленным кислотам.
Соляная кислота ( HCl )
Соляная кислота – это техническое название хлороводородной кислоты. Получают ее путем растворения в воде газообразного хлороводорода – HCl . Ввиду невысокой его растворимости в воде, концентрация соляной кислоты при обычных условиях не превышает 38%. Поэтому независимо от концентрации соляной кислоты процесс диссоциации ее молекул в водном растворе протекает активно:
Образующиеся в этом процессе ионы водорода H + выполняют роль окислителя, окисляя металлы, расположенные в ряду активности левее водорода. Взаимодействие протекает по схеме:
Me + HCl соль + H 2 ↑
При этом соль представляет собой хлорид металла ( NiCl 2 , CaCl 2 , AlCl 3 ), в котором число хлорид-ионов соответствует степени окисления металла.
Соляная кислота является слабым окислителем, поэтому металлы с переменной валентностью окисляются ей до низших положительных степеней окисления:
Fe 0 → Fe 2+
Co 0 → Co 2+
Ni 0 → Ni 2+
Cr 0 → Cr 2+
Mn 0 → Mn 2+ и др .
2 Al + 6 HCl → 2 AlCl 3 + 3 H 2 ↑
2│ Al 0 – 3 e - → Al 3+ - окисление
3│2 H + + 2 e - → H 2 – восстановление
Соляная кислота пассивирует свинец ( Pb ). Пассивация свинца обусловлена образованием на его поверхности трудно растворимого в воде хлорида свинца ( II ), который защищает металл от дальнейшего воздействия кислоты:
Pb + 2 HCl → PbCl 2 ↓ + H 2 ↑
Серная кислота ( H 2 SO 4 )
В промышленности получают серную кислоту очень высокой концентрации (до 98%). Следует учитывать различие окислительных свойств разбавленного раствора и концентрированной серной кислоты по отношению к металлам.
Разбавленная серная кислота
В разбавленном водном растворе серной кислоты большинство ее молекул диссоциируют:
Образующиеся ионы Н + выполняют функцию окислителя.
Как и соляная кислота, разбавленный раствор серной кислоты взаимодействует только с металлами активными и средней активности (расположенными в ряду активности до водорода).
Химическая реакция протекает по схеме:
1│2Al 0 – 6e - → 2Al 3+ - окисление
Металлы с переменной валентностью окисляются разбавленным раствором серной кислоты до низших положительных степеней окисления:
Mn 0 → Mn 2+ и др .
Свинец ( Pb ) не растворяется в серной кислоте (если ее концентрация ниже 80%) , так как образующаяся соль PbSO 4 нерастворима и создает на поверхности металла защитную пленку.
Концентрированная серная кислота
В концентрированном растворе серной кислоты (выше 68%) большинство молекул находятся в недиссоциированном состоянии, поэтому функцию окислителя выполняет сера, находящаяся в высшей степени окисления ( S +6 ). Концентрированная H 2 SO 4 окисляет все металлы, стандартный электродный потенциал которых меньше потенциала окислителя – сульфат-иона SO 4 2- (0,36 В). В связи с этим, с концентрированной серной кислотой реагируют и некоторые малоактивные металлы.
Процесс взаимодействия металлов с концентрированной серной кислотой в большинстве случаев протекает по схеме:
Me + H 2 SO 4 (конц.) соль + вода + продукт восстановления H 2 SO 4
Продуктами восстановления серной кислоты могут быть следующие соединения серы:
Практика показала, что при взаимодействии металла с концентрированной серной кислотой выделяется смесь продуктов восстановления, состоящая из H 2 S , S и SO 2. Однако, один из этих продуктов образуется в преобладающем количестве. Природа основного продукта определяется активностью металла: чем выше активность, тем глубже процесс восстановления серы в серной кислоте.
Взаимодействие металлов различной активности с концентрированной серной кислотой можно представить схемой:

Алюминий ( Al ) и железо ( Fe ) не реагируют с холодной концентрированной H 2 SO 4 , покрываясь плотными оксидными пленками, однако при нагревании реакция протекает.
Ag , Au , Ru , Os , Rh , Ir , Pt не реагируют с серной кислотой.
Концентрированная серная кислота является сильным окислителем, поэтому при взаимодействии с ней металлов, обладающих переменной валентностью, последние окисляются до более высоких степеней окисления, чем в случае с разбавленным раствором кислоты:
Fe 0 → Fe 3+ ,
Cr 0 → Cr 3+ ,
Mn 0 → Mn 4+ ,
Sn 0 → Sn 4+
Свинец ( Pb ) окисляется до двухвалентного состояния с образованием растворимого гидросульфата свинца Pb ( HSO 4 )2 .
Азотная кислота
Азотная кислота HNO3 – это сильная одноосновная кислота-гидроксид. При обычных условиях бесцветная, дымящая на воздухе жидкость, температура плавления −41,59 °C, кипения +82,6 °C ( при нормальном атмосферном давлении). Азотная кислота смешивается с водой во всех соотношениях. На свету частично разлагается.
Валентность азота в азотной кислоте равна IV, так как валентность V у азота отсутствует. При этом степень окисления атома азота равна +5. Так происходит потому, что атом азота образует 3 обменные связи и одну донорно-акцепторную, является донором электронной пары.
Поэтому строение молекулы азотной кислоты можно описать резонансными структурами:


Обозначим дополнительные связи между азотом и кислородом пунктиром. Этот пунктир по сути обозначает делокализованные электроны. Получается формула:

Способы получения
В лаборатории азотную кислоту можно получить разными способами:
1. Азотная кислота образуется при действии концентрированной серной кислоты на твердые нитраты металлов. При этом менее летучая серная кислота вытесняет более летучую азотную.
Например , концентрированная серная кислота вытесняет азотную из кристаллического нитрата калия:
2. В промышленности азотную кислоту получают из аммиака . Процесс осуществляется постадийно.
1 стадия. Каталитическое окисление аммиака.
2 стадия. Окисление оксида азота (II) до оксида азота (IV) кислородом воздуха.
3 стадия. Поглощение оксида азота (IV) водой в присутствии избытка кислорода.
Химические свойства
Азотная кислота – это сильная кислота . За счет азота со степенью окисления +5 азотная кислота проявляет сильные окислительные свойства .
1. Азотная кислота практически полностью диссоциирует в водном растворе.
2. Азотная кислота реагирует с основными оксидами, основаниями, амфотерными оксидами и амфотерными гидроксидами.
Например , азотная кислота взаимодействует с оксидом меди (II):
Еще пример : азотная кислота реагирует с гидроксидом натрия:
3. Азотная кислота вытесняет более слабые кислоты из их солей (карбонатов, сульфидов, сульфитов).
Например , азотная кислота взаимодействует с карбонатом натрия:
4. Азотная кислота частично разлагается при кипении или под действием света:
5. Азотная кислота активно взаимодействует с металлами. При этом никогда не выделяется водород! При взаимодействии азотной кислоты с металлами окислителем всегда выступает азот +5. Азот в степени окисления +5 может восстанавливаться до степеней окисления -3, 0, +1, +2 или +4 в зависимости от концентрации кислоты и активности металла.
металл + HNO3 → нитрат металла + вода + газ (или соль аммония)
С алюминием, хромом и железом на холоду концентрированная HNO3 не реагирует – кислота «пассивирует» металлы, т.к. на их поверхности образуется пленка оксидов, непроницаемая для концентрированной азотной кислоты. При нагревании реакция идет. При этом азот восстанавливается до степени окисления +4:
Золото и платина не реагируют с азотной кислотой, но растворяются в «царской водке» – смеси концентрированных азотной и соляной кислот в соотношении 1 : 3 (по объему):
HNO3 + 3HCl + Au → AuCl3 + NO + 2H2O
Концентрированная азотная кислота взаимодействует с неактивными металлами и металлами средней активности (в ряду электрохимической активности после алюминия). При этом образуется оксид азота (IV), азот восстанавливается минимально:
С активными металлами (щелочными и щелочноземельными) концентрированная азотная кислота реагирует с образованием оксида азота (I):
Разбавленная азотная кислота взаимодействует с неактивными металлами и металлами средней активности (в ряду электрохимической активности после алюминия). При этом образуется оксид азота (II).
С активными металлами (щелочными и щелочноземельными), а также оловом и железом разбавленная азотная кислота реагирует с образованием молекулярного азота:
При взаимодействии кальция и магния с азотной кислотой любой концентрации (кроме очень разбавленной) образуется оксид азота (I):
Очень разбавленная азотная кислота реагирует с металлами с образованием нитрата аммония:
Таблица . Взаимодействие азотной кислоты с металлами.
| Азотная кислота | ||||
| Концентрированная | Разбавленная | |||
| с Fe, Al, Cr | с неактивными металлами и металлами средней активности (после Al) | с щелочными и щелочноземельными металлами | с неактивными металлами и металлами средней активности (после Al) | с металлами до Al в ряду активности, Sn, Fe |
| пассивация при низкой Т | образуется NO2 | образуется N2O | образуется NO | образуется N2 |
6. Азотная кислота окисляет и неметаллы (кроме кислорода, водорода, хлора, фтора и некоторых других). При взаимодействии с неметаллами HNO3 обычно восстанавливается до NO или NO2, неметаллы окисляются до соответствующих кислот, либо оксидов (если кислота неустойчива).
Например , азотная кислота окисляет серу, фосфор, углерод, йод:
Безводная азотная кислота – сильный окислитель. Поэтому она легко взаимодействует с красным и белым фосфором . Реакция с белым фосфором протекает очень бурно. Иногда она сопровождается взрывом.
Видеоопыт взаимодействия фосфора с безводной азотной кислотой можно посмотреть здесь.
Видеоопыт взаимодействия угля с безводной азотной кислотой можно посмотреть здесь.
7. Концентрированная а зотная кислота окисляет сложные вещества (в которых есть элементы в отрицательной, либо промежуточной степени окисления): сульфиды металлов, сероводород, фосфиды, йодиды, соединения железа (II) и др. При этом азот восстанавливается до NO2, неметаллы окисляются до соответствующих кислот (или оксидов), а металлы окисляются до устойчивых степеней окисления.
Например , азотная кислота окисляет оксид серы (IV):
Еще пример : азотная кислота окисляет иодоводород:
Сера в степени окисления -2 окисляется без нагревания до простого вещества, при нагревании до серной кислоты.
Например , сероводород окисляется азотной кислотой без нагревания до молекулярной серы:
При нагревании до серной кислоты:
Соединения железа (II) азотная кислота окисляет до соединений железа (III):
8. Азотная кислота окрашивает белки в оранжево-желтый цвет («ксантопротеиновая реакция«).
Ксантопротеиновую реакцию проводят для обнаружения белков, содержащих в своем составе ароматические аминокислоты. К раствору белка прибавляем концентрированную азотную кислоту. Белок свертывается. При нагревании белок желтеет. При добавлении избытка аммиака окраска переходит в оранжевую.

Видеоопыт обнаружения белков с помощью азотной кислоты можно посмотреть здесь.
Азотная кислота
Азотная кислота является одной из самых сильных минеральных кислот, в концентрированном виде выделяет пары желтого цвета с резким запахом. За исключением золота и платины растворяет все металлы.
Применяют азотную кислоту для получения красителей, удобрений, органических нитропродуктов, серной и фосфорной кислот. В результате ожога азотной кислотой образуется сухой струп желто-зеленого цвета.

В промышленности азотную кислоту получают в результате окисления аммиака на платино-родиевых катализаторах.
Чистая азотная кислота впервые была получена действием на селитру концентрированной серной кислоты:
Является одноосновной сильной кислотой, вступает в реакции с основными оксидами, основаниями. С солями реагирует при условии выпадения осадка, выделения газа или образования слабого электролита.

При нагревании азотная кислота распадается. На свету (hv) также происходит подобная реакция, поэтому азотную кислоту следует хранить в темном месте.
Азотная кислота способна окислить все неметаллы, при этом, если кислота концентрированная, азот обычно восстанавливается до NO2, если разбавленная - до NO.

В любой концентрации азотная кислота проявляет свойства окислителя, при этом азот восстанавливается до степени окисления от +5 до -3. На какой именно степени окисления остановится азот, зависит от активности металла и концентрации азотной кислоты.
Для малоактивных металлов (стоящих в ряду напряжений после водорода) реакция с концентрированной азотной кислотой происходит с образованием нитрата и преимущественно NO2.
С разбавленной азотной кислотой газообразным продуктом преимущественно является NO.
В реакциях с металлами, стоящими левее водорода в ряду напряжений, возможны самые разные газообразные (и не газообразные) продукты: бурый газ NO2, NO, N2O, атмосферный газ N2, NH4NO3.
Помните о закономерности: чем более разбавлена кислота и активен металл, тем сильнее восстанавливается азот. Ниже представлены реакции цинка с азотной кислотой в различных концентрациях.

Посмотрите на таблицу ниже, в которой также отражены изученные нами закономерности.
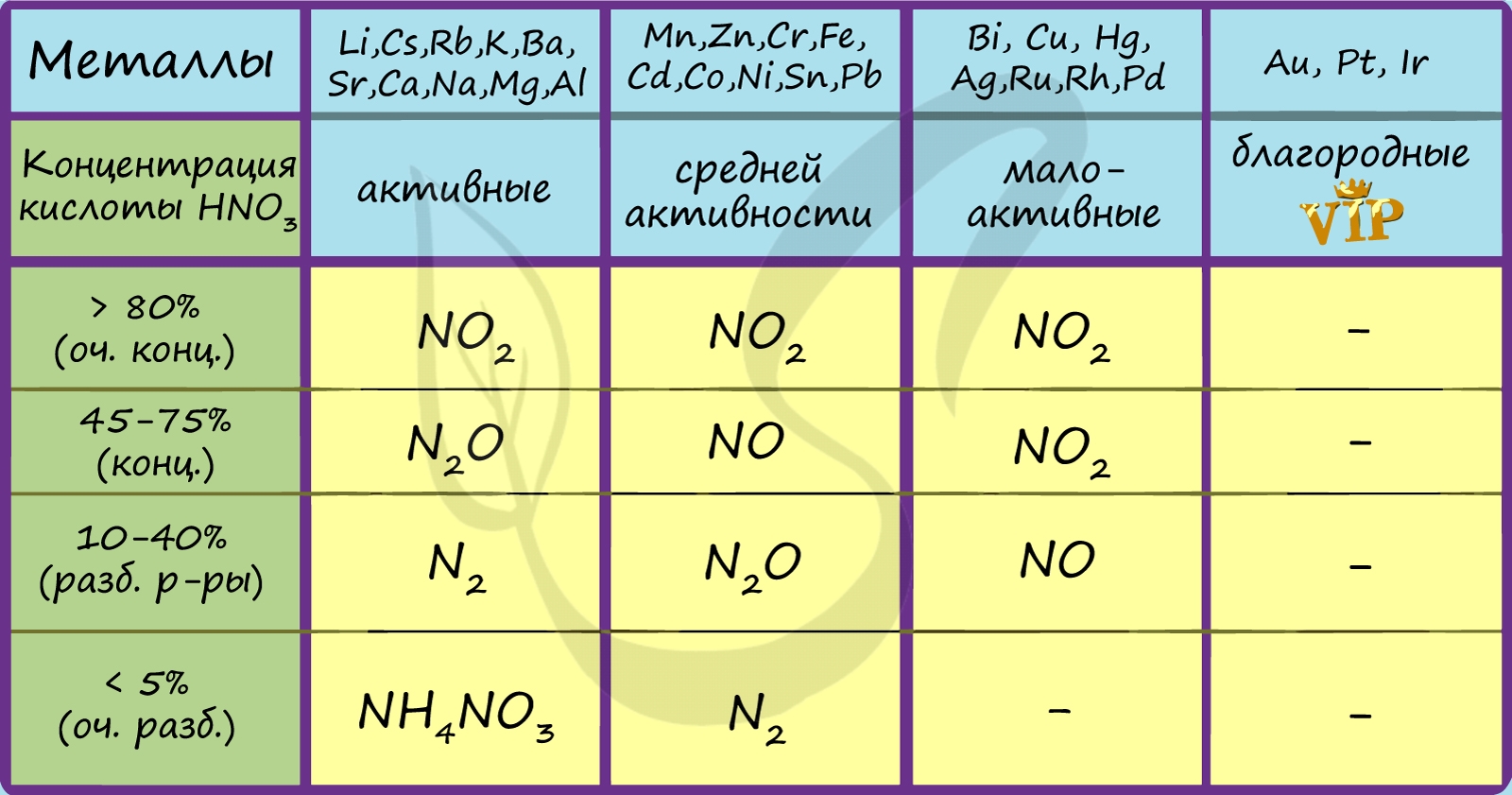
Концентрированная холодная азотная кислота пассивирует хром, железо, алюминий, никель, свинец и бериллий. Это происходит за счет оксидной пленки, которой покрыты данные металлы.
Al + HNO3(конц.) ⇸ (реакция не идет)
При нагревании или амальгамировании (покрытие ртутью) перечисленных металлов реакция с азотной кислотой идет, так как оксидная пленка на поверхности металлов разрушается.
Соли азотной кислоты - нитраты NO3 -
Получают нитраты в ходе реакции азотной кислоты с металлами, их оксидами и основаниями.
В реакциях с оксидами и основаниями газообразный продукт обычно не выделяется.

Нитрат аммония получают реакция аммиака с азотной кислотой.
Обратите внимание на следующую закономерность: концентрированная азотная кислота, как правило, окисляет железо и хром до +3. Разбавленная кислота - до +2.
- Реакции с металлами, основаниями и кислотами
Как и для всех солей, из нитратов можно вытеснить металл другим более активным. Соли реагируют с основаниями и кислотами, если в результате реакции выпадает осадок, выделяется газ или образуется слабый электролит (вода).

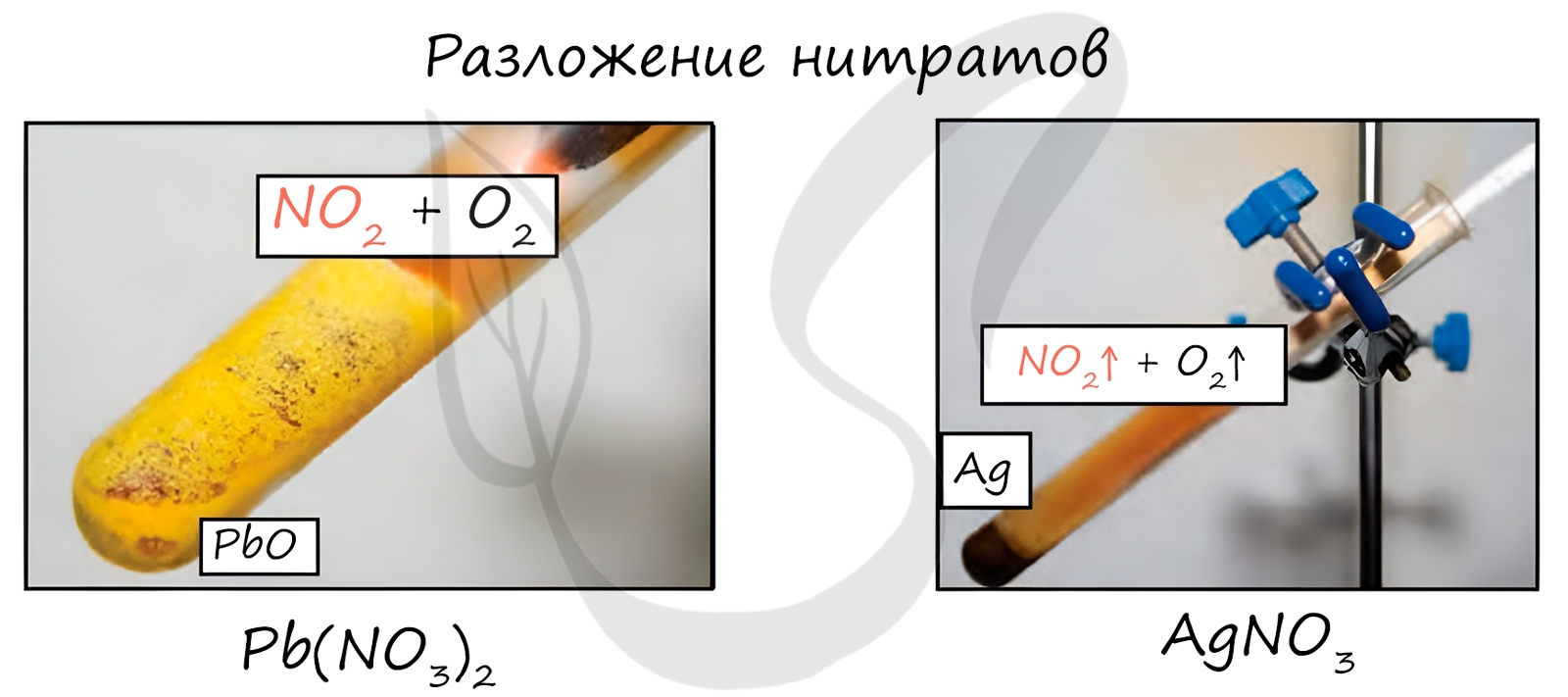
Нитраты разлагаются в зависимости от активности металла, входящего в их состав.

Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Блиц-опрос по теме Азотная кислота
Холодная концентрированная азотная кислота не вступает в реакцию с алюминием, происходит пассивирование.
2. Реакция концентрированной азотной кислоты с малоактивными металлами сопровождается выделением газа
В реакциях концентрированной азотной кислоты и малоактивных металлов преимущественно выделяется NO2.
3. Если в результате реакции активного металла с азотной кислотой выделилось твердое вещество, то речь идет о
Твердый продукт, образовавшийся в ходе реакции с азотной кислотой, нитрат аммония - NH4NO3
Разложение нитрата аммония протекает по схеме: AgNO3 → Ag + NO2 + O2
Азотной кислотой окрашивает пораженную в результате ожога кожу в желтый цвет.
Азотная кислота свойства
Азотная кислота это химическое соединение водорода H, азота N и кислорода O, формула азотной кислоты HNO3. Химически чистая кислота тяжелая бесцветная жидкость.
Получают тремя способами: действием серной кислоты на нитраты, окислением аммиака и дуговым способом.

Что такое азотная кислота
Чистая азотная кислота — бесцветная жидкость уд. веса 1,53, кипящая при 86°, а при —41° застывающая в прозрачную кристаллическую массу, образуя две кристаллические модификации с моноклинной и ромбической решётками.
На воздухе она, подобно концентрированной соляной кислоте, «дымит», так как пары ее образуют с влагой воздуха мелкие капельки тумана.
С водой азотная кислота смешивается в любом отношении, причем 68%-ный раствор кипит при 120,5° и перегоняется без изменения.
Серная кислота и азотная кислота образует кислотное соединение меланж.
- Меланж — окислитель для ракетного топлива из концентрированной азотной кислоты с добавкой растворённого в ней амила.
- Меланж — использующаяся для нитрования смесь концентрированных азотной и серной кислот в соотношении примерно 9 объёмных частей к 1.
Такой состав имеет обыкновенная продажная азотная кислота уд. веса 1,4. Концентрированная кислота, содержащая 96—98% HNO3 и окрашенная растворенной в ней двуокисью азота в красно-бурый цвет, известна под названием дымящей азотной кислоты.
Азотная кислота не отличается особенной химической прочностью. Уже под влиянием света она постепенно разлагается на воду, кислород и двуокись азота:
Чем выше температура и чем концентрированнее кислота, тем быстрее идет разложение. Поэтому получаемая из селитры азотная кислота всегда бывает окрашена двуокисью азота в желтоватый цвет.
Чтобы избежать разложения, перегонку ведут под уменьшенным давлением, под которым азотная кислота закипает при температуре, близкой к 20°.
Азотная кислота принадлежит к числу наиболее сильных кислот; в разбавленных растворах она сполна распадается на ионы Н • и NO3‘.
Химические свойства азотной кислоты
Самым характерным свойством азотной кислоты является ее ярко выраженная окислительная способность. Азотная кислота — один из энергичнейших окислителей.
Многие металлоиды легко окисляются ею, превращаясь в соответствующие кислоты.
Так, например, сера при кипячении с азотной кислотой постепенно окисляется в серную кислоту, фосфор — в фосфорную и т. д.
Тлеющий уголек, погруженный в концентрированную азотную кислоту, не только не гаснет, но ярко разгорается, разлагая кислоту с образованием красно-бурой двуокиси азота.
Иногда при окислении выделяется так много тепла, что окисляющееся вещество само собой загорается без предварительного подогревания.
Пример окислительных свойств азотной кислоты
Нальем, например, в фарфоровую чашку немного дымящей азотной кислоты, поставим чашку на дно широкого стакана и, набрав в пипетку скипидара, будем по каплям пускать его в чашку с кислотой.
Каждая капля, попадая в кислоту, воспламеняется и сгорает, образуя большое пламя и облако копоти (рис. 2). Нагретые древесные опилки также загораются от капли дымящей азотной кислоты.
Азотная кислота действует почти на все металлы, за исключением золота, платины и некоторых редких металлов, превращая их в азотнокислые соли.
Так как последние растворимы в воде, то азотной кислотой постоянно пользуются на практике для растворения металлов, особенно таких, как медь, серебро, свинец, на которые другие кислоты не действуют или действуют очень медленно.
Как получить азотную кислоту
В лабораторных условиях азотную кислоту получают действием концентрированной серной кислоты на нитраты, в основном это нитрат калия KNO3, нитрат натрия NaNO3, а также нитрат аммония NH4NO3.
Для этого нитрат помещают в перегоночную колбу и добавляют с излишком серную кислоту, реакция протекает при нагревании, поэтому полученная кислота имеет желтоватый цвет из за частичного разложения кислоты.
Реакция получения азотной кислоты и нитратов:
2. В промышленных масштабах азотную кислоту получают в несколько этапов окислением аммиака NH3.
При 750° и определенном составе смеси происходит почти количественное превращение аммиака в окись азота:
Окись азота легко переходит в двуокись азота, которая с водой образует техническую азотную кислоту, это основной промышленный способ получения.
3. Азотную кислоту можно получить из воздуха дуговым методом. В основе этого метода, впервые технически осуществленного в Норвегии в 1905 г., лежит описанная в реакция непосредственного соединения азота с кислородом.
Необходимая для этой реакции высокая температура получается при помощи электрической душ, питаемой мощным источником электрического тока.
Азотная кислота с металлами
Замечательно, что, как нашел еще М В, Ломоносов, некоторые металлы (железо, алюминий и др.), легко растворяющиеся в разбавленной азотной кислоте, не растворяются в холодной концентрированной азотной кислоте.
По видимому, это происходит вследствие образования на их поверхности тонкого, очень плотного слоя окисла, защищающего металл от дальнейшего действия кислоты.
Такие металлы после обработки их концентрированной азотной кислотой становятся «пассивными», т. е. утрачивают способность растворяться также и в разбавленных кислотах.
Концентрированная азотная кислота реагирует со всеми металлами (кроме золота, платины, палладия) с образованием нитратов и оксида азота (+4) воды:
Фактически концентрированная азотная кислота не реагирует с железом, алюминием, свинцом, оловом, но на их поверхности она образует оксидную плёнку, предохраняющую растворение общей массы металла:
В зависимости от степени разбавленности, азотная кислота образует следующие продукты реакции:
В чом проявляються окислительные свойства азотной кислоты
Окислительные свойства азотной кислоты обусловливаются неустойчивостью ее молекул и присутствием в них азота в его высшем состоянии окисления, отвечающем положительной валентности, равной 5.
Производя окисление, азотная кислота последовательно восстанавливается в следующие соединения:
Степень восстановления азотной кислоты зависит как от ее концентрации, так и от % активности восстановителя.
Чем более кислота разбавлена, тем сильнее она восстанавливается. Концентрированная азотная кислота всегда восстанавливается до оксида азота NO2.
Разбавленная азотная кислота восстанавливается обычно до NO или при действии более активных металлов, как, например, Fe, Zn, Mg, — до N2O.
Если же кислота очень разбавлена, то главным продуктом восстановления является NH3, образующий с избытком кислоты аммонийную соль NH4NO3.
Реакция окисления азотной кислотой
Уравнение реакции азотной кислоты;
Учащемуся рекомендуется самому составить полные уравнения этих реакций.
Следует отметить, что при действии разбавленной азотной кислоты на металлы водород, как правило, не выделяется.
При окислении металлоидов азотная кислота обычно восстанавливается до NO. Например:
Приведенные выше схемы иллюстрируют наиболее типичные случаи окислительного действия азотной кислоты.
Вообще же необходимо заметить, что все реакции окисления, идущие с уча-стием азотной кислоты, протекают очень сложно вследствие одновременного образования различных продуктов восстановления и до сих пор не могут считаться вполне выясненными.
Царская водка
Смесь, состоящая из 1 объема азотной и 3 объемов соляной кислоты, называется царской водкой.
Царская водка растворяет некоторые металлы, не растворяющиеся в азотной кислоте, в том числе и «царя металлов» — золото.
Действие ее объясняется тем, что азотная кислота окисляет соляную кислоту с выделением свободного хлора и образованием хлористого нитрозила NOCl:
Хлористый нитрозил является промежуточным продуктом реакции и разлагается на окись азота и хлор:
Выделяющийся хлор соединяется с металлами, образуя хлориды металлов, поэтому при растворении металлов в царской водке получаются соли соляной, а не азотной кислоты:
Взаимодействие азотной кислоты с органическими веществами
На многие органические вещества азотная кислота действует таким образом, что один или несколько атомов водорода в молекуле органического соединения замещаются нитрогруппами — NO2.
Этот процесс, получивший название нитрования, играет чрезвычайно важную роль в органической химии.
На этом основано получение нитро соединений, важнейшие из них:
1.Тринитроглицерин или динамит, взрывчатое вещество, взрывается от удара, сотрясения, огня.
Для того , чтобы обезопасить его взрывные свойства добавляют аммиачную селитру.
2. Тринитротолуол и тринитробензол или тол, тратил — взрывчатое вещество которое взрывается от сильного удара (инициирующие взрывчатые вещества).
3. Тринитрофенол аналогично динамиту тоже нестабильно и может взорваться от удара или сотрясения, использовался до изобретения тратила в наполнении снарядов, что иногда приводило к разрыву орудий.
4. Динитрофенол — стабилен к ударам и поджиганию горит но не взрывается, детонирует только от воздействия инициирующих взрывчатых веществ.
5. Тринитроклетчатка или тринитроцеллюлоза — пироксилин взрывчатое вещество.
6. Пироксилиновый порох это смесь динамита с пироксилином, и т.д.
Азотный ангидрид
При действии на азотную кислоту фосфорного ангидрида последний отнимает от азотной кислоты элементы воды и в результате образуются азотный ангидрид и метафосфорная кислота.
Это не стойкое твердое взрывчатое вещество в виде бесцветных ромбических кристаллов, при комнатной температуре разлагается на диоксид азота и кислород быстрое нагревание приводит к взрыву.
Получение азотного ангидрита
Пропусканием сухого хлора над сухим нитратом серебра:
4 AgNO3 + 2 Cl2 → 4 AgCl + 2N2O5 + O2, ( в данной реакции может образоваться хлорид серебра и хлорнитрат).
Путём взаимодействия оксида азота(IV) с озоном:
Промышленное получение осуществляется электролизом азотной кислоты в присутствии тетроксида диазота:
Растворы азотного ангидрида в неполярных растворителях, например, в четырёххлористом углероде применяются в качестве мягкого нитрующего агента.
Для чего нужна азотная кислота
Азотная кислота является самым важным соединением азота благодаря разнообразному применению, которое она находит в народном хозяйстве.
В больших количествах азотная кислота расходуется в производстве азотных удобрений и органических красителей.
Она применяется как окислитель во многих химических процессах, используется в производстве серной кислоты по нитрозному способу, служит для растворения металлов, для получения нитратов, применяется для изготовления целлюлозных лаков, кинопленки и в ряде других химических производств.
Азотная кислота идет также на изготовление бездымного пороха и взрывчатых веществ, необходимых для обороны страны и широко используемых в горнорудном деле и при различных земляных работах (строительство каналов, плотин и т. п.).
Как различить соляную серную и азотную кислоты
Соляная кислота в реакциях с растворимыми в воде солями серебра дает нерастворимый осадок хлорида серебра AgCl, эта реакция используется как качественная для определения серебра в растворе и соляной кислоты.
Азотная кислота (разбавленная) реагирует с медью с образованием бурого дыма, в состав которого входит оксид азота и азотная кислота.
Серная кислота концентрированная на вид маслянистая тяжелая жидкость без запаха, на воздухе не дымит, для определения нужно произвести качественную реакцию на сульфат-ион – реакция с хлоридом бария.
Для этого в пробирку с серной кислотой нужно добавить хлорид бария если это серная кислота то на дно колбы выпадет осадок.
Почему азотная кислота не образует кислых солей?
Азотная кислота не образует кислых солей потому, что она является одноосновной кислотой, т. е. имеет всего один катион водорода, который и замещается при образовании соли.
Одноосновные кислоты образуют одну кислую соль, двухосновные — две.
Похожие страницы:
Содержание статьи1 АЗОТНАЯ КИСЛОТА1.1 История получения азотной кислоты1.2 Химически чистая азотная кислота АЗОТНАЯ КИСЛОТА Это азот содержащая неорганическое соединение, в.
Техническая азотная кислота Получение азотной кислоты осуществляется тремя способами, которые мы опишем в том порядке, в каком они начали применяться.
Азотистая кислота HNO2 Если нагревать калиевую или натриевую селитру, то они теряют часть своего кислорода и переходят в соли азотистой.
Развитие азотной промышленности Азотная промышленность охватывает в основном производство аммиака, азотной кислоты и азотных удобрений. Начало ее развитию в СССР.
Гидразин N2H4. Азотистоводородная кислота HN3 Кроме аммиака, азот образует еще два соединения с водородом, не имеющие, однако, такого значения, как.
Содержание статьи1 Пиросерная кислота H2S2O71.1 Применение пиросерной кислоты1.2 Получение солей Пиросерная кислота H2S2O7 При растворении серного ангидрида в серной кислоте.
Читайте также:
