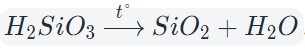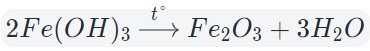Металлы которые не окисляются кислородом
Обновлено: 14.05.2024
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH - | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | - | - | Н | Н | Н | |
| F - | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | - | Н | Р | Р |
| Cl - | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br - | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I - | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | - | - | - | Н | - | - | Н | - | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS - | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | - | Н | ? | Н | Н | ? | М | М | - | Н | ? | ? |
| HSO3 - | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | - | Н | Р | Р |
| HSO4 - | Р | Р | Р | Р | Р | Р | Р | Р | - | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 - | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | - | Р |
| NO2 - | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | - | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO - | Р | Р | Р | Р | Р | Р | Р | Р | Р | - | Р | Р | - | Р | Р | Р | Р | Р | Р | Р | - | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые (
Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую:
Скопируйте эту ссылку, чтобы разместить результат запроса " " на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Внимание, если вы не нашли в базе сайта нужную реакцию, вы можете добавить ее самостоятельно. На данный момент доступна упрощенная авторизация через VK. Здесь вы можете выбрать параметры отображения органических соединений. Эти параметры действуют только для верхнего изображения вещества и не применяются в реакциях.
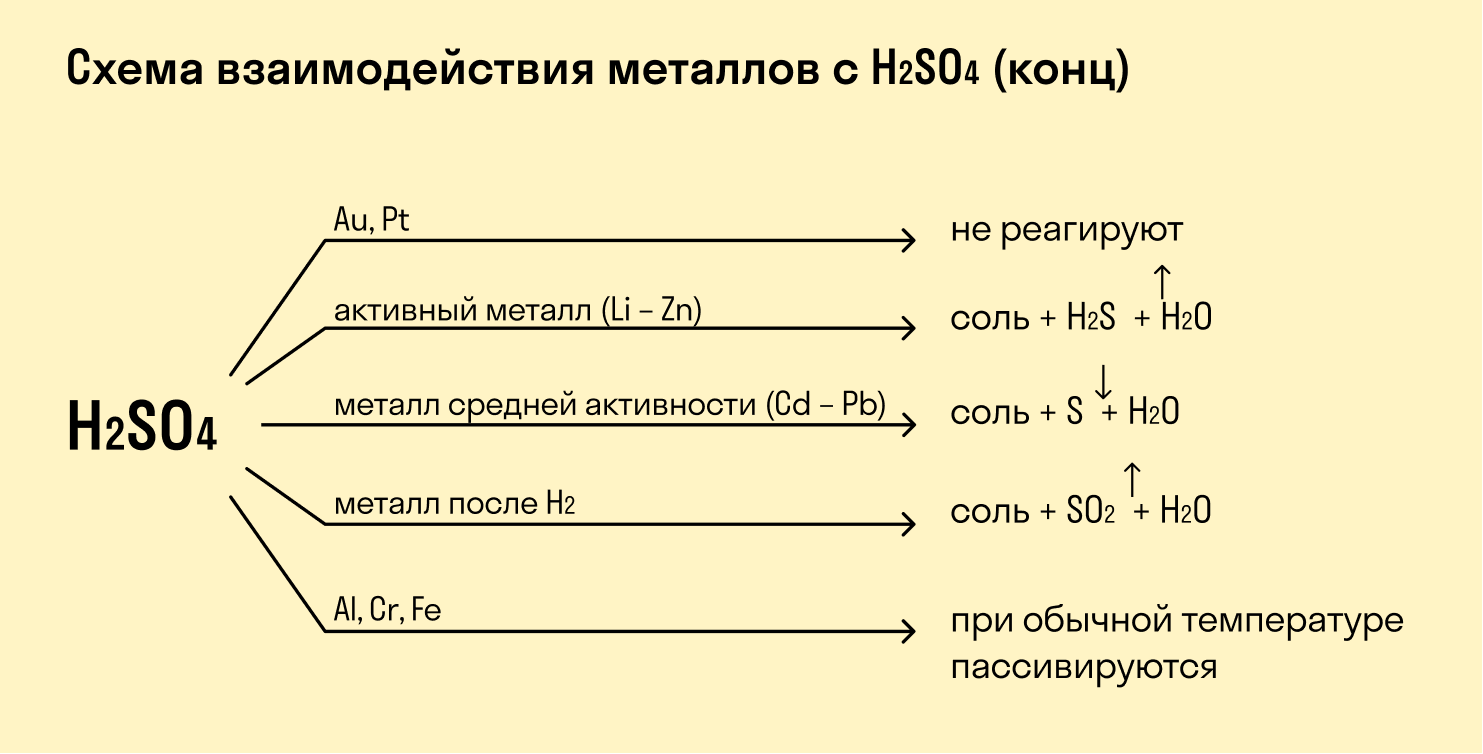
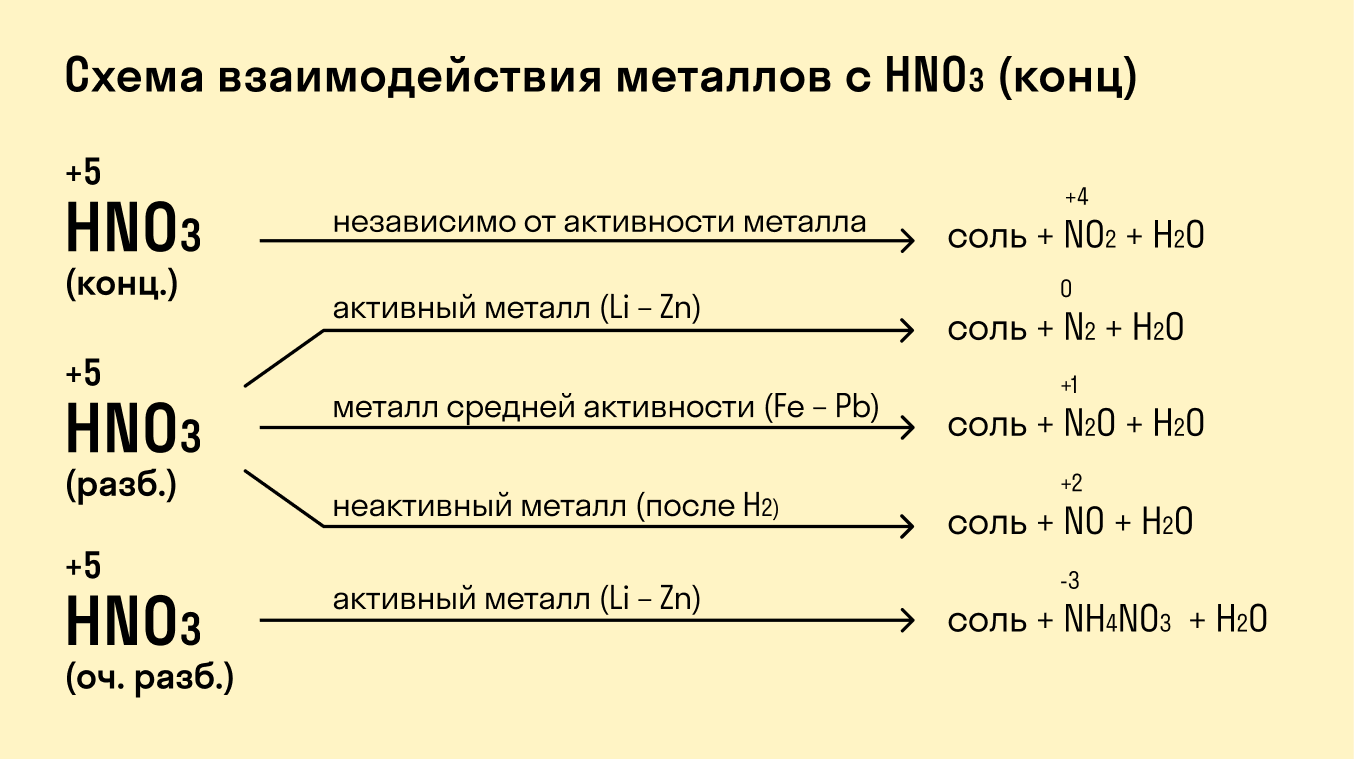
Корректная работа сайта обеспечена на всех браузерах, кроме Internet Explorer. Если вы пользуетесь Internet Explorer, смените браузер. На сайте есть сноски двух типов: Подсказки - помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация - такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Химические свойства металловХарактерным химическим свойством металлов является их восстановительная активность, т.е. способность переходить в состояние положительно заряженного иона, теряя при этом электроны: Количественно восстановительная активность металлов определяется: величиной Еи атома металла (для реакций, протекающих в газовой фазе); величиной стандартного электродного потенциала металла j°iCn/мс (для реакций, протекающих в растворах). При этом следует иметь в виду тот факт, что величина j? Ме п+/ Me изменяется в зависимости от условий процесса, т.к. образовавшиеся ионыМе п+ могут участвовать в процессе комплексообразования. Восстановительная активность металлов проявляется при взаимодействии их с окислителями. Отношение металлов к окислителям - простым веществамМеталлы чаще всего реагируют со следующими окислителями - простыми веществами: кислородом, галогенами, серой, азотом, водородом. Отношение металлов к кислороду. Большинство металлов окисляется кислородом воздуха, но при различных условиях: По отношению к кислороду все металлы принято подразделять на 4 группы: Металлы, активно окисляющиеся кислородом воздуха при обычных условиях. К ним относят: элементы 1А, ПА (кроме бериллий, магний), ШБ (кроме скандия) групп. При взаимодействии указанных металлов с кислородом могут образовываться различные продукты: Z N ci + U - N cV2 О 2 пероксид натрия - Ѕ Металлы, окисляющиеся только с поверхности (с образованием плотной оксидной пленки, предохраняющей металл от дальнейшего окисления). К этой группе металлов относят берилий, магний, скандий, алюминий, цинк, хром, свинец. Например, при окислении алюминия образуется оксидная пленка толщиной менее 30 нм, которая защищает металл от дальнейшего окисления. Металлы, не окисляющиеся при обычных условиях кислородом воздуха (кобальт, никель медь, теллур, рений, висмут и др.) окисляются при нагревании. Поверхностный слой (преимущественно оксидного характера) при этом металл не защищает. Металлы, для которых устойчивы высшие степени окисления, в частности, элементы У1Б-группы, окисляются с образованием высших оксидов. Металлы не окисляющиеся кислородом в отсутствие других реагентов: золото, серебро, палладий, иридий, платина. Для оксидов этих металлов величина D) G° (298 К) > 0, следовательно, образующиеся оксиды этих металлов должны распадаться в момент образования. В некоторых случаях металлы, не взаимодействующие с кислородом, окисляются им в присутствии других соединений. Например, молекулы аммиака, способствующие комплексообразованию, облегчают процесс окисления меди кислородом. Медные изделия на воздухе покрываются зеленоватым налетом - патиной, состоящей преимущественно из основного карбоната меди. Серебряные предметы на воздухе темнеют из-за образования на поверхности металла сульфида серебра. Медь, серебро и золото растворяются в цианидах (в присутствии кислорода). Аллотропная модификация кислорода - озон (02) также является достаточно сильным окислителем, взаимодействующим даже с малоактивными металлами. Отношение металлов к галогенам. Практически все металлы при нагревании окисляются галогенами (F2, СЬ, Вг2,12) с образованием соответствующих галидов (при обычных условиях с галогенами взаимодействуют только элементы 1А-группы). Большинство металлов взаимодействуют с галогенами при нагревании. Отношение металлов к сере. Ртуть с серой взаимодействует при стандартных условиях. Все остальные металлы (за исключением золота, платины, палладия) взаимодействуют с серой при нагревании. Отношение металлов к азоту. При обычных условиях с азотом взаимодействует только литий. Натрий, калий, рубидий, цезий - взаимодействуют с азотом в электрическом разряде. Алюминий, марганец, магний, а также элементы ШБ, IVB, VB, VIB - групп взаимодействуют с азотом при нагревании. Не взаимодействуют с азотом элементы IB, ПБ, VIПБ - групп, а также - олово, свинец, висмут, технеций, рений. Отношение металлов к водороду. При нагревании с водородом взаимодействуют металлы 1А и ПА - групп. Окислителем в данных реакциях является водород. С остальными металлами водород непосредственно не реагирует, но образует со многими из них твердые растворы. Это приводит к повышению хрупкости и снижению пластичности металла. Способность некоторых металлов (алюминий, элементы УБ, VIB, УШБ - групп) поглощать (адсорбировать) своей поверхностью значительные объемы водорода широко используют в катализе. Так, один объем палладия при 80°С может поглотить до 900 объемов водорода, что позволяет использовать его (как и некоторые другие металлы, например, никель) в качестве катализатора в реакциях гидрирования (восстановления водородом). Отношение металлов к окислителям - сложным веществам. В качестве окислителей сложного состава, с которыми чаще всего контактируют металлы, обычно рассматривают воду, водные растворы щелочей и кислот. По химической активности в водных средах все металлы условно делят на: активные - стоящие в ряду напряжений от лития по алюминий (включительно), средней активности - стоящие в ряду напряжений от алюминия до водорода, малоактивные - стоящие в ряду напряжений после водорода. Следует отметить, что восстановительная активность металлов может существенно изменяться в зависимости от условий протекания реакции. В частности, при комплексообразовании величина электродного потенциала металла значительно уменьшается. Аналогичный характер изменения величины электродного потенциала металла наблюдают, если в процессе реакции образуются малорастворимые соединения. Отношение металлов к воде. В реакциях данного типа роль окислителя играют ионы водорода, образующиеся при диссоциации молекул воды. При pH = 7 jAm m = "0.41 В, следовательно, с водой теоретически могут реагировать все металлы, имеющие величину j° меньше - 0,41 В. Реально же наблюдается следующее: а) активные металлы интенсивно взаимодействуют с водой, вытесняя при этом водород. Аналогичная реакция с магнием протекает при нагревании, исключения составляют: - берилий, алюминий и скандий, поверхность которых покрыта прочными оксидными пленками, нерастворимыми в воде; магний, образующийся гидроксид которого - Mg (OH) 2, малорастворим; б) металлы средней активности при стандартных условиях с водой практически не реагируют, т.к. они или покрыты оксидными пленками, или образуют труднорастворимые гидроксиды (хром, никель, цинк) на поверхности металлов. Данные металлы могут разлагать воду при достаточно высоких температурах (до 1000°С). в) малоактивные металлы с водой при обычных условиях не взаимодействуют, поскольку величина их стандартного электродного потенциала значительно больше потенциала окислителя (-0,41 В) и термодинамически данная реакция невозможна. Отношение металлов к водным растворам щелочей. С водными растворами щелочей взаимодействуют металлы, расположенные в ряду напряжений до водорода и образующие амфотерные гидроксиды: берилий, алюминий, цинк, хром, олово, свинец. Взаимодействие часто обусловлено сдвигом величины электродного потенциала металла в сторону отрицательных значений за счет процесса образования гидроксокомплексов. Тем не менее, данный процесс возможен. Его можно представить в виде двух более простых: 1) взаимодействие металла с водой. 2) растворение образующегося амфотерного гидроксида в избытке щелочи с образованием гидроксокомплекса. Отношение металлов к кислотам. По окислительной активности кислоты условно делят на 2 группы: 1) кислоты - слабые окислители. В растворах этих кислот окислителем является ион водорода. 2) кислоты - сильные окислители. Окислителями в растворах этих кислот являются кислородсодержащие анионы. Отношение металлов к кислотам - слабым окислителям. Величина стандартного электродного потенциала окислителя (Н+) при pH = 0 равна j°2ii+л 12 = О В. Следовательно, металлы, стоящие в ряду напряжений до водорода (j°MCn - мс < 0), должны вытеснять его из растворов этих кислот. Исключение составляют металлы, которые при взаимодействии с данными кислотами образуют труднорастворимые соединения. Некоторые малоактивные металлы, не взаимодействующие с разбавленными растворами кислот - слабых окислителей, взаимодействуют с концентрированными растворами этих же кислот. В частности, медь не взаимодействует с разбавленными растворами соляной кислоты, но растворяется в ее концентрированных растворах за счет процесса комплексообразования. Ряд металлов, для которых характерны устойчивые соединения в высшей степени окисления образуют анионные комплексы. Отношение металлов к кислотам - сильным окислителям. а). Отношение металлов к концентрированной серной кислоте. Окислителем в концентрированных растворах серной кислоты является сера в ионах HSCV, SO4 2 '. В зависимости от активности металла он может восстанавливаться до H2S, S или до S02. Кроме этих соединений, во всех трех случаях основными продуктами реакции также являются соответствующая соль (сульфат или гидросульфат) и вода. Некоторые металлы взаимодействуют с концентрированными и разбавленными растворами серной кислоты неодинаково. Так, олово с разбавленной серной кислотой образует соль катионного типа, повышая свою степень окисления до (+2), а с концентрированной серной кислотой образует соль, в которой олово находится в высшей степени окисления (+4). В концентрированных растворах серной кислоты пассивируются на холоду алюминий, хром, железо, кобальт, никель, титан, цирконий, гафний, молибден, вольфрам и др. Не взаимодействуют с серной кислотой: платина, золото, рутений, родий, иридий, и др. б). Отношение металлов к разбавленной азотной кислоте. Окислителем в растворах азотной кислоты является нитрат-ион: N0/. Как и в предыдущем случае, состав основных продуктов реакции определяется активностью металла, участвующего во взаимодействии. Пассивация - торможение (или полное прекращение) химического процесса за счет продуктов взаимодействия (образование труднорастворимых оксидных, гидроксидных, солевых и иных пленок на поверхности металла). Пассивируются в разбавленных растворах азотной кислоты (на холоду) алюминий, молибден, вольфрам и др. Не взаимодействуют: платина, золото, рутений, родий, иридий. в). Отношение металлов к концентрированной азотной кислоте. В отличие от взаимодействия металлов с разбавленной HN03 в данном случае состав продуктов реакции менее разнообразен. В большинстве случаев нитрат-ион восстанавливается до N02. Часто процесс протекает при нагревании. Ряд элементов, имеющих высокие (+4 и более) степени окисления при взаимодействии с концентрированной азотной кислотой образует гидроксиды (оксиды) в данной степени окисления. Пассивируются в концентрированных растворах азотной кислоты (на холоду) бериллий, алюминий, хром, железо, кобальт, никель, титан, цирконий, гафний, свинец, висмут но при нагревании ряд металлов начинает активно взаимодействовать с азотной кислотой. Не взаимодействуют: платина, золото, иридий, рутений, родий, ниобий, тантал. г). Отношение металлов к смесям кислот. Ряд малоактивных металлов (золото, рутений, смий) не растворяется (или очень плохо) в перечисленных выше кислотах - сильных окислителях. Однако, в смесях кислот, в частности, HN03 + ЗНС1 ("царская водка”) эти металлы растворяются. Вместо соляной кислоты при растворении ряда металлов предпочтительнее использовать HF (плавиковая кислота). Отношение металлов к смесям окислителей. Для решения ряда технологических вопросов, связанных с получением или обработкой некоторых металлов, иногда приходится использовать в качестве окислителей различные смеси сложных веществ. Можно привести процессы окисления ряда металлов в щелочной среде: Оксиды
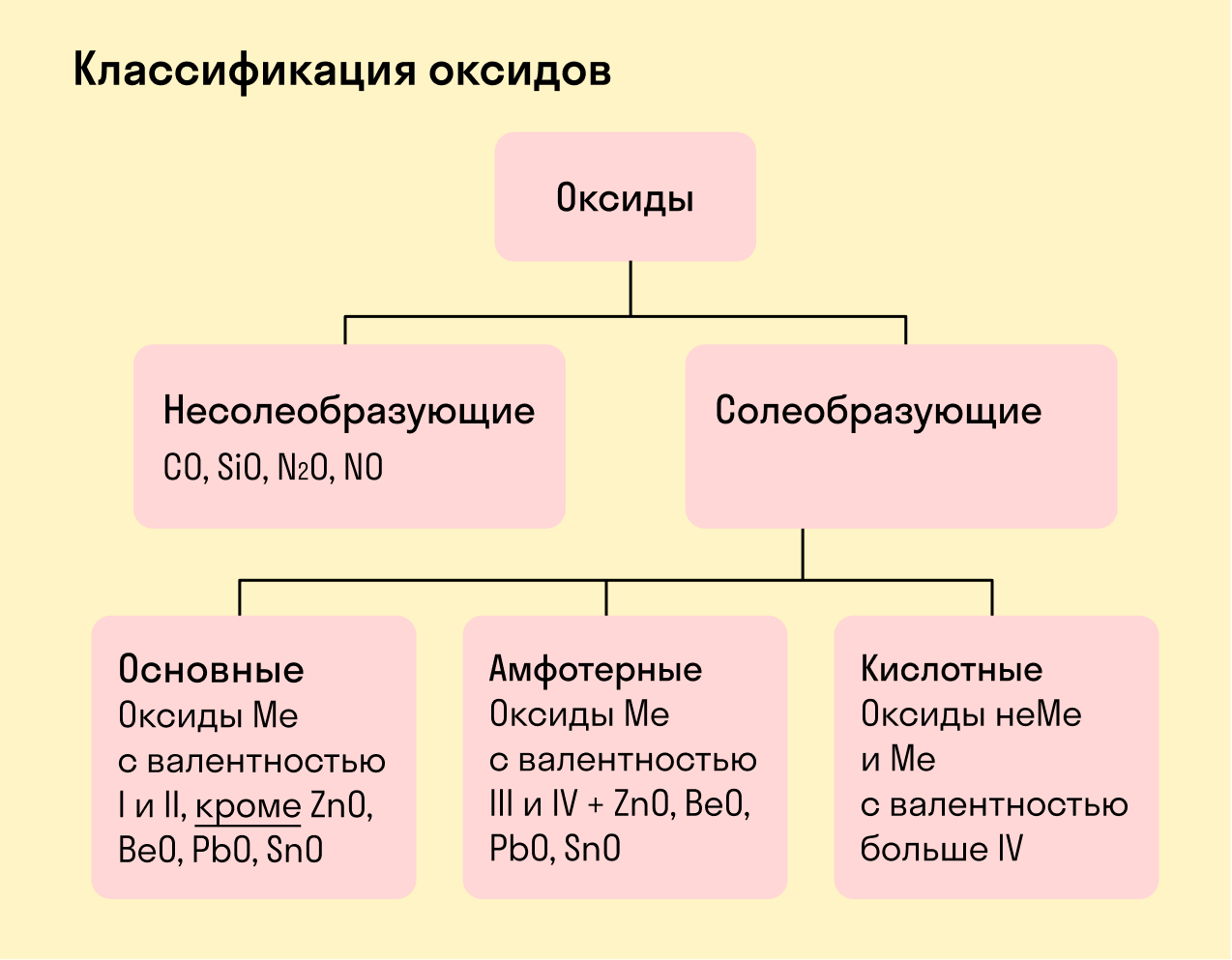
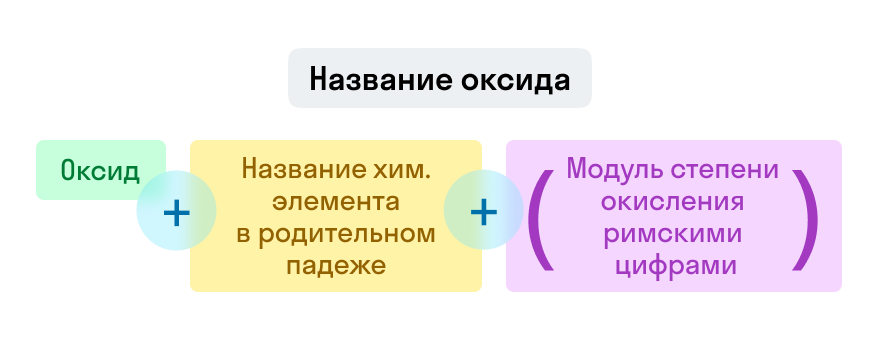
Знакомство с оксидами обычно начинается на уроках химии в 8 классе. Из этой статьи вы узнаете, что такое оксиды в химии, их классификацию и свойства, а также способы получения. О чем эта статья: Определение оксидовОксиды — это сложные вещества, состоящие из двух химических элементов (т. е. бинарные соединения), один из которых — кислород в степени окисления −2. Общая формула оксидов: ЭxOy, где Э – химический элемент, а x и y — индексы, определяемые степенью окисления химических элементов. Виды оксидовВсе оксиды делятся на солеобразующие и несолеобразующие. Несолеобразующие оксиды — это оксиды, которые не взаимодействуют с кислотами и щелочами, то есть не способны образовать соли. К несолеобразующим оксидам относят: CO, SiO, N2O, NO. Солеобразующие оксиды — это оксиды, которые взаимодействуют с кислотами и щелочами с образованием солей. Солеобразующие оксиды делятся на три группы: Основные оксиды — это оксиды, образованные металлами со степенью окисления +1 или +2. Примеры основных оксидов: Na +1 2O, Ca +2 O, Ba +2 O. Амфотерные оксиды — оксиды, образованные металлами со степенью окисления +3 или +4. К амфотерным оксидам относят также: ZnO, BeO, PbO, SnO. Несмотря на то, что эти металлы проявляют степень окисления +2 в данных соединениях, их оксиды проявляют амфотерные свойства. Примеры амфотерных оксидов: Al +3 2O3, Fe2 +3 O3. Кислотные оксиды — оксиды, образованные металлами с валентностью V и более или неметаллами с любой валентностью (за исключением несолеобразующих оксидов, то есть CO, SiO, N2O, NO). Если один и тот же химический элемент образовывает несколько оксидов, то с увеличением степени окисления основные свойства оксидов ослабевают и усиливаются кислотные. CrO (оксид хрома (II)) — проявляет основные свойства; Cr2O3 (оксид хрома (III)) — проявляет амфотерные свойства; CrO3 (оксид хрома (VI)) — проявляет кислотные свойства. Закрепим знания о типах оксидов, изучив схему: Номенклатура оксидовНазвания оксидов строятся по систематической номенклатуре следующим образом: Пишем слово «оксид». Указываем название второго химического элемента в родительном падеже. Если этот элемент имеет переменную валентность, то указываем валентность элемента в этом соединении в скобках римской цифрой. Примеры названий оксидов: Fe2O3 — оксид железа (III). Читается: феррум два о три. Na2O — оксид натрия. Читается: натрия два о. SO3 — оксид серы (VI). Читается: эс о три. До появления систематической номенклатуры вещества называли по присущим им специфическим свойства (цвету, запаху и т. д.). Такой способ названия веществ — тривиальная номенклатура. Некоторые названия используются и сейчас. Названия некоторых оксидов: таблицаХимическая формула оксида Бытовое (тривиальное название) Возможное научное название Химические свойства основных оксидов1. Взаимодействие с водойС водой способны реагировать оксиды тех металлов, которым соответствуют растворимые гидроксиды. То есть с водой реагируют только оксиды щелочных и щелочноземельных металлов. Основный оксид + вода = основание Оксид магния взаимодействует с водой только при нагревании. 2. Взаимодействие с кислотными оксидами и кислотамиОсновные оксиды, соответствующие щелочам, взаимодействуют со всеми кислотными оксидами и кислотами. Оксиды неактивных металлов взаимодействуют только с кислотными оксидами, соответствующими сильным кислотам, или с сильными кислотами. Основный оксид + кислотный оксид = соль Основный оксид + кислота = соль + вода 3. Взаимодействие с амфотерными оксидамиВ эту реакцию могут вступать только основные оксиды щелочных или щелочноземельных металлов. При сплавлении двух оксидов образуется соль. Основный оксид + амфотерный оксид = соль Как составлять такие соли: металл в этой соли берем из основного оксида, а кислотный остаток из амфотерного оксида (они проявляют более кислотные свойства). Химические свойства кислотных оксидовКислотные оксиды взаимодействуют с водой с образованием соответствующих кислот. За исключением SiO2, которому соответствует нерастворимая кремниевая кислота. Кислотный оксид + вода = кислота 2. Взаимодействие с основными оксидами и щелочамиКислотные оксиды сильных кислот способны взаимодействовать с любыми основными оксидами или основаниями. Кислотный оксид + основный оксид = соль Кислотный оксид + основание = соль + вода Кислотные оксиды, соответствующие слабым кислотам (такие как CO2, SO2), способны взаимодействовать с основными оксидами, соответствующим щелочам, а также с щелочами. 3. Взаимодействие с амфотерными оксидами и гидроксидамиС амфотерными оксидами в реакцию вступают кислотные оксиды — как правило, сильных кислот. Кислотный оксид + амфотерный оксид = соль Кислотный оксид + амфотерный оксид = соль + вода Химические свойства амфотерных оксидовАмфотерные оксиды не взаимодействуют с водой — даже при нагревании! Амфотерный оксид + вода ≠ 2. Взаимодействие с кислотными оксидами и кислотойАмфотерные оксиды взаимодействуют только с сильными и средними кислотами и их оксидами. Амфотерный оксид + кислотный оксид = соль Амфотерный оксид + кислота = соль + вода 3. Взаимодействие с основными оксидамиАмфотерные оксиды взаимодействуют только с теми оксидами, которые соответствуют щелочам. Реакция протекает только в расплаве, так как в растворе такие оксиды взаимодействуют преимущественно с водой с образованием щелочей. Амфотерный оксид + основный оксид (расплав) = соль 4. Взаимодействие со щелочамиПродукты взаимодействия амфотерных оксидов со щелочами зависят от условий проведения реакции. В растворе образуются комплексные соли, а при сплавлении – средние соли. Амфотерный оксид + щелочь (раствор) + вода = комплексная соль Амфотерный оксид + щелочь (расплав) = средняя соль + вода Получение оксидов1. Окисление металловПочти все металлы окисляются кислородом до устойчивых степеней окисления. Металлы с переменной степенью окисления, как правило, образуют соединения в степени окисления +3: При взаимодействии щелочных металлов (элемента IA группы) образуются пероксиды Me2O2 или надпероксиды MeO2, где Ме — щелочной металл. 2. Окисление простых веществ — неметалловПри окислении неметаллов в избытке кислорода, как правило, образуются высшие оксиды (это оксиды, в которых неметалл проявляют высшую степень окисления): При недостаточном количестве кислорода образуются оксиды неметаллов в промежуточной степени окисления: Существуют и исключения. Например, сера окисляется лишь до оксида серы (IV) даже в избытке кислорода: Или азот, который взаимодействует с кислородом только при температуре 2 000̊С или под действием электрического разряда с образованием оксида азота (II): Галогены (элементы VIIA группы) вовсе не взаимодействуют с кислородом, так же как и инертные газы (элементы VIIIA группы). 3. Разложение гидроксидовНекоторые кислоты и гидроксиды неустойчивы и самопроизвольно разлагаются по схеме: Гидроксид (кислота) = оксид + вода Оксиды тяжелых металлов (нерастворимые гидроксиды) и кремниевая кислота разлагаются при нагревании по той же самой схеме. 4. Окисление сложных веществСложные бинарные (состоящие из двух химических элементов) соединения окисляются с образованием двух оксидов этих элементов в устойчивых степенях окисления. Также оксиды получают разложением солей, например, карбонатов, нитратов сульфатов и т. д. Мы узнали, какие вещества в химии называют оксидами, какие бывают оксиды, а также разобрали свойства каждого вида. Осталось подкрепить теорию практикой — а сделать это можно на курсах по химии в онлайн-школе Skysmart!
Свойства металлов начинают изучать на уроках химии в 8–9 классе. В этом материале мы подробно разберем химические свойства этой группы элементов, а в конце статьи вы найдете удобную таблицу-шпаргалку для запоминания. 8 класс, 9 класс, ЕГЭ/ОГЭ Металлы — это химические элементы, атомы которых способны отдавать электроны с внешнего энергетического уровня, превращаясь в положительные ионы (катионы) и проявляя восстановительные свойства. В окислительно-восстановительных реакциях металлы способны только отдавать электроны, являясь сильными восстановителями. В роли окислителей выступают простые вещества — неметаллы (кислород, фосфор) и сложные вещества (кислоты, соли и т. д.). Металлы в природе встречаются в виде простых веществ и соединений. Активность металла в химических реакциях определяют, используя электрохимический ряд, который предложил русский ученый Н. Н. Бекетов. По химической активности выделяют три группы металлов. Ряд активности металловМеталлы средней активности Общие химические свойства металловВзаимодействие с неметалламиЩелочные металлы сравнительно легко реагируют с кислородом, но каждый металл проявляет свою индивидуальность: оксид образует только литий натрий образует пероксид калий, рубидий и цезий — надпероксид Остальные металлы с кислородом образуют оксиды: 2Zn + O2 = 2ZnO (при нагревании) Металлы, которые в ряду активности расположены левее водорода, при контакте с кислородом воздуха образуют ржавчину. Например, так делает железо: С галогенами металлы образуют галогениды: Медный порошок реагирует с хлором и бромом (в эфире): При взаимодействии с водородом образуются гидриды: Взаимодействие с серой приводит к образованию сульфидов (реакции протекают при нагревании): Реакции с фосфором протекают до образования фосфидов (при нагревании): Основной продукт взаимодействия металла с углеродом — карбид (реакции протекают при нагревании). Из щелочноземельных металлов с углеродом карбиды образуют литий и натрий: Калий, рубидий и цезий карбиды не образуют, могут образовывать соединения включения с графитом: С азотом из металлов IA группы легко реагирует только литий. Реакция протекает при комнатной температуре с образованием нитрида лития: Взаимодействие с водойВсе металлы I A и IIA группы реагируют с водой, в результате образуются растворимые основания и выделяется H2. Литий реагирует спокойно, держась на поверхности воды, натрий часто воспламеняется, а калий, рубидий и цезий реагируют со взрывом: Металлы средней активности реагируют с водой только при условии, что металл нагрет до высоких температур. Результат данной реакции — образование оксида. Неактивные металлы с водой не взаимодействуют. Взаимодействие с кислотамиЕсли металл расположен в ряду активности левее водорода, то происходит вытеснение водорода из разбавленных кислот. Данное правило работает в том случае, если в реакции с кислотой образуется растворимая соль. 2Na + 2HCl = 2NaCl + H2 При взаимодействии с кислотами-окислителями, например, азотной, образуется продукт восстановления кислоты, хотя протекание реакции также неоднозначно. Металлы IА группы: Металлы IIА группы Такие металлы, как железо, хром, никель, кобальт на холоде не взаимодействуют с серной кислотой, но при нагревании реакция возможна. Взаимодействие с солямиМеталлы способны вытеснять из растворов солей другие металлы, стоящие в ряду напряжений правее, и могут быть вытеснены металлами, расположенными левее: Zn + CuSO4 = ZnSO4 + Cu На металлы IА и IIА группы это правило не распространяется, так как они реагируют с водой. Реакция между металлом и солью менее активного металла возможна в том случае, если соли — как вступающие в реакцию, так и образующиеся в результате — растворимы в воде. Взаимодействие с аммиакомЩелочные металлы реагируют с аммиаком с образованием амида натрия: Взаимодействие с органическими веществамиМеталлы IА группы реагируют со спиртами и фенолами, которые проявляют в данном случае кислотные свойства: Также они могут вступать в реакции с галогеналканами, галогенпроизводными аренов и другими органическими веществами. Взаимодействие металлов с оксидамиДля металлов при высокой температуре характерно восстановление неметаллов или менее активных металлов из их оксидов. 3Са + Cr2O3 = 3СаО + 2Cr (кальциетермия) Вопросы для самоконтроляС чем реагируют неактивные металлы? С чем связаны восстановительные свойства металлов? Верно ли утверждение, что щелочные и щелочноземельные металлы легко реагируют с водой, образуя щелочи? Методом электронного баланса расставьте коэффициенты в уравнении реакции по схеме: Mg + HNO3 → Mg(NO3)2 + NH4NO3 + Н2O Как металлы реагируют с кислотами? Подведем итогиОт активности металлов зависит их химические свойства. Простые вещества — металлы в окислительно-восстановительных реакциях являются восстановителями. По положению металла в электрохимическом ряду можно судить о том, насколько активно он способен вступать в химические реакции (т. е. насколько сильно у металла проявляются восстановительные свойства). Напоследок поделимся таблицей, которая поможет запомнить, с чем реагируют металлы, и подготовиться к контрольной работе по химии. Таблица «Химические свойства металлов»Mg, Al, Mn, Zn, Cr, Fe, Ni, Sn, Pb Cu, Hg, Ag, Pt, Au Восстановительная способность металлов в свободном состоянии Возрастает справа налево Взаимодействие металлов с кислородом Быстро окисляются при обычной температуре Медленно окисляются при обычной температуре или при нагревании Взаимодействие с водой Выделяется водород и образуется гидроксид При нагревании выделяется водород и образуются оксиды Водород из воды не вытесняют Взаимодействие с кислотами Вытесняют водород из разбавленных кислот (кроме HNO3) Не вытесняют водород из разбавленных кислот Реагируют с концентрированными азотной и серной кислотами С кислотами не реагируют, растворяются в царской водке Взаимодействие с солями Не могут вытеснять металлы из солей Более активные металлы (кроме щелочных и щелочноземельных) вытесняют менее активные из их солей Взаимодействие с оксидами Для металлов (при высокой температуре) характерно восстановление неметаллов или менее активных металлов из их оксидов Степень окисления элемента
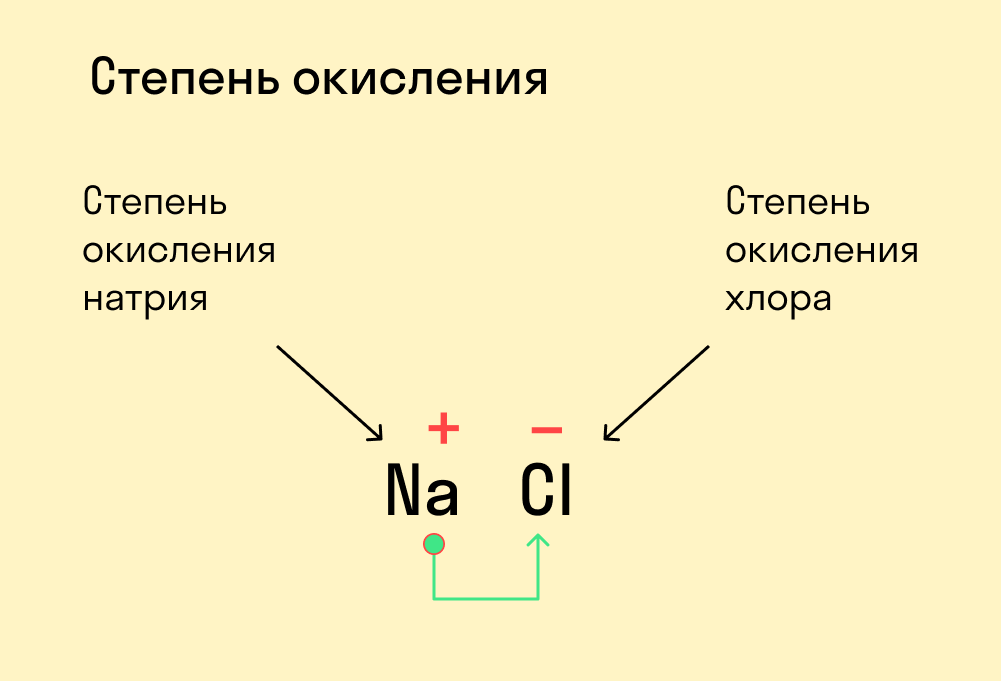
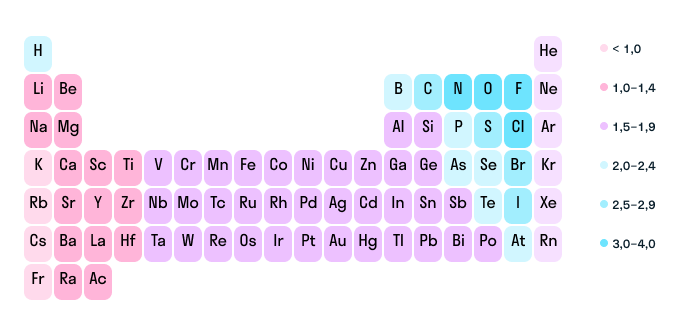
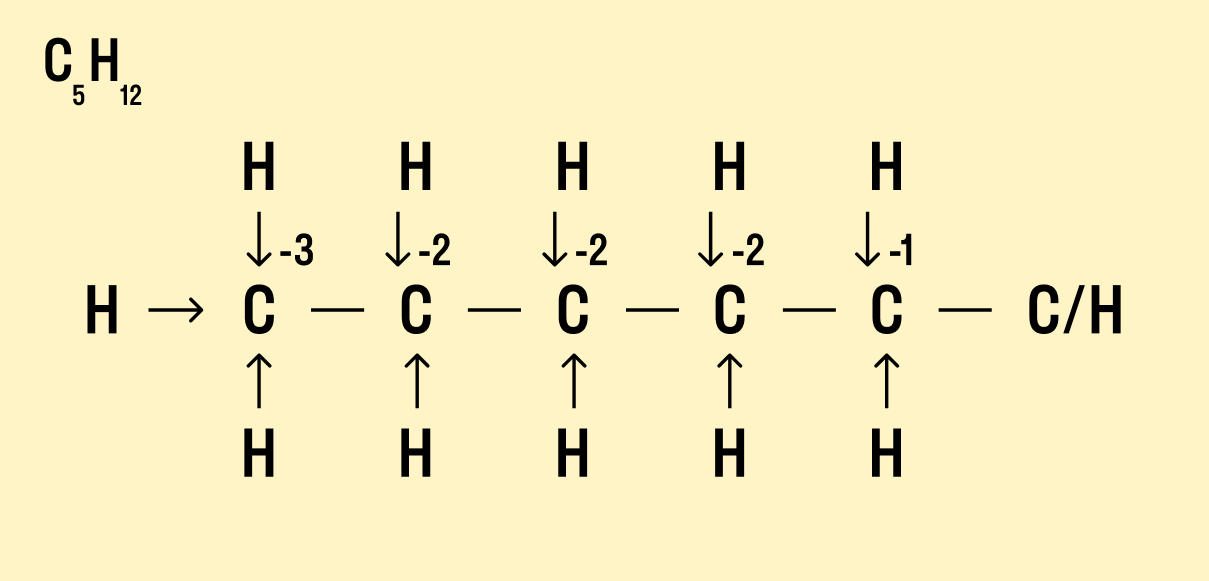
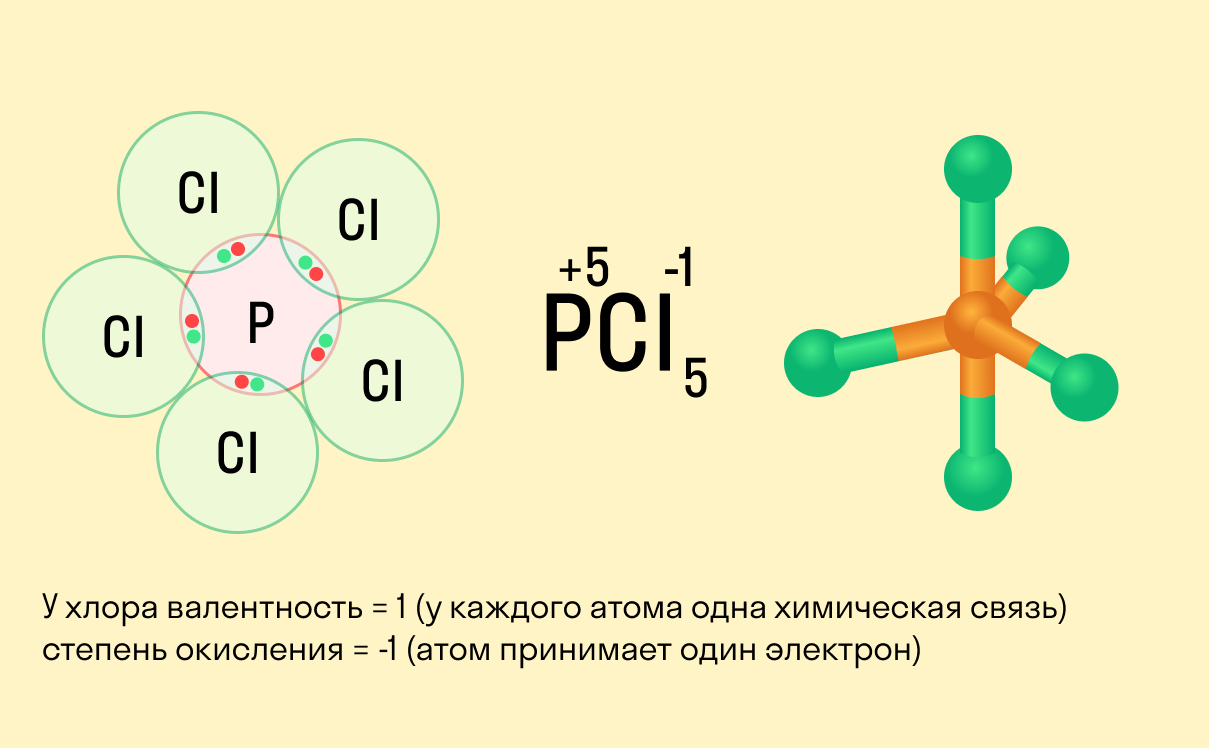
В химии степень окисления элементов говорит о том, как проходят окислительно-восстановительные реакции, а точнее — как при этом атомы перераспределяют между собой электроны. Это не очень сложная тема, но в ней часто бывает путаница. Разберемся, как считать степень окисления в разных соединениях. Что такое степень окисленияДля начала давайте вспомним, как проходят химические связи в молекуле вещества. Взаимодействуя между собой, атомы могут притягивать или отдавать электроны для образования общей электронной пары. Атом с более высокой электроотрицательностью (ЭО) притягивает электроны и приобретает отрицательный заряд, а атом с меньшей ЭО, напротив, отдает электроны и обретает положительный заряд. Степень окисления — это условный заряд, который предположительно обретет атом после перемещения электронов. Он вычисляется из предположения, что все свободные электроны полностью перемещаются от одного атома к другому и все образованные связи — ионные. Почему в определении степени окисления мы говорим об условном заряде? Потому что в реальности он может быть другим, а химические связи атома в соединении не обязательно будут ионными. Но мы предполагаем, что все именно так, чтобы немного упростить расчеты. Это помогает в составлении формул и классификаций. Запомните: Численно степень окисления равна количеству электронов, которые перешли от одного атома к другому. У атома с меньшей ЭО, который отдает электроны, — положительная степень окисления. У атома с большей ЭО, который притягивает электроны, — отрицательная степень окисления. Простые вещества, такие как Cl2, O2 и т. д., имеют степень окисления, равную 0, поскольку смещения электронов в данном случае не происходит. Как рассчитать степень окисленияКак мы уже выяснили выше, определить степень окисления элемента (иначе говоря, окислительное число) помогает электроотрицательность. Значения ЭО легко узнать, пользуясь таблицей Менделеева или шкалой относительной электроотрицательности. Сравните, у какого химического элемента в соединении ЭО выше — этот элемент будет притягивать электроны и приобретет отрицательный заряд. Шкала относительной электроотрицательности В нейтральной молекуле все окислительные числа в сумме образуют ноль. В ионе их сумма равна заряду иона. Это правило поможет составить уравнение и посчитать степень окисления любого химического элемента в соединении, если известны данные по остальным элементам. Еще больше облегчат расчеты следующие закономерности: у водорода в гидридах окислительное число −1, а во всех остальных веществах оно равно +1; у кислорода степень окисления в оксидах равна −2, в пероксидах −1, в соединениях с фтором +2; у неметаллов в соединениях с водородом и металлами окислительное число всегда отрицательное; у металлов степень окисления всегда положительная. Также есть элементы, которые во всех соединениях отдают или принимают одинаковое количество электронов, поэтому их окислительное число — постоянная величина. Алгоритм действийИтак, мы знаем основные закономерности. Давайте разберемся, как находить степени окисления на примерах. Предлагаем следующий алгоритм действий. Посмотрите, является ли вещество элементарным. Если да — значит, оно находится в химически несвязанном состоянии и окислительное число равно 0. Это правило подходит как для веществ, образованных из отдельных атомов, так и для тех, что включают многоатомные молекулы одного и того же элемента. Пример Степень окисления Cl2, S8 равна 0. Если это соединение, определите, состоит ли оно из ионов. В многоатомном ионе сумма всех степеней окисления равна его заряду. Узнайте эту сумму из таблицы растворимости и составьте уравнение с известными окислительными числами. Допустим, нужно определить заряд азота в ионе аммония. Согласно таблице растворимости заряд иона аммония NH4 + равен +1. Это значит, что сумма степеней окисления в этом соединении тоже будет равна +1. Также известно, что водород всюду, кроме гидридов, имеет заряд +1. В данном случае есть 4 атома водорода, т. е. +1 × 4. Составим формулу: х + (+1) × 4 = +1. Значит х = −3. Окислительное число азота в ионе аммония равно −3, т. е. N -3 H4 +1 . Если соединение — нейтральная молекула, составьте уравнение, учитывая, что все окислительные числа в сумме равны 0. Допустим, нужно определить степень окисления серы в соединении Na2SO4. Мы знаем, что у щелочного металла Na постоянное окислительное число +1. Кислород, согласно вышеизложенным правилам, в оксидах имеет заряд −2. Составим уравнение: (+1) × 2 + х + (−2) × 4 = 0. Значит х = −6. Степень окисления серы равна −6, т. е. Na2 +1 S -6 O4 -2 . Как узнать степень окисления нескольких элементовА как быть, если неизвестны окислительные числа двух и более элементов в соединении? В математике уравнения с двумя неизвестными не всегда имеют решение. Но в химии есть выход: можно разделить химическую формулу на несколько частей, которые имеют постоянные заряды. Как вычислить степень окисления в сложном веществе (NH4)2SO4? Посмотрим на него как на соединение двух ионов с известными зарядами: NH4 + и SO4 2- . Поскольку мы знаем окислительные числа водорода и кислорода, найти заряды азота и серы в каждом ионе не составит труда. В ионе NH4 + формула для определения заряда азота будет следующей: х + (+1) × 4 = 1. Понятно, что х = −3, т. е. степень окисления азота −3. В ионе SO4 2- формула для серы х + (−2) × 4 = −2. Следовательно, х = 6, т. е. заряд серы равен +6. Получаем следующие окислительные числа: (N -3 H4 +1 )2S +6 O4 -2 . Как определить высшую и низшую степень окисленияВыделяют высшую (или максимально положительную) и низшую (максимально отрицательную) степени окисления. В диапазоне между ними располагаются окислительные числа, которые могут принадлежать данному химическому элементу в различных соединениях. Для четных групп характерны четные числа в диапазоне, а для нечетных групп — нечетные. Высшая степень окисления совпадает с номером группы элемента (для элементов в главной подгруппе) в короткой форме периодической системы. Низшая степень окисления равна числу, которое получится, если от номера группы элемента отнять 8. Исключения: фтор, железо, кобальт, родий, подгруппа никеля, кислород, благородные газы (помимо ксенона). Проиллюстрируем на примере, как найти высшую и низшую степень окисления. По степени окисления можно понять, как поведет себя вещество в окислительно-восстановительных реакциях. Если в соединении главный действующий элемент имеет высшую степень окисления, оно является окислителем, а если он имеет низшую степень окисления — восстановителем. Например, серная кислота является окислителем, поскольку у серы в данном случае заряд +6. А вот в сернистой кислоте у серы заряд всего +4, поэтому она может проявлять и окислительную способность, и восстановительную. В сероводороде заряд серы равен −2, и это минимальная степень окисления, а значит, данное вещество — восстановитель. Как найти степень окисления в органическом соединенииВ органической химии определять окислительные числа элементов немного сложнее, поскольку все органические вещества включают углерод, известный большим количеством неполярных связей. Если у нас всего один атом углерода, можно использовать стандартный способ. Рассчитайте степень окисления углерода в метаноле H3C−OH. Мы знаем, что водород Н имеет окислительное число +1, а у кислорода в данном случае оно равно −2. Составим уравнение: х + (+1) × 4 + (+2) × 1 = 0 Заряд углерода равен −2, т. е. C -2 H4 +1 O -2 . Но что делать, если атомов углерода больше? Придется анализировать структурную формулу, чтобы понять, какие химические связи есть между элементами и сколько электронов они теряют/приобретают в результате. Такой вариант нахождения окислительного числа называют графическим. Графический методНарисуйте структурную формулу соединения. Изобразите стрелками химические связи и смещение атомов (все связи между атомами углерода С−С считайте неполярными). Посчитайте, сколько стрелок ведет к атому (это «−») и сколько от него (это «+»), а затем суммируйте «+» и «−», чтобы узнать степень окисления. Валентность и степень окисления: в чем разница?Школьники, которые только начали изучать данные разделы химии, нередко путают степень окисления и валентность. Численно эти показатели могут совпадать (но далеко не всегда), а вот по смыслу они в корне различаются. Валентность показывает, какое количество связей способен образовать один атом, а степень окисления — сколько электронов перемещается в результате этих связей. Между этими двумя понятиями есть следующие отличия: валентность не имеет знака, в то время как у окислительного числа он есть («+» или «−»); валентность равна нулю только в том случае, если атом не имеет связей с другими частицами, а степень окисления может быть равна нулю и при наличии таких связей; вычисляя степень окисления, мы предполагаем, что в соединении ионные связи, хотя на самым деле это может быть не так, а валентность всегда имеет реальный смысл. Поэтому отождествлять эти два понятия ни в коем случае не стоит. Более того, не нужно ориентироваться на валентность, пытаясь определить окислительное число. Читайте также:
|