Металлы не претерпевающие аллотропические превращения список
Обновлено: 18.05.2024
Превращения в металлах и сплавах в твердом состоянии по своей физической сущности во многом напоминают кристаллизацию жидких металлов. Эти превращения называют фазовой перекристаллизацией, а при их исследованиях используют те же подходы в отношении механизмов и кинетики формирования новой фазы, включая образование зародышей и последующий их рост.
В чистых металлах основными превращениями в твердом состоянии являются аллотропические (полиморфные), а также магнитные превращения. В сплавах превращения в твердом состоянии дополняются целым рядом превращений, таких как эвтектоидное, перитектоидное, растворение и выделение избыточных фаз и др. Их изучение потребует знания диаграмм фазового равновесия и будет кратко рассмотрено позже.
Аллотропическим (полиморфным) превращением называют изменение пространственной решетки кристаллического тела. В качестве примеров аллотропических превращений можно привести превращение низкотемпературной аллотропической формы a - Fe с объемно-центрированной кубической решеткой в высокотемпературную форму g - Fe с гранецентрированной кубической решеткой, при температуре 911 °С и последующее превращение при температуре 1392 °С g - Fe в d - Fe с объемно-центрированной кубической решеткой, аналогичной a - Fe. Аналогичные превращения можно наблюдать в титане, цирконии и т.д. В титане и цирконии низкотемпературной аллотропической формой являются a - Ti, a - Zr с гексагональной плотноупакованной решеткой. При температуре выше 882° С для титана и 862° С для циркония образуются b - Ti и b - Zr, обладающие объемно-центрированной решеткой.
Аллотропическое превращение заключается в том, что атомное строение кристаллического тела изменяется при нагреве и охлаждении при переходе через критическую точку. Сам процесс перестройки кристаллической решетки происходит изотермически при постоянной температуре, кривая охлаждения сплава претерпевающая аллотропические превращения, аналогична кривой, наблюдаемой при затвердевании жидкого металла (рисунок 2. 11). Температура перехода называется критической точкой превращения. При температуре (Т0) наблюдается фазовое равновесие двух аллотропических разновидностей.
| Рисунок 2.11. Термическая кривая для случая аллотропического при охлаждении | Рисунок 2.12. Изменение свободной энергии системы при аллотропическом превращении |
Аналогично процессу кристаллизации аллотропическое превращение идет с поглощением тепла при нагреве и выделением его при охлаждении. Аллотропическое превращение (также по аналогии с процессом кристаллизации) происходит путем образования зародышей и их последующего роста, в связи с чем оно протекает всегда с наличием переохлаждения (при охлаждении) и перенагрева при нагреве.
Аллотропическое превращение происходит так же как и процесс кристаллизации, в связи со стремлением системы к уменьшению свободной энергии, и поскольку линии, характеризующие изменения свободной энергии в зависимости от температуры, пересекаются при температуре Т0 (рисунок 2.12). При температурах выше Т0 стабильной является b - фаза, при более низкой температуре стабильной оказывается a - фаза, имеющая меньший запас свободной энергии.
В процессах кристаллизации основным препятствием образования твердых кристаллов являются затраты энергии на образование границы раздела фаз. Это вызывает необходимость переохлаждения для начала процесса кристаллизации.
При аллотропическом превращении кроме энергии, затрачиваемой на образование границы раздела фаз, необходимы дополнительные затраты энергии на преодоление упругого сопротивления твердой фазы, связанные с тем, что полиморфные превращения всегда приводят к изменением объема. Поскольку затраты энергии для образования зародышей при аллотропическом превращении больше, чем при кристаллизации из жидкого состояния, то переохлаждение при превращениях в твердом состоянии должны быть гораздо больше, чем при кристаллизации.
Аллотропические превращения могут протекать по двум механизмам:
1. диффузионным (нормальным) путем,
2. бездиффузионным (мартенситным) путем.
В отдельных металлах эти превращения могут протекать как по одному, так и по другому механизму, что будет зависеть от скорости охлаждения.
Диффузионный механизм аллотропического превращения заключается в том, что атомы, располагающиеся в решетке высокотемпературной модификации путем диффузионного перемещения, занимают новые места, характерные для новой аллотропической формы: низкотемпературной модификации.
Следовательно, развитие диффузионного механизма аллотропического превращения наиболее благоприятно при высоких температурах, обеспечивающих большую скорость диффузионного перемещения атомов. Кроме того, если температура превращения настолько высока, что обеспечивает высокую пластичность, то затраты энергии на преодоление упругого сопротивления тела образованию и росту новой фазы, отличающейся от новой фазы удельным объемом становятся меньше, в связи с чем аллотропическое превращение протекает при минимальном переохлаждении. Зародыши новой фазы появляются на границах зерен старой фазы и на других дефектах кристаллов. В дальнейшем происходит рост этих зародышей за счет перехода атомов из старой фазы в новую. Наряду с этим наблюдается продолжение зарождения новых зародышей образующейся фазы.
При переходе металла из одного кристаллографического состояния в другое происходит не только изменение кристаллической структуры, но и имеет место полный процесс фазовой перекристаллизации, при которой на месте старых зерен образуются совершенно новые зерна с новым расположением границ. Причем на месте старого одного зерна могут возникнуть несколько новых или на месте нескольких старых - одно новое зерно.
Этот процесс зависит, главным образом, от скорости охлаждения и степени переохлаждения, которые в основном определяют количество образующихся в единицу времени центров кристаллизации и скорость роста новой фазы. Чем выше скорость охлаждения и выше степени переохлаждения, тем больше количество центов кристаллизации, тем более дисперсными являются зерна новой фазы.
Поскольку аллотропические превращения происходят в твердой среде, наиболее интенсивно процесс фазовой перекристаллизации будет происходить в том случае, если длина диффузных путей будет минимальной. А это означает, что при образовании зародышей должен соблюдаться принцип структурного и размерного соответствия. Он сформулирован С.Т. Конобеевским и заключается в том, что: "форма и ориентировка зародышей новой фазы при кристаллизации должны соответствовать минимуму поверхностной энергии при данном объеме, а минимум поверхностной энергии обеспечивается при максимальном сходстве в расположении атомов на соприкасающихся гранях старой и новой фаз".
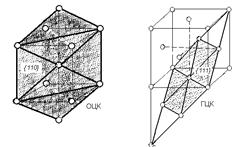 | Рисунок 2.13. Близкие по строению плоскости в решетке ОЦК и в ГЦК решетке |
Поэтому зарождение новой фазы начинается на плоскостях, которые являются наиболее сходными у обеих кристаллических решеток. Например, при переходе g - Fe в a - Fe наибольшее сходство имеют плоскости в g - Fe и в a - Fe (рисунок 2.13).
Преобразованием плоскостей g в a и направлений [110] g в [111] a во всем объеме металла протекает рассматриваемое аллотропическое превращение. При этом происходит лишь небольшой поворот кристаллографических направлений, при котором обеспечиваются углы 70°30¢ и 54°45¢ соответствующие расположению атомов в объемно-центрированном кубе.
Форма выделений новой фазы в основном определяется упругой энергией, возникающей при выделении. Если при аллотропическом превращении наблюдается большая степень размерного и структурного соответствия кристаллов старой и новой фаз, упругая энергия системы минимальна, а кристаллы новой фазы имеют форму дисков (пластин). Кроме того, на форму выделяющихся кристаллов оказывает влияние степень анизотропии упругих свойств обеих фаз. Если модули упругости возникающей фазы для всех направлений меньше, чем модули переходной фазы, в этом случае форма выделений - диски или пластины. Если модуль новой фазы только для одного из направлений меньше, чем модуль исходной фазы, то может появиться игольчатая форма выделений.
Появление новой фазы с новым удельным объемом может способствовать развитию сопутствующих процессов, таких как наклеп (фазовый) и рекристаллизации. Кроме того, на развитие аллотропии может оказывать влияние наличие примесей, которые могут играть роль дополнительных зародышевых центров. Все эти дополнительные параметры могут оказать влияние на окончательную структуру и свойства металла, претерпевшего аллотропическое превращение. В результате собирательной рекристаллизации, сопутствующей аллотропическому превращению, происходит укрупнение зерна, причем тем больше, чем выше температура нагрева. В случае же нагрева до температур, лежащих выше критической точки, когда происходит образование зерен новой фазы, но не успевает начаться укрупнение зерна, обычно получается очень маленькое зерно.
Бездиффузионный или мартенситный механизм аллотропического превращения осуществляется при низких температурах, при которых диффузия или самодиффузия почти не осуществляется. Это превращение происходит или в металлах с низкой температурой аллотропического перехода или при сильном переохлаждении высокотемпературной аллотропической формы в металлах с высокой температурой превращения. Так у кобальта, у которого Т0 = 420 °С, аллотропическое превращение идет только бездиффузионным путем. В железе, титане, цирконии и других металлах с высокой температурой Т0 при большом переохлаждении превращение идет бездиффузионным путем, а при малом переохлаждении - диффузионным путем. При мартенситном аллотропическом превращении новая фаза образуется путем кооперативного и закономерного перемещения атомов таким образом, что они сохраняют своих соседей и смещаются по отношению один к другому на расстояния, не превышающие междуатомные. Основное предположение мартенситного превращения заключается в том, что в процессе перехода старой фазы в новую сохраняется сопряженность (когерентность) их пространственных решеток. При наличии когерентности двух фаз поверхностная энергия границы очень мала, что способствует интенсивному росту образовавшихся кристаллов.
Упругая энергия сравнительно велика, она все время возрастает в процессе роста кристалла. Это происходит до тех пор, пока не будет превзойден предел упругости в переходной зоне. При этом в ней происходит пластический сдвиг, нарушающий когерентность кристаллических решеток старой и новой фаз. Возникновение некогерентной границы приостанавливает рост данного кристалла мартенситной фазы. Дальнейшее увеличение количества образующейся фазы происходит путем образования новых зародышей и мгновенного их роста. Скорость роста кристаллов при мартенситном превращении очень велика и достигает скорости звука. Скорость образования центров кристаллизации подчиняется общим закономерностям фазовых превращений. При развитии мартенситного механизма аллотропического превращения участки новой фазы располагаются вдоль определенных кристаллографических плоскостей старой фазы и выглядят под микроскопом в виде иголок или пластин. Это является результатом структурного и размерного соответствия, устанавливающегося между решетками старой и новой фаз.
Важной особенностью мартенситного превращения является то, что в изотермических условиях превращения только часть старой фазы переходит в новую. Дальнейшее превращение может протекать только при понижении температуры. Мартенситное превращение происходит в интервале температур. Различают точки Мн и Мк - начало и конец мартенситного превращения. Во многих случаях превращение не доходит до конца даже при очень низких температурах. Установлено, что мартенситное превращение, как и нормальное - диффузионное обратимо. Образование высокотемпературной формы из низкотемпературной при достаточной степени перенагрева может происходить бездиффузионным путем.
Магнитное превращение, наблюдаемое в ферромагнитных материалах, не является обычным фазовым превращением. Оно не связано с перемещением диффузией атомов, а вызывается только изменением взаимодействия магнитно нескомпенсированных d или f - электронов, обусловливающих возникновение ферромагнетизма. Характер изменения магнитных свойств зависит от физической природы металла. Температура потери магнитных свойств, называемая точкой Кюри, не зависит от скорости нагрева или охлаждения. Эта температура постоянна для каждого металла. Для железа она равна 768° С, никеля - 365- 370° С, кобальта - 1050° С.
Многие твердые тела способны существовать при различных условиях температуры и давления в нескольких кристаллических разновидностях (модификациях). О таких телах говорят, что они полиморфны или обладают полиморфизмом. Углерод, например, может существовать в двух полиморфных формах или модификациях: в виде алмаза с весьма сложной кристаллической решеткой (решетка типа алмаза) и графита (гексагональная решетка). Применительно к простым кристаллическим образованиям, типичным для металлов, принято говорить не о полиморфизме, а об аллотропии и об аллотропических модификациях.
Аллотропия свойственна не менее чем двенадцати металлам, Ряд из которых имеют важнейшее техническое значение (Sn, Ti, Zr. Сг, Mn, Fe, Co, Ni, V, Np, Pu).
Аллотропические модификации, число которых в некоторых случаях доходит до пяти, принято обозначать греческими буквами а, р, у, 8, « с добавлением символа элемента, например a-Sn, y-Fe, e-Pu и т. д.
Железо при разных температурах способно кристаллизоваться в кубической объемноцентрированной и в кубической гране-центрированной решетках. Оно находится в виде аллотропической модификации альфа (объемноцентрированный куб) в пределах от абсолютного нуля до 910°, модификации гамма (гране-центрированный куб) в пределах от 910 до 140Г и от 1401 до точки плавления 1539° — вновь в виде модификации альфа.
При нагревании и охлаждении чистого железа на кривых температура — время (рис. 1) при переходе одной аллотропической модификации в другую наблюдаются температурные точки скачкообразного превращения в виде горизонтальных участков.
На кривой нагревания заметны две такие остановки: первая наблюдается при 910°, где а-железо переходит в у-железо, и вторая при 1401°, где Т-железо вновь превращается в a-железо. Остановки при 768° и при 1539° не являются точками аллотропических превращений, так как первая остановка сопровождается не перестройкой решетки, а лишь потерей железом магнитных свойств. Вторая остановка при 1539° характеризует не перестройку решетки, а ее разрушение, т. е. переход металла в жидкое состояние.
Из изложенного следует, что на кривой нагревания имеется четыре критические точки:
1) при 768° точка магнитного превращения, при которой железо в процессе нагревания утрачивает магнитность (международное обозначение Асг);
2) при 910° точка аллотропического превращения а-железа немагнитного в т-железо (обозначение Ас3);
3) при 1401° точка аллотропического превращения у-железа вновь в a-железо немагнитное (Ас4);
4) при 1539° точка плавления.
При охлаждении превращения идут в обратном порядке. Критическими точками окажутся: точка затвердевания при 1539°; точка Аг4 при 1401°, точка Аг3 при 898° вместо 910° вследствие температурного отставания или гистерезиса и точка Агг при 768°.
Кобальт при температурах до 419° имеет гексагональную решетку (а-Со), а от 419 и до точки плавления 1492° — гране-центрированную кубическую (р-Со). Олово при комнатных и более высоких температурах существует в виде модификации fi-Sn (белое олово) с тетрагональной решеткой, а при температурах ниже 13,2° — в виде модификации a-Sn (серое олово) со сложной пространственной решеткой типа решетки алмаза.
Полиморфизм (аллотропия) присущ всем химическим элементам, с изменением температуры изменяющим свою валентность, т. е. способным отдавать в среду электронного газа переменное число электронов.
Такое изменение электронного газа сопровождается перестройкой пространственной решетки, причем новая модификация, как обладающая меньшим запасом свободной энергии, оказывается в данной температурной области более устойчивой по сравнению с прежней.
1.Кристаллическое строение металлов. Типы кристаллических решёток.
Все тела состоят из атомов. Тела, в которых атомы расположены беспорядочно, называютаморфными(стекло, канифоль, воск, смола и др.).Кристаллические тела(все металлы и металлические сплавы), характеризуются упорядоченным расположением атомов. В металлах и металлических сплавах атомы находятся в узлах пространственных кристаллических решеток.
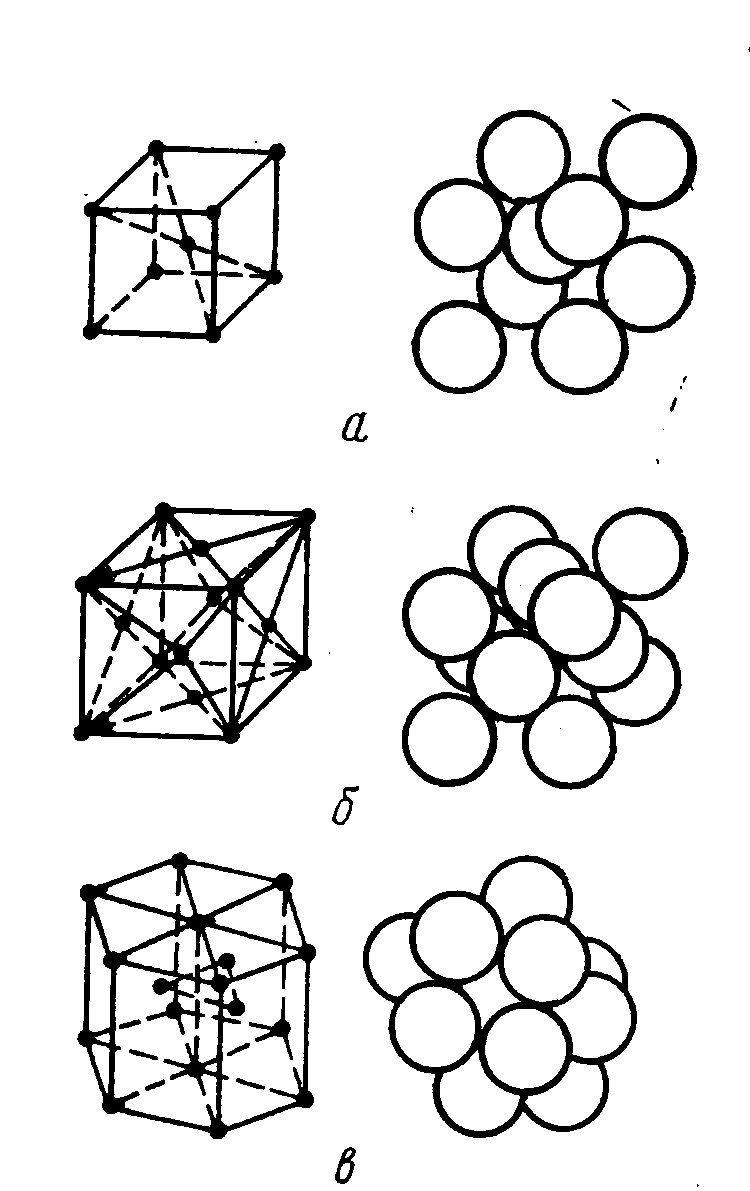
В процессе кристаллизации металлов и сплавов могут образовываться кристаллические решетки разного типа. Наиболее распространенными являются объемно-центрированная кубическая (рис.1, а) (К,V, Сr,Fеа, Мо,W), гранецентрированная кубическая (рис.1, б) (Аl,Fe, Ni, Сu, Аg, Аu, Рb) и гексагональная решетки(рис.1, а) (Ве, Мg, Со,Zn, Тi). Гранецентрированная кубическая и гексагональная решетки характеризуются наиболее плотной упаковкой атомов и их компактным размещением.
Расстояния между соседними атомами в кристаллической решетке (параметр решётки) Рис.1
исключительно малы. Для их измерения пользуются особой единицей - ангстремом (А°), который равен 1А°=10 -8 см, или нанометром (1 нм=10 -9 см).
2. Аллотропические превращения в металлах.
Некоторые металлы в твердом состоянии (железо, марганец, кобальт и др.) в зависимости от температуры нагрева могут иметь кристаллические решетки различного строения и, следовательно, обладать различными свойствами. Это явление называется аллотропией, илиполиморфизмом.Кроме того, известен полиморфизм под влиянием температуры и давления. При нагреве до 2000 °С и давлении ~ 10 10 Па углерод в форме графита перекристаллизовывается в алмаз.
Аллотропические формы принято обозначать буквами греческого алфавита: альфа, бета, гамма и т. д.
К металлам, не претерпевающим аллотропических превращений в твердом состоянии при нагревании и охлаждении, относятся алюминий, магний, медь и др. Большое число технически важных металлов (олово, цинк, никель, кобальт и др.) подвержено аллотропическим изменениям.
3. Процесс кристаллизации. Дефекты кристаллического строения.
Кристаллизациейназывается образование кристаллов в металлах и сплавах при переходе из жидкого состояния в твёрдое (первичная кристаллизация), а также перекристаллизация в твёрдом состоянии (вторичная кристаллизация).
Процесс кристаллизации металла складывается из двух элементарных процессов: образования центров кристаллизации (зародышей) и роста кристаллов из этих центров. При температуре кристаллизации в жидком металле сначала образуются центры кристаллизации, причем их роль играют разные примеси, мельчайшие шлаковые и неметаллические включения. После образования зародышей атомы жидкого металла, расположенные беспорядочно, начинают располагаться вокруг этих зародышей и образуют кристаллы правильной геометрической формы. Так как кристаллизация начинается одновременно во многих местах и рост кристаллов идет по всем направлениям, то смежные кристаллы, сталкиваясь между собой, мешают свободному росту каждого. Это приводит к тому, что кристаллы приобретают неправильную внешнюю форму, несмотря на их упорядоченное внутреннее строение. Кристаллы неправильной формы принято называть кристаллитами, полиэдрами, или зернами. Образовавшиеся реальные кристаллы имеют те или иные несовершенства (дефекты) кристаллического строения, которые принято классифицировать по характеру их измерения в пространстве на точечные (нульмерные), линейные (одномерные),

Рис. 2. Точечные дефекты в кристаллической решетке:
а — вакансия; б — межузельный атом; в — примесный атом внедрения
поверхностные (двухмерные), объемные (трехмерные).
Наиболее распространены точечные. К ним относят вакансии(узлы в кристаллической решетке, свободные от атомов),межузельные атомы (атомы, находящиеся вне узлов кристаллической решетки), а такжепримесные атомы(рис.2).
7 Аллотропическое превращение и магнитное превращение в металлах (превращения в твердых состояниях.
Пространственные кристаллические решетки в некоторых металлах не всегда являются постоянными. При определенных условиях решетки могут изменяться. Это изменение происходит главным образом под влиянием температуры. Не исключено влияние и других факторов — изменения давления, наличия посторонних примесей и т. п. Способность металла иметь различные формы кристаллической решетки называется аллотропией, или полиформизмом. Аллотропические превращения происходят в железе, олове, титане, кобальте и других металлах. Медь, алюминий не претерпевают аллотропических превращений. Сущность аллотропии состоит в том, что при определенных температурах в твердом металле возникают новые центры кристаллизации, в процессе роста которых образуется новая решетка. Формирование новой решетки происходит с поглощением тепла при нагревании и с выделением тепла при охлаждении. Поэтому в период перестройки решетки температура остается неизменной и на кривой охлаждения характеризуется горизонтальной площадкой. Различные формы кристаллической решетки для данного металла называются модификациями. Модификацию, существующую при низких температурах, обозначают буквой а. Важнейшее значение в технике имеют аллотропические превращения в железе. До 1535° железо остается жидким, а при 1535° начинается кристаллизация железа. После затвердевания образуется решетка объемноцентрированного куба б-железа с параметром 2,93 А. Эта решетка сохраняется до 1390°, после чего происходит перестройка ее на новую модификацию у, имеющую гранецентрированную кубическую решетку с параметром 3,65 А. Ниже температуры 910° железо неустойчиво и переходит в новую форму, имеющую объемноцентрированную кубическую решетку с параметром 2,9 А. При температуре 768° происходит последняя температурная остановка, но она связана не с перестройкой решетки, а с образованием модификации а и появлением магнитных свойств.
8 Дефекты кристаллического строения металлов (дислокация) и их влияние на прочность.
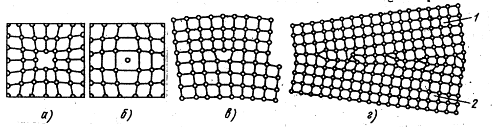
В кристаллах всегда имеются дефекты (несовершенства) строения, обусловленные нарушением правильного расположения атомов кристаллической решетки. Дефекты кристаллического строения подразделяют по геометрическим признакам на точечные, линейные и поверхностные. Атомы совершают колебательные движений возле узлов решетки, и с повышением температуры амплитуда этих колебаний увеличивается. Большинство атомов данной кристаллической решетки имеют одинаковую (среднюю) энергию и колеблются при данной температуре с одинаковой амплитудой. Однако отдельные атомы обладают энергией, значительно большей средней энергии, и перемещаются из одного места в другое. Наиболее легко перемещаются атомы поверхностного слоя, выходя на поверхность. Место, где находился такой атом, называется вакансией (рис. 2, а). Рис. 2. Дефекты в кристаллах: а - вакансия, б — внедренный атом, в краевая линейная дислокация, г - неправильное расположение атомов на границе зерен 1 и 2 На это место через некоторое время перемещается один из атомов соседнего слоя и т. д. Таким образом вакансия перемещается в глубь кристалла. С повышением температуры количество вакансий увеличивается и они чаще перемещаются из одного узла в другой. В диффузионных процессах, протекающих в металлах, вакансии играют определяющую роль. К точечным дефектам относят также атом, внедренный в междоузлие кристаллической решетки (рис. 2, б), и замещенный атом, когда место атома одного металла замещается в кристаллической решетке другим, чужеродным атомом. Точечные дефекты вызывают местное искажение кристаллической решетки. Линейные дефекты являются другим важнейшим видом несовершенства кристаллической решетки, когда в результате сдвига на одно межатомное расстояние одной части решетки относительно другой вдоль какой-либо плоскости число рядов атомов в верхней части решетки на один больше, чем в нижней. В данном случае в верхней части решетки появилась как бы лишняя атомная плоскость (экстраплоскость). Край экстраплоскости, перпендикулярный направлению сдвига, называется краевой, или линейной, дислокацией (рис. 2, в), длина которой может достигать многих тысяч межатомных расстояний. Шириной дислокации считают расстояние от центра дефекта до места решетки без искажения. Ширина дислокации мала и составляет несколько атомных расстояний. Кристаллическая решетка в зоне дислокации упруго искажена, поскольку атомы в этой зоне смещены относительно их равновесного состояния. Для дислокации характерна их легкая подвижность. Это объясняется тем, что атомы, образующие дислокацию, стремятся переместиться в равновесное состояние. Дислокации образуются в процессе кристаллизации металлов (см. гл.1, § 2), а также при пластической деформации, термической обработке и других процессах. Поверхностные дефекты представляют собой границы раздела между отдельными кристаллами (рис. 2, г). На границе раздела атомы кристалла расположены менее правильно, чем в его объеме. Кроме того, по границам раздела скапливаются дислокации и вакансии, а также концентрируются примеси, что еще больше наpyшает порядок расположения атомов. При этом сами кристаллы разориентированы, т. е. могут быть повернуты относительно друг друга на десятки градусов. Прочность металла может либо увеличиваться вследствие искажений кристаллической решетки вблизи границ, либо уменьшаться из-за наличия примесей и концентрации дефектов. Дефекты в кристаллах существенно влияют на свойства металлов.
Анизотропия кристаллов. Неодинаковость физических свойств среды в разных направлениях называют анизотропией. Анизотропия кристаллов обусловлена различаем плотности упаковки атомов в решетке в различных направлениях. Все кристаллы анизотропны, а аморфные тела (стекло, смола) изотропны, т. е. имеют одинаковую плотность атомов в различных направлениях. Анизотропия свойств важна при использовании монокристаллов — одиночных кристаллов, частицы которых расположены единообразно по всему их объему. Монокристаллы имеют правильную кристаллическую огранку (в форме естественных многогранников), анизотропны по механическим, электрическим и другим физическим свойствам. Металлы и сплавы, применяемые в технике, обычно имеют поликристаллическую структуру, т. е. состоят из множества мелких и различно ориентированных кристаллов, не имеющих правильной кристаллической огранки и называемых кристаллитами (или зернами). В каждом зерне поликристалла наблюдается анизотропия. Однако вследствие разнообразной, беспорядочной ориентировки кристаллографических плоскостей в различных зернах поликристалл может иметь одинаковые свойства по разным направлениям и не обнаруживать анизотропию (когда размеры зерен значительно меньше размеров пол и кристалла и количество их весьма велико). Это обстоятельство во многих случаях позволяет рассматривать поликристаллическое тело как подобное изотропному, несмотря на анизотропию свойств отдельных составляющих его зерен. 9 Упругая и пластическая деформация.
Деформация – это изменение формы и размеров тела, деформация может вызываться воздействием внешних сил, а также другими физико-механическими процессами, которые происходят в теле. К деформациям относятся такие явления, как сдвиг, сжатие, растяжение, изгиб и кручение.
Упругая деформация – это деформация, которая исчезает после снятия нагрузки. Упругая деформация не вызывает остаточных изменений в свойствах и структуре металла; под действием приложенной нагрузки происходит незначительное обратимое смещение атомов.
При растяжении монокристалла возрастают расстояния между атомами, а при сжатии атомы сближаются. При смещении атомов из положения равновесия нарушается баланс сил притяжения и электростатического отталкивания. После снятия нагрузки смещенные атомы из-за действия сил притяжения или отталкивания возвращаются в исходное равновесное состояние и кристаллы приобретают первоначальные размеры форму.
Деформация может быть упругой, исчезающей после снятия нагрузки, и пластической, остающейся после снятия нагрузки.
Самое малое напряжение вызывает деформацию, причем начальные деформации являются всегда упругими и их величина находится в прямой зависимости от напряжения. Основными механическими свойствами являются прочность, пластичность, упругость.
Важное значение имеет пластичность, она определяет возможность изготовления изделий различными способами обработки давлением. Эти способы основаны на пластическом деформировании металла.
Материалы, которые имеют повышенную пластичность, менее чувствительны к концентраторам напряжений. Для этого проводят сравнительную оценку различных металлов и сплавов, а также контроль их качества при изготовлении изделий.
Физическая природа деформации металлов
Под действием напряжений происходит изменение формы и размеров тела. Напряжения возникают при действии на тело внешних сил растяжения, сжатия, а также в результате фазовых превращений и некоторых других физико-химических процессов, которые связанны с изменением объема. Металл, который находится в напряженном состоянии, при любом виде напряжения всегда испытывает напряжения нормальные и касательные, деформация под действием напряжений может быть упругой и пластической. Пластическая происходит под действием касательных напряжений.
Упругая – это такая деформация, которая после прекращения действия, вызвавшего напряжение, исчезает полностью. При упругом деформировании происходит изменение расстояний между атомами в кристаллической решетке металла.
С увеличением межатомных расстояний возрастают силы взаимного притяжения атомов. При снятии напряжения под действием этих сил атомы возвращаются в исходное положение. Искажение решетки исчезает, тело полностью восстанавливает свою форму и размеры. Если нормальные напряжения достигают значения сил межатомной связи, то произойдет хрупкое разрушение путем отрыва. Упругую деформацию вызывают небольшие касательные напряжения.
Пластической называется деформация, остающаяся после прекращения действия вызвавших ее напряжений. При пластической деформации в кристаллической решетке металла под действием касательных напряжений происходит необратимое перемещение атомов. При небольших напряжениях атомы смещаются незначительно и после снятия напряжений возвращаются в исходное положение. При увеличении касательного напряжения наблюдается необратимое смещение атомов на параметр решетки, т. е. происходит пластическая деформация.
При возрастании касательных напряжений выше определенной величины деформация становится необратимой. При снятии нагрузки устраняется упругая составляющая деформации. Часть деформации, которую называют пластической, остается.
При пластической деформации необратимо изменяется структура металла и его свойства. Пластическая деформация осуществляется скольжением и двойникованием.
Скольжение в кристаллической решетке протекает по плоскостям и направлениям с плотной упаковкой атомов, где сопротивление сдвигу наименьшее. Это объясняется тем, что расстояние между соседними атомными плоскостями наибольшее, т. е. связь между ними наименьшая. Плоскости скольжения и направления скольжения, лежащие в этих плоскостях, образуют систему скольжения. В металлах могут действовать одна или одновременно несколько систем скольжения.
Металлы с кубической кристаллической решеткой (ГЦК и ОЦК) обладают высокой пластичностью, скольжение в них происходит во многих направлениях.
Процесс скольжения не следует представлять как одновременное передвижение одной части кристалла относительно другой, оно осуществляется в результате перемещения в кристалле дислокаций. Перемещение дислокации в плоскости скольжения ММ через кристалл приводит к смещению соответствующей части кристалла на одно межплоскостное расстояние, при этом справа на поверхности кристалла образуется ступенька.
2.2. Аллотропия (полиморфизм) металлов
Аллотропией, или полиморфизмом, называется способность металлов в твердом состоянии иметь различное кристаллическое строение, а следовательно, и свойства при различных температурах.
Процесс перехода из одной кристаллической формы в другую называется аллотропическим (полиморфным) превращением. Аллотропические формы обозначают начальными буквами греческого алфавита: альфа α, бета β, гамма γ, дельта δ и т. д., начиная с той формы, которая существует при более низкой температуре.
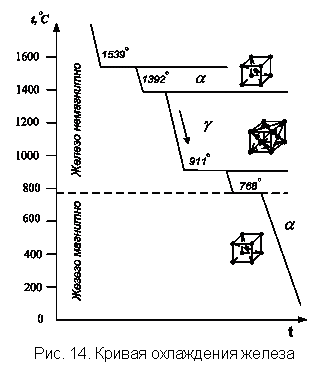
На рис. 14 приведена кривая охлаждения железа, характеризующая аллотропические превращения. Железо имеет объемно центрированную кубическую решетку до температуры 911 °С и в интервале 1392–1539 °С (Feα), а от температуры 911 до 1392 °С имеет гранецентрированную кубическую решетку Feγ. Высокотемпературная α-модификация (от 1392 до 1539 °С) иногда обозначается Feδ (δ – железо). При температуре 768 °С происходит изменение магнитных свойств: ниже 768 °С железо магнитно, выше 768 °С железо немагнитно.
Характерным примером является аллотропия олова. При температуре ниже 18 °С устойчива модификация α-олова (Snα), называемая серым оловом, а выше 18 °С – модификация β-олова (Snβ), называемая белым оловом.
Решетка белого олова более компактна, чем серого олова, и превращение Snβ Snα идет со значительным увеличением объема. Поэтому при образовании на белом олове бугорка серого олова последнее, вследствие больших объемных изменений, рассыпается в порошок. Это явление получило название «оловянной чумы», превращение необратимо.
Максимального значения скорость аллотропического превращения Snβ Snα достигает при переохлаждении примерно до температуры – 30 °С. Поэтому опасность «оловянной чумы» особенно велика при хранении олова в зимнее время в холодном помещении.
2.3. Основные сведения о сплавах
Должны знать, что металлическим сплавом называется вещество, состоящее из двух или более элементов (металлов или металлов с металлоидами), обладающее металлическими свойствами. Обычным способом приготовления сплавов является сплавление, но иногда применяют спекание, электролиз или возгонку.
В большинстве случаев входящие в сплав элементы в жидком состоянии полностью растворимы друг в друге, т. е. представляют собой жидкий раствор, в котором атомы различных элементов более или менее равномерно перемешаны друг с другом (рис. 15, а). В твердом виде сплавы способны образовывать твердые растворы, химические соединения и механические смеси (рис. 15, б, в, г).
в Химическое
г Механическая

Рис. 15. Структура и строение элементарной ячейки пространственной кристаллической решетки различных сплавов из двух металлов А к В: – атомы металлаA; – атомы металла В
Твердый раствор. Во многих сплавах при переходе в твердое состояние (при кристаллизации) сохраняется однородность распределения атомов различных элементов и, следовательно, сохраняется и растворимость. Образовавшийся в этом случае кристалл (зерно) называется твердым раствором.
Микроструктура твердого раствора в условиях равновесия представляет собой совершенно однородные и одинаковые по составу зерна и похожа на структуру чистого металла (рис. 15, б). Твердый раствор, как и чистый металл, имеет одну кристаллическую решетку. Различие состоит только в том, что в кристаллической решетке чистого металла все узлы заняты атомами одного элемента, а в твердом растворе — атомами различных элементов, образующих этот твердый раствор.
Растворимость в твердом состоянии может быть неограниченной и ограниченной. Растворимость твердого раствора, полученного при любом количественном соотношении элементов, называется неограниченной.Растворимость твердого раствора, полученного при определенном количественном соотношении элементов, называется ограниченной.
По расположению атомов в кристаллической решетке различают твердые растворы замещения и твердые растворы внедрения.
В твердом растворе замещения атомы растворенного элемента занимают узлы атомов элемента растворителя, т. е. расположены в узлах общей кристаллической решетки (рис. 16, а).
В твердом растворе внедрения атомы растворенного элемента располагаются внутри кристаллической решетки элемента растворителя между атомами металла-растворителя (рис. 16, б).
При образовании твердых растворов свойства сплавов изменяются плавно и отличаются от свойств элементов, из которых они состоят.
Химическое соединение. Особый характер металлической связи в сплавах приводит к образованию особого вида химических соединений. В отличие от обычных химических соединений многие металлические соединения имеют переменный состав, который может изменяться в широких пределах. Характерной особенностью металлического химического соединения является образование кристаллической решетки (см. рис. 13, б), отличной от решеток образующих элементов, и существенное изменение всех свойств.
Иногда в металлических сплавах образуются также химические соединения с нормальной валентностью, например, оксиды, сульфиды, а также соединения металлов с резко отличным электронным строением атомов (Mg2Sn, Mg2Pb и др.).
Механическая смесь. Если элементы, входящие в состав сплава, не растворяются друг в друге в твердом состоянии и не вступают в химическую реакцию с образованием соединения, то при этих условиях из атомов каждого элемента образуется отдельная кристаллическая решетка, и кристаллы (зерна) элементов, входящие в сплав, образуют механическую смесь (рис. 15,г). При образовании механической смеси, когда каждый элемент кристаллизуется самостоятельно, свойства сплава получаются средними между свойствами элементов, которые его образуют.
Механические смеси образуются также в случаях, когда элементы обладают ограниченной растворимостью, а также когда образуют химическое соединение. Если в сплаве количество элементов превышает их предельную растворимость, то возникает механическая смесь двух насыщенных твердых растворов. При наличии в сплаве химического соединения образуется механическая смесь из зерен твердого раствора и химического соединения и т. д.
При изучении процессов, происходящих в металлах и сплавах при их превращениях, и описании их строения в металловедении пользуются следующими понятиями: «фаза», «структура», «система», «компонент».
Фазой называются однородные составные части системы (металла или сплава), имеющие одинаковый состав, кристаллическое строение, свойства и одинаковое агрегатное состояние.
Например, жидкий металл является однофазной системой; смесь жидкого металла и твердых кристалликов – двухфазной системой, так как свойства жидкого металла значительно отличаются от свойств твердых кристалликов. Фазами могут быть отдельные металлы, их химические соединения, а также растворы на основе металлов.
Под структурой понимают форму, размеры и характер взаимного расположения соответствующих фаз в металлах и сплавах.
Структурными составляющими сплава называются обособленные части сплава, имеющие одинаковое строение с присущими им характерными особенностями. Структурные составляющие могут состоять из одной, двух или более фаз. Одна из важнейших задач металловедения – определение взаимосвязи между составом, структурой и свойствами.
Системой называется совокупность фаз, находящихся в равновесии при определенных внешних условиях (температура, давление). Система, может быть, простой, если она состоит из одного элемента, и сложной, если она состоит из нескольких элементов.
Компонентами называют вещества, образующие систему. Компонентами могут быть элементы (металлы и неметаллы) или устойчивые химические соединения.
Читайте также:
