Накопление тяжелых металлов в растениях
Обновлено: 17.05.2024
ТЯЖЁЛЫЕ МЕТАЛЛЫ / РАСТИТЕЛЬНЫЕ СООБЩЕСТВА / ТОКСИЧНОСТЬ / АНТРОПОГЕННОЕ ЗАГРЯЗНЕНИЕ / ТЕХНОГЕННОЕ ВОЗДЕЙСТВИЕ / HEAVY METALS / PLANT ASSOCIATIONS / TOXICITY / ANTHROPOGENIC POLLUTION / TECHNOGENIC EXPOSURE
Аннотация научной статьи по экологическим биотехнологиям, автор научной работы — Чикенева Ирина Валерьевна
Поступление тяжёлых металлов в окружающую среду может быть естественным (природным) и техногенным. Наиболее мощные потоки металлов возникают вокруг предприятий чёрной и особенно цветной металлургии. При длительном их поступлении вокруг таких предприятий образуются зоны с высоким уровнем содержания тяжёлых металлов в почве и скудной растительностью.
Похожие темы научных работ по экологическим биотехнологиям , автор научной работы — Чикенева Ирина Валерьевна
Приоритетность накопления макроэлементов в исследуемых растительных сообществах, находящихся под техногенным прессом (на примере Орско-Новотроицкого промышленного узла)
Особенности накопления тяжелых металлов в исследуемых растительных сообществах, развивающихся в зоне промпредприятий Орско-Новотроицкого промузла
PECULIARITIES OF HEAVY METALS ACCUMULATION IN PLANT ASSOCIATIONS AND THEIR IMPACT ON THE ENVIRONMENT
It is pointed out that heavy metals can get into the environment in a natural or technogenic way. The heaviest metal flows are being observed in the vicinity of enterprises of iron and steel industry and non-ferrous metal manufacture in particular. In cases of long-lasting metal flows the zones with high levels of heavy metals content in soil and poor vegetation are being formed near such enterprises.
Текст научной работы на тему «Особенности накопления тяжёлых металлов в изучаемых растительных сообществах и их воздействие на окружающую среду»
Особенности накопления тяжёлых металлов в изучаемых растительных сообществах и их воздействие на окружающую среду
И.В. Чикенева, к.б.н., Оренбургский ГПУ
Группа тяжёлых металлов (ТМ) объединяет свыше 40 химических элементов с атомной массой более 50 а.е.м. К наиболее токсичным химическим элементам относят бериллий, кобальт, никель, медь, цинк, олово, теллур, рубидий, серебро, кадмий, золото, ртуть, свинец, сурьму, висмут, платину. Для живых организмов важны и необходимы все химические элементы, поэтому правильнее будет рассматривать не токсичность, а токсичную концентрацию элемента [1—3].
Значительное развитие промышленности привело к тому, что содержание тяжёлых металлов в почвах постоянно повышается. На способность металлов мигрировать в почве и переходить в растения большое влияние оказывает увлажнённость, температура, освещение, кислотно-щелочная реакция среды [1, 4]. Так, Ю.М. Алексеев предлагает следующий убывающий ряд фитотоксичности: №
себя ионы мышьяка, селена, алюминия, кадмия, хрома, железа, марганца, цинка и др. Токсичность металла в чистом виде меньше, чем в сочетании с другими металлами. Также был описан антагонистический характер взаимоотношений отдельных химических элементов. Г.М. Илькун указывает, что существует обратная линейная связь между содержанием никеля и кальция, никеля и марганца и положительная — между никелем и кобальтом, кобальтом и марганцем [5]. Наряду с корневым поглощением у растений присутствует и внекорневое. Корни являются мощным биологическим барьером для токсических веществ, однако в условиях аэрогенного загрязнения среды тяжёлыми металлами разница в их накоплении в корнях и надземной части меньше, чем в экспериментах, когда ими загрязняется только почва [3].
ТМ отличаются от других металлов высоким содержанием в промышленных отходах и высокой токсичностью, своей долговечностью и практической невыводимостью из системы: почва — растения — животные — человек [2]. Источники и пути техногенного рассеивания тяжёлых металлов разнообразны. Наиболее значительными являются выбросы в атмосферу при высокотемпературных технологических процессах (металлургическое производство, сжигание мазута, масел, каменного угля и т.д.). Известно, что интенсивность вовлечения в био-
геохимический круговорот соединений ТМ из техногенных источников примерно в 100 раз выше, чем из природных.
Эти металлы относятся к категории неспецифических загрязняющих веществ, так как присутствуют практически во всех почвах в том или ином количестве. Большая часть их относится к микроэлементам, содержание их в почве находится в пределах микроконцентраций, измеряемых в миллиграммах на килограмм почвы. Как недостаток, так и избыток микроэлементов в почвах приводит к различным отклонениям в развитии растений. Таким образом, загрязнение среды может действовать в двух направлениях: с одной стороны, устранять ограничения в доступности для растений необходимых металлов, с другой — повышать поступление металлов до их токсических уровней [1, 4, 6].
Наиболее мощные потоки металлов возникают вокруг предприятий чёрной и особенно цветной металлургии. При длительном поступлении из стационарных источников их содержание в почвах сопоставимо с количеством в естественных геохимических аномалиях или даже превосходит его. Вокруг крупных предприятий образуются зоны с высоким уровнем содержания тяжёлых металлов в почве и скудной растительностью [1, 4, 7].
Основное количество поллютантов от предприятий чёрной и цветной металлургии поступает в почву в виде техногенной пыли. Поступление тяжёлых металлов из атмосферы на растительный и почвенный покровы осуществляется в виде сухих и влажных выпадений (осадков в виде дождя и снега, туманов и росы) [3].
Попадающие на поверхность почвы или растений соединения металлов поглощаются и частично перерабатываются в процессе естественного круговорота веществ. Некоторые металлы обладают большей подвижностью и быстро выносятся из почвы в ходе вертикальной и горизонтальной миграции, другие, менее подвижные, способны к длительной миграции в окружающей среде.
Разумеется, различные металлы имеют неодинаковые пределы обнаружения в почве. Известно, что содержание металлов зависит также от типа самой почвы. Миграция большинства элементов происходит тем интенсивнее, чем ниже содержание в ней гумуса и чем легче гранулометрический состав.
Продолжительность пребывания загрязняющих веществ в почвах гораздо больше, чем в других частях биосферы, и, по мнению А. Кабата-Пендиас и Х. Пендиас, практически вечно. При этом первый период полуудаления ТМ значителен и сильно варьирует: для цинка — от 70 до 510 лет, для кадмия — от 13 до 1100 лет, для меди — от 310 до 1500 лет и для свинца — от 740 до 5900 лет [6].
Химический состав растений зависит от состава сред, на которых произрастают растения, но не повторяет его, так как растения избирательно поглощают необходимые им элементы в соответствии с физиологическими и биохимическими потребностями [4].
Влияние избытка тяжёлых металлов на растения может быть как прямым, так и косвенным. Прямое влияние связано с непосредственным накоплением металлов растениями, косвенное — с негативным воздействием тяжёлых металлов на состав и свойства почвы и на её плодородие [5].
Изучение реакции растений на загрязнение среды тяжёлыми металлами является одной из задач биологического мониторинга окружающей среды. Специфические характеристики обмена у различных видов растений обусловливают их избирательную способность к накоплению одного или нескольких элементов [5].
Материалы и методы. Изучение степного комплекса в районе Орско-Новотроицкого промузла проводили в каждый вегетационный период (май — сентябрь) 2006—2007 гг. За время исследований на 4 стационарных участках было заложено 120 учётных площадок и 4 почвенных профиля. Для определения количественного содержания тяжёлых металлов было отобрано 252 образца (132 надземных и 120 подземных).
Участок № 1. N 51°13.803' E 058°24.803', высота 273 м, направление В 182 км. Располагается в 3 км на запад от Новотроицкого комбината (ОХМК), в 70 м севернее дороги Орск — Ново-троицк. Почва: чернозём южный маломощный глубокосолончаковый (гипсовый) на охристых глинах древней коры выветривания. Растительное сообщество — залесскоковыльно-полынково-типчаковое (Festuca valesiaca-Artemisia austriaca-Stipa zalesskii).
Участок № 2. N 51°13.512' E 058°22.983', высота 210 м, направление В 181 км. В 0,5 км на запад от Новотроицкого комбината ОХМК. Почва: чернозём южный карбонатный маломощный на жёлто-охристой коре выветривания. Растительное сообщество — залесскоковыльное (Stipa zalesskii).
Участок № 3. N 51°14.916' E 058°33.066', высота 204 м, направление В 191 км. В 0,5 км восточнее ЮУНК г. Орска. Почва: чернозём южный карбонатный малогумусный маломощный тяжёлосуглинистый. Растительное сообщество — молочайно-пырейно-житняковое (Agropyron pectinatum-Elytrigia repens — Euphorbia virgata).
Участок № 4. N 51°21.561' E 058°06.506', высота 345 м, направление В 158 км. В 30 км западнее г. Орска. Контрольный участок. Почва: чернозём южный маломощный тяжёлосуглинистый. Растительное сообщество-грудницево-залесскоковыльное (Stipa zalesskii-Galatella villosa).
На протяжении вегетативного периода с мая по сентябрь закладывались площадки (50 х 50 см), где травостой срезали на уровне почвы. Ветошь выбирали из укосных образцов при их разборе. Подстилку собирали с площадок после снятия надземной массы. Разделённые таким образом образцы высушивали до воздушно-сухого состояния. Запас корней учитывали методом монолитов. На площадке, с которой убрана надземная часть растительного сообщества, вынимали почвенный монолит размером 50 х50 см на глубину распространения корней (примерно 50 см). Отобранную почву укладывали в плотные мешки и этикировали. В лаборатории крупные корни выбирали вручную, остальные промывали водой на сите. Подземные органы делили на мёртвые и живые. Корни помещали в цилиндр, наполненный водой, где живые корни оседали на дно, а мёртвые всплывали. Корни, выбранные таким методом, извлекали из цилиндра и сушили до воздушно-сухого состояния. Сбор образцов проводили в трёхкратной повторности [4].
Были приняты следующие обозначения: G — зелёная надземная масса, L — подстилка, D — ветошь, R — живые корни, V — мёртвые корни, «av» указывает среднее значение за определённый период, «max» определяет максимальное значение соответствующего запаса за период, М — минерализация надземного органического вещества, W — его минерализация в подземной сфере. Единица измерения запасов и приростов — ц/га [3].
С целью установления промышленного воздействия на растительный покров отбирали пробы надземных и подземных органов растений для биогеохимических анализов. Подготовка проб растительных образцов проводилась в соответствии с требованиями к отбору проб при общих и локальных загрязнениях [8]. В полученных вытяжках определяли содержание тяжёлых металлов (Zn, Cu, Pb, Cd, Co, Mn, Ni) на атомно-адсорбционном спектрофотометре
типа С-115 ТМ в ФГУ ГЦАС «Оренбургский». Полученные данные пересчитывали кг/га.
Результаты исследования. По динамике содержания ТМ в растительных сообществах нами выявлена приоритетность их накопления в исследованных сообществах, блоках [8].
Залесскоковыльно-полынково-типчаковое сообщество. В среднем (табл. 1) за весь период исследования в данном сообществе в наибольшей степени накапливается Мп и N1, причём N1 занимает лидирующее положение в блоке G, а в 2007 г. и в блоке L. Соответственно в остальных блоках наиболее активно накапливается Мп. Менее активно аккумулируется Сё и Со.
Залесскоковыльное сообщество. В среднем за период исследования можно сказать, что в 2006 г. Мп в наибольшей степени накапливается в блоках G и L. В блоке D на первое место выходит 7п, оставляя за собой Мп и N1 в порядке снижения. В 2007 г. в надземной сфере растительных сообществ лидирует Мп, в подземной — №. В ветоши на первом месте — /п. Менее активно аккумулируется Сё, Со, РЬ (табл. 2).
Молочайно-пырейно-житняковое сообщество. В наибольшей степени за период исследования во всех блоках молочайно-пырейно-житнякового сообщества накапливается № (табл. 3). Далее в порядке снижения следует Мп и в двух случаях Со, причём № занимает лидирующее положение в блоке G, а в 2007 г. и в блоке L. Менее активно аккумулируется Сё и РЬ.
Высокое содержание № относительно других ТМ в основных блоках исследуемых сообществ связано с особенностями промышленной деятельности ЮУНК, где основным видом выпускаемой предприятием продукции является никель гранулированный.
Грудницево-залесскоковыльное сообщество. В наибольшей степени в 2006 г. в блоках G, R, и V накапливается Мп, далее в порядке снижения идут 7п и N1 (табл. 4). В блоке D на первое место выходит N1, оставляя за собой Мп в порядке
1. Приоритетность содержания ТМ с мая по сентябрь в залесскоковыльно-полынково-типчаковом сообществе (среднее)
G Ni > Mn > Zn > Cu > Pb > Co > Cd G Ni > Mn > Zn > Cu > Co > Pb > Cd
D Mn > Ni > Cu > Zn > Pb > Cd > Co D Mn > Zn > Pb > Ni > Cu > Co > Cd
L Mn > Ni > Zn > Pb > Cu > Co > Cd L Ni > Mn > Zn > Pb > Cu > Co > Cd
R Mn > Ni > Zn > Cu > Co > Pb > Cd R Mn > Zn > Ni > Cu > Pb > Co > Cd
V Mn > Zn > Ni > Cu > Pb > Co > Cd V Mn > Zn > Ni > Cu > Pb > Co > Cd
2. Приоритетность содержания ТМ с мая по сентябрь в залесскоковыльном
G Mn > Zn > Ni > Pb > Cu > Cd > Co G Mn > Zn > Ni > Pb > Cu > Co > Cd
D Zn > Mn > Ni > Cu > Pb > Co > Cd D Mn > Zn > Ni > Pb > Cu > Co > Cd
L Mn > Ni > Zn > Pb > Cu > Co > Cd L Mn > Zn > Pb > Ni > Cu > Co > Cd
R Ni > Mn > Cu > Zn > Co > Pb > Cd R Ni > Mn > Zn > Cu > Co > Pb > Cd
V Ni > Mn > Zn > Cu > Pb > Co > Cd V Ni > Mn > Co > Cu > Zn > Pb > Cd
3. Приоритетность содержания ТМ с мая по сентябрь в молочайно-пырейно-житняковом сообществе (среднее)
G Ni > Mn > Cu > Zn > Co > Pb > Cd G Ni > Mn > Cu > Zn > Co > Pb > Cd
D Ni > Mn > Zn > Cu > Pb > Co > Cd D Ni > Mn > Zn > Cu > Pb > Co > Cd
L Ni > Mn > Zn > Cu > Co > Pb > Cd L Ni > Co > Cu > Mn > Zn > Pb > Cd
R Ni > Mn > Cu > Zn > Co > Pb > Cd R Ni > Mn > Cu > Co > Zn > Pb > Cd
V Ni > Cu > Mn > Co > Zn > Pb > Cd V Ni > Co > Mn > Cu > Zn > Pb > Cd
4. Приоритетность содержания ТМ с мая по сентябрь в грудницево-залесскоковыльном сообществе (среднее)
G Mn > Zn > Cu > Ni > Pb > Co=Cd G Ni > Mn > Zn > Cu > Co > Pb > Cd
D Ni > Mn > Zn > Cu > Co > Pb > Cd D Mn > Zn > Ni > Pb > Cu > Co > Cd
L Cu > Zn > Mn > Ni > Pb > Co > Cd L Mn > Ni > Zn > Cu > Co > Pb > Cd
R Mn > Ni > Zn > Cu > Pb > Co > Cd R Mn > Zn > Ni > Cu > Pb > Co > Cd
V Mn > Zn > Ni > Cu > Pb > Co > Cd V Mn > Zn > Ni > Cu > Co > Pb > Cd
снижения. В блоке L наиболее активно аккумулируется Си. В 2007 г. в фитомассе лидирует N1, в остальных блоках — Мп, на второе место выходит 2п. Менее активно накапливается Сё, Со, РЬ.
Нами выявлена следующая тенденция: в залесскоковыльно-полынково-типчаковом и молочайно-пырейно-житняковом сообществах концентрация /п, N1, РЬ, Мп увеличивается в одинаковых пропорциях (в 6 раз). Такая же зависимость отмечена между залесскоко-выльным и грудницево-залесскоковыльным сообществами (в 1,5 раза). Это связано с тем, что залесскоковыльно-полынково-типчаковое и молочайно-пырейно-житняковое сообщества находятся примерно на одинаковом удалении от источника загрязнения, где и оседает большее количество ТМ. Залесскоковыльное сообщество, находящееся в непосредственной близости к ОХМК, возможно, располагается на таком удалении, где осаждение ТМ невелико. Напротив, грудницево-залесскоковыльное сообщество развивается на достаточном удалении от влияния промпредприятий (в 30 км), находясь в наименьшей досягаемости выбросов. Другой причиной такой зависимости может быть видовой состав
сообществ. Так, в фитоценозах, где доминантом является Stipa zalesskii, содержание тяжёлых металлов в общесуммарном зачёте невысокое в отличие от других исследуемых растительных сообществ [8].
В зависимости от особенностей динамики ТМ в природе, а также структуры, строения и расположения растительных сообществ, аккумуляция металлов блоками исследуемых фитоценозов проходит с различной активностью.
1. Алексеев Ю.М. Тяжёлые металлы в почвах и растениях. Л.: Агропромиздат, 1987. 142 с.
2. Добровольский В.В. Тяжёлые металлы: загрязнение окружающей среды и глобальная геохимия // Тяжёлые металлы в окружающей среде. М.: МГУ, 1980. С. 3-11.
3. Ильин В.Б. Тяжёлые металлы в системе почва — растение. Новосибирск: Наука, 1991. С. 148.
4. Кин Н.О. Современное состояние растительного покрова в зоне влияния газоперерабатывающих предприятий Западного Казахстана: дисс. . канд. биол. наук. Оренбург, 2000. 241 с.
5. Илькун Г.М. Загрязнители атмосферы и растения. Киев: Наукова думка, 1978. 110 с.
6. Кабата-Пендиас А., Пендиас X. Микроэлементы в почвах и растениях. М.: Мир, 1989. 439 с.
7. Donaubauer E. Was ist Saurer Ragen, Wodurch sterben die Walder // Gemeinwirtschaft. 1983. Bd. 2. S. 33—37.
8. Чикенева И.В. Эколого-биогеохимическая оценка растительного покрова зоны влияния Орско-Новотроицкого промышленного узла: дисс. . канд. биол. наук. Оренбург, 2009. 174 с.
Накопление тяжелых металлов в растениях в зависимости от уровня загрязнения почв

В статье рассматриваются проблемы загрязнения окружающей среды от деятельности металлургической промышленности. Приведены основные загрязняющие вещества металлургического производства. Даны содержания тяжелых металлов в почве и растениях.
In the article it is considered a problem of environmental pollutioncaused by mining industry. The main polluters of thi mining and metallurgical complex are given by stages of regeneration cycle. Recommendations on refining the ecologicalcondition
Одним из основных принципов концепции устойчивого развития является: право на развитие должно быть реализовано таким образом, чтобы удовлетворять потребности в развитии сохранении окружающей среды нынешнего и будущих поколений. Так как особенность многих видов природных ресурсов проявляется в том, что их использование ограничено во времени. Уровень их потребления сегодня должен жестко предопределять возможность удовлетворения потребности в них в будущем. Именно с этой проблемой природопользования связан вопрос рационального использования природных ресурсов, так как предприятия перерабатывающей промышленности в основной своей части являются эколого-опасными. Поэтому решение данных проблем предопределяет необходимость поиска оптимального, рационального обеспечения текущих и будущих потребностей и выработки обоснованной политики недропользования и охраны окружающей среды [1]. В настоящее время воздействие человека на окружающую среду по своим масштабам превосходит способности природы к самовосстанавлению. Опасны мигрирующие отходы не полностью протекающих технологических процессов: газовые выбросы, сточные воды промышленных предприятий, содержащие токсичные соединения и попадающие в почву и водоемы [2].
Наиболее крупные загрязнители окружающей среды в Южно-Казахстанской области сосредоточены в городе Шымкент. Среди них АО ПК «Южполиметалл» расположен в территории города и оказывает существенное влияние на загрязнение окружающей среды, а неблагоприятная экологическая обстановка в районе свинцового производства складывалась годами. АО ПК “Южполиметалл” оказывает существенное влияние на накопление тяжелых металлов в почве и растениях.
Мы изучили закономерности распространения и аккумуляции тяжелых металлов растениями в зависимости от содержания их в почве и определили содержание тяжелых металлов в почве и растениях распространенных участках территории города
Для исследования использованы были следующие методы: атомно-адсорбционным метод определения содержания тяжелых металлов в почве и растениях (свинец, кадмйя, цинк и медь).
Для оценки пространственного распределения тяжелых металлов в г.Шымкент были выбраны 4 пункта исследования.
Пункт № 1 расположен в 200 м от АО ПК “Южполиметалл”. Пункт № 2 расположен на расстоянии 3 км от свинцового производства, в центре города. Пункт № 3 расположен на расстоянии 5 км в северо-восточном направлении города. Пункт № 4 — контрольный пункт, расположенный в 80 км от города. Из выше перечисленных пунктов отбирались пробы почвы и растения, как подорожник ланцетолистный (Plantago lanceolata), мятлик луговой (Paa protensis) и ячмень заячий (Hordeum leporinum), клен ясенелистный (acer negundo), тополь черный (Populus nigra), карагач (Ulmus pumila), ива Вавилонская (Salix babilonica), акация белая (Robinia pseudoacacia)
Данные о содержании тяжелых металлов в почве представлен в рисунке 1.
Как видно из таблицы, содержание свинца в почве показало, что максимальная концентрация данного элемента характерна для района металлургического производства. Содержание свинца в пункте № 1 составило 946,11 ± 5,04 мг/кг, что превышает ПДК в 27 раз, а контрольный показатель в 45 раз. Это объясняется тем, что 30–35 % промышленных выбросов оседают на территории производства. Высокотоксичный свинец является основным выбросом свинцового производства, так как происходит накопление его в почве. В других пунктах исследования по мере удаления от свинцового производства наблюдается снижение содержания свинца в почве.
Содержание цинка в почве составляет в пункте № 1 171,30±4,64 мг/кг, то-есть по сравнению с контрольным пунктом в 14 раз превышает контрольный показатель, а ПДК в 2 раза. Высокое содержание цинка так-же отмечаны в пункте № 2, оно составляет 20,65±2,14 мг/кг, что превышает контрольный показатель в 10 раз, но не превышает ПДК. В других пунктах содержание цинка не превышает показатель контрольного пункта. Наиболее высокие содержания меди и кадмия так-же были установлены в производственном пункте. Во всех других пунктах содержание меди не превышает ПДК, но по сравнению с контрольным пунктом превышает контрольный показатель. Содержание кадмия во всех пунктах превышает ПДК.
Высокие содержания выше указанных тяжелых металлов установлены в районе АО ПК “Южполиметалл” (пункт № 1). В других пунктах по мере удаления от производства содержание тяжелых металлов в почве снижается.
Рис. 1. Содержание тяжелых металлов в почве (мг/кг)
Почва является важнейшим объектом окружающей среды. В отличие от других объектов окружающей среды (воздух, вода), где протекают процессы самоочищения, почва обладает этим свойствам в незначительной мере. Более того для некоторых веществ, в частности для тяжелых металлов почва является едким акцептором.
Тяжелые металлы прочно сорбируются и взаимодейтвуют с почвенным гумусом, образуя труднорастворимые соединения. Таким образом идет их накопление в почве. Наряду с этим в почве под воздействием различных факторов происходит постоянная миграция поподающих в нее веществ и перенос их на большие расстояния [3].Тяжелые металлы попадающие в почву с выбросами предприятий, прочно связываются уже в верхнем слое. Максимальное содержание металлов в почвах наблюдается на расстояниях 1–3 км от источников загрязнения [4].
Данные о содержании тяжелых металлов в растениях представлены на рисунке 2,3.
Как видно из рисунка, акация белая, тополь черный и мятлик луговой аккумулирует свинец в высокой степени. Его содержание в пункте № 1 составило в акаций белой 292,9 мг/кг, что превышает ПДК 58 раз, а контрольный показатель в 15 раз. Содерание свинца в тополе 91,42 мг/кг (18 ПДК), контрольный показатель превышает в 5 раз, в мятлике луговой — 67,14 мг/кг, что превышает контрольный показатель в 27 раза, а ПДК — в 13 раз. Содержание свинца в ячмене тоже высокое, оно составило 42,14±2,32 мг/кг, что превышает контрольный показатель в 21 раз, а ПДК — в 8 раз. У подорожника ланцетолистного содержание свинца составляет 31,07±2,65 мг/кг, что превышает контрольный показатель в 15 раз, а ПДК — в 6 раз. Анализ результатов определения содержания цинка в изучаемых видов растениий также показал различную аккумулятивную способность.
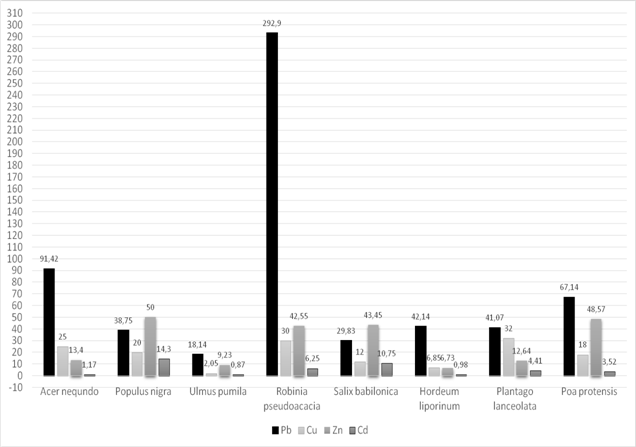
Рис. 2. Содержание тяжелых металлов в растениях (Пункт № 1- район ЗАО «Южполиметалл»), (мг/кг)
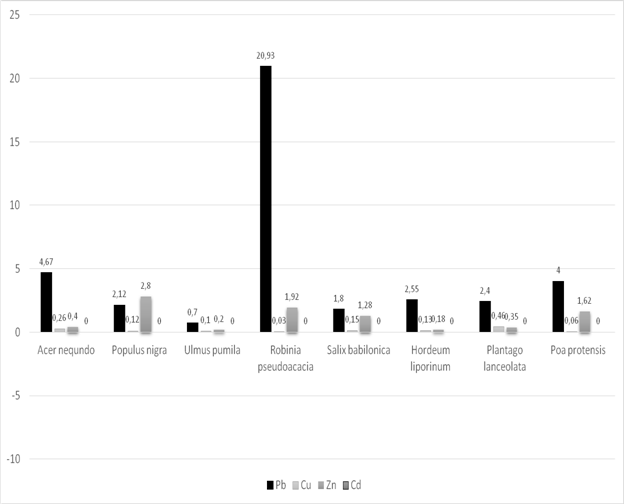
Рис. 3 Содержание тяжелых металлов (Пункт № 4 — контрольный пункт), (мг/кг) ПДК: Свинец–5мг/кг; цинк–30мг/кг; кадмий–0,3мг/кг.
Максимальное содержание цинка в растениях так-же было отмечано в пункте № 1, у мятлика лугового оно составляет 48,57±3,46 мг/кг, что превышает ПДК 1,6 раза, а контрольный показатель в 12 раз. У подорожника ланцетолистного и ячменя заячего содержание цинка не превышает ПДК, но намного выше по сравнению с контрольным пунктом. Содержание кадмия во всех растениях значительно выше ПДК.
Результаты проведенных исследований показали, что с увеличением поступления в почву тяжелых металлов, соответственно повышается уровень поглощения тяжелых металлов растениями.Таким образом, результаты исследований свидетельствуют о загрязнении почв и растений тяжелыми металлами металлургического производства.
1. Окружающая среда и устойчивое развитие в Казахстане. Обзор ПРООН. Алматы, 2004г. 210 с.
2. Гринь А. В., Ли С. К. Поступление тяжелых металлов в растения в зависимости от их содержания по миграции // Тезисы докладов II — Всемирного совещания по миграции загрязненных веществ в почвах и определенных сферах. Ленинград, 1980г. — С. 46–48.
3. Микшевич Н. В., Ковальчук Л. А. Тяжелые металлы в системе “почва — растения — животные” в зоне действия медеплавильного предприятия // Материалы 2 — Всесоюзной Международной Конференции по ТМ в окружающей среде и охраны природы. 1988г. — С. 127–129.
4. Садовников Л. К. Влияние промышленных предприятий на окружающую среду// Тезисы доклодов. Мониторинг содержания ТМ в почвах естественных и техногенных ландшафтов. г. Пущино, 1984г. –С.163
Основные термины (генерируются автоматически): контрольный показатель, окружающая среда, почва, контрольный пункт, металл, пункт, раз, свинцовое производство, содержание свинца, содержание цинка.
Фитотоксичное действие тяжелых металлов при техногенном загрязнении окружающей среды
В работе описаны загрязнение окружающей среды тяжелыми металлами, распространение и аккумуляция металлов в природной среде и их негативные воздействия на растения.
The pollution plumbum producing plant is influence on heavy metals accumulation processing of plants. Theheavymetalswillbechangedofplantsgename.
Основными источниками антропогенного поступления тяжелых металлов в окружающую среду являются металлургические предприятия, тепловые электростанции, карьеры и шахты по добыче полиметаллических руд, транспорт, химические средства защиты сельскохозяйственных культур от болезней и вредителей, сжигание нефти и различных отходов и пр. Наиболее мощные ореолы тяжелых металлов возникают вокруг предприятий черной и особенно цветной металлургии в результате атмосферных выбросов. Действие загрязняющих веществ распространяется на десятки километров от источника поступления элементов в атмосферу. По приведенным ниже данным можно судить о размерах антропогенной деятельности человека: вклад техногенного свинца составляет 94–97 %(остальное природные источники)., кадмия-84–89 %процентов, меди-56–87 %, никеля-66–75 %, ртути -58 % [1,2].
Заметное загрязнение атмосферного воздуха и почвы происходит за счет транспорта, в том числе авиационного. Большинство тяжелых металлов, содержащихся в пылегазовых выбросах промышленных предприятий, как правило, более растворимы, чем природные соединения [3].
Тяжелые металлы - это группа химических элементов с относительной атомной массой более 40. Появление в литературе термина «Тяжелые металлы» было связано с проявлением токсичности некоторых металлов и опасности их для живых организмов. Однако в эту группу вошли и некоторые микроэлементы, жизненная необходимость и широкий спектр биологического действия которых неопровержимо доказаны. Влияние микроэлементов на жизнедеятельность животных и человека активно изучается и в медицинских целях. В настоящее время выявлено, что многие заболевания, синдромы и патологические состояние вызваны дефицитом, избытком и дисбалансом микроэлементов в живом организме и имеют общее название «микроэлементы».
Фитотоксичное действие тяжелых металлов проявляется, как правило, при высоком уровне техногенного загрязнения ими почв и во многом зависит от свойсв и особенностей поведения конкретного металла. Однако в природе ионы металлов редко встречаются изолированно друг от друга. Поэтому разнообразные комбинативные сочетания и концентрации разных металлов в среде приводят к изменениям свойств отдельных элементов в результате их антогонического воздействия на живые организмы [4].
Растительная пища является основным источником поступления ТМ организм человека и животных. По данным с ней поступают 40–80 % тяжелых металлов, и только 20–40 %. — с воздухом и водой. Поэтому от уровня накопления тяжелых металлов в растениях, используемых в пищу, в значительной степени зависит здоровье населения. Химический состав растений, как известно, отражает элементный состав почв. Поэтому избыточное накопление тяжелых металлов растениями обусловлено, прежде всего, их высокими концентрациями в почвах.
Несмотря на существенную изменчивость различных растений к накоплению тяжелых металлов, биоаккумуляция элементов имеет определенную тенденцию, позволяющую упорядочить их в несколько групп: 1) Cd,Cs, Rb — элементы интенсивного поглощения; 2) Zn, Mo, Cu, Pb, Co, As –средней степени поглощения; 3) Mn, Ni, Cr –слабого поглощения; 4) Se, Fe, Ba, Te — элементы труднодоступные растениям.
Другой путь поступления тяжелых металлов в растения — некорневое поглощение из воздушных потоков. Поступление элементов в растения через листья (или фолиярное поглощение) происходит, главным образом, путем неметаболического проникновения через кутикулу. Тяжелые металлы, поглощенные листьями могут переносится в другие органы и ткани и включаться в обмен веществ.
Свинец и кадмий относятся высокотоксичным металлам. В придорожных растениях количество свинца резко повышено, оно в 10–100 раз выше по сравнению с растениями, растущими вдали от дорог. Между содержанием свинца в растениях и расстоянием дерева от дороги существует доказуемая обратная зависимость. Свинец в достаточно высокой концентрации тормозит прорастание семян растений, замедляет рост корней в длину, а также образование корневых волосков. Листья отравленных свинцом растений становятся хлоротичными в межжилковых зонах. Особенно сильно поражаются молодые листья. Высокое содержание свинца в растениях негативно влияет на рост и развитие:
- снижается активность фотосистемы І и ІІ, причем фотосистема-ІІ более чувствительная к действию этого фитотоксиканта.
- оказывает ингибирующее влияние на реакцию Хилла, т. е. на способность изолированных хлоропластов на свету выделять кислород.
- в хлорпластах растений наблюдается подавление образования АТФ;
- вызывает потерю тургора клетками растений;
- прекращается деление клеток корня;
- подавляется образования корнеплодов, урожайность культурных растений;
- снижается количество каротина и аскорбиновой кислоты;
Некоторые травянистые растения, чувствительны по отношению к свинцу: ячмень, овес, пшеница, картофель. Среди дикорастущих следует отметить смолевку, которая от высокого содержания свинца приобретает карликовую форму, листья и стебли становятся темно-красными, а цветки мелкими и невзрачными [5].
Главным загрязнителем окружающей среды кадмием является цветная металлургия и обработка цветных металлов. Кроме того кадмий поступает в атмосферу при сгорании мусора и отходов. Большое количество кадмия обнаруживается в растения, произрастающих поблизости от автодорог. Так, например в хвое ели обыкновенной, растущей поблизости автодорог количество кадмия возрастает в 11–17 раз. Симптомы избыточного поступления в растения кадмия проявляются в постепенном изменении окраски кончиков листьев и черешков до красновато-бурой и пурпурной. При этом листья скручиваются и опадают. Кадмий замедляет темпы роста растений. При внесении его в количестве 20 мг на 1 кг почвы урожай растения снижался на 50 %. По силе своего действия кадмий превосходит многие другие тяжелые металлы. Гибель растений отмечается при концентрации кадмия в почве в количестве 30 мг/кг и выше. Большое количество кадмия поступает в почву при разработке и добыче цинковых руд. На таких почвах нельзя выращивать растения, ибо этот токсикант аккумулируется в тканях растений и может затем поступать в организм человека. Накопления кадмия происходит главным организм человека. Одна из причин торможения роста растений, произрастающих в присутствии кадмия — резкое ослабление интенсивности фотосинтеза. Присутствие в 1 кг листьев 96 мг этого элемента снижает интенсивность фотосинтеза на 50 % [6].
Поступление тяжелых металлов в растения может происходить непосредственно из воздуха с оседающей на листья и хвою пылью и транслокации из почвы: доля тяжелых металлов в составе пыли на поверхности листьев вблизи источника составляет в среднем 30 проц. от общего содержания в них тяжелых металлов. В понижениях и с наветренной стороны это доля может доходить до 60 %. По мере удаления от источника роль атмосферного загрязнения заметно уменьшается.
Главным загрязнителем атмосферы кадмием является цветная металлургия и обработка цветных металлов. Кроме того, кадмий поступает в окружающую среду при сгорании некоторых видов топлива и особенно при сжигании мусора и отходов. Из атмосферы кадмий поступает в почву. Загрязнение ее этим элементом носит устойчивый характер, поскольку из почвы он вымывается медленно. Большое количество кадмия обнаруживается в растения, произрастающих поблизости от автомобильных дорог. Так, например в хвое ели обыкновенной, растущей поблизости от автострад, количество кадмия возрастает в 11–17 раз. Симптомы избыточного поступления в растения кадмия проявляются в постепенном изменении окраски кончиков листьев и черешков до красновато-бурой и пурпурной. При этом листья скручиваются и становятся хлоратичными и опадают. По силе своего действия на растения кадмий превосходит многие другие тяжелые металлы. Гибель растений отмечается при концентрации этого элемента в почве в количестве 30 мг/кг. Вблизи предприятий, выбрасывающих в атмосферу кадмий наблюдается резкое снижение урожайности и даже гибель культурных растений. Накопление кадмия происходит главным образом в корнях растений (риса, пшеницы), однако часть его достигает органов. Одна из причин торможения роста растений, произрастающих в присутствии кадмия, резкое ослабление интенсивности фотосинтеза. Присутствие в 1 кг листьев 96 мг этого элемента снижает интенсивность фотосинтеза на 50 %. Существует прямая зависимость между содержанием кадмия в почве и поступлением его в растения.
Токсическое влияние оказывают на растения и другие металлы, загрязняющие природную среду, например бериллий, марганец, медь, хром, ванадий, цинк и др.
1. Кузнецов А. В. Контроль техногенного загрязнения почв и растений // Агрохимический вестник. –1997г. -№ 5, -С. 7–9
2. Минеев В. Г. Проблема тяжелых металлов в современном земледелии // Тяжелые металлы и радионуклиды. –М., 1994г. –С. 42–48
3. Бутовский Р. О. Тяжелые металлы как техногенные химические загрязнители и их токсичность для почвенных беспозвоночных животных //Агрохимия.-2005 г. -№ 4, -С 73–91.
4. Алексеев Ю. В. Тяжелые металлы в почвах и растениях. –Ленинград, 1987 г. –С. 141–144.
5. Зырин Н. Г. Тяжелые металлы в почвах и растениях в районе медеплавильного завода. –м., 1986г. –С. 81
6. Артомонов В. И. Растения и чистота природной среды. –М., 1986 г. –С. 27–31.
Основные термины (генерируются автоматически): металл, растение, кадмий, окружающая среда, почва, лист, организм человека, цветная металлургия, элемент, главный образ.
Тяжелые металлы и их влияние на растения Текст научной статьи по специальности «Экологические биотехнологии»
Аннотация научной статьи по экологическим биотехнологиям, автор научной работы — Узаков З.З.
Постоянный рост народонаселения и быстрое развитие производства привели в конце XX-го века ситуацию с состоянием окружающей среды во многих странах и регионах мира на грань экологического кризиса. К числу основных факторов деградации природной среды относится ее загрязнение различными поллютантами, среди которых одно из главных мест занимают тяжелые металлы . В силу сказанного становится понятной актуальность исследований, посвященных влиянию тяжелых металлов на растения. В настоящее время они активно ведутся во многих странах мира.
Похожие темы научных работ по экологическим биотехнологиям , автор научной работы — Узаков З.З.
Текст научной работы на тему «Тяжелые металлы и их влияние на растения»
МЕЖДУНАРОДНЫЙ НАУЧНЫЙ ЖУРНАЛ «СИМВОЛ НАУКИ» № 1-2/2018 ISSN 2410-700Х
преподаватель, Каршинский государственный университет,
ТЯЖЕЛЫЕ МЕТАЛЛЫ И ИХ ВЛИЯНИЕ НА РАСТЕНИЯ
Постоянный рост народонаселения и быстрое развитие производства привели в конце XX-го века ситуацию с состоянием окружающей среды во многих странах и регионах мира на грань экологического кризиса. К числу основных факторов деградации природной среды относится ее загрязнение различными поллютантами, среди которых одно из главных мест занимают тяжелые металлы. В силу сказанного становится понятной актуальность исследований, посвященных влиянию тяжелых металлов на растения. В настоящее время они активно ведутся во многих странах мира.
Тяжелые металлы, природная, техногенная, почва, экология, химические элементы, ртуть,
свинец, кадмий, цинк, медь, мышьяк.
Термин «тяжелые металлы» был впервые употреблен еще в 1817 году немецким химиком Леопольдом Гмелиным (Leopold Gmelin), который разделил известные в то время химические элементы на три группы: неметаллы, легкие металлы и тяжелые металлы (Habashi, 2009).
Однако до сих пор не существует единого понимания, что же такое «тяжелые металлы». Более того, в техническом отчете IUPAC (International Union of Pure and Applied Chemistry - Международный союз теоретической и прикладной химии) за 2002 год отмечено, что термин «тяжелый металл» имеет неверное толкование из-за противоречивых определений. На сегодняшний день выделены лишь критерии, по которым определяется принадлежность того или иного химического элемента к данной группе. Среди них: плотность, атомный вес и атомное число. Словосочетание «тяжелые металлы» часто рассматривается с природоохранной точки зрения (Duffus, 2002), и тогда при включении элемента в эту группу учитываются не столько его физические и химические свойства, сколько биологическая активность, токсичность для живых организмов, распространенность в природной среде, степень вовлеченности в природные и техногенные циклы [1, с. 7].
Тяжелые металлы относятся преимущественно к рассеянным химическим элементам, поэтому загрязнению ими подвергается земная поверхность, в частности, почвенный покров и гидросфера, а также атмосфера (Добровольский, 1983, 2004). В силу этого повышение их концентрации в окружающей среде вследствие естественного или антропогенного поступления может носить глобальный характер. К естественным источникам тяжелых металлов относятся горные породы (из продуктов, выветривания которых сформировался почвенный покров), вулканы, космическая пыль, эрозия почв, испарение с поверхности морей и океанов, выделение их растительностью (Кабата-Пендиас, Пендиас, 1989; Добровольский, 1992; Богдановский, 1994) [1, с. 9].
Тяжелые металлы (ртуть, свинец, кадмий, цинк, медь, мышьяк) относятся к числу распространенных и весьма токсичных загрязняющих веществ. Они широко применяются в различных промышленных производствах, поэтому, несмотря на очистные мероприятия, содержание соединения тяжелых металлов в промышленных сточных водах довольно высокое. Прежде всего, представляют интерес те металлы, которые наиболее широко и в значительных объемах используются в производственной деятельности и в результате накопления во внешней среде представляют серьезную опасность с точки зрения их биологической активности и токсических свойств. К таким тяжелым металлам относятся свинец, ртуть,
МЕЖДУНАРОДНЫЙ НАУЧНЫЙ ЖУРНАЛ «СИМВОЛ НАУКИ» № 1-2/2018 ISSN 2410-700Х кадмий, цинк, висмут, кобальт, никель, медь, олово, сурьма, ванадий, марганец, хром, молибден и мышьяк.
Многие тяжелые металлы относятся к микроэлементам. То есть химическим элементам, присутствующим в организмах в низких концентрациях (обычно тысячные доли процента и ниже).
Значительное количество химических элементов, постоянно обнаруживаемых в организмах, оказывает определенное влияние на течение процессов обмена веществ и на ряд физиологических функций. Количественное содержание биоэлементов, входящих в состав организмов, сильно варьирует в зависимости от среды обитания, способа питания, видовой принадлежности и т. п. Помимо общего благоприятного влияния на процессы роста и развития, установлено специфическое воздействие ряда микроэлементов на важнейшие физиологические процессы — например, фотосинтез у растений. [2, с. 13]
При увеличении содержания металлов в почве снижается её общая биологическая активность, и это резко отражается на росте и развитии растений, причём разные растения реагируют на избыток металлов по-разному. Металлы распределяются по органам растений неравномерно. В наибольшей степени металлы накапливаются в листьях. Это обусловлено многими причинами, одна из которых - локальное накопление металлов в результате перехода их в малоподвижную форму. Например, в случае медной интоксикации окраска некоторых листьев у растений изменяется до красной и буро-коричневой, что свидетельствовало о разрушении хлорофилла.
Токсичность тяжелых металлов связана с их физико-химическими свойствами, со способностью к образованию прочных соединений с рядом функциональных группировок на поверхности и внутри клеток. Симптомы "отравления" растений тяжелыми металлами внешне проявляются в замедлении их роста и развития, изменении цвета и увядании листьев, уродливости и недоразвитости корневой системы.
Реакция растений на повышенные концентрации тяжёлых металлов (концентрация в почве, мг/кг):
Pb (100-500). Ингибирование дыхания и подавление процесса фотосинтеза, иногда увеличение содержания кадмия и снижение поступления цинка, кальция, фосфора, серы, снижение урожайности, ухудшение качества растениеводческой продукции. Внешние симптомы - появление темно-зеленых листьев, скручивание старых листьев, чахлая листва.
Cd (1-13). Нарушение активности ферментов, процессов транспирации и фиксации СО2, торможение фотосинтеза, ингибирование биологического восстановления NO2 до NO, затруднение поступления и метаболизма в растениях ряда элементов питания. Внешние симптомы - задержка роста, повреждение корневой системы, хлороз листьев.
Zn (140-250). Хлороз молодых листьев.
Cr (200-500).Ухудшение роста и развития растений, увядание надземной части, повреждение корневой системы, хлороз молодых листьев, резкое снижение содержания в растениях большинства незаменимых макро и микроэлементов (К, Р, Fe, Mn, Cu, B и др.).
Ni (30-100). Подавление процессов фотосинтеза и транспирации. При этом наблюдаются явления эндемического заболевания растений, например уродливые формы. Типичные симптомы повреждающего токсического действия никеля: хлороз, появление желтого окрашивания с последующим некрозом, остановка роста корней и появления молодых побегов или ростков, деформация частей растения, необычная пятнистость, в некоторых случаях — гибель всего растения. [2, с. 33].
Список использованной литературы:
1. Титов А.Ф., Казнина Н.М., Таланова В.В. Тяжелые металлы и растения. Петрозаводск: Карельский научный центр РАН, 2014. 194 с.
2. СЛ. Давыдова, В.И. Тагасов Тяжелые металлы как супертоксиканты XXI века: Учеб. пособие. - М.: Изд-во РУДН, 2002. - 140 с.
Содержание тяжелых металлов в лекарственных растениях

Введение
В современной медицине широко используются синтетические лекарственные средства. Их выпуск год от года возрастает. Но на протяжении всей истории человечества лекарственные растения применяются для лечения различных заболеваний. Используются они и в наши дни. [1, 2]. Опыт практической медицины показал, что можно разумно сочетать современные синтетические препараты и давно известные народные средства на основе лекарственных растений [3]. Во флоре Челябинской области насчитывается около 150 видов лекарственных растений [4].
Бурное развитие промышленности и широкое использование автотранспорта привело к значительному возрастанию уровня тяжелых металлов в окружающей среде. Тяжелые металлы обладают способностью к миграции и накоплению в пищевых цепях. В данном контексте необходимо учитывать содержание тяжелых металлов в лекарственных растениях.
Цель настоящей работы — собрать информацию о лекарственных растениях и определить содержание тяжелых металлов в выбранных растениях.
В рамках поставленной цели были решены следующие задачи: (1) определить значение лекарственных растений в жизни человека; (2) проанализировать многообразие лекарственных растений Челябинской области; (3) осуществить сбор лекарственных растений, подготовить пробы, провести химический анализ на тяжелые металлы.
Объект исследования — лекарственные растения Челябинской области.
Предмет исследования — видовой состав и содержание тяжелых металлов в лекарственных растениях. В работе были использованы такие методы как анализ литературы, полевые исследования, рентгенофлуоресцентный анализ. Гипотеза состояла в следующем: в лекарственных растениях, произрастающих у автомобильных дорог, содержатся больше тяжелых металлов, чем в растущих на экологически чистых территориях.
Экспериментальная часть
Сбор материала проводился на территории Центрального района города Челябинска на газонах вдоль автодорог и в глубине соснового леса (условно-чистая территория). Растения высушивались до воздушно-сухого состояния. Затем сухие образцы измельчали в ступке, а затем прессовали в форме таблетки диаметром ~4 см (Рис. 1). Образцы были проанализированы в лаборатории Центра нанотехнологий Южно-Уральского государственного университета с использованием рентгенофлуориметра Rigaku SuperMini200. При использовании метода РФА с образцом не происходит никаких химических изменений. Использовался полуколичественный метод анализа, содержание металлов представлено в виде массовых процентов оксидов элементов.
Результаты и их обсуждение
Был проведен элементный состав нескольких лекарственных растений — подорожника, клевера и тысячелистника, собранных в черте города Челябинске и в глубине соснового леса (Табл. 1).
Исследования показали, что растения, собранные в городе, содержат большее количество тяжелых металлов (марганца, железа, цинка, меди и хрома). Гипотеза подтвердилась — в лекарственных растениях, произрастающих у автомобильных дорог, содержатся загрязняющие потенциально токсичные металлы. Поэтому в таких местах нельзя заготавливать лекарственные растения.

Рис. 1. Таблетирование образцов
Результаты рентгенофлуоресцентного анализа, % масс.
Читайте также:
