Общая характеристика металлов главной подгруппы iii группы строение их атомов
Обновлено: 04.10.2024
К III группе относятся бор, алюминий, галлий, индий, таллий (главная подгруппа), а также скандий, иттрий, лантан и лантаноиды, актиний и актиноиды (побочная подгруппа).
У элементов подгруппы скандия на внешнем электронном уровне также находится по три электрона. Однако эти элементы относятся к переходным d-элементам, электронная конфигурация их валентного слоя d 1 s 2 . Эти электроны все три элемента довольно легко отдают.
Элементы подгруппы лантаноидов имеют отличительную конфигурацию внешнего электронного уровня, у них застраивается 4f-уровень и исчезает d-уровень. Начиная с церия все элементы, кроме гадолиния и лютеция, имеют электронную конфигурацию внешнего электронного уровня 4f n 6s 2 (гадолиний и лютеций имеют 5d 1 -электроны) Число n изменяется от 2 до 14. Поэтому в образовании валентных связей принимают участие s- и f-электроны. Чаще всего степень окисления лантаноидов +3 реже +4.
Электронное строение валентного слоя актиноидов во многом напоминает электронное строение валентного слоя лантаноидов Все лантанойды и актинойды — типичные металлы.
Все элементы III группы обладают очень сильным сродством к кислороду, и образование их оксидов сопровождается выделением большого количества теплоты. Элементы III группы находят самое разнообразное применение.
Бор был открыт Ж. Гей-Люссаком и Л Тенаром в 1808 г. Содержание его в земной коре составляет 1,2∙10 - 3 %.
Соединения бора с металлами (бориды) обладают высокой твердостью и термостойкостью. Поэтому их используют для получения сверхтвердых и жаропрочных специальных сплавов. Большой термостойкостью обладают карбид и нитрид бора. Последний применяют в качестве высокотемпературной смазки. Кристаллогидрат тетрабората натрия Na2B4O7∙10Н2О (бура) имеет постоянный состав, его растворы применяют в аналитической химии для установления концентрации растворов кислот. Реакция буры с кислотой протекает по уравнению:
Содержание галлия в земной коре составляет 1,9∙10 - 3 %. Он был предсказан Д. И. Менделеевым (экаалюминий) и открыт французским химиком Р. Э. Лекок де Буабодраном в 1875 г. Свойства галлия почти полностью совпали со свойствами экаалюминия, предсказанными Д. И. Менделеевым на основе периодического закона Соединения галлия с элементами VI группы (серой, селеном, теллуром) являются полупроводниками. Жидким галлием наполняют высокотемпературные термометры.
Индий был открыт Т. Рихтером и Ф. Райхом в 1863 г. Содержание ею в земной коре составляет 2,5∙10 - 6 %. Добавка индия к сплавам меди увеличивает устойчивость последних к действию морской воды. Присадка этого металла к серебру увеличивает блеск серебра и препятствует его тускнению на воздухе. Индиевые покрытия предохраняют металлы от коррозии. Он входит в состав некоторых сплавов, применяющихся в стоматологии, а также некоторых легкоплавких сплавов (сплав индия, висмута, свинца, олова и кадмия плавится при 47 °С). Соединения индия с различными неметаллами обладают полупроводниковыми свойствами.
Таллий был открыт У. Круксом в 1861 г. Содержание его в земной коре составляет 10 - 4 % Сплав таллия (10%) с оловом (20%) и свинцом (70%) обладает очень высокой кислотоупорностью, он выдерживает действие смеси серной, соляной и азотной кислот. Таллий повышает чувствительность фотоэлементов к инфракрасному излучению, исходящему от нагретых предметов. Соединения таллия весьма ядовиты и вызывают выпадение волос.
Галлий, индий и таллий относятся к рассеянным элементам Содержание их в рудах, как правило, не превышает тысячных долей процента.
Соединения скандия, иттрия, лантана и лантаноидов были известны еще в начале XIX в. Чистый скандий был выделен Л. Ф. Нильсоном в 1879 г. Содержание этого элемента в земной коре составляет 10 - 3 %. Иттрий был открыт Ю Гадолином в 1794 г. Его содержание в земной коре составляет 2,9∙10 - 3 %. Содержание в земной коре лантана, открытого К. Г. Мосандером в 1839 г., составляет 4,9∙10 - 3 %. Применяются эти металлы в основном для получения специальных сплавов, обладающих специфическими электрическими и магнитными свойствами. Кроме того, лантаноиды используются для приготовления различных пирофорных составов, церий — для получения алюминиевых сплавов. Добавка церия увеличивает электропроводность алюминия и улучшает его механические свойства, облегчает прокатку вольфрама. Диоксид церия применяется при шлифовке оптического стекла.
К семейству актиноидов относятся наиболее тяжелые элементы, следующие в периодической системе за актинием.
Из актиноидов практическое применение находят уран, торий и плутоний.
Уран был открыт М. Г. Клапротом в 1789. Содержание его в земной коре составляет 2,5∙10 - 4 %. В природе уран встречается в виде трех изотопов: 238 92U — 99,285%, 235 92U — 0,71%, 234 92U — 0,005%.
Изотоп 235 92U способен самопроизвольно распадаться. Поэтому уран, используемый в реакторах в качестве ядерного горючего, обогащают с целью увеличения в нем содержания изотопа 235 92U. Для этого изотопа существует понятие критической массы, при достижении которой начинается цепная реакция и происходит ядерный взрыв. Если масса 235 92U меньше критической, скорость реакции самопроизвольного распада можно регулировать. Это свойство 235 92U используется в ядерном реакторе. Соединения урана применяются также в качестве красителей в полиграфической и силикатной промышленности.
Диоксид тория был открыт Й. Я. Берцелиусом в 1828 г., но металлический торий получен сравнительно недавно. Содержание тория в земной коре составляет 1,3∙10 - 3 %. Небольшие добавки итого металла к вольфраму увеличивают срок службы электроспиралей в лампах накаливания (торий поглощает газы, способствующие быстрому износу вольфрамовой нити). Диоксид тория применяется в медицине, а также при изготовлении некоторых катализаторов.
Плутоний был открыт Г. Сиборгом, Э. Макмилланом, Дж. Кеннеди и А. Валем в 1940 г. Содержание его в земной коре ничтожно. Получают плутоний из продуктов распада горючего ядерных реакторов. Используется он для тех же целей, что и уран-235.
Алюминий
Алюминий — элемент IIIА-группы второго периода периодической системы. Электронная конфигурация атома ns 2 p 1 ; алюминий относится к блоку p-элементов. Алюминий имеет в соединениях постоянную степень окисления (+3). Алюминий — серебристо-белый металл, легкий и прочный. Температура плавления 660 °С, температура кипения 2500 °С, плотность 2,7 г/см 3 .
Алюминий впервые получен химическим путем датским химиком Х. К. Эрстедом в 1825 г. В 1854 г французский химик А. Э. Сент-Клер Девиль выделил его электрохимическим методом.
Нахождение в природе. Алюминий является самым распространенным в природе металлом. Содержание его в земной коре составляет 8,05%. Важнейшие природные соединения алюминия — алюмосиликаты, боксит, корунд.
Алюмосиликаты составляют основную массу земной коры. Продукт их выветривания — глина и полевые шпаты (ортоклаз, альбит, анортит). Основу глин составляет каолин Al2O3∙2SiO2∙2Н2О.
Боксит — горная порода, из которой получают алюминий. Состоит главным образом из гидратов оксида алюминия Al2O3∙nН2О.
Физические свойства. Алюминий — серебристо-белый легкий металл, плавящийся при 660 °С. Очень пластичный, легко вытягивается в проволоку и раскатывается в листы из него можно изготовить фольгу толщиной менее 0,01 мм. Алюминий обладает очень большой тепло- и электропроводностью.
Химические свойства. Алюминий — очень активный металл. В ряду напряжений он стоит после щелочных и щелочноземельных металлов. Однако на воздухе он довольно устойчив, так как его поверхность покрывается очень плотной пленкой оксида, предохраняющей металл от контакта с воздухом. Если с алюминиевой проволоки снять защитную оксидную пленку, то алюминий начнет энергично взаимодействовать с кислородом и водяными парами воздуха, превращаясь в рыхлую массу — гидроксид алюминия:
Эта реакция сопровождается выделением теплоты.
Очищенный от защитной оксидной пленки алюминий взаимодействует с водой с выделением водорода:
Алюминий хорошо растворяется в разбавленных серной и соляной кислотах:
2 Al + 6 HCl = 2 AlCl3 + 3 Н2,
Разбавленная азотная кислота на холоду пассивирует алюминий, но при нагревании алюминий растворяется в ней с выделением монооксида азота, гемиоксида азота свободного азота или аммиака, например:
Концентрированная азотная кислота пассивирует алюминий.
Так как оксид и гидроксид алюминия обладают амфотерными свойствами, алюминий легко растворяется в водных растворах всех щелочей, кроме гидроксида аммония:
Порошкообразный алюминий легко взаимодействует со всеми неметаллами. Для начала реакций необходимо нагревание, затем они протекают очень интенсивно и сопровождаются выделением большого количества теплоты:
2 Al + 3 Вr2 = 2 АlВr3 (бромид алюминия),
2 Al + 3 S = Al2S3 (сульфид алюминия),
2 Al + N2 = 2 AlN (нитрид алюминия),
4 Al + 3 С = Al4C3 (карбид алюминия).
Сульфид алюминия может существовать только в твердом виде. В водных растворах он подвергается полному гидролизу с образованием гидроксида алюминия и сероводорода:
Алюминий легко отнимает кислород и галогены у оксидов и солей других металлов. Реакция сопровождается выделением большого количества теплоты:
Процесс восстановления металлов из их оксидов алюминием называется алюмотермией. Алюмотермией пользуются при получении некоторых редких металлов, которые образуют прочную связь с кислородом (ниобий, тантал молибден, вольфрам и др.), а также для сваривания рельсов. Если с помощью специального запала поджечь смесь мелкого порошка алюминия и магнитного железняка Fe3O4 (термит), то реакция протекает самопроизвольно с разогреванием смеси до 3500 °С. Железо при такой температуре находится в расплавленном состоянии.
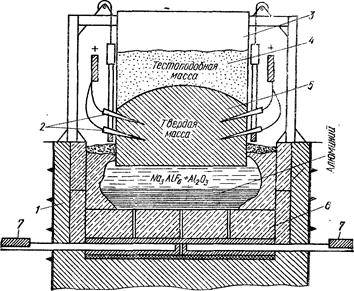
Рис. 9.1. Электролитическая ванна для получения алюминия: 1— огнеупорная футеровка; 2 — токоподводы: 3 — алюминиевый кожух; 4 — электродная масса; 5 — ввод; 6 — графитовый катод; 7 — токоподводящие шины.
Получение. Впервые алюминий был получен восстановлением из хлорида алюминия металлическим натрием:
АlСl3 + 3 Na = 3 NaCl + Al.
В настоящее время его получают электролизом расплавленных солей в электролитических ваннах (рис. 9.1). В качестве электролита служит расплав, содержащий 85-90% криолита — комплексной соли 3NaF∙AlF3 (или Na3AlF6) и 10-15% глинозема — оксида алюминия Аl2О3. Такая смесь плавится при температуре около 1000 °С.
При растворении в расплавленном криолите глинозем ведет себя как соль алюминия и алюминиевой кислоты и диссоциирует на катионы алюминия и анионы кислотного остатка алюминиевой кислоты:
Криолит также диссоциирует:
При пропускании электрического тока на аноде в первую очередь разряжается анион АlO3 3- :
а на катоде выделяется алюминий: Al 3+ + 3e - = Al 0 , полное уравнение процесса:
Расход глинозема все время восполняется. Количество криолита практически не меняется, лишь незначительные его потери происходят вследствие образования на аноде тетрафторида углерода CF4.
Электролитическое производство алюминия требует больших затрат электроэнергии (на получение 1 т алюминия расходуется около 20 000 кВт∙ч электроэнергии), поэтому алюминиевые заводы строят вблизи электростанций.
Применение. Из алюминия изготовляют фольгу, применяемую в радиотехнике и для упаковки пищевых продуктов. Алюминием покрывают стальные и чугунные изделия в целях предохранения их от коррозии: изделия нагревают до 1000 °С в смеси алюминиевого порошка (49%), оксида алюминия (49%) и хлорида алюминия (2%). Этот процесс называется алитированием. Алитированные изделия выдерживают нагревание до 1000 °С, не подвергаясь коррозии. Сплавы алюминия, отличающиеся большой легкостью и прочностью, применяются в производстве теплообменных аппаратов, в самолето- и машиностроении.
Оксид алюминия Аl2O3. Белое вещество с температурой плавления 2050 °С. В природе оксид алюминия встречается в виде корунда и глинозема. Прозрачные кристаллы корунда красивой формы и окраски, окрашенные соединениями хрома в красный цвет, называют рубинами, а окрашенный соединениями титана и железа в синий цвет — сапфирами. Рубины и сапфиры являются драгоценными камнями. В настоящее время их получают искусственно.
Оксид алюминия обладает амфотерными свойствами, но он не растворяется в воде, кислотах и щелочах. При кипячении в концентрированном растворе щелочи он лишь частично переходит в раствор. Оксид алюминия переводят в растворимое состояние сплавлением со щелочами или пиросульфитом калия:
Полученные сплавы растворяются в воде (выщелачивают).
Алюминаты образуются при сплавлении оксида алюминия с оксидами, гидроксидами и карбонатами металлов IA- и IIА-групп, например:
Природный корунд — очень твердое вещество. Он применяется для изготовления наждачных кругов и шлифовальных порошков. Рубин используют для изготовления втулок часовых и других точных механизмов.
Глинозем используется как сырье для получения алюминия. Обезвоженный оксид алюминия служит адсорбентом при очистке и разделении органических веществ методом хроматографии.
Гидроксид алюминия Al(ОН)3 ¾ белое вещество, при нагревании теряющее воду, превращающееся в оксид алюминия. Гидроксид алюминия обладает амфотерными свойствами. Свежеосажденный гидроксид легко растворяется в кислотах и щелочах (кроме гидроксида аммония):
Гидроксид алюминия является слабым основанием и еще более слабой кислотой, поэтому соли алюминия находятся в растворе только в присутствии избытка кислоты, а алюминаты — только в присутствии избытка щелочи. При разбавлении растворов водой эти соединения сильно гидролизуют.
Высушенный гидроксид алюминия, потерявший часть воды, не растворяется ни в кислотах, ни в щелочах и этим напоминает оксид алюминия.
Гидроксид алюминия при нагревании разлагается, образуя сначала метагидроксид, а затем — оксид:
Растворимые соли алюминия гидролизуются по катиону (кислая реакция среды). Сульфид алюминия гидролизуется полностью, карбонат и сульфит не существуют.
Гидроксид алюминия обладает свойством поглощать различные вещества, поэтому его применяют при очистке воды.
Общая характеристика металлов IА–IIIА групп в связи с их положением в Периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов
Атомы элементов IА–IIIА групп имеют сходство в строении электронных оболочек и закономерностях изменения свойств, что приводит к некоторому сходству их химических свойств и свойств их соединений.
Металлы IA (первой группы главной подгруппы) также называются «щелочные металлы«. К ним относятся литий, натрий, калий, рубидий, цезий. Франций – радиоактивный элемент, в природе практически не встречается. У всех металлов IA группы на внешнем энергетическом уровне, на s-подуровне в основном состоянии есть один неспаренный электрон:
… ns 1 — электронное строение внешнего энергетического уровня щелочных металлов
Металлы IA группы — s-элементы. В химических реакциях они отдают один валентный электрон, поэтому для них характерна постоянная степень окисления +1.
Рассмотрим характеристики элементов IA группы:
Все щелочные металлы — сильные восстановители. Это самые активные металлы, которые могут непосредственно взаимодействовать с неметаллами. С ростом порядкового номера и уменьшением энергии ионизации металлические свойства элементов усиливаются. Щелочные металлы образуют с кислородом оксиды Э2О. Оксиды щелочных металлов реагируют с водой с образованием основания (щелочи):
Водородные соединения щелочных металлов — это гидриды с общей формулой ЭН. Степень окисления водорода в гидридах равна -1.
Металлы IIA (второй группы главной подгруппы) — щелочноземельные. Раньше к щелочноземельным металлам относили только кальций, стронций, барий и радий, но по решению ИЮПАК бериллий и магний также называются щелочноземельными.
У щелочноземельных металлов на внешнем энергетическом уровне расположены два электрона. В основном состоянии это два спаренных электрона на s-подуровне:
… ns 2 — электронное строение внешнего энергетического уровня элементов IIA группы
Щелочноземельные металлы — s-элементы. Отдавая два валентных электрона, они проявляют постоянную степень окисления +2. Все элементы подгруппы бериллия — сильные восстановители, но восстановительные свойства выражены слабее, чем у щелочных металлов.
Характеристики элементов IIA группы:
Металлы подгруппы бериллия довольно активны. На воздухе они легко окисляются, образуя основные оксиды с общей формулой ЭО. Этим оксидам соответствуют гидроксиды Э(ОН)2.
Первый элемент IIA группы, бериллий, по большинству свойств гораздо ближе к алюминию (диагональное сходство). Это проявляется в свойствах бериллия. Например, он не взаимодействует с водой. Магний взаимодействует с водой только при нагревании. Кальций, стронций и барий — это типичные металлы. Они реагируют с водой при обычных условиях.
Элементам IIA группы соответствуют гидриды с общей формулой ЭН2.
Элементы IIIA (третьей группы главной подгруппы) — это бор, алюминий, галлий, индий, таллий и нихоний. В основном состоянии содержат на внешнем энергетическом уровне три электрона, которые распределены по s- и р-подуровням:
… ns 2 nр 1 — электронное строение внешнего энергетического уровня элементов IIIA группы
Все элементы подгруппы бора относятся к р-элементам. В химических соединениях проявляются степень окисления +3. Хотя для таллия более устойчивая степень окисления +1.
Металлические свойства у элементов подгруппы бора выражены слабее, чем у элементов IIA подгруппы. Элмент бор относится к неметаллам. Энергия ионизации атома у бора наибольшая среди элментов IIIA подгруппы. Алюминий относится к типичным металлам, но оксид и гидроксид алюминия проявляют амфотерные свойства. У таллия более сильно выражены металлические свойства, в степени окисления +1 он близок по свойствам к щелочным металлам. Наибольшее практическое значение среди элементов IIIA подгруппы имеет алюминий.
Общая характеристика подгруппы
С ростом заряда ядра многие важнейшие характеристики элементов изменяются немонотонно, в том числе и атомный радиус. Соответственно, свойства простых веществ, оксидов, гидроксидов и других соединений этих элементов имеют неоднозначный характер изменения. Особенно резко выделяется первый элемент подгруппы - бор, являющийся единственным неметаллом среди s 2 p 1 -элементов. Бор проявляет диагональное сходство с элементом главной подгруппы IV группы - кремнием Si.
Алюминий - важнейший элемент подгруппы, также имеет целый ряд специфических особенностей, отличающих его от бора, с одной стороны, и от подгруппы галлия, с другой стороны.
Характеристические соединения
Отношение к воде
слабая кислота 1-основная
амфотерный (идеальный амфолит)
основный со слабыми признаками амфотерности
амфотерный (основные свойства преобладают)
основание (подобен щелочам)
Алюминий
13Аl [Ne] 3s 2 3p 1
1 стабильный изотоп 27 Al
Кларк в земной коре 8,8 % по массе, самый распространенный металл. В свободном виде не встречается.
Основная форма нахождения в природе - Аl2O3 (в составе различных силикатов, полевых шпатов и глин). Встречается также в виде двойных солей: KAl(SO4)2, Na3[AlF6] и др.

Физические свойства
Простое вещество алюминий - лёгкий, парамагнитный металл серебристо-белого цвета, легко поддающийся формовке, литью, механической обработке. Алюминий обладает высокой тепло- и электропроводностью, стойкостью к коррозии за счёт быстрого образования прочных оксидных плёнок, защищающих поверхность от дальнейшего взаимодействия. Алюминий обладает высокой электропроводностью и теплопроводностью, обладает высокой светоотражательной способностью. По электропроводности занимает 4-е место после Сu, Аg, Аu.
Способы получения
1. Электролиз расплава AlCl3:
2. Основной промышленный способ - электролиз расплава Al2O3 (глинозема) в криолите 3NaF • AlF3:
AlCl3 + ЗК = Al + 3KCl
Химические свойства
Аl - очень химически активный металл, однако при обычных условиях ведет себя довольно инертно - имеет высокую температуру воспламенения, со многими веществами реагирует только при высокой температуре; все реакции с участием Al проходят через первоначальный замедленный период. Такое химическое поведение алюминия объясняется наличием на его поверхности очень тонкой, прочной, газо- и водонепроницаемой пленки Al2O3. При нарушении цельности этой пленки AI реагирует со многими веществами как активный восстановитель:
Al 0 - Зе - → Аl 3+
В подавляющем большинстве соединений атомы алюминия связаны с соседними атомами ионными связями.
1. Взаимодействие с кислородом и другими неметаллами (галогенами, серой, азотом, углеродом).
Наиболее активно реагирует порошкообразный Al (алюминиевая пудра).
При обычной температуре реакция протекает только на поверхности. После нагревания до температуры воспламенения измельченный Аl сгорает с высоким экзотермичным эффектом.
б) 2Al + 3Cl2 = 2АlСl3 хлорид
Реакция с I2 протекает в присутствии воды. С F2 реакции нет. т. к. в первый же момент образуется прочный поверхностный слой AlF3.
2Al + N2 = 2AlN нитрид
4Al + ЗС = АlС3 карбид
г) C Н2 алюминий непосредственно не соединяется.
2. Взаимодействие с водой в присутствии щелочи.
1) растворение оксидной пленки Al2O3;
2) предотвращение образования нерастворимого гидроксида Аl(ОН)3.
Na[Al(OH)4] - тетрагидроксо-алюминат натрия
В отсутствие щелочи алюминий может вытеснять Н2 из воды в следующих условиях:
1) если его поверхность амальгамировать (покрыть ртутью);
2) в вакууме или в среде инертного газа после предварительной очистки поверхности металла от оксидной пленки.
3. Взаимодействие с «неокисляющими» кислотами (HCl, H2SO4 разб. и др.)
2Al + 6Н + → 2Al 3+ + 3H2↑
4. Взаимодействие с очень концентрированными HNO3 и H2SO4
При обычной Т реакции не протекают, т. к. происходит пассивирование поверхности Al, связанное с внедрением в нее атомарного или молекулярного кислорода, а также образованием его нерастворимых соединений с Al.
При нагревании реакции протекают довольно активно:
5. Взаимодействие с разбавленной HNO3
Реакция медленно протекает при обычной Т, при нагревании - более быстро.
6. Взаимодействие с органическими кислотами
Реакции протекают с разбавленными уксусной и лимонной кислотами при нагревании, ускоряются в присутствии NaCl:
Периодический закон
Периодический закон — это фундаментальный закон, который был сформулирован Д.И. Менделеевым в 1869 году.
В формулировке Дмитрия Ивановича Менделеева периодическ ий закон звучал так: « Свойства элементов, формы и свойства образуемых ими соединений находятся в периодической зависимости от величины их атомной массы .» Периодическое изменение свойств элементов Менделеев связывал с атомной массой. Понимание периодичности изменения многих свойств позволило Дмитрию Ивановичу определить и описать свойства веществ, образованных еще не открытыми химическими элементами, предсказать природные рудные источники и даже места их залегания.

Более поздние исследования показали, что свойства атомов и их соединений зависят в первую очередь от электронного строения атома. А электронное строение определяется свойствами атомного ядра. В частности, зарядом ядра атома .
Поэтому современная формулировка периодического закона звучит так:
« Свойства элементов, форма и свойства образованных ими соединений находятся в периодической зависимости от величины заряда ядер их атомов «.
Следствие периодического закона – изменение свойств элементов в определенных совокупностях, а также повторение свойств по периодам, т.е. через определенное число элементов. Такие совокупности Менделеев назвал периодами.
Периоды – это горизонтальные ряды элементов с одинаковым количеством заполняемых электронных уровней. Номер периода обозначает число энергетических уровней в атоме элемента. Все периоды (кроме первого) начинаются щелочным металлом ( s -элементом), а заканчиваются благородным газом.
Группы – вертикальные столбцы элементов с одинаковым числом валентных электронов, равным номеру группы. Различают главные и побочные подгруппы. Главные подгруппы состоят из элементов малых и больших периодов, валентные электроны которых расположены на внешних ns— и np— подуровнях.
1. Периодическая система химических элементов Д.И. Менделеева
Периодическая система элементов Д. И. Менделеева состоит из семи периодов, которые представляют собой горизонтальные последовательности элементов, расположенные по возрастанию заряда их атомного ядра.
Каждый период (за исключением первого) начинается атомами щелочных металлов (Li, Na, К, Rb, Cs, Fr) и заканчивается благородными газами (Ne, Ar, Kr, Xe, Rn), которым предшествуют типичные неметаллы.
В периодах слева направо возрастает число электронов на внешнем уровне.
В периодах слева направо постепенно ослабевают металлические и усиливаются неметаллические свойства.
1) Li 2) Ca 3) Cs 4) N 5) S
Ответ: 154
1) Be 2) Ba 3) Mg 4) N 5) F
Ответ: 541
В первом периоде имеются два элемента – водород и гелий. При этом водород условно размещают в IA или VIIA подгруппе, так как он проявляет сходство и со щелочными металлами, и с галогенами. Как и щелочные металлы, водород является восстановителем. Отдавая один электрон, водород образует однозарядный катион H + . Как и галогены, водород – неметалл, образует двухатомную молекулу H2 и может проявлять окислительные свойства при взаимодействии с активными металлами:
2Na + H2 → 2NaH
В четвертом периоде вслед за Са расположены 10 переходных элементов (от скандия Sc до цинка Zn), за которыми находятся остальные 6 основных элементов периода ( от галлия Ga до криптона Кr). Аналогично построен пятый период. Переходными элементами обычно называют любые элементы с валентными d– или f–электронами.
Шестой и седьмой периоды имеют двойные вставки элементов. За элементом Ва расположены десять d–элементов (от лантана La — до ртути Hg), а после первого переходного элемента лантана La следуют 14 f–элементов — лантаноидов (Се — Lu). После ртути Hg располагаются остальные 6 основных р-элементов шестого периода (Тl — Rn).
В седьмом (незавершенном) периоде за Ас следуют 14 f–элементов- актиноидов (Th — Lr). В последнее время La и Ас стали причислять соответственно к лантаноидам и актиноидам. Лантаноиды и актиноиды помещены отдельно внизу таблицы.
В Периодической системе каждый элемент расположен в строго определенном месте, которое соответствует его порядковому номеру .
Элементы в Периодической системе разделены на восемь групп (I – VIII), которые в свою очередь делятся на подгруппы — главные , или подгруппы А и побочные , или подгруппы Б. Подгруппа VIIIБ-особая, она содержит триады элементов, составляющих семейства железа (Fе, Со, Ni) и платиновых металлов (Ru, Rh, Pd, Os, Ir, Pt).
Внутри каждой подгруппы элементы проявляют похожие свойства и схожи по химическому строению. А именно:
В главных подгруппах сверху вниз усиливаются металлические свойства и ослабевают неметаллические.
В зависимости от того, какая энергетическая орбиталь заполняется в атоме последней, химические элементы можно разделить на s-элементы, р-элементы, d- и f-элементы.
У атомов s-элементов заполняются s-орбитали на внешних энергетических уровнях. К s-элементам относятся водород и гелий, а также все элементы I и II групп главных подгрупп (литий, бериллий, натрий и др.). У p-элементов электронами заполняются p-орбитали. К ним относятся элементы III-VIII групп, главных подгрупп. У d-элементов заполняются, соответственно, d-орбитали. К ним относятся элементы побочных подгрупп.
Номер периода соответствует числу заполняемых энергетических уровней.
Номер группы, как правило, соответствует числу валентных электронов в атоме (т.е. электроном, способных к образованию химической связи).
Номер группы, как правило, соответствует высшей положительной степени окисления атома. Но есть исключения!
О каких же еще свойствах говорится в Периодическом законе?
Периодически зависят от заряда ядра такие характеристики атомов, как орбитальный радиус, энергия сродства к электрону, электроотрицательность, энергия ионизации, степень окисления и др.
2. Радиус атома
Рассмотрим, как меняется атомный радиус . Вообще, атомный радиус – понятие довольно сложное и неоднозначное. Различают радиусы атомов металлов и ковалентные радиусы неметаллов.
Радиус атома металла равен половине расстояния между центрами двух соседних атомов в металлической кристаллической решетке. Атомный радиус зависит от типа кристаллической решетки вещества, фазового состояния и многих других свойств.
Мы говорим про орбитальный радиус изолированного атома .
Орбитальный радиус – это теоретически рассчитанное расстояние от ядра до максимального скопления наружных электронов.
Орбитальный радиус завит в первую очередь от числа энергетических уровней, заполненных электронами.
Чем больше число энергетических уровней, заполненных электронами, тем больше радиус частицы.
Например , в ряду атомов: F – Cl – Br – I количество заполненных энергетических уровней увеличивается, следовательно, орбитальный радиус также увеличивается.

Если количество заполняемых энергетических уровней одинаковое, то радиус определяется зарядом ядра частицы.
Чем больше заряд ядра, тем сильнее притяжение валентных электронов к ядру.
Чем больше притяжение валентных электронов к ядру, тем меньше радиус частицы. Следовательно:
Чем больше заряд ядра атома (при одинаковом количестве заполняемых энергетических уровней), тем меньше атомный радиус.
Например , в ряду Li – Be – B – C количество заполненных энергетических уровней, заряд ядра увеличивается, следовательно, орбитальный радиус также уменьшается.

В группах сверху вниз увеличивается число энергетических уровней у атомов. Чем больше количество энергетических уровней у атома, тем дальше расположены электроны внешнего энергетического уровня от ядра и тем больше орбитальный радиус атома.
В главных подгруппах сверху вниз увеличивается орбитальный радиус.
В периодах же число энергетических уровней не изменяется. Зато в периодах слева направо увеличивается заряд ядра атомов. Следовательно, в периодах слева направо уменьшается орбитальный радиус атомов.
В периодах слева направо орбитальный радиус атомов уменьшается.

1) O 2) Se 3) F 4) S 5) Na
Решение:
В одной группе Периодической системы находятся элементы кислород O, селен Se и сера S.
В группе снизу вверх атомный радиус уменьшается, а сверху вниз – увеличивается. Следовательно, правильный ответ: O, S, Se или 142.
Ответ: 142
1) K 2) Li 3) F 4) B 5) Na
Решение:
В одном периоде Периодической системы находятся элементы литий Li, фтор F и натрий Na.
В периоде слева направо атомный радиус уменьшается, а справа налево – увеличивается. Следовательно, правильный ответ: Li, B, F или 243.
Ответ: 243
1) Ca 2) P 3) N 4) О 5) Ti
p-элементы это фосфор Р, азот N, кислород О.
В периоде слева направо атомный радиус уменьшается, а справа налево – увеличивается. В группе — сверху вниз увеличивается. Следовательно, правильный ответ: P, N, O или 234.
Ответ: 234
Рассмотрим закономерности изменения радиусов ионов : катионов и анионов.
Катионы – это положительно заряженные ионы. Катионы образуются, если атом отдает электроны.
Радиус катиона меньше радиуса соответствующего атома. С увеличением положительного заряда иона радиус уменьшается.
Например , радиус иона Na + меньше радиуса атома натрия Na:

Анионы – это отрицательно заряженные ионы. Анионы образуются, если атом принимает электроны.
Радиус аниона больше радиуса соответствующего атома.
Радиусы ионов также зависят от числа заполненных энергетических уровней в ионе и от заряда ядра.
Например , радиус иона Cl – больше радиуса атома хлора Cl.
Изоэлектронные ионы – это ионы с одинаковым числом электронов. Для изоэлектронных частиц радиус также определяется зарядом ядра: чем больше заряд ядра иона, тем меньше радиус.
Например : частицы Na + и F ‒ содержат по 10 электронов. Но заряд ядра натрия +11, а у фтора только +9. Следовательно, радиус иона Na + меньше радиуса иона F ‒ .
3. Электроотрицательность
Еще одно очень важное свойство атомов – электроотрицательность (ЭО).
Электроотрицательность – это способность атома смещать к себе электроны других атомов при образовании связи. Оценить электроотрицательность можно только примерно. В настоящее время существует несколько систем оценки относительной электроотрицательности атомов. Одна из наиболее распространенных – шкала Полинга.

По Полингу наиболее электроотрицательный атом – фтор (значение ЭО≈4). Наименее элекроотрицательный атом –франций (ЭО = 0,7).
В главных подгруппах сверху вниз уменьшается электроотрицательность.
В периодах слева направо электроотрицательность увеличивается.
1) Mg 2) P 3) O 4) N 5) Ti
Элементы-неметаллы – это фосфор Р, кислород О и азот N.
Электроотрицательность увеличивается в группах снизу вверх и слева направо в периодах. Следовательно, правильный ответ: P, N, O или 243.
Положение в ПСХЭ. Электронное строение атомов
Находясь только в больших периодах (IV, V, VI), d-элементы образуют «вставные декады» (по 10 элементов) между s- и р- элементами, поэтому имеют общее название - переходные элементы.
Кроме этих 30 d-элементов, имеющих стабильные изотопы, искусственно синтезированы несколько радиоактивных d- элементов, занимающих свои места внезавершенном VII периоде.
В атомах d-элементов содержится от 1 до 10 электронов на d-подуровне предвнешнего электронного слоя и 2 (или 1 в случае проскока е-) электрона на s-подуровне внешнего электронного слоя. Общая формула электронной конфигурации валентных подуровней в атомах d -элементов.

Сравнение d -металлов с щел. Me и щел.-зем. Me
В каждом большом периоде d-элементы располагаются после двух s-элементов, которые являются щелочным и щелочноземельным металлами:
Радиусы атомов уменьшаются
Заряды ядер атомов увеличиваются
Поэтому d-металлы являются менее активными, чем щелочные и щелочноземельные металлы.
Возможные валентности и степени окисления
Вотличие от щелочных и щелочноземельных Me, большинство d-металлов имеют переменную валентность и переменную степень окисления. Это объясняется тем, что валентными в атомах d-элементовявляются не только s-электроны внешнего слоя, но и все или некоторые d -электроны предвнешнего слоя.
Положение в ПСЭ. Электронное строение атомов
Для d-металлов III - VII групп высшая Ви высшая С.О. равны номеру группы, т. е. суммарному числу е - на (n -1)d и ns-подуровнях; например у d -элементов четвертого периода:
Высшая степень окисления
Для d-металлов VIII группы высшая В и высшая с о., как правило, меньше суммарного числа е - на (n - 1)d и ns -подуровнях;
d-Металлы II группы, атомы которых имеют завершенную структуру d-подуровня (n -1)d10, проявляют в своих соединениях постоянную В = II и постоянную с.о. = +2.
Наиболее характерными валентностями и степенями окисления для d-металлов I группы являются: Сu - II и +2; Ag - I и +1; Au - III и +3.
Способность к комплексообразованию
Важной особенностью атомов d-металлов является наличие свободных орбиталей (на (n - 1)d -, ns - образованию и nр-подуровнях), что позволяет им образовывать донорно-акцепторные (координационные) связи с различными донорами неподеленных электронных пар (молекулы NH3, Н2O, ионы ОН - , CN - и др.).
Вследствие этого d-металлы образуют многочисленные и разнообразные комплексные соединения; например:
В свободном состоянии d -металлы (как и вообще все металлы) являются восстановителями. Восстановительная активность различных d - металлов изменяется в широких пределах: среди них есть металлы средней активности, находящиеся в ряду напряжений до водорода (Fe, Cr , Zn , Mn и др.); малоактивные металлы (Сu, Нg и др.) и благородные металлы (Au , Pt и др.), располагающиеся в ряду напряжений после водорода.
Окислительно-восстановительные свойства d-металлов и их соединений
Соединения d-элементов могут выполнять как восстановительные, так и окислительные функции. Соединения с невысокими степенями окисления являются восстановителями, а соединения с высокими степенями окисления - окислителями;
Кислотно-основные свойства оксидов и гидроксидов d-металлов
При увеличении степени окисления металла основной характер оксидов и гидроксидов ослабляется, а кислотный характер усиливается:
Читайте также:
