Оксиды покрывают поверхность металла
Обновлено: 21.09.2024
Варианты ответа:а)ниже температуры воспламенения его в кислороде.
б) выше температуры кипения его в кислороде.
в) выше температуры воспламенения его в кислороде.
Задание№3
Увеличение содержания углерода в стали сопровождается:
Варианты ответа:а) углерод не влияет на резку стали;
б) понижение температуры плавления и повышением температуры воспламенения в кислороде;
в) повышение температуры плавления и понижение температуры
воспламенения в кислороде.
Задание№4
Температура плавления оксидов должна быть:
Варианты ответа:а) ниже температуры плавления самого металла;
б) выше температуры плавления самого металла;
в) оксиды расплавляются при любых условиях
Задание№5
При резке хромистых сталей образуются оксиды хрома с температурой плавления:
Варианты ответа:а) 2000 °С;
Задание№6
При резке алюминия образуются оксиды с температурой плавления около:
Варианты ответа:а)1500°С;
б) 2000 °С;
в) 2050 °С
Задание№7
Оксиды покрывают поверхность металла:
Варианты ответа:а)не влияют на процесс резки
б) прекращают дальнейший процесс резки;
в) улучшают процесс резки
Задание№8
Разделительную резку применяют:
Варианты ответа:а) прирезке металла;
б) связанных с разрезкой металла на части ;
в) для вырезки различного вида заготовок, раскроя листового металла, разделки кромок под сварку и других работ
Задание№9
Сущность процесса резки заключается:
Варианты ответа: а)металл вдоль линии разреза нагревают до температуры кипения его в кислороде, он сгорает в струе кислорода;
б) металл вдоль линии разреза нагревают и образующиеся оксиды выдуваются этой струёй из места разреза;
в) металл вдоль линии разреза нагревают до температуры воспламенения его в кислороде, он сгорает в струе кислорода, а образующиеся оксиды выдуваются этой струёй из места разреза.
Задание№10
Поверхностную резку применяют для:
Варианты ответа:а) снятия поверхностного слоя металла;
б) фигурной резке;
в) раскроя листового металла
Задание№11
При строжке резак совершает возвратно-поступательное движение:
Варианты ответа:а) без наклона
б) как строгальный резец;
Задание№12
Резаки при кислородной резке служат:
Варианты ответа:а) для правильного смешения горючих газов или паров жидкости с кислородом, образования подогревающего пламени и подачи в зону резки струи чистого кислорода;
б) для подачи горючих газов;
в) образованию подогревающего пламени и подачи газов
Задание№13
Резаки классифицируют по назначению:
Варианты ответа:а) универсальные и специальные;
б) простые;
в) сложные
Задание№14
Подогревающее пламя играет большую роль:
Варианты ответа:а) чем меньше толщина метала;
б) чем больше толщина металла;
в) не зависит от толщины металла
Задание№15
Резаки отличаются:
Варианты ответа:а)по назначению;
б) большими размерами сечений инжекторов и мундштуков;
в) по наконечнику
Задание№16
Для машинной резки применяют стационарные:
Варианты ответа:а)резаки типа РЗР;
б) шарнирные машины АСШ-2 и АСШ-70;
в) машина «Микрон-2
Задание№17
Усовершенствованные машины типа АСШ-74 производят резку листовой стали:
Варианты ответа:а) толщиной до 150 мм со скоростью 0,1. 1,6 м/мин;
б) толщиной до 50 мм со скоростью 0,1. 1,6 м/мин;
в) толщиной до 100 мм со скоростью 0,1. 1,6 м/мин.
Задание№18
Машина типа АСШ-70 с наличием пантографического устройства, позволяющего производить вырезку одновременно:
Варианты ответа:а) трех деталей;
б) двух деталей;
в) пяти деталей
Задание№19
При резке листового материала толщиной до 20. 30 мм мундштук резака устанавливают под углом:
Варианты ответа:а) 0. 25° к поверхности;
б) 0. 5° к поверхности, а затем под углом 20. 30° в сторону, обратную движению резака;
в) 0. 15° к поверхности, а затем под углом 20. 40° в сторону, обратную движению резака.
Задание№20
Резку металла большой толщины выполняют следующим образом, мундштук резака вначале устанавливают:
Варианты ответа:а) перпендикулярно поверхности разрезаемого металла, а затем и режущий кислород располагался вдоль вертикальной грани разрезаемого металла;
б) горизонтально поверхности разрезаемого металла, а затем и режущий кислород располагался вдоль вертикальной грани разрезаемого металла;
в) вертикально вдоль вертикальной грани разрезаемого металла
Задание№21
Предварительный подогрев металла производится:
Варианты ответа: а)до 400. 500 °С что позволяет производить резку с повышенной скоростью.
б) до 300. 400 °С что позволяет производить резку с повышенной скоростью.
Задание№22
Давление режущего кислорода устанавливают в зависимости:
Варианты ответа: а) толщины разрезаемого металла и чистоты кислорода;
б) от остатка газа в баллоне;
в) конфигурации заготовки
Задание№23
Ширина и чистота разреза зависят:
Варианты ответа:а)от способа резки и толщины разрезаемого металла;
б) от толщины металла;
в) от толщины металла и давления кислорода
Задание№24
Кислородно-флюсовая резка, сущность которой заключается в следующем:
Варианты ответа:а) нагревается металл до температуры300° и подается флюс в зону резания;
б) при нагревании металла подается флюс и открывается режущий;
в) в зону резания с помощью специальной аппаратуры непрерывно подается порошкообразный флюс, при сгорании которого выделяется дополнительная теплота, и повышается температура места разреза
Задание№25
Расстояние от торца мундштука резака до поверхности разрезаемого металла устанавливается в пределах:
Варианты ответа:а) 10. 15 мм;
б) 15. 20 мм;
в) 20. 30 мм
Задание№26
Механические свойства низкоуглеродистой стали при резке:
Варианты ответа:а) почти не изменяются;
б) изменяются;
в изменяется химический состав стали
Задание№27
Применяют кислородно-флюсовую резку для резки:
Варианты ответа:а) цветных металлов;
б) черных металлов
в) чугуна
Задание№28
Мощность пламени при флюсовой резки берется
Варианты ответа:а) на 10. 15% выше, чем при обычной газовой резке.
б) на 15. 25% выше, чем при обычной газовой резке.
в) не изменяется
Задание№29
Чугун толщиной 50 мм режут:
Варианты ответа:а) со скоростью 70. 100 мм/мин;
б) со скоростью 30. 50 мм/мин;
в) со скоростью 50. 60 мм/мин;
Задание№30
На 1 м разреза расходуется:
Варианты ответа:а) 1. 3 м 3 кислорода, 0,16. 0,30 м ацетилена и 3,5. 6 кг флюса;
б) 2,5. 4,5 м 3 кислорода, 0,20. 0,30 м ацетилена и 3,5. 6 кг флюса;
в) 2. 4 м 3 кислорода, 0,16. 0,25 м ацетилена и 3,5. 6 кг флюса
Тест МДК 02.02 для профессии «Электрогазосварщик»
Раздел «Резка металла»
Вариант №2
Уровень усвоения: 2
Инструкция: из предложенных вариантов выберите один правильный и запишите его букву.
Задание№1
Под газопламенной резкой (чаще ее называют кислородной) понимают способ:
Варианты ответа: а) строжкой;
б) разделения металла по прямому или криволинейному контуру;
Задание№2
Процесс сгорания разрезаемого металла распространяется:
Варианты ответа:а) на всю толщину, образующиеся окислы выдуваются из места реза струей режущего кислорода;
б) не на всю толщину, образующиеся окислы выдуваются из места реза струей режущего кислорода;
в) только на поверхность металла
Задание№3
Среднеуглеродистые и высокоуглеродистые стали режутся:
Варианты ответа:а) хорошо;
б) плохо;
в) удолетворительно
Задание№4
Легирующие примеси в сочетании с углеродом:
Варианты ответа: а)одинаково влияют на способность стали поддаваться кислородной резке.
б) удовлетворительно влияют на способность стали поддаваться кислородной резке.
в) неодинаково влияют на способность стали поддаваться кислородной резке.
Задание№5
Для кислородной резки пригодны горючие газы и пары горючих жидкостей, дающие температуру пламени при сгорании в смеси с кислородом:
Варианты ответа: а) не менее 1800°С
б) более 2000°С
в) не менее 1200°С
Задание№6
С понижением чистоты кислорода:
Варианты ответа: а) повышается производительность резки и увеличивается расход кислорода;
б) снижается производительность резки и увеличивается расход кислорода;
в) не изменяется расход кислорода
Задание№7
Для кислородной резки с применением ацетилена используют оборудование для ацетиленовой сварки:
Варианты ответа:а) применяют газовый резак обычно безинжекторного типа
б) применяют газовый резак обычно инжекторного типа
в) копьевой ствол
Задание№8
Рабочий конец кислородного копья предварительно нагревается до температуры
Варианты ответа:а)1350–1400°С без постороннего источника нагрева;
б) 1300–1350°С с помощью постороннего источника нагрева;
в)1350–1400°С с помощью постороннего источника нагрева
Задание№9
При прожигании отверстия торец копья необходимо:
Варианты ответа:а) постоянно прижимать к материалу, отрывая его лишь на короткое время при возвратно-поступательном движении;
б) держать от края металла 15мм;
в) не постоянно прижимать к материалу
Задание№10
Диаметр отверстия от прожигании отверстия копья составляет:
Варианты ответа:а) 50–100 мм и не зависит от диаметра кислородного копья;
б) 10–50 мм и зависит от диаметра кислородного копья
в) 30–90 мм и зависит от диаметра кислородного копья
Задание№11
Скорость прожигания отверстия диаметром 50–60 мм составляет не более:
Варианты ответа: а)30 мм/мин при расходе кислорода около 25 м3 на 1м отверстия и 20 м трубок;
б) 50 мм/мин при расходе кислорода около 35 м3 на 1м отверстия и 25 м трубок;
в) 100 мм/мин при расходе кислорода около 35 м3 на 1м отверстия и 25 м трубок.
Задание№12
Воздушно-дуговая резка заключается в расплавлении металла по линии реза:
Варианты ответа:а) электрической дугой и принудительном удалении сжатым воздухом образующегося под действием дуги расплава;
б) электрической дугой и кислородом;
в) электрической дугой и пропаном
Задание№13
Наилучшая производительность воздушно-дуговой резки достигается при диаметре электрода:
Варианты ответа:а) 6–12 мм;
Задание№14
Целесообразно использовать электроды при воздушно-дуговой резки:
Варианты ответа:а) покрытые защитно-разгружающим слоем из меди или композиции на основе алюминия;
б) с целлюлозным покрытием;
в) с мешанным покрытием
Задание№15
Плазменная резка заключается:
Варианты ответа:а) в проплавлении разрезаемого металла за счет теплоты, генерируемой сжатой плазменной дугой, и интенсивном удалении расплава плазменной струей.
б) в окисления разрезаемого металла за счет теплоты, генерируемой сжатой плазменной дугой, и интенсивном удалении расплава плазменной струей.
в) в проплавлении разрезаемого металла за счет кислорода, генерируемой сжатой плазменной дугой, и интенсивном удалении расплава плазменной струей.
Задание№16
Резка плазменной струей используется:
Варианты ответа:а) для обработки неметаллических материалов, поскольку они не обязательно должны быть электропроводными;
б) для черных сплавов;
в) для цветных металлов
Задание№17
Температура в плазменной дуге может достигать
Варианты ответа:а) 5000–10000°С;
б) 25000–30000°С;
в) 8000-25000°С
Задание№18
Электроды для плазменной резки изготавливают:
Варианты ответа:а) металлические;
б) угольные;
в) из меди, гафния, вольфрама (активированного иттрием, лантаном или торием) и других материалов
Задание№19
Расход плазмообразующего газа может достигать:
Варианты ответа:а)около 200 м/с при силе тока 250А.
б) около 800 м/с при силе тока 250А;
в) около 500 м/с при силе тока 250А.
Задание№20
Специальные резаки марок РПА-2-72, РПК-2-72, РЗР-2, РК-02 могут разрезать металл толщиной:
Варианты ответа:а) от 200 до 800 мм.
б) от 50-100мм
в) 300-500мм
Задание№21
Резак РК-02, или керосинорез:
Варианты ответа:а) имеет обогреваемый подогревающим пламенем испаритель;
б) рычагом пуска режущего кислорода и дополнительным вентилем;
в) рычагом пуска режущего кислорода и несколькими вентилями
Задание№22
Установка УФР-5 предназначена для порошково-кислородной резки железобетона толщиной до 300 мм:
Варианты ответа:а) работает на ацетилене в смеси с кислородом;
б) работает на пропане или бутане в смеси с кислородом;
в) работает на карбиде в смеси с кислородом
Задание№23
Глубина отверстия, прожигаемого в железобетоне УФР-5, может составить:
Варианты ответа:а)500мм
б) 700мм
в) 1,500мм.
Задание№24
Шарнирные установки АСШ («Огонек») и АСШ-В для кислородной резки имеют пантограф, позволяющий производить фигурную вырезку:
Варианты ответа:а) пяти деталей небольших размеров при толщине материала от 5 до 100 мм при скорости резания до 1600 мм/мин.
б) одной детали при толщине материала от 5 до 100 мм при скорости резания до 1600 мм/мин.
в) трех деталей небольших размеров при толщине материала от 5 до 100 мм при скорости резания до 1600 мм/мин
Задание№25
Если толщина металла не достигает 300 мм:
Варианты ответа: а) окислительного пламени;
б) то достаточно нормального пламени;
в) науглероживающегося пламени
Задание№26
Если скорость движения резака правильная:
Варианты ответа:а) поток искр и шлака вырывается из разреза прямо вниз, а кромки получаются чистыми, без натеков и подплавлений;
б) поток искр и шлака вырывается из разрезав бок, а кромки получаются чистыми, без натеков и подплавлений.
в) то поток искр и шлака вырывается из разреза горизонтально, а кромки получаются чистыми, без натеков и подплавлений.
Задание№27
При работе с металлом большей толщины (100-200 мм) угол наклона резака:
Варианты ответа:а) уменьшить до 10-15°;
б) прибавит до 30°;
в) уменьшить до 5°
Задание№28
При разрезании металла толщиной свыше 100 мм и при резке, выполняемой на газах-заменителях ацетилена, расстояние следует увеличить:
Варианты ответа:а) на 30-40% для предотвращения перегрева мундштука.
б) на 10-15% для предотвращения перегрева мундштука.
в) на 50% для предотвращения перегрева мундштука.
Задание№29
При резке отливок и поковок толщиной 300-800 мм можно воспользоваться:
Варианты ответа:а) универсальным резаком;
б) керосинорезом;
в) ручным резаком типа РЗР-2;
Задание№30
Неравномерный нагрев и охлаждение деталей или заготовок в процессе резки приводит:
Оксиды на поверхности металлов, механизм их образования и роста. Сравнительная характеристика физической и химической стойкости оксидов
В атмосферных условиях металлы покрыты оксидными пленками. Первично образующаяся на металле оксидная пленка может иметь аморфную или кристаллическую структуру. Например, в случае окисления алюминия при комнатной температуре образуется аморф-ная пленка толщиной 20¸45Å, которая при нагреве становится кри-сталлической. Первичная пленка на железе меди, цинке с самого на-чала имеет кристаллическое строение. Образование аморфных или кристаллических первичных оксидных пленок зависит не только от физико-химической природы окисляемого металла, но и от условий ее образования, в основном от температуры.
При комнатной температуре в атмосфере воздуха вначале окисление металла идет быстро, но при достижении определенной толщины пленки процесс окисления практически заканчивается. Так, при окислении меди приблизительно через 2 часа толщина пленки достигает 24Å, а затем почти не изменяется. После образования первичной пленки дальнейшее окисление определяется скоростью диффузии через нее металла и кислорода. При диффузии металла зоной роста является внешняя поверхность оксидной пленки. При диффузии кислорода зоной роста является граница металл-оксидная пленка. При соизмеримых скоростях встречной диффузии металла и кислорода зона роста находится внутри оксидной пленки. Схема роста оксидной пленки в этом случае представлена на рис. 1
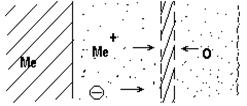 |
Рис. 1 – Схема роста оксидной пленки при соизмеримых скоростях встречной диффузии металла и кислорода
Так как оксидные пленки на металлах имеют кристаллическую структуру, обладающую ионной, а также электронной проводимостью, то при диффузии через пленку перемещаются не непосредственные атомы металла, а ионы и свободные электроны. Это не исключает возможности атомной диффузии, но поскольку радиусы ионов металлов значительно меньше атомов, то можно предположить, что основной диффузионный поток от металла будет состоять из их ионов. Кислород же проникает внутрь оксидной пленки в виде атомов, а не ионов, т.к. размер атомов кислорода в два с лишним раза меньше радиуса иона кислорода.
В процессе образования оксидных пленок закон их роста может быть различным, что в основном определяется соотношением объема оксида Vокк объему металла Vм, из которого он образовался. Например, это отношение для некоторых металлов имеет следующее значение:
Mg – 0,35 Zn – 1,57 Ni – 1,64
Sn – 1,31 Cu – 1,71 W – 3,50
Al – 1,38 Fe – 1,78
= k, (1)
где y – толщина оксидной пленки;
t– время окисления;
k – константа.
После интегрирования зависимости (4.1) получим
y = kt + A(2)
Линейный характер роста пленки устанавливается через некоторое время после начала окисления, когда пленка достигает критической величины. Это наблюдается на щелочных и щелочноземельных металлах, а также на таких металлах как ванадий, молибден, вольфрам, образующих оксиды, легко испаряющиеся при нагреве.
y 2 = kt + A(3)
Для некоторых металлов рост пленки можно описать зависимостью
y n = kt + A (4)
(Частный случай – кубическая парабола при n = 3)
Иногда наблюдается логарифмическая зависимость роста оксидной пленки.
y = ln(kt)(5)
Скорость роста оксидной пленки в процессе окисления зависит от температуры. С повышением температуры скорость увеличивается в соответствии с зависимостью
= Ае – Q / RT ,(6)
где Q – энергия активации процесса;
R – газовая постоянная;
T – абсолютная температура.
Следует отметить, что рассмотренные закономерности роста оксидной пленки соблюдается лишь для чистых металлов. Наличие даже следов примесей может сильно изменить свойства поверхности металла и характер реакций его с кислородом.
Образующиеся на металлах в результате окисления пленки делятся на тонкие, средние и толстые. Тонкими принято считать невидимые пленки от мономолекулярных до 400Å, средними от 400 до 5000Å и толстыми – выше 5000Å (0,5 мкм). В процессе пайки металлов большое значение имеют не только толщины, но и свойства оксидных пленок. Плотные, прочно связанные с металлом оксидные пленки труднее удалить с поверхности металла, что осложняет процесс пайки. Чем менее компактна оксидная пленка, чем слабее ее связь с металлом и, чем менее устойчива она при нагреве, тем меньше затруднений возникает в процессе удаления ее при пайке.
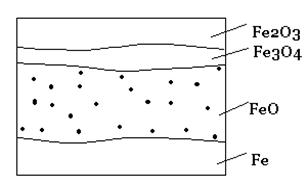
При окислении железа кислородом возможно образование разных соединений в соответствии с диаграммой состояния железо-кислород. Оксидная пленка на железе обычно имеет четко выраженный слоистый характер. На границе с металлом образуется монооксид железа FeO, соответствующая наименьшему содержанию кислорода в оксиде, затем следует промежуточный слой монооксида-оксида железа Fe3O4 и на внешней поверхности пленки – высший оксид Fe2O3. Предполагается, что поверхностный слой металла, находящийся под оксидной пленкой, содержит некоторое количество кислорода в виде твердого раствора с металлом.
Прилегающий к металлу слой монооксида железа FeO (вюстит) имеет кубическую кристаллическую решетку по типу каменной соли. FeO устойчив только при температурах выше 570 0 С. При более низких температурах он не образуется, а при медленном охлаждении распадается с выделением металла по реакции:
4FeO Þ Fe + Fe3O4
При температуре 1377 0 С монооксид железа плавится.
Монооксид-оксид железа Fe3O4 (магнетит) имеет кристалличесую кубическую решетку. Магнетит кристаллографически является самостоятельной фазой, а не молекулярной смесью монооксида и оксида железа. Он устойчив при всех температурах, начиная от комнатной и до точки плавления железа. При нагреве в окислительной среде магнетит переходит в оксид железа a-Fe2O3. Этот переход совершается в две стадии. При нагреве до температуры 220 0 С образуется промежуточная структура оксида g- Fe2O3 с сохранением кубической шпинельной решетки. Двухвалентное железо при этом превращается в трехвалентное:
 |
При дальнейшем нагреве до 400-500 0 С оксид теряет магнитные свойства и образуется решетка оксида железа a- Fe2O3.
Рис. 2 – Микроструктура оксидной пленки на железе (схема)
Оксид железа Fe2O3 (гематит) имеет ромбоэдрическую структуру. Гематит устойчив в широком интервале температур, но при нагреве выше 1100 0 С частично разлагается. При температуре плавления железа гематит полностью диссоциирует на железо и кислород.
При окислении меди образуются три вида оксидов – монооксид меди Cu2O, оксид меди CuO и полуторный оксид меди Cu2O3. Имеются также предположения об образовании в интервале 950-1050 0 С соединения типа недооксида Cu4O. Окисление меди начинается с адсорбции газа на ее поверхности. При комнатной температуре на воздухе происходит образование оксида меди, кристаллизующегося в кубической решетке. Кристаллическая решетка оксида меди ориентирована так, что ребра и грани кубической решетки Cu2O лежат параллельно и граням кубической решетки меди.
Нагрев меди выше 250 0 С вызывает более интенсивное окисление, при этом пленка состоит из смеси оксида и монооксида меди. Рост пленки происходит по диффузионному механизму; предполагают, что при повышенных температурах через пленку диффундируют ионы меди, имеющие малый размер. При 300 0 С и выдержке 5÷10 мин в атмосфере воздуха медь покрывается цветами побежалости.
Наряду с монооксидом меди при окислении также образуется полуторный оксид меди, который, как и монооксид, имеет красный цвет. Кристаллическая решетка его соответствует решетке монооксида меди и отличается от последней только удельной проводимостью. Полуторный оксид меди неустойчив, он начинает разлагаться при 75 0 С. При 400 0 С разложение происходит по уравнению
В интервале 400 – 500 0 С и выдержке 5¸15 мин окисная пленка на меди двухслойная. К металлу примыкает монооксид меди, верхний более тонкий слой состоит из оксида меди, имеющий почти черный цвет. Оксидная пленка в интервале 600 – 800 0 С имеет мелкокристаллическую структуру и плохую связь с металлом. Выше 800 0 С образовавшийся оксид меди разлагается по уравнению
4 CuO Þ 2 Cu2O + O2
В интервале 800 – 950 0 С пленка состоит только из монооксида меди. Этот интервал характерен несколько более прочной связью пленки с основным металлом. При 950¸1050 0 С оксидная пленка приобретает ярко малиновый цвет, что связано, по-видимому, с образованием соединения Cu4O. Оксидная пленка в этом интервале имеет крупнокристаллическую структуру и наиболее прочно держится на металле.
Алюминий при взаимодействии с кислородом при комнатной температуре окисляется с образованием первичной оксидной пленки толщиной 40¸100 мкм. Дальнейшее окисление алюминия тормозится, т.к. образовавшаяся пленка надежно изолирует металл от кислорода. Для оксида алюминия известны модификации a, b, g и др. Наряду с оксидом алюминия известны оксиды состава Al2O – недооксид алю-миния и AlO – субоксид алюминия, существующие при высоких температурах. Первоначально образующийся на поверхности алюми-ния оксидный слой в атмосферных условиях представляет собой аморфное образование. Умеренное нагревание этого слоя до темпе-ратуры выше 200 0 С приводит к возникновению модификации g- Al2O3. В результате взаимодействия с влагой воздуха в оксидной пленке на поверхности алюминия могут образовываться гидрооксиды.
Применяемые в качестве припоев металлы и сплавы также имеют на своей поверхности оксидную пленку. Нагрев под пайку при недостаточной защите может вызывать дальнейшее окисление припоя. Наличие на поверхности припоя в процессе пайки оксидной пленки приводит к ухудшению условий пайки и свойств паяных соединений. Поэтому для получения качественных паяных соединений необходима очистка припоя перед пайкой и надежные условия удаления оксидов в процессе пайки.
В зависимости от состава припои имеют различную окисляемость. Наибольшей стойкостью при высоких температурах отличаются припои на основе никеля.
При легировании основы паяемого металла или припоя легирующие элементы по-разному могут влиять на образование оксидной пленки. Скорость окисления металла может или уменьшаться или увеличиваться. Если легирующие элементы обладают меньшим сродством к кислороду по сравнению с основным металлом, то они обычно остаются под оксидной пленкой в неокисленном состоянии.
На основе анализа состава и строения оксидных пленок можно видеть, что даже при самых благоприятных условиях окисления чистых металлов и сплавов в атмосфере воздуха образующиеся пленки имеют толщину более 20Å. Силы взаимодействия атомов металлов между собой практически исчезают на расстояниях более 10 ангстрем, поэтому обеспечить взаимодействие паяемого металла и расплавленного припоя при наличии на их поверхности оксидных пленок невозможно. Следовательно, металлы необходимо тщательно очищать от оксидных пленок и загрязнений, для чего перед пайкой надо производить механическую зачистку или травление их поверхности в растворах щелочей или кислот. Однако за время между очисткой и пайкой на поверхности металлов вновь образуется тонкая оксидная пленка. Поэтому непосредственно в процессе пайки необходимо удалять оксидную пленку не только с паяемого металла, но и с расплавленного припоя, что достигается применением при пайке флюсов, искусственных газовых сред, вакуума, а также физико-механическими способами разрушения оксидной пленки.
Виды и способы оксидирования металла
Оксидированием стали создается защитная пленка из сложных окислов, которая препятствует образованию ржавчины. Узнайте о видах обработки, особенностях химического, анодного и термического процессов.

Ни один материал, включая сталь, не может служить вечно. Его необходимо защищать от влаги, солнечных лучей и низких температур. Оксидирование металла создает на его поверхности тонкую защитную пленку, не позволяющую кислороду из воздуха и воде разрушать материал. При этом изменяются технические характеристики сталей, алюминия и его сплавов.

С точки зрения химии оксидирование – это реакция окисления металла и образование на поверхности тонкого слоя кристаллов, связанных кислородом и другими веществами. Технология нанесения защитного покрытия имеет несколько видов различной сложности. Самая простая использовалась несколько веков назад и доступна любому желающему покрыть защитной пленкой деталь в домашних условиях. Сложная технология требует специального оборудования и осуществляется только в условиях производства.
Суть и назначение технологии
В своей основе оксидирование стали имеет окислительно-восстановительную реакцию металла при его взаимодействии с кислородом воздуха, электролитом или специальными кислотно-щелочными растворами. В результате на поверхности детали образуется защитная пленка, повышающая технические характеристики металла:
- увеличивает твердость;
- снижает образование задиров;
- повышает способность деталей к прирабатыванию;
- увеличивает срок службы;
- создает декоративное покрытие.
Добавление в электролит растворов для окрашивания позволяет создавать изделия из металла с поверхностями разных цветов.
Покрытие оксидной пленкой применяют для различных материалов. В ювелирной промышленности и при создании бижутерии используют оксидирование многих металлов:
- серебра;
- алюминия;
- меди;
- титана;
- латуни;
- бронзы.
Сущность обработки – в увеличении прочности и придании дополнительной декоративности. Изделия из серебра хорошо держат форму. Это позволяет создавать украшения с острыми углами и тонким орнаментом. С помощью оксидов создается патина, имитирующая старину, и другие эффекты.

В зависимости от характеристик и свойств металла используют различные технологии создания сложных окислов на поверхности.
К положительным качествам оксидирования относится его распределение по поверхности тонкой пленкой в несколько микрон – тысячных долей миллиметра. При этом не меняются размеры деталей и посадочных мест сверху и на поверхности.
Виды оксидирования металла
- микродуговое;
- горячее;
- холодное.
К микродуговому относится способ нанесения оксидной пленки с помощью электролизной установки. Деталь помещается в ванну с электролитом. К ней подключается «+» постоянного тока. К ванне – провод с «–». При прохождении тока на поверхности образуются микроочаги с высокой температурой и давлением. В результате происходит окисление. Микродуговое оксидирование применяют для покрытия алюминия, серебра и их сплавов.
Процесс горячего оксидирования стали заключается в нагреве детали или раствора, в котором она находится, для ускорения процесса образования пленки сложных окислов.
К холодным технологиям относятся, в основном, методы химического покрытия и плазменного, когда поверхность насыщается кислородом под воздействием микротоков или в насыщенном растворе солей.
Химическое
Химическое оксидирование проводится погружением деталей в различные растворы. Низкотемпературный процесс покрытия осуществляют при температуре 30–180 °C. Сталь погружают в раствор щелочей или кислот с добавлением марганца. Затем, после извлечения из ванны, промасливают – смазывают маслом или на несколько секунд погружают в него деталь.
Электрохимическое покрытие оксидами проводится при низких температурах – до 100 °C. Электролит представляет собой раствор нескольких нитратов и хроматов. Получают черное покрытие стали.
Пищевая нержавейка содержит много легирующих веществ, включая хром и марганец. Она требует для покрытия сложного оборудования. В домашних условиях ее можно оксидировать в растворе натриевой селитры. Поверхность приобретает яркий синий цвет.
Анодное
Анодное оксидирование небольших деталей доступно делать в домашней мастерской. Для этого надо иметь аккумулятор или выпрямитель тока. Анод подключается к детали и источнику постоянного тока. При погружении стали в раствор слабокислого электролита возникает движение электронов, и вместе с ними частицы солей и кислот проникают в верхний слой металла. В результате образуются кристаллы железа со сложными окислами. Они постепенно покрывают всю поверхность детали слоем в несколько микрон.
Регулировать скорость процесса для образования оксидной пленки нужной толщины можно изменением силы тока и повышением температуры электролита. Анодирование влияет на первоначальные характеристики стали и цветных металлов:
- изменяет цвет;
- увеличивает прочность;
- пленка имеет низкую электропроводность;
- не допускает образования простых окислов железа – коррозии.
Термическое
Кто наблюдал за сваркой деталей или их нагревом в термопечах, видел на поверхности цвета побежалости: от желтого оттенка до синего тона, переходящего в черный. Они зависят от температуры, до которой нагрелась сталь в конкретной точке. Чем сильнее прогрет металл, тем больше он окислен, имеет более темный цвет.
Достаточно нагреть поверхность до 300 ⁰C, чтобы провести термическое оксидирование. На стали появится тонкая пленка окислов желтого и светло-коричневого цвета. Чем выше содержание легирующих веществ, тем сильнее надо греть сталь.
Часто нагрев используют для более активного протекания химического и анодного оксидирования стали. Помещенный в горячий раствор натриевой селитры или смеси кислот металл быстрее вступает в реакцию.
Плазменное
Метод холодного оксидирования – плазменное покрытие деталей. Окисление происходит при низкой температуре. Деталь помещают в плазму, которую создают токи ВЧ или СВЧ, аналогичные микроволновой печи. В камере высокое содержание кислорода.
Плазменное оксидирование применяют, в основном, для повышения светочувствительности и электропроводности деталей оптических приборов и плат.
Лазерное
Оксидировать деталь с помощью лазера можно только в условиях промышленного предприятия. Деталь устанавливается на столе или зажимается в патроне, набирается программа, и лазер прогревает узкие полоски одна возле другой по всей поверхности. Оптимальный вариант – использование станков ЧПУ.
Недостаток лазерного оксидирования сталей – в покрытии заготовок только снаружи. В отверстия малого диаметра головка лазерной установки не войдет.
Оксидирование своими руками
Делать защитное покрытие в домашних условиях проще всего по старинному рецепту. Для этого стальной предмет следует очистить от всех видов загрязнений, протравить в слабом растворе кислоты. Любое оставшееся пятно будет препятствовать процессу оксидирования стали.
- Нагреть конструкционную сталь до 300 ⁰C. Легированные и углеродистые стали требуют более высоких температур. Чем больше легирующих элементов, тем сильнее следует греть.
- Опустить горячую заготовку в льняное масло на 8–18 минут.
- Для получения плотного слоя, надежно защищающего сталь от ржавчины, и создания изоляционного слоя, процедуру следует повторить 4–6 раз.
Каленые стали при нагреве до температуры выше 300 ⁰C могут отпуститься – стать мягче. Поэтому металл после закалки греют индуктором токами ТВЧ до 250–280 ⁰C. Если нет возможности нагреть только поверхность заготовки, температуру снижают до 220–250 °C, увеличив количество нагревов и погружений.
Льняное масло использовали в прошлые века. Сейчас его можно заменить веретенным, широко применяемым для закалки стали.
Оксидирование стали – интересный процесс. С его помощью можно самостоятельно защитить от коррозии небольшие изделия, крепеж в автомобиле и других устройствах.
Какой метод больше всего понравился нашим читателям и что они готовы применить на практике? Нам интересно ваше мнение.
Оксидирование стали
Одной из важных задач по сохранению металлических конструкций является борьба с вредным воздействием окружающей среды. Повышенная влажность, наличие в воздухе химически активных элементов, способных разрушать целостность металла, особенно стали, приводит к ухудшению таких показателей как надёжность и прочность.
Для решения этой задачи готовые изделия покрывают различными видами защитных покрытий.

Существуют различные методы повышения поверхностной устойчивости и антикоррозийности.
Одним из таких методов является создание на поверхности стали защитной плёнки, используя специальные способы обработки.
Понимание сущности назначения этого процесса требует ответа на вопрос — что такое оксидирование?
Сущность заключается в использовании свойств окислительно — восстановительной реакции, в результате чего на поверхности стали образуется защитная плёнка. Так же производится оксидирование стали.
Этот процесс позволяет решить следующие задачи:
- Защитить стальные конструкции от образования коррозии (особенно это актуально в современном строительстве, где применяются металлические конструкции).
- Ограничить воздействие агрессивных составляющих внешней среды (растворов кислот, щелочей, химических элементов, разрушающих целостность стали).
- Создать поверхностный слой, обладающий хорошими электроизоляционными характеристиками.
- Придать деталям, отдельным элементам, конструкции в целом оригинальные декоративные и эстетические свойства.
Оксидирование металла производится следующими методами:
- С применением химических реакций (химическое оксидирование стали).
- Использование электрохимических процессов (анодное оксидирование).
- Проведением термической обработки (термический метод).
- Создание низкотемпературной плазмы (плазменный метод).
- Лазерным (применяются специальные лазерные установки).

Рассмотрим каждый метод подробнее.
Химическое оксидирование
Этот процесс предполагает обработку металлов растворами, смесями, расплавами химических элементов (такие окислы как окислы хрома). Данное оксидирование позволяет провести так называемую пассивацию поверхности металла. Он предполагает создание в близком к поверхности слое металла неактивного (пассивного) образования. Создаётся тонкий поверхностный слой, защищающий основную часть конструкции.
Технологически этот процесс реализовывается посредством опускания подготовленной металлической детали в раствор щёлочи или кислоты, заданного процентного соотношения.
Выдерживают его там определённое время, которое позволяет полностью провести окислительно — восстановительную реакцию. Затем деталь тщательно промывают, подвергают естественной сушке, окончательной обработке.

Химическое оксидирование стали
Для создания кислотной ванны применяют три вида химически активных кислот: соляную, азотную, ортофосорную. Ускорение протекания химической реакции стимулируют добавлением в раствор кислоты соединений марганца, калия, хрома. Реакция окисления протекает при температуре раствора в интервале от 30 °С до 100 °С.
Применение растворов на основе щелочных соединений позволяет использовать добавки соединений нитрата натрия и диоксида марганца. В этом случае температура раствора необходимо повышать до 180 °С, а с добавками и до 300 °С.
После проведенной процедуры деталь промывают и просушивают. Иногда для закрепления процесса химической реакции применяют бихромат калия. Для увеличения срока сохранения образованной плёнки проводят химическое оксидирование с промасливанием. Иногда такой процесс называют химоксидирование. При окончательном покрытии маслом получается надёжное покрытие от коррозии, обладающее эффектным высоко декоративным чёрным цветом.
Анодное оксидирование
Такой вид называется – электрохимическое оксидирование стали. Иногда его называют и анодное оксидирование стали. Также применяют термин анодирование. В его основу заложен химический процесс электролиза. Его можно проводить как в твёрдых, так и в жидких электролитах. Подготовленную заготовку помещают в ёмкость с оксидным раствором.
Протекание реакции электролиза возможно при создании разности потенциалов между двумя элементами.
Поверхность окисляемого изделия характеризуется положительным потенциалом. Из раствора выделяют химически активные элементы с отрицательным потенциалом. Взаимодействие разнополярных элементов и называется реакцией электролиза (в нашем случае анодирования).

Протекание реакции анодирования можно выполнить в домашних условиях. Требуется чётко выполнять условия техники безопасности. В реакции участвуют вредные реактивные жидкости и небезопасное напряжение.
Применение анодного оксидирования позволяет создавать защитные плёнки различной толщины. Создание толстых плёнок возможно благодаря применению раствора серной кислоты.
Тонкие плёнки получают в растворах борной или ортофосфорной кислоты. С помощью анодирования можно придать поверхностному слою металла красивые декоративные оттенки. С этой целью процесс проводят в органических кислотах. В качестве таких растворов применяют щавелевую, малеиновую, сульфосалициловую
Специальным процессом анодирования считается микродуговое оксидирование. Оно позволяет получать покрытия, обладающие высокими физическими и механическими характеристиками. К ним относятся: защитные, изоляционные, декоративные, теплостойкие и антикоррозийные свойства. В этом случае оксидирование производится под действием переменного или импульсного тока в специальных ваннах заполненных электролитом. Такими электролитами являются слабощелочные составы.

Анодное оксидирование в домашних условиях
Анодирование позволяет получить поверхностный слой, обладающий следующими свойствами:
- надёжное антикоррозионное покрытие;
- хорошие электрические изоляторы;
- тонкий, но стойкий поверхностный слой;
- оригинальную цветовую гамму.
К анодированию нержавеющей стали требуется специальный подход. Это связано с тем, что такая сталь считается нейтральным (инертным) сплавом. Поэтому на производстве при анодировании большого количества деталей применяют двух этапную процедуру.
На первом этапе анодирование нержавеющей стали производят совместно с другим, более подходящим для этого процесса металлом. Это может быть никель, медь, другой металл или сплав.
На втором этапе производят оксидирование непосредственно самой нержавеющей стали. Для упрощения процесса оксидирования сегодня ведутся разработки специальных добавок, так называемых пассивирующих паст. Эти составы ускоряют процесс реакции нержавеющей стали.
Термическое оксидирование
Согласно термину оксидирование происходит при относительно высоких температурах. Величина этого показателя зависит от марки стали. Например, процесс термического оксидирование обычной стали происходит в специальных печах. Внутри создаётся температура, близкая к 350 °С. Класс легированных сталей подвергаются термическому оксидированию при более высоких температурах. Необходимо разогреть заготовку до 700 °С. Обработка продолжается в течение одного часа. Этот процесс получил название воронение стали.
Воронение стали Стальной пистолет после воронения
Плазменное оксидирование
Такое оксидирование проводят в среде с высокой концентрацией кислорода с помощью низкотемпературной плазмы. Плазма создаётся благодаря разрядам, возникающим при подаче токов высокой или сверхвысокой частоты.
Плазменное оксидирование используют для формирования оксидированных плёнок на достаточно небольших поверхностях.
В основном его применяют в электронике и микроэлектронике. С его помощью образуют слои на поверхности полупроводниковых соединений, так называемых p-n переходах. Такие плёнки используют в транзисторах, диодах (в том числе в туннельных диодах), интегральных микросхемах. Кроме этого она используется для повышения светочувствительного эффекта в фотокатодах.

Разновидностью плазменного оксидирования является оксидирование с применением высокотемпературной плазмы. Иногда её заменяют на дуговой разряд с повышением температуры до 430 °С и выше. Применение этой технологии позволяет значительно повысить качество образуемых покрытий.
Лазерное оксидирование
Эта технология достаточно сложна и требует специального оборудования. Для проведения оксидирования используют:
- импульсное лазерное излучение;
- непрерывное излучение.
В обоих случаях применяются лазерные установки инфракрасного диапазона. За счёт лазерного прогрева верхнего слоя материала удаётся получить достаточно стойкую защитную плёнку. Однако этот метод применяется только для поверхности небольшой площади.

Организовать процесс оксидирования небольших металлических изделий можно в домашней лаборатории. При точном соблюдении последовательности технологических операций добиваются качественного оксидирования.
Весь процесс следует разделить на три этапа:
- Подготовительный этап (включает подготовку необходимого оборудования, реактивов, самой детали).
- Этап непосредственного оксидирования.
- Завершающий этап (удаление вредных следов химического процесса).
На подготовительном этапе проводят следующие работы:
- Грубая зачистка поверхности (применяется щётка по металлу, наждачная бумага, полировочная машина с соответствующими дисками).
- Окончательная механическая полировка поверхности.
- Снятие жирового налёта и остатков полировки. Его называют декопирование. Он проводится в пяти процентном растворе серной кислоты. Время пребывания обрабатываемой детали в растворе равно одной минуте.
- Промывание детали. Эту процедуру проводят в тёплой кипячёной воде. Целесообразно её провести несколько раз.
- Завершающей операцией является так называемое пассирование. Вымытую после обработки деталь, помещают чистую кипячёную воду, в которой предварительно растворяют хозяйственное мыло. Этот раствор вместе с деталью подогревают и доводят до состояния кипения. Процедуру кипения продолжают в течение нескольких минут.

Оксидирование в домашних условиях
На этом предварительный этап заканчивается.
Основной этап оксидирования состоит из следующих операций:
- В нейтральную посуду (лучше с эмалированным покрытием), заливается вода. В ней растворяют около едкий натр. Объём вещества зависит от количества воды. Целесообразно получить раствор около 5 процентов.
- В полученный раствор полностью погружают обрабатываемую деталь.
- Раствор с погруженной деталью нагревают до 150 градусов. Практически это процесс кипячения. Он продолжается примерно два часа. Используя инструмент, проверяют качество процесса. Если необходимо время может быть увеличено.
На завершающем этапе с деталью производят следующие операции:
- Деталь извлекают из ванны с реактивом.
- Укладывают на ровную поверхность, дают её остыть естественным образом (без принудительного охлаждения). Желательно создать условия, ограничивающие контакт с окружающим воздухом.
- Визуально проверяют качество полученного оксидирования. Отсутствие непокрытых участков, плотность образованной плёнки, итоговый цвет.
Таким образом, проводить оксидирование можно и в домашних условиях. Главное, соблюдать указанные рекомендации.
Покрытие оксидными плёнками как способ защиты от коррозии металлов

В своей основе оксидирование стали имеет окислительно-восстановительную реакцию металла при его взаимодействии с кислородом воздуха, электролитом или специальными кислотно-щелочными растворами. В результате на поверхности детали образуется защитная пленка, повышающая технические характеристики металла:
Добавление в электролит растворов для окрашивания позволяет создавать изделия из металла с поверхностями разных цветов.
Покрытие оксидной пленкой применяют для различных материалов. В ювелирной промышленности и при создании бижутерии используют оксидирование многих металлов:

К положительным качествам оксидирования относится его распределение по поверхности тонкой пленкой в несколько микрон – тысячных долей миллиметра. При этом не меняются размеры деталей и посадочных мест сверху и на поверхности.



Незамерзающие жидкости
Несмотря на то что наиболее популярным теплоносителем отопительных систем пока остается обычная вода, все большее число пользователей отдают предпочтение антифризам. Незамерзающие жидкости хорошо подходят прежде всего для частных домовладений, расположенных в дачных и коттеджных поселках, где перебои с электроснабжением случаются достаточно часто. Использование антифризов особенно удобно в загородных домах с сезонным проживанием. В состав качественных теплоносителей входит пакет присадок, исключающий возникновение накипи и ржавчины на металлических поверхностях элементов отопительного контура. Так, теплоноситель «THERMAGENT –30 °С ЭКО», который производится на основе пропиленгликоля высшего сорта с применением новейшей технологии Organic Acid Technology, содержит набор высокоэффективных присадок, способных обеспечить длительную безаварийную работу системы отопления любого жилого или служебного помещения.
Процесс оксидирования стали имеет несколько разновидностей:
Химическое оксидирование проводится погружением деталей в различные растворы. Низкотемпературный процесс покрытия осуществляют при температуре 30–180 °C. Сталь погружают в раствор щелочей или кислот с добавлением марганца. Затем, после извлечения из ванны, промасливают – смазывают маслом или на несколько секунд погружают в него деталь.
Электрохимическое покрытие оксидами проводится при низких температурах – до 100 °C. Электролит представляет собой раствор нескольких нитратов и хроматов. Получают черное покрытие стали.
Пищевая нержавейка содержит много легирующих веществ, включая хром и марганец. Она требует для покрытия сложного оборудования. В домашних условиях ее можно оксидировать в растворе натриевой селитры. Поверхность приобретает яркий синий цвет.
Кто наблюдал за сваркой деталей или их нагревом в термопечах, видел на поверхности цвета побежалости: от желтого оттенка до синего тона, переходящего в черный. Они зависят от температуры, до которой нагрелась сталь в конкретной точке. Чем сильнее прогрет металл, тем больше он окислен, имеет более темный цвет.
Достаточно нагреть поверхность до 300 ⁰C, чтобы провести термическое оксидирование. На стали появится тонкая пленка окислов желтого и светло-коричневого цвета. Чем выше содержание легирующих веществ, тем сильнее надо греть сталь.
Часто нагрев используют для более активного протекания химического и анодного оксидирования стали. Помещенный в горячий раствор натриевой селитры или смеси кислот металл быстрее вступает в реакцию.
Оксидировать деталь с помощью лазера можно только в условиях промышленного предприятия. Деталь устанавливается на столе или зажимается в патроне, набирается программа, и лазер прогревает узкие полоски одна возле другой по всей поверхности. Оптимальный вариант – использование станков ЧПУ.
Недостаток лазерного оксидирования сталей – в покрытии заготовок только снаружи. В отверстия малого диаметра головка лазерной установки не войдет.






Зачем бороться с коррозией
Смысл использования присадок заключается прежде всего в защите внутренних поверхностей отопительной системы от накипи и ржавчины. Негативный эффект коррозии состоит в следующем:
- радиатор, покрытый изнутри ржавчиной, отдает меньше тепла. Котел или другой генератор тепла работает с повышенной нагрузкой, и, как следствие, возрастают расходы на поддержание комфортной температуры в помещении;
- попадая в теплоноситель, частицы ржавчины перемещаются по системе и стирают резиновые уплотнения, с которыми вступают в соприкосновение;
- если не бороться с коррозией в течение длительного времени, это может привести не только к засорению, но и к полному разрушению теплообменника котла. Частицы ржавчины затрудняют циркуляцию теплоносителя и засоряют фильтр котла;
- развитие коррозии увеличивает риск прорыва труб на изгибах, в местах сужения и выхода объемных колен радиатора в трубопровод, где давление теплоносителя выше.

Льняное масло использовали в прошлые века. Сейчас его можно заменить веретенным, широко применяемым для закалки стали.
Недостатки неорганических присадок
Теплоносители, в составе которых используются силикатные ингибиторы коррозии, отличаются невысокой стоимостью и при соблюдении правил эксплуатации достаточно эффективно выполняют свои функции. Вместе с тем силикаты выделяют гель и абразив, которые загрязняют оборудование и вызывают перебои в функционировании системы. Если незамерзающая жидкость содержит фосфаты, то при разбавлении теплоносителя водой (например, для изменения температуры замерзания) образуется осадок. Для нитритов характерно быстрое окисление – вещество переходит в неактивную форму и оседает. Взаимодействие аминов и нитритов ведет к образованию канцерогенных соединений. Осадок неорганических добавок повышает вязкость теплоносителя, наслаивается на внутренних поверхностях системы, ухудшает пропускную способность труб.

Особенности процесса
Поверхность алюминиевых деталей покрыта оксидной плёнкой, которая обладает высокой химической стойкостью, а также температурой плавления выше в 2 раза, чем чистого металла. В интервале от +2500С до +3000С алюминий становится неустойчивым и подплавляется. Минимальная температур плавления оксидной плёнки составляет +5000С.
При пайке соединяемые детали под наружным слоем начинают плавится. Поэтому пайщику нужно устранить негативное влияние оксидного слоя. Принцип всех способов основан на удалении плёнки, а также повышении адгезионных свойств.
Методы удаления оксидного слоя:
- механический — использование абразивных инструментов для зачистки,
- химический — применение флюсов со специальными составами,
- электрохимический — основан на процессах электролиза.
Оба способа проводятся только в среде с отсутствием доступа кислорода.
Удельная поверхность алюминиевого лома
Потеря алюминия из-за его окисления при переплаве в печи какой-нибудь загрузки лома пропорциональна удельной площади этого лома. Удельная площадь выражается соотношением
где m – общая масса партии лома, A – общая площадь поверхности всех кусочков лома, составляющих эту загрузку.
Удельная площадь поверхности алюминиевых отходов является критическим параметром. Ее величина увеличивается с уменьшением размеров частиц лома. Так, у куба со стороной 10 см площадь поверхности равна 600 кв. см , а у эквивалентных по массе 1000 кубиков со стороной 1 см – в 10 раз больше. Поэтому скорость окисления этих кубиков будет в 10 раз больше, чем большого куба.
Натуральный метод
1. Отварите 2-4 яйца в кипящей воде 15 минут.
2. Выньте вареные яйца из воды и положите на разделочную доску. Ложкой разомните яйца вместе со скорлупой.
3. Раздавленные яйца переложите в пластиковый пакет с застёжкой-молнией. Пакет должен быть достаточно большим, чтобы в нём поместилось изделие. В качестве альтернативного варианта можно взять большую воздухонепроницаемую ёмкость.
4. Медный предмет поместите в пластиковый пакет и закройте его. Если в пакет вы кладёте больше одного предмета, убедитесь, что они не касаются друг друга, чтобы они оксидировались со всех сторон. Яичные желтки обязательны, потому что в них содержится большое количество серы, окисляющей медь.
5. 20 минут спустя выньте медный предмет из пакета с помощью металлических щипцов. Вы заметите, что поверхность меди потемнела. Если вы хотите более тёмную патину, оставьте изделие в пакете на всю ночь.
6. Выньте изделие из пакета и ополосните слегка тёплой водой, чтобы смыть яйцо.
Читайте также:
