При какой температуре шипит слюна на металле
Обновлено: 27.09.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Жжение в глазах: причины появления, при каких заболеваниях возникает, диагностика и способы лечения.
Определение
Жжение в глазах, ощущение песка, зуда – крайне неприятные симптомы, которые могут возникать как в результате сильного перенапряжения, длительного сидения за компьютером, неблагоприятных условий окружающей среды, так и на фоне различных заболеваний и патологических процессов.
Попытки самостоятельно избавиться от жжения в глазах могут только усугубить состояние, особенно когда причина не ясна.
Разновидности жжения в глазах
Общепринятой классификации состояний и заболеваний, проявляющихся ощущением жжения в глазах, не существует, поэтому следует ориентироваться на причины, вызывающие данное состояние – они могут быть эндогенными и экзогенными.
Возможные причины жжения в глазах
Сильный ветер, задымление или большое количество пыли – достаточно частая причина жжения в глазах. Если глаза успокаиваются после прекращения действия раздражающего фактора, повода для беспокойства нет.
Жжение в глазах может быть реакцией на попадание химических веществ, таких как шампунь, мыло, хлорированная вода бассейна, косметика и т.д.
Длительное ношение контактных линз также может вызывать неприятные ощущения, которые человек описывает как жжение, или песок в глазах.
Дискомфорт глаз (жжение в сочетании с зудом и покраснением) часто сопутствует аллергическим реакциям на смог, дым, пыль, плесень, пыльцу или перхоть домашних животных. Однако даже чистый, но горячий и сухой воздух может вызвать столь неприятный симптом – это объясняется тем, что слезная пленка, защищающая глаза, быстро высыхает и не успевает восстановиться.
Попадание инородного предмета в глаза также может привести к жжению, зуду и рези.
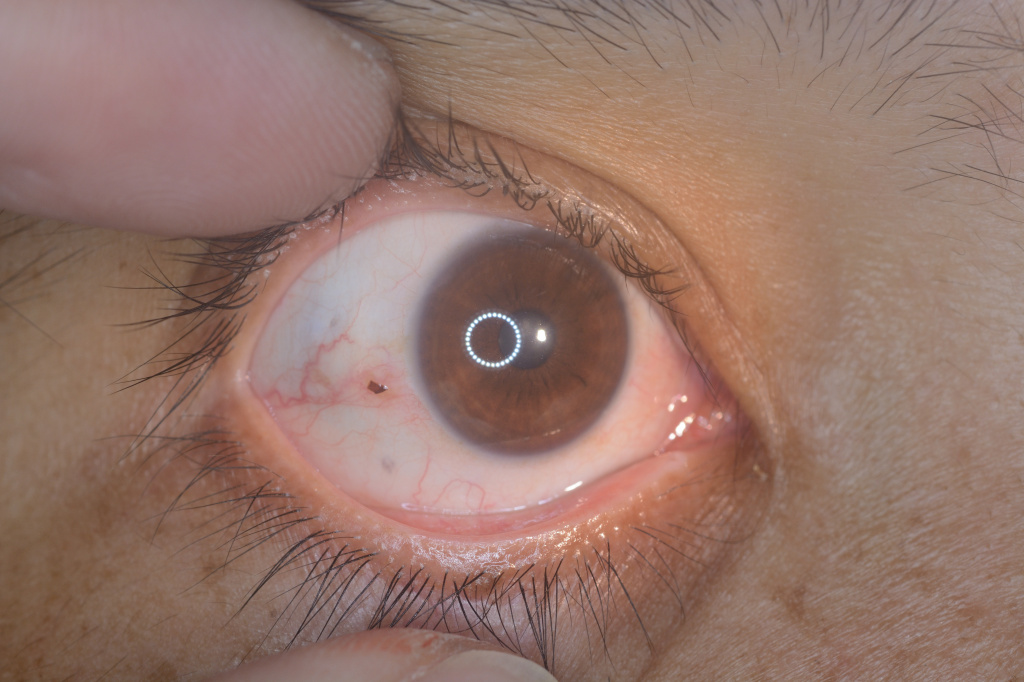
В ряде случаев жжение сигнализирует о серьезных заболеваниях органов зрения, к которым относятся офтальморозацеа (хроническое воспалительное заболевание, поражающее различные структуры глаза), кератит (воспаление роговицы глаза), синдром сухого глаза (характеризуется снижением выработки слезы, что приводит к нарушению естественной защиты глаз) и блефарит (воспаление века).
Конъюнктивит (воспаление слизистой оболочки глаза) различной этиологии, в том числе ставший осложнением ОРВИ, гриппа и других инфекционных заболеваний, всегда проявляется жжением в глазах. Предвестником конъюнктивита может быть так называемый ячмень (воспаление волосяного мешочка ресницы или сальной железы Цейсса).
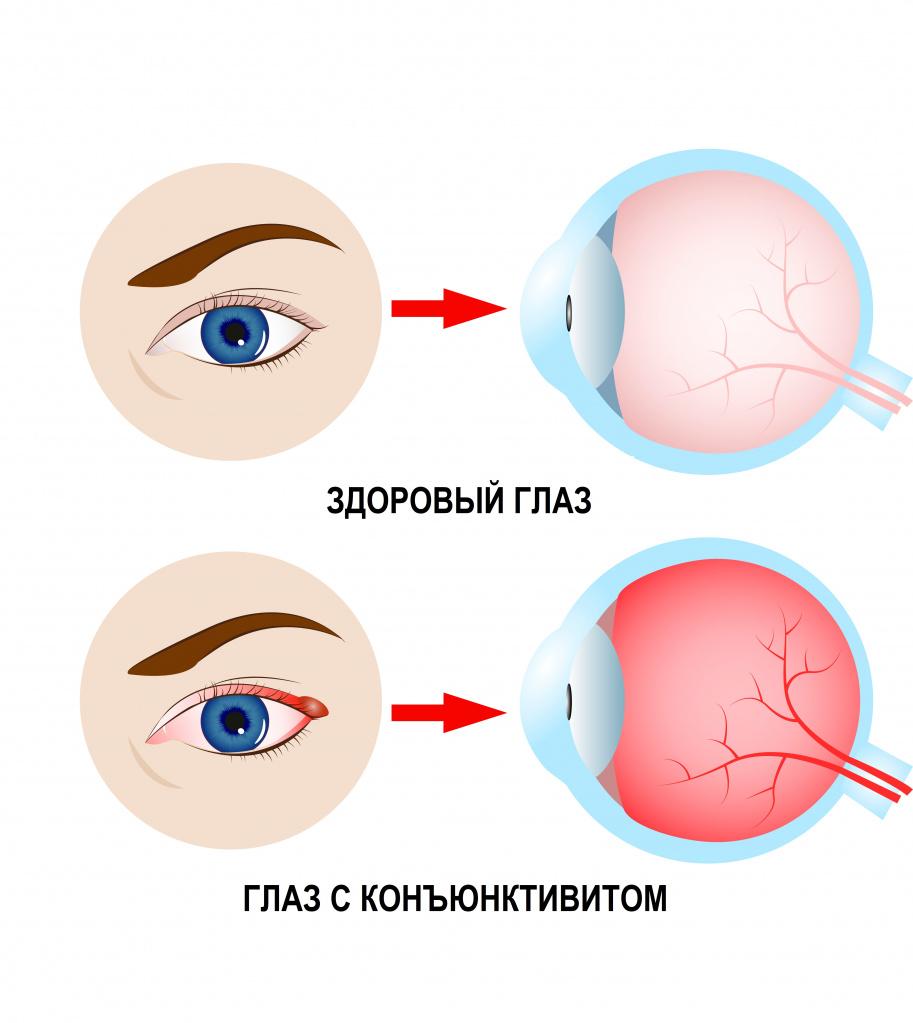
В редких случаях ощущение жжения и песка в глазах является симптомом более серьезных заболеваний: увеита (воспаления сосудистой оболочки глаза, которое может привести к снижению и даже потере зрения) или орбитального целлюлита (инфекционного воспаления мягких тканей, расположенных позади глаза).
Таким образом, появление жжения в глазах характерно для следующих заболеваний и состояний:
- Синдром сухого глаза.
- Конъюнктивит (воспаление слизистой оболочки глаза).
- Блефарит (воспаление кожи век).
- Кератит (воспалительный процесс в роговице глаза).
- Хронический мейбомиит (воспаление желез, находящихся в веке).
- Орбитальный целлюлит.
- Увеит.
- Офтальморозацеа.
- Аутоиммунные заболевания (синдром Шегрена).
- Некорректное использование контактных линз.
- Травмы глаз.
Лечением заболеваний глаз занимается врач-офтальмолог. Он назначает необходимые анализы, проводит дополнительные специализированные обследования. В случае подозрения на инфекционное или аутоиммунное заболевание может потребоваться консультация врача-инфекциониста и ревматолога.
Диагностика и обследования при жжении в глазах
Тщательный сбор анамнеза с учетом всех жалоб пациента, осмотр и проведение диагностических исследований помогут установить правильный диагноз.
- Клинический анализ крови с развернутой лейкоцитарной формулой необходим для выявления воспалительных процессов при различных инфекционных заболеваниях.
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий.
При какой температуре шипит слюна на металле
Коррозионные свойства слюны. Влияние слюны на зубные протезы
Опыт работы с серебряно-палладиевым сплавом показал не только положительные физико-химические и механические, но главным образом активные биологические качества его. Именно эти качества позволяют считать серебряно-палладиевый сплав представителем нового направления материаловедения — биологического. В последние годы биологическое материаловедение получило интенсивное развитие. Создаются, например, новые сплавы на основе золота, палладия и серебра.
Эти сплавы электрохимически нейтральны относительно друг друга, так как окислительно-восстановительные потенциалы золота (+1,42 В), серебра ( + 0,8 В) и палладия (+ 1,2 В) приблизительно равны. Электрохимическая индифферентность составляющих компонентов сплавов для зубных протезов является необходимым условием биологического материаловедения.
С этой целью неблагородные сплавы (нержавеющая сталь, хромокобальт) покрывают слоем благородных, химически бездеятельных металлов (золото, палладий, нитридтитан) — методом гальванопластики, вакуумного напыления и др. Высокие прочностные свойства и электрохимическая индифферрентность достигаются разработкой и внедрением в практику фарфоровых масс «Гамма», «Сикор», МК. для изготовления коронок и металлокерамики.
В нейтральной среде (рН 7,0) электрохимическая реакция сопровождается избытком водородных ионов, т. е. повышенной кислотностью. Это явление подтверждается и клинически: у больных, имеющих протезы из нержавеющей стали или хромокобальтового сплава, появляется чувство кислоты, жжения в полости рта. Оно может несколько стихать или усиливаться во время приема пищи (растительная пища создает кислую среду, белковая — щелочную). По-видимому, таким больным следует рекомендовать белковую пищу для нейтрализации избытка водородных ионов.
В кислотной среде происходит выраженный процесс растворения металлического протеза — анодных участков.
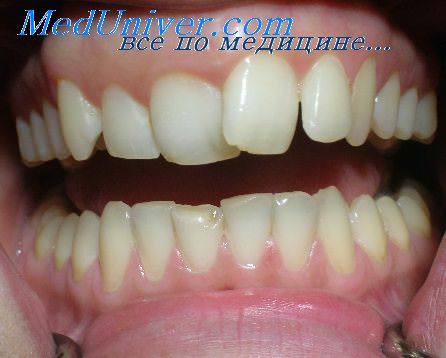
Таким образом, анодные реакции коррозии протезов характеризуются изменением электродных потенциалов вследствие перехода ионов металлов из твердой фазы (металлические протезы) в жидкую (слюну). Эти положения были подтверждены нами в эксперименте и клинике ортопедической стоматологии.
Нержавеющая сталь, предложенная в 30-х годах для зубного протезирования, испытывалась на коррозийную стойкость. Д. Н. Цитрин и В. Н. Дятлова (1934) определяли степень коррозии, учитывая потерю массы и изменение вида испытуемой детали. Потери массы были крайне незначительны и определялись весовым методом. Внешний вид образцов не менялся. На основании этих данных авторы пришли к выводу, что нержавеющая сталь является удовлетворительным сплавом для зубного протезирования.
Однако из электрохимии известно, что коррозия определяется также и качеством и количеством компонентов, выходящих в среду из испытуемых (образцов) сплавов металлов. Нами разработан и применен метод химико-спектрального анализа для определения процессов коррозии в искусственной среде. При составлении искусственной среды мы руководствовались данными литературы о химическом составе слюны человека.
Искусственную среду помещали в прибор, представляющий собой кварцевый сообщающийся сосуд, покрытый теплоизоляционным слоем для поддержания постоянной температуры. Нагревание (37°С) жидкости в сосуде осуществляли электрическим током, подведенным под теплоизоляционный слой через лабораторный автотрансформатор ТИП-1. В одном колене сосуда находилась мешалка для перемешивания и соединения с электромотором, в другом — штатив для испытуемых образцов, в основании сосуда — кран для забора проб. Сосуд закрывали пробками из фторопласта.
Общее количество искусственной среды составляло 1000 г. Для анализа брали 8 см3 испытуемой жидкости, делили на две пробы (4 см3) и определяли среднее значение. Отбор проб проводили через каждые 6 дней. Взято 15 проб, проведено 30 анализов, изучено 150 спектрограмм. Спектральный анализ выявил коррозионные изменения в испытуемой среде. Исследование на коррозию проводили и при рН среды 5,5 (максимальный сдвиг рН, возможный в полости рта), и при температуре 37° С. Для испытания на коррозию были взяты три мостовидных протеза из нержавеющей стали с припоем (масса до опыта 6,92 г, после опыта 6,86 г), потери составили 0,06 г (0,87%). Время испытания 3 мес (2100 ч). В течение этого времени определяли качественную и количественную характеристику коррозионного процесса.
При осмотре (до опыта) мостовидные протезы в местах паек вследствие образования окисных продуктов имели потемнения, наружная поверхность была отполированной, блестящей. Перед началом исследования мостовидные протезы тщательно полировали. Внутренняя поверхность коронок матовая. После опыта в местах паек коронок и промежуточной части поверхность зелено-синяя, образовалась окисная пленка в виде «наростов», после снятия которой обнаружены кратерообразные углубления («язвы»).
Механическое надламывание в этих местах привело к разлому коронки. Поверхность полированной части мостовидных протезов стала тусклой, внутри коронок появилась окисная пленка темно-желтого цвета. Эти явления можно объяснить процессом коррозии.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Коррозия мостовидных протезов. Влияние слюны на нержавеющую сталь
Продуктами электрохимических реакций являются ионы металлов (микроэлементы), поступающие в слюну из корродирующих сплавов. Динамика изменения микроэлементов состава слюны находится в прямой зависимости от степени электрохимических процессов в полости рта. Высокие концентрации микроэлементов установлены нами в слюне, лиц с аллергическим и токсическим стоматитом, вызванным протезом (400 человек) из нержавеющей стали, по сравнению с нормой (50 человек).
Наиболее выраженные колебания обнаружены в содержании железа, никеля, меди, серебра, хрома, титана.
Изменение количественного содержания микроэлементов в слюне тесно связано с процессами коррозии мостовидных протезов из нержавеющей стали. Это установлено нами при исследовании снятого паяного протеза из нержавеющей стали после работы его в полости рта. С этой целью обследовано 30 человек в возрасте от 35 до 58 лет. Первую группу составили 8 больных, у которых мостовидные протезы были сняты по причине отрыва промежуточных частей в местах пайки (10 протезов).
Во вторую группу вошло 22 больных с парестезией полости рта (16) и аллергией на металлические протезы (6). У этих больных протезы снимали после установления причинной зависимости заболеваемости от металлических конструкций. Снято и исследовано более 35 протезов. Диагноз заболевания ставился на основании данных клинических и лабораторных исследований (спектральный анализ слюны, анализ крови, аллергологические тесты).
Снятые мостовидные протезы из нержавеющей стали исследовали на сканирующем электронном микроскопе микрозондовым анализатором. В каждом протезе изучали три зоны: припой, контакт припоя с коронкой и припой с промежуточной (литой) частью. Всего исследовано 90 зон мостовидных протезов, проведено 30 спектральных анализов слюны.
При исследовании припоя у больных первой группы обнаружены сетка коррозионных трещин и межкристаллитная коррозия, что свидетельстует об одновременном действии механических напряжений и коррозионной среды. Как известно, межкристаллитная коррозия возникает при совместном действии агрессивной среды и внутренних напряжений. В полости рта протезы в значительной степени подвержены электрохимической коррозии, усиленной вследствие взаимодействия разнородных металлов (сталь — припой).
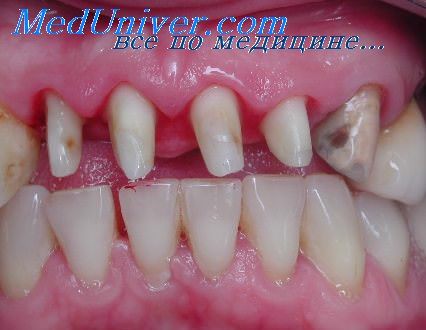
У больных этой группы отмечена большая протяженность мостовидных протезов, построенных без учета состояния пародонта опорных зубов и зубов-антагонистов. В этом случае напряжения в металле усиливают коррозионный процесс. Усилению коррозии способствует также наличие зазоров вследствие некачественного выполнения шва, вызывающих щелевую коррозию [Жук Н. Т., 1976]. Нарушение температуры пайки в интервале 450—850° С приводит к межкристаллитной коррозии. При этом по границам зерен происходит выделение карбидов .
В зоне контакта припоя с коронкой отмечается коррозионное растрескивание и механическое разрушение. В литой части мостовидного протеза (третья зона) коррозионный процесс выражен очень слабо. При осмотре больных второй группы мостовидные протезы в местах паек (припой) имели толстые, большие по площади, пористые окисные пленки. Известно, что коррозии противостоят только весьма тонкие пассивирующие слои. Мостовидные протезы после их снятия разрушали механическим способом на границе коронка — припой.
При исследовании зоны излома на сканирующем электронном микроскопе обнаружено несколько крупных пор. Поверхностные поры, сообщающиеся со средой полости рта, и поры внутри шва (припоя) содержали продукты коррозии и являлись очагом щелевой коррозии. Структура припоя пористая, поверхность ее совпадает с составляющими эвтектики серебро — медь. Однако характер распределения медных и марганцевых включений в припое не всегда равномерен: встречаются большие и малые скопления марганца, меди и участки, где включения отсутствуют. Серебряные включения распределены в припое равномерно.
Наличие в структуре отдельных микрообластей, богатых медью, характеризуется пониженным сопротивлением коррозии. Известно также, что включения обусловливают степень выраженности электрохимических реакций в полости рта, так как их электродные потенциалы различны.
Таким образом, в полости рта протезы из нержавеющей стали подвергаются коррозии. В поверхностных порах припоя наблюдается щелевая коррозия. Продукты ее (микропримеси железа, меди, марганца, серебра и др.) поступают в полость рта, что подтверждается данными спектрального анализа слюны. Процесс этот во времени является постоянным. Коррозия происходит на всей глубине припоя. В зоне, прилегающей к коронкам, припой корродирует в меньшей степени.
В литой структуре стали коррозия выражена слабо. Возникновению межкристаллитной коррозии способствуют механические напряжения в металле, значительная протяженность протезов, нарушения конфигурации паяного шва и образование зазоров.
Мостовидные протезы с межкристаллитной коррозией в полости рта способны разрушаться по шву (пайки).
Способы определения температуры без термопар
В любительской практике для определения температуры нагретой детали без измерительных приборов можно использовать несколько методов.
Первый метод "по цвету накала"
Сталь при нагреве выше 530°С излучает световые лучи различного цвета в зависимости от температуры нагрева.
| Цвет каления стали | Температура нагрева, °С | |
| Темно коричный (заметен в темноте) | 530-580 | |
| Коричнево-красный | 580-650 | |
| Темно-красный | 650-730 | |
| Темно-вишнево-красный | 730-770 | |
| Вишнево-красный | 770-800 | |
| Светло-вишнево-красный | 800-830 | |
| Светло-красный | 830-900 | |
| Оранжевый | 900-1050 | |
| Темно-желтый | 1050-1150 | |
| Светло-желтый | 1150-1250 | |
| Ослепительно-белый | 1250-1350 |
В таблице приведены цвета каления стали, соответствующие условиям обычного дневного освещения, и температуры нагрева, соответствующие этим цветам.
При определении температуры нагрева на глаз следует иметь в виду, что окружающие световые условия (дневной яркий свет, слабое искусственное или естественное освещение) в значительной степени искажают действительную температуру нагрева металла. Кроме этого, подобный метод не может быть точным в связи с индивидуальными особенностями глаз наблюдателя. При достаточном опыте ошибка не выходит за пределы 25-30 градусов
Второй метод "по цветам отпуска (побежалости)"
При нагреве металла от 200 до 300 градусов на зачищенной наждаком поверхности появляются цвета побежалости (таблица «Цвета отпуска») за счёт образования плёнок окислов различной плотности; каждая из плёнок отражает лучи только определённого цвета.
| Цвет отпуска | Температура нагрева, °С | |
| Светло-желтый | 220 | |
| Соломенно-желтый | 240 | |
| Коричнево-желтый | 255 | |
| Красно-коричневый | 265 | |
| Пурпурно-красный | 275 | |
| Фиолетовый | 285 | |
| Васильково-синий | 295 | |
| Светло-синий | 315 | |
| Серый | 330 |
Метод cпички
Спички - самое легкое и доступное средство получить огонь. Однако при помощи обычной спички можно определять температуры предварительного и сопутствующего подогрева при сварке.
Чаще всего спички делают из осины, липы, тополя или американской сосны. Надо отметить, что большинство российских предприятий делают спички из осины. Головка спички состоит из бертолетовой соли и калиевого хромпика, которые отдают кислород при высокой температуре. А для того чтобы температура не повышалась слишком сильно, в состав включают катализатор – пиролюзит. Также спичечная головка состоит из серы, клея и сульфида фосфора, которые заставляют спичку гореть. А чтобы скоростью горения можно было управлять, в массу добавляют молотое стекло, цинковые белила и железный сурик.

Для воспламенения серной головки спички необходима температура, которая превышает более, чем 180 градусов по Цельсию. Если прикоснуться головкой спички к металлу, разогретому до такой температуры, то она загорится.
Метод слюны
На самый ранних уроках по физике в школе ученики получают знания, что вода кипит при температуре 100 градусов по Цельсию. Поэтому капнув водой на разогретый металл (в крайнем случае плюнув на трубу) можно определить нагрета ли труба до температуры выше 100 градусов или нет.

Несмотря на обилие методов безинструментального контроля для их применения необходимо обладать большим опытом. Но и в любом случае все эти методы имеют достаточно высокую погрешность. Поэтому при возможности рекомендуется использовать высокоточные поверенные регистраторы температуры, термопары или пирометры.
Внепищеводные проявления гастроэзофагеальной рефлюксной болезни
Говоря о ларингофарингеальных проявлениях рефлюксной болезни, следует сказать, что изменения слизистой оболочки глотки и гортани встречаются у пациентов с ГЭРБ в 1,5-2 раза чаще, чем у пациентов без таковой. И наиболее частой формой поражения служит laryngitis posterior, так называемый «задний ларингит», при котором ларингоскопически в области задней трети голосовых связок обнаруживают отек, гиперемию, эрозии и воспалительные гранулемы. Нами было обследовано 262 больных, страдавших гастроэзофагеальной рефлюксной болезнью. Эрозивная форма рефлюксной болезни была выявлена у 27% больных и неэрозивная – у 72% больных. Патология ЛОР-органов выявлена в целом у 67% пациентов. Обратите внимание на то, что, чаще всего мы выявляли хронический фарингит – в 33% случаев. В общей массе больных хроническим фарингитом преобладали пациенты с гипертрофической формой заболевания. И, проводя лечение ингибиторами протонной помпы – здесь уже длительное лечение, в течение 12 недель – нам удалось уменьшить проявления хронического фарингита, и особенно его гипертрофической формы.
Когда мы говорим о стоматологических проявлениях рефлюксной болезни, то действие различных химических субстанций на ротовую полость широко известно, однако, соляная кислота была признана причиной в патологических изменений ротовой полости сравнительно недавно. Лишь в 1971-ом году G.Howden впервые описал патологические изменения в полости рта у больных с грыжей пищеводного отверстия диафрагмы.
Все изменения в полости рта при ГЭРБ можно разделить на поражение мягких тканей (красная кайма губ, слизистая оболочка, язык, ткани пародонта) и твердых тканей зуба, а также изменения состава ротовой жидкости. Всего нами было обследовано 88 пациентов, страдавших гастроэзофагеальной рефлюксной болезнью. Эрозивная ГЭРБ была диагностирована в 73 почти процентах случаев, и у 24% имела место неэрозивная форма заболевания. Позвольте представить несколько наших наблюдений. Отек языка, фестончатость боковых поверхностей языка, очаг десквамации на спинке языка, эрозия твердых тканей зубов вследствие повторяющихся забросов соляной кислоты. Назначение ингибиторов протонной помпы привело к положительной динамике и состояния слизистой оболочки полости рта, и динамике состояния языка. В заключение мне хотелось бы привести одно небольшое наше клиническое наблюдение. Больной 70 лет страдает инфекционно-аллергической бронхиальной астмой среднетяжелого течения в течение десяти лет. В последние шесть месяцев у него появились ночные приступы удушья. Проводилась терапия бекотидом, вентолином, и в эти же последние три месяца больной отметил периодически возникавшую изжогу, боль в подложечной области. На высоте изжоги больной самостоятельно принимал питьевую соду и жидкие антациды. Пациенту была назначена терапия ингибитором протонной помпы. На фоне терапии прекратилась изжога, уменьшилось число дневных приступов и практически полностью прекратились ночные приступы, состояние стабилизировалось. Больной уезжает в санаторий и весь свой традиционный набор препаратов для лечения бронхиальной астмы он берет с собой, а вот Ланзоптол, посчитав, что изжога прошла и все нормально, он с собой не берет. Какое-то время сохраняется последействие, но далее у больного вновь появляется изжога, вновь появляются ночные приступы, усиливаются симптомы бронхообструкции, увеличивается частота дневных приступов, увеличивается потребность в бронхолитиках. Через три дня, после того как пациент возобновил приём ингибитора протонной помпы, изжога пошла на убыль, на убыль пошли дневные приступы, прекратились ночные приступы, сократилась потребность в бронхолитиках.
Таким образом, результаты проведенного исследования свидетельствуют о необходимости тщательного обследования пациентов, страдающих гастроэзофагеальной рефлюксной болезнью врачами различных специальностей – пульмонологами, кардиологами, оториноларингологами и стоматологами для своевременной диагностики и проведения адекватной терапии внепищеводных проявлений гастроэзофагеальной рефлюксной болезни. Благодарю за внимание!
Читайте также:
