При помощи металлической химической связи образовано вещество
Обновлено: 18.05.2024
Прошу вас, пожалуйста, помогите. умоляю, это очень срочно.
Часть А. Выберите один правильный ответ.
А1. Элемент третьего периода главной подгруппы II группы Периодической системы химических элементов Д. И. Менделеева:
а) алюминий б) бериллий в) магний г) натрий
А2. Пара химических элементов, имеющих на внешнем электронном уровне по 4 электрона: а) Р и С б) Si и Ca в) C и Si г) C и N
А3.Число электронов, протонов и нейтронов в атоме фтора F:
а) p+—9, n0—10, e—19 б) p+—10, n0—9, e- —10
в) p+—10, n0—9, e- —9 г) p+—9, n0—10, e- —9
А4. Какой из перечисленных элементов проявляет наиболее ярко выраженные металлические свойства: а) алюминий б) натрий в) магний г) кремний
А5. При помощи металлической химической связи образовано вещество:
а) кислород б) поваренная соль в) медь г) вода
А6. Вещество, в котором сера проявляет степень окисления +4, имеет формулу:
а) H2S б) SO2 в) SO3 г) Na2S
А7. Ряд формул, в котором все вещества являются оксидами:
а) ZnO, ZnCl2, HCl б) SO3, MgO, CuO в) KOH, K 2O, MgO г) HNO3, P2O5, NaCl
А8. Вещество, имеющее формулу NaNO3, называется:
а) карбонат натрия б) нитрит натрия в) хлорид натрия г) нитрат натрия
А9. Уравнение реакции обмена:
а) CaO+SiO2= CaSiO3 б) FeS+ 2HCl= FeCl 2+H2 S
в) 2 KClO3 = 2KCl+ 3O2 г) Mg+ 2HCl= MgCl 2+ H2
А10. С раствором гидроксида натрия NaOH взаимодействует вещество, формула которого: а) HCl б) MgO в) KOH г) Mg
А11. Укажите правильную последовательность действий при разделении смеси поваренной соли и речного песка:
а) выпаривание, фильтрование, растворение в воде
б) фильтрование, выпаривание, растворение в воде
в) растворение в воде, выпаривание, фильтрование
г) растворение в воде, фильтрование, выпаривание
А12. Количество вещества, соответствующее 36 г воды H2O:
а)1 моль б) 2 моль в) 3 моль г) 5 моль
А13. В каком ряду расположены сернистая кислота, хлорид калия, гидроксид кальция:
а) H2SO4, H2SiO3, H3PO4 б) HNO3, K2CO3, KOH
в) HNO2, Na2S, Mg(NO3)2 г) H2SO3, KCl, Ca(OH)2
А14. В каком ряду расположены только основные оксиды:
а) SO3, SiO2, P2O5 б) H2O, K2O, KOH
в) HNO3, Na2O, Mg(NO3)2 г) Li2O, K2О, CaO
А15. Чему равна сумма коэффициентов в уравнении реакции:
Na2CO3 + HNO3 = NaNO3 + H2O + CO2 - а) 8 б) 6 в) 7 г) 5
А16. Какое из веществ взаимодействует с гидроксидом натрия:
а) соляная кислота б) алюминий в) оксид калия г) гидроксид калия
А17. Реакция взаимодействия фосфорной кислоты и гидроксида лития относится к реакциям: а) соединения б) разложения в) обмена г) замещения
А18. К окислительно-восстановительным реакциям НЕ относится реакция между:
а) соляной кислотой и карбонатом кальция б) азотной кислотой и магнием
в) углеродом и кислородом г) железом и сульфатом меди
А19. Какой объем занимает 2,5 моль О2 :
а) 560 л б) 56 л в) 5,6 л г) 22 л
А20. Какое количество вещества составляет 0,6 х 1023 молекул углекислого газа:
а) 1 моль б) 0,1 моль в) 0,01 моль г) 0,001 моль
В1. Схема распределения электронов по слоям атома химического элемента – 2,8,7. Химическая формула высшего оксида этого элемента _______________
В2. Расположите формулы веществ по типам химической связи в следующем порядке: ковалентная неполярная—ковалентная полярная—ионная—металлическая
а) Ca б) H2S в) KBr г) N2 _________________________________
В3. Установите соответствие между формулой вещества и его принадлежностью к определенному классу неорганических соединений.
Класс веществ: Формула вещества:
1) оксиды а) NaOH г) NaNO3
2) основания б)HClд)H2
3) кислоты в)CaO е) NaHCO3
В4. Установите соответствие между фрагментами уравнений в левом столбике и в правом столбиках:
1) CaCl2+ K2CO3 ® а) 2KCl + CO2 + H2O
2) SO3 + NaOH ® б) Na2SO4 + 2H2O
3) NaOH + H2SO4 ® в) Na2SO3 + 2H2O
4) K2CO3 + HCl ® г) CaCO3 + 2KCl
В5. Массовая доля кислорода в азотной кислоте HNO3 равна __________%
С1. Пронумеруйте реакции и запишите уравнения химических реакций, соответствующих схеме превращений:
Mg® MgO® MgSO4® Mg(OH)2 ® Mg(NO3)2 ® Mg
С2. Определите массу карбоната кальция CaCO3, если при его термическом разложении выделяется 45 литров углекислого газа.
При помощи металлической химической связи образовано вещество 1) алмаз 2) поваренная соль 3)медь 4) водород?
При помощи металлической химической связи образовано вещество 1) алмаз 2) поваренная соль 3)медь 4) водород.

Металлическая химическая связь в 3)

Для какого вещества характерно образование молекулярной решётки : 1?
Для какого вещества характерно образование молекулярной решётки : 1.
Поваренная соль 3.

Помогите пожалуйста?
Металлической химической связью образовано вещество -
Масса 2ммоль углекислого газа СО₂ равны :

При помощи металлической химической связи образовано вещество : а)кислород?
При помощи металлической химической связи образовано вещество : а)кислород.

4. (2 бал?
) Химическая связь является 4.
При помощи металлической химической ковалентной неполярной в веществе : связи образовано вещество : а.
Б. Поваренная соль.
Для какого из перечисленных ниже веществ харектерно образование молекулярной решетки?
Для какого из перечисленных ниже веществ харектерно образование молекулярной решетки?
А) лед б)поваренная соль в) металлическая медь.

Какой тип химической связи должен быть в металлическом водороде?
Какой тип химической связи должен быть в металлическом водороде?
Определите виды химической связи в веществах : алмаз, поваренная соль, вода, сталь?
Определите виды химической связи в веществах : алмаз, поваренная соль, вода, сталь.
Какое вещ - во образовано при помощи металлической химической связи : 1 - кислород, 2 - поваренная соль, 3 - медь, 4 - вода?
Какое вещ - во образовано при помощи металлической химической связи : 1 - кислород, 2 - поваренная соль, 3 - медь, 4 - вода.
Какая химическая связь в соединение поваренной соли?
Какая химическая связь в соединение поваренной соли?
При помощи ионной химической связи образовано вещество с формулой?
При помощи ионной химической связи образовано вещество с формулой.
Вы находитесь на странице вопроса При помощи металлической химической связи образовано вещество 1) алмаз 2) поваренная соль 3)медь 4) водород? из категории Химия. Уровень сложности вопроса рассчитан на учащихся 5 - 9 классов. На странице можно узнать правильный ответ, сверить его со своим вариантом и обсудить возможные версии с другими пользователями сайта посредством обратной связи. Если ответ вызывает сомнения или покажется вам неполным, для проверки найдите ответы на аналогичные вопросы по теме в этой же категории, или создайте новый вопрос, используя ключевые слова: введите вопрос в поисковую строку, нажав кнопку в верхней части страницы.
Я про алюминийАлюминий – легкий, прочный и пластичный металл. Это один из самых востребованных металлов, и по темпам роста потребления он давно и с большим отрывом оставил позади сталь, никель, медь и цинк. Алюминий без преувеличений можно назвать ..
Тому що рН показує ступінь концентрації катіонів гідрогену у воді, що є дуже важливим для косметики.
1. дано N(NH3) = 4. 816 * 10 ^ 23 - - - - - - - - - - - - - - - - - - - - - - - - - - - - - V(NH3) - ? N(NH3) / N(A) = V(NH3) / Vm V(NH3) = N(NH3) * Vm / N(A) = 4. 816 * 10 ^ 23 * 22. 4 / 6. 02 * 10 ^ 23 = 15. 58 L ответ 15. 58 л 2) дано m(O2)..
Соотвественно правильным ответом будет являться : 4) KCl ; 5) AgCl ; 6) NH4Cl.

Дано W(O) = 47 % - - - - - - - - - - - - - - - - E - ? Е - это неизвестный элемент W(O) = Ar(O) * n / M(X2O3) * 100% 47% = 16 * 3 / 2x + 48 * 100% 94x + 2256 = 4800 X = 27 - это алюминий Al2O3 ответ алюминий.

Напиши нормально не понятно или сфоткай.
В SO3 32 / (32 + 3 * 16) = 0, 4 или 40 %.

Реакции есть на фотографии.
4HCl + MnO2 = MnCl2 + Cl2 + 2H2O соляная кислота отдаёт в свободном виде половину имеющегося хлора. M(Cl общ. ) = 1000 * 0, 365 * 0, 9726 = 355 г масса выделившегося хлора = 355 / 2 = 177, 5 г.

Типы химической реакции соединение, разложение замещение.
© 2000-2022. При полном или частичном использовании материалов ссылка обязательна. 16+
Сайт защищён технологией reCAPTCHA, к которой применяются Политика конфиденциальности и Условия использования от Google.
Ответ - в натрий ( он же металл).
Верны ли следующие суждения?
Верны ли следующие суждения?
А. химический элемент кальций образует вещества, в которых наблюдается все типы химических связей.
Б. вещества кальций Са и нитрид кальция Са3N2 образованы соответственно с помощью металлической и ковалентной неполярной связей.
1)оба суждения верны
2)верно только А
3)верно только Б
4)оба суждения неверны.
Напишите формулы веществ, образованных элементами 2 - го периода с помощью всех типов химической связи?
Напишите формулы веществ, образованных элементами 2 - го периода с помощью всех типов химической связи.
Верны ли след сужденияA?
Верны ли след суждения
Химический элемент кальций образует вещества в которых наблюдается все типы химических связей
Вещества кальций и нитрид кальция Ca3N2 образованы соответсвтвенно с помощью металлической и ковалентной не полярной связью
Что такое металлическая химическая связь?
Что такое металлическая химическая связь.
Химическая связь при помощи которой образована первичная связь структуры белка?
Химическая связь при помощи которой образована первичная связь структуры белка.
Медь - металл, а следовательно молекулы меди соединены при помощи металлической химической связи.
Разделите названия веществ на 2 группы : неорганические вещества и органические : Вода, кислород, жиры, медь, водород, белки, поваренная соль, углеводы?
Разделите названия веществ на 2 группы : неорганические вещества и органические : Вода, кислород, жиры, медь, водород, белки, поваренная соль, углеводы.
Простыми веществами являются все вещества в группе а) кислород , вода, железо б)вода сахар поваренная соль в) углекислый газ алюминий медь гсеребро золото железо?
Простыми веществами являются все вещества в группе а) кислород , вода, железо б)вода сахар поваренная соль в) углекислый газ алюминий медь гсеребро золото железо.
На странице вопроса Какое вещ - во образовано при помощи металлической химической связи : 1 - кислород, 2 - поваренная соль, 3 - медь, 4 - вода? из категории Химия вы найдете ответ для уровня учащихся 10 - 11 классов. Если полученный ответ не устраивает и нужно расшить круг поиска, используйте удобную поисковую систему сайта. Можно также ознакомиться с похожими вопросами и ответами других пользователей в этой же категории или создать новый вопрос. Возможно, вам будет полезной информация, оставленная пользователями в комментариях, где можно обсудить тему с помощью обратной связи.
Металлическая химическая связь - характеристика, способы образования и свойства
Металлическая химическая связь характерна для металлов и их сплавов в кристаллическом состоянии. Образуется за счет обобществления валентных электронов. Для этого типа строения вещества не характерно образование направленных структурированных связей.
Следует отличать различные типы связи элементов кристаллов - металлическую, ионную и водородную, свойственную кристаллам льда.
Схема образования металлической связи на примерах
Механизм создания металлической связи предусматривает отрыв частично свободных электронов от атома с образованием катионов с положительным зарядом, формирующих “остов” кристаллической решетки и электронного облака. При этом металлический кристалл не приобретает положительного или отрицательного заряда.
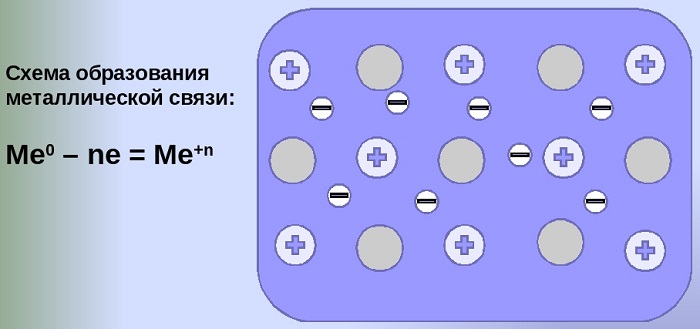
Общий случай формирования связывания металлических атомов в химии, соответствующий данному выше определению:
здесь n - число электронов, участвующих в образовании связи, как правило, от 1 до 3.
В левой части уравнения - атом металла, отдающий электроны, в правой - образовавшийся в результате ион.
Формула показывает, что в кристалле постоянно происходит присоединение и отдача электронов.
Схемы формирования связи на примере атомов различной валентности:
- K - e⁻ ⇆ K;
- Cu - 2e⁻ ⇆ Cu;
- Al - 3e⁻ ⇆ Al.
Отделяющиеся от атома электроны перемещаются на свободные валентные орбитали, которые обобществляются и позволяют всем электронам перемещаться в пределах кристалла. Отделение электронов выгодно атому с точки зрения энергетического баланса, так как позволяет сформировать электронно-стабильную оболочку.
Характерные кристаллические решетки
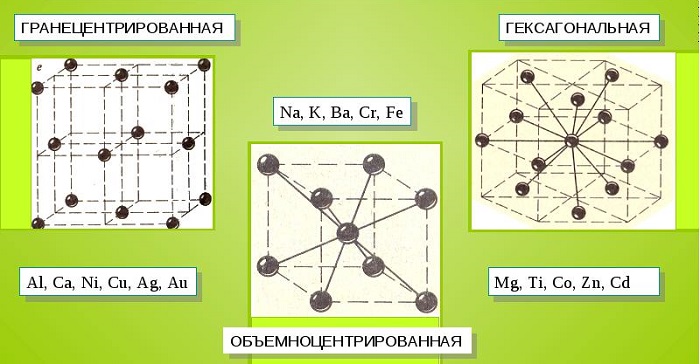
Металлические кристаллы подразделяются на 3 основных типа:
- Объемно-центрированную кубическую решетку, в которой, помимо размещения атомов в четырех вершинах куба, один из них размещается в центре объемной фигуры. Такой тип организации твердого вещества характерен для ряда металлов, включая K, Na и Li, вольфрам, хром, ниобий и др.
- Гранецентрированная кубическая решетка характеризуется расположением атомов в центре граней. Всего в ячейке задействовано 10 атомов, 4 в вершинах и 6 на гранях. Такая решетка встречается у меди, драгметаллов (серебра и золота) и металлов платиновой группы: Pd, Pt.
- Гексагональное строение решетки предполагает размещение атомов в углах и внутри 6-гранной призмы. Ячейка состоит из 15 атомов и свойственна магнию, кальцию, осмию, бериллию и ряду других металлических элементов.
Общими свойствами всех решеток являются высокая симметрия и плотная упаковка составляющих их атомов. Некоторые элементы периодической таблицы формируют уникальную структуру, например, элементарная ячейка In имеет тетрагональное строение.
Для сплавов, являющихся химическими соединениями, также характерно образование кристаллов перечисленных видов, при этом атомы каждого металла занимают определенное место в структуре.
Например, в сплаве никеля и алюминия атомы Al размещаются по углам, а атом Ni - в центре ОЦК ячейки. Свойства сплава и его структура влияют на класс прочности изделия, изготовленного из этого материала.
Физические свойства металлической связи
Физические характеристики металлических кристаллов обусловлены способностью обобществленных электронов свободно перемещаться внутри кристалла.

Характеристики, отличающие подобные вещества:
хорошая электропроводность, благодаря наличию условно свободного электронного облака;
высокая проводимость тепла;
низкая реакционная способность или инертность;
пластичность - большинство металлов можно гнуть и ковать.
Высокий уровень организации вещества обусловливает металлический блеск. Следует иметь в виду, что повышение прочности при пластической деформации и легировании приводит к образованию частично ковалентной связи.
При деформации могут возникать области повышенной прочности и низкими пластическими свойствами, похожие на вещества с ковалентной связью (например, алмаз).
Сходства и отличия металлической химической связи от ионной
Помимо рассматриваемой, металлы могут образовывать другие виды связи, включая простую ионную.
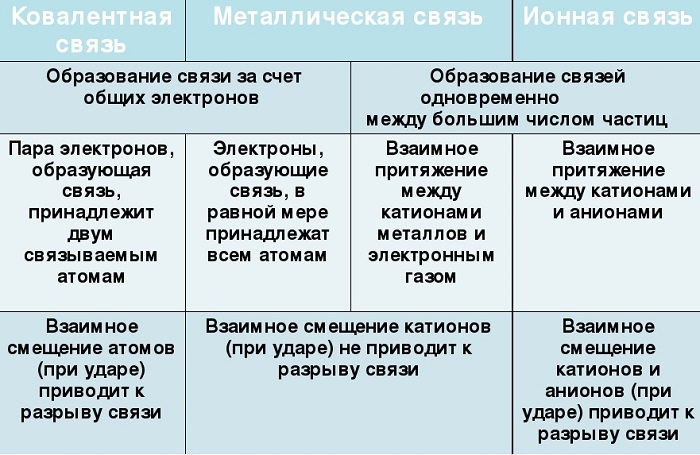
Их общие черты:
участие металлов, при этом металлическая связь формируется исключительно атомами металла, а ионная образуется между металлическим и неметаллическим элементами;
металл высвобождает электроны и становится катионом;
соединения могут существовать в кристаллической форме.
Кристаллы с ионным характером соединения отличают следующие параметры:
- В узлах размещаются как положительно, так и отрицательно заряженные ионы. Каркас металлической решетки формируют исключительно катионы.
- Узлы удерживаются за счет электростатического взаимодействия.
- При низких температурах кристаллические вещества, образованные за счет ионного взаимодействия, проявляют свойства диэлектриков (не проводят ток).
- Переход электронов с атома металла происходит на орбиты атома неметалла.
Характерный пример кристалла с ионной связью - поваренная соль, решетка которой сформирована из ионов Na⁺ и Cl⁻. Такие кристаллические вещества не обладают пластичностью и блеском.
Читайте также:
