Процесс кристаллизации расплавов металлов
Обновлено: 14.05.2024
Кристаллизация расплавов обладает рядом преимуществ по сравнению с рассмотренными выше методами разделения, например с ректификацией, экстракцией: низкие расходы энергии, возможность разделения азеотропных и близкокипящих смесей, проведения процесса при низких температурах и др. Этот процесс все шире применяется в химической технологии (в производстве удобрений, щелочей и др.) в основном для отверждения и разделения расплавов на фракции и для выращивания монокристаллов. Отметим, что между процессами кристаллизации расплавов и из растворов нет принципиального термодинамического различия. Процесс разделения кристаллизацией расплавов часто называют фракционным плавлением.
На рис. 23-14 представлена зависимость температуры t от времени τ процесса медленного нагревания твердого вещества. Из этого рисунка видно, что на кривой t = f(τ) имеется горизонтальный участок, соответствующий температуре tnл плавления. Этот участок наблюдается до тех пор, пока произойдет полное расплавление вещества и выделится теплота фазового превращения.
Отметим, что образование кристаллов в расплаве (их возникновение и рост) происходит так же, как и при кристаллизации из растворов. При этом для оценки скорости процесса вместо пересыщения используют переохлаждение.
При однократном фракционном плавлении исходную смесь вначале медленно охлаждают до полной кристаллизации. Затем образовавшуюся кристаллическую массу нагревают от температуры кристаллизации до температуры фракционирования. Полученную суспензию отфильтровывают, причем кристаллическая фаза оказывается более обогащенной высокоплавким компонентом.
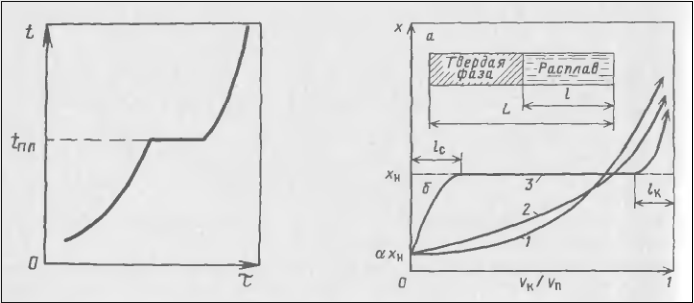
Рис. 23-14. Зависимость температуры t от времени τ нагрева твердого вещества
Рис. 23-15. Схема затвердевания вещества (а) и распределения концентраций по длине образца (б) при направленной кристаллизации (аɭ):
1-при полном перемешивании; 2-при частичном перемешивании расплава; 3 - при диффузионном переносе.
Для повышения эффективности процесса используют многократное (или многоступенчатое) фракционное плавление. Схемы многоступенчатого разделения на основе однократного фракционного плавления аналогичны схемам многоступенчатой фракционной кристаллизации (см. рис. 23-5 и 23-6). Так же аналогичен и расчет процесса фракционного плавления (см. разд. 23.4).
Процессы фракционного плавления применяют, например, для выделения нафталина из разбавленных нафтеновых фракций, разделения изомеров ксилола, опреснения воды, концентрирования водных растворов, фракционирования жиров и т.п. Для проведения процессов фракционного плавления используют вальцовые, ленточные, барабанные и другие кристаллизаторы, а также кристаллизаторы с псевдоожиженным слоем.
Направленная кристаллизация. Этот метод кристаллизации (фракционирования), как и рассмотренные выше, возможен вследствие различия равновесных составов сосуществующих фаз при переходе вещества из одного агрегатного состояния в другое. Он основан на отводе теплоты от границы раздела фаз, что вызывает направленное передвижение фронта кристаллизации вдоль очищаемого образца. Это передвижение обеспечивают медленным перемещением зон нагрева и охлаждения (рис. 23-15, а). Процесс направленной кристаллизации наиболее рационально применять для глубокой очистки небольших количеств веществ, предварительно очищенных другими методами.
Поскольку состав образующейся в процессе кристаллизации твердой фазы отличается от состава расплава, то при движении фронта кристаллизации вдоль образца происходит перераспределение примеси между обеими фазами. Отметим, что при α < 1 концентрация примеси в твердой фазе ниже, чем в расплаве, а при α>1 -выше.
Полагаем, что коэффициент диффузии в твердой фазе равен нулю, а на поверхности раздела фаз устанавливается равновесие (т.е. х = αу, где х и y-концентрации примеси соответственно в твердой фазе и расплаве). Примем также, что при перемещении в зоне расплава фронт кристаллизации вдоль образца остается плоским. Тогда уравнение материального баланса примесного компонента в процессе направленной кристаллизации в дифференциальной форме можно записать следующим образом:
где Vp и Vк - объемы соответственно расплава и твердой фазы.
Очевидно, что полный объем образца = Vp+Vк. Поскольку в уравнении (23.32) d = — dVK, то
, (23.33)
где хн - начальная концентрация примеси в образце.
При известной зависимости х =f(y) уравнение (23.33) решается аналитически. Если эта зависимость линейна (т. е. а = const), решение уравнения (23.33) принимает следующий вид:
x = ). (23.34)
Обычно сечение образца постоянно по всей его длине. В этом случае уравнение (23.34) можно записать следующим образом (рис. 23-15, а):
гдеОтметим, что уравнение (23.34) является аналогом уравнения (23.20), полученного для случая кристаллизации из растворов.
Распределение примеси по длине образца в зависимости от степени перемешивания расплава представлено на рис. 23 – 15,б.
Зонная плавка. Этот вид кристаллизационного процесса глубокой очистки веществ в отличие от направленной кристаллизации проводится (рис. 23 – 16) при медленном (со скоростью 0,5-20 см/ч) перемещении вдоль образца очищаемого вещества 1 нагревателя 4,
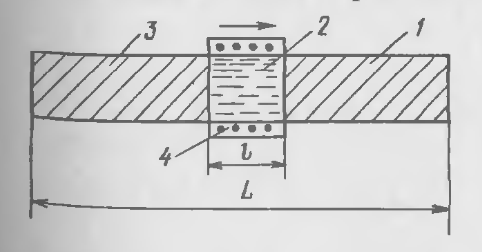
Рис. 23 – 16. Схема зонной плавки:
1 – исходный образец; 2– зона расплава; 3- зона кристаллизации после очистки, 4-нагреватель
создающею в образце зону 2 расплава длиной ɭ . По длине L образца образуются две подвижные межфазные границы. По одну из этих границ происходит плавление материала образца, по другую - его затвердевание (зона 3). При движении расплавленной зоны 2 вдоль образца вследствие различной растворимости примеси в расплаве и твердой фазе ее концентрация в образце перераспределяется.
Процесс кристаллизации расплавов металлов
Размер зерна металла сильно влияет на его механические свойства
Кристаллизация-переход легированного металла из жидкого состояния в твердое-когда расплав переходит в термодинамически более стабильное состояние с меньшей свободной энергией, свободная энергия кристалла становится меньше свободной энергии жидкой фазы.
Показано влияние температуры на свободную энергию жидкой и твердой фаз.
При температуре плавления жидкая и твердая фазы присутствуют одновременно. Реальный процесс кристаллизации происходит, когда металл переохлаждается ниже теоретической температуры кристаллизации. Это значение называется степенью гипотермии.
Тепловые кривые, характеризующие кристаллизацию чистых металлов при охлаждении с разной скоростью.
Первоначально, когда металл находится в жидком состоянии, температура системы плавно падает. При достижении температуры Tm на кривой охлаждения появляется горизонтальная область, так как отвод тепла в окружающую среду компенсируется скрытой теплотой кристаллизации, выделяющейся в процессе кристаллизации.
- В конце кристаллизации температура снова плавно падает. При медленном охлаждении степень переохлаждения мала, а кристаллизация происходит при температуре, близкой к теоретической кристаллизации temperature. As скорость охлаждения увеличивается, степень переохлаждения увеличивается, а кристаллизация происходит при низких температурах.
Чем более жидкий металл»чист», тем выше температура переохлаждения. Процесс кристаллизации начинается с образования кристаллического ядра в центре кристаллизации и продолжается процессом увеличения его количества и размеров. С увеличением степени гипотермии увеличивается количество ядер и скорость кристаллизации. Но при дальнейшем увеличении степени гипотермии скорость роста и кристаллизации ядер уменьшается.
Процесс кристаллизации может протекать только при переохлаждении металла
Рост кристаллов состоит из присоединения новых атомов из жидкой фазы к ядру.
Центр кристаллизации-Черный квадрат ядра — возникает естественным образом во время переохлаждения металла. Очень маленькие ядра неустойчивы, они возникают и растворяются. Чем больше степень гипотермии, тем более устойчиво ядро и тем меньше его критическое значение size. In кроме того, эмбрион растет в размерах, но одновременно появляется новый.
- Число ядер невелико, но кристаллы растут свободно и сохраняют правильную геометрическую форму. shape. In места, где отдельные кристаллы соприкасаются, рост отдельных граней прекращается, а грани развиваются в местах, где есть свободное пространство. liquid. As в результате кристаллы не имеют правильной геометрической формы.
Термические кривые
Такие кристаллы называются crystallites. As центр кристаллизации увеличивается, при заданном объеме образуется больше кристаллов, что приводит к уменьшению конечного размера кристалла. Однако уменьшение скорости нуклеации числа ядер при критической температуре ограничивает возможность регулирования размера за счет увеличения скорости.
- Для контроля размера частиц часто используется искусственное введение вещества, которое создает центр кристаллизации и превращает его в melt. In промышленные металлы, инородные включения, такие как включения шлака, частицы футеровки печи и оксиды металлов часто служат центром кристаллизации.
В большинстве случаев кристаллизация металла происходит с высокой скоростью, когда металл вводится в форму, и расплав кристаллизуется во время литья в форме.
Когда охлаждение металла ускоряется, кристаллы растут неравномерно. Рост ядра вдоль 1 оси в направлении максимального градиента температуры значительно превышает рост вдоль другой оси, и происходит так называемая кристаллизация дендрита.
Влияние температуры на свободную энергию
С ростом осей 4-го, 5-го высших порядков. Все промежутки, которые ранее занимал жидкий металл, постепенно заполняются-кристаллизация дендрита замедляется.
| Реферат на тему | На заказ | Образец и пример |
| Процесс кристаллизации расплавов металлов | Чаще всего кристаллизация металлов происходит с высокой скоростью (кристаллизация при заливке металла в форму, кристаллизация расплава при заливке в форму). | Когда охлаждение металла ускоряется, кристаллы растут неравномерно. |
Дендритная кристаллизация отчетливо выражается в присутствии примесей и посторонних атомов в жидком металле, дефиците усадочной оболочки, плавлении и кристаллизации реальных сплавов, заполняющих пространство поверхностного слоя.
Образовавшиеся кристаллы растут свободно, но имеют более или менее правильную геометрическую форму.
Однако, если кристаллы сталкиваются во время роста, они нарушают свою нормальную форму, так как в этих областях рост плоскости прекращается.
Кристаллизация металлов происходит с большой скоростью
Рост продолжится только в тех областях, где есть свободный доступ к liquid. As в результате кристаллы в процессе роста, изначально имеющие геометрически правильную форму, после затвердевания приобретают неправильную внешнюю форму, поэтому их называют микрокристаллами или зернами.
| Рост ядра вдоль 1 оси (в направлении максимального градиента температуры) значительно превышает рост вдоль другой оси,и происходит так называемая кристаллизация дендрита. |
| Практический рекристаллизационный отжиг составляет 600-700°С для низкоуглеродистой стали, латуни и бронзы-560 … 700°с, алюминиевый сплав-350 … 450°с, титановый сплав-550 … Он производится при температуре 750°С. |
Процесс кристаллизации протекает быстрее, и за единицу времени и за единицу объема образуется больше ядер в центре кристаллизации, а скорость их роста увеличивается.
- Чем выше скорость зарождения, тем медленнее рост, тем меньше размер кристаллов, выращенных из одного ядра, и, следовательно, тем тоньше структура металла.
Образовательный сайт для студентов и школьников
© Фирмаль Людмила Анатольевна — официальный сайт преподавателя математического факультета Дальневосточного государственного физико-технического института
Кристаллизация металлов схема и процесс
В газах нет никакой регулярности в расположении частиц, частицы движутся хаотично, и газы стремятся занять как можно больший объем. Твердые кристаллические тела имеют правильную структуру, в которой атомы и ионы находятся в узлах кристаллической решетки (так называемый ближний порядок), а отдельные ячейки и блоки находятся определенным образом относительно друг друга. В жидкости определенная ориентация приходится не на весь объем, а на относительно устойчивую группу или небольшое число атомов, образующих флуктуации. При понижении температуры стабильность колебаний возрастает,
что свидетельствует о способности расти. Таким образом, жидкость характеризуется только близким порядком атомов. Людмила Фирмаль
По мере повышения температуры твердого тела подвижность атомов в узле решетки увеличивается, амплитуда колебаний увеличивается, и при достижении определенной температуры, называемой температурой плавления, температура плавления атома из узла является важной константой, и информация о ней содержится во всех справочниках: ртуть-38,9, температура плавления до температуры плавления нержавеющей стали 3410°C При охлаждении жидкости с последующим затвердеванием наблюдается обратная картина. При охлаждении жидкости, наоборот, подвижность атома уменьшается, и атом образуется ближе к точке плавления атома, заполняя его подобно кристаллу.
Эти группы являются центрами кристаллизации или зародышем, который впоследствии увеличивает слой кристаллов. При достижении температуры плавления-затвердевания кристаллическая решетка вновь формируется, и металл доводится до твердого состояния. Переход металлов из жидкого состояния в твердое при определенной температуре называется кристаллизацией. Рассмотрены термодинамические условия кристаллизации. Энергетическое состояние любой системы складывается из энергии движения молекул, атомов, электронов, ядерной энергии, энергии упругого изгиба кристаллической решетки и других видов энергии. Харрис 1.21 неравновесные (1), метастабильные (2)и стабильные (3)Положения шариков Свободная энергия — это такая составляющая внутренней энергии, которая может быть преобразована в работу в изотермических условиях.
- Свободная энергия изменяет свое значение за счет изменения температуры, плавления, полиморфных превращений и др.:F=U-TS, где F-свободная энергия, U-полная внутренняя энергия системы, T-температура, S-энтропия. Согласно второму закону термодинамики, каждая система стремится к минимуму свободной энергии. Самопроизвольно текущий процесс идет только в том случае, если новое состояние более стабильно, то есть запас свободной энергии меньше. Например, шар стремится скатиться вниз по наклонной плоскости, уменьшая при этом свою свободную энергию. Естественно, самопроизвольный возврат шара с наклонной плоскостью вверх невозможен, так как он увеличивает свободную энергию(рис. 1.21). Процесс кристаллизации подчиняется тем же законам.
Металл затвердевает, когда твердое тело имеет меньше свободной энергии и когда жидкое состояние имеет меньше свободной энергии. Изменение свободной энергии жидкости и твердого тела с изменением температуры показано на рисунке. 1.22 при повышении температуры величина свободной энергии обоих состояний уменьшается, но закон изменения свободной энергии изменяется в зависимости от жидкого состояния вещества и состояния твердого тела. Существуют теоретические и практические температуры кристаллизации. Ts-это теория RJ=Fn или равновесной температуры кристаллизации. При такой температуре Рав- ТПЛ ТКР Присутствие металлов как в жидком, так и в твердом состоянии маловероятно.
Фактическая кристаллизация начинается только в том случае, если этот процесс термодинамически благоприятен для системы DR=RZh-RTV, что требует переохлаждения. Людмила Фирмаль
Температура, при которой фактически происходит кристаллизация, называется Рис 1.22 влияние температуры на изменение энергии Гельмгольца F (свободная энергия) жидких и твердых металлов Ирис 1.23 кривая температуры кристаллизации металла с различными скоростями охлаждения Фактическая температура кристаллизации T. разность между теоретической и фактической температурами кристаллизации называется степенью переохлаждения: at=Ts-TKR. Чем больше степень переохлаждения, тем больше разница в свободной энергии AR, тем сильнее происходит кристаллизация. На диаграмме показаны тепловые кривые, характеризующие процесс охлаждения при различных скоростях. Степень переохлаждения мала и происходит при температуре, близкой к равновесию кристаллизации, с постепенным охлаждением, соответствующим кривой 1.23..
Горизонтальная область на тепловой кривой объясняется выделением скрытой теплоты кристаллизации, которая компенсирует тепловыделение. По мере увеличения скорости охлаждения (кривые v2, v3) степень переохлаждения возрастает, и процесс кристаллизации протекает при постоянно понижающейся температуре. Помимо скорости охлаждения, степень переохлаждения зависит от чистоты металла. Чем чище металл, тем выше степень переохлаждения. Поскольку переохлаждение до фактической температуры кристаллизации необходимо во время затвердевания, перегрев происходит во время плавления до тех пор, пока не будет достигнута фактическая температура плавления. Д. К.
Даже в Черновцах процесс кристаллизации состоит из 1)зарождения центров кристаллизации;2) роста кристаллов из этих центров. При температуре, близкой к температуре затвердевания, в жидком металле образуется небольшая группа атомов, называемых колебаниями, и атомы заполняются таким же образом, как и твердые кристаллы. Из некоторых таких колебаний образуются зародыши, или центры кристаллизации. По мере увеличения степени переохлаждения увеличивается число центров кристаллизации, образующихся за единицу времени. Кристаллы начинают расти вокруг образовавшихся центров кристаллизации. В то же время в жидкой фазе образуется новый центр кристаллизации. Увеличение общей массы затвердевшего металла происходит за счет появления новых центров кристаллизации и роста существующих.
Схема последовательных стадий процесса коагуляции показана на рисунке. 1.24, а-Г. 43A5 рисунок. 1.24 схема кристаллизации металла — *Х0 Четыре.- Х: 8г Взаимный рост кристаллов объясняет неправильную форму частиц. Настоящие твердые кристаллы неправильной формы называются кристаллитами. Скорость полной кристаллизации зависит от хода обоих элементарных процессов. Она определяется скоростью зарождения центров кристаллизации (NW) и скоростью роста (CP) кристаллов из этих центров(рис. 1.25). Величины СЗ и СР зависят от степени переохлаждения. При равновесной температуре=0 и Sz=O, CP=0. С увеличением Ат разница в свободной энергии AR=RZh-RTV увеличивается, растет с хорошей степенью подвижности атомов Sz и CP и достигает максимума. Последующее уменьшение Sz и CP объясняется уменьшением подвижности атома с уменьшением температуры.
При низких значениях коэффициента диффузии перегруппировка атомов жидкости в твердую кристаллическую решетку затруднена. При очень сильном переохлаждении NW и CP равны нулю, жидкость не кристаллизуется, а превращается в аморфное тело. В реальных металлах, как правило, реализуются только восходящие ветви кривых NW и SR, а с ростом at скорость обоих процессов возрастает. Ранее, если аморфное состояние достигалось только для солей, силикатов, органических веществ, то с помощью специальной технологии можно добиться высокой скорости охлаждения (более 106°С/С) и высокой температуры стекла металла.
Металл в стеклянном состоянии характеризуется особыми физико-механическими свойствами. Ядрами кристаллизации могут быть основные металлы, примеси, колебания в атомах различных твердых тел. Первый- Т. » Степень переохлаждения — это температура В одних случаях образуется однородный эмбрион, в других-гетерогенный. Возникновение однородного центра кристаллизации требует значительных энергозатрат. Для того чтобы эмбрион обладал достаточной термодинамической и физической силой, необходимо соответствовать- Рис 1.25 влияние степени переохлаждения на нуклеацию и скорость роста кристаллов Ирис 1.26, энергия Гельмгольца изменяется в зависимости от размера эмбриона В случае критического размера ГК.
Изменение свободной энергии при равномерном зарождении центров кристаллизации описывается формулой AF=-4/Zpg3&.ФГ++4lg2st, где\ФГ является изменение свободной энергии объема, и является свободной поверхностной энергии. Энергия, определяемая приведенной зависимостью, включает в себя затраты на появление зародыша и формирование интерфейса. Изменение энергии отрицательно, если процесс кристаллизации происходит при уменьшении свободной энергии, и положительно, если энергия системы увеличивается. Графически эта связь имеет вид, показанный на рисунке. Если зародыш 1,26 G0, если g=GK, так как AF положительна и ее значение увеличивается.
С увеличением Ат в случае заливки жидкого металла в холодную металлическую форму скорость зарождения возрастает, и образуется большое количество мелких кристаллов. Размер частиц определяется не только степенью переохлаждения. Важную роль играет нагрев металла и температура отливки, ее химический состав, в частности, наличие примесей. В практических условиях самопроизвольное образование кристаллов в жидких металлах затруднено. Источниками образования зародыша являются различные твердые частицы, такие как неметаллические включения, оксиды, продукты раскисления. Чем больше примесей, тем больше Центр, тем лучше зерно. Иногда в металлы специально вводимые вещества при кристаллизации способствуют измельчению зерен. Эта операция называется изменением.
С введением магниевого сплава зерна магния 45 минут 1.27 дендритная кристаллическая фигура (Д. К. Для Чернова) Он уменьшается более чем в 10 раз: от 0,2-0,3 мм до 0,01-0,02 мм. В кристаллизации реальных слитков и отливок направление тепловыделения играет важную роль. Кристаллизация начинается со стенок кристаллизатора или пресс-формы. В направлении рассеивания тепла, то есть перпендикулярно стенке кристаллизатора, кристаллы растут быстрее, чем в другом направлении. В этом случае формируется первичная ось. При этом по краям их находятся начало и рост перпендикулярной им оси вторичной, затем третьей, etc. as в результате образуются разветвленные дендриты, называемые дендритами(рис. 1.27).
Так как при затвердевании происходит так называемая селективная кристаллизация, то есть, прежде всего, границы зерен более обогащаются примесями, так как затвердевает более чистый металл. Неоднородность химического состава в дендритах называется разжижением дендритов. В большей степени, чем другие элементы, углерод, сера, фосфор подвержены разжижению. Структура слитка тихой стали раковина усадка частиц (дендритов), получаемых в стальных слитках, может иметь различные формы, размеры и ориентации. Структура стального слитка восходит к 1878 году. К. впервые описан Черновым. Схема структуры слитка из нержавеющей стали показана на рисунке. 1.28 структура слитка состоит из внешней мелкозернистой зоны I, зоны 11 столбчатых кристаллов и зоны 111 равноосных кристаллов.
Внешняя тонкая область состоит из мелких кристаллов, которые не ориентированы в пространстве. Рис 1.28 структура слитка и образование стали вызвано резким перепадом температур: холодная стенка жидкого металла-мельница. Металл в этой зоне сильно переохлаждается, образуется большое количество кристаллических центров, которые приобретают мелкозернистую структуру. После образования кортикальной зоны изменяется состояние теплоотвода, уменьшается градиент температуры соседних слоев жидкого металла, уменьшается степень переохлаждения. В результате направления отвода тепла от относительно небольшого числа центров кристаллизации, то есть перпендикулярно стенкам кристаллизатора, столбчатые кристаллы начинают расти, образуя вторую зону.
Их развитие сбоку подавляется соседними дендритами. Третья зона-зона равноосных кристаллов. В центре слитка отсутствует удельное направление тепловыделения. Здесь бактерии обычно представляют собой различные мелкие твердые частицы, которые выталкиваются в центр слитка во время кристаллизации. Очень важно относительное распределение столбчатых и равноосных зон в объеме слитка. В зоне столбчатых кристаллов металл более плотный, но на стыке он имеет мало прочности. Кристаллизация, в которой соединяются зоны столбчатых кристаллов, называется транскрипционной кристаллизацией.
Для цветных металлов токарная обработка полезна, так как металл становится плотнее, а его высокие пластические трещины не образуются при деформации. Поскольку иногда трещины образуются на стыке двух кристаллов во время деформации, переходная кристаллизация стали нежелательна. Основными дефектами слитков являются усадка оболочки, усадочная пористость и разжижение. Усадочная пористость обычно формируется вблизи усадочной оболочки и вдоль оси слитка. Образование усадочных оболочек и усадочной пористости обусловлено тем, что все металлы, кроме висмута, имеют меньший удельный объем в твердом состоянии, чем в жидком.
2. Процесс кристаллизации расплавов металлов
Кристаллизация — переход металла (сплава) из жидкого состояния в твердое — происходит в условиях, когда расплав переходит к термодинамически более устойчивому состоянию с меньшей свободной энергией (свободная энергия кристалла меньше свободной энергии жидкой фазы).
Влияние температуры на свободную энергию жидкой (Gж) и твердой фазы (Gт) показано на рис. 1а.
При температуре плавления Тпл жидкая и твердая фазы существуют одновременно. Реальный процесс кристаллизации протекает при переохлаждении металла ниже теоретической температуры кристаллизации Тпл. Величина ∆Т= Тпл - Ткр называется степенью переохлаждения.
Термические кривые, характеризующие процесс кристаллизации чистых металлов при охлаждении с разной скоростью, приведены на рис. 1 б (v— скорость охлаждения, v1 < v2 < v3).
Вначале, когда металл находится в жидком состоянии, температура системы уменьшается плавно. При достижении температуры Тпл на кривой охлаждения появляется горизонтальная площадка, так как отвод теплоты в окружающую среду компенсируется выделяющейся при кристаллизации скрытой теплотой кристаллизации.
По окончании кристаллизации температура вновь уменьшается плавно. При медленном охлаждении (v1) степень переохлаждения мала, и кристаллизация протекает при температуре, близкой к теоретической температуре кристаллизации Тпл. С увеличением скорости охлаждения степень переохлаждения возрастает, и кристаллизация происходит при более низких температурах.
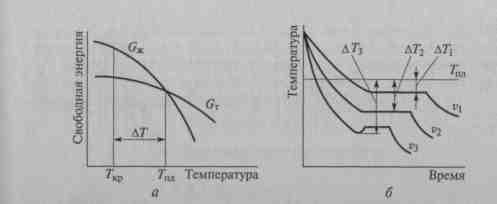
Рисунок 1. Охлаждение расплава и начало кристаллизации
а — изменение свободной энергии (G) в жидком (G Ж) и твердом (G т) состоянии в зависимости от температуры: Ткр — температура начала кристаллизации; Тпл — температура, при которой жидкая и твердая фазы существуют одновременно; ∆T — степень переохлаждения; б — кривые охлаждения металлов при кристаллизации: ∆T1, ∆T2, ∆T3 — степень переохлаждения при скорости охлаждения v1, v2, v3 соответственно.
Чем «чище» жидкий металл, тем выше температура переохлаждения. Процесс кристаллизации начинается с образования кристаллических зародышей (центров кристаллизации) и продолжается в процессе роста их числа и размеров. С повышением степени переохлаждения увеличиваются число зародышей и скорость кристаллизации. Но при дальнейшем повышении степени переохлаждения скорость роста зародышей и скорость кристаллизации уменьшаются.
Рост кристаллов заключается в присоединении к зародышам все новых атомов из жидкой фазы (рис. 2 а). Центры кристаллизации — зародыши (черные квадраты) — самопроизвольно возникают при переохлаждении металла. Очень маленькие зародыши неустойчивы, возникнув, они растворяются. Чем больше степень переохлаждения, тем устойчивее зародыши, тем меньше их критический размер. Далее зародыши увеличиваются в размере, одновременно появляются новые зародыши.
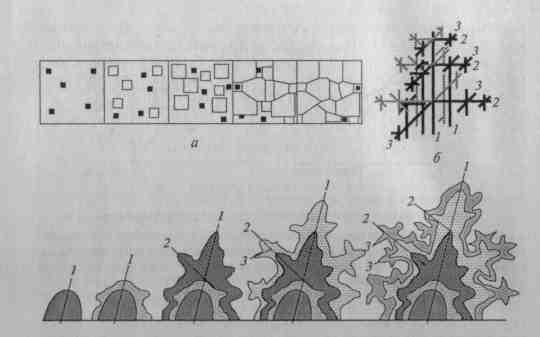
Пока число зародышей невелико, кристаллы растут свободно и сохраняют правильную геометрическую форму. В местах соприкосновения отдельных кристаллов рост их отдельных граней прекращается, развиваются грани в тех местах, где есть свободная жидкость. В результате кристаллы не имеют правильной геометрической формы. Такие кристаллы называются кристаллитами. Чем больше центров кристаллизации, тем больше образуется кристаллов в данном объеме, тем мельче окончательный размер кристаллов. Однако уменьшение скорости зарождения числа зародышей при критических температурах ограничивает возможность регулирования их размера повышением скорости охлаждения. Рис. 2. Схема кристаллизации металла
С целью регулирования размеров зерен часто применяют искусственное введение в расплав веществ, создающих центры кристаллизации (модифицирование). В технических металлах в качестве центров кристаллизации часто выступают инородные включения (например, шлаковые включения, частички футеровки печи, оксиды металлов).
а — схема роста кристаллов; б — структура дендрита; в — схема образования дендрита; ■ — зародыши; 1, 2, 3 — оси кристаллизации.
В большинстве случаев кристаллизация металлов происходит с большой скоростью (кристаллизация при заливке металла в изложницу, кристаллизация расплава при литье в металлические формы). При ускоренном охлаждении металла кристаллы растут неравномерно. Рост зародышей по одной из осей (в направлении наибольшего градиента температур) значительно опережает рост по другим осям, происходит так называемая дендритная кристаллизация.
Д.К.Чернов, описывая рост дендрита (рис. 2 б), ввел понятие «порядок осей кристаллизации». После образования зародыша его развитие (рис. 2 в) идет в направлении наибольшего градиента температур (ось первого порядка). Увеличение размеров осей первого порядка происходит не только в длину, одновременно увеличивается и ее ширина. В дальнейшем от осей первою порядка под определенными углами начинают расти новые оси, называемые осями второго и третьего порядка.
По мере роста осей более высокого порядка (четвертого, пятого и т.д.) постепенно заполняются все промежутки, ранее занятые жидким металлом, — дендритная кристаллизация замедляется.
Дендритная кристаллизация отчетливо выражена в условиях недостатка жидкого металла для заполнения пространства (поверхностные слои, усадочная раковина) и при наличии примесей и посторонних атомов в расплаве (кристаллизация реальных сплавов).
Процесс кристаллизации металлов
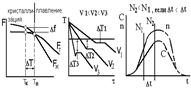
При температуре Тп величины свободных энергий жидкого и твердого состояния равны. Процесс кристаллизации протекает при температуре, меньшей Тп. Для начала затвердевания необходимо переохлаждение (разность энергий). Переохлаждение тем больше, чем больше скорость изменения.
Процесс кристаллизации происходит в два этапа: образование зародышей кристаллов; рост образовавшихся кристаллов.
В реальных металлах центрами кристаллизации являются тугоплавкие частицы и стенки литейной формы.
В чистых металлах центрами кристаллизации служат области с дальним порядком расположения атомов (кластеры), т.е. их строение близко к строению кристаллической решетки.
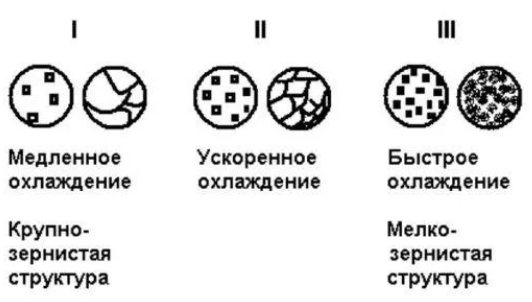
Чем больше скорость охлаждения (степень переохлаждения), тем более мелкозернистая структура образуется. Если скорость охлаждения порядка 10 5 -10 6 градусов в секунду, получается аморфная структура.
5.Строение металлического слитка. Особенности строения литого и деформированного металла.
Кристаллизация стального слитка идет в три стадии. Сначала на поверхности слитка образуется зона мелких кристаллов за счет влияния холодных стенок формы, которые обеспечивают в начальный момент времени высокую скорость охлаждения. Затем растут большие кристаллы, вытянутые по направлению отвода теплоты (столбчатые кристаллы). В середине слитка, где наблюдается наименьшая степень переохлаждения, образуются большие равновесные кристаллы. При некоторых условиях (перегретый жидкий металл, малое содержание примесей) зона крупных равновесных кристаллов почти исчезает. Структура слитка состоит практически из одних столбчатых кристаллов - транскристаллическая.
Зона столбчатых кристаллов обладает наибольшей плотностью, но в местах стыка столбчатых кристаллов собираются нерастворимые примеси, и такие слитки часто расьтрескиваются при обработке давлением.
В верхней части слитка, затвердевающей в последнюю очередь, концентрируется усадочная раковина. Там содержится много количества усадочных пор. Слиток имеет неоднородный состав. По направлению от поверхности к центру и снизу вверх увеличивается концентрация углерода и вредных примесей: серы и фосфора. Химическая неоднородность по отдельным зонам слитка называется зональной ликвацией. Она отрицательно влияет на механические свойства.
Пластическая деформация металлов и сплавов как тел поликристаллических, имеет некоторые особенности по сравнению с пластической деформацией монокристалла. Деформация поликристаллического тела складывается из деформации отдельных зерен и деформации в приграничных объемах.
Плоскости скольжения зерен произвольно ориентированны в пространстве, поэтому под влиянием внешних сил напряжения в плоскостях скольжения отдельных зерен будут различны. Деформация начинается в отдельных зернах, в плоскостях скольжения которых возникают максимальные касательные напряжения. Соседние зерна будут разворачиваться и постепенно вовлекаться в процесс деформации. Деформация приводит к изменению формы зерен: зерна получают форму, вытянутую в направлении наиболее интенсивного течения металла (поворачиваются осями наибольшей прочности вдоль направления деформации.
Металл приобретает волокнистое строение. Волокна с вытянутыми вдоль них неметаллическими включениями являются причиной неодинаковости свойств вдоль и поперек волокон. Одновременно с изменением формы зерен в процессе пластической деформации происходит изменение ориентировки в пространстве их кристаллической решетки.
Деформированный металл находится в неравновесном состоянии. Переход к равновесному состоянию связан с уменьшением искажений в кристаллической решетке, снятием напряжений, что определяется возможностью перемещения атомов.
При повышении температуры металла в процессе нагрева после пластической деформации диффузия атомов увеличивается и начинают действовать процессы разупрочнения, приводящие металл в более равновесное состояние – возврат и рекристаллизация.
Возврат. Небольшой нагрев вызывает ускорение движения атомов, снижение плотности дислокаций, устранение внутренних напряжений и восстановление кристаллической решетки
Рекристаллизация – процесс зарождения и роста новых недеформированных зерен при нагреве наклепанного металла до определенной температуры.
Нагрев металла до температур рекристаллизации сопровождается резким изменением микроструктуры и свойств. Нагрев приводит к резкому снижению прочности при одновременном возрастании пластичности. Также снижается электросопротивление и повышается теплопроводность.
1 стадия – первичная рекристаллизация (обработки) заключается в образовании центров кристаллизации и росте новых равновесных зерен с неискаженной кристаллической решеткой. Новые зерна возникают у границ старых зерен и блоков, где решетка была наиболее искажена. Количество новых зерен постепенно увеличивается и в структуре не остается старых деформированных зерен.
Движущей силой первичной рекристаллизации является энергия, аккумулированная в наклепанном металле. Система стремится перейти в устойчивое состояние с неискаженной кристаллической решеткой.
2 стадия – собирательная рекристаллизация заключается в росте образовавшихся новых зерен.
Движущей силой является поверхностная энергия зерен. При мелких зернах поверхность раздела большая, поэтому имеется большой запас поверхностной энергии. При укрупнении зерен общая протяженность границ уменьшается, и система переходит в более равновесное состояние.
Основными факторами, определяющими величину зерен металла при рекристаллизации, являются температура, продолжительность выдержки при нагреве и степень предварительной деформации
С повышением температуры происходит укрупнение зерен, с увеличением времени выдержки зерна также укрупняются. Наиболее крупные зерна образуются после незначительной предварительной деформации 3…10 %. Такую деформацию называют критической. И такая деформация нежелательна перед проведением рекристаллизационного отжига.
Практически рекристаллизационный отжиг проводят дпя малоуглеродистых сталей при температуре 600…700 o С, для латуней и бронз – 560…700 o С, для алюминевых сплавов – 350…450 o С, для титановых сплавов – 550…750 o С.
Читайте также:
