Реакция глюкозы с активными металлами
Обновлено: 19.09.2024
В молекулах спиртов, помимо связей С–С и С–Н, присутствуют ковалентные полярные химические связи О–Н и С–О.
| Электроотрицательность кислорода (ЭО = 3,5) больше электроотрицательности водорода (ЭО = 2,1) и углерода (ЭО = 2,4). |
Электронная плотность обеих связей смещена к более электроотрицательному атому кислорода:
| Атом кислорода в спиртах находится в состоянии sp 3 -гибридизации. |
В образовании химических связей с атомами C и H участвуют две 2sp 3 -гибридные орбитали, а еще две 2sp 3 -гибридные орбитали заняты неподеленными электронными парами атома кислорода.
Поэтому валентный угол C–О–H близок к тетраэдрическому и составляет почти 108 о .
Водородные связи и физические свойства спиртов
Спирты образуют межмолекулярные водородные связи. Водородные связи вызывают притяжение и ассоциацию молекул спиртов:
Поэтому этиленгликоль – жидкость с относительно высокой температурой кипения.
Водородные связи образуются не только между молекулами спиртов, но и между молекулами спиртов и воды. Поэтому спирты очень хорошо растворимы в воде. Молекулы спиртов в воде гидратируются:
| Чем больше углеводородный радикал, тем меньше растворимость спирта в воде. Чем больше ОН-групп в спирте, тем больше растворимость в воде. |
Химические свойства этиленгликоля
Спирты – органические вещества, молекулы которых содержат, помимо углеводородной цепи, одну или несколько гидроксильных групп ОН.
1. Кислотные свойства
| Спирты – неэлектролиты, в водном растворе не диссоциируют на ионы; кислотные свойства у них выражены слабее, чем у воды. |
1.1. Взаимодействие с раствором щелочей
При взаимодействии этиленгликоля с растворами щелочей реакция практически не идет, т. к. образующийся алкоголят почти полностью гидролизуется водой.
Равновесие в этой реакции так сильно сдвинуто влево, что прямая реакция не идет. Поэтому этиленгликоль не взаимодействует с растворами щелочей.
1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
Этиленгликоль взаимодействует с активными металлами (щелочными и щелочноземельными).
| Например, этиленгликоль взаимодействует с калием с образованием гликолята калия и водорода . |
Алкоголяты под действием воды полностью гидролизуются с выделением спирта и гидроксида металла.
2. Реакции замещения группы ОН
2.1. Взаимодействие с галогеноводородами
При взаимодействии этиленгликоля с галогеноводородами группы ОН замещаются на галоген и образуются дигалогеналкан.
| Например, этиленгликоль реагирует с бромоводородом. |
2.2. Этерификация (образование сложных эфиров)
Многоатомные спирты вступают в реакции с карбоновыми кислотами, образуя сложные эфиры.
| Например, этиленгликоль реагирует с уксусной кислотой с образованием эфира: |

2.4. Взаимодействие с кислотами-гидроксидами
Этиленгликоль взаимодействует и с неорганическими кислотами, например, азотной или серной.
| Например, при взаимодействии этиленгликоля с азотной кислотой образуется нитроэтиленгликоль : |
3. Дегидратация
В присутствии концентрированной серной кислоты от спиртов отщепляется вода. При высокой температуре (180 о С) протекает внутримолекулярная дегидратация этиленгликоля и образуется соответствующий ацетальдегид.
4. Окисление этиленгликоля
Реакции окисления в органической химии сопровождаются увеличением числа атомов кислорода (или числа связей с атомами кислорода) в молекуле и/или уменьшением числа атомов водорода (или числа связей с атомами водорода).
Типичные окислители — оксид меди (II), перманганат калия KMnO4, K2Cr2O7, кислород в присутствии катализатора.
4.1. Окисление оксидом меди (II)
Этиленгликоль можно окислить оксидом меди (II) при нагревании. При этом медь восстанавливается до простого вещества.

4.2. Окисление кислородом в присутствии катализатора
Этиленгликоль можно окислить кислородом в присутствии катализатора (медь, оксид хрома (III) и др.).

4.3. Жесткое окисление
При жестком окислении под действием перманганатов или соединений хрома (VI) этиленгликоль окисляется до щавелевой кислоты.
| Например, при взаимодействии этиленгликоля с перманганатом калия в серной кислоте образуется щавелевая кислота |
4.4. Горение этиленгликоля
При сгорании этиленгликоля образуется углекислый газ и вода и выделяется большое количество теплоты.
5. Дегидрирование этаниленгликоля
При нагревании спиртов в присутствии медного катализатора протекает реакция дегидрирования.
| Например, при дегидрировании этиленгликоля образуется этандиаль |
Получение этиленгликоля
1. Щелочной гидролиз дигалогеналканов
При взаимодействии дигалогеналканов с водным раствором щелочей образуются двухатомные спирты. Атомы галогенов в дигалогеналканах замещаются на гидроксогруппы.
| Например, при нагревании 1,2-дихлорэтана с водным раствором гидроксида натрия образуется этиленгликоль |
2. Гидрирование карбонильных соединений
| Например, при гидрировании этандиаля образуется этиленгликоль |
О=CН-CH=O + 2H2 → CH2(OH)-CH2OH
3. Гидролиз сложных эфиров
При гидролизе сложных эфиров этиленгликоля и карбоновых кислот образуются этиленгликоль и карбоновая кислота.
4. Мягкое окисление алкенов
Мягкое окисление протекает при низкой температуре в присутствии перманганата калия. При этом раствор перманганата обесцвечивается.
В молекуле алкена разрывается только π-связь и окисляется каждый атом углерода при двойной связи.
Химия. 10 класс
В молекуле глюкозы имеются альдегидная и гидроксильные группы, поэтому для неё характерны химические свойства как альдегидов, так и многоатомных спиртов.
Сначала рассмотрим реакции с участием альдегидной группы молекулы глюкозы. Поскольку альдегидная группа имеется только в линейной форме глюкозы, в уравнениях реакции будем записывать формулу глюкозы в линейной форме.
1. Присоединение водорода. Восстановление
Альдегидная группа глюкозы может присоединить молекулу водорода. Эта реакция сопровождается разрывом π-связи между атомами углерода и кислорода альдегидной группы:
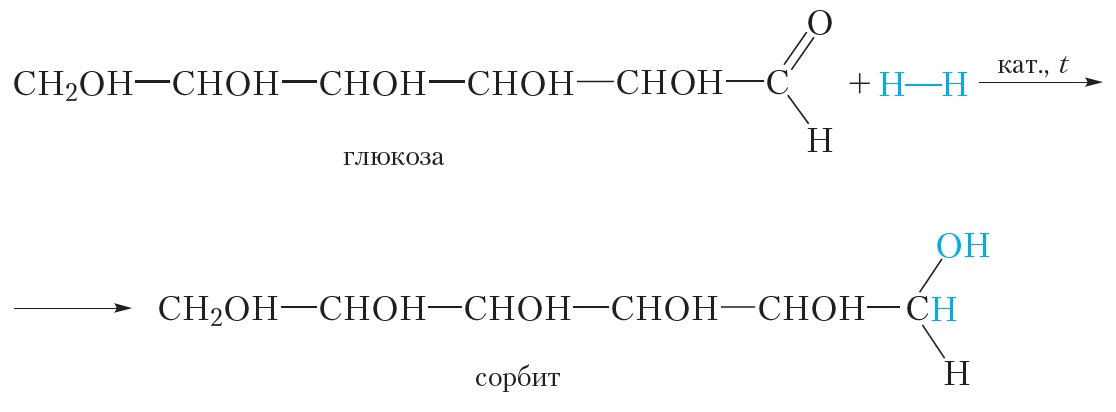
Образующийся шестиатомный спирт называется сорбит. Он имеет сладкий вкус и используется в качестве заменителя сахара.
В результате присоединения водорода молекула глюкозы восстанавливается, поэтому реакцию с водородом также называют реакцией восстановления.
2. Окисление аммиачным раствором оксида серебра
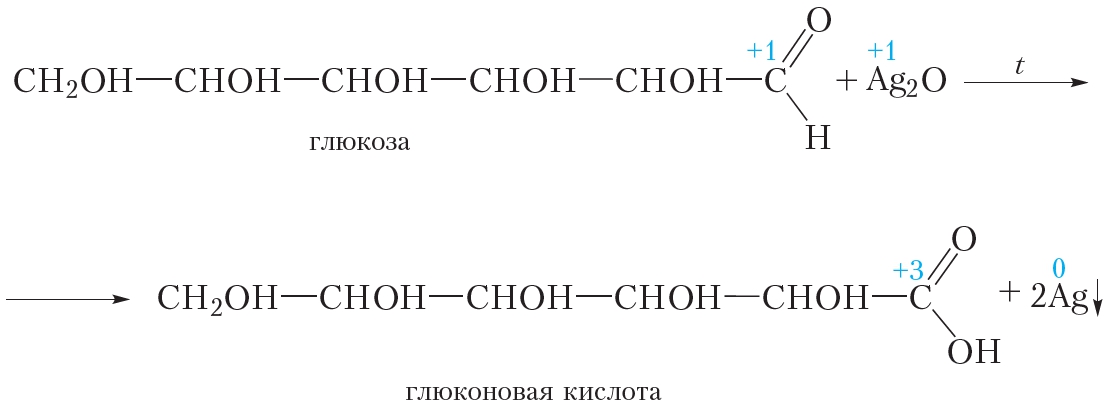
Глюкоза даёт качественную реакцию на альдегиды, восстанавливая серебро из аммиачного раствора оксида серебра (реакция «серебряного зеркала»). При этом альдегидная группа молекулы глюкозы окисляется до карбоксильной:
В результате реакции образуется глюконовая кислота.
3. Взаимодействие с гидроксидом меди(II)
Взаимодействие с гидроксидом меди(II) является качественной реакцией как на многоатомные спирты, так и на альдегиды. Глюкоза проявляет свойства как многоатомных спиртов, так и альдегидов. Рассмотрим, что будет наблюдаться при взаимодействии глюкозы с гидроксидом меди(II). Смешаем в пробирке растворы щёлочи и сульфата меди(II). При этом выпадает голубой осадок гидроксида меди(II):
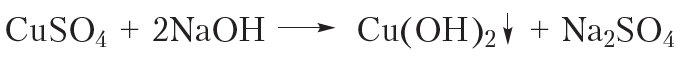
При добавлении в пробирку водного раствора глюкозы происходит растворение гидроксида меди(II) и образуется прозрачный раствор васильково-синего цвета. Такой же эффект наблюдается при действии многоатомных спиртов на свежеосаждённый гидроксид меди(II). Как и в случае многоатомных спиртов, растворение гидроксида меди(II) при взаимодействии с глюкозой происходит вследствие образования растворимого в воде комплексного соединения (§ 25). Эта реакция является качественной реакцией на многоатомные спирты.
В то же время взаимодействие глюкозы с гидроксидом меди(II) имеет интересную особенность, которая позволяет легко отличить глюкозу от многоатомных спиртов. Нагреем содержимое пробирки на пламени спиртовки. В случае многоатомного спирта васильково-синий раствор закипит, но окраска его не изменится. Проба с глюкозой ведёт себя совершенно иначе. При нагревании в пробирке сначала образуется жёлтый осадок, который затем краснеет. Образующаяся смесь напоминает морковный сок. Уравнение протекающей реакции:
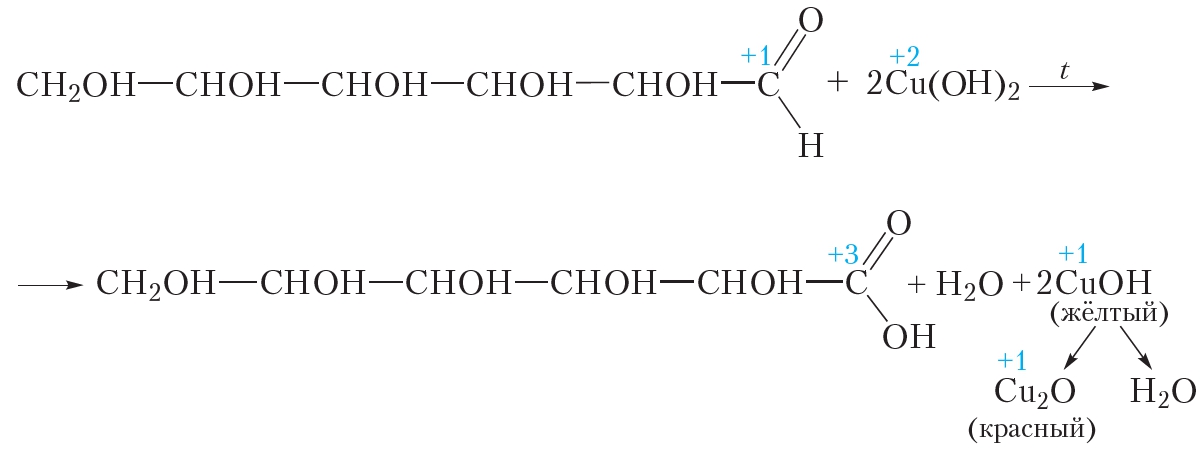
Красный осадок представляет собой оксид меди(I) Cu2O. В данной реакции гидроксид меди(II) восстанавливается до оксида меди(I), а глюкоза окисляется до глюконовой кислоты.
В описанном эксперименте глюкоза сначала проявляет свойства многоатомного спирта, растворяя свежеосаждённый гидроксид меди(II). При нагревании смеси происходит реакция уже с альдегидной группой глюкозы — ионы меди(II) окисляют её до карбоксильной группы.
4. Спиртовое брожение
Некоторые микроорганизмы, например дрожжи, обладают способностью преобразовывать глюкозу в этиловый спирт. Этот процесс называется спиртовым брожением глюкозы:
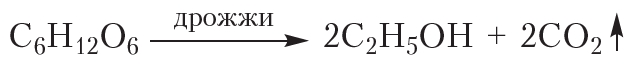
Молочнокислые бактерии обладают способностью преобразовывать глюкозу в молочную кислоту. Этот процесс называется молочнокислым брожением глюкозы:

Молочная кислота является замечательным природным консервантом. Она образуется при скисании молока и содержится в кисломолочных продуктах (простокваша, кефир, творог и др.) которые, в отличие от свежего молока, могут храниться достаточно долго. Наличием молочной кислоты обусловлен кислый вкус этих продуктов. Молочная кислота образуется также в процессах квашения капусты, мочения яблок, силосования зелёных кормов, она препятствует протеканию процессов гниения и позволяет сохранять продукты долгое время.
Глюкоза широко встречается в природе в составе многих овощей и фруктов. Особенно много её в винограде, поэтому глюкозу часто называют виноградным сахаром.
Глюкоза используется в медицине как лекарственный препарат, в частности при ослаблении и интоксикации организма.
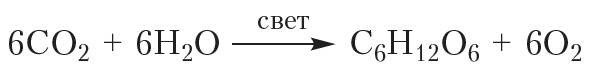
В природе глюкоза образуется в зелёных растениях в процессе фотосинтеза:
В промышленности глюкозу получают из целлюлозы и крахмала, подробнее об этом — в следующих параграфах.
В молекуле глюкозы имеются альдегидная и гидроксильные группы, поэтому для неё характерны химические свойства как альдегидов, так и многоатомных спиртов.
Глюкоза даёт качественную реакцию на многоатомные спирты — образование раствора васильково-синего цвета при взаимодействии со свежеосаждённым гидроксидом меди(II).
Глюкоза даёт качественные реакции на альдегидную группу, окисляясь до глюконовой кислоты при нагревании с гидроксидом меди(II) или аммиачным раствором оксида серебра.
Как и альдегиды, глюкоза присоединяет водород. При этом происходит восстановление глюкозы и образуется шестиатомный спирт сорбит.
Под действием бактерий глюкоза подвергается спиртовому брожению с образованием этанола и молочнокислому брожению с образованием молочной кислоты.
Глюкоза
Глюкоза (С6Н12О6) – представляет собой кристаллы белого цвета, сладкие на вкус и хорошо растворимые в воде.
Молекулы глюкозы могут существовать в линейной (альдегидоспирт с пятью гидроксильными группами) и циклической форме (α- и β-глюкоза), причем вторая форма получается из первой при взаимодействии гидроксильной группы при 5-м атоме углерода с карбонильной группой (рис. 1).
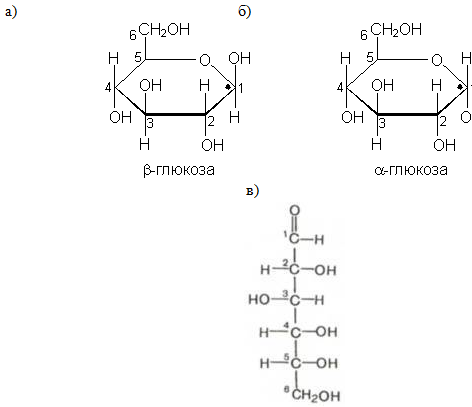
Рис. 1. Формы существования глюкозы: а) β-глюкоза; б) α-глюкоза; в) линейная форма
Получение глюкозы
В промышленности глюкозу получают гидролизом полисахаридов – крахмала и целлюлозы:
Химические свойства глюкозы
Для глюкозы характерны следующие химические свойства:
1) Реакции, протекающие при участии карбонильной группы:
— глюкоза окисляется аммиачным раствором оксида серебра (1) и гидроксидом меди (II) (2) в глюконовую кислоту при нагревании
— глюкоза способна восстанавливаться в шестиатомный спирт – сорбит
— глюкоза не вступает в некоторые реакции, характерные для альдегидов, например, в реакцию с гидросульфитом натрия.
2) Реакции, протекающие при участии гидроксильных групп:
— глюкоза дает синее окрашивание с гидроксидом меди (II) (качественная реакция на многоатомные спирты);
— образование простых эфиров. При действии метилового спирта на один из атомов водорода замещается на группу СН3. В эту реакцию вступает гликозидный гидроксил, находящийся при первом атоме углерода в циклической форме глюкозы
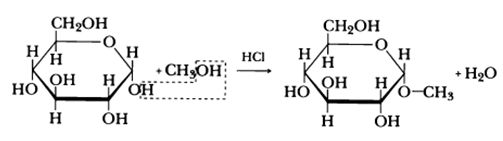
— образование сложных эфиров. Под действием уксусного ангидрида все пять групп –ОН в молекуле глюкозы замещаются на группу –О-СО-СН3.
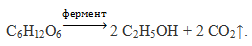
Применение глюкозы
Глюкоза находит широкое применение в текстильной промышленности при крашении и печатании рисунков; изготовлении зеркал и елочных украшений; в пищевой промышленности; в микробиологической промышленности как питательная среда для получения кормовых дрожжей; в медицине при самых разнообразных заболеваниях, особенно при истощении организма.
Примеры решения задач
| Задание | Составьте уравнения реакций между глюкозой и следующими веществами: а) водородом (в присутствии катализатора); б) азотной кислотой; в) аммиачным раствором оксида серебра. При каких условиях протекают эти реакции? |
| Ответ | При взаимодействии глюкозы с водородом в присутствии катализатора (обычно никель) и при нагревании происходит её восстановление. Продуктом этой реакции является шестиатомный спирт – сорбит, который применяется в качестве заменителя сахара: |
Качественной реакцией на альдегидную группу является реакция «серебряного зеркала» (глюкоза представляет собой альдегидоспирт) в результате чего выделяется серебро в чистом виде и образуется карбоновая кислота:
Окисление глюкозы в жестких условиях, например, концентрированной азотной кислотой, приводит к образованию глюкаровой кислоты:
| Задание | Рассчитайте объем оксида углерода (IV), приведенный к нормальным условиям, который выделится при спиртовом брожении 225 г глюкозы. |
| Решение | Запишем уравнение реакции спиртового брожения глюкозы: |
Рассчитаем количество вещества глюкозы:
M(C6H12O6) = 2×Ar(C) + 12×Ar(H) + 6×Ar(O) = 2×12 + 12×1 + 6×16 = 180г/моль;
Согласно уравнению реакции n(C6H12O6) : n(CO2) = 1 : 2, значит
Реакция глюкозы с активными металлами
Химические свойства глюкозы, как и других альдоз, обусловлены присутствием в ее молекуле: а)альдегидной группы; б) спиртовых гидроксилов; в) полуацетального (гликозидного) гидроксила.
Специфические свойства
1. Брожение (ферментация) моносахаридов
Важнейшим свойством моносахаридов является их ферментативное брожение, т.е. распад молекул на осколки под действием различных ферментов. Брожению подвергаются в основном гексозы в присутствии ферментов, выделяемых дрожжевыми грибками, бактериями или плесневыми грибками. В зависимости от природы действующего фермента различают реакции следующих видов:
1) Спиртовое брожение
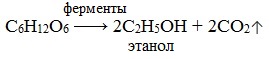
2) Молочнокислое брожение
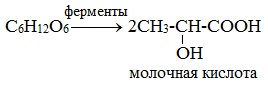
(образуется в организмах высших животных при мышечных сокращениях).
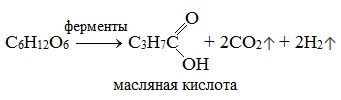
3) Маслянокислое брожение
4) Лимоннокислое брожение
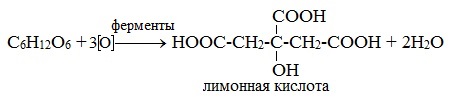
Реакции с участием альдегидной группы глюкозы (свойства глюкозы как альдегида)
1. Восстановление (гидрирование) с образованием многоатомного спирта
В ходе этой реакции карбонильная группа восстанавливается и образуется новая спиртовая группа:
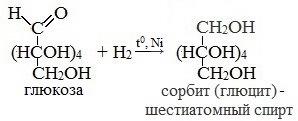
Cорбит содержится во многих ягодах и фруктах, особенно много сорбита в плодах рябины.
2. Окисление
1) Окисление бромной водой
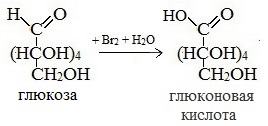
Качественные реакции на глюкозу как альдегид!
Протекающие в щелочной среде при нагревании реакции с аммиачным раствором Ag2O (реакция серебряного зеркала») и с гидроксидом меди (II) Cu (OH)2 приводят к образованию смеси продуктов окисления глюкозы.
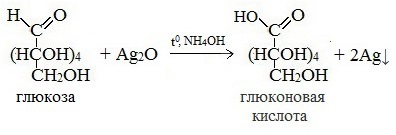
2) Реакция серебряного зеркала
Соль этой кислоты – глюконат кальция – известное лекарственное средство.
Видеоопыт «Качественная реакция глюкозы с аммиачным раствором оксида серебра (I)»
3) Окисление гидроксидом меди (II)
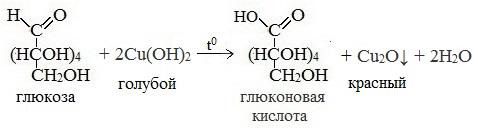
В ходе этих реакций альдегидная группа – СНО окисляется до карбоксильной группы – СООН.
Реакции глюкозы с участием гидроксильных групп (свойства глюкозы как многоатомного спирта)
1. Взаимодействие с Cu (ОН)2 с образованием глюконата меди (II)
Качественная реакция на глюкозу как многоатомный спирт!
Подобно этиленгликолю и глицерину, глюкоза способна растворять гидроксид меди (II), образуя растворимое комплексное соединение синего цвета:
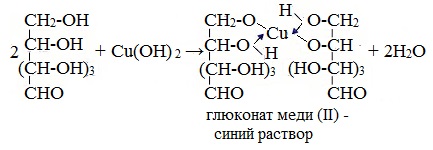
Прильём к раствору глюкозы несколько капель раствора сульфата меди (II) и раствор щелочи. Осадка гидроксида меди не образуется. Раствор окрашивается в ярко-синий цвет.
В данном случае глюкоза растворяет гидроксид меди (II) и ведет себя как многоатомный спирт, образуя комплексное соединение.
Видеоопыт «Качественная реакция глюкозы с гидроксидом меди (II)»
2. Взаимодействие с галогеналканами с образованием простых эфиров
Являясь многоатомным спиртом, глюкоза образует простые эфиры:
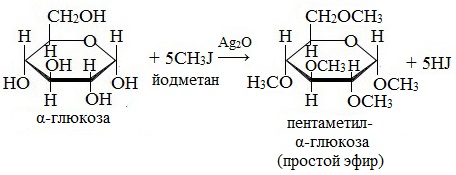
Реакция происходит в присутствии Ag2O для связывания выделяющегося при реакции НI.
3. Взаимодействие с карбоновыми кислотами или их ангидридами с образованием сложных эфиров.
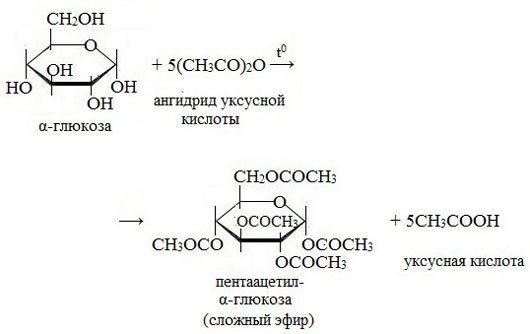
Например, с ангидридом уксусной кислоты:
Реакции с участием полуацетального гидроксила
1. Взаимодействие со спиртами с образованием гликозидов
Гликозиды – это производные углеводов, у которых гликозидный гидроксил замещен на остаток какого-либо органического соединения.
Содержащийся в циклических формах глюкозы полуацетальный (гликозидный) гидроксил является очень реакционноспособным и легко замещается на остатки различных органических соединений.
В случае глюкозы гликозиды называются глюкозидами. Связь между углеводным остатком и остатком другого компонента называется гликозидной.
Гликозиды построены по типу простых эфиров.
При действии метилового спирта в присутствии газообразного хлористого водорода атом водорода гликозидного гидроксила замещается на метильную группу:
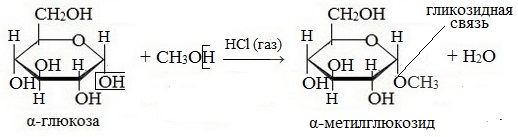
В данных условиях в реакцию вступает только гликозидный гидроксил, спиртовые гидроксильные группы в реакции не участвуют.
Гликозиды играют чрезвычайно важную роль в растительном и животном мире. Существует огромное число природных гликозидов, в молекулах которых с атомом С (1) глюкозы остатки самых различных соединений.
Реакции окисления
Более сильный окислитель – азотная кислота НNO3 – окисляет глюкозу до двухосновной глюкаровой (сахарной) кислоты:
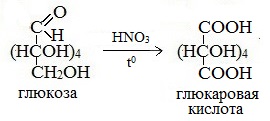
В ходе этой реакции и альдегидная группа – СНО и первичная спиртовая группа — СН2ОН окисляются до карбоксильных – СООН.
Видеоопыт «Окисление глюкозы кислородом воздуха в присутствии метеленового голубого»
Глюкоза С6Н12O6 представляет собой наиболее распространенный и наиболее важный моносахарид — гексозу. Она является структурной единицей большинства пищевых ди- и полисахаридов.
Биологическая роль глюкозы
Глюкоза образуется в природе в процессе фотосинтеза, протекающего под действием солнечного света в листьях растений:Глюкоза – ценное питательное вещество. Она является обязательным компонентом крови и тканей животных и непосредственным источником энергии для клеточных реакций. При окислении ее в тканях освобождается энергия, необходимая для нормальной жизнедеятельности организмов:
Глюкоза – необходимый компонент обмена углеводов. Она необходима для образования в печени гликогена (запасной углевод человека и животных).
Уровень содержания глюкозы в крови человека постоянен. Во всем объеме крови взрослого человека содержится 5-6 г глюкозы. Такого количества достаточно для покрытия энергетических затрат организма в течение 15 минут его жизнедеятельности.
При снижении ее уровня в крови или высокой концентрации и невозможности использования, как это происходит при сахарном диабете, наступает сонливость, может наступить потеря сознания (гипогликемическая кома).
Строение глюкозы. Изомерия
В молекуле глюкозы присутствуют альдегидная и гидроксильная группы.
Видеоопыт «Распознавание глюкозы с помощью качественных реакций»
Моносахаридам свойственна также иная структура, возникающая в результате внутримолекулярной реакции между карбонильной группой с одним из спиртовых гидроксидов. Такая реакция внутри одной молекулы сопровождается ее циклизацией.

Известно, что наиболее устойчивыми являются 5-ти и 6-ти членные циклы. Поэтому, как правило, происходит взаимодействие карбонильной группы с гидроксилом при 4-м или 5-м углеродном атоме.
В результате взаимодействия карбонильной группы с одной из гидроксильных глюкоза может существовать в двух формах: открытой цепной и циклической.
Образование циклической формы глюкозы при взаимодействии альдегидной группы и спиртового гидроксила при С5 приводит к появлению нового гидроксила у С1 называемого полуацетальным (крайний правый). Он отличается от других большей реакционной способностью, а циклическую форму в этом случае называют также полуацетальной.
В кристаллическом состоянии глюкоза находится в циклической форме, а при растворении частично переходит в открытую и устанавливается состояние подвижного равновесия.
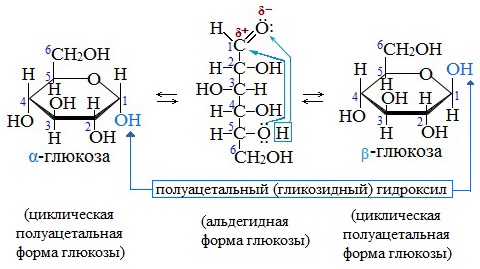
Например, в водном растворе глюкозы существуют следующие структуры:
Подвижное равновесие между взаимопревращающимися структурными изомерами (таутомерами) называется таутомерией. Данный случай относится к цикло-цепной таутомерии моносахаридов.
Циклические α- и β-формы глюкозы представляют собой пространственные изомеры, отличающиеся положением полуацетального гидроксила относительно плоскости кольца.
В α-глюкозе этот гидроксил находится в транс-положении к гидроксиметильной группе -СН2ОН, в β-глюкозе – в цис-положении.
С учетом пространственного строения шестичленного цикла
формулы этих изомеров имеют вид:
Видеофильм «Глюкоза и ее изомеры»
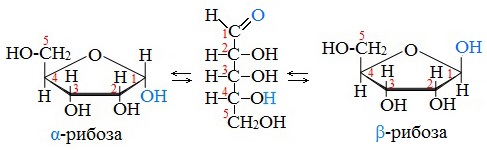
Аналогичные процессы происходят и в растворе рибозы:
В твердом состоянии глюкоза имеет циклическое строение.
Обычная кристаллическая глюкоза – это α-форма. В растворе более устойчива β-форма (при установившемся равновесии на неё приходится более 60% молекул).
Доля альдегидной формы в равновесии незначительна. Это объясняет отсутствие взаимодействия с фуксинсернистой кислотой (качественная реакция альдегидов).
Явление существования веществ в нескольких взаимопревращающихся изомерных формах было названо А. М. Бутлеровым динамической изомерией. Позднее это явление было названо таутомерией.
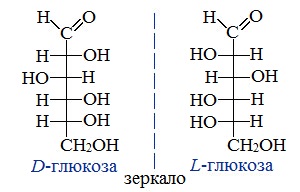
Для глюкозы кроме явления таутомерии характерны структурная изомерия с кетонами (глюкоза и фруктоза – структурные межклассовые изомеры) и оптическая изомерия:
Физические свойства глюкозы
Глюкоза – бесцветное кристаллическое вещество, хорошо растворимое в воде, сладкое на вкус (лат. «глюкос» – сладкий).
Она содержится в растительных и живых организмах, особенно много ее содержится в виноградном соке (отсюда и название – виноградный сахар), в спелых фруктах и ягодах. Мед в основном состоит из смеси глюкозы с фруктозой.
В крови человека ее содержится примерно 0,1 %
Видеоопыт «Определение глюкозы в виноградном соке»
Получение глюкозы
Основным способом получения моносахаридов, имеющим практическое значения, является гидролиз ди- и полисахароидов.
1. Гидролиз полисахаридов
Глюкозу чаще всего получают гидролизом крахмала (промышленный способ получения):
2. Гидролиз дисахаридов3. Альдольная конденсация формальдегида (реакция А.М. Бутлерова)
Первый синтез углеводов из формальдегида в щелочной среде осуществил А.М. Бутлеров в 1861 году.
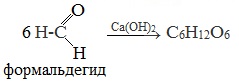
4. Фотосинтез
В природе глюкоза образуется в растениях в результате фотосинтеза:

Применение глюкозы
Глюкоза применяется в медицине в качестве укрепляющего лечебного средства при явлениях сердечной слабости, шоке, для приготовления лечебных препаратов, консервирования крови, внутривенного вливания, при самых разнообразных заболеваниях (особенно при истощении организма).
Широко применяют глюкозу в кондитерском деле (изготовление мармелада, карамели, пряников и т. д.)
Глюкоза находит широкое применение в текстильной промышленности при крашении и печатании рисунков.
Глюкоза применяется в качестве исходного продукта при производстве аскорбиновых и глюконовых кислот, для синтеза ряда производных сахаров и т.д.
Она применяется в производстве зеркал и елочных игрушек (серебрение).
В микробиологической промышленности как питательная среда для получения кормовых дрожжей.
Большое значение имеют процессы брожения глюкозы. Так, например, при квашении капусты, огурцов, молока происходит молочнокислое брожение глюкозы, так же как и при силосовании кормов. Если подвергаемая силосованию масса недостаточно уплотнена, то под влиянием проникшего воздуха происходит маслянокислое брожение и корм становится непригоден к применению.
На практике используется также спиртовое брожение глюкозы, например при производстве пива.
Фруктоза
В отличие от глюкозы она может без участия инсулина проникать из крови в клетки тканей. По этой причине фруктоза рекомендуется в качестве наиболее безопасного источника углеводов для больных диабетом.
Как и глюкоза, она может существовать в линейной и циклических формах. В линейной форме фруктоза представляет собой кетоноспирт с пятью гидроксильными группами.
Строение ее молекулы можно выразить формулой:
Имея гидроксильные группы, фруктоза, как и глюкоза, способна образовывать сахараты и сложные эфиры. Однако вследствие отсутствия альдегидной группы она в меньшей степени подвержена окислению, чем глюкоза. Фруктоза, также как и глюкоза, не подвергается гидролизу.
Фруктоза вступает во все реакции многоатомных спиртов, но, в отличие от глюкозы, не реагирует с аммиачным раствором оксида серебра.
Читайте также:


