Реакция угольной кислоты с металлами
Обновлено: 25.04.2024
У́гольная кислота́ — слабая двухосновная кислота с химической формулой . В чистом виде неустойчива [2] . Образуется в малых количествах при растворении углекислого газа в воде [1] , в том числе и углекислого газа из воздуха. Образует ряд устойчивых неорганических и органических производных: соли (карбонаты и гидрокарбонаты), сложные эфиры, амиды и др.
Содержание
Физические свойства
Молекула угольной кислоты имеет плоское строение. Центральный углеродный атом имеет sp²-гибридизацию. В гидрокарбонат- и карбонат-анионах происходит делокализация π-связи. Длина связи C—O в карбонат-ионе составляет 129 пм.
Химические свойства
Равновесие в водных растворах и кислотность
Угольная кислота существует в водных растворах в состоянии равновесия с гидратом диоксида углерода:
>" />
, константа равновесия при 25 °C <\mathsf<[CO_2 \cdot H_2O]>> = 1,70\cdot 10^" />
Скорость прямой реакции 0,039 с −1 , обратной — 23 с −1 .
В свою очередь растворённый гидрат диоксида углерода находится в равновесии с газообразным диоксидом углерода:
" />
Данное равновесие при повышении температуры сдвигается вправо, а при повышении давления — влево (подробнее см. Абсорбция газов).
Угольная кислота подвергается обратимому гидролизу, создавая при этом кислую среду:
, константа кислотности при 25 °C ><\mathsf<[H_2CO_3]>> = 2,5 \cdot 10^" />
Однако, для практических расчётов чаще используют кажущуюся константу кислотности, учитывающую равновесие угольной кислоты с гидратом диоксида углерода:
Гидрокарбонат-ион подвергается дальнейшему гидролизу по реакции
" />
, константа кислотности при 25 °C ] \cdot [H_3O^+]>><\mathsf<[HCO_3^-]>> = 4,68 \cdot 10^" />
Таким образом, в растворах, содержащих угольную кислоту, создается сложная равновесная система, которую можно изобразить в общем виде следующим образом:
CO_2 \cdot H_2O \rightleftarrows H_2CO_3 \stackrel HCO_3^- \stackrel CO_3^ (*)>" />
Значение pH в такой системе, соответствующей насыщенному раствору диоксида углерода в воде при 25 °C и давлении 760 мм рт. ст., можно рассчитать по формуле:
\lg (K_a" />
, где L = 0,034 моль/л — растворимость CO2 в воде при указанных условиях.
Разложение
При повышении температуры раствора и/или понижении парциального давления диоксида углерода равновесие в системе смещается влево, что приводит к разложению части угольной кислоты на воду и диоксид углерода. При кипении раствора угольная кислота разлагается полностью:
Взаимодействие с основаниями и солями
Угольная кислота вступает в реакции нейтрализации с растворами оснований, образуя средние и кислые соли — карбонаты и гидрокарбонаты соответственно:
(конц.) (разб.)
При взаимодействии угольной кислоты с карбонатами образуются гидрокарбонаты:
Получение
Угольная кислота образуется при растворении в воде диоксида углерода:
Содержание угольной кислоты в растворе увеличивается при понижении температуры раствора и увеличении давления углекислого газа.
Также угольная кислота образуется при взаимодействии её солей (карбонатов и гидрокарбонатов) с более сильной кислотой. При этом бо́льшая часть образовавшейся угольной кислоты, как правило, разлагается на воду и диоксид углерода:
Применение
Угольная кислота всегда присутствует в водных растворах углекислого газа (см. Газированная вода).
В биохимии используется свойство равновесной системы изменять давление газа пропорционально изменению содержания ионов оксония (кислотности) при постоянной температуре. Это позволяет регистрировать в реальном времени ход ферментативных реакций, протекающих с изменением pH раствора.
Органические производные
Угольную кислоту формально можно рассматривать как карбоновую кислоту с гидроксильной группой вместо углеводородного остатка. В этом качестве она может образовывать все производные, характерные для карбоновых кислот [3] .
Некоторые представители подобных соединений перечислены в таблице.
| Класс соединений | Пример соединения |
|---|---|
| Сложные эфиры | поликарбонаты |
| Хлорангидриды | фосген |
| Амиды | мочевина |
| Нитрилы | циановая кислота |
| Ангидриды | пироугольная кислота |
См. также
Примечания
- ↑ 123 В водном растворе бо́льшая часть угольной кислоты обратимо переходит в гидрат диоксида углерода по реакции H2CO3 ⇄ CO2·H2O
- ↑Угольная кислота теперь обнаружена и в газовой фазе - пора снова переписывать учебники
- ↑Нейланд О. Я. Органическая химия. — М .: Высшая школа, 1990. — С. 640—652. — 751 с. — ISBN 5-06-001471-1
Литература
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Hg2 2+ | Pb 2+ | Sn 2+ | Cu + | Cu 2+ | |
| OH − | P | P | P | — | P | М | Н | М | Н | Н | Н | — | Н | Н | Н | Н | Н | — | — | Н | Н | Н | Н | |
| F − | P | Н | P | P | Р | М | Н | Н | М | Р | Н | Н | Н | Р | Р | М | Р | Р | М | М | Н | Р | Н | Р |
| Cl − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | Н | М | — | Н | Р |
| Br − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | Н | М | Р | H | Р |
| I − | P | P | P | P | Р | Р | Р | Р | Р | Р | ? | Р | — | Р | Р | Р | Р | Н | Н | Н | Н | М | Н | — |
| S 2− | P | P | P | P | — | Р | М | Н | Р | — | — | Н | — | Н | Н | Н | Н | Н | Н | — | Н | Н | Н | Н |
| SO3 2− | P | P | P | P | Р | М | М | М | Н | ? | ? | М | ? | Н | Н | Н | М | Н | Н | Н | Н | ? | Н | ? |
| SO4 2− | P | P | P | P | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Н | Р | Р | Р |
| NO3 − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | — | Р | Р |
| NO2 − | P | P | P | P | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? | ? | ? |
| PO4 3− | P | Н | P | P | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | ? | Н | Н | Н | Н |
| CO3 2− | М | Р | P | P | Р | Н | Н | Н | Н | — | — | Н | — | Н | Н | — | — | Н | — | Н | — | — | ? | — |
| CH3COO − | P | Р | P | P | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | М | Р | — | Р | Р |
| CN − | P | Р | P | P | Р | Р | Р | Р | Р | ? | Н | Н | — | Н | Н | Н | Н | Н | Р | Н | Р | — | — | Н |
| SiO3 2− | H | Н | P | P | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | ? | Н | ? | ? | ? |
- Неорганические кислоты
- Неорганические кислородсодержащие кислоты
- Соединения углерода
Wikimedia Foundation . 2010 .
Полезное
Смотреть что такое "Угольная кислота" в других словарях:
УГОЛЬНАЯ КИСЛОТА — Н2СО3, очень слабая и непрочная двухосновная кислота. Образуется при растворении диоксида углерода в воде. Дает соли карбонаты и гидрокарбонаты … Большой Энциклопедический словарь
УГОЛЬНАЯ КИСЛОТА — (H2CO3) очень слабая и непрочная двухосновная кислота, образующаяся при растворении в воде диоксида углерода (углекислого газа) CO2. Дает 2 ряда солей: карбонаты и бикарбонаты (гидрокарбонаты). В природе широко распространены нормальные карбонаты … Российская энциклопедия по охране труда
Угольная кислота — УГОЛЬНАЯ КИСЛОТА, H2CO3, образуется при растворении углерода диоксида в воде. Важнейшие производные карбонаты, мочевина (карбамид). … Иллюстрированный энциклопедический словарь
угольная кислота — Н2СО3, очень слабая и непрочная двухосновная кислота. Образуется при растворении диоксида углерода в воде. Даёт соли карбонаты и гидрокарбонаты. * * * УГОЛЬНАЯ КИСЛОТА УГОЛЬНАЯ КИСЛОТА, Н2СО3, очень слабая и непрочная двухосновная кислота.… … Энциклопедический словарь
УГОЛЬНАЯ КИСЛОТА, H2CO3 — УГОЛЬНАЯ КИСЛОТА, H2CO3, образуется при растворении углерода диоксида в воде. Важнейшие производные карбонаты, мочевина (карбамид) … Современная энциклопедия
УГОЛЬНАЯ КИСЛОТА Н 2 СO 3 — очень слабая кислота, существующая только в водном растворе. Угольная кислота образуется при растворении диоксида углерода в воде (Н2O+СO2=Н2СО3). Угольная кислота образует соли: средние (карбонаты) и кислые (гидрокарбонаты) … Металлургический словарь
Угольная кислота — H2CO3, слабая двухосновная кислота, при нормальных условиях существующая только в разбавленных водных растворах. У. к. образуется при растворении в воде двуокиси углерода: 2, при нормальных условиях не превышает 1% от содержания CO2.… … Большая советская энциклопедия
УГОЛЬНАЯ КИСЛОТА — Н2СО3, очень слабая и непрочная двухосновная кислота. Образуется при растворении диоксида углерода в воде. Даёт соли карбонаты и гидрокарбонаты … Естествознание. Энциклопедический словарь
Угольная кислота — (медико санит.) см. Углерод … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
УГОЛЬНАЯ КИСЛОТА — H2CO3, образуется при растворении CO2 в воде. Проявляет св ва слабой к ты. Равновесие CO2+H2O H2CO3 смещено влево, поэтому меньшая часть CO2 находится в р ре в виде H2CO3. Для У. к. константы диссоциации K1=4,27 … Химическая энциклопедия
Физические и химические свойства угольной кислоты
При растворении в водной среде углекислый газ образует слабую двухосновную угольную кислоту. Угольная кислота характеризуется наличием ряда органических и неорганических производных: соли, гидрокарбонаты и карбонаты. Соединение является неустойчивым и при обычных условиях не выделяется в свободном состоянии из водных растворов.
Угольной кислотой называют слабую двухосновную кислоту, химическая формула которой имеет вид H 2 C O 3 , образуется в малых количествах в процессе растворения углекислого газа в воде.
С помощью угольной кислоты получают:
- соли (карбонаты и гидрокарбонаты);
- другие более слабые органические и неорганические кислоты (например, кремниевую);
- разнообразные органические производные.
При рассмотрении структурной (графической) формулы угольной кислоты можно сделать вывод о последовательности связей между атомами внутри молекулы:
Молекула угольной кислоты характеризуется плоским строением. Центральный углеродный атом имеет s p 2 -гибридизацию. В гидрокарбонат- и карбонат-анионах можно наблюдать делокализацию π -связи. Длина связи C — O в карбонат-ионе равна 130 пм.
Химическая формула угольной кислоты:
Молекула угольной кислоты включает в состав:
- два атома водорода (Ar = 1 а.е.м.);
- один атом углерода (Ar = 12 а.е.м.);
- три атома кислорода (Ar = 16 а.е.м.).
Исходя из химической формулы, определяют молекулярную массу угольной кислоты:
M r ( H 2 C O 3 ) = 2 × A r ( H ) + A r ( C ) + 3 × A r ( O ) ;
M r ( H 2 C O 3 ) = 2 × 1 + 12 + 3 × 16 = 2 + 12 + 48 = 62
Угольную кислоту формально допустимо рассматривать в виде карбоновой кислоты. При этом гидроксильная группа заменяет углеводородный остаток. В данной форме вещество способно образовывать все производные, которые характерны для карбоновых кислот. Некоторые из подобных соединений:
Угольная кислота, являясь слабым электролитом, обладает способностью в небольшой степени диссоциировать на ионы в водном растворе по уравнению:
H 2 C O 3 ↔ H + + ( H C O 3 ) -
Ионная формула угольной кислоты:
Электронная формула угольной кислоты:
Физические и химические свойства
Физические свойства угольной кислоты:
- безводная угольная кислота имеет вид кристаллического вещества без цвета;
- вещество является устойчивым только при низких температурах;
- температура сублимации кристаллов составляет –30 °C. Если повышение температуры продолжается, кристаллы разлагаются в полной степени;
- молярная масса 62,025 г/моль;
- плотность 1 , 668 г / с м 3 ;
- характеристика растворимости в воде 0,21 г/100 мл.
Угольная кислота может существовать в виде раствора водной среды. При этом вещество уравновешивает гидрат диоксида углерода С О 2 . В данном случае можно наблюдать сдвиг равновесного состояния в достаточно сильной степени в сторону разложения кислоты:
C O 2 · H 2 O ( p ) ⇄ H 2 C O 3 ( p ) C O 2 · H 2 O ( p ) ⇄ H 2 C O 3 ( p )
Постоянная состояния равновесия при температурном режиме в 25 °C:
K p = [ H 2 C O 3 ] [ C O 2 · H 2 O ] = 1 , 70 · 10 - 3 K p = [ H 2 C O 3 ] [ C O 2 · H 2 O ] = 1 , 70 · 10 - 3
Прямая реакция протекает со скоростью 0,039 с−1, обратная — 23 с−1.
С другой стороны, растворенный гидрат диоксида углерода пребывает в состоянии равновесия с газообразным диоксидом углерода С О 2 :
C O 2 · H 2 O ( p ) ⇄ C O 2 ↑ + H 2 O C O 2 · H 2 O ( p ) ⇄ C O 2 ↑ + H 2 O
Рассматриваемое равновесие при нагревании сдвигается в правую сторону, а при повышении давления — в левую сторону.
Угольная кислота является слабым электролитом. Это объясняется тем, что в водном растворе вещество диссоциирует частично, то есть обладает небольшой степенью диссоциации:
H 2 C O 3 + H 2 O ⇄ H C O 3 - + H 3 O + H 2 C O 3 + H 2 O ⇄ H C O 3 - + H 3 O +
Константа кислотности при 25 °C:
K a 1 = [ H C O 3 - ] · [ H 3 O + ] [ H 2 C O 3 ] = 2 , 5 · 10 - 4 K a 1 = [ H C O 3 - ] · [ H 3 O + ] [ H 2 C O 3 ] = 2 , 5 · 10 - 4
Стоит отметить, что на практике при расчетах применяют кажущуюся постоянную кислотности с учетом равновесного состояния угольной кислоты и гидрата диоксида углерода:
K a ' = [ H C O 3 - ] · [ H 3 O + ] [ C O 2 · H 2 O ] = 4 , 27 · 10 - 7 K a ' = [ H C O 3 - ] · [ H 3 O + ] [ C O 2 · H 2 O ] = 4 , 27 · 10 - 7
Гидрокарбонат-ион подвергается дальнейшей диссоциации в соответствии с уравнением реакции:
H C O 3 - + H 2 O ⇄ C O 3 2 - + H 3 O + H C O 3 - + H 2 O ⇄ C O 3 2 - + H 3 O +
K a 2 = [ C O 3 2 - ] · [ H 3 O + ] [ H C O 3 - ] = 4 , 68 · 10 - 11 K a 2 = [ C O 3 2 - ] · [ H 3 O + ] [ H C O 3 - ] = 4 , 68 · 10 - 11
В результате в растворах, которые содержат угольную кислоту, формируется система в равновесном состоянии сложной структуры, которую можно записать в общем виде таким образом:
C O 2 ⇄ H 2 O C O 2 · H 2 O ⇄ H 2 C O 3 ⇄ - H + H C O 3 - ⇄ - H + C O 3 2 - ( * ) C O 2 ⇄ H 2 O C O 2 · H 2 O ⇄ H 2 C O 3 ⇄ - H + H C O 3 - ⇄ - H + C O 3 2 - ( * )
Характеристика водородного показателя pH в рассматриваемой системе, которая соответствует насыщенному раствору диоксида углерода в воде при 25 °C и давлении 760 мм рт. ст., определяют по формуле:
pH ≈ - 1 2 lg ( K a ' · L ) = 3 , 9 p H ≈ - 1 2 lg ( K a ' · L ) = 3 , 9
где L = 0 , 034 моль/л — определяется, как показатель растворимости C O 2 в водной среде при заданных параметрах.
Когда раствор нагревают и/или снижают парциальное давление диоксида углерода, наблюдается смещение равновесия в сторону разложения угольной кислоты на воду и диоксид углерода. В процессе кипения раствора происходит полное разложение угольной кислоты:
H 2 C O 3 ⟶ H 2 O + C O 2 ↑ H 2 C O 3 ⟶ H 2 O + C O 2 ↑
Угольная кислота вступает в реакции нейтрализации с растворами оснований. В результате такого взаимодействия образуются средние и кислые соли в виде карбонатов (например, N a 2 C O 3 ) и гидрокарбонатов (например, N a H C O 3 ):
H 2 C O 3 + 2 N a O H H 2 C O 3 + 2 N a O H
⟶ N a 2 C O 3 + 2 H 2 O ⟶ N a 2 C O 3 + 2 H 2 O
H 2 C O 3 + N a O H H 2 C O 3 + N a O H ( р а з б . )
⟶ N a H C O 3 + H 2 O ⟶ N a H C O 3 + H 2 O
H 2 C O 3 + C a ( O H ) 2 ⟶ C a C O 3 ↓ + 2 H 2 O H 2 C O 3 + C a ( O H ) 2 ⟶ C a C O 3 ↓ + 2 H 2 O
H 2 C O 3 + N H 3 · H 2 O ⟶ N H 4 H C O 3 + H 2 O H 2 C O 3 + N H 3 · H 2 O ⟶ N H 4 H C O 3 + H 2 O
Химическая реакция угольной кислоты с карбонатами сопровождается образованием гидрокарбонатов:
H 2 C O 3 + N a 2 C O 3 ⟶ 2 N a H C O 3 H 2 C O 3 + N a 2 C O 3 ⟶ 2 N a H C O 3
H 2 C O 3 + C a C O 3 ⟶ C a ( H C O 3 ) 2 H 2 C O 3 + C a C O 3 ⟶ C a ( H C O 3 ) 2
Способы получения и сфера применения
Образование угольной кислоты в процессе растворения в воде диоксида углерода:
C O 2 + H 2 O ⇄ C O 2 · H 2 O ⇄ H 2 C O 3 C O 2 + H 2 O ⇄ C O 2 · H 2 O ⇄ H 2 C O 3
Концентрация угольной кислоты в растворе повышается в условиях понижения температуры раствора и увеличения давления углекислого газа.
Другим способом получения угольной кислоты является взаимодействие ее солей (карбонатов и гидрокарбонатов) с более сильной кислотой. В результате образовавшаяся угольная кислота в большей степени при разложении образует воду и диоксид углерода:
N a 2 C O 3 + 2 H C l ⟶ 2 N a C l + H 2 C O 3 N a 2 C O 3 + 2 H C l ⟶ 2 N a C l + H 2 C O 3
H 2 C O 3 → H 2 O + C O 2 ↑ H 2 C O 3 → H 2 O + C O 2 ↑
Угольная кислота всегда присутствует в водных растворах углекислого газа.
В области биохимии высоко ценится способность равновесной системы изменять давление углекислого газа С О 2 (диоксида углерода) пропорционально изменению содержания ионов гидроксония H 3 O + (кислотности среды) в условиях постоянной температуры. Данное свойство позволяет регистрировать в реальном времени ход ферментативных реакций, протекающих с изменением pH раствора.
Угольная кислота нашла широкое применение в пищевой промышленности, является важным компонентом в производстве разнообразных шипучих напитков.
Гидроксиды угольной и кремневой кислот
Формулы угольной и кремниевой кислот, их химические свойства по отношению к металлам,оксидам,основаниям, специфические свойства.
Н2СО3 — существует только в растворе:
Н2SiO3— твердое вещество, практически нерастворимо в воде, поэтому катионы водорода в воде практически не отщепляются. В связи с этим такое общее свойство кислот, как действие на индикаторы, Н2SiO3 не обнаруживает, она еще слабее угольной кислоты.
Н2SiO3 — непрочная кислота и при нагревании постепенно разлагается:
Н2CO3 реагирует с металлами, оксидами металлов, основаниями:
б) Н2CO3 + СаО = СаСO3 + Н20
Карбонаты, соли угольной кислоты H2CO3.
Различают нормальные (средние) карбонаты, с анионом СО3 2- (например, KHCO3), кислые карбонаты (гидрокарбонаты или бикарбонаты), с анионом НСО - 3 (например, КНСОз) и основные карбонаты [например, Cu2(OH)2СОз — минерал малахит]. В воде растворимы только нормальные карбонаты щелочных металлов, аммония и таллия. В результате значительного гидролизарастворы их показывают щелочную реакцию. Наиболее трудно растворимы нормальные карбонаты кальция,стронция, бария и свинца (2-валентного). Кислые карбонаты хорошо растворимы в воде.
При нагревании карбонаты, как правило, разлагаются (CaCO3 = CaO + CO2) ещё до достижения точки плавления; исключение представляют карбонаты щелочных металлов и таллия. Гидрокарбонаты при нагревании переходят в нормальные карбонаты (2NaHCO3 = Na2CO3 + H2O + CO2). Сильными кислотами нормальные и кислые карбонаты разлагаются с выделением CO2 (K2CO3 + H2SO4 = K2SO4 + H2O + CO2).
| Углерод (С), кремний (Si), германий (Ge), олово (Sn), свинец (РЬ): ns2np2.Углерод и кремний углерод …2s2 2p2 кремния … 2S22P63S23p2 Со:-4,+2,+4 Оксиды 2С+О2=2СО 2СО+О2=2СО2 при восстановлении диоксида углерода раскалённым углём: СО2+С2CO Кислотные свойства: СО2 восст-ые св-ва СО: 2Mg + CO2 = 2MgO + C PdCl2+CO+H2OPd+CO2+2HCl CO2 + H2O ↔ H2CO3 Ca(OH)2 + CO2 = CaCO3↓ + H2O Fe2O3+CO2Fe+3CO2 KOH + CO2 → KHCO3 SiO2+ C=CO+ SiO Гидроксид: формально C(OH)4(H4CO4) моментально отщепляет воду и превращается вH2CO3 SiO неустойчив,диспропорционирование: 2 SiO(г)= SiO2(кр)+ Si(кр) Si+O2=SiO2 Na2SiO3(HCl,-NaCl)H4SiO4(H2O)mSiO2*nH2O(осадок,гидроксид) Кислотные свойства: SiO2— кислотный оксид, не реагирующий с водой.SiO2+CaO=CaSiO3 SiO2+MgSi+MgO SiO2+4NaOH=Na4SiO4+2H2O SiO2+4HF=SiF4+2H2O SiO2+Na2CO3(сплав)Na2SiO3(жидкое стекло)+CO2 Примеры растворимых и малорастворимых карбонатов Растворимые карбонаты: K2CO3, Na2CO3, Li2CO3,(NH4)2CO3 Сa(HCO3)2(определяет времен.жесткость воды)CaCO3+CO2+H2O Малорастворимые карбонаты: BaCO3, СaCO3, СоCO3 |
44. Получение и химические свойства галогеноводородных кислот
Галогеноводороды
Соединения галогенов с водородом НХ, где X — любой галоген, называются галогеноводородами. Вследствие высокой электроотрицательности галогенов связующая электронная пара смещена в их сторону, поэтому молекулы этих соединений полярны.
Галогеноводороды — бесцветные газы, с резким запахом, легко растворимы в воде. 1При 0°С в 1 объеме воды растворяете 500 объемов НС1, 600 объемов HBr и 450 объемов HI. Фтороводород смешивается с водой в любых соотношениях. Высокая растворимость этих соединений в воде позволяет получать концентрированные растворы.
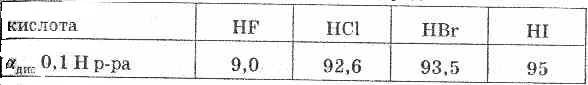
При растворении в воде галогеноводороды диссоциируют по типу кислот. HF относится к слабо диссоциированным соединениям, что объясняется особой прочностью связи в куле. Остальные же растворы галогеноводородов относятся к числу сильных кислот. HF — фтороводородная (плавиковая) кислота НС1 — хлороводородная (соляная) кислота HBr — бромоводородная кислота HI — иодоводородная кислота
Сила кислот в ряду HF — НСl — HBr — HI возрастает, что объясняется уменьшением в том же направлении энергии связи и увеличением межъядерного расстояния. HI — самая сильная кислота из ряда галогеноводородных кислот.
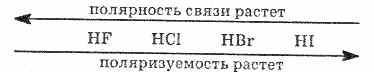
Поляризуемость растет вследствие того, что вода поляризует
больше ту связь, чья длина больше. Соли галогеноводородных кислот носят соответственно следующие названия: фториды, хлориды, бромиды, иодиды.
Химические свойства галогеноводородных кислот
В сухом виде галогеноводороды не действуют на большинство металлов.
1. Водные растворы галогеноводородов обладают свойствами бескислородных кислот. Энергично взаимодействуют со многими металлами, их оксидами и гидроксидами; на металлы, стоящие в электрохимическом ряду напряжений металлов после водорода, не действуют. Взаимодействуют с некоторыми солями и газами.

Фтороводородная кислота разрушает стекло и силикаты:
Поэтому она не может храниться в стеклянной посуде.
2. В окислительно-восстановительных реакциях галогеноводородные кислоты ведут себя как восстановители, причем восстановительная активность в ряду Сl-, Br-, I- повышается.
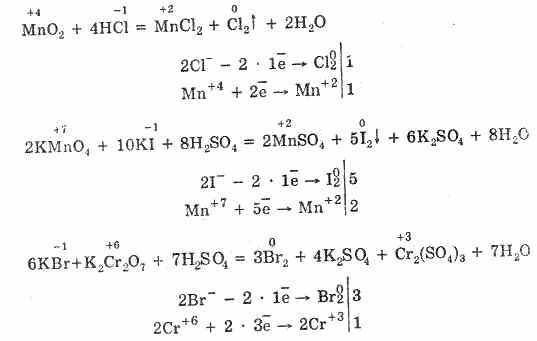
Фтороводород получают действием концентрированной серной кислоты на плавиковый шпат:
Хлороводород получают непосредственным взаимодействием водорода с хлором:
Это синтетический способ получения.
Сульфатный способ основан на реакции концентрированной
серной кислоты с NaCl.
При небольшом нагревании реакция протекает с образованием НСl и NaHSO4.
При более высокой температуре протекает вторая стадия реакции:
Но аналогичным способом нельзя получить HBr и HI, т.к. их соединения с металлами при взаимодействии с концентрировавной серной кислотой окисляются, т.к. I- и Br- являются сильными восстановителями.
Бромоводород и иодоводород получают гидролизом PBr3 и PI3: PBr3+3Н2O=3HBr+Н3PO3 PI3+3Н2О=3HI+Н3РO3
45. Гибридизация атомных орбиталей. Геометрическое строение молекул и ионов. Влия- ние неподеленной электронной пары на геометрическую конфигурацию и химические свойства молекул и ионов. (из прошлого экзамена взято)
Гибридизация орбиталей — гипотетический процесс смешения разных (s, p, d, f) орбиталей центрального атома многоатомной молекулы с возникновением одинаковых орбиталей, эквивалентных по своим характеристикам.
Угольная кислота и ее соли
Диоксид углеродаСО2 (углекислый газ) - при обычных условиях это газ без цвета и запаха, слегка кисловатого вкуса, тяжелее воздуха примерно в 1,5 раза, растворим в воде, достаточно легко сжижается (при комнатной температуре под давлением около 60 ∙ 10 5 Па его можно превратить в жидкость). При охлаждении до −56,2ºС жидкий диоксид углерода затвердевает и превращается в снегообразную массу.
Во всех агрегатных состояниях состоит из неполярных линейных молекул. Химическое строение молекулы СО2 определяется sp-гибридизацией центрального атома углерода и образованием дополнительных πр-р-связей: О = С = О.
Некоторая часть растворенного в воле СО2 взаимодействует с ней сообразованием угольной кислоты:
Углекислый газ очень легко поглощается растворами щелочей с образованием карбонатов и гидрокарбонатов:
Молекулы СО2 очень устойчивы термически, распад начинается только при температуре 2000ºС. Поэтому диоксид углерода не горит и не поддерживает горения обычного топлива. Но в его атмосфере горят некоторые простые вещества, атомы которых проявляют большое сродство к кислороду, например, магний при нагревании загорается в атмосфере СО2.
Угольная кислота H2CO3 – соединение непрочное, существует только в водных растворах. Большая часть растворенного в воде углекислого газа находится в виде гидратированных молекул CO2, меньшая – образует угольную кислоту.
Водные растворы, находящиеся в равновесии с CO2 атмосферы, являются кислыми: [CO2] = 0,04 М и рН ≈ 4.
Угольная кислота – двухосновная, относится к слабым электролитам, диссоциирует ступенчато (К1 = 4, 4 ∙ 10 −7 ; К2 = 4, 8 ∙ 10 −11 ). При растворении CO2 в воде устанавливается следующее динамическое равновесие:
При нагревании водного раствора углекислого газа растворимость газа понижается, CO2 выделяется из раствора, и равновесие смещается влево.
Будучи двухосновной, угольная кислота образует два ряда солей: средние соли (карбонаты) и кислые (гидрокарбонаты). Большинство солей угольной кислоты бесцветны. Из карбонатов растворимы в воде лишь соли щелочных металлов и аммония.
В воде карбонаты подвергаются гидролизу, и поэтому их растворы имеют щелочную реакцию:
Дальнейший гидролиз с образованием угольной кислоты в обычных условиях практически не идет.
Растворение в воде гидрокарбонатов также сопровождается гидролизом, но в значительно меньшей степени, и среда создается слабощелочная (рН ≈ 8).
Карбонат аммония (NH4)2CO3 отличается большой летучестью при повышенной и даже при обычной температуре, особенно в присутствии паров воды, которые вызывают сильный гидролиз.
Сильные кислоты и даже слабая уксусная кислота вытесняют из карбонатов угольную кислоту:
В отличие от большинства карбонатов, все гидрокарбонаты в воде растворимы. Они менее устойчивы, чем карбонаты тех же металлов и при нагревании легко разлагаются, превращаясь в соответствующие карбонаты:
Сильными кислотами гидрокарбонаты разлагаются, как и карбонаты:
Из солей угольной кислоты наибольшее значение имеют карбонат натрия (сода), карбонат калия (поташ), карбонат кальция (мел, мрамор, известняк), гидрокарбонат натрия (питьевая сода) и основной карбонат меди (CuOH)2CO3 (малахит).
Основные соли угольной кислоты в воде практически нерастворимы и при нагревании легко разлагаются:
Термическая устойчивость карбонатов зависит от поляризационных свойств ионов, входящих в состав карбоната. Чем больше поляризующее действие оказывает катион на карбонат-ион, тем ниже температура разложения соли. Если катион способен легко деформироваться, то карбонат-ион сам также будет оказывать поляризующее действие на катион, что приведет к резкому снижению температуры разложения соли.
Карбонаты натрия и калия плавятся без разложения, а большинство остальных карбонатов при нагревании разлагаются на оксид металла и углекислый газ:
Оксид углерода (II)
Молекула СО имеет следующую структуру
:С≡О:
Две связи образованы за счет спаривания 2р-электронов атомов углерода и кислорода, третья связь образована по донорно-акцепторному механизму за счет свободной 2р-орбитали углерода и 2р-электронной пары атома кислорода. Дипольный момент молекулы незначителен, при этом эффективный заряд на атоме углерода отрицательный, а на атоме кислорода – положительный.
Поскольку строение молекулы СО сходно со строением молекулы азота, похожи их физические свойства. СО имеет очень низкие температуры плавления (- 204ºС) и кипения (- 191,5ºС), это бесцветный, очень ядовитый газ, без запаха, совсем немного легче воздуха. Плохо растворим в воде, и с ней не взаимодействует.
СО считается несолеобразующим оксидом, т.к. при обычных условиях не взаимодействует ни с кислотами, ни со щелочами. Он образуется при горении угля и углеродистых соединений при ограниченном доступе кислорода, также при взаимодействии углекислого газа с раскаленным углем: СО2 + С = 2СО.
В лаборатории его получают из мурвьиной кислоты действием на нее концентрированной серной кислоты при нагревании:
Можно использовать также и щавелевую кислоту. Серная кислота в этих реакциях выступает как водоотнимающее средство.
В обычных условиях СО химически достаточно инертен, но при нагревании проявляет восстановительные свойства, что широко используется в пирометаллургии для получения некоторых металлов: Fe2O3 + 3CO = 2Fe + 3CO2.
На воздухе СО горит голубоватым пламенем с выделением большого количества теплоты: 2СО + О2 = 2СО2 + 569 кДж.
Помимо кислорода на прямом солнечном свету или в присутствии катализатора (активного угля) СО соединяется с хлором, образуя фосген:
Фосген – бесцветный газ с характерным запахом. В воде он малорастворим, но как хлорангидрид угольной кислоты постепенно гидролизуется по схеме: COCl2 + 2H2O = 2HCl + H2CO3. Вследствие высокой токсичности фосген применяли как боевое отравляющее средство в первую мировую войну. Обезвредить его можно с помощью гашеной извести.
При нагревании СО окисляется и серой: СО + S = COS.
Молекула СО может выступать в качестве лиганда в различных комплексных соединениях. За счет несвязывающей электронной пары углерода она проявляет σ-донорные свойства, а за счет свободных π-разрыхляющих орбиталей проявляет π-акцепторные свойства. Особый интерес представляют карбонильные комплексы d-металлов, т.к. термическим разложением карбонилов получают металлы высокой чистоты.
Угольная кислота - свойства, получение и применение
При растворении углекислого газа в воде образуется двухосновная слабая угольная кислота, которая характеризуется включением ряда неустойчивых органических и неорганических производных, в том числе солей, гидрокарбонатов и карбонатов. Этот элемент сегодня широко используется в пищевой промышленности, он незаменим при производстве различных шипучих напитков. Это непостоянное соединение, которое в свободном состоянии выделить из воды крайне сложно.

Угольная кислота способна существовать в равновесии с диоксидом углерода в водных растворах. Однако при изменении условий, в частности, температуры, этот карбонатный класс склонен распадаться, одновременно происходит окисление гидроксида. Также встречается безводная форма, которая представляет собой небольшие бесцветные кристаллы, образующиеся при температурах ниже минус 30 градусов. При ее нагревании происходит диссоциация угольной кислоты, при которой твёрдая форма полностью разлагается.
Соляный ангидрид свое название получил из-за формулы угольной кислоты, в которой содержится СО2. Газ может подвергаться обратному гидролизу, создавая устойчивую кислую среду. В растворах, содержащих эти элементы, возникает равновесная сложная система, которая сохраняет свою химическую формулу и физические свойства. При повышении температуры стабильность и равновесие такого раствора нарушается, а кислота начинает разлагаться. Полностью этот процесс завершается при кипячении водного раствора.
Угольная кислота, графическая формула которой выглядит как H2CO3, имеет нейтральную реакцию, образуя кислые и средние соли, в том числе гидрокарбонаты и карбонаты. На сегодняшний день это вещество отлично изучено, химикам известна степень, молярное уравнение, масса, константа и степень валентности. Такие соединения получили широкое распространение в пищевой промышленности, их используют в качестве консервантов и раскислителей, а также в бытовой химии для изготовления различных чистящих и моющих средств.
Способы получения
Наибольшее распространение на сегодняшний день получила технология изготовления кислоты угольной путем растворения в воде структурной газовой формы диоксида углерода. Для производства этих соединений используют соответствующие установки, позволяющие увеличивать давление углекислоты, одновременно понижая температуру раствора. В подобных условиях концентрация угольной кислоты увеличивается и в последующем имеется возможность получения твердой формы за счёт понижения температуры до отметки -35 градусов и ниже.

Также в последние годы популярностью стала пользоваться технология производства солей путем взаимодействия гидрокарбонатов и карбонатов с еще более сильными кислотами. При этом лучшая часть полученных соединений разлагается на диоксид углерода и воду. Преимуществом такой технологии является простота используемого оборудования, не требуется одновременно охлаждать растворы и повышать давление CO2, но при этом отмечается большое количество отходов. Недостатком этой технологии является то, что требуется утилизировать углеродный диоксид, который превращается в пар.
Используемые сегодня высокотехнологичные установки позволяют получать чистую кислоту угольную, в особенности при применении технологии с экстремально низкими температурами. В последующем необходимо лишь обеспечить правильное хранение кристаллов, которые при температурах выше минус 30 градусов начинают растворяться, быстро теряя все свои свойства. Также возможно производство и последующее хранение различных солей на основе этого соединения, которые сохраняют свою форму и параметры даже при положительных температурах и доступе воздуха.
Особенности применения
Угольная кислота и её соли сегодня активно используются в различных сферах жизнедеятельности человека. Они применяются в медицине, строительстве и кулинарии. Без этих микроэлементов невозможно было бы получение и возникновение следующих составов и материалов:
- мраморный камень;
- известняковые породы;
- кристаллическая и пищевая сода;
- мел;
- поташ.
Также из кислоты угольной получают углекислый газ, который требуется для изготовления газированной воды. Свойства этих соединений изменять показатели давления в зависимости от содержания ионов и кислотности позволяют на их основе выпускать хладагенты для морозильников и солнечных генераторов.

Такие кислоты и соли широко используются в пищевой промышленности, они полностью безопасны для организма человека. Из нее делаются разнообразные консерванты, которые не ухудшают свойства продуктов питания, существенно продлевая их срок хранения. Это соединение используется в качестве антиокислителя, его добавляют в кофе, чай и сыры. С открытием этой кислоты появилась возможность изготавливать разнообразные шипучие напитки, в том числе минералку, Coca- Cola и даже шампанское.
В последние годы широкое распространение получила литиевая соль, которую изготавливают из этой кислоты. Она применяется для производства керамических изделий, также ее добавляют в топливо для реактивных двигателей. Сегодня это химическое соединение активно применяется в стекловарении. На его основе выполняют специальные добавки, которые повышают прочность и эксплуатационные характеристики конечного материала. Силикатное стекло, в которое была добавлена литиевая соль, отличается не только прочностью, но и великолепными показателями проницаемости светового потока.
Кислоту угольную активно используют пожарные бригады, что позволяет им эффективно бороться с огнём. В жидком виде такие соединения содержат в специальных емкостях, после чего под высоким давлением направляют в распылители, смешивая со специальными химикатами, образующими густую пену. Это позволяет не только бороться с открытым пламенем, но и быстро тушить горящую нефть и различные нефтепродукты.
Использование в сельском хозяйстве
Кислота угольная сегодня широко используется в сельском хозяйстве для производства различных качественных минеральных удобрений. Это экологически чистые компоненты, которые применяются для подкормки различных овощных, фруктовых и плодовых культур, позволяя существенно повысить показатели урожайности.
На основе кислоты угольной выполняются следующие минеральные удобрения:
- кальцинированная сода;
- литиевая соль;
- карбамид или мочевина.

Наибольшее распространение сегодня получила мочевина или как она стала сегодня называться карбамид. Это простое в использовании эффективное удобрение, которое отличается универсальностью. С одинаковым успехом его можно вносить под плодовые деревья, фрукты и овощи, различные декоративные растения.
Несомненным преимуществом таких удобрений на основе угольной кислоты является доступная стоимость минеральных составов, их простота использования, эффективность и полная экологичность.
Средняя стоимость
На сегодняшний день в России имеется несколько крупных производителей кислоты угольной, которые изготавливают как соли, так и чистые вещества. В среднем стоимость одного килограмма такого соединения составляет 3−4 тысячи рублей.

Также востребован мел, который изготавливают с использованием этой кислоты, он применяется в кормовых и технических целях. За одну тонну мела обычно просят 1200 рублей.
В редких случаях используется так называемый угольный снег, то есть кристаллы твердой формы этой кислоты. Они имеют крайне высокую стоимость, доходящую до 10000 рублей за килограмм и более. При этом необходимо обеспечить соответствующие условия хранения, в том числе поддержание температуры на уровне минус 30−35 градусов, что предупреждает его разложение. Это соединение применяется в химической промышленности, а также при производстве разнообразных продуктов питания.
Читайте также:
