Самый радиоактивный металл на земле
Обновлено: 15.05.2024
Калифорний - Это Металл серебристо-белого цвета с ярким блеском, искусственного происхождения, который в окружающей среде не существует, он добывается только лабораторно в очень небольших количествах и только в двух местах на планете: В России и США:
1.
Драгоценные металлы вовсе не являются такими дорогими, если сравнивать их с некоторыми искусственно полученными металлами. Например, радиоактивный элемент Калифорний-252 стоит неимоверных 27 миллионов долларов за 1 грамм (дороже только антиматерия, которая оценивается в 60 триллионов долларов за 1 грамм). Ежегодно в мире производят лишь 40 миллиграмм этого материала, поэтому мировой запас Калифорния составляет ничтожных 8 грамм. Регулярно Калифорний производят в Окриджской национальной лаборатории в США и в Димитровграде Ульяновской области. Далее предлагаем взглянуть на процесс производства почти самого дорогого в мире материала.
2.
В 80 километрах от Ульяновска, на реке Черемшан, находится город Димитровград с населением около 100 000 человек. Его главное предприятие – Научно-исследовательский институт атомных реакторов (НИИАР), который был создан в 1956 году по иницитиве Курчатова. Изначально он был опытной станцией для испытаний ядерных реакторов, но в настоящее время спектр направлений деятельности значительно расширился. Сейчас в НИИАР испытывают различные материалы, чтобы определить, как они себя ведут в условиях продолжительного радиактивного излучения, создают радионуклидные источники и препараты, которые применяют в медицине и исследованиях, решают технические вопросы экологически чистых технологий и просто ведут научную деятельность. В НИИАР работает около 3500 сотрудников и 6 реакторов.
Известны 20 изотопов, наиболее ценным из них является калифорний-252 с периодом полураспада в 2,6 года.
Температура плавления металла 900 градусов Цельсия, температура кипения оценивается в 1300-1500 градусов Цельсия. Калифорний радиоактивен, является мощным источником нейтронов и токсичен. Ежегодно производят не больше нескольких сот миллиграммов 252-го изотопа.

Откуда взялся калифорний на Земле? Предположительно, из ядерного взрыва. Мощный поток нейтронов, возникающих в процессе цепной реакции, вызывает серию ядерных превращений примерно по такой схеме: атом урана или плутония захватывает нейтрон и если не делится, то претерпевает распад - испускает либо альфа-, либо бета-частицу. В первом случае он перепрыгивает через один элемент назад, а во втором становится следующим элементом. Захватив новый нейтрон, тот, в свою очередь, может претерпеть бета-распад и увеличить свой номер еще на единицу. А может до того поймать еще один нейтрон и стать более тяжелым изотопом следующего элемента — это называется r-процесс. Так, в те несколько долей секунды, которые длится активная фаза взрыва и плотность потока нейтронов высока, неизбежно образуется какое-то количество атомов тяжелых элементов и, в частности, калифорния. Во всяком случае, так утверждает Томас Альбрехт-Шмитт из университета штата Флорида, опубликовавший соответствующую статью о калифорнии в сентябрьском номере журнала «Nature Chemistry» за 2014 год. Причем образуются какие-то долгоживущие изотопы, коль скоро их обнаружили при анализе мест ядерных взрывов 40-х годов. Кстати, самые долгоживущие изотопы: калифорний-251 с периодом полураспада 898 лет и калифорний-249 - 345 лет. То есть родившиеся в ядерных и термоядерных испытаниях атомы калифорния вполне могут сохраниться до сих пор. Однако поскольку соответствующие документы о последствиях ядерных взрывов были засекречены, официально рождение калифорния приходится на опыты Гленна Сиборга в феврале 1950 года по бомбардировке мишеней в циклотроне в Беркли: для калифорния мишенью служил кюрий, а снарядом: альфа-частица. Как пишет Альбрехт-Шмитт, есть подозрения, что калифорний вместе с порождающим его кюрием, а также америцием имеется и в отработанном ядерном топливе. Поскольку атомщики заинтересованы в переработке этого топлива, сейчас активно развивается химия калифорния и других тяжелых актиноидов: очищать от них нужно и само топливо, и получающиеся при этом жидкие отходы. Ведь калифорний спососо6ен спонтанно делиться, а дополнительный расщепляющийся элемент в придачу к урану в топливном стержне совсем не нужен, и, кроме того, активность всех трех элементов очень велика, убрав их, можно снизить вредоносность таких жидких отходов.
Как получают калифорний? Его делают в специальных реакторах с большим потоком нейтронов. Таких реакторов на Земле два - в американском Окридже и в нашем Димитровграде. На первый приходится 70% изготавливаемого калифорния-252, а годовой объем этого производства составляет примерно 25 мг. Чтобы сделать калифорний, надо сначала получить фермий и с помощью нейтронов обратить его в берклий-249. Тот, поймав нейтрон, станет берклием-250 и за счет бета-распада обратится в калифорний-250. Получив еще два нейтрона, он и станет желаемым калифорнием-252. Стоит калифорний в сотни тысяч раз дороже золота - десятки миллионов долларов за грамм.
Зачем нужен калифорний - 252? Этот наиболее востребованный изотоп не распадается - он делится, причем период его полураспада не мал и не велик - 2,6 года. При делении получаются не только осколки, но и много нейтронов с широким спектром энергий - один миллиграмм калифорния-252 в секунду выделяет 2,5 млрд нейтронов. Неудивительно, что на его основе сделали множество нейтронных источников. Они нужны для нескольких видов работы. Вот их перечень. Нейтроны помогают проводить нейтрон-активационный анализ на присутствие какого-то элемента. Схема его такова: нейтрон попадает в атом элемента и превращает его в радиоактивный изотоп. При распаде тот дает, например, гамма-квант, который удается зафиксировать. Так легко обнаруживать взрывчатку - в ней много атомов азота, и они светятся под нейтронным лучом. Мощный нейтронный поток от калифорниевого источника позволяет эту процедуру проводить быстро - в 80-х годах их стали устанавливать в аэропортах для борьбы с террористами. Сейчас, правда, на смену приходят другие источники нейтронов, менее опасные и не такие дорогие. Благодаря высокой проникающей способности нейтроны калифорния проходят сквозь почву и позволяют находить противопехотные и противотанковые мины. Используют их и для просвечивания крупных металлических конструкций - в них ищут дефекты. Важны такие портативные источники и для геологов - вызывая свечение воды и нефти, они дают пространственное расположение нефтеносных слоев под буровой. Очень важная функция калифорниевых источников - запуск ядерной реакции в топливных блоках атомных электростанций: нейтроны нужны для инициации цепной реакции. Третья большая область применения - онкология. Нейтроны оказывают гораздо более разрушительное действие на клетки, нежели мягкие виды облучения. Поэтому в 80-х годах калифорний начали применять при неоперабельных видах рака в различных полостях - раке матки, раке желудка. Как правило, сначала опухоль насыщают бором, он-то и ловит нейтроны калифорния, обеспечивая высокую дозу вторичного облучения именно в нужном месте. Нельзя сказать, что удается достичь существенного успеха - рак и был и остается неизлечимой болезнью. Но вот, например, свежие данные врачей из Полицейского госпиталя Гуандуна («Chinese Journal of Cancer», 2017, которые лечили калифорниевым облучением рак матки. Спустя три года после лечения у пациенток с первой стадией не было замечено следов болезни в 86% случаев, а общая выживаемость составила 90%, при 2 и 3 стадиях, соответственно 65 и 85%, а вот при четвертой стадии получилось гораздо хуже - 0 и 17%. При этом, согласно китайской статистике, при химиотерапии выживаемость за пять лет при 2 и 3 стадиях рака составляет 53-74%, а для 4 стадии: 20-30%. В общем, медики внимательно присматриваются к этому новому методу лечения и пытаются подобрать более эффективные методики, только дело это небыстрое.
P.S.
И лечит и колечит. Но, при этом не доступен, обычному "Смертному".
Зачем калифорний физикам? Этот элемент участвует в уникальных экспериментах, которыми физики пытаются выяснять пути синтеза новых элементов. Один из них - опыты по изучению ионов с большим содержанием нейтронов, которые проводят в Аргоннской национальной лаборатории Минэнерго США на установке CARIBU (Californium Rare Isotope Breeder Upgrade). Источником этих ионов как раз и служит калифорний-252. При его спонтанном делении образуются осколки - ионы менее тяжелых элементов, которые еще не пришли в равновесие и содержат много лишних нейтронов. Их бережно собирают и охлаждают в ловушке, заполненной гелием, разделяют с помощью магнитных полей, электронным пучком сдирают значительную часть электронных оболочек, и такие полуголые ядра собирают в пучки, которые либо отправляют в линейный ускоритель, где разгоняют до высоких энергий, либо отправляют в установку низкоэнергетических пучков. Эти ионы и служат объектами либо инструментами исследований. Есть предложения использовать калифорниевые ионы для решения чрезвычайно важного вопроса: постоянна ли постоянная тонкой структуры - одна из важнейших фундаментальных констант, определяющих конфигурацию нашего мира. Подозрения о том, что она меняется либо с течением времени, либо в пространстве, стали закрадываться после выявления особенностей спектров свечения квазаров - они как раз расположены на границе видимой Вселенной, то есть очень давно и далеко от нас. По идее, заметить аномалии в поведении постоянной тонкой структуры можно и на Земле, проследив за изменениями спектральных линий в точнейших атомных часах. Однако в имеющихся часах точность измерения слишком мала для этого. Ее можно поднять, если использовать ионы, потерявшие много электронов, и весьма перспективными оказываются ионы радиоактивных актиноидов.
А вот у калифорния-249 есть совершенно неожиданное использование - именно из него была сделана мишень весом в 10 мг, бомбардировкой которой ядрами кальция-48 был получен самый тяжелый элемент таблицы Менделеева - 118, оганессон. К сожалению, калифорний оказался последним мало-мальски стабильным элементом, из которого можно сделать мишень, - остальные живут столь мало, что провести опыты по их бомбардировке проверенным кальцием-48 нельзя. Поэтому после синтеза оганессона физики взяли паузу и ищут новые идеи для дальнейшего продвижения в сторону гипотетического острова стабильности со сверхтяжелыми элементами.
Сейчас в Дубне строят фабрику тяжелых элементов - модернизируют ускоритель тяжелых ионов, чтобы вести обстрел мишени десятикратно более мощным пучком. Предполагается, что такой пучок из ядер титана-44 при ударе о мишень из калифорния даст первые изотопы 119-го элемента.
Можно ли из калифорния сделать атомную пулю? Нет, только маленький ракетный снаряд. Расчет тут простой. Спонтанно-делящийся элемент может взорваться в результате развития цепной реакции. Однако его масса должна быть больше критической – при меньшей массе нейтронов для поддержания цепной реакции не хватит. Критическая масса калифорния-252 - 2,7 кг. При плотности 15 г/см3 это будет цилиндр высотой 15 см и диаметром 2 см. И по размеру, и по массе это соответствует ударной части противотанкового снаряда. Однако при огромной стоимости калифорния нет никакого смысла использовать такой снаряд, чтобы вывести из строя многократно более дешевый танк. Поэтому использовать калифорний в качестве компонента вооружений можно только в фантастических произведениях.
Калифорний назван в честь Калифорнийского университета в Беркли, где в 1950 году его получила группа ученых под руководством обладателя Нобелевской премии по химии и участника Манхэттенского проекта Гленна Сиборга.
Создатель калифорния и один из основоположников ядерной химии Гленн Сиборг причастен к открытию десяти новых элементов таблицы Менделеева, один из которых в его честь получил название сиборгий.
С калифорнием работают только Научно-исследовательский институт атомных реакторов (НИИАР) в Димитровграде и Национальная лаборатория Оук-Ридж в США.
Калифорний относится к числу самых дорогих веществ в мире. По некоторым оценкам, один грамм этого вещества стоит 26 миллионов долларов.
P.S. Если сравнить "Некие" материалы, (Опять же по весу) якобы доставленные с луны. и, сопоставить "Некие" материалы входящие в стостав производства калифорния-252 - То вырисовываюсться "Некие" похожие показатели, а тем более - цыфры (По стоимости).
Радиоактивный металл и его свойства. Какой самый радиоактивный металл
Среди всех элементов периодической системы значительная часть принадлежит таким, о которых большинство людей говорят со страхом. А как же иначе? Ведь они являются радиоактивными, а это означает прямую угрозу здоровью людей.
Попробуем разобраться, какие же именно элементы являются опасными, и что они собой представляют, а также выясним, в чем заключается их вредоносное действие на организм человека.

Общее понятие о группе радиоактивных элементов
В данную группу входят металлы. Их достаточно много, располагаются они в периодической системе сразу после свинца и до самой последней ячейки. Главный критерий, по которому принято относить тот или иной элемент к группе радиоактивных, - это его способность обладать определенным периодом полураспада.
Другими словами, радиоактивный распад - это преобразование ядра металла в другое, дочернее, которое сопровождается испусканием излучения определенного вида. При этом происходят превращения одних элементов в другие.
Радиоактивный металл - это тот, у которого хотя бы один изотоп является таковым. Даже если всего разновидностей будет шесть, и при этом лишь одна из них будет носителем данного свойства, весь элемент станет считаться радиоактивным.
Виды излучений
Основными вариантами излучения, которое испускается металлами при распадах, являются:
- альфа-частицы;
- бета-частицы или нейтринный распад;
- изомерный переход (гамма-лучи).
Есть два варианта существования подобных элементов. Первый - это естественный, то есть когда радиоактивный металл встречается в природе и самым простым путем под влиянием внешних сил с течением времени преобразуется в иные формы (проявляет свою радиоактивность и распадается).

Вторая группа - это искусственно созданные учеными металлы, способные к быстрому распаду и мощному выделению большого количества радиационного излучения. Делается это для использования в определенных сферах деятельности. Установки, в которых производятся ядерные реакции по превращениям одних элементов в другие, называются синхрофазотронами.
Разница между двумя обозначенными способами полураспада очевидна: в обоих случаях он самопроизвольный, однако лишь искусственно полученные металлы дают именно ядерные реакции в процессе деструктуризации.
Основы обозначения подобных атомов
Так как у большей части элементов лишь один или два изотопа являются радиоактивными, принято указывать конкретный вид при обозначениях, а не весь элемент в целом. Например, свинец - это просто вещество. Если же принимать во внимание, что он - радиоактивный металл, то следует называть его, например, "свинец-207".
Периоды полураспада рассматриваемых частиц могут сильно варьироваться. Есть изотопы, которые существуют лишь 0,032 секунды. Но наравне с ними встречаются и те, что распадаются миллионы лет в земных недрах.
Радиоактивные металлы: список
Полный перечень всех принадлежащих к рассматриваемой группе элементов может быть достаточно внушительным, ведь всего к ней относятся около 80 металлов. В первую очередь это все, стоящие в периодической системе после свинца, включая группу лантаноидов и актиноидов. То есть висмут, полоний, астат, радон, франций, радий, резерфордий и так далее по порядковым номерам.

Выше обозначенной границы располагается множество представителей, каждый из которых также имеет изотопы. При этом некоторые из них могут быть как раз радиоактивными. Поэтому важно, какие разновидности имеет химический элемент. Радиоактивный металл, точнее одна из его изотопных разновидностей, есть практически у каждого представителя таблицы. Например, их имеют:
- кальций;
- селен;
- гафний;
- вольфрам;
- осмий;
- висмут;
- индий;
- калий;
- рубидий;
- цирконий;
- европий;
- радий и другие.
Таким образом, очевидно, что элементов, проявляющих свойства радиоактивности, очень много - подавляющее большинство. Часть из них безопасна из-за слишком длинного периода полураспада и содержится в природе, другая же создана искусственно человеком для различных нужд в науке и технике и является крайне опасной для организма людей.
Характеристика радия
Название элементу дано его первооткрывателями - супругами Кюри, Пьером и Марией. Именно эти люди впервые обнаружили, что один из изотопов этого металла - радий-226 - это наиболее устойчивая форма, обладающая особыми свойствами радиоактивности. Это произошло в 1898 году, и о подобном явлении только стало известно. Подробным его изучением как раз и занялись супруги химики.
Этимология слова берет корни из французского языка, на котором оно звучит как radium. Всего известно 14 изотопных модификаций данного элемента. Но наиболее устойчивые формы с массовыми числами:
Ярко выраженной радиоактивностью обладает форма 226. Сам по себе радий - химический элемент под номером 88. Атомная масса [226]. Как простое вещество способен к существованию. Представляет собой серебристо-белый радиоактивный металл с температурой плавления около 670 0 С.

С химической точки зрения проявляет достаточно высокую степень активности и способен реагировать с:
- водой;
- органическими кислотами, формируя устойчивые комплексы;
- кислородом, образуя оксид.
Свойства и применение
Также радий - химический элемент, который формирует ряд солей. Известны его нитриды, хлориды, сульфаты, нитраты, карбонаты, фосфаты, хроматы. Также есть двойные соли с вольфрамом и бериллием.
То, что радий-226 может быть опасен для здоровья, его первооткрыватель Пьер Кюри узнал не сразу. Однако сумел убедиться в этом, когда провел эксперимент: сутки он ходил с привязанной к плечевой части руки пробиркой с металлом. На месте контакта с кожей появилась незаживающая язва, избавиться от которой ученый не мог больше двух месяцев. От своих экспериментов над явлением радиоактивности супруги не отказались, поэтому и умерли оба от большой дозы облучения.
Помимо отрицательного значения, существует и ряд областей, в которых радий-226 находит применение и приносит пользу:
Плутоний и его изотопы
Данный элемент был открыт в сороковых годах XX века американскими учеными. Впервые его выделили из урановой руды, в которой он сформировался из нептуния. Последний при этом - результат распада уранового ядра. То есть все они между собой тесно взаимосвязаны общими радиоактивными превращениями.

Существует несколько устойчивых изотопов данного металла. Однако наиболее распространенной и важной практически разновидностью является плутоний-239. Известны химические реакции данного металла с:
- кислородом,
- кислотами;
- водой;
- щелочами;
- галогенами.
По своим физическим свойствам плутоний-239 является хрупким металлом с температурой плавления 640 0 С. Основные способы воздействия на организм - это постепенное формирование онкологических заболеваний, накапливание в костях и вызывание их разрушения, заболевания легких.
Область использования - в основном ядерная промышленность. Известно, что при распаде одного грамма плутония-239 выделяется такое количество теплоты, которое сравнимо с 4-мя тоннами сгоревшего угля. Именно поэтому этот вид металла находит такое широкое применение в реакциях. Ядерный плутоний - источник энергии в атомных реакторах и термоядерных бомбах. Он же используется при изготовлении электрических аккумуляторов энергии, срок службы которых может достигать пяти лет.
Уран - источник радиации
Данный элемент был открыт в 1789 году химиком из Германии Клапротом. Однако исследовать его свойства и научиться применять их на практике люди сумели лишь в XX веке. Основная отличительная особенность в том, что радиоактивный уран способен при естественном распаде образовывать ядра:
- свинца-206;
- криптона;
- плутония-239;
- свинца-207;
- ксенона.
В природе этот металл светло-серого цвета, обладает температурой плавления свыше 1100 0 С. Встречается в составе минералов:
- Урановые слюдки.
- Уранинит.
- Настуран.
- Отенит.
- Тюянмунит.
Известны три стабильных природных изотопа и 11 искусственно синтезированных, с массовыми числами от 227 до 240.

В промышленности широко используется радиоактивный уран, способный быстро распадаться с высвобождением энергии. Так, его используют:
- в геохимии;
- горном деле;
- ядерных реакторах;
- при изготовлении ядерного оружия.
Влияние на организм человека ничем не отличается от предыдущих рассмотренных металлов - накопление приводит к повышенной дозе облучения и возникновению раковых опухолей.
Трансурановые элементы
Самыми главными из металлов, стоящих вслед за ураном в периодической системе, являются те, что были открыты совсем недавно. Буквально в 2004 году в свет вышли источники, подтверждающие рождение на свет 115 элемента периодической системы.
Им стал самый радиоактивный металл из всех известных на сегодняшний день - унунпентий (Uup). Его свойства остаются не изученными до сих пор, ведь период полураспада составляет 0,032 секунды! Рассмотреть и выявить подробности строения и проявляемые особенности при таких условиях просто невозможно.
Однако его радиоактивность во много раз превосходит показатели второго по данному свойству элемента - плутония. Тем не менее используется на практике не унунпентий, а более "медленные" его товарищи по таблице - уран, плутоний, нептуний, полоний и прочие.
Еще один элемент - унбибий - теоретически существует, однако доказать это практически ученые разных стран не могут с 1974 года. Последняя попытка была совершена в 2005 году, однако оказалась не подтвержденной общим советом ученых-химиков.
Торий
Был открыт еще в XIX веке Берцелиусом и назван в честь скандинавского бога Тора. Является слаборадиоактивным металлом. Такой особенностью обладают пять из его 11-ти изотопов.
Основное применение в ядерной энергетике основано не на способности испускать огромное количество тепловой энергии при распаде. Особенность в том, что ядра тория способны захватывать нейтроны и превращаться в уран-238 и плутоний-239, которые уже и вступают непосредственно в ядерные реакции. Поэтому и торий можно отнести к группе рассматриваемых нами металлов.

Полоний
Серебристо-белый радиоактивный металл под номером 84 в периодической системе. Открыт был все теми же ярыми исследователями радиоактивности и всего, что с ней связано, супругами Марией и Пьером Кюри в 1898 году. Главная особенность этого вещества в том, что оно свободно существует около 138,5 дней. То есть таков период полураспада данного металла.
В природе встречается в составе урановых и других руд. Используется как источник энергии, причем достаточно мощной. Является стратегическим металлом, так как применяется для изготовления ядерного оружия. Количество строго ограничено и находится под контролем каждого государства.
Также используется для ионизации воздуха, устранения статического электричества в помещении, при изготовлении космических обогревателей и прочих схожих предметов.
Воздействие на организм человека
Все радиоактивные металлы обладают способностью проникать сквозь кожу человека и накапливаться внутри организма. Они очень плохо выводятся с продуктами жизнедеятельности, вообще не выводятся с потом.
Со временем начинают поражать дыхательную, кровеносную, нервную системы, вызывая в них необратимые изменения. Воздействуют на клетки, заставляя их функционировать неправильно. В результате происходит образование злокачественных опухолей, возникают онкологические заболевания.
Поэтому каждый радиоактивный металл - большая опасность для человека, особенно если говорить о них в чистом виде. Нельзя трогать их незащищенными руками и находиться в помещении вместе с ними без специальных защитных приспособлений.
Радий – полезные свойства, особенности и угроза металла
По названию этого химического элемента названо явление радиоактивности. Радий – самый радиоактивный металл на планете. Однако ему нашли применение ученые, геологи и врачи.

Что представляет собой
Радий – это химический элемент таблицы Д.И. Менделеева №88.
Металл цвета серебра – продукт многоступенчатого распада урана-238:
- В темноте радий испускает голубоватый свет. По этой характеристике его легко отличить от других элементов.
- В честь него назван феномен радиоактивности.
Радиоактивность измеряется в кюри (Ки). 1 Ки – это 37 миллиардов распадов ежесекундно.
- Относится к щелочноземельным металлам.
- Структура кристаллической решетки – объемно-центрированный куб.
- Известно 35 природных и созданных изотопов элемента, все нестабильны. Самый устойчивый – 226 (период полураспада 1603 года). Некоторые «живут» доли секунды.
Международное обозначение и формула элемента – Radium (Ra).
Как был открыт
Открытие радия (1898 год) – заслуга Марии Кюри:
- Годами она работала с урановой смолкой. Это были отходы с местного предприятия. После извлечения урана они должны были быть «чистыми», но «фонили» сильнее чистого урана.
- Позднее к ней присоединился супруг Пьер и коллега Жан Бемон.
- Лишь через 12 лет была получена первая в истории «песчинка» чистого радия.
В тонне урановой смолки, которую перерабатывали супруги Кюри, было 0,1 г радия.
- Первые образцы стали самым дорогим веществом на планете: цена 1 г радия превосходила стоимость двух центнеров золота.
Попутно Мария открыла элемент, который назвала полонием – в честь своей родной страны Польши.

Отопление радием-камин 21 века. Французская карточка 1910 года
За открытие радия Марии Склодовской-Кюри присудили в 1911 году Нобелевскую премию.
В радии как металле с «подсветкой» видели неисчерпаемый источник тепла и света. Однако вскоре обнаружилась смертельная опасность радиации для биологических структур.
Название восходит к латинскому radius – луч. Так радиоактивный элемент назвали за постоянную светимость.
Ра – верховный бог Солнца у древних египтян.
Физико-химические характеристики
Химические свойства этого щелочноземельного металла сходны с барием, но проявляются интенсивнее:
- Реакция с водой сопровождается образованием водорода.
- На воздухе радий тускнеет, покрываясь оксидно-нитридным слоем.
- Образует самые прочные (из щелочноземельных металлов) соединения с органическими кислотами.

Главное свойство вещества – радиоактивность:
Благодаря радиоактивности радий, его соединения отсвечивают в темноте.
| Свойства атома | |
|---|---|
| Название, символ, номер | Ра́дий / Radium (Ra), 88 |
| Атомная масса (молярная масса) | 226,0254 а. е. м. (г/моль) |
| Электронная конфигурация | [Rn] 7s2 |
| Химические свойства | |
| Радиус иона | (+2e) 143 пм |
| Электроотрицательность | 0,9 (шкала Полинга) |
| Электродный потенциал | Ra←Ra2+ −2,916 В |
| Степени окисления | 2 |
| Энергия ионизации (первый электрон) | 1-й 509,3 (5,2785) кДж/моль (эВ) 2-й 979,0 (10,147) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
| Плотность (при н. у.) | (при к.т.) 5,5 г/см³ |
| Температура плавления | 1233 K |
| Температура кипения | 2010 K |
| Уд. теплота плавления | 8,5 кДж/моль |
| Уд. теплота испарения | 113 кДж/моль |
| Молярная теплоёмкость | 29,3 Дж/(K·моль) |
| Молярный объём | 45,0 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | кубическая объёмноцентрированая |
| Параметры решётки | 5,148 |
| Прочие характеристики | |
| Теплопроводность | (300 K) (18,6) Вт/(м·К) |
| Номер CAS | 7440-14-4 |
Нахождение в природе
Радий – рассеянный элемент, микроконцентрации обнаружены в различных объектах.

Радиоактивный элемент Радия
Элемент распределен по биосфере неравномерно:
- Главный источник металла – урановая руда.
- Радий всегда содержат руды тория.
- Вымываясь оттуда, попадает в воду, нефтяные, газоносные пласты. Найден во вторичных минералах свинца.
Тонна урана из урановой руды содержит 0,34 г радия. Тонна земной коры – 1 мкг.
За более чем 120 лет – со времени открытия – на Земле удалось получить полтора кг вещества.
Все природные изотопы радия сведены в таблицу:
| Изотоп | Историческое название | Семейство | Период полураспада | Тип распада | Дочерний изотоп (историческое название) |
|---|---|---|---|---|---|
| Радий-223 | актиний Х (AcX) | ряд урана-235 | 11,435 дня | α | радон-219 (актинон, An) |
| Радий-224 | торий Х (ThX) | ряд тория-232 | 3,66 дня | α | радон-220 (торон, Tn) |
| Радий-226 | радий (Ra) | ряд урана-238 | 1602 года | α | радон-222 (радон, Rn) |
| Радий-228 | мезоторий I (MsTh1) | ряд тория-232 | 5,75 года | β | актиний-228 (мезоторий II, MsTh2) |
Технология получения
- Радий выделяют из урановой руды, получение металла базируется на электролизе. Рабочим материалом выступают растворенный хлорид радия и ртуть как катод.
- Второй способ получения – из природных вод, которые выщелачивают радий из минералов с ураном в составе.
Производство относится к вредным: требуются специальные средства защиты, соблюдение правил техники безопасности.
Где используется
Использовать новое вещество начали сразу. Супруги Кюри не запатентовали продукт, считая его всеобщим достоянием. Предприимчивые граждане воспользовались этим.
«Философский камень»
Рынок Европы и Америки заполонила чудодейственная продукция: «молодильные» кремы, пудры, зубные пасты. Мошенники изготавливали также хлеб, печенье, шоколадки, «лечебную» воду, средство для повышения потенции.
Бум продержался двадцать лет, пока не была доказана опасность увлечения веществом.
Промышленность
Радий был микрокомпонентом светящейся краски. Ею снабжали циферблаты армейских компасов, часов, авиационных, морских приборов. В 1970-х радий заменили менее агрессивным тритием.

Советский армейский компас. Жёлтая краска содержит радий
Сферы применения единичны:
- В сплаве с бериллием – производитель альфа-частиц в радиево-бериллиевых накопителях нейтронов.
- Светящиеся составы (с сульфидом цинка).
- Маркер качества литья, сварных швов.
- Нейтрализация электростатических зарядов.
Применение вещества ограничивается главным недостатком – радиоактивностью.
Другие сферы
- Геологи применяют радиевые изотопы для определения возраста минералов, осадочных пород.
- Для геохимиков это индикатор движения океанской воды и концентрации урана.
- Ювелиры облучают радием драгоценные камни для улучшения цвета.
- Для медицины радий – источник газа радона (его добавляют в лечебные ванны). Кратковременное облучение радием – метод борьбы с онкологией.
Биологическое воздействие
Радий проникает в живые организмы:
- В растительном мире его больше в стволах деревьев.
- Организм животных и человека получает его с водой, пищей.
- Четыре пятых поступившего радия оседает в костях.
- Концентрация вещества определяется пищевым рационом и районом проживания.
По стандартам РФ, кубический метр воздуха не должен содержать более 0,000001 мкг радия.
Нанодозы вещества полезны, превышение чревато онкологией. Поэтому критически важно видеть барьер, после которого достоинства материала становятся недостатками.
Радиоактивные металлы
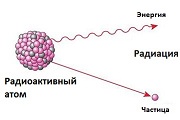
Радиоактивные металлы — это металлы, которые самопроизвольно излучают поток элементарных частиц во внешнюю среду. Этот процесс называют альфа(α), бета(β), гамма(γ) излучением или просто радиоактивным излучением.
Все радиоактивные металлы со временем распадаются и превращаются в стабильные элементы (иногда проходя целую цепочку превращений). У разных элементов радиоактивный распад может длиться от нескольких миллисекунд до нескольких тысяч лет.
Рядом с названием радиоактивного элемента часто указывается массовое число его изотопа. Например, Технеций-91 или 91 Tc. Разные изотопы одного и того же элемента как правило имеют общие физические свойства и различаются лишь длительностью радиоактивного распада.

Список радиоактивных металлов
| Название рус. | Название eng. | Самый стабильный изотоп | Период распада |
|---|---|---|---|
| Технеций | Technetium | Tc-91 | 4.21 x 10 6 лет |
| Прометий | Promethium | Pm-145 | 17.4 года |
| Полоний | Polonium | Po-209 | 102 года |
| Астат | Astatine | At-210 | 8.1 часов |
| Франций | Francium | Fr-223 | 22 минут |
| Радий | Radium | Ra-226 | 1600 лет |
| Актиний | Actinium | Ac-227 | 21.77 лет |
| Торий | Thorium | Th-229 | 7.54 x 10 4 лет |
| Протактиний | Protactinium | Pa-231 | 3.28 x 10 4 лет |
| Уран | Uranium | U-236 | 2.34 x 10 7 лет |
| Нептуний | Neptunium | Np-237 | 2.14 x 10 6 лет |
| Плутоний | Plutonium | Pu-244 | 8.00 x 10 7 лет |
| Америций | Americium | Am-243 | 7370 лет |
| Кюрий | Curium | Cm-247 | 1.56 x 10 7 лет |
| Беркелий | Berkelium | Bk-247 | 1380 лет |
| Калифорний | Californium | Cf-251 | 898 лет |
| Эйнштейний | Einsteinium | Es-252 | 471.7 дней |
| Фермий | Fermium | Fm-257 | 100.5 дней |
| Менделевий | Mendelevium | Md-258 | 51.5 дней |
| Нобелий | Nobelium | No-259 | 58 минут |
| Лоуренсий | Lawrencium | Lr-262 | 4 часа |
| Резенфордий | Rutherfordium | Rf-265 | 13 часов |
| Дубний | Dubnium | Db-268 | 32 часа |
| Сиборгий | Seaborgium | Sg-271 | 2.4 минуты |
| Борий | Bohrium | Bh-267 | 17 секунд |
| Ганий | Hassium | Hs-269 | 9.7 секунд |
| Мейтнерий | Meitnerium | Mt-276 | 0.72 секунды |
| Дармштадий | Darmstadtium | Ds-281 | 11.1 секунды |
| Рентгений | Roentgenium | Rg-281 | 26 секунд |
| Коперниций | Copernicium | Cn-285 | 29 секунд |
| Унунтрий | Ununtrium | Uut-284 | 0.48 секунд |
| Флеровий | Flerovium | Fl-289 | 2.65 секунд |
| Унунпентий | Ununpentium | Uup-289 | 87 миллисекунд |
| Ливерморий | Livermorium | Lv-293 | 61 миллисекунда |
Радиоактивные элементы делятся на естественные (существующие в природе) и искусственные (получаемые в результате лабораторного синтеза). Естественных радиоактивных металлов не много — это полоний, радий, актиний, торий, протактиний и уран. Их наиболее стабильные изотопы встречаются в природе, чаще в виде руды. Все остальные металлы из списка созданы человеком.
Самый радиоактивный металл
Самый радиоактивный металл на данный момент — ливерморий. Его изотоп Ливерморий-293 распадается всего за 61 милисекунду. Впервые этот изотоп был получен в Дубне, в 2000 году.
Другой очень радиоактивный металл — унунпентий. Изотоп унунпентий-289 имеет чуть больший период распада (87 милисекунд).
Из более-менее стабильных, практически применяемых веществ, самым радиоактивным металлом считается полоний (изотоп полоний-210). Это серебристый белый радиоактивный металл. Хотя его период полураспада достигает 100 и более дней, даже один грамм этого вещества раскаляется до 500°C, а излучение может мгновенно убить человека.
Что такое радиация
Всем известно, что радиация очень опасна и лучше держаться подальше от радиоактивного излучения. С этим трудно поспорить, хотя в реальности мы постоянно подвержены влиянию радиации, где бы не находились. В земле залегает довольно большое количество радиоактивной руды, а из космоса на Землю постоянно прилетают заряженные частицы.
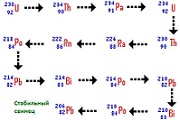
Кратко говоря, радиация это самопроизвольное испускание элементарных частиц. От атомов радиоактивного вещества отделяются протоны и нейтроны, «улетая» во внешнюю среду. Ядро атома при этом постепенно изменяется, превращаясь в другой химический элемент. Когда все нестабильные частицы отделяются от ядра, атом перестает быть радиоактивным. Например, торий-232 в конце своего радиоактивного распада превращается в стабильный свинец.
Наука выделяет 3 основных вида радиоактивного излучения
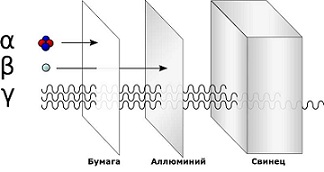
Альфа излучение(α) — поток альфа-частиц, положительно заряженных. Они сравнительно большие по размеру и плохо проходят даже через одежду или бумагу.
Бета излучение(β) — поток бета-частиц, негативно заряженных. Они довольно малы, легко проходят через одежду и проникают внутрь клеток кожи, что наносит большой вред здоровью. Но бета-частицы не проходят через плотные материалы, такие как алюминий.
Гамма излучение(γ) — это высокочастотная электромагнитная радиация. Гамма-лучи не имеют заряда, но содержат очень много энергии. Скопление гамма-частиц излучает яркое свечение. Гамма-частицы проходят даже через плотные материалы, что делает их очень опасными для живых существ. Их останавливают только самые плотные материалы, например, свинец.
Все эти виды излучения так или иначе присутствуют в любой точке планеты. Они не представляют опасности в малых дозах, но при высокой концентрации могут причинить очень серьезный ущерб.
Изучение радиоактивных элементов



Первооткрывателем радиоактивности является Вильгельм Рентген. В 1895 году этот Прусский физик впервые наблюдал радиоактивное излучение. На основе этого открытия был создан знаменитый медицинский прибор, названый в честь ученого.
В 1896 г изучение радиоактивности продолжил Анри Беккерель, он экспериментировал с солями урана.
В 1898 г Пьер Кюри в чистом виде получил первый радиоактивный металл — Радий. Кюри хоть и открыл первый радиоактивный элемент, однако, не успел толком его изучить. И выдающиеся свойства радия привели к быстрой гибели ученого, который беспечно носил свое «детище» в нагрудном кармане. Великое открытие отомстило своему первооткрывателю — Кюри умер в возрасте 47 лет от мощной дозы радиоактивного облучения.
В 1934 г был впервые синтезирован искусственный радиоактивный изотоп.
Сейчас изучением радиоактивности занимаются множество ученых и организаций.
Добыча и синтез



Даже естественные радиоактивные металлы не встречаются в природе в чистом виде. Их синтезируют из урановой руды. Процесс получения чистого металла чрезвычайно трудоемок. Состоит он из нескольких стадий:
- концентрирование (дробление и выделение осадка с ураном в воде);
- выщелачивание - то есть, перевод уранового осадка в раствор;
- выделение чистого урана из полученного раствора;
- перевод урана в твердое состояние.
В итоге, из тонны урановой руды можно получить всего несколько граммов урана.
Синтез искусственных радиоактивных элементов и их изотопов проходит в специальных лабораториях, в которых создаются условия для работы с подобными веществами.
Практическое применение
Чаще всего, радиоактивные металлы используют для выработки энергии.
Ядерные реакторы — это устройства, использующие уран для нагревания воды и создания потока пара, который вращает турбину, с помощью чего вырабатывается электричество.


Вообще, сфера применения радиоактивных элементов довольно широка. Они используются для изучения живых организмов, диагностирования и лечения болезней, выработки энергии и для мониторинга промышленных процессов. Радиоактивные металлы являются основой для создания ядерного оружия — самого разрушительного оружия на планете.
Читайте также:
