Самым легким металлом является
Обновлено: 04.10.2024
Хотя человек на примере отдельных столовых приборов неоднократно убеждался, что металлические предметы способны оказаться вовсе и не тяжелыми, все-таки металл представляется последнему в первую очередь как нечто, с трудом поддающееся разрушению под воздействием внешних сил, а оттого и по весу впечатляющее.
Однако в этой статье речь пойдет о самых легких металлах в мире: какими свойствами обладают, для чего используются и чем представляют интерес — об этом расскажет редакция 24СМИ.
Титан (Ti)
Открытый в конце XVIII столетия и сразу добавленный в периодическую таблицу Менделеева под 22-м номером химический элемент серебристого цвета с атомной массой в 47,867 а. е. м. (атомная единица массы) и плотностью в 4,5 г/см^3 отличается впечатляющей прочностью.
Также среди свойств металла, получившего статус самого твердого из используемых, выделяют отличную антикоррозионную устойчивость. Это справедливо и для сплавов, получаемых на основе титана, причем собственные прочностные характеристики последние сохраняют даже при температурах в 300 °C, что делает их незаменимыми в текущий период времени в авиации и ракетостроении.
Получивший название в честь титанов из древнегреческой мифологии металл входит в десятку самых распространенных в природе элементов, месторождения которого открыты на всех континентах, исключая Антарктиду. Причем Россия занимает по концентрации руд с содержанием рассматриваемого элемента второе место в мире после КНР.
Помимо уже упомянутых отраслей, титановые сплавы востребованы в кораблестроении, химической, автомобильной и оборонной промышленности, а также на пищевом производстве и в сельском хозяйстве. Благодаря собственной инертности титан без проблем способен контактировать с тканями живых организмов, не вызывая опасных для здоровья химических реакций, а потому активно используется в медицине, начиная с протезирования и изготовления имплантатов и заканчивая созданием хирургических инструментов.
Алюминий (Al)
Алюминий относится к наиболее распространенным цветным металлам. Открытый в 1825 году и до освоения технологии промышленного изготовления стоивший дороже золота, элемент с атомным номером 13 и массой в 26,982 а. е. м. имеет плотность 2,7 г/см^3 и отличается наличием парамагнитных свойств, правда, слабых.
Хорошо проводит тепло и электричество, не поддается коррозионному воздействию, зато подвержен механическому, в том числе легко подвергается сгибанию. Сплавы на основе этого легкого металла характеризуются пластичностью, удовлетворительной прочностью и не поддаются коррозии, а также хорошо свариваются.
По распространенности в мире алюминий стоит на первом месте среди металлов и на третьем среди химэлементов периодической таблицы, уступая только кислороду и кремнию. Добыча его ведется более чем в 15 странах, лидеры среди которых — Китай, Россия и Канада. Мировые запасы этого элемента в разы превышают текущую потребность в его применении.
Сфера использования алюминия и сплавов на основе этого материала обширна. Это и черная металлургия, и пиротехника, использовался даже для изготовления ювелирных украшений в тот период, когда представлял исключительную ценность из-за неотработанного техпроцесса. В Японии он применяется в таком качестве до сих пор, заменяя иногда серебро в украшениях.
О посуде и столовых приборах из этого гибкого металла знают все, а вот в качестве конструкционных материалов используют преимущественно алюминиевые сплавы, обладающие требуемыми характеристиками в плане прочности. Также алюминий добавляют в «автоматные стали» для облегчения обработки — благодаря ему достигается четкое открепление от прута детали после завершения обработки.
Бериллий (Be)
В отличие от предыдущих, этот металл, расположенный в таблице химэлементов под номером 4, отличает сероватый цвет, а также повышенная токсичность. Характеризуется хрупкостью при сравнительной твердости, превосходящей показатели алюминия и магния. Плотность — 1,8 г/см^3. Атомная масса — 9 углеродных единиц.
Открытый в конце XVIII века, в чистом виде впервые был получен только спустя 30 лет, в 1828 году. Название свое унаследовал от минерала берилла, который, в свою очередь, наименованием обязан индийскому городу Белуру, прославившемуся месторождением изумрудов — драгоценных камней, представляющих собой разновидность упомянутой породы.
Бериллий часто встречается в составе темноцветных минералов, а также в магматических породах. Месторождения, содержащие этот металл, расположены на территории Южной Америки и Африки. На евразийском континенте также ведется добыча, преимущественно в Индии, Казахстане и России, в границах которой находятся два месторождения — в Свердловской области и в Бурятии.
Металл применяют в легировании сплавов в качестве добавки, делающей получаемые материалы более твердыми, прочными и устойчивыми к коррозии. Слабое поглощение бериллием рентгеновского излучения позволяет применять его при создании детекторов гамма-лучей. Применяется и в ядерной энергетике в качестве замедлителя нейтронов. Бериллиевые сплавы используют в аэрокосмической технике и для изготовления лазерных излучателей.
Также металл хорошо проводит звуковые волны, благодаря чему применяется в конструкции акустических устройств, однако из-за высокой сложности обработки для исключения негативных качеств, включая токсичность, изготовленные на его основе компоненты отличаются повышенной стоимостью. Представляет опасность для человека — накапливаясь в организме, приводит к тяжелому поражению органов дыхания, а также характеризуется выраженным канцерогенным воздействием.
Магний (Mg)
Расположенный в таблице Менделеева под 12-м номером ковкий металл с атомной массой 24,307 а. е. м. и плотностью 1,7 г/см^3 впервые был получен в чистом виде в 1808 году. Пластичен и легко поддается прессованию и резанию.
Характеризуется высокой температурой плавления (650 °C) и коррозионной стойкостью. При создании на основе магния сплавов механические характеристики металла существенно повышаются, что сильно расширяет область применения такого рода материалов.
Элемент входит в список наиболее распространенных на Земле и встречается как в коре, так и в морской воде, как правило, в составе солей и минералов. Природные месторождения самородного магния чрезвычайно редки — пара таких расположены на территории России, в Восточной Сибири, и Таджикистана. Лидером по производству магния на 2020-й считаются США.
Главным образом применяется для получения всевозможных сплавов, как легких, так и сверхлегких, сфера использования которых — это самолето- и автомобилестроение. Также благодаря горючим свойствам применяется в пиротехнике и при создании зажигательных и осветительных ракет в оборонной промышленности.
Без магниевого порошка с добавками окислителей прежде невозможной была бы фотография — хотя в сравнении с прошлым магниевые вспышки используются намного реже, спрос на них по-прежнему сохраняется. Также магний относится к веществам, важным для нормальной жизнедеятельности организма и протекания обменных процессов, так что препараты на его основе применяются в медицине — в кардиологии, неврологии и при борьбе с гастроэнтерологическими расстройствами.
Литий (Li)
Вот и дошло дело до элемента, который является самым легким в мире металлом. Плотность лития, расположенного в периодической таблице на месте под цифрой 3, равна всего 0,5 г/см^3, что меньше этого показателя у воды, так что чистый литий не тонет. Атомная масса элемента колеблется от 6,398 до 6,997 а. е. м. в зависимости от изотопа. Открыт в 1817-м, а в металлическом виде получен спустя всего год.
Характеризуется повышенной химической активностью и потому в природе легко образует сложносоставные соединения. Пластичен, хорошо обрабатывается прокаткой и прессом. Цвет — серебристый. При комнатной температуре с кислородом реагирует слабо. Воспламенение происходит при 300 °C.
В природе встречается в породообразующих минералах и в отложениях озер с сильным содержанием солей. Среди разрабатываемых месторождений наиболее известны чилийские, австралийские и аргентинские, хотя встречаются таковые и на территории других стран, в том числе Китая. В России главное скопление пород с содержанием лития — в Мурманской области. В стране с 2017 года работает в формате эксперимента установка по добыче металла из руд с низким содержанием элемента, благодаря которой процедура возможна при незначительных финансовых и трудовых затратах.
Соли лития используются при создании лазерного оборудования и оптики, в качестве окислителей и восстановителей в химпроме, а также в медицине и различных отраслях промышленности, включая текстильную (как отбеливатели), пищевую (как консерванты) и косметическую. Литиевые сплавы применяются для изготовления высокоэффективных проводников, в том числе анодов, необходимых для электролиза.
Элемент применяется также при создании аккумуляторов, в том числе и щелочных, а не только твердотельных. В малых количествах литий потребен человеческому организму, поскольку участвует в обмене веществ, а также влияет на психоэмоциональную возбудимость и иммунную защиту.
Какой металл самый легкий? Его свойства и особенности
Слово «металл» часто ассоциируется с тяжеловесностью. Это далеко не так. Все металлы обладают очень разными свойствами. Некоторые из них настолько лёгкие, что даже не тонут в воде. Какой металл самый легкий? Какие у него свойства? Давайте узнаем.
Самые легкие металлы в мире
Лёгкими называют металлы, которые обладают небольшой плотностью. Это отнюдь не редкое явление. Вещества с такими характеристиками составляют примерно 20 % от массы земной коры. Они активно добываются и широко применяются в промышленности.
Самым лёгким металлом является литий. Кроме наименьшей атомной массы, он обладает и наименьшей плотностью, которая в два раза ниже, чем у воды. После лития идут калий, натрий, алюминий, рубидий, цезий, стронций и т. д. В их число входит и титан, который обладает самой высокой прочностью среди металлов.
Легкостью и прочностью обладает также алюминий. В земной коре он третий по распространённости. Пока люди не научились получать его промышленным путём, металл был дороже золота. Сейчас килограмм алюминия можно купить примерно за 2 доллара. Его применяют как в ракетной технике и военной промышленности, так и для изготовления пищевой фольги и кухонных предметов.

Литий
Литий находится в первой группе периодической таблицы элементов. Он стоит под номером 3, после водорода и гелия, и обладает самой маленькой атомной массой среди всех металлов. Простое вещество – литий, при нормальных условиях имеет серебристо-белый цвет.
Это самый лёгкий щелочной металл с плотностью 0,534 г/см³. Из-за этого он всплывает не только в воде, но и в керосине. Для его хранения обычно используют парафин, газолин, минеральные масла или петролейный эфир. Литий очень мягкий и пластичный, легко режется ножом. Чтобы расплавить этот металл, его нужно нагреть до температуры 180,54 °C. Закипит он только при 1340 °C.
В природе существует только два стабильных изотопа металла: Литий-6 и Литий-7. Кроме них, есть 7 искусственных изотопа и 2 ядерных изомера. Литий является промежуточным продуктом в реакции превращения водорода в гелий, участвуя, таким образом, в процессе образования звёздной энергии.

Реакции с литием
Учитывая его щелочную природу, можно предположить, что он очень активен. Однако металл является самым спокойным представителем своей группы. При нормальной комнатной температуре литий слабо реагирует с кислородом и многими другими веществами. Свой «бурный нрав» он проявляет после нагревания, тогда он вступает в реакцию с кислотами, различными газами и основаниями.
В отличие от других щелочных металлов с водой он реагирует мягко, образуя гидроксид и водород. С сухим воздухом реакции практически нет. Но если он влажный, то литий медленно реагирует с его газами, образуя нитрид, карбонат и гидроксид.
При определённых температурах самый легкий металл активен с аммиаком, этиловым спиртом, галогенами, водородом, углеродом, кремнием, серой.

Сплавы лития
Свойства лития повышают отдельные качества металлов, из-за чего его часто используют в сплавах. Полезной является его реакция с окислами, водородом, сульфидами. При нагревании он образует с ними нерастворимые соединения, которые легко извлечь из расплавленных металлов, очистив их от этих веществ.
Для придания сплаву стойкости к коррозии и пластичности его смешивают с магнием и алюминием. Медь в сплаве с ним становится более плотной и менее пористой, лучше проводит электричество. Самый легкий металл повышает твёрдость и пластичность свинца. При этом он повышает температуру плавления многих веществ.
Благодаря литию металл становится прочным и устойчивым к разрушениям. При этом он не утяжеляет их. Именно поэтому сплавы на его основе применяются в космической инженерии и авиации. Главным образом используются смеси с кадмием, медью, скандием и магнием.
Нахождение в природе и значение
Самый легкий металл имеет около 30 собственных минералов, но только 5 из них используются в промышленности: пенталит, амблигонит, лепидолит, циннвальдит и сподумен. Кроме того, находится он в солёных озёрах. Всего в земной коре содержится 0,005 % этого металла.

Большие промышленные запасы лития находятся на всех континентах. Его добывают в Бразилии, Австралии, ЮАР, Канаде, США и других странах. После чего применяют его в электронике, металлургии, лазерных материалах, ядерной энергетике и даже медицине.
Большое содержание лития есть в гумусах, что говорит о его участии в круговороте природных веществ. Металл присутствует в организме животных, а также во многих растениях. Литием богаты персики, грибы, редис, картофель, морковь.
В нашем организме он содержится в печени, крови, лёгких, костях и других органов. Недостаток лития приводит к нарушениям в работе нервной системы и мозга. Он повышает устойчивость организма к болезням, активизирует деятельность ферментов. С помощью него борются с болезнью Альцгеймера, психическими расстройствами, склерозом, а также различными зависимостями.
Токсичность
Несмотря на важную биологическую роль лития в нашем организме, он может быть опасным. Самый легкий металл достаточно токсичен и способен вызывать отравления. При горении он провоцирует раздражение и отёки слизистых оболочек. Если на них попадет кусочек целого металла, произойдёт то же самое.

Литий нельзя брать в руки без перчаток. Взаимодействуя с влагой в воздухе или влагой на коже, он легко вызывает ожог. С расплавленным металлом нужно быть ещё осторожнее, так как его активность повышается в разы. При работе с ним нужно помнить, что это щелочь. Уменьшить его действие на кожу можно обычным уксусом.
В организме литий повышает устойчивость иммунной системы и улучшает работу нервной системы. Но его переизбыток сопровождается головокружением, сонливостью, потерей аппетита. Отравление металлом приводит к снижению либидо, слабости в мышцах, набору веса. При этом может ухудшиться зрение, память и наступить кома. Работать с литием нужно всегда в перчатках, защитном костюме и очках.
ТОП-20 самых легких металлов

К легким причисляют металлы, плотность которых колеблется в диапазоне 5-7,5 граммов на кубический сантиметр. Еще один определяющий показатель — атомный вес. Легкие металлы задействованы в фармацевтической, энергетической, автомобильной, авиакосмической и других отраслях промышленности, в металлургии, строительной сфере и медицине. Они составляют 20 % от массы земной коры. ТОП-20 самых легких металлов во вселенной собраны в нашем перечне.
Это самый легкий металл из существующих в мире. Он выделяется серебристо-белым окрасом, предельно низким атомным весом и плотностью, которая в два раза меньше, нежели у воды. Пластичный литий имеет тридцать минералов, два изотопа природного происхождения. Температура плавления щелочного металла составляет +180,5 градуса Цельсия.
Литий — уникальный элемент, который всплывает на поверхности керосина. Он редко эксплуатируется в чистом виде, поскольку очень активен, легко вступает в реакции с окружающей средой. Это токсичный металл, поэтому в быту не применяется, но подходит для создания пиротехники, используется в роли окислителя, в пищевой промышленности, электронике, при производстве аккумуляторов, смартфонов, электромобилей. Литий в сорок раз меньше весит, чем иридий и осмий. Он был открыт в 1817 году шведским ученым — выделен из природного петалита.

Калий
Вторую строчку в ТОПе занимает калий. Это мягкий щелочной металл. В природе он обнаруживается исключительно в химических соединениях — в морской воде. Калий реактивно окисляется при попадании на воздух. Его открыли в 1807 году — выделили путем электролиза. К свойствам его относятся:
В жидком виде металл применяется для производства теплоносителей. Важнейший биогенный элемент используется при изготовлении удобрений, в гальванотехнике.

Натрий
Это высоко-реактивный металл с бело-серебристым окрасом (относится к категории щелочных). Мягкий натрий без труда режется ножом, блестит на срезе. В природе он содержится в морской воде. На воздухе он легко окисляется до оксида натрия. Этот легкий металл плавится при +97 градусах Цельсия, а кипит — при +882 градусах. Натрий впервые был добыт путем электролиза химиком Хэмфри Дэви в Великобритании.
Этот металл активно эксплуатируется в металлургии, при изготовлении энергоемких аккумуляторов, в создании ядерных реакторов и при анализе органических веществ, в газоразрядных лампах.

Рубидий
Один из самых легких щелочных металлов, с плотностью выше чем у воды. Рубидий имеет серый цвет с белым отливом. Его смогли выделить немецкие химики в 1861 году методом пламенной спектроскопии. Этот металл вступает в химическую реакцию с водой, самовоспламеняется на воздухе, плавится при +39,3 градусах Цельсия.
Рубидий — моноизотопный, радиоактивный элемент. Он занимает 23 ступень по уровню распространенности в земной коре, встречается чаще меди и цинка. Этот металл используется при изготовлении пиротехнической продукции, в ядерной медицине и промышленности. Его эксплуатация важна при производстве паровых турбин, топливных генераторов.

Кальций
Это щелочноземельный металл, легко взаимодействующий с углекислым газом и кислородом. Кальций имеет серую тусклую поверхность со светло-желтым оттенком. Получают его путем электролиза или алюминотермии. Природный калий состоит из трех изотопов. По степени распространенности элементов в земной коре он занимает пятое место. Металлический кальций плавится при +884 градусах Цельсия. Он активно применяется при выплавке стали из-за сходства по свойствам с кислородом. Кальций используется в металлургии, для выделения азота из чистого аргона, при производстве циркония и урана.

Магний
Этот металл с малой атомной массой был получен в 1808 году. Он характеризуется пластичностью, без труда поддается резке, обработке. Магний плавится при +650 градусах, не боится коррозии.
В составе минералов и солей металл обнаруживается в земной коре, морской воде. Залежи природного магния находятся в Таджикистане и Восточной Сибири. Он используется в автомобиле- и самолетостроении, при производстве пиротехники, поскольку обладает высокими горючими свойствами. Магний применяется и при создании вооружения. В порошкообразной форме он применяется в фотографическом мастерстве.

Бериллий
Сероватый цвет, высокая хрупкость и токсичность характеризуют еще один легкий металл. В чистом виде он был получен в 1828 году. Название металл получил от известного минерала — берилла. В природе он встречается в магме, горных породах. Бериллий добывают в Индии, Бурятии, Казахстане.
Этот металл применяется в виде добавок при легировании сплавов. Он почти не поглощает рентгеновское излучение, поэтому применяется при создании детекторов гамма-излучения. Используется бериллий в аэрокосмической промышленности, в акустике, задействован в ядерной энергетике.

Цезий
Один из самых мягких и легких металлов с температурой плавления всего +28,6 градуса Цельсия. При комнатной температуре он находится в полужидком состоянии. Он представляет собой вещество золотистого цвета, отлично отражает свет. Этот металл открыли в 1860 году в Германии, но в чистом виде его получил уже шведский химик и только через 22 года.
Цезий используется как катализатор в органическом и неорганическом синтезе, в инфракрасных аппаратах и очках, при изготовлении светящихся трубок. Он применяется в энергетике и медицинской сфере. Кстати, на основе цезия создают твердые электролиты для автомобильного топлива.

Стронций
Месторождения стронциевых руд разрабатываются в Тульской области и в Дагестане. Стронций эксплуатируется в металлургии, пищевой и радиоэлектронной промышленности.

Алюминий
Один из самых распространенных металлов, который был открыт в 1825 году. До запуска масштабного производства алюминий ценился выше золота. Он обладает незначительными парамагнитными свойствами, проводит электрический ток и тепло. Алюминий подвергается механическому воздействию, но не коррозийному. Сплавы на его основе могут похвастаться пластичностью. Этот металл занимает третье место по степени распространенности в земной коре, плавится при +660 градусах.
Алюминий находит применение в черной металлургии, при производстве пиротехники, посуды, столовых приборов, в авиационной промышленности.

Барий
Это щелочноземельный металл, который быстро окисляется на воздухе, реагирует с водой, воспламеняется даже при слабом нагревании. Он активно взаимодействует с разбавленными кислотами. К другим свойствам бария относятся:
Серебристо-белый металл применяется в ядерно-энергетической отрасли, пиротехнике, оптике. В чистом виде барий получили в 1774-ом.

Титан
Металл насыщенного серебристого окраса был открыт в конце восемнадцатого века немецким химиком — выделен из минерала рутила. Образец металлического титана получили лишь в 1825 году. Он характеризуется высокой удельной прочностью и устойчивостью к коррозии. По концентрации титановых руд Россия находится на второй позиции в мире после Китая. К свойствам металла относятся:
- пластичность;
- хорошая ударная вязкость;
- температура плавления, которая составляет +1670 градусов Цельсия.
Титан используется в авиа-, кораблестроении, при производстве трубопроводов, в химической, автомобильной промышленности, при создании вооружения.

Германий
Хрупкий металл стального цвета с четко выраженным блеском. Это твердосплавный элемент, который плавится при +938 градусах Цельсия, кипит при +2850 градусах, является полупроводником. Германий был выделен в 1886 году немецким химиком Клеменсом Винклером. Это аномальное вещество, плотность которого увеличивается при плавлении.
Главные сферы применения германия — волоконная и тепловизорная оптика, электроника, химическая промышленность (в качестве катализаторов).

Галлий
Это мягкий, хрупкий металл стального цвета с синеватым оттенком. Он выделен в 1875 году французским химиком. Галлий плавится при +29,7 градусах Цельсия. Это один из наиболее дорогих металлов, свыше 97 % которого уходит на производство полупроводников. Галлий активно используется в медицине — в онкологии, в качестве антисептика.

Теллур
Хрупкий белый металл с блеском, применяется при производстве свинцовых сплавов. На просвет он выглядит красно-коричневым. Редкое, слегка токсичное вещество было обнаружено в Трансильвании в конце восемнадцатого века. Но выделить его в чистом виде удалось только через 17 лет. При нагревании металл становится пластичным. Он плавится при +448,8 градусах Цельсия.
Теллур широко применяется при создании полупроводников, в процессе вулканизации каучука. Металл используют при изготовлении ламп, специальных марок халькогенидных стекол.

Ванадий
Это пластичный металл средней твердости сине-стального цвета. Ванадий — хороший полупроводник. Он обладает высокими показателями теплоизоляции, отличается:
- податливостью;
- прочностью (тверже большинства сплавов).
Это редкий тугоплавкий элемент, который был открыт в 1801 году мексиканским профессором минералогии. Но сам ученый назвал его хроматом свинца. В чистом виде из железной руды ванадий был получен только в 1830 году шведским химиком. Этот металл плавится при +1887 градусах Цельсия. Он применяется как легирующая добавка для сталей, для изготовления электроники, сувенирной продукции, в металлургии, автомобильной промышленности, при производстве буровых установок.

Цирконий
Этот металл обладает высокой коррозийной стойкостью. Он встречается в природе в виде четырех стабильных изотопов. Серо-белый блестящий переходный металл отличается химической стойкостью. Он плавится при +1852 градусах Цельсия. Температура плавления составляет 4377 градусов. Цирконий встречается в 140 минералах, но не в самородном виде.
Металл был открыт в 1789 году, а в чистом виде — получен по истечении 35 лет после этого. Цирконий широко используется в авиационной, космической промышленности и медицине.

Это металл, который становится пластичным при 150 градусах Цельсия, а при 210 градусах — может деформироваться. Температура плавления — низкая. Она составляет 418 градусов. Металл характеризуется:
- высокой электропроводностью;
- химической активностью — сплавляется с щелочами, подвергается воздействию серной кислоты.
Цинк имеет голубовато-серый окрас. Он тускнеет на воздухе и покрывается слоем оксида, имеет пять стабильных изотопов. Этот металл был получен в 1746 году в Германии путем прокалки смеси оксида с углем. Цинк применяется при производстве ювелирных украшений (сплавы добавляются в золото), в автомобилестроении, для защиты металлов от коррозии, при изготовлении аккумуляторов и батареек.

Тугоплавкий, твердый металл с характерным блеском, имеет голубовато-белый окрас. Он царапает стекло, в чистом виде характеризуется пластичностью, отлично поддается механической обработке. При наличии азотно-кислородных примесей становится хрупким. Температура плавления — 1856 градусов Цельсия. Хром — составляющий компонент стали, который повышает ее прочность, закаливаемость, жаростойкость. Он был открыт во Франции в 1797 году. Химик Воклен выделил тугоплавкий металл с примесью карбидов. Используется хром в легированных сталях, в качестве эстетических гальванических покрытий. Он относится к токсичным элементам.

Марганец
Этот серебристо-серый металл напоминает железо. Он обладает незначительными парамагнитными свойствами, медленно окисляется и тускнеет на воздухе. Это твердый и хрупкий металл, который был открыт в 1774 году. Марганец имеет температурные показатели плавления и кипения 1246 и 2061 градус Цельсия соответственно.
Марганец используется для раскисления стали при ее выплавке, в металлургии и химической промышленности. Металл является остродефицитным сырьем в России. Известно лишь несколько месторождений (в Кемеровской области, Красноярском крае).
Время работы: с 10:00 до 21:00,
Выходной день: вторник
«Ретро-кафе»: в дни работы Планетария с 10:00 до 20:00.
Элементы: Литий – самый лёгкий металл
Элемент №3 Таблицы Менделеева был открыт в 1817 году шведским минералогом и химиком, учеником знаменитого Берцелиуса - Августом Арфведсоном, при изучении минерала петалита (LiAlSi4O10), найденном на железном руднике Уто в Швеции. Точно установив, что содержания кремния, алюминия и кислорода в минерале составляют 96% массы минерала, учёный предположил, что оставшиеся 4% принадлежат неизвестному щелочному металлу. В чистом виде новый элемент впервые выделил британский химик и геолог Гемфри Дэви в 1818 году. Позже, по предложению Берцелиуса, новый металл получил название литий, так как был найден в камнях, от др. греч. λίθος — камень. В большинстве европейских языков, как и в латыни, элемент №3 называется Lithium и обозначается символом Li.

Петалит (LiAlSi4O10), месторождение Palelni (Мьянма), 4х2 см
Литий — серебристо-белый металл, мягкий, твёрже натрия, но мягче свинца, легко режется ножом. Среди щелочных металлов литий имеет самую высокую температуру плавления и кипения (180 и 1340 °C, соответственно) и самую низкую плотность среди всех металлов - 0,53 г/см³. Это самый лёгкий металл в Таблице Менделеева, поэтому он всплывает в воде.

Литий — серебристо-белый металл.
Согласно космологической теории Большого взрыва литий вместе с водородом и гелием, является одним из первичных элементов, которые появились в результате этого события 13,8 миллиарда лет назад. Среднее содержание (кларк) лития в земной коре составляет 40 г/т. Его основные минералы: лепидолит KLi1,5Al1,5[Si3AlO10](F, OH)2 и сподумен LiAl[Si2O6]. Исходным сырьём для получения этого металла являются минеральные литиевые руды (например, сподумен) и рассолы соляных озёр, богатые его соединениями. Почти все месторождения литиевых руд являются комплексными и отрабатываются для получения лития c попутным извлечением ряда других ценных компонентов. Месторождения этого элемента известны в Боливии, США,Чили, Аргентине, Конго, Китае, Бразилии, Сербии. Солончак Уюни в Боливии — крупнейшее в мире комплексное месторождение литиевых руд.

Солончак Уюни, Боливия.
В России более 50 % запасов литиевых руд сосредоточено в редко-метальных месторождениях Мурманской области.
Самая распространённая область применения этого элемента - литиевые источники питания, которые используются там, где нужна компактность. Литий применяется при изготовлении стекол и керамики, защитных покрытий, смазочных материалов. Его используют в ядерной энергетике, медицине, металлургии и многих других областях промышленного производства.
Легкие металлы
В настоящее время такое понятие, как «легкие металлы», отсутствует в номенклатуре ИЮПАК. Таковыми принято называть металлы, имеющие небольшую плотность (как правило до 4,5 г/см 3 ) или вес. Стоит отметить, что в настоящее время существуют такие металлы, которые легко держатся на воде, а некоторые из них имеют вес, в разы меньший пенопласта, но при этом все равно остаются достаточно прочными.
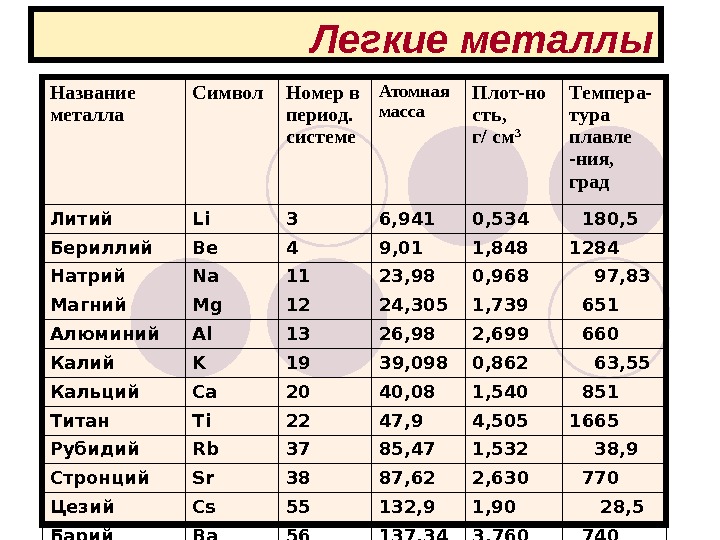
Группа легких металлов, как правило, включает в себя следующие: алюминий, олово, магний, титан, бериллий и литий. Кроме этого, к данной группе металлов часто также добавляют галлий, индий, таллий, висмут и кадмий.
Наиболее важными металлами данной группы с точки зрения технического применения являются алюминий, магний, титан, бериллий. Именно данные металлы служат в качестве основы сплавов. Алюминиевые сплавы являются наиболее значимой и распространенной группой, однако, не смотря на это, для специфического применения также предлагаются и материалы из титана и бериллия.
Свойства легких металлов
Алюминий
Алюминий является металлом, идеально сочетающим в своих характеристиках легкость и прочность. Его первооткрывателем является датский физик Ганс Эрстед, который в 1825 году восстановил хлорид алюминия амальгамой калия при воздействии высоких температур, в результате чего и выделил данный металл.
Имеет характерный серебристо-белый окрас. Плотность металла составляет 2712 кг/м 3 . Плавится при температуре: 658 0 С (для технического алюминий) и 660 0 С (для алюминия высокой чистоты). Удельная теплота плавления алюминия – 390 кДж/кг. Закипает при температуре 2515,8 0 С. Имеет удельную теплоемкость 897Дж/кг*К. Обладает достаточно высокой пластичностью, которая составляет 35% у технического алюминия и 50% у чистого металла.
Первым изделием, для изготовления которого был применен алюминий, стала детская погремушка. Однако, с тех далеких времен, алюминий стал достаточно распространенным материалом. В настоящее время он нашел свое широкое применение во многих сферах человеческой деятельности. Однако, наибольший процент потребления данного металла приходится на упаковочную промышленность, особенно для банок с напитками.

Также следует отметить, что алюминий активно применяется наряду со сталью и в машиностроении. В настоящее время существует огромное множество алюминиевых сплавов, которые отвечают огромному количеству определенных и необходимых требований. Среди данных сплавов можно выделить две основные группы – литейные и деформируемые. Сплавы из каждой группы также можно разделить на те, которые способны дисперсионно твердеть и те, которые не способны. Чтобы материал сделать более прочным применяются:
- наклеп;
- легирование;
- дисперсионное твердение (старение).
Для того, чтобы получить оптимальные характеристики стареющих сплавов, их необходимо подвергнуть измельчению. В связи с этим, для дисперсионного старения деформируемых сплавов используется термообработка. Ее также могут применять с целью повышения прочности.
Среди наиболее важных литейных сплавов стоит выделить Al-Si, которые образуют эвтектическую систему с эвтектической точкой при 11,7% Si и 577 0 С. Сплавы, имеющие в своем составе содержание Si в пределах 11-13% называют близкими к эвтектическим. Кроме этого, они также известны как силуминовое литье. Стоит отметить, что если охлаждение сплава с содержанием Si 13% осуществляется медленно, то первично выделяющийся твердый раствор Si образует крупные, угловатые, игольчатые кристаллы, что, в свою очередь, чревато ярко выраженной хрупкостью подобных сплавов. Одним словом, такая структура является крайне неблагоприятной. Для того, чтобы подобного не происходило, применяют облагораживание металлов – т.е. добавляют в плавку 0,1% Na. При этом происходит очищение кристаллов кремния, а также их округление и, в конечном итоге, образование тонкодиспергированной эвтектики. Благодаря подмешиванию в сплав натрия происходит снижение эвтектической температуры до 564 0 С.
Если же сплав охлаждается за относительно короткий промежуток времени, что происходит в кокильном литье, то происходит действие, подобное облагораживанию металлов – сдвиг эвтектической точки при помощи переохлаждения. В результате происходит образование достаточно чистой эвтектической структуры, что избавляет от необходимости облагораживания металлов путем добавления в них натрия.
Деформируемые сплавы имеют в своем составе значительно меньшее количество легирующих элементов и примесей, в отличие от литейных сплавов. Деформируемые сплавы, обычно, отвечают более высоким требованиям. В связи с этим, для их выплавки применяется металлургический алюминий. К нестареющим деформированным сплавам относятся AlMg-сплавы. Они отличаются своей высокой твердостью и прочностью по причине легирования. Данные свойства сохраняются даже при отжиге и сварке.
К высокопрочным сплавам нового поколения относятся Al-Li- сплавы.
Титан
Представляет собой легкий тугоплавкий металл с характерным серебристо-белым цветом. Отличается своей высокой устойчивостью к коррозии. Данным свойством он обязан стабильному пассивированному оксидному слою, который образуется за достаточно короткий промежуток времени при слабых средствах окисления.

Для титановых сплавов характерна высокая жаропрочность, которая может достигать 1200 – 1400Н/мм 2 . Именно титановые сплавы занимают ячейку между алюминиевыми сплавами и жаропрочными сталями, поскольку могут применятся до температуры 500 0 С, а также до 1000 0 С при непродолжительном использовании.
Титановый сплав используется для изготовления деталей, которые подвергаются сильной нагрузке, с целью их облегчения. Например, шатуны для высокомощных двигателей изготавливаются именно из титановых сплавов. Это связано с тем, что данный материал обладает идеальным соотношением прочности на разрыв к плотности Rm/p.
Однако, для титановых сплавов характерна достаточно высокая стоимость, что препятствует их широкому применению, в отличие от Al-сплавов.
Титану, как и железу, присуще аллотропное превращение. Титан сохраняет свою гексагональную структуру до температуры 882 0 С.
Среди наиболее важных легирующих элементов, которыми обогащаются технические титановые сплавы, следует назвать ванадий, олово, молибден, цирконий, ниобий, а также хром и алюминий.
Самый легкий металл
Литий
Представляет собой легкий щелочной металл с характерным серебристо-белым окрасом, обладающий высокой мягкостью и пластичностью. Литий тверже натрия, однако по мягкости ему уступает свинец. Поддается обработке путем прессования и прокатки. В условиях комнатной температуры литий обладает кубической объемноцентрированной решеткой. Кристаллическая решетка относится к пространственной группе Р63/mmc.
Литий имеет самые высокие температуры плавления и кипения (180,54 0 С и 1340 0 С соответственно) из всех остальных щелочных металлов, а также самую низкую плотность в условиях комнатной температуры (0,533 г/см 3 , что является практически вдвое меньше, чем плотность воды). Благодаря своей низкой плотности литий может держаться не только на поверхности воды, но и плавать на поверхности керосина.

Литий имеет атом достаточно малых размеров, благодаря чему литий наделен особыми свойствами. Например, смешение лития и натрия возможно осуществить только лишь при температуре ниже 380 0 С. А вот с расплавленным калием, рубидием и цезием литий, в отличие от иных пар щелочных металлов, смешивающихся друг с другом в любых соотношениях, вообще невозможно смешать.
Первооткрывателем лития является шведский химик Иоганн Арфведсон, который в 1817 году выделил литий из минерала петалита.
Использование лития в чистом виде не возможно в связи с активным взаимодействием его с окружающей средой. Литий нашел свое широкое применение в медицине, пищевой, текстильной, силикатной промышленностях. Также его используют во время изготовления пиротехники, термоядерного оружия, оптики. Нередко литий может выступать в роли окислителя. Отдельные его сплавы также применяются в электронике и авиакосмической промышленности.
Кроме лития, также имеют свойство держаться на воде калий и натрий, остальные же металлы из группы легких являются тяжелее воды.
Металлургия легких металлов
Производство легких металлов, как и других, начинается с добычи руд или другого вида сырья. Добыча легких цветных металлов относится к цветной металлургии.
Для производства алюминия используется природное сырье – глинозем, который добывается из бокситов. Кроме этого, также для добычи алюминия могут быть использованы нефелины и алуниты. Производство алюминия имеет два основных этапа – производство глинозема и производство металлического алюминия.
Для производства титана используются титановые руды. На территории России они находятся на 19 месторождениях, семь из которых являются россыпными.
Руды легких металлов, особенно алюминия, в отличие от тяжелых, по содержанию полезного компонента сходны с железной рудой и являются транспортабельными. В связи с этим вполне рациональным является их перевозка на дальние расстояния.
Читайте также:
