Сера с металлами образует
Обновлено: 23.04.2024
Сера, её физические и химические свойства. Биологическое значение серы, её применение (демеркуризация).
СЕРА S
Cера в природе
PbS - свинцовый блеск
Cu2S – медный блеск
ZnS – цинковая обманка
FeS2 – пирит, серный колчедан, кошачье золото
H2S – сероводород (в минеральных источниках и природном газе)
CaSO4 * 2H2O - гипс
MgSO4 * 7H2O – горькая соль (английская)
Na2SO4 *10H2O – глауберова соль (мирабилит)
Твердое кристаллическое вещество желтого цвета , нерастворима в воде, водой не смачивается (плавает на поверхности), t°кип = 445°С.
Одно из особенных физических свойств серы - флотация, способность мелкого порошка серы всплывать, тогда, как ее крупные кристаллы тонут в воде. Дело в том, что сера не смачивается водой, и ее частички держатся на поверхности воды за счет прилипших к ним мелких пузырьков воздуха. Это свойство используют при отделении самородной серы от примесей. Руду размалывают, заливают водой, а снизу продувают воздухом, сера всплывает, а примеси остаются на дне.
Для серы характерны несколько аллотропных модификаций, но наиболее известные видоизменения: ромбическая (кристаллическая), моноклинная (игольчатая) и пластическая.
Ромбическая (a - сера) - S8
t°пл. = 113°C; ρ = 2,07 г/см 3 . Наиболее устойчивая модификация.
Моноклинная (b - сера) - S8
темно-желтые иглы, t°пл. = 119°C; ρ = 1,96 г/см3. Устойчивая при температуре более 96°С; при обычных условиях превращается в ромбическую.
коричневая резиноподобная (аморфная) масса. Неустойчива, при затвердевании превращается в ромбическую.
Строение атома серы
Размещение электронов по уровням и подуровням
Основное состояние
1s 2 2s 2 2p 6 3s 2 3p 4
Размещение электронов по
орбиталям (последний слой)
В основном состоянии
Первое возбуждённое состояние
Второе возбуждённое состояние
Получение серы
1. Промышленный метод - выплавление из руды с помощью водяного пара.
2. Неполное окисление сероводорода (при недостатке кислорода).
3. Реакция Вакенродера
Химические свойства серы
Сера - окислитель S 0 + 2ē→ S -2
1. Взаимодействие серы со всеми щелочными и щелочноземельными металлами, медью, ртутью, серебром без нагревания:
Ртуть обладает высокой летучестью. Её пары ядовиты. Эта реакция лежит в основе удаления и обезвреживания ртути, например из разбитого медицинского термометра. Места, из которых нельзя извлечь капельки ртути, засыпают порошком серы. Сера и ртуть вступают в реакцию при соприкосновении. В результате образуется химически инертное и безвредное вещество.
Этот процесс называется демеркуризацией
2. Взаимодействие серы c остальными металлами (кроме Au,Pt) при повышенной t°:
3.Взаимодействие серы с некоторыми неметаллами с образованием бинарных соединений:
Сера - восстановитель: S - 4ē → S +4 ;
1. Взаимодействие серы c кислородом:
2. Взаимодействие серы c галогенами (кроме йода):
**Взаимодействие серы с кислотами - окислителями:
Вулканизация каучука, получение эбонита, производство спичек, пороха, в борьбе с вредителями сельского хозяйства, для медицинских целей (серные мази для лечения кожных заболеваний), для получения серной кислоты и т.д.
Домашнее задание параграф 21; упражнения 1, 3, 4 стр. 99-100.
Закончите уравнения реакций, расставьте коэффициенты методом электронного баланса, укажите окислитель, восстановитель.
№2. Осуществите превращения по схеме:
Содержание серы в организме человека массой 70 кг - 140 г.
В сутки человеку необходимо 1 г серы.
Серой богаты горох, фасоль, овсяные хлопья, пшеница, мясо, рыба, плоды и сок манго.
Сера входит в состав гормонов, витаминов, белков, она есть в хрящевой ткани, в волосах, ногтях. При недостатке серы в организме наблюдается хрупкость ногтей и костей, выпадение волос.
Следите за своим здоровьем!
Соединения серы могут служить лекарственными препаратами;
Сера – основа мази для лечения грибковых заболеваний кожи, для борьбы с чесоткой. Тиосульфат натрия Na2S2O3 используется для борьбы с нею.
Многие соли серной кислоты содержат кристаллизационную воду: ZnSO4×7H2O и CuSO4×5H2O. Их применяют как антисептические средства для опрыскивания растений и протравливания зерна в борьбе с вредителями сельского хозяйства.
Железный купорос FeSO4×7H2O используют при анемии.
BaSO4 применяют при рентгенографическом исследовании желудка и кишечника.
Алюмокалиевые квасцы KAI(SO4)2×12H2O - кровоостанавливающее средство при порезах.
Минерал Na2SO4×10H2O носит название «глауберова соль» в честь открывшего его в VIII веке немецкого химика Глаубера И.Р.Глаубер во время своего путешествия внезапно заболел. Он ничего не мог есть, желудок отказывался принимать пищу. Один из местных жителей направил его к источнику. Как только он выпил горькую соленую воду, сразу стал есть. Глаубер исследовал эту воду, из нее выкристаллизовалась соль Na2SO4×10H2O. Сейчас ее применяют как слабительное в медицине, при окраске хлопчато- бумажных тканей. Соль также находит применение в производстве стекла.
Тысячелистник обладает повышенной способностью извлекать из почвы серу и стимулировать поглощение этого элемента с соседними растениями.
Чеснок выделяет вещество – альбуцид, едкое соединение серы. Это вещество предотвращает раковые заболевания, замедляет старение, предупреждает сердечные заболевания.
Сера с металлами образует
Сера - элемент VIa группы 3 периода периодической таблицы Д.И. Менделеева. Относится к группе халькогенов - элементов VIa группы.
Сера - S - простое вещество имеет светло-желтый цвет. Использовалась еще до нашей эры в составе священных курений при религиозных обрядах.

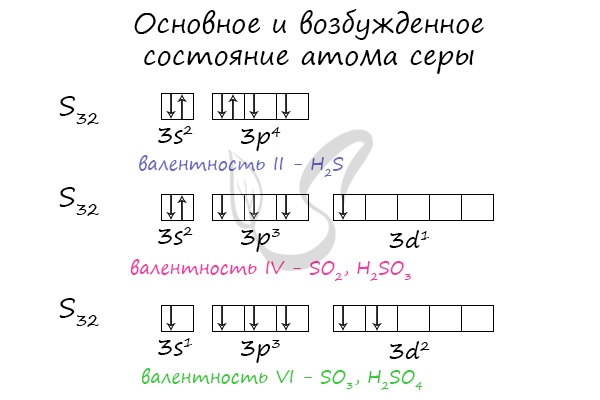
Основное и возбужденное состояние атома серы
Электроны s- и p-подуровня способны распариваться и переходить на d-подуровень. Как и всегда, количество валентных электронов отражает количество возможных связей у атома.
В разных электронных конфигурациях сера способна принимать валентности: II, IV и VI.
Природные соединения
- FeS2 - пирит, колчедан
- ZnS - цинковая обманка
- PbS - свинцовый блеск (галенит), Sb2S3 - сурьмяный блеск, Bi2S3 - висмутовый блеск
- HgS - киноварь
- CuFeS2 - халькопирит
- Cu2S - халькозин
- CuS - ковеллин
- BaSO4 - барит, тяжелый шпат
- CaSO4 - гипс
В местах вулканической активности встречаются залежи самородной серы.

В промышленности серу получают из природного газа, который содержит газообразные соединения серы: H2S, SO2.
Серу можно получить разложением пирита
В лабораторных условиях серу можно получить слив растворы двух кислот: серной и сероводородной.
- Реакции с неметаллами
На воздухе сера окисляется, образуя сернистый газ - SO2. Реагирует со многими неметаллами, без нагревания - только со фтором.

При нагревании сера бурно взаимодействует со многими металлами с образованием сульфидов.
При взаимодействии с концентрированными кислотами (при длительном нагревании) сера окисляется до сернистого газа или серной кислоты.
Сера вступает в реакции диспропорционирования с щелочами.
Сера вступает в реакции с солями. Например, в кипящем водном растворе сера может реагировать с сульфитами с образованием тиосульфатов.
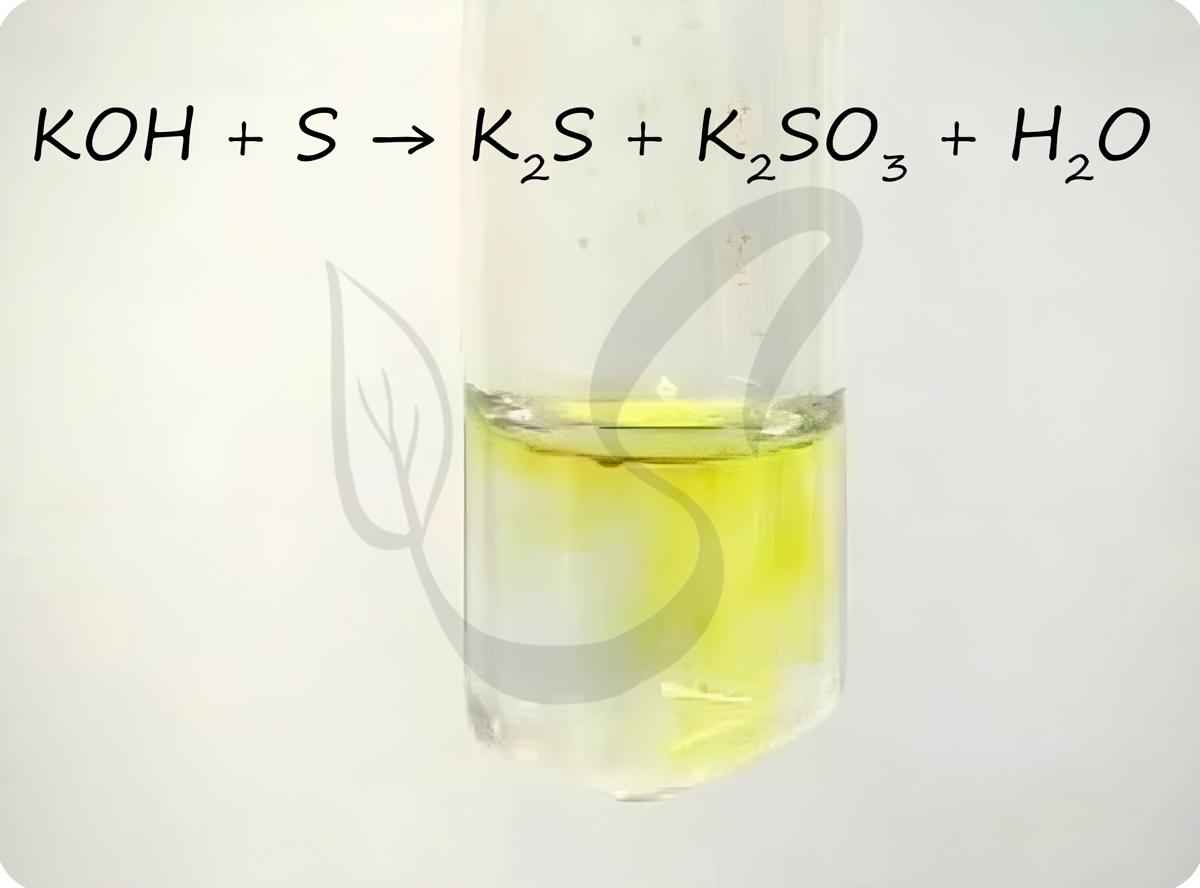
Сероводород - H2S
Бесцветный газ с характерным запахом тухлых яиц. Огнеопасен. Используется в химической промышленности и в лечебных целях (сероводородные ванны).

Сероводород получают в результате реакции сульфида алюминия с водой, а также взаимодействия разбавленных кислот с сульфидами.

Сероводород плохо диссоциирует в воде, является слабой кислотой. Реагирует с основными оксидами, основаниями с образованием средних и кислых солей (зависит от соотношения основания и кислоты).
KOH + H2S = KHS + H2O (гидросульфид калия, избыток кислоты)
Металлы, стоящие в ряду напряжений до водорода, способны вытеснить водород из кислоты.
Сероводород - сильный восстановитель (сера в минимальной степени окисления S 2- ). Горит в кислороде синим пламенем, реагирует с кислотами.

Качественной реакцией на сероводород является реакция с солями свинца, в ходе которой образуется сульфид свинца.
Оксид серы - SO2
Сернистый газ - SO2 - при нормальных условиях бесцветный газ с характерным резким запахом (запах загорающейся спички).

В промышленных условиях сернистый газ получают обжигом пирита.
В лаборатории SO2 получают реакцией сильных кислот на сульфиты. В ходе подобных реакций образуется сернистая кислота, распадающаяся на сернистый газ и воду.
Сернистый газ получается также в ходе реакций малоактивных металлов с серной кислотой.
С основными оксидами, основаниями образует соли сернистой кислоты - сульфиты.

Химически сернистый газ очень активен. Его восстановительные свойства продемонстрированы в реакциях ниже.
В присутствии сильных восстановителей SO2 способен проявлять окислительные свойства (понижать степень окисления).
Сернистая кислота
Слабая, нестойкая двухосновная кислота. Существует лишь в разбавленных растворах.
Диссоциирует в водном растворе ступенчато.
В реакциях с основными оксидами, основаниями образует соли - сульфиты и гидросульфиты.
H2SO3 + KOH = H2O + KHSO3 (соотношение кислота - основание, 1:1)
С сильными восстановителями сернистая кислота принимает роль окислителя.
Как и сернистый газ, сернистая кислота и ее соли обладают выраженными восстановительными свойствами.

Оксид серы VI - SO3
Является высшим оксидом серы. Бесцветная летучая жидкость с удушающим запахом. Ядовит.
В промышленности данный оксид получают, окисляя SO2 кислородом при нагревании и присутствии катализатора (оксид ванадия - Pr, V2O5).
В лабораторных условиях разложением солей серной кислоты - сульфатов.
Является кислотным оксидом, соответствует серной кислоте. При реакции с основными оксидами и основаниями образует ее соли - сульфаты и гидросульфаты. Реагирует с водой с образованием серной кислоты.
SO3 + 2KOH = K2SO4 + 2H2O (основание в избытке - средняя соль)
SO3 + KOH = KHSO4 + H2O (кислотный оксид в избытке - кислая соль)

SO3 - сильный окислитель. Чаще всего восстанавливается до SO2.

Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
VI группа главная подгруппа периодической таблицы Менделеева (кислород, сера)
К элементам главной подгруппы VI группы периодической таблицы Менделеева относятся:
Общая характеристика элементов 6 группы главной подгруппы
От O к Po (сверху вниз в периодической таблице)
Увеличивается
- атомного радиуса,
- металлических, основных, восстановительных свойств,
Уменьшается
- электроотрицательность,
- энергия ионизация,
- сродство к электрону.

Электронные конфигурации у данных элементов схожи, все они содержат 6 электронов на внешнем слое ns 2 np 4 :
Электронное строение кислорода и серы
Нахождение в природе кислорода и серы
Кислород занимает первое место среди элементов по распространенности в земной коре. Содержится он главным образом в силикатах и составляет около 47 % массы твёрдой земной коры. В больших количествах связанного кислорода содержится в воде — 85,82 % по массе. Также кислород содержится более, чем в 1500 соединений земной коры. В атмосфере доля свободного кислорода составляет 20,95 % по объёму и 23,10 % по массе.
Сера встречается в виде самородной серы, сульфатов (CaSO4∙2H2O, CaSO4∙H2O, Na2SO4∙10H2O, MgSO4∙7H2O), сульфидов (FeS2, CuS, CuFeS2, PbS, ZnS, HgS) и в промышленных газах.
Самородная сера встречается в местах вулканической активности совместно с сернистыми фумаролами и сернистыми водами (с содержанием > 25 %).

Аллотропные модификации серы
Кислород
Способы получения кислорода
В природе
Кислород образуется в процессе фотосинтеза:
Промышленный способ
Лабораторный способ
- термическое окислительно-восстановительное разложение солей:
- Для автономного дыхания кислород получают в герметически замкнутых помещениях и в аппаратах при помощи реакции:
Физические свойства кислорода
При обычных условиях молекулярный кислород O2 – это малорастворимый в воде газ без цвета, запаха и вкуса.
При сильном охлаждении под давлением переходит в бледно — голубую жидкость с Ткип = — 183°С. При Т = -219°С образует сине — голубые кристаллы.
Химические свойства кислорода
Кислород — сильный окислитель, уступающий по химической активности только фтору.
Вступает во взаимодействия со всеми элементами, кроме инертных газов (Не, Ne и Аг). Со многими простыми веществами реагирует непосредственно при обычных условиях или при нагревании или в присутствии катализаторов (кроме Au, Pt, Hal2, благородные газы).
Большинство реакций с участием О2 экзотермичны, часто часто сопровождаются горением, иногда — взрывом.
Взаимодействие с простыми веществами
С металлами
- Кислород взаимодействует с металлами, с образованием оксидов металлов:
- Сщелочными металламив результате реакций образуются различные кислородсодержащие продукты:
4Li + О2 = 2Li2O оксид лития
К + О2 = КО2 супероксид калия
- С железом образуется смесь оксидов:
- С марганцем образуется диоксид марганца:
С неметаллами
При взаимодействии с неметаллами (кроме фтора и инертных газов) образуются оксиды, со степенью окисления кислорода – 2:
Окисление сложных веществ
Горение сульфидов
Горение водородных соединений
Окисление оксидов
Кислород окисляет входящие в оксид элементы до более высокой степени окисления:
Окисление гидроксидов и солей
Окисление гидроксидов и солей в водных растворах происходит, если исходное вещество неустойчиво на воздухе:
Окисление аммиака
В отсутствие катализатора при окислении аммиака кислородом образуется азот, а в присутствии катализатора — оксида азота(II):
Окисление фосфина
На воздухе самопроизвольно воспламеняется:
Окисление силана
На воздухе он самовоспламеняется (часто со взрывом) с образованием SiO2 и H2O:
Окисление органических веществ
- Все органические соединения горят, окисляясь кислородом воздуха полностью:
Продукты окисления различных элементов, входящих в молекулы органических соединений:
Кроме горения возможны также реакции неполного окисления:
Способы получения серы
- Извлечение самородной серы из ее месторождений или вулканов
- Получение серы из серной руды с помощью пароводяного, фильтрационного, термического, центрифугального и экстракционного методов.
- Переработка природных газов, содержащих H2S и их окисление при недостатке О2.
Физические свойства серы
Сера — твердое хрупкое вещество желтого цвета. Не смачивается водой и практически нерастворимо в ней. Имеет несколько аллотропных модификаций. См. аллотропные модификации серы.
Химические свойства серы
При обычных температуре и давлении химическая активность серы небольшая. При нагревании сера довольно активна, и проявляет свойства как окислителя, так и восстановителя.
Свойства окислителя сера проявляет при взаимодействии с элементами, расположенными ниже и левее в Периодической системе, а свойства восстановителя — с элементами, расположенными выше и правее в Периодической системе.
Непосредственно сера не взаимодействует с азотом и йодом.
Взаимодействие с простыми веществами
С кислородом
Горение серы на воздухе с образованием оксида серы (IV):
В присутствии катализаторов:
С водородом
С водородом сера вступает в реакцию при нагревании, образуя сероводород:
С галогенами
При взаимодействии со всеми галогенами, кроме йода образуются галогениды:
С фосфором
Взаимодействие серы с фосфором приводит к образованию сульфидов фосфора
С углеродом
В реакции серы с углеродом образуется сероуглерод:
С металлами
При взаимодействии с металлами сера выступает в качестве окислителя, образуя сульфиды.
Щелочные металлы реагируют с серой без нагревания, остальные металлы (кроме золота Au и платины Pt) –при нагревании:
Взаимодействие со сложными веществами
С водой
Сера вступает в реакцию диспропорционирования с перегретым паром:
С окислителями
В реакциях с окислителями сера окисляется до оксида серы (IV) SO2 или до серной кислоты H2SO4 при протекании реакции в растворе:
С щелочами
При взаимодействии с щелочами сера диспропорционирует до сульфита и сульфида:
Соединения серы
Сероводород H2S – это бинарное летучее водородное соединение соединение с серой. H2S — бесцветный ядовитый газ, с неприятным удушливым запахом тухлых яиц. При концентрации > 3 г/м 3 вызывает смертельное отравление.
Сероводород тяжелее воздуха и легко конденсируется в бесцветную жидкость. Растворимость в воде H2S при обычной температуре составляет 2,5.
В твердом состоянии имеет молекулярную кристаллическую решетку.
Геометрическая форма молекулы сероводорода представляет собой сцепленные между собой атомы H-S-H с валентным углом 92,1 о .

Качественная реакция для обнаружения сероводорода
Для обнаружения анионов S 2- и сероводорода используют реакцию газообразного H2S с Pb(NO3)2:
Влажная бумага, смоченная в растворе Pb(NO3)2 чернеет в присутствии H2S из-за получения черного осадка PbS.
Химические свойства серы
H2S является сильным восстановителем
При взаимодействии H2S с окислителями образуются различные вещества — S, SО2, H2SO4
- Взаимодействие с кислотами-окислителями:
- Взаимодействие со сложными окислителями:
- Сероводородная кислота H2S двухосновная кислота и диссоциирует по двум ступеням:
1-я ступень: H2S → Н + + HS —
2-я ступень: HS — → Н + + S 2-
H2S очень слабая кислота, несмотря на это имеет характерные для кислот химические свойства. Взаимодействует:
- с малоактивными металлами (Аg, Си, Нg) при совместном присутствии окислителей:
- с некоторыми солями сильных кислот, если образующийся сульфид металла нерастворим в воде и в сильных кислотах:
Реакция с нитратом свинца в растворе – это качественная реакция на сероводород и сульфид-ионы.
Сульфиды
Получение сульфидов
- Непосредственно из простых веществ:
S + Fe → FeS
- Восстановление сульфатов при прокаливании с углем:
Физические свойства сульфидов
Сульфиды – это бинарные соединения серы с элементами с меньшей электроотрицательностью, в том числе с некоторыми неметаллами (С, Si, Р, As и др.).
По растворимости в воде и кислотах сульфиды классифицируют на:
- растворимые в воде — сульфиды щелочных металлов и аммония;
- нерастворимые в воде, но растворимые в минеральных кислотах — сульфиды металлов, расположенных до железа в ряду активности (белые и цветные сульфиды ZnS, MnS, FeS, CdS);
- нерастворимые ни в воде, ни в минеральных кислотах — черные сульфиды (CuS, HgS, PbS, Ag2S, NiS, CoS)
- гидролизуемые водой — сульфиды трехвалентных металлов (алюминия и хрома (III))
По цвету сульфиды можно разделить на:
Химические свойства сульфидов
Обратимый гидролиз сульфидов
- Хорошо растворимыми в воде являются сульфиды щелочных металлов и аммония, но в водных растворах они в значительной степени подвергаются гидролизу. Реакция среды — сильнощелочная:
S 2- + H2O → HS — + ОН —
- Сульфиды щелочно-земельных металлов и Mg, при взаимодействии с водой подвергаются полному гидролизу и переходят в растворимые кислые соли — гидросульфиды:
При нагревании растворов сульфидов гидролиз протекает и по 2-й ступени:
Необратимый гидролиз сульфидов
- Сульфиды некоторых металлов (Cr2S3, Fe2S3, Al2S3) подвергаются необратимому гидролизу, полностью разлагаясь в водных растворах:
Нерастворимые сульфиды гидролизу не подвергаются
NiS + HСl ≠
- Некоторые из сульфидов растворяются в сильных кислотах:
- Сульфиды Ag2S, HgS, Hg2S, PbS, CuS не pacтворяются не только в воде, но и во многих кислотах.
- Сульфиды обладают восстановительными свойствами и вступают в реакции с окислителями:
- Окислительный обжиг сульфидов является важной стадией переработки сульфидного сырья в различных производствах
Взаимодействия сульфидов с растворимыми солями свинца, серебра, меди являются качественными на ион S 2− :
Оксид серы (IV), диоксид серы, сернистый газ, сернистый ангидрид (SO2)
Способы получения сернистого газа
- Окисление серы, сероводорода и сульфидов кислородом воздуха:
- Действие высокой температуры на сульфиты (термическое разложение):
- Действие сильных кислот на сульфиты:
- Взаимодействие концентрированной H2SO4 с восстановителями, например с неактивными металлами:
Физические свойства сернистого газа
При обычной температуре SO2 — газ с резким запахом без цвета. В воде растворим хорошо — при 20°С в 1 л воды растворяется 40 л SO2.
Химические свойства сернистого газа
SO2 – типичный кислотный оксид. За счет того, что сера находится в промежуточной степени окисления (+4) SO2 может проявлять свойства как окислителя так и восстановителя.
- При растворении в воде SO2 частично соединяется с молекулами воды с образованием слабой сернистой кислоты.
- Как кислотный оксид, SO2 вступает в реакции с щелочами и оксидами щелочных и щелочноземельных металлов:
- При взаимодействии с окислителями SO2проявляет восстановительные свойства. При этом степень окисления серы повышается:
Обесцвечивание раствора перманганата калия KMnO4 является качественной реакцией для обнаружения сернистого газа и сульфит-иона
- SO2 проявляет окислительные свойства при взаимодействии с сильными восстановителями, восстанавливаясь чаще всего до свободной серы:
Оксид серы (VI), триоксид серы, серный ангидрид (SO3)
Способы получения серного ангидрида
- SO3 можно получить из SO2путем каталитического окисления последнего кислородом:
- Разложением сульфата железа (III):
Физические свойства серного ангидрида
При обычных условиях SO3 представляет собой бесцветную жидкость с характерным резким запахом. На воздухе SO3 «дымит» и сильно поглощает влагу.
SO3 – тяжелее воздуха, хорошо растворим в воде.
Химические свойства серного ангидрида
Оксид серы (VI) – это кислотный оксид.
- Хорошо поглощает влагу и реагирует с водой образуя серную кислоту:
- Как кислотный оксид, SO3взаимодействует с щелочами и основными оксидами, образуются средние или кислые соли:
SO3 + MgO → MgSO4 (при сплавлении):
SO3 + ZnO = ZnSO4
- SO3проявляет сильные окислительные свойства, так как сера в находится в максимальной степени окисления (+6).
Вступает в реакции с восстановителями:
- При растворении в концентрированной серной кислоте образует олеум (раствор SO3 в H2SO4).
Сернистая кислота (H2SO3)
Способы получения сернистой кислоты
При растворении в воде SO2 образует слабую сернистую кислоту, которая сразу частично разлагается:
Физические свойства сернистой кислоты
Сернистая кислота H2SO3 – двухосновная кислородсодержащая кислота. При обычных условиях неустойчива.
Валентность серы в сернистой кислоте равна IV, а степень окисления +4.

Химические свойства сернистой кислоты
Общие свойства кислот
- Сернистая кислота – слабая кислота, диссоциирует в две стадии. Образует два типа солей:
- кислые – гидросульфиты
Соли сернистой кислоты, сульфиты и гидросульфиты
Способы получения сульфитов
Соли сернистой кислоты получаются при взаимодействии SO2 с щелочами и оксидами щелочных и щелочноземельных металлов:
Физические свойства сульфитов
Сульфиты щелочных металлов и аммония растворимы в воде, сульфиты остальных металлов — нерастворимы или не существуют.
Гидросульфиты металлов хорошо растворимы в Н2O, а некоторые из них, такие как Ca(HSO3)2 существуют только в растворе.
Химические свойства сульфитов
Cернистая кислота – двухосновная, образует нормальные (средние) соли — сульфиты Mex(SO3)y и кислые соли — гидросульфиты Me(HSO3)x.
- Водные растворы сульфитов подвергаются гидролизу. Реакция среды – щелочная(окрашивают лакмус в синий цвет):
Реакции, протекающие без изменения степени окисления:
- Нормальные сульфиты в водных растворах, при избытке SO2, переходят в гидросульфиты:
- Ионно-обменные реакции с другими солями, протекающие с образованием нерастворимых сульфитов:
Сульфиты, также как и SO2, могут быть как восстановителями, так и окислителями, т.к. атомы серы в анионах находятся в промежуточной степени окисления +4
- Окисление водных растворов сульфитов, и гидросульфитов до сульфатов:
- Твердые сульфиты при хранении на воздухе также медленно окисляются до сульфатов:
- При нагревании сухих сульфитов с активными восстановителями (С, Mg, Al, Zn) сульфиты превращаются в сульфиды:
- При нагревании сухих сульфитов до высоких температур сульфиты диспропорционируют, превращаются в смесь сульфатов и сульфидов:
Серная кислота (H2SO4)
Способы получения серной кислоты
В промышленности серную кислоту производят из серы, сульфидов металлов, сероводорода и др.
Наиболее часто серную кислоту получают из пирита FeS2.
Основные стадии получения серной кислоты включают:
1.Обжиг пирита в кислороде в печи для обжига с получением сернистого газа:
2. Очистка полученного сернистого газа от примесей в циклоне, электрофильтре.
3. Осушка сернистого газа в сушильной башне
4. Нагрев очищенного газа в теплообменнике.
5. Окисление сернистого газа в серный ангидрид в контактном аппарате:
6. Поглощение серного ангидрида серной кислотой в поглотительной башне – получение олеума.

Физические свойства, строение серной кислоты
При обычных условиях серная кислота – тяжелая бесцветная маслянистая жидкость, хорошо растворимая в воде. Максимальная плотность равна 1,84 г/мл
При растворении серной кислоты в воде выделяется большое количество теплоты. Поэтому, по правилам безопасности в лаборатории при приготовлении разбавленного раствора серной кислоты во избежание разбрызгивания необходимо наливать серную кислоту в воду тонкой струйкой по стеклянной палочке при постоянном перемешивании. Но не наоборот!
Валентность серы в серной кислоте равна VI.
Качественные реакции для обнаружения серной кислоты и сульфат ионов
Для обнаружения сульфат-ионов используют реакцию с растворимыми солями бария. В результате взаимодействия, образуется белый кристаллический осадок сульфата бария:
Химические свойства серной кислоты
Серная кислота — сильная двухосновная кислота, образует два типа солей: средние – сульфаты, кислые – гидросульфаты.
- Серная кислота практически полностью диссоциирует в разбавленном в растворе по первой ступени и достаточно по второй ступени:
Характерны все свойства кислот:
- Реагирует с основными оксидами, основаниями, амфотерными оксидами, амфотерными гидроксидами и аммиаком:
- Вытесняетболее слабые кислоты из их солей в растворе (карбонаты, сульфиды и др.) и летучие кислоты из их солей (кроме солей HBr и HI):
- Концентрированная серная кислота реагирует с твердыми солями, например нитратом натрия, хлорида натрия.
Разбавленная серная кислота взаимодействует с металлами, расположенными в ряду напряжения металлов до водорода. В результате реакции образуются соль и водород:
Концентрированная серная кислота — сильный окислитель. Реакция с металлами протекает без вытеснения водорода из кислоты. В зависимости от активности металла образуются различные продукты реакции:
- Активные металлы и цинк при обычной температуре с концентрированной серной кислотой образуют соль, сероводород (или серу) и воду:
- Металлы средней активности с концентрированной H2SO4 образуют соль, серу и воду:
- Такие металлы, как железо Fe, алюминий Al, хром Cr пассивируются концентрированной серной кислотой на холоде. При нагревании, при удалении оксидной пленки реакция возможна.
- Неактивные металлы восстанавливают концентрированную серную кислоту до сернистого газа:
- В реакциях с неметаллами концентрированная серная кислота также проявляет окислительные свойства:
- Концентрированная серная кислота широко используется в химических процессах как водоотнимающий агент, т.к. проявляет сильное водоотнимающее действие. В органической химии ее используют при получении спиртов, простых и сложных эфиров, альдегидов и т.д.
Соли серной кислоты, сульфаты, гидросульфаты
Способы получения солей серной кислоты
Сульфаты можно получить при взаимодействии серной кислоты с металлами, оксидами, гидроксидами (см. Химические свойства серной кислоты). А также при взаимодействии с другими солями, если продуктом реакции является нерастворимое соединение.
Физические свойства солей серной кислоты
Кристаллы разного цвета. Многие средние и кислые сульфаты растворимы в воде. Плохо растворяются или не растворяются в воде сульфаты многозарядных щёлочноземельных металлов (BaSO4, RaSO4), сульфаты лёгких щёлочноземельных металлов (CaSO4, SrSO4) и сульфат свинца.
Средние сульфаты щелочных металлов термически устойчивы. Кислые сульфаты щелочных металлов при нагревании разлагаются.
Многие средние сульфаты образуют устойчивые кристаллогидраты:
CuSO4 ∙ 5H2O − медный купорос
FeSO4 ∙ 7H2O − железный купорос
ZnSO4 ∙ 7H2O − цинковый купорос
KАl(SO4)2 x 12H2O – алюмокалиевые квасцы.
Химические свойства солей серной кислоты
Разложение сульфатов на различные классы соединений в зависимости от металла, входящего в состав соли.
Читайте также:
