Сероводородная кислота с металлами
Обновлено: 14.05.2024
Сера (S) в природе встречается в соединениях и свободном виде. Распространены и соединения серы, такие как свинцовый блеск PbS, цинковая обманка ZnS, медный блеск Cu2S. Для получения серы основным источником служит железный колчедан (пирит) FeS2. Газовую серу получают из газов, образованных при коксовании и газификации угля.
Существует несколько известных аллотропных модификаций серы:
1) циклическая форма;
2) моноклинная форма;
3) кристаллическая ромбическая форма.
При температуре 20–25 °C (комнатная) наиболее устойчива желтая ромбическая сера (a-сера, r = 2,1 г/см3). При температурном интервале от 95,4 °C до 119,3 °C (температура плавления) наиболее стабильной является моноклинная сера (b-сера). При комнатной температуре кристаллы моноклинной серы постепенно переходят в монолит микроскопических кристаллов ромбической серы. При резком охлаждении сильно нагретой серы происходит образование пластической серы.
Реже встречается пурпурная сера, образующаяся при быстрой конденсации паров серы на поверхности, охлаждаемой жидким азотом.
Сера находится в VI группе третьего периода периодической системы. Имеет на внешнем электронном слое атома шесть электронов.
Проявляет степень окисления от -2 до +6.
Сера не растворима в воде, но растворима в органических растворителях. Является диэлектриком.
Сера – неметалл с типичными для него свойствами. Взаимодействует со многими металлами непосредственно (медью, железом, цинком), выделяя при этом теплоту. Среди металлов лишь золото, платина и рутений не вступают в реакцию с серой. Взаимодействует также с большинством неметаллов, за исключением азота и йода.
Химические свойства:
1) при нагревании сера реагирует с водородом, образуя сероводород: S + Н2 = H2S;
2) взаимодействуя с металлами, сера образует сульфиды: S + Fe = FeS; 2Al + 3S = Al2S3;
3) при сжигании серы в струе кислорода образуется сернистый газ или сернистый ангидрид SO2: S + O2 = SO2;
4) чистая сера способна проявлять восстановительные свойства: S + 2HNO3 = H2SO4 + 2NO.
Сера используется в большом количестве в народном хозяйстве. Серу используют для получения резины – при помощи серы происходит ее затвердевание (вулканизация).
Каучук с высоким содержанием серы называется эбонит, являющийся качественным электрическим изолятором. Для уничтожения некоторых сельскохозяйственных вредителей серу применяют в виде серного цвета. Серу используют для приготовления спичек, синей краски (ультрамарина), сероуглерода, серной кислоты.
Сероводород и сульфиды.
Сероводород (H2S) – бесцветный газ с резким запахом гниющего белка. В природе встречается вводах минеральных ключей вулканических газах, гниении отбросов, а также при разложении белков погибших растений и животных.
1) прямой синтез из элементов, при температуре 600 °C;
2) воздействием на сульфиды натрия и железа соляной кислотой.
Физические свойства: сероводород тяжелее воздуха, очень ядовит. Сжижение его происходит при -60,8 °C, затвердение – при -85,7 °C. Легко воспламеняется на воздухе. Растворим в воде – при температуре 20 °C в 1 литре воды можно растворить 2,5 литра сероводорода, при этом образуется сероводородная кислота.
Химические свойства: сероводород – сильный восстановитель, в зависимости от условий (температура, pH раствора, концентрация окислителя) при взаимодействии с окислителями он окисляется до диоксида серы или серной кислоты:
1) горит голубоватым пламенем на воздухе:
2) при высокой температуре разлагается:
3) вступает в реакцию с галогенами:
4) взаимодействует с окислителями:
5) серебро при взаимодействии с сероводородом темнеет:
Применение: сероводород используют как химический реактив, а также как сырье для получения серы и серной кислоты.
Сероводородная кислота – слабая кислота. Водный раствор сероводорода.
Сульфиды – средние соли сероводородной кислоты.
1) взаимодействие металлов с серой при высокой температуре: Fe + S = FeS;
2) взаимодействие сводными растворами солей металлов: CuSO4 + H2S = CuS? + H2SO4;
3) сульфиды подвергаются гидролизу:
Взбалтывая раствор сульфида с серой можно обнаружить после выпаривания остаток, содержащий полисульфиды (многосернистые металлы).
Полисульфиды – соединения с большим содержанием серы, например Na2S2, Na2S5.
Для сульфидов характерны соединения переменного состава (FeS1,01—FeS1,14).
Природные сульфиды – основа руд цветных и редких металлов, поэтому их используют в металлургии. Некоторые сульфиды используют в производстве серной кислоты(FeS2 – железный колчедан). В химической и легкой промышленности применяют сульфиды щелочных и щелочноземельных металлов (в качестве основы люминофоров). В электронной технике используются как полупроводники.
БИЛЕТ №38
Оксиды серы, сернистая кислота и ее соли.
Окси́д се́ры(IV) (диокси́д се́ры, двуокись серы, серни́стый газ, серни́стый ангидри́д) — SO2. В нормальных условиях представляет собой бесцветный газ с характерным резким запахом (запах загорающейся спички). Под давлением сжижается при комнатной температуре. Растворяется в воде с образованием нестойкой серни́стой кислоты; растворимость 11,5 г/100 г воды при 20 °C, снижается с ростом температуры. Растворяется также в этаноле, се́рной кислоте. SO2 — один из основных компонентов вулканических газов.
Получение
· Промышленный способ получения — сжигание серы или обжиг сульфидов, в основном — пирита:
· В лабораторных условиях и в природе SO2 получают воздействием сильных кислот на сульфиты и гидросульфиты. Образующаяся сернистая кислота H2SO3 сразу разлагается на SO2 и H2O:
· Также диоксид серы можно получить действием концентрированной серной кислоты на малоактивные металлы при нагревании:
Химические свойства
· Спектр поглощения SO2 в ультрафиолетовом диапазоне.
· Относится к кислотным оксидам. Растворяется в воде с образованием сернистой кислоты (при обычных условиях реакция обратима):
· Со щелочами образует сульфиты:
· Химическая активность SO2 весьма велика. Наиболее ярко выражены восстановительные свойства SO2, степень окисления серы в таких реакциях повышается:
Предпоследняя реакция является качественной реакцией на сульфит-ион SO32− и на SO2 (обесцвечивание фиолетового раствора).
· В присутствии сильных восстановителей SO2 способен проявлять окислительные свойства. Например, для извлечения серы из отходящих газов металлургической промышленности используют восстановление SO2 оксидом углерода(II):
· Или для получения фосфорноватистой кислоты:
Применение
Большая часть оксида серы(IV) используется для производства сернистой кислоты. Используется также в виноделии в качестве консерванта (пищевая добавка E220). Так как этот газ убивает микроорганизмы, им окуривают овощехранилища и склады. Оксид серы(IV) используется для отбеливания соломы, шелка и шерсти, то есть материалов, которые нельзя отбеливать хлором. Применяется он также и в качестве растворителя в лабораториях. При таковом его применении следует помнить о возможном содержании в SO2 примесей в виде SO3, H2O, и как следствие присутствия воды H2SO4 и H2SO3. Их удаляют пропусканием через растворитель концентрированной H2SO4; это лучше делать под вакуумом или в другой закрытой аппаратуре[1]. Оксид серы(IV) применяется также для получения различных солей сернистой кислоты.
Сероводород
Сероводород H2S – это бинарное соединение водорода с серой, относится к летучим водородным соединениям. Следовательно, сероводород бесцветный ядовитый газ, с запахом тухлых яиц. Образуется при гниении. В твердом состоянии имеет молекулярную кристаллическую решетку.
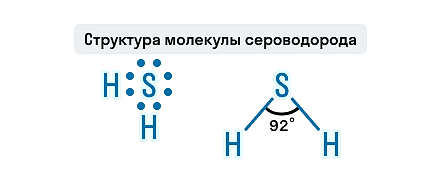
Геометрическая форма молекулы сероводорода похожа на структуру воды — уголковая молекула. Но валентный угол H-S-H меньше, чем угол H-O-H в воде и составляет 92,1 о .

Способы получения сероводорода
1. В лаборатории сероводород получают действием минеральных кислот на сульфиды металлов, расположенных в ряду напряжений левее железа.
Например , при действии соляной кислоты на сульфид железа (II):
FeS + 2HCl → FeCl2 + H2S↑
Еще один способ получения сероводорода – прямой синтез из водорода и серы:
Еще один лабораторный способ получения сероводорода – нагревание парафина с серой.
Видеоопыт получения и обнаружения сероводорода можно посмотреть здесь.
2. Также сероводород образуется при взаимодействии растворимых солей хрома (III) и алюминия с растворимыми сульфидами. Сульфиды хрома (III) и алюминия необратимо гидролизуются в водном растворе.
Например: х лорид хрома (III) реагирует с сульфидом натрия с образованием гидроксида хрома (III), сероводорода и хлорида натрия:
Химические свойства сероводорода
1. В водном растворе сероводород проявляет слабые кислотные свойства. Взаимодействует с сильными основаниями, образуя сульфиды и гидросульфиды:
Например , сероводород реагирует с гидроксидом натрия:
H2S + 2NaOH → Na2S + 2H2O
H2S + NaOH → NaНS + H2O
2. Сероводород H2S – очень сильный восстановитель за счет серы в степени окисления -2. При недостатке кислорода и в растворе H2S окисляется до свободной серы (раствор мутнеет):
В избытке кислорода:
3. Как сильный восстановитель, сероводород легко окисляется под действием окислителей.
Например, бром и хлор окисляют сероводород до молекулярной серы:
H2S + Br2 → 2HBr + S↓
H2S + Cl2 → 2HCl + S↓
Под действием избытка хлора в водном растворе сероводород окисляется до серной кислоты:
Например , азотная кислота окисляет сероводород до молекулярной серы:
При кипячении сера окисляется до серной кислоты:
Прочие окислители окисляют сероводород, как правило, до молекулярной серы.
Например , оксид серы (IV) окисляет сероводород:
Соединения железа (III) также окисляют сероводород:
H2S + 2FeCl3 → 2FeCl2 + S + 2HCl
Бихроматы, хроматы и прочие окислители также окисляют сероводород до молекулярной серы:
Серная кислота окисляет сероводород либо до молекулярной серы:
Либо до оксида серы (IV):
4. Сероводород в растворе реагирует с растворимыми солями тяжелых металлов : меди, серебра, свинца, ртути, образуя черные сульфиды, нерастворимые ни в воде, ни в минеральных кислотах.
Например , сероводород реагирует в растворе с нитратом свинца (II). при этом образуется темно-коричневый (почти черный) осадок, нерастворимый ни в воде, ни в минеральных кислотах:
Взаимодействие с нитратом свинца в растворе – это качественная реакция на сероводород и сульфид-ионы.
Видеоопыт взаимодействия сероводорода с нитратом свинца можно посмотреть здесь.
Кислоты. Химические свойства и способы получения

Перед изучением этого раздела рекомендую прочитать следующую статью:
Кислоты – сложные вещества, которые при взаимодействии с водой образуют в качестве катионов только ионы Н + (или Н3О + ).
По растворимости в воде кислоты можно поделить на растворимые и нерастворимые . Некоторые кислоты самопроизвольно разлагаются и в водном растворе практически не существуют (неустойчивые) . Подробно про классификацию кислот можно прочитать здесь.


Получение кислот
1. Взаимодействие кислотных оксидов с водой. При этом с водой реагируют при обычных условиях только те оксиды, которым соответствует кислородсодержащая растворимая кислота.
кислотный оксид + вода = кислота
Например , оксид серы (VI) реагирует с водой с образованием серной кислоты:
При этом оксид кремния (IV) с водой не реагирует:
2. Взаимодействие неметаллов с водородом. Таким образом получают только бескислородные кислоты.
Неметалл + водород = бескислородная кислота
Например , хлор реагирует с водородом:
H2 0 + Cl2 0 → 2 H + Cl —
3. Электролиз растворов солей. Как правило, для получения кислот электролизу подвергают растворы солей, образованных кислотным остатком кислородсодержащих кислот. Более подробно этот вопрос рассмотрен в статье Электролиз.
Например , электролиз раствора сульфата меди (II):
4. Кислоты образуются при взаимодействии других кислот с солями. При этом более сильная кислота вытесняет менее сильную.
Например: карбонат кальция CaCO3 (нерастворимая соль угольной кислоты) может реагировать с более сильной серной кислотой.
5. Кислоты можно получить окислением оксидов, других кислот и неметаллов в водном растворе кислородом или другими окислителями.
Например , концентрированная азотная кислота окисляет фосфор до фосфорной кислоты:
Химические свойства кислот
1. В водных растворах кислоты диссоциируют на катионы водорода Н + и анионы кислотных остатков. При этом сильные кислоты диссоциируют почти полностью, а слабые кислоты диссоциируют частично.
Например , соляная кислота диссоциирует почти полностью:
HCl → H + + Cl –
Если говорить точнее, происходит протолиз воды, и в растворе образуются ионы гидроксония:
HCl + H2O → H3O + + Cl –
Многоосновные кислоты диссоциируют cтупенчато.
Например , сернистая кислота диссоциирует в две ступени:
HSO3 – ↔ H + + SO3 2–
2. Кислоты изменяют окраску индикатора. Водный раствор кислот окрашивает лакмус в красный цвет, метилоранж в красный цвет. Фенолфталеин не изменяет окраску в присутствии кислот.
3. Кислоты реагируют с основаниями и основными оксидами .
С нерастворимыми основаниями и соответствующими им оксидами взаимодействуют только растворимые кислоты.
нерастворимое основание + растворимая кислота = соль + вода
основный оксид + растворимая кислота = соль + вода
Например , гидроксид меди (II) взаимодействует с растворимой бромоводородной кислотой:
При этом гидроксид меди (II) не взаимодействует с нерастворимой кремниевой кислотой.
С сильными основаниями (щелочами) и соответствующими им оксидами реагируют любые кислотами.

Щёлочи взаимодействуют с любыми кислотами — и сильными, и слабыми . При этом образуются средняя соль и вода. Эти реакции называются реакциями нейтрализации . Возможно и образование кислой соли, если кислота многоосновная, при определенном соотношении реагентов, либо в избытке кислоты. В избытке щёлочи образуется средняя соль и вода:
щёлочь(избыток)+ кислота = средняя соль + вода
щёлочь + многоосновная кислота(избыток) = кислая соль + вода
Например , гидроксид натрия при взаимодействии с трёхосновной фосфорной кислотой может образовывать 3 типа солей: дигидрофосфаты, фосфаты или гидрофосфаты.
При этом дигидрофосфаты образуются в избытке кислоты, либо при мольном соотношении (соотношении количеств веществ) реагентов 1:1.
При мольном соотношении количества щелочи и кислоты 1:2 образуются гидрофосфаты:
В избытке щелочи, либо при мольном соотношении количества щелочи и кислоты 3:1 образуется фосфат щелочного металла.

4. Растворимые кислоты взаимодействуют с амфотерными оксидами и гидроксидами.
Растворимая кислота + амфотерный оксид = соль + вода
Растворимая кислота + амфотерный гидроксид = соль + вода
Например , уксусная кислота взаимодействует с гидроксидом алюминия:

5. Некоторые кислоты являются сильными восстановителями. Восстановителями являются кислоты, образованные неметаллами в минимальной или промежуточной степени окисления, которые могут повысить свою степень окисления (йодоводород HI, сернистая кислота H2SO3 и др.).
Например , йодоводород можно окислить хлоридом меди (II):
4H I — + 2 Cu +2 Cl2 → 4HCl + 2 Cu + I + I2 0
6. Кислоты взаимодействуют с солями.
Кислоты реагируют с растворимыми солями только при условии, что в продуктах реакции присутствует газ, вода, осадок или другой слабый электролит . Такие реакции протекают по механизму ионного обмена.
Кислота1 + растворимая соль1 = соль2 + кислота2/оксид + вода

Например , соляная кислота взаимодействует с нитратом серебра в растворе:
Ag + NO3 — + H + Cl — → Ag + Cl — ↓ + H + NO3 —
Кислоты реагируют и с нерастворимыми солями. При этом более сильные кислоты вытесняют менее сильные кислоты из солей .
Например , карбонат кальция (соль угольной кислоты), реагирует с соляной кислотой (более сильной, чем угольная):
7. Кислоты взаимодействуют с кислыми и основными солями. При этом более сильные кислоты вытесняют менее сильные из кислых солей. Либо кислые соли реагируют с кислотами с образованием более кислых солей.
кислая соль1 + кислота1 = средняя соль2 + кислота2/оксид + вода
Например , гидрокарбонат калия реагирует с соляной кислотой с образованием хлорида калия, углекислого газа и воды:
KHCO3 + HCl → KCl + CO2 + H2O
Ещё пример : гидрофосфат калия взаимодействует с фосфорной кислотой с образованием дигидрофосфата калия:
При взаимодействии основных солей с кислотами образуются средние соли. Более сильные кислоты также вытесняют менее сильные из солей.
Например , гидроксокарбонат меди (II) растворяется в серной кислоте:
Основные соли могут взаимодействовать с собственными кислотами. При этом вытеснения кислоты из соли не происходит, а просто образуются более средние соли.
Например , гидроксохлорид алюминия взаимодействует с соляной кислотой:
Al (OH) Cl2 + HCl → AlCl3 + H2O
8. Кислоты взаимодействуют с металлами.
При этом протекает окислительно-восстановительная реакция. Однако минеральные кислоты и кислоты-окислители взаимодействуют по-разному.
К минеральным кислотам относятся соляная кислота HCl, разбавленная серная кислота H2SO4, фосфорная кислота H3PO4, плавиковая кислота HF, бромоводородная HBr и йодоводородная кислоты HI и др.
Такие кислоты взаимодействуют только с металлами, расположенными в ряду активности до водорода:

При взаимодействии минеральных кислот с металлами образуются соль и водород:
минеральная кислота + металл = соль + H2↑
Например , железо взаимодействует с соляной кислотой с образованием хлорида железа (II):
Fe + 2 H + Cl → Fe +2 Cl2 + H2 0
Кислоты-окислители (азотная кислота HNO3 любой концентрации и серная концентрированная кислота H2SO4(конц)) при взаимодействии с металлами водород не образуют, т.к. окислителем выступает не водород, а азот или сера. Продукты восстановления азотной или серной кислот бывают различными. Определять их лучше по специальным правилам. Эти правила подробно разобраны в статье Окислительно-восстановительные реакции . Я настоятельно рекомендую выучить их наизусть.
9. Некоторые кислоты разлагаются при нагревании.
Угольная H2CO3, сернистая H2SO3 и азотистая HNO2 кислоты разлагаются самопроизвольно, без нагревания:
Кремниевая H2SiO3, йодоводородная HI кислоты разлагаются при нагревании:
Химические свойства. Газообразный Н 2 S горит на воздухе голубым пламенем, образуя оксид серы (IV) и воду:
Газообразный Н 2 S горит на воздухе голубым пламенем, образуя оксид серы (IV) и воду:
2Н 2 S + 30 2 = 2SO 2 + 2Н 2 О.
Собственная ионизация жидкого сероводорода ничтожно мала.
В воде сероводород мало растворим, водный раствор H2S является очень слабой кислотой:
H2S → HS + H Ka = 6.9×10 моль/л; pKa = 6.89.
Реагирует с основаниями:
H2S + 2NaOH = Na2S + 2H2O
H2S + NaOH = NaHS + H2O
Сероводород — сильный восстановитель. На воздухе горит синим пламенем:
2H2S + ЗО2 = 2Н2О + 2SO2
при недостатке кислорода:
2H2S + O2 = 2S + 2H2O.
Сероводород реагирует также со многими другими окислителями, при его окислении в растворах образуется свободная сера или SO4, например:
3H2S + 4HClO3 = 3H2SO4 + 4HCl
2H2S + SO2 = 2Н2О + 3S
Сероводород встречается в вулканических газах, а также в воде некоторых минеральных источников – Пятигорска и Мацесты (на Кавказе), Любеня-Великого (Львовская область) и др. Природные сероводородные воды используются для лечения. Сероводород всегда образуется при гниении остатков растительных и животных организмов и расписании других органических веществ, в которые входит сера. Поэтому неприятный запах сероводорода распространяется от выгребных ям, сточных вод и особенно от тухлых яиц. Но в больших количествах в природе сероводород не накапливается, потому что он легко окисляется кислородом воздуха и разлагается.
Хотя сероводород и образуется при взаимодействии водорода с серой при нагревании, но его удобнее добывать при действии соляной кислоты на сульфид железа:
Сероводород – бесцветный газ, немного тяжелее воздуха с неприятным запахом. В воде растворяется очень хорошо. В 1 объеме воды при обычной температуре растворяется 2,58 объемы сероводорода. Раствор H 2 S в воде называют сероводородной водой. Сероводород – очень ядовитый. Длительное вдыхание воздуха, содержащего 1 объем сероводорода на 2000 объемов воздуха, может вызвать тяжелое отравление. При отравлении возникают головная боль, тошнота, головокружение. Отравленная сероводородом человек теряет способность чувствовать его запах. Вдыхание больших концентраций сероводорода может быть смертельным. Поэтому работать с ним следует очень осторожно.
Химическая связь серы с водородом в молекуле сероводорода ковалентная:
но общие электронные пары смещены от атомов водорода к атомам серы, поэтому сера проявляет отрицательную валентность. В водном растворе это смещение является еще большим.
В химическом отношении сероводород - сильный восстановитель. Восстановительные свойства его обуславливаются тем, что ион серы S 2 - сравнительно легко теряет два электрона и превращается в нейтральный атом серы S 0, а под воздействием сильных окислителей теряет шесть электронов и превращается в положительно заряженные ионы S 4 +. Так, при достаточном доступе кислорода сероводород горит на воздухе с образованием двуокиси серы и водяного пара:
При недостаточном доступе кислорода, или при охлаждении его пламени он сгорает с образованием воды и выделением свободной серы:
По этой же реакцией сероводород медленно окисляется в водном растворе. Поэтому когда сероводородной водой оставить на длительное время в контакте с воздухом, то H 2 S полностью окисляется и свободная сера выделится в виде мути. В водном растворе сероводород легко окисляется также галогенами и другими окислителя.
Водный раствор H2S (формула сероводордной кислоты) называется иначе сероводородной водой или сероводородной кислотой. Это одна из самых слабых минеральных кислот (индикаторы в ней не изменяют свою окраску), диссоциирует в 2 стадии:
H2S -- H+ + HS– K1 дисс. ≈ 6 ∙ 10-8
HS– -- H+ + S2– K2 дисс. ≈ 1 ∙ 10-14
Растворы сероводородной кислоты являются разбавленными, их максимальная молярная концентрация при 20оС и атмосферном давлении не превышает 0,12 моль/л, а степень диссоциации по первой ступени при этом составляет ~ 0,011%.
Сероводородная кислота может реагировать с металлами, стоящими в ряду напряжений до H2, проявляя окислительные свойства за счет ионов H+. Но такие реакции при обычных условиях протекают очень медленно из-за малой концентрации ионов H+ в растворе и, главным образом, на поверхности металла, т.к. большинство солей сероводородной кислоты нерастворимы в H2O. Аналогично H2S реагирует и с оксидами металлов, нерастворимыми гидроксидами.
Нерастворимые средниесоли сероводородной кислоты (сульфиды) получают взаимодействием серы с металлами или в реакциях обмена между растворами солей:
Na2S + CuSO4 = CuS↓ + Na2SO4
K2S + FeCl2 = FeS↓ + 2KCl
Растворимые сульфиды образованы щелочными и щелочноземельными металлами. Их можно получить взаимодействием растворов кислоты с металлами или щелочами. При этом в зависимости от молярного соотношения между исходными веществами могут образовываться как кислые (гидросульфиды), так и средние соли.
H2S + NaOH = NaHS + H2O (при недостатке щелочи)
H2S + 2NaOH = Na2S + 2H2O (в избытке щелочи)
В водных растворах средние соли сильно гидролизуются:
Na2S + HOH -- NaHS + NaOH
S2– + HOH -- HS– + OH–
поэтому их растворы имеют щелочную реакцию.
Сульфиды щелочноземельных металлов в водном растворе по первой стадии гидролизуются почти на 100% и существуют в виде растворимых кислых солей:
2CaS + 2HOH = Ca(HS)2 + Ca(OH)2
Сульфиды некоторых металлов (Al2S3, Fe2S3, Cr2S3) в H2O гидролизуются полностью:
Al2S3 + 6 H2O = 2Al(OH)3 + 3 H2S
Большинство сульфидов тяжелых металлов очень плохо растворимы в H2O.
Некоторые сульфиды (CuS, HgS, Ag2S, PbS) не разлагаются растворами сильных кислот. Поэтому сероводородная кислота может вытеснить сильные кислоты из водных растворов их солей, образованных данными металлами:
CuSO4 + H2S = CuS↓ + H2SO4
HgCl2 + H2S = HgS↓ +2HCl
Сероводородная кислота на воздухе медленно окисляется кислородом с выделением серы:
2H2S + О2 = 2S↓ + 2H2O
Поэтому со временем растворы H2S при хранении мутнеют.
Благодаря этой реакции, сероводород не накапливается в верхних слоях воды Черного моря, которые содержат много растворенного кислорода.
Сероводородная кислота, как и сероводород, является сильным восстановителем и окисляется теми же окислителями, что и H2S, с образованием аналогичных продуктов.
Сульфиды тяжелых металлов имеют различную яркую окраску и применяются для получения минеральных красок, используемых в живописи.
Важным свойством сульфидов является их окисление кислородом при обжиге. Эта реакция используется в металлургии для получения цветных металлов из сульфидных руд:
2CuS + 3O2 -- 2CuO + 2SO2↑
При обжиге сульфидов активных металлов образующиеся SO2 и оксид металла могут реагировать между собой с образованием солей сернистой кислоты:
Na2O + SO2 -- Na2SO3
Химические свойства: сероводород– сильный восстановитель, в зависимости от условий (температура, pH раствора, концентрация окислителя) при взаимодействии с окислителями он окисляется до диоксида серы или серной кислоты:
Химия сероводорода

Чтобы сдать ОГЭ в 9‑м классе, нужно знать, что такое сероводород, и помнить его химические свойства. Давайте узнаем, что это за вещество, как его получают и в какие реакции оно вступает.
· Обновлено 5 марта 2022
Ждём вас 8 октября в 13:00. Вместе с педагогами, психологами и другими экспертами в образовании и воспитании ответим на главные вопросы мам и пап.
Сероводород — это молекулярное соединение с ковалентной полярной связью. По-другому это вещество называется сернистым водородом или сульфидом водорода. Химическая формула сероводорода — H2S.
Строение и физические свойства сероводорода
Сероводород — это бесцветный газ с характерным запахом тухлых яиц, сладкий на вкус, тяжелее воздуха. Малорастворим в воде, хорошо растворим в спирте. На воздухе легко воспламеняется. Очень ядовит.
Вдыхание паров сероводорода даже в малых количествах может привести к тяжелому отравлению. Признак сильного отравления парами сероводорода — потеря обоняния, перестает ощущаться характерный неприятный запах газа.
Противоядия при отравлении сероводородом — вещества-окислители. При слабом отравлении необходимо выйти на свежий воздух, то есть повысить концентрацию вдыхаемого кислорода. В случае более сильного отравления полезно очень осторожно вдохнуть пары хлора.
Состав H2S представлен двумя элементами-неметаллами, атомы которых связаны ковалентной полярной связью. Молекула этого газа имеет угловое строение, этим она схожа с молекулой воды, но по сравнению с водой в молекуле сероводорода слабые водородные связи. Связи S—H образуют валентный угол, равный 92,1о, как показано на структурной формуле сероводорода.
Знание физических свойств сульфида водорода может спасти кому-то жизнь, и это не единственное применение химической теории на практике. На курсах подготовки к ОГЭ по химии в онлайн-школе Skysmart ученики не только разбирают задания экзамена, но и учатся применять полученные знания в реальной жизни.
Бесплатный курс для современных мам и пап от Екатерины Мурашовой. Запишитесь и участвуйте в розыгрыше 8 уроков

Способы получения сероводорода
Сероводород встречается в природе в вулканических газах и водах минеральных источников. Также он образуется в результате разложения белков погибших животных и растений, при гниении пищевых отбросов.
При высокой температуре сера взаимодействует с водородом, в результате образуется газ — сероводород:
Практический способ получения сероводорода — действие разбавленных кислот на сульфиды:
Полный гидролиз, в результате которого выделяется газ и выпадает осадок:
Сероводород можно получить путем нагревания смеси парафина и серы:
Действие концентрированной серной кислоты на щелочные и щелочноземельные металлы:
Химические свойства сероводорода
Горение
На воздухе сероводород горит голубым пламенем. Процесс может протекать в двух направлениях:
Полное горение. Продукты реакции — диоксид серы и вода:
Если внести в пламя сероводорода холодный предмет, например фарфоровую чашку, температура пламени значительно снизится и сероводород окислится до свободной серы, оседающей на чашке в виде желтого налета:
Растворимость в воде
Сероводород растворим в воде. Его раствор называют сероводородной водой или сероводородной кислотой. Формула сероводородной кислоты — H2S. Если кислота долго находится на воздухе и особенно на свету, она мутнеет, т. к. сера окисляется.
Сероводородная кислота — это слабая кислота, она диссоциирует ступенчато, в основном диссоциация протекает по первой ступени:
Свойства кислот
Так как раствор сероводорода является кислотой, то для него характерны свойства кислот:
изменение цвета индикатора — лакмус становится розовым в растворе сероводорода;
взаимодействие с активными металлами:
раствор сероводорода реагирует с основными оксидами:
взаимодействие со щелочами:
сероводородная кислота может вступать в реакции обмена с солями, если одним из продуктов реакции будет нерастворимый сульфид:
Взаимодействие с аммиаком
Раствор сероводородной кислоты взаимодействует с аммиаком:
Окисление металлов
Сероводород может окислять малоактивные металлы в присутствии кислорода:
Реакции с галогенами
Сероводород вступает в реакции с галогенами:
Качественные реакции
Качественная реакция на сероводород — бумага, смоченная раствором нитрата свинца (II), чернеет в присутствии сероводорода:
Восстановительные свойства
В молекуле сероводорода сера имеет низшую степень окисления, следовательно, сероводород проявляет свойства сильного восстановителя. При взаимодействии с сильнейшими окислителями он окисляется до серы, оксида серы (IV) или серной кислоты. Полнота окисления зависит от условий протекания химической реакции: температуры, pH раствора и концентрации окислителя:
в реакции с бромной водой наблюдается обесцвечивание раствора:
окисление сероводорода подкисленным раствором перманганата калия:
сероводород в кислой среде реагирует с дихроматом калия:
взаимодействие с кислотами-окислителями (HNO3, H2SO4):
Пошаговый гайд от Екатерины Мурашовой о том, как перестать делать уроки за ребёнка и выстроить здоровые отношения с учёбой.

Вопросы для самопроверки
Охарактеризуйте физические свойства сульфида водорода.
Перечислите свойства сероводородной кислоты. От чего зависит образование сульфидов и гидросульфидов?
Схеме превращений S −2 → S +4 соответствует уравнение:
Составьте уравнения четырех реакций, которые могут протекать между NaOH, H2S, CuCl2.
Верны ли следующие суждения?
А. Сероводород при взаимодействии со щелочами образует два вида солей: средние и кислые.
Б. Сероводород — восстановитель.
Читайте также:
