Символы химических элементов металлов
Обновлено: 17.05.2024
Ключевые слова конспекта:Химические элементы, знаки химических элементов.
В химии очень важным является понятие «химический элемент» (слово «элемент» по-гречески означает «составная часть»). Чтобы понять его сущность, вспомните, чем различаются смеси и химические соединения.
Например, железо и сера свои свойства в смеси сохраняют. Поэтому можно утверждать, что смесь порошка железа с порошком серы состоит из двух простых веществ — железа и серы. Так как химическое соединение сульфид железа образуется из простых веществ — железа и серы, то хочется утверждать, что сульфид железа тоже состоит из железа и серы. Но познакомившись со свойствами сульфида железа, мы понимаем, что этого утверждать нельзя. Это сложное вещество, образовавшееся в результате химического взаимодействия, обладает совершенно другими свойствами, нежели исходные вещества. Потому что в состав сложных веществ входят не простые вещества, а атомы определённого вида.
ХИМИЧЕСКИЙ ЭЛЕМЕНТ — это определённый вид атомов.
Так, например, все атомы кислорода независимо от того, входят ли они в состав молекул кислорода или в состав молекул воды, — это химический элемент кислород. Все атомы водорода, железа, серы — это соответственно химические элементы водород, железо, сера и т. д.
В настоящее время известно 118 различных видов атомов, т. е. 118 химических элементов. Из атомов этого сравнительно небольшого числа элементов образуется огромное многообразие веществ. (Понятие «химический элемент» будет уточнено и расширено в дальнейших конспектах).
Пользуясь понятием «химический элемент», можно уточнить определения простых и сложных веществ: ПРОСТЫМИ называют вещества, которые состоят из атомов одного химического элемента. СЛОЖНЫМИ называют вещества, которые состоят из атомов разных химических элементов.
Следует различать понятия «простое вещество» и «химический элемент», хотя их названия в большинстве случаев совпадают. Поэтому каждый раз, когда мы встречаем слова «кислород», «водород», «железо», «сера» и т. д., нужно понимать, о чём идёт речь — о простом веществе или о химическом элементе. Если, например, говорят: «Растворённым в воде кислородом дышат рыбы», «Железо — это металл, который притягивается магнитом», это значит, что речь идёт о простых веществах — кислороде и железе. Если же говорят, что кислород или железо входит в состав какого-либо вещества, то имеют в виду кислород и железо как химические элементы.
Химические элементы и образуемые ими простые вещества можно разделить на две большие группы: металлы и неметаллы. Примерами металлов служат железо, алюминий, медь, золото, серебро и др. Металлы пластичны, имеют металлический блеск, хорошо проводят электрический ток. Примерами неметаллов служат сера, фосфор, водород, кислород, азот и др. Свойства неметаллов разнообразны.
Знаки химических элементов
Каждый химический элемент имеет своё название. Для упрощённого обозначения химических элементов используют химическую символику. Химический элемент обозначают начальной или начальной и одной из последующих букв латинского названия данного элемента. Так, водород (лат. hydrogenium — гидрогениум) обозначают буквой Н, ртуть (лат. hydrargyrum — гидраргирум) — буквами Hg и т. д. Предложил современную химическую символику шведский химик Й. Я. Берцелиус в 1814 году
Сокращённые буквенные обозначения химических элементов — это знаки (или символы) химических элементов. Химический символ (химический знак) обозначает один атом данного химического элемента.
Список символов химических элементов

Список символов химических элементов — символы (знаки), коды или сокращения, используемые для краткого или наглядного представления наименований химических элементов и одноимённых простых веществ. Прежде всего это символы химических элементов и атомные номера (порядковый номер химического элемента) в Периодической системе элементов. Помимо них, в локальных целях могут использоваться:
- — уникальный цифровой идентификатор химических элементов и веществ, внесённых в реестр Химической реферативной службы (англ.Chemical Abstracts Service );
- сокращения, используемые в российской металлургии при маркировке компонентов в составе сплавовцветных и чёрныхметаллов;
- символы, используемые в нумизматике для обозначения монетных металлов;
- символы, используемые на финансовом рынке для обозначения некоторых металлов (прежде всего благородных) в качестве валютных ценностей или биржевых товаров; ;
- другие локальные системы кодирования и маркировки.
Содержание
Введение

Семь металлов алхимии соответствовали семи небесным светилам: золото — Солнце, серебро — Луна, олово — Юпитер, медь — Венера, свинец — Сатурн, ртуть — Меркурий, железо — Марс (гравюра из алхимического трактата Василия Валентина «Азот», XV век)
В настоящее время известно 118 химических элементов и более 400 простых веществ. Если не принимать в расчёт вещества сложные, то классическая европейская алхимия выделяла семь металлов (золото, серебро, железо, медь, олово, ртуть, свинец), три полуметалла (мышьяк, сурьму и висмут) и три неметалла (серу, углерод, фосфор). В Трактате по элементарной химии (фр. Traité élémentaire de chimie ), изданном в 1789 году, основоположник современной химии Лоран Лавуазье упоминал 17 металлов и полуметаллов, а также 6 неметаллов. В I половине XIX века были открыты некоторые металлы платиновой группы, новые щелочные, щелочноземельные и редкоземельные металлы. В конце XIX века началось исследование радиоактивных элементов. Во II половине XX веке были искусственно получены элементы трансурановые [1] .

Параллельно развивалась система краткой записи наименований химических элементов. Прежде всего это символика средневековой европейской алхимии, включавшая символические изображения, буквенные сокращения, а также их сочетания, и использовавшаяся для представления веществ, химических операций и приборов. Она сформировалась в XIII веке и просуществовала до конца XVIII века, периода становления химии как науки. В 1787 году французы Жан Гассенфратц [fr] и Пьер Адет [fr] предложили обозначать химические вещества более простыми знаками и буквами, которые при этом были бы тождественны для близких элементов. Так, все металлы должны были обозначаться кругами с начальной буквой латинского названия металла в середине, щёлочи — треугольниками. В начале XIX века получила распространение система английского химика Джона Дальтона, который ввёл обозначения в виде кружков, внутри которых помещались точки, чёрточки, начальные буквы английских названий элементов. В 1814 году шведский химик Йёнс Берцелиус предложил использовать простые буквенные символы химических элементов, которые и легли в основу современной системы обозначений [3] [2] .

Современные символы химических элементов состоят из первой буквы или из первой и одной из следующих букв латинского названия элемента (например, H — водород от лат. Hydrogenium , Ca — кальций от лат. Calcium , Rg — рентгений от лат. Roentgenium ). Отдельно или слева внизу от символа (1H, 20Ca, 111Rg) для обозначения химических элементов может использоваться атомный номер, он же порядковый номер химического элемента в Периодической системе химических элементов, равный количеству протонов в атомном ядре. Для новооткрытых трансурановых элементов, которые пока не получили утверждённого Международным союзом теоретической и прикладной химии (ИЮПАК) названия, используют трёхбуквенные обозначения, означающие числительное — порядковый номер. Например, Uut — унунтрий (лат. Ununtrium , 113), Uuh — унунгексий (лат. Ununhexium , 116). Утверждённые ИЮПАК символы являются международными, однако наряду с ними или вместо них в некоторых странах могут использоваться обозначения, произведённые от национальных названий элементов. Например, во Франции вместо международных символов азота (N), бериллия (Be) и вольфрама (W) могут использоваться сокращения Az (от фр. Azote ), Gl (фр. Glucinium ) и Tu (фр. Tungstène ). В США вместо знака ниобия (Nb) может применяться символ Cb (от лат. Columbium ) [3] . В Китае используется символика, основанная на иероглифах.
Документы XVII—XIX веков
В данном разделе приведены фрагменты некоторых работ алхимиков и химиков, представляющие собой списки химических элементов и их соединений, где указаны в том числе используемые в период создания работы символы.

Таблица химических и философских образов из книги Василия Валентина The Last Will and Testament (1670)

Аппараты и символы из книги Карло Ланцилотти (Carlo Lancillotti) и Иоганна Ланге (Johann Lange) Der brennende Salamander, oder Zerlegung, der zu der Chimie gehörigen Materien (1681)

Символы химии из второго тома Энциклопедии Дидро (1763)

Химические знаки из книги Торберна Бергмана A Dissertation on Elective Attractions (1775)

Таблица простых тел из книги Антуана Лавуазье Traité élémentaire de chimie (1789)

Символы, предложенные Антуаном Лавуазье (1789)

Элементы, их символы и атомные веса из книги Джона Дальтона A new system of chemical philosophy (1808)

Символы алхимии и нумизматики
 |  |
| Аверс золотой монеты | Аверс серебряной монеты |
| Современные памятные монеты России, на которых монетные металлы обозначены международными символами Au и Ag | |
В алхимии не существовало единой системы краткой записи наименований химических элементов, веществ и их соединений. Так, Торберн Бергман обозначал висмут символом [5] , Иоганн Эркслебен — буквой W (от устаревшего нем. Wismut, Wismuth ) [6] , в прочих источниках используется символ Нептуна — ♆. При этом применение алхимических символов не ограничивалось самой алхимией, они встречаются в геральдике (например, алхимический символ фосфора на гербе карликового государства Науру), в нумизматической литературе.
В древности основными монетными металлами были золото, серебро и медь. Все три входят в подгруппу меди, которая иногда называется монетной группой. И хотя для изготовления денег они использовались чаще всего в составе сплавов (стерлинг, бронза, латунь, электр и другие), в нумизматической литературе древние монеты, как правило, подразделяются только на золотые, серебряные и медные (бронзовые) вне зависимости от содержания примесей. Для краткого обозначения этих трёх металлов и их сплавов используются сокращения их латинских наименований, которые часто пишутся в виде лигатур:
- — AU или AV (от лат.Aurum, Avrvm ); — AR (от лат.Argentum , которое, в свою очередь, происходит от др.-греч. ἄργυρος , что означает «белый», «блестящий»); — AE (от лат.Aes , означавшего «медь», «бронза» и служившего названием древнеримских бронзовых слитков и монет ассов).
В таблице представлены:
Wikimedia Foundation . 2010 .
Полезное
Смотреть что такое "Список символов химических элементов" в других словарях:
Список химических элементов по символам — См. также: Список химических элементов по атомным номерам и Алфавитный список химических элементов Содержание 1 Символы, используемые в данный момент … Википедия
Символы химических элементов — Химический знак двухатомной молекулы хлора 35 Cимволы химических элементов (химические знаки) условное обозначение химических элементов. Вместе с химическими формулами, схемами и уравнениями химических реакций образуют формальный язык… … Википедия
Список знаков валют — Обзорная статья о знаках (символах) валют Знаки валют Об отдельных знаках см. статьи Символ рубля, Символ доллара, Символ евро, Символ фунта, Символ драма, Символ драхмы, Символ денария, Символ риала, Символ рупии, Символ иены, Символ… … Википедия
Медные монеты — … Википедия
Хронология открытий человечества — См. также: Хронология изобретений человечества История науки … Википедия
Знаковые системы — Список знаковых систем (систем обозначений и т.п.), используемых человеческой цивилизацией, за исключением письменностей, для которых имеется отдельный список. Содержание 1 Критерии включения в список 2 Математика … Википедия
Медицина — I Медицина Медицина система научных знаний и практической деятельности, целями которой являются укрепление и сохранение здоровья, продление жизни людей, предупреждение и лечение болезней человека. Для выполнения этих задач М. изучает строение и… … Медицинская энциклопедия
Мнемоника — Содержание 1 Основной метод запоминания в современной мнемонике 2 История … Википедия
Химический элемент — Химический элемент совокупность атомов с одинаковым зарядом ядра и числом протонов, совпадающим с порядковым (атомным) номером в таблице Менделеева[1]. Каждый химический элемент имеет свои название и символ, которые приводятся в… … Википедия
Дальтон, Джон — Джон Дальтон John Dalton Дата рожден … Википедия
1. Общая характеристика элементов металлов
Из \(118\) известных на данный момент химических элементов \(96\) образуют простые вещества с металлическими свойствами, поэтому их называют металлическими элементами .
Металлические химические элементы в природе могут встречаться как в виде простых веществ, так и в виде соединений. То, в каком виде встречаются металлические элементы в природе, зависит от химической активности образуемых ими металлов.
Металлические элементы, образующие химически активные металлы ( Li–Mg ), в природе чаще всего встречаются в виде солей (хлоридов, фторидов, сульфатов, фосфатов и других).
Соли, образуемые этими металлами, являются главной составной частью распространённых в земной коре минералов и горных пород.


В растворённом виде соли натрия, кальция и магния содержатся в природных водах. Кроме того, соли активных металлов — важная составная часть живых организмов. Например, фосфат кальция Ca 3 ( P O 4 ) 2 является главной минеральной составной частью костной ткани.
Металлические химические элементы, образующие металлы средней активности ( Al–Pb ), в природе чаще всего встречаются в виде оксидов и сульфидов.


Металлические элементы, образующие химически неактивные металлы ( Cu–Au ), в природе чаще всего встречаются в виде простых веществ.
 |  |  |
| Рис. \(7\). Самородное золото Au | Рис. \(8\). Самородное серебро Ag | Рис. \(9\). Самородная платина Pt |
Исключение составляют медь и ртуть, которые в природе встречаются также в виде химических соединений.

В Периодической системе химических элементов металлы занимают левый нижний угол и находятся в главных (А) и побочных (Б) группах.
Рис. \(13\). Положение металлов в Периодической системе. Знаки металлических химических элементов расположены ниже ломаной линии B — Si — As — Te
В электронной оболочке атомов металлов на внешнем энергетическом уровне, как правило, содержится от \(1\) до \(3\) электронов. Исключение составляют только металлы \(IV\)А, \(V\)А и \(VI\)А группы, у которых на наружном энергетическом уровне находятся соответственно четыре, пять или шесть электронов.
В атомах металлов главных подгрупп валентные электроны располагаются на внешнем энергетическом уровне, а у металлов побочных подгрупп — ещё и на предвнешнем энергетическом уровне.
Радиусы атомов металлов больше, чем у атомов неметаллов того же периода. В силу отдалённости положительно заряженного ядра атомы металлов слабо удерживают свои валентные электроны.
Рис. \(14\). Характер изменения радиусов атомов химических элементов в периодах и в группах. Радиусы атомов металлов существенно больше, чем радиусы атомов неметаллов, находящихся в том же периоде
Главное отличительное свойство металлов — это их сравнительно невысокая электроотрицательность (ЭО) по сравнению с неметаллами.

Рис. \(15\). Величины относительных электроотрицательностей (ОЭО) некоторых химических элементов (по Л. Полингу). ОЭО металлических химических элементов уступает соответствующей величине неметаллических химических элементов
Атомы металлов, вступая в химические реакции, способны только отдавать электроны, то есть окисляться, следовательно, в ходе превращений могут проявлять себя в качестве восстановителей .
Символы химических элементов металлов

Общая характеристика некоторых элементов
в связи с их положением в Периодической системе
Элемент ЕГЭ: 1.2.2. Общая характеристика металлов IA-IIIA групп в связи с их положением в Периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов. 1.2.3. Характеристика переходных элементов (меди, цинка, хрома, железа)… 1.2.4. Общая характеристика неметаллов IVA-VIIA групп…
1.2.2. Общая характеристика металлов IA-IIIA групп …
Все элементы IА–IIIА-групп Периодической системы относят к металлам (кроме бора). На внешнем энергетическом уровне эти элементы имеют не более трех электронов, что соответствует номеру группы, в которой они расположены.
Металлы IA-группы называют щелочными, так как при взаимодействии с водой они образуют щелочи. Металлы IIА-группы, за исключением бериллия и магния, называют щелочноземельными.
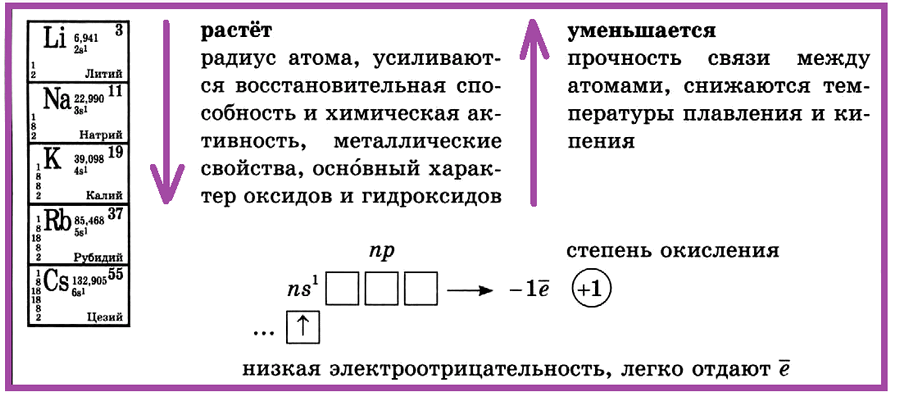
I группа, главная подгруппа —
щелочные металлы (литий, натрий, калий, рубидий, цезий).
I группа, главная подгруппа — щелочные металлы: литий, натрий, калий, рубидий, цезий. С увеличением порядкового номера в ПСХЭ растет радиус атома, усиливаются восстановительная способность и химическая активность, металлические свойства, основный характер оксидов и гидроксидов.
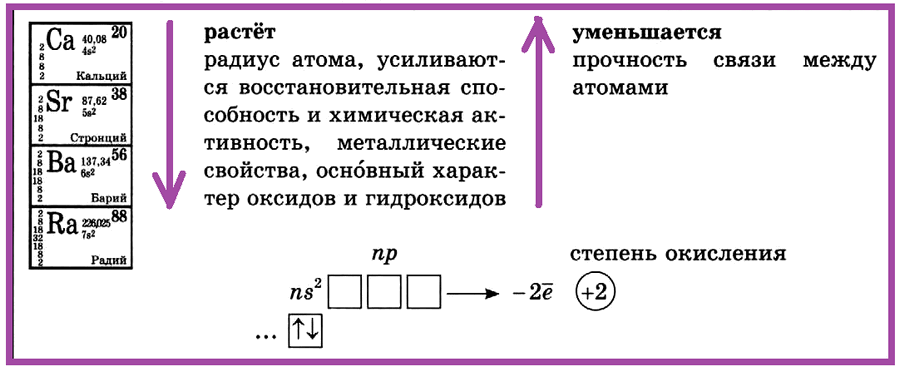
II группа, главная подгруппа —
щёлочноземельные металлы (кальций, стронций, барий, радий)
II группа, главная подгруппа — щёлочноземельные металлы: кальций, стронций, барий, радий. С увеличением порядкового номера в ПСХЭ растет радиус атома, усиливаются восстановительная способность и химическая активность, металлические свойства, оснОвный характер оксидов и гидроксидов.
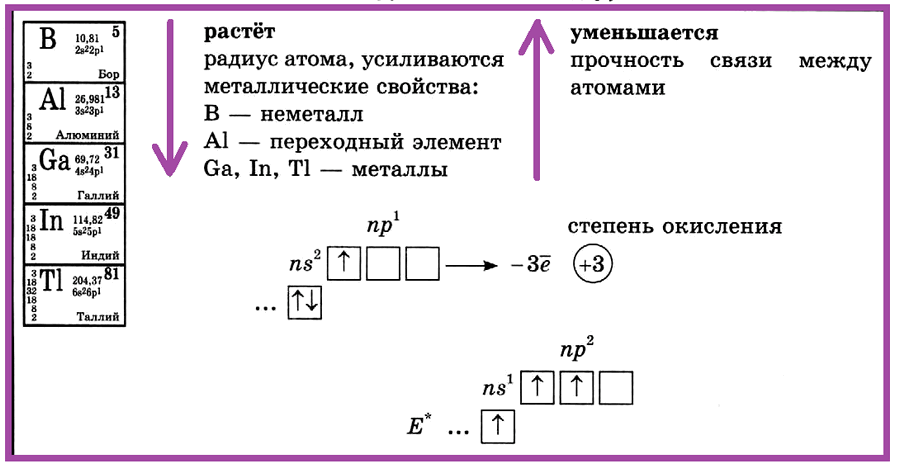
Элементы III группы главной подгруппы
(бор, алюминий, галлий, индий, таллий)
Элементы III группы главной подгруппы: бор, алюминий, галлий, индий, таллий. С увеличением порядкового номера в ПСХЭ растет радиус атома, усиливаются металлические свойства. В — неметалл, Аl — переходный элемент, Ga, In, Тl — металлы.
1.2.3. Характеристика переходных элементов (меди, цинка, хрома, железа) …
Понятие переходный элемент относится к d-элементам, занимающим переходное положение между s- и p-элементами. Они расположены в побочных подгруппах (группах IБ-VIIIБ). Все d-элементы являются металлами, валентные электроны которых расположены на ns- и (n–1)d-подуровнях, т.е. они имеют электронную конфигурацию: (n–1)d 1–10 ns 1–2 .
Читайте также: