Сколько металлов в 4 периоде
Обновлено: 17.05.2024
Переходные металлы (элементы) располагаются в побочных подгруппах Периодической системы Д.И. Менделеева. Их подразделяют на d-элементы и f-элементы. f-элементы – это лантаноиды и актиноиды.
В общем виде электронное строение переходных элементов можно представить следующим образом: (n – 1) d x ns y . На ns-орбитали содержится один или два электрона, остальные валентные электроны находятся на (n - 1) d-орбитали. Поскольку число валентных электронов заметно меньше числа орбиталей, то простые вещества, образованные переходными элементами, являются металлами.
Название "переходные" связано с тем, что в периодах переходные элементы вклиниваются между s- и р-элементами.
В отличие от s- и p-элементов, у которых заполняются внешние оболочки (соответственно ns- и np-оболочки), у переходных металлов заполняются внутренние (n — 1) d-оболочки (d-элементы) или (n — 2) f-оболочки (f-элементы).
Все переходные элементы имеют следующие общие свойства:
- Небольшие значения электроотрицательности.
- Переменные степени окисления. Почти для всех d-элементов, в атомах которых на внешнем ns-подуровне находятся 2 валентных электрона, известна степень окисления +2.
- Начиная с d-элементов III группы Периодической системы химических элементов Д. И. Менделеева, элементы в низшей степени окисления образуют соединения, которые проявляют основные свойства, в высшей — кислотные, в промежуточной — амфотерные.
- Для всех переходных элементов характерно образование комплексных соединений.
При образовании соединений атомы металлов могут использовать не только валентные s- и p-электроны, но и d-электроны. Поэтому для d-элементов гораздо более характерна переменная валентность, чем для элементов главных подгрупп. Благодаря этому свойству переходные металлы часто образуют комплексные соединения.
Все переходные элементы металлы. Поэтому в своих соединениях они проявляют положительные степени окисления. Большинство из них имеет характерный металлический блеск. По сравнению с s-металлами их прочность в целом значительно выше. В частности, для них характерны свойства: высокий предел прочности на разрыв; тягучесть; ковкость (их можно расплющить ударами в листы).
Есть три примечательных элемента из семейства переходных металлов. Эти элементы — железо, кобальт и никель, и они являются единственными элементами которые способны создавать магнитное поле.
Переходные элементы, кроме Fe и Ti, мало распространены в земной коре.
Значение переходных металлов для организма и жизнедеятельности.
Без переходных металлов наш организм существовать не может. Железо – это действующее начало гемоглобина. Цинк участвует в выработке инсулина. Кобальт – центр витамина В-12. Медь, марганец и молибден, а также некоторые другие металлы входят в состав ферментов.
Многие переходные металлы и их соединения используются в качестве катализаторов. Например, реакция гидрирования алкеновна платиновом или палладиевом катализаторе. Полимеризация этилена проводится с помощью титансодержащих катализаторов.
Большое использование сплавов переходных металлов: сталь, чугун, бронза, латунь, победит. При исследовании сплавов прослеживается уникальное значение железа для человека. Сплавы даже разделяют на черные и цветные по содержанию в них железа.
Переходные металлы 4 период:
Не нашли что искали? Вы можете оставить заявку, в форме обратной связи.
Портал Gosstanart.info не осуществляет коммерческой деятельности, не сотрудничает с рекламодателями, производителями товаров и компаниями предоставляющими услуги. Просьба, не обращаться с коммерческими предложениями! Вся информация, представленная на портале, результат независимых исследований и является свободно распространяемой информацией.
Элемент периода 4 - Period 4 element

A элемент 4 периода является одним из химические элементы в четвертой строке (или период ) периодической таблицы элементов. Таблица Менделеева выстроена в ряды, чтобы проиллюстрировать повторяющиеся (периодические) тенденции в химическом поведении элементов по мере увеличения их атомного номера: новая строка начинается, когда химическое поведение начинает повторяться, что означает, что элементы с аналогичным поведением попадают в одно и то же вертикальные колонны. Четвертый период содержит 18 элементов, начиная с калия и заканчивая криптоном - по одному элементу на каждую из восемнадцати групп. Он видит первое появление d-блока (который включает переходные металлы ) в таблице.
Содержание
- 1 Свойства
- 1.1 Атомная структура
- 3.1 Калий
- 3.2 Кальций
- 4,1 Скандий
- 4,2 Титан
- 4,3 Ванадий
- 4,4 Хром
- 4,5 Марганец
- 4,6 Железо
- 4,7 Кобальт
- 4,8 Никель
- 4,9 Медь
- 4,10 Цинк
- 5.1 Галлий
- 5.2 Германий
- 5.3 Мышьяк
- 5.4 Селен
- 5.5 Бром
- 5.6 Криптон
Свойства
Каждый из этих элементов стабилен, и многие из них чрезвычайно распространены в земной коре и / или ядре; это последний период без каких-либо нестабильных элементов. Многие переходные металлы в периоде 4 очень прочны и поэтому обычно используются в промышленности, особенно железо. Известно, что три соседних элемента токсичны: мышьяк один из наиболее известных ядов, селен токсичен для человека в больших количествах и бром, токсичная жидкость. Многие элементы необходимы для выживания человека, например, кальций, который формирует кости.
Атомная структура
Продвижение к увеличению атомного номера, принцип Ауфбау заставляет элементы периода помещать электроны на подоболочки 4s, 3d и 4p в указанном порядке. Однако есть исключения, например хром. Первые одиннадцать элементов - K, Ca, и переходные металлы - имеют от 1 до 11 валентных электронов соответственно, которые расположены на 4s и 3d.
Двенадцать электронов по электронной конфигурации из аргона достигают конфигурации цинка, а именно 3d 4s. От этого элемента заполненная трехмерная подоболочка эффективно отделяется от химии, и последующий тренд выглядит очень похоже на тенденции в периодах 2 и 3. Элементы p-блока периода 4 имеют свою валентную оболочку, состоящую из 4s и 4p подоболочки четвертой (n = 4) оболочки и подчиняются правилу октетов.
Для квантовой химии именно в этот период происходит переход от упрощенной парадигмы электронной оболочки к исследованию множества подоболочек различной формы, относительное расположение которых уровней энергии регулируется взаимодействием различных физических воздействий. Металлы периода s-блока помещают свой дифференцирующий электрон на 4s, имеющие вакансии среди номинально более низких n = 3 состояний - явление, невидимое для более легких элементов. Напротив, семь элементов от цинка до криптона являются самыми тяжелыми, если все электронные оболочки ниже валентной оболочки заполнены полностью. Это невозможно в последующие периоды из-за существования f-подоболочки, начиная с n = 4.
Список элементов
Химический элемент Химическая серия Электронная конфигурация 19 K Калий Щелочной металл [Ar] 4s 20 Ca Кальций Щелочноземельный металл [Ar] 4s 21 Sc Скандий Переходный металл [Ar] 3d 4s 22 Ti Титан Переходный металл [Ar] 3d 4s 23 V Ванадий Переходный металл [Ar] 3d 4s 24 Cr Хром Переходный металл [Ar] 3d 4s (*) 25 Mn Марганец Переходный металл [Ar] 3d 4s 26 Fe Железо Переходный металл [Ar] 3d 4s 27 Co Кобальт Переходный металл [Ar] 3d 4s 28 Ni Никель Переходный металл [Ar] 3d 4s 29 Cu Медь Переходный металл [Ar] 3d 4s (*) 30 Zn Цинк Металл после перехода [Ar] 3d 4s 31 Ga Галлий Металл после перехода [Ar] 3d 4s 4p 32 Ge Германий Металлоид [Ar] 3d 4s 4p 33 As Мышьяк Металлоид [Ar] 3d 4s 4p 34 Se Селен Реактивный неметалл al [Ar] 3d 4s 4p 35 Br Бром Реактивный неметалл [Ar] 3d 4s 4p 36 Kr Криптон Благородный газ [Ar] 3d 4s 4p Цвет фона показывает подкатегорию в тенденции металл – металлоид – неметалл:
Металл Металлоид Неметалл Неизвестные. химические. свойства Щелочной металл Щелочноземельный металл Лантанид Актинид Переходный металл Постпереходный металл Реактивный неметалл благородный газ элементы s-блока
Калий
Калий (K) - это щелочной металл, помещенный под натрий и более рубидия, и является первым элементом периода 4. Он является одним из наиболее реактивных элементов в периодической таблице, поэтому обычно встречается только в соединениях. Он очень быстро окисляется на воздухе, что объясняет его быструю реакцию с кислородом при контакте с воздухом. На свежем воздухе он довольно серебристый, но быстро начинает тускнеть, поскольку вступает в реакцию с воздухом. Он достаточно мягкий, чтобы его можно было разрезать ножом, и он является вторым наименее плотным элементом . Калий имеет относительно низкую точку плавления ; он растает, просто поместив его под небольшой открытый огонь. Он также менее плотен, чем вода, и может, в свою очередь, плавать.
Кальций
Кальций (Ca) - второй элемент в периоде. щелочноземельный металл, кальций почти никогда не встречается в природе из-за его высокой реакционной способности с водой. Он играет одну из наиболее широко известных и признанных биологических ролей у всех животных и некоторых растений, составляя кости и зубы, и используется в некоторых приложениях в клетках, таких как сигналы для клеточных процессов. Он считается самым распространенным минералом в массе тела.
элементы d-блока
Скандий
Скандий (Sc) - третий элемент в период, и является первым переходным металлом в периодической таблице. Скандий довольно распространен в природе, но его трудно выделить, поскольку он наиболее распространен в редкоземельных соединениях, из которых сложно выделить элементы. Из-за вышеупомянутых фактов у скандия очень мало коммерческих применений, и в настоящее время его единственное основное применение - это алюминиевые сплавы .
Титан
Титан (Ti) является элементом группы 4. Титан - один из наименее плотных металлов, а также один из самых прочных и устойчивых к коррозии, и поэтому он имеет множество применений, особенно в сплавах с другими элементами, такими как железо. Благодаря своим вышеупомянутым свойствам, он обычно используется в самолетах, клюшках для гольфа и других объектах, которые должны быть прочными, но легкими.
Ванадий
Ванадий (V) является элементом группы 5. Ванадий никогда не встречается в природе в чистом виде, но обычно содержится в соединениях. Ванадий во многом похож на титан, например, он очень устойчив к коррозии, однако, в отличие от титана, он окисляется на воздухе даже при комнатной температуре. Все соединения ванадия обладают по крайней мере некоторым уровнем токсичности, а некоторые из них чрезвычайно токсичны.
Хром (Cr) является элементом группы 6. Хром, как титан и ванадий до него, чрезвычайно устойчив к коррозии и действительно является одним из основных компонентов нержавеющей стали. Хром также имеет много красочных соединений и поэтому очень часто используется в пигментах, таких как хромовый зеленый.
Марганец
Марганец (Mn) является элементом группы 7. Марганец часто встречается в сочетании с железом. Марганец, как и хром до него, является важным компонентом нержавеющей стали , предотвращающим ржавление железа. Марганец также часто используется в пигментах, например, хром. Марганец также ядовит; если вдохнуть достаточно, это может вызвать необратимые неврологические нарушения.
Железо
Железо (Fe) является элементом группы 8. Железо является наиболее распространенным на Земле элементом того периода и, вероятно, самым известным из них. Это основной компонент стали. Железо-56 имеет самую низкую плотность энергии среди изотопа любого элемента, что означает, что это самый массивный элемент, который может быть произведен в сверхгигант звёздах. Железо также находит применение в организме человека; гемоглобин частично состоит из железа.
Кобальт
Кобальт (Co) является элементом группы 9. Кобальт обычно используется в пигментах, так как многие соединения кобальта имеют синий цвет. Кобальт также является основным компонентом многих магнитных и высокопрочных сплавов. Единственный стабильный изотоп, кобальт-59, является важным компонентом витамина B-12, в то время как кобальт-60 является компонентом ядерных осадков и может быть опасен в достаточно больших количествах из-за своей радиоактивности.
Никель
Никель (Ni) является элементом группы 10. Никель редко встречается в земной коре, в основном из-за того, что он реагирует с кислородом воздуха, причем большая часть никеля на Земле поступает из никелево-железных метеоритов. Однако никель очень распространен в ядре Земли ; наряду с железом это один из двух основных компонентов. Никель является важным компонентом нержавеющей стали, и во многих суперсплавах.
Медь (Cu) является элементом группы 11. Медь - один из немногих металлов, которые не имеют белого или серого цвета, единственными другими являются золото и цезий. Медь использовалась людьми в течение тысяч лет для придания красноватого оттенка многим объектам и даже является важным питательным веществом для человека, хотя слишком много ядовито. Медь также обычно используется в качестве консерванта древесины или фунгицидов.
Цинк (Zn) является элементом группы 12. Цинк - один из основных компонентов латуни, используемой с 10 века до нашей эры. Цинк также невероятно важен для человека; почти 2 миллиарда человек в мире страдают от дефицита цинка. Однако слишком много цинка может вызвать дефицит меди. Цинк часто используется в батареях, удачно названных угольно-цинковыми батареями, и важен для многих покрытий, поскольку цинк очень устойчив к коррозии.
Элементы p-блока
Галлий
Галлий (Ga) - это элемент в группе 13, в группе алюминий. Галлий примечателен тем, что он имеет температуру плавления около 303 кельвина, примерно при комнатной температуре. Например, в обычный весенний день он будет твердым, а в жаркий летний день - жидким. Галлий является важным компонентом сплава галинстан наряду с оловом. Галлий также можно найти в полупроводниках.
Германий
Германий (Ge) является элементом группы 14. Германий, как и вышеупомянутый кремний, является важным полупроводником и обычно используется в диодах и транзисторах, часто в сочетании с мышьяком. Германий довольно редко встречается на Земле, что привело к его сравнительно позднему открытию. Германий в соединениях иногда может раздражать глаза, кожу или легкие.
Мышьяк
Мышьяк (As) является элементом группы 15. Мышьяк, как упоминалось выше, часто используется в полупроводниках в сплавах с германием. Мышьяк в чистом виде и в некоторых сплавах невероятно ядовит для всей многоклеточной жизни и, как таковой, является обычным компонентом пестицидов. Мышьяк также использовался в некоторых пигментах до того, как была обнаружена его токсичность.
Селен
Селен (Se) является элементом группы 16. Селен - первый неметалл в период 4, со свойствами, подобными сере. Селен довольно редко встречается в природе в чистом виде, в основном он встречается в таких минералах, как пирит, но даже в этом случае он встречается довольно редко. Селен необходим человеку в следовых количествах, но в больших количествах он токсичен. Селен - это калькоген. Селен имеет мономольную структуру красного цвета. Но это металлический серый цвет по своей кристаллической структуре.
Бром (Br) является элементом группы 17 (галоген). В природе не существует в элементарной форме. Бром едва ли жидкий при комнатной температуре, его температура кипения составляет около 330 кельвинов. Бром также довольно токсичен и вызывает коррозию, но относительно инертные бромид-ионы можно найти в галите или поваренной соли. Бром часто используется в качестве антипирена, потому что многие соединения могут быть получены для высвобождения свободных атомов брома.
Криптон
Криптон (Kr) - это благородный газ, помещенный под аргоном и над ксеноном. Криптон, как благородный газ, редко взаимодействует с самим собой или другими элементами; Хотя соединения были обнаружены, все они нестабильны и быстро распадаются, и поэтому криптон часто используется в люминесцентных лампах. Криптон, как и большинство благородных газов, также используется в освещении из-за множества спектральных линий и по вышеупомянутым причинам.
Биологическая роль
Многие элементы периода 4 играют роль в контроле функции белка как вторичные мессенджеры, структурные компоненты или кофакторы фермента . Градиент калия используется клетками для поддержания мембранного потенциала, который позволяет активировать нейромедиатор и облегчает диффузию среди других процессов. Кальций является обычной сигнальной молекулой для белков, таких как кальмодулин, и играет критическую роль в запуске сокращения скелетных мышц у позвоночных. Селен является компонентом неканонической аминокислоты, селеноцистеина ; белки, содержащие селеноцистеин, известны как селенопротеины. Марганцевые ферменты используются как эукариотами, так и прокариотами и могут играть роль в вирулентности некоторых патогенных бактерий. Ванабины также известные как ванадий-ассоциированные белки, обнаружены в клетках крови некоторых видов морских брызг. Роль этих белков оспаривается, хотя есть некоторые предположения, что они действуют как переносчики кислорода. Ионы цинка используются для стабилизации цинкового пальца milleu многих ДНК-связывающих белков.
Элементы периода 4 также могут быть обнаружены в комплексе с органическими небольшие молекулы с образованием кофакторов. Наиболее известным примером этого является гем : железосодержащее порфирин соединение, ответственное за переносящую кислород функцию миоглобина и гемоглобина а также каталитическая активность ферментов цитохрома. Гемоцианин заменяет гемоглобин в качестве предпочтительного переносчика кислорода в крови некоторых беспозвоночных, включая подковообразных крабов, тарантулы и осьминоги. Витамин B 12 представляет собой одно из немногих биохимических применений кобальта.
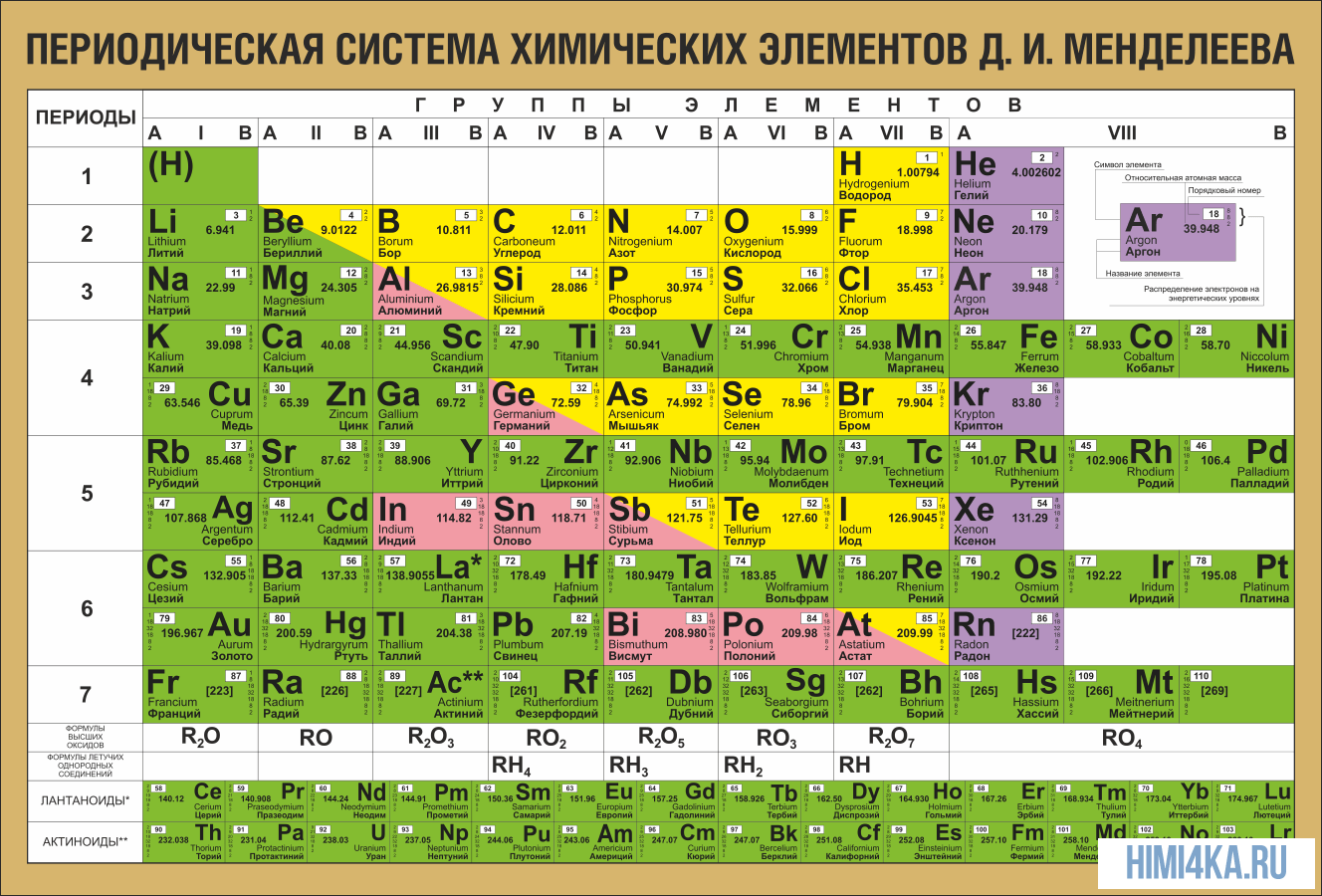
ПЕРИОДИЧЕСКАЯ ТАБЛИЦА МЕНДЕЛЕЕВА
Еще в школе, сидя на уроках химии, все мы помним таблицу на стене класса или химической лаборатории. Эта таблица содержала классификацию всех известных человечеству химических элементов, тех фундаментальных компонентов, из которых состоит Земля и вся Вселенная. Тогда мы и подумать не могли, что таблица Менделеева бесспорно является одним из величайших научных открытий, который является фундаментом нашего современного знания о химии.
![Таблица Менделеева]()
На первый взгляд, ее идея выглядит обманчиво просто: организовать химические элементы в порядке возрастания веса их атомов. Причем в большинстве случаев оказывается, что химические и физические свойства каждого элемента сходны с предыдущим ему в таблице элементом. Эта закономерность проявляется для всех элементов, кроме нескольких самых первых, просто потому что они не имеют перед собой элементов, сходных с ними по атомному весу. Именно благодаря открытию такого свойства мы можем поместить линейную последовательность элементов в таблицу, очень напоминающую настенный календарь, и таким образом объединить огромное количество видов химических элементов в четкой и связной форме. Разумеется, сегодня мы пользуемся понятием атомного числа (количества протонов) для того, чтобы упорядочить систему элементов. Это помогло решить так называемую техническую проблему «пары перестановок», однако не привело к кардинальному изменению вида периодической таблицы.
В периодической таблице Менделеева все элементы упорядочены с учетом их атомного числа, электронной конфигурации и повторяющихся химических свойств. Ряды в таблице называются периодами, а столбцы группами. В первой таблице, датируемой 1869 годом, содержалось всего 60 элементов, теперь же таблицу пришлось увеличить, чтобы поместить 118 элементов, известных нам сегодня.
Периодическая система Менделеева систематизирует не только элементы, но и самые разнообразные их свойства. Химику часто бывает достаточно иметь перед глазами Периодическую таблицу для того, чтобы правильно ответить на множество вопросов (не только экзаменационных, но и научных).
The YouTube ID of 1M7iKKVnPJE is invalid.
Периодический закон
Существуют две формулировки периодического закона химических элементов: классическая и современная.
Классическая, в изложении его первооткрывателя Д.И. Менделеева: свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величин атомных весов элементов.
Современная: свойства простых веществ, а также свойства и формы соединений элементов находятся в периодической зависимости от заряда ядра атомов элементов (порядкового номера).
Графическим изображением периодического закона является периодическая система элементов, которая представляет собой естественную классификацию химических элементов, основанную на закономерных изменениях свойств элементов от зарядов их атомов. Наиболее распространёнными изображениями периодической системы элементов Д.И. Менделеева являются короткая и длинная формы.
![]()
Группы и периоды Периодической системы
Группами называют вертикальные ряды в периодической системе. В группах элементы объединены по признаку высшей степени окисления в оксидах. Каждая группа состоит из главной и побочной подгрупп. Главные подгруппы включают в себя элементы малых периодов и одинаковые с ним по свойствам элементы больших периодов. Побочные подгруппы состоят только из элементов больших периодов. Химические свойства элементов главных и побочных подгрупп значительно различаются.
Периодом называют горизонтальный ряд элементов, расположенных в порядке возрастания порядковых (атомных) номеров. В периодической системе имеются семь периодов: первый, второй и третий периоды называют малыми, в них содержится соответственно 2, 8 и 8 элементов; остальные периоды называют большими: в четвёртом и пятом периодах расположены по 18 элементов, в шестом — 32, а в седьмом (пока незавершенном) — 31 элемент. Каждый период, кроме первого, начинается щелочным металлом, а заканчивается благородным газом.
Физический смысл порядкового номера химического элемента: число протонов в атомном ядре и число электронов, вращающихся вокруг атомного ядра, равны порядковому номеру элемента.
![]()
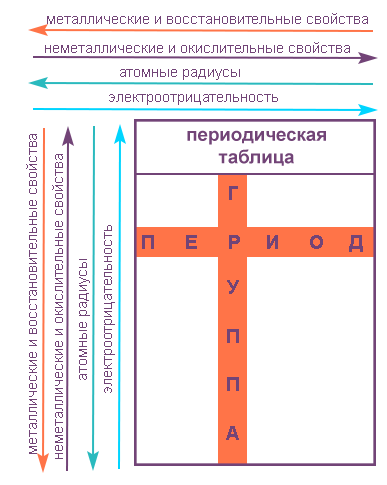
Свойства таблицы Менделеева
Напомним, что группами называют вертикальные ряды в периодической системе и химические свойства элементов главных и побочных подгрупп значительно различаются.
Свойства элементов в подгруппах закономерно изменяются сверху вниз:
- усиливаются металлические свойства и ослабевают неметаллические;
- возрастает атомный радиус;
- возрастает сила образованных элементом оснований и бескислородных кислот;
- электроотрицательность падает.
Все элементы, кроме гелия, неона и аргона, образуют кислородные соединения, существует всего восемь форм кислородных соединений. В периодической системе их часто изображают общими формулами, расположенными под каждой группой в порядке возрастания степени окисления элементов: R2O, RO, R2O3, RO2, R2O5, RO3, R2O7, RO4, где символом R обозначают элемент данной группы. Формулы высших оксидов относятся ко всем элементам группы, кроме исключительных случаев, когда элементы не проявляют степени окисления, равной номеру группы (например, фтор).
Оксиды состава R2O проявляют сильные основные свойства, причём их основность возрастает с увеличением порядкового номера, оксиды состава RO (за исключением BeO) проявляют основные свойства. Оксиды состава RO2, R2O5, RO3, R2O7 проявляют кислотные свойства, причём их кислотность возрастает с увеличением порядкового номера.
Элементы главных подгрупп, начиная с IV группы, образуют газообразные водородные соединения. Существуют четыре формы таких соединений. Их располагают под элементами главных подгрупп и изображают общими формулами в последовательности RH4, RH3, RH2, RH.
Соединения RH4 имеют нейтральный характер; RH3 — слабоосновный; RH2 — слабокислый; RH — сильнокислый характер.
Напомним, что периодом называют горизонтальный ряд элементов, расположенных в порядке возрастания порядковых (атомных) номеров.
В пределах периода с увеличением порядкового номера элемента:
- электроотрицательность возрастает;
- металлические свойства убывают, неметаллические возрастают;
- атомный радиус падает.
![]()
Элементы таблицы Менделеева
Щелочные и щелочноземельные элементы
К ним относятся элементы из первой и второй группы периодической таблицы. Щелочные металлы из первой группы — мягкие металлы, серебристого цвета, хорошо режутся ножом. Все они обладают одним-единственным электроном на внешней оболочке и прекрасно вступают в реакцию. Щелочноземельные металлы из второй группы также имеют серебристый оттенок. На внешнем уровне помещено по два электрона, и, соответственно, эти металлы менее охотно взаимодействуют с другими элементами. По сравнению со щелочными металлами, щелочноземельные металлы плавятся и кипят при более высоких температурах.
Щелочные металлы Щелочноземельные металлы Литий Li 3 Бериллий Be 4 Натрий Na 11 Магний Mg 12 Калий K 19 Кальций Ca 20 Рубидий Rb 37 Стронций Sr 38 Цезий Cs 55 Барий Ba 56 Франций Fr 87 Радий Ra 88 Лантаниды (редкоземельные элементы) и актиниды
Лантаниды — это группа элементов, изначально обнаруженных в редко встречающихся минералах; отсюда их название «редкоземельные» элементы. Впоследствии выяснилось, что данные элементы не столь редки, как думали вначале, и поэтому редкоземельным элементам было присвоено название лантаниды. Лантаниды и актиниды занимают два блока, которые расположены под основной таблицей элементов. Обе группы включают в себя металлы; все лантаниды (за исключением прометия) нерадиоактивны; актиниды, напротив, радиоактивны.
Лантаниды Актиниды Лантан La 57 Актиний Ac 89 Церий Ce 58 Торий Th 90 Празеодимий Pr 59 Протактиний Pa 91 Неодимий Nd 60 Уран U 92 Прометий Pm 61 Нептуний Np 93 Самарий Sm 62 Плутоний Pu 94 Европий Eu 63 Америций Am 95 Гадолиний Gd 64 Кюрий Cm 96 Тербий Tb 65 Берклий Bk 97 Диспрозий Dy 66 Калифорний Cf 98 Гольмий Ho 67 Эйнштейний Es 99 Эрбий Er 68 Фермий Fm 100 Тулий Tm 69 Менделевий Md 101 Иттербий Yb 70 Нобелий No 102 Галогены и благородные газы
Галогены и благородные газы объединены в группы 17 и 18 периодической таблицы. Галогены представляют собой неметаллические элементы, все они имеют семь электронов во внешней оболочке. В благородных газахвсе электроны находятся во внешней оболочке, таким образом с трудом участвуют в образовании соединений. Эти газы называют «благородными, потому что они редко вступают в реакцию с прочими элементами; т. е. ссылаются на представителей благородной касты, которые традиционно сторонились других людей в обществе.
Галогены Благородные газы Фтор F 9 Гелий He 2 Хлор Cl 17 Неон Ne 10 Бром Br 35 Аргон Ar 18 Йод I 53 Криптон Kr 36 Астат At 85 Ксенон Xe 54 — Радон Rn 86 Переходные металлы
Переходные металлы занимают группы 3—12 в периодической таблице. Большинство из них плотные, твердые, с хорошей электро- и теплопроводностью. Их валентные электроны (при помощи которых они соединяются с другими элементами) находятся в нескольких электронных оболочках.
Переходные металлы Скандий Sc 21 Титан Ti 22 Ванадий V 23 Хром Cr 24 Марганец Mn 25 Железо Fe 26 Кобальт Co 27 Никель Ni 28 Медь Cu 29 Цинк Zn 30 Иттрий Y 39 Цирконий Zr 40 Ниобий Nb 41 Молибден Mo 42 Технеций Tc 43 Рутений Ru 44 Родий Rh 45 Палладий Pd 46 Серебро Ag 47 Кадмий Cd 48 Лютеций Lu 71 Гафний Hf 72 Тантал Ta 73 Вольфрам W 74 Рений Re 75 Осмий Os 76 Иридий Ir 77 Платина Pt 78 Золото Au 79 Ртуть Hg 80 Лоуренсий Lr 103 Резерфордий Rf 104 Дубний Db 105 Сиборгий Sg 106 Борий Bh 107 Хассий Hs 108 Мейтнерий Mt 109 Дармштадтий Ds 110 Рентгений Rg 111 Коперниций Cn 112 Металлоиды
Металлоиды занимают группы 13—16 периодической таблицы. Такие металлоиды, как бор, германий и кремний, являются полупроводниками и используются для изготовления компьютерных чипов и плат.
Металлоиды Бор B 5 Кремний Si 14 Германий Ge 32 Мышьяк As 33 Сурьма Sb 51 Теллур Te 52 Полоний Po 84 Постпереходными металлами
Элементы, называемые постпереходными металлами, относятся к группам 13—15 периодической таблицы. В отличие от металлов, они не имеют блеска, а имеют матовую окраску. В сравнении с переходными металлами постпереходные металлы более мягкие, имеют более низкую температуру плавления и кипения, более высокую электроотрицательность. Их валентные электроны, с помощью которых они присоединяют другие элементы, располагаются только на внешней электронной оболочке. Элементы группы постпереходных металлов имеют гораздо более высокую температуру кипения, чем металлоиды.
Постпереходные металлы Алюминий Al 13 Галлий Ga 31 Индий In 49 Олово Sn 50 Таллий Tl 81 Свинец Pb 82 Висмут Bi 83 Неметаллы
Из всех элементов, классифицируемых как неметаллы, водород относится к 1-й группе периодической таблицы, а остальные — к группам 13—18. Неметаллы не являются хорошими проводниками тепла и электричества. Обычно при комнатной температуре они пребывают в газообразном (водород или кислород) или твердом состоянии (углерод).
Неметаллы Водород H 1 Углерод C 6 Азот N 7 Кислород O 8 Фосфор P 15 Сера S 16 Селен Se 34 Флеровий Fl 114 Унунсептий Uus 117 А теперь закрепите полученные знания, посмотрев видео про таблицу Менделеева и не только.
Отлично, первый шаг на пути к знаниям сделан. Теперь вы более-менее ориентируетесь в таблице Менделеева и это вам очень даже пригодится, ведь Периодическая система Менделеева является фундаментом, на котором стоит эта удивительная наука.
Периодический закон и Периодическая система химических элементов Д.И. Менделеева
![]()
Группы и периоды Периодической системы. Физический смысл порядкового номера химического элемента
Закономерности изменения свойств элементов и их соединений в связи с положением в Периодической системе химических элементов Д.И. Менделеева
Оксиды состава R2O проявляют сильные основные свойства, причём их основность возрастает с увеличением порядкового номера, оксиды состава RO (за исключением BeO) проявляют основные свойства.
Оксиды состава RO2, R2O5, RO3, R2O7 проявляют кислотные свойства, причём их кислотность возрастает с увеличением порядкового номера.
Тренировочные задания
1. Среди перечисленных химический элемент с максимальным радиусом атома — это
1) неон
2) алюминий
3) калий
4) кальций2. Среди перечисленных химический элемент с минимальным радиусом атома — это
1) алюминий
2) бор
3) калий
4) неон3. Наиболее ярко металлические свойства выражены у элемента
1) Rb
2) Li
3) Mg
4) Ca4. Наиболее ярко неметаллические свойства выражены у элемента
5. Наибольшее число валентных электронов у элемента
1) фтор
2) водород
3) натрий
4) сера6. Наименьшее число валентных электронов у элемента
1) кислород
2) кремний
3) водород
4) кальций7. Металлические свойства элементов возрастают в ряду
1) Ba, Li, Cs, Mg
2) Al, Mg, Ca, K
3) Li, Cs, Mg, Ba
4) Na, Mg, Li, Al8. Неметаллические свойства элементов ослабевают в ряду:
1) N, S, Br, Cl
2) O, S, Se, Te
3) Se, I, S, O
4) N, P, O, F9. Химические элементы перечислены в порядке возрастания атомного радиуса в ряду
1) углерод, бериллий, магний
2) калий, магний, алюминий
3) хлор, натрий, фтор
4) азот, фосфор, фтор10. Химические элементы перечислены в порядке убывания атомного радиуса в ряду
1) водород, бор, алюминий
2) углерод, кремний, калий
3) натрий, хлор, фтор
4) сера, кремний, магний11. Кислотные свойства водородных соединений усиливаются в ряду
12. Кислотные свойства водородных соединений ослабевают в ряду
13. Основные свойства соединений усиливаются в ряду
1) LiOH – KOH – RbOH
2) LiOH – KOH – Ca(OH)2
3) Ca(OH)2 – KOH – Mg(OH)2
4) LiOH – Ca(OH)2 – KOH14. Основные свойства соединений ослабевают в ряду
15. Во втором периоде Периодической системы элементов Д.И. Менделеева с увеличением заряда ядра у химических элементов:
1) возрастает электроотрицательность
2) уменьшается заряд ядра
3) возрастает атомный радиус
4) возрастает степень окисления16. Наиболее сильной кислотой, образованной элементом второго периода, является
1) угольная
2) азотная
3) фтороводородная
4) азотистая17. Наиболее сильное основание образует химический элемент
1) магний
2) литий
3) алюминий
4) калий18. Наиболее сильная бескислородная кислота соответствует элементу
1) селен
2) фтор
3) йод
4) сера19. В ряду элементов Li → B → N → F
1) убывает атомный радиус
2) возрастают металлические свойства
3) уменьшается число протонов в атомном ядре
4) увеличивается число электронных слоёв20. В ряду элементов Li → Na → K → Rb
1) убывает атомный радиус
2) ослабевают металлические свойства
3) уменьшается число протонов в атомном ядре
4) увеличивается число электронных слоёвПереходные металлы 5 период
Читайте также: