Сложные и простые вещества металлы и неметаллы
Обновлено: 18.05.2024
Мета́ллы (от лат. metallum — шахта, рудник) — группа элементов, в виде простых веществ, обладающих характерными металлическими свойствами, такими, как высокие тепло- и электропроводность, положительный температурный коэффициент сопротивления, высокая пластичность, ковкость и металлический блеск.
Из 118 химических элементов, открытых на данный момент (из них не все официально признаны), к металлам относят:
Таким образом, к металлам, возможно, относится 94 элемента из всех открытых; все остальные являются неметаллами.
В астрофизике термин «металл» может иметь другое значение и обозначать все химические элементы тяжелее гелия (см. Металличность).
Кроме того, в физике металлам [как проводникам] противоставляется полупроводники и диэлектрики (см. также Полуметалл (спинтроника)).
Слово «металл» заимствовано из немецкого языка. Отмечается в «Травнике» Николая Любчанина, написанном в 1534 году: «…злато и серебро всех металей одолеваетъ». Окончательно усвоено в Петровскую эпоху. Первоначально имело общее значение «минерал, руда, металл»; разграничение этих понятий произошло в эпоху М. В. Ломоносова.
Немецкое слово «metall» заимствовано из латинского языка, где «metallum» — «рудник, металл». Латинское, в свою очередь, заимствовано из греческого языка (μεταλλον — «рудник, копь»).
Бо́льшая часть металлов присутствует в природе в виде руд и соединений. Они образуют оксиды, сульфиды, карбонаты и другие химические соединения. Для получения чистых металлов и дальнейшего их применения необходимо выделить их из руд и провести очистку. При необходимости проводят легирование и другую обработку металлов. Изучением этого занимается наука металлургия. Металлургия различает руды чёрных металлов (на основе железа) и цветных (в их состав не входит железо, всего около 70 элементов). Золото, серебро и платина относятся также к драгоценным (благородным) металлам. Кроме того, в малых количествах они присутствуют в морской воде и в живых организмах (играя при этом важную роль).
Известно, что организм человека на 3 % состоит из металлов. Больше всего в организме кальция (в костях) и натрия, выступающего в роли электролита в межклеточной жидкости и цитоплазме. Магний накапливается в мышцах и нервной системе, медь — в печени, железо — в крови.
Все металлы (кроме ртути и, условно, франция) при нормальных условиях находятся в твёрдом состоянии, однако обладают различной твёрдостью. Ниже в таблице приводится твёрдость некоторых металлов по шкале Мооса.
Температуры плавления чистых металлов лежат в диапазоне от −39 °C (ртуть) до 3410 °C (вольфрам). Температура плавления большинства металлов (за исключением щелочных) высока, однако некоторые «нормальные» металлы, например, олово и свинец, можно расплавить на обычной электрической или газовой плите.
В зависимости от плотности, металлы делят на лёгкие (плотность 0,53 ÷ 5 г/см³) и тяжёлые (5 ÷ 22,5 г/см³). Самым лёгким металлом является литий (плотность 0.53 г/см³). Самый тяжёлый металл в настоящее время назвать невозможно, так как плотности осмия и иридия — двух самых тяжёлых металлов — почти равны (около 22.6 г/см³ — ровно в два раза выше плотности свинца), а вычислить их точную плотность крайне сложно: для этого нужно полностью очистить металлы, ведь любые примеси снижают их плотность.
Большинство металлов пластичны, то есть металлическую проволоку можно согнуть, и она не сломается. Это происходит из-за смещения слоёв атомов металлов без разрыва связи между ними. Самыми пластичными являются золото, серебро и медь. Из золота можно изготовить фольгу толщиной 0.003 мм, которую используют для золочения изделий. Однако не все металлы пластичны. Проволока из цинка или олова хрустит при сгибании; марганец и висмут при деформации вообще почти не сгибаются, а сразу ломаются. Пластичность зависит и от чистоты металла; так, очень чистый хром весьма пластичен, но, загрязнённый даже незначительными примесями, становится хрупким и более твёрдым. Некоторые металлы, такие, как золото, серебро, свинец, алюминий, осмий, могут срастаться между собой, но на это могут уйти десятки лет.
Все металлы хорошо проводят электрический ток; это обусловлено наличием в их кристаллических решётках подвижных электронов, перемещающихся под действием электрического поля. Серебро, медь и алюминий имеют наибольшую электропроводность; по этой причине последние два металла чаще всего используют в качестве материала для проводов. Очень высокую электропроводность имеет также натрий, в экспериментальной аппаратуре известны попытки применения натриевых токопроводов в форме тонкостенных труб из нержавеющей стали, заполненных натрием. Благодаря малому удельному весу натрия, при равном сопротивлении натриевые «провода» получаются значительно легче медных и даже несколько легче алюминиевых.
Высокая теплопроводность металлов также зависит от подвижности свободных электронов. Поэтому ряд теплопроводностей похож на ряд электропроводностей, и лучшим проводником тепла, как и электричества, является серебро. Натрий также находит применение как хороший проводник тепла; широко известно, например, применение натрия в клапанах автомобильных двигателей для улучшения их охлаждения.
Цвет у большинства металлов примерно одинаковый — светло-серый с голубоватым оттенком. Золото, медь и цезий соответственно жёлтого, красного и светло-жёлтого цвета.
На внешнем электронном уровне у большинства металлов небольшое количество электронов (1-3), поэтому они в большинстве реакций выступают как восстановители (то есть «отдают» свои электроны)
С кислородом реагируют все металлы, кроме золота, платины. Реакция с серебром происходит при высоких температурах, но оксид серебра(II) практически не образуется, так как он термически неустойчив. В зависимости от металла на выходе могут оказаться оксиды, пероксиды, надпероксиды:
оксид лития
пероксид натрия
надпероксид калия
С азотом реагируют только самые активные металлы, при комнатной температуре взаимодействует только литий, образуя нитриды:
С водородом реагируют только самые активные металлы, то есть металлы IA и IIA групп, кроме Be. Реакции осуществляются при нагревании, при этом образуются гидриды. В реакциях металл выступает как восстановитель, степень окисления водорода −1:
С углеродом реагируют только наиболее активные металлы. При этом образуются ацетилениды или метаниды. Ацетилениды при взаимодействии с водой дают ацетилен, метаниды — метан.
С кислотами металлы реагируют по-разному. Металлы, стоящие в электрохимическом ряду активности металлов (ЭРАМ) до водорода, взаимодействуют практически со всеми кислотами.
2. Немета́ллы — химические элементы с типично неметаллическими свойствами, которые занимают правый верхний угол Периодической системы. Расположение их в главных подгруппах соответствующих периодов следующее:
| Группа | I | III | IV | V | VI | VII | VIII |
|---|---|---|---|---|---|---|---|
| 1-й период | H | He | |||||
| 2-й период | B | C | N | O | F | Ne | |
| 3-й период | Si | P | S | Cl | Ar | ||
| 4-й период | As | Se | Br | Kr | |||
| 5-й период | Te | I | Xe | ||||
| 6-й период | At | Rn |
Характерной особенностью неметаллов является большее (по сравнению с металлами) число электронов на внешнем энергетическом уровне их атомов. Это определяет их большую способность к присоединению дополнительных электронов, и проявлению более высокой окислительной активности, чем у металлов.
Неметаллы имеют высокие значения сродства к электрону, большую электроотрицательность и высокий окислительно-восстановительный потенциал.
Благодаря высоким значениям энергии ионизации неметаллов, их атомы могут образовывать ковалентные химические связи с атомами других неметаллов и амфотерных элементов. В отличие от преимущественно ионной природы строения соединений типичных металлов, простые неметаллические вещества, а также соединения неметаллов имеют ковалентную природу строения.
В свободном виде могут быть газообразные неметаллические простые вещества — фтор, хлор, кислород, азот, водород, инертные газы, твёрдые — иод, астат, сера, селен, теллур, фосфор, мышьяк, углерод, кремний, бор, при комнатной температуре в жидком состоянии существует бром.
У некоторых неметаллов наблюдается проявление аллотропии. Так, для газообразного кислорода характерны две аллотропных модификации — кислород (O2) и озон (O3), у твёрдого углерода множество форм — алмаз, астралены, графен, графит, карбин, лонсдейлит, фуллерены, стеклоуглерод, диуглерод, углеродные наноструктуры (нанопена, наноконусы, нанотрубки, нановолокна) и аморфный углерод уже открыты, а ещё возможны и другие модификации, например, чаоит и металлический углерод.
В молекулярной форме в виде простых веществ в природе встречаются азот, кислород и сера. Чаще неметаллы находятся в химически связанном виде: это вода, минералы, горные породы, различные силикаты, фосфаты, бораты. По распространённости в земной коре неметаллы существенно различаются. Наиболее распространёнными являются кислород, кремний, водород; наиболее редкими — мышьяк, селен, иод.
Простые и сложные вещества

Из этой статьи вы узнаете, какие вещества называются простыми, а какие сложными, в чем их различия и особенности строения.
О чем эта статья:
Прежде чем переходить к понятиям простых и сложных веществ и к их строению, давайте вспомним, что такое химический элемент.
Химический элемент — это группа атомов с одинаковым зарядом ядра, который обусловливает его (элемента) химические свойства.
В зависимости от того, как соединяются друг с другом химические элементы, выделяют два типа веществ: простые и сложные.
Что такое простые вещества
Простые вещества — это вещества, образованные атомами только одного типа химического элемента. Например: H2, Na, P, Al.
Простые вещества делятся на два типа: металлы и неметаллы.
Металлы
Имеют общие между собой физические свойства. Обладают металлическим блеском, высокой тепло- и электропроводностью, твердые (за исключением ртути), пластичные и ковкие.
К простым веществам — металлам относятся: Na, Ca, Fe и т. д.
Почти все металлы имеют немолекулярное строение, т. е. состоят из атомов или ионов.
Неметаллы
Среди неметаллов выделить общие физические свойства практически невозможно. Они могут находиться в разных агрегатных состояниях, обладать различным цветом и т. д.
К простым веществам — неметаллам относятся: P, C, F2 и т. д.
Большинство неметаллов имеют молекулярное строение, т. е. состоят из молекул. При этом молекулы могут быть:
одноатомные: He, Si, Ar и другие;
двухатомные: F2, O2, H2, N2, Cl2, Br2, I2. Эти простые вещества всегда пишутся с индексом 2, их необходимо запомнить;
трехатомные — например, молекула озона O3;
и другие многоатомные.
Некоторые неметаллы имеют немолекулярное (атомное) строение: красный фосфор, кремний, алмаз и графит.
Металлы и неметаллы сильно отличаются друг от друга физическими и химическими свойствами.
При этом запоминать, к какому типу относится то или иное вещество, не нужно, достаточно посмотреть в таблицу Менделеева:
Проведите диагональ от 5-го до 85-го номера химических элементов.
Все химические элементы, находящиеся ниже и левее проведенной диагонали, образуют простые вещества — металлы (кроме водорода).
Выше диагонали химические элементы, находящиеся в главных подгруппах, образуют простые вещества — неметаллы, а в побочных — металлы.
Например, фосфор (порядковый номер — 15) расположен в таблице Менделеева выше диагонали и в главной подгруппе V группы. Значит, простое вещество фосфор — неметалл.
В большинстве случаев названия химического элемента и простого вещества совпадают. Поэтому необходимо научиться различать характеристики простого вещества и химического элемента.
Характеристика химического элемента
Характеристика простого вещества
Расположение в периодической системе (атомный номер, номер группы или периода)
Относительная атомная масса
Строение атома (число электронов, протонов или нейтронов, количество заполненных энергетических уровней)
Распространенность в природе
Содержание в соединении (например, в растительных белках или аминокислотах)
Значения электроотрицательности, сродства к электрону, энергии ионизации
Как правило, когда мы характеризуем простое вещество, то говорим о его физических или химических свойствах:
Влияние на живой организм
Температуры кипения и плавления
Взаимодействие с другими веществами
Содержание в каких-либо смесях веществ (например, газов)
Аллотропия
Аллотропия — это возможность образования химическим элементом нескольких простых веществ, которые отличаются друг от друга строением и свойствами.
Образующиеся простые вещества называют аллотропными модификациями.
Аллотропия характерна для следующих химических элементов:
углерод (алмаз, графит, графен, углеродные нанотрубки, фуллерен и другие);
фосфор (красный, белый и черный);
кислород (кислород и озон);
кремний (аморфный и кристаллический);
Рассмотрим две аллотропные модификации углерода:


The image 1 is a derivative of "Crystal" by manfredxy on Envato Elements.
The image 2 is a derivative of "Rough Graphite rock" by vvoennyy on Envato Elements.
Алмаз — бесцветное прозрачное вещество. Является одним из самых твердых веществ. Не проводит электрический ток.
Графит представляет собой вещество серо-черного цвета, обладает металлическим блеском. Имеет высокую тепло- и электропроводность.
Что такое сложные вещества
Сложные вещества — это вещества, образованные атомами нескольких химических элементов.
Например, молекула HNO3 состоит из одного атома водорода, одного атома азота и трех атомов кислорода.
К сложным веществам в химии относятся две большие группы веществ: неорганические и органические.
Неорганические вещества
Неорганические вещества делятся на 4 вида:
Оксиды — вещества, молекулы которых состоят из двух химических элементов, один из которых — кислород в степени окисления −2.
Основания — вещества, молекулы которых состоят из катиона металла и гидроксильной группы (—OH).
Кислоты — вещества, молекулы которых состоят из катиона водорода (H+), способного замещаться атомом металла, и кислотного остатка.
Соли — вещества, состоящие из катиона металла и кислотного остатка.
Кратко о классификации веществ можно узнать из схемы:
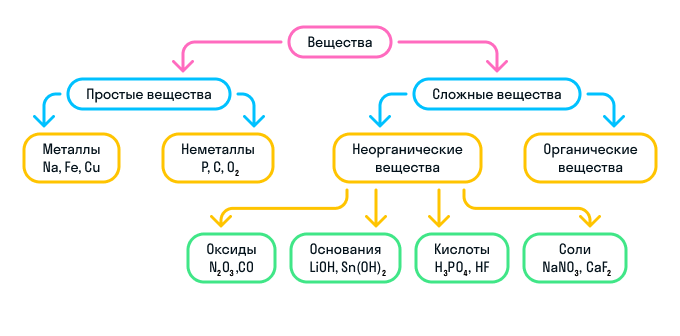
Номенклатура неорганических веществ
Названия простых веществ чаще всего совпадают с названием химического элемента, а для сложных веществ существует два вида номенклатуры: тривиальная и систематическая.
В тривиальной номенклатуре вещества названы в соответствии с их особенностями, например специфическим запахом или окраской.
В систематической номенклатуре название зависит от вида неорганического вещества.
Оксиды
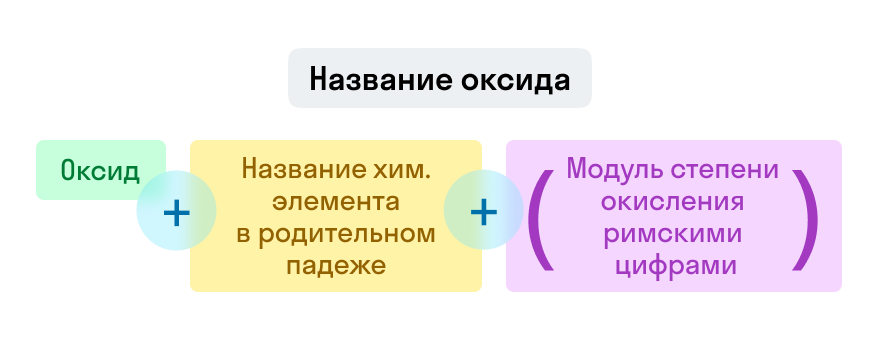
Примеры названий оксидов:
Fe2O3 — оксид железа (III). Читается: феррум два о три;
Na2O — оксид натрия. Читается: натрий два о.
Основания
Примеры названий гидроксидов:
Fe(OH)3 — гидроксид железа (III). Читается: феррум о аш трижды;
NaOH — гидроксид натрия. Читается: натрий о аш.
Соли
Примеры названий солей:
KNO3 — нитрат калия. Читается: калий эн о три;
AlCl3 — хлорид алюминия. Читается: алюминий хлор три.
Кислоты
Названия кислот, кислотных остатков и их формулы необходимо выучить, они приведены в таблице ниже.
Виды простых и сложных веществ
В неорганической химии вещества по составу делятся на простые и сложные.
- состоят из атомов одного химического элемента: сера S, углерод С, железо Fe, серебро Ag;
- подразделяют на металлы и неметаллы (включая благородные газы).
Сложные вещества — соединения:
- состоят из атомов двух или более химических элементов: N a 2 O , H C l , C u S O 4 ;
- подразделяют на: оксиды, основания, кислоты и соли.
Классификация простых веществ
1. Простые вещества условно делят на две группы: металлы и неметаллы.
Неметаллы в Периодической системе — это все элементы VIII А-группы (благородные газы) и VII А-группы (галогены), элементы VI А-группы (кроме полония), элементы V А-группы: азот, фосфор, мышьяк; углерод, кремний (IV А-группа); бор (III А-группа), а также водород. Остальные элементы относят к металлам.
Отличия свойств металлов и неметаллов приведены в таблице 1:
- газообразные: водород H 2 , азот N 2 , фтор F 2 ;
- жидкие: только бром B r 2 ;
- твёрдые: кремний Si, бор B, мышьяк As.
Амфотерные элементы находятся в А-группах Периодической системы: бериллий Be, алюминий Al, галлий Ga, германий Ge, олово Sn, свинец Pb, сурьма Sb, висмут Bi, полоний Po и др., а также большинство элементов Б-групп: хром Cr, марганец Mn, железо Fe, цинк Zn, кадмий Cd, золото Au и др., проявляют и металлические (оснóвные для соединений), и неметаллические (кислотные для соединений) свойства.
Благородные (инертные) газы (VIII А-группа Периодической системы): гелий He, неон Ne, аргон Ar, криптон Kr, ксенон Xe и радиоактивный радон Rn:
- обнаруживаются в воздухе, в малых количествах — в воде, горных породах, природных газах;
- не имеют цвета, вкуса и запаха;
- крайне химически инертны;
- используются в источниках света для создания освещения различных цветов (Ne — огненно-красный, Xe— синевато-серый, тусклый, Ar — фиолетово-голубой и др).
2. Сложные соединения и их отличия от простых веществ.
Сложные вещества бывают органические, в основе которых лежит углерод, и неорганические (безуглеродные и некоторые углеродсодержащие соединения: карбиды, карбонаты, оксиды углерода и другие). Неорганические чаще всего подразделяют на оксиды, основания, кислоты и соли.
Главные отличия сложных неорганических веществ:
- Свойства элементов, входящих в соединение, не сохраняются. Например, металл кальций Ca и неметалл хлор C l 2 . Каждому из этих простых веществ присущи свои характеристики. А соль C a C l 2 имеет новые, отличные от характеристик простых веществ, свойства, сходные со свойствами класса солей.
- В ходе химических реакций сложное вещество может быть получено или разложено на составные части.
- Количественный состав сложного соединения всегда одинаков, независимо от места нахождения и способа получения (для веществ молекулярного состава).
Классификация неорганических соединений и их основные свойства приведены в таблице 2.
- газы: N O , C O 2
- жидкости: H 2 O
- твёрдые: C u O , S i O 2
- газы: H 2 S , H C l
- жидкости: H N O 3 , H 2 S O 4
- твёрдые: H 3 P O 4 , H 3 B O 3
- оксиды металлов (оснóвные): K 2 O , CaO;
- оксиды неметаллов (кислотные): N 2 O 5 , S O 3 ;
- амфотерные: ZnO, A l 2 O 3 .
- оснóвные: LiOH, C a ( O H ) 2 ;
- амфотерные: B e ( O H ) 2 , C r ( O H ) 3 .
- кислородсодержащие: H 2 S O 4 , H N O 3 ;
- бескислородные: H J , H 2 S .
- средние: N a 3 ( P O 4 ) 2 , C a C l 2 ;
- кислые: K H C O 3 , N a 2 H P O 4 ;
- оснóвные: Mg(OH)Cl, C u 2 ( O H ) 2 C O 3 ;
- комплексные: K 2 [ B e ( C O 3 ) 2 ] .
Классы и номенклатура неорганических веществ
Номенклатура — способ называния веществ.
Химическая формула — представление состава вещества с использованием символов химических элементов, числовых индексов и других знаков. Химическое название определяется составом вещества и изображается с помощью слова или группы слов. Названия строятся по номенклатурным правилам, с использованием русских названий элементов, кроме случаев, когда традиционно употребляются латинские корни (таблица 3):
| Ag — аргент | C — карб, карбон | H — гидр, гидроген | N — нитр | Pb — плюмб, | Si — сил, силик, силиц |
| As — арс, арсен | Cu — купр | Hg — меркур | Ni — никкол | S — сульф | Sn -станн |
| Au — аур | Fe — ферр | Mn — манган | O — окс, оксиген | Sb — стиб | |
| Например, оксид натрия N a 2 O , карбонат кальция C a C O 3 , перманганат калия K M n O 4 | |||||
- Названия простых веществ чаще всего совпадают с русскими названиями соответствующих химических элементов. По необходимости к ним добавляется числовая греческая приставка: моно — 1, ди (латинский) — 2, три — 3, тетра — 4, пента — 5, гекса — 6, гепта — 7, окта — 8, нона (латинский) — 9, дека — 10. Например, (моно) кальций Ca, (моно) медь Cu, дикислород O 2 , трикислород O 3 , тетрафосфор P 4 . Исключение: аллотропные модификации: углерода С — графит, сажа, алмаз; кислорода — озон O3.
- Названия сложных веществ составляют по химической формуле справа налево. Для каждого класса веществ существуют свои правила составления формул и названий:
- формула оксидов: ЭnOm, где n и m — числовые индексы, определяющиеся степенями окисления элементов. Например,
Li+1 и O-2→ L i 2 O ; Al+3 и O-2→ A l 2 O 3 ; N+5 и O-2→ N 2 O 5 .
Название оксида: слово «оксид» в именительном падеже + название элемента Э в родительном падеже: оксид лития L i 2 O , оксид алюминия A l 2 O 3 .
Если элемент образует несколько оксидов, то в конце добавляют степень окисления римскими цифрами, заключая их в скобки:
- P 2 O 5 — пентаоксид (ди)фосфора или оксид фосфора (V), читается: «оксид фосфора пять»;
- F e 2 O 3 — триоксид (ди)железа или оксид железа (III), читается: «оксид железа три».
Оксиды, которым соответствуют кислоты, также называют ангидридами: серный ангидрид S O 3 , азотный ангидрид N 2 O 5 и др.
- формула оснований: Me+n(OH-)n, где нижний индекс n — количество гидроксид-анионов OH-.
K+1 и OH- → KOH, Mg+2 и OH- → M g ( O H ) 2 .
Название: слово «гидроксид» в именительном падеже + название элемента в родительном падеже: гидроксид калия, гидроксид магния.
Если элемент образует несколько гидроксидов, то в конце добавляют степень окисления римскими цифрами, заключая их в скобки:
F e ( O H ) 2 — гидроксид железа (II), C r ( O H ) 3 — гидроксид хрома (III).
- формула кислот HnК, где K — кислотный остаток.
Названия бескислородных кислот: корень русского названия элемента, образующего кислоту + суффикс «о» + «-водородная кислота», например: HBr — бромоводородная кислота, HCl — хлороводородная кислота, H 2 S — сероводородная кислота.
Названия кислородсодержащих кислот: русское название образующего элемента + «кислота», с учетом правил:
- Если элемент находится в высшей степени окисления, то окончание будет «-ная» или «-овая»: H 2 S O 4 — серная кислота, H 3 A s O 4 — мышьяковая кислота. Окончание меняется с понижением степени окисления в последовательности: «-оватая» ( H C l O 3 — хлорноватая кислота), «-истая» ( H C l O 2 — хлористая кислота), «-оватистая» (HClO— хлорноватистая кислота).
- Если оксиду соответствует не одна кислота, то к названию кислоты с минимальным числом атомов кислорода, добавляется приставка «мета», а к названию кислоты с максимальным числом атомов кислорода — «орто», например, H P O 3 — метафосфорная кислота, H 3 P O 4 — ортофосфорная кислота.
Названия наиболее распространенных кислот и их остатков приведены в таблице 4:
| Формула и название кислоты | Название кислотного остатка, образующего соль |
| H A l O 2 метаалюминиевая | метаалюминат |
| H 3 A l O 3 ортоалюминиевая | ортоалюминат |
| H A s O 3 метамышьяковая | метаарсенат |
| H 3 A s O 4 ортомышьяковая | ортоарсенат |
| H 3 B O 3 ортоборная | ортоборат |
| HBr бромоводородная | бромид |
| HBrO бромноватистая | гипобромит |
| H B r O 3 бромноватая | бромат |
| HCN циановодородная | цианид |
| H 2 C O 3 угольная | карбонат |
| HCl хлороводородная | хлорид |
| HClO хлорноватистая | гипохлорит |
| H C l O 2 хлористая | хлорит |
| H C l O 3 хлорноватая | хлорат |
| H C l O 4 хлорная | перхлорат |
| HF фтороводородная | фторид |
| HJ йодоводородная | йодид |
| H M n O 4 марганцовая | перманганат |
| H N O 2 азотистая | нитрит |
| H N O 3 азотная | нитрат |
| H P O 3 метафосфорная | метафосфат |
| H 3 P O 4 ортофосфорная | ортофосфат |
| H 2 S сероводородная | сульфид |
| H 2 S O 3 сернистая | сульфит |
| H 2 S O 4 серная | сульфат |
| H 2 S i O 3 метакремниевая | метасиликат |
| H 3 S i O 4 ортокремниевая | ортосиликат |
Название образуется в зависимости от типа соли.
- Средние соли — наименование кислотного остатка в именительном падеже + наименование катиона в родительном падеже, если необходимо, добавляется степень окисления: хлорид натрия NaCl, сульфат меди (II) C u S O 4 и т.д.
- Кислые (только для многоосновных кислот) — приставка «гидро», при необходимости добавляется числовое значение (ди—, три—, тетра— и т.д.) + название кислотного остатка + название катиона: гидрокарбонат натрия N a H C O 3 , дигидроортофосфат бария B a ( H 2 P O 4 ) 2 .
- Оснóвные — приставка «гидроксо» с числовым значением, если необходимо + название кислотного остатка + название катиона: гидроксохлорид магния MgOHCl, дигидроксохлорид железа (III) F e ( O H ) 2 C l .
- Двойные — анион в именительном падеже + катионы через дефис в родительном падеже: ортофосфат аммония—магния N H 4 M g P O 4 метасиликат алюминия—лития L i A l ( S i O 3 ) 2 .
- Смешанные — название анионов через дефис в именительном падеже + название катиона в родительном падеже: хлорид-гипохлорит кальция Ca(ClO)Cl; нитрат-йодат натрия N a 2 I O 3 ( N O 3 ) .
- Комплексные — название катиона в именительном падеже + название аниона в родительном падеже: хлорид диамминсеребра (I) [ A g ( N H 3 ) 2 ] C l ; тетрагидроксоалюминат натрия N a [ A l ( O H ) 4 ] .
- номенклатура бинарных соединений.
Бинарные соединения — сложные вещества, состоящие из двух элементов. В таких соединениях встречается два типа химической связи: ковалентная полярная (для неметаллов и некоторых амфотерных элементов) или ионная (для солей бескислородных кислот).
Названия строятся по схеме: к корню более электроотрицательного элемента добавляется окончание -ид (оксид, гидрид, карбид и т.д.) в именительном падеже + название второго элемента в родительном падеже, при необходимости добавляется числовое значение степени окисления: C S 2 — дисульфид углерода или сульфид углерода (IV), M n F 4 — тетрафторид марганца или фторид марганца (IV).
Для некоторых есть тривиальные названия: N H 3 — аммиак, S i Н 4 — силан, P H 3 — фосфин и др.
Строение и химические свойства
Простые вещества состоят из атомов одного химического элемента:
- одноатомные: благородные газы — гелий He, неон Ne, аргон Ar, криптон Kr, ксенон Xe и радон Rn;
- двухатомные: водород H 2 , кислород O 2 , азот N 2 и галогены: хлор C l 2 , йод J 2 , бром B r 2 ;
- трех и более атомные: озон O 3 , белый фосфор P 4 , кристаллическая (ромбическая и моноклинная) сера S 8 .
Порядок соединения атомов при образовании из них веществ обусловливает особенности строения веществ. Различают вещества молекулярного и немолекулярного строения. Немолекулярное строение имеют все металлы и большинство их соединений, графит, красный фосфор, алмаз, кремний Si и др. Большинство неметаллов и их соединений состоят из молекул, т. е. имеют молекулярное строение.
Химические свойства металлов и неметаллов
1. Химические свойства металлов определяются способностью отдавать свободные электроны с внешнего уровня. Они являются восстановителями. Взаимодействие идет с:
- неметаллами:
- +кислород O 2 (кроме золота и металлов группы платины) → оксиды: 2 C a + O 2 → 2 C a O ;
- +галогены ( F 2 , C l 2 , B r 2 ) → галогениды (фторид, хлорид, бромид и т.д.): C u + B r 2 → C u B 2 ;
- +азот, фосфор, сера, водород → нитриды, фосфиды, сульфиды, гидриды: 3 C a + N 2 → C a 3 N 2 .
- водой (только щелочные и щелочно-земельные металлы) → гидроксиды: 2 N a + 2 H 2 O → 2 N a O H + H 2 ↑ ;
- кислотами (металлы, стоящие в ряду активности до водорода) → соль: M g + 2 H C l → M g C l 2 + H 2 ↑ ;
- растворами солей менее активных металлов: F e + C u S O 4 → F e S O 4 + C u , при следующих условиях:
- соли, вступающие в реакцию и получающиеся в ходе нее, должны быть растворимы;
- металл вытесняет из соли другой металл, если находится левее в ряду активности;
- щелочные и щелочно-земельные металлы в данном случае будут вступать в реакцию с водой, а не с солью.
- оксидами (более активный металл вытесняет менее активный): F e 2 O 3 + 2 A l → A l 2 O 3 + 2 F e .
2. Химические свойства неметаллов обусловлены свободными электронами (от 3 до 7) на внешнем электронном уровне.
- окислительные свойства наиболее характерны (стремятся присоединять электроны) в реакциях с:
- металлами: O 2 + 2 M g → 2 M g O ; S + 2 N a → N a 2 S ;
- неметаллами:
- кислород O 2 (из галогенов реагирует только фтор): S + O 2 → S O 2 ;
- водород H 2 (кроме кремния, фосфора и бора) : С + 2 H 2 → C 4 ;
- неметалл c меньшей электроотрицательностью: 3 S + 2 P → P 2 S 3 (нагревание без доступа воздуха, сера — окислитель);
- солями (вытесняют менее активные неметаллы): C l 2 + 2 N a B r → 2 N a C l + B r 2 .
- восстановительные свойства (исключение: фтор F — всегда окислитель) в некоторых реакциях с:
- неметаллами, электроотрицательность которых ниже: C + O 2 → C O 2 (углерод — восстановитель);
- сложными веществами — окислителями ( C u O , H N O 3 ) : S + 6 H N O 3 → H 2 S O 4 + 6 N O 2 ↑ + 2 H 2 O .
- и окислительные, и восстановительные свойства проявляют хлор, сера, фосфор, йод и бром в реакциях диспропорционирования:
- C l 2 0 + H 2 O → H C l - 1 + H C l + 1 O ;
- 3 S 0 + 6 N a O H → 2 N a 2 S - 2 + N a 2 S + 6 O 3 + 3 H 2 O .
Химические свойства благородных газов
- плохо растворяются в воде и вступают в реакции с другими веществами только в специально созданных условиях;
- не горят; вытесняют кислород из воздуха, снижая его содержание до критически низких показателей, приводящих к смерти.
Строение и основные химические свойства сложных веществ
Сложные соединения имеют ионную или ковалентную связь между атомами.
- оснóвные + кислоты → соли: C a O + 2 H C l → C a C l 2 + H 2 O ;
- кислотные + основания → соли: S O 3 + 2 N a O H → N a 2 S O 4 + H 2 O ;
- амфотерные реагируют и с кислотами, и с основаниями → соли:
Z n O + H 2 S O 4 → Z n S O 4 + H 2 О ,
Z n O + 2 N a O H + H 2 O → N a 2 [ Z n ( O H ) 4 ] .
Все основания реагируют с кислотами (реакция нейтрализации):
- K O H + 2 H C l → K C l + H 2 O ;
- 2 F e ( O H ) 3 + 3 H 2 S O 4 → F e 2 ( S O 4 ) 3 + 6 H 2 O .
1. Щелочи взаимодействуют с:
- неметаллами: 6 K O H + 3 S → K 2 S O 3 + 2 K 2 S + 3 H 2 O ;
- кислотными оксидами: 2 N a O H + N O 2 → N a N O 2 + N a N O 3 + H 2 O .
2. Нерастворимые основания разлагаются при нагревании: C u ( O H ) 2 → C u O + H 2 O .
- + основания (реакция нейтрализации): 2 F e ( O H ) 3 + 3 H 2 S O 4 → F e 2 ( S O 4 ) 3 + 6 H 2 O ;
- + металлы, стоящие левее водорода в ряду активности: M g + 2 H C l → M g C l 2 + H 2 ↑ ;
- + основные и амфотерные оксиды: C a O + H 2 S O 4 → C a S O 4 + H 2 O ; Z n O + H 2 S O 4 → Z n S O 4 + H 2 O ;
- + соли: B a C l 2 + H 2 S O 4 → B a S O 4 + 2 H C l .
- + кислоты (сильные): N a 2 S i O 3 + 2 H C l → H 2 S i O 3 ↓ + 2 N a C l ;
- + щёлочи, если образуется нерастворимое основание: F e C l 3 + 3 N a O H → F e ( O H ) 3 ↓ + 3 N a C l ;
- + металлы: Z n + P b ( N O 3 ) 2 → P b ↓ + Z n ( N O 3 ) 2 ;
- + соли при условии необратимости реакции: N a 2 C O 3 + C a ( N O 3 ) 2 → C a C O 3 ↓ + 2 N a N O 3 .
Также о химических свойствах неорганических соединений можно почитать в статье «Классы неорганических соединений».
Технологическая карта урока химии на тему "Простые и сложные вещества. Металлы и неметаллы" (8 класс)

хлор
Этот газ с резким специфическим запахом, тяжелее воздуха,
при испарении стелется над землей в виде тумана, может проникать в нижние этажи и подвалы зданий.
Пары сильно раздражают органы дыхания,
глаза, кожу.
При вдыхании высоких концентраций возможен смертельный исход

Поваренная соль
Она жизненно необходима для жизнедеятельности человека, равно как всех прочих живых существ


ПРОБЛЕМНЫЙ ВОПРОС
Как не запутаться
в многообразии веществ?

Классификация веществ
Вещества
Простые
состоят из атомов одного химического элемента
Сложные
состоят из атомов разных химических элементов

1. Немолекулярное строение ,
2. Твердые вещества (искл. Hg),
3. Цвет – от серебристо-белого до темно-серого,
4. Непрозрачны,
5. Характерен металлический блеск,
6. Пластичны , наиболее - Au, Ag, Cu, Al,
7. Твердость различна: мягкие – натрий, золото, твердые – хром, титан,
8. Температуры плавления изменяются в широком интервале.
1. Молекулярное и немолекулярное строение,
2. Агрегатное состояние различно,
3. Цвет разнообразный. Сера – желтая, бром – красно-коричневый,
4. Прозрачные и непрозрачные,
5. Металлический блеск нехарактерен,
6. Диэлектрики (искл. – графит, кремний),
7. Хрупкие,
8. Температуры плавления изменяются в широком интервале.

Вопросы для закрепления:
На какие группы делятся вещества по
составу?
Какие вещества называются простыми?
Какие вещества называются сложными?
На какие группы делятся простые вещества?
Какими физическими свойствами обладают металлы?
Какие свойства характерны для неметаллов?
Чем отличаются химические соединения от смесей?

«Можно не любить химию,
но прожить без неё сегодня и завтра нельзя»
О.М. Нефёдов
(российский химик, академик РАН)
Выбранный для просмотра документ Технологическая карта урока.doc
Технологическая карта урока
Простые и сложные вещества. Металлы и неметаллы
сформировать понятие о простых и сложных веществах; познакомить с делением простых веществ на металлы и неметаллы, научить определять металлы и неметаллы по расположению в Периодической системе; научить различать понятия: «простое вещество» и «химический элемент», «сложное вещество» и «смесь»;
проверить знания символов и названий химических элементов; научить записывать формулы простых и сложных веществ; способствовать формированию положительного отношения к знаниям, воспитание интереса к обучению, формирование межличностных отношений.
Образовательные: раскрыть понятия «простое вещество» и «сложное вещество»; сформировать представление о простых веществах – металлах и неметаллах.
Развивающие: развивать познавательный интерес к химии; создать условия для овладения приемами изучения состава вещества; формировать умение получать, обрабатывать и анализировать информацию; развивать умение логично излагать свою точку зрения.
Воспитательные: формировать умение работать в парах; развивать чувство товарищества и взаимопомощи; воспитывать толерантные отношения в классе.
Личностные УУД: готовность и способность обучающихся к саморазвитию, мотивации к обучению и познанию, самоопределение, ценностно-смысловые установки обучающихся, отражающие их индивидуально-личностные позиции, социальные компетенции, личностные качества;
Регулятивные УУД: целеполагание, самоконтроль, самооценка.
Коммуникативные УУД: обеспечение возможности сотрудничества: умение слышать, слушать и понимать партнера, оказывать поддержку друг другу и эффективно сотрудничать как с учителем, так и со сверстниками, построение речевых высказываний, работа с информацией, построение вопросов .
Познавательные УУД: умение находить и использовать в тексте нужную информацию, умение преобразовывать информацию, строить логичное рассуждение, анализировать и обобщать изученную информацию.
Знать: химические понятия «простое вещество», «сложное вещество», «металлы», «неметаллы», «смеси», «химические соединения».
Уметь: классифицировать вещества по составу (простые и сложные).
Личностные: рефлексия собственной деятельности, установление обучающимися связи между целью учебной деятельности и ее мотивом.
Метапредметные: выбор, принятие и сохранение учебной цели и задачи, умение структурировать знания, умение строить речевое высказывание.
простое вещество, сложное вещество, металл, неметалл.
биология, ОБЖ, информатика, литература
Вещества: цинк в гранулах, алюминий в гранулах, сера, поваренная соль, сахар, аммиачная селитра.
Ф- фронтальная, И – индивидуальная, П – парная
Этапы урока
Формируемые УУД
Деятельность учителя
Деятельность ученика
Организаци-онный
Личностные УУД: самооценка и готовность к уроку.
Метапредметные УУД: учебно-познавательный интерес, организация рабочего места.
Читайте также:
