Сложные вещества образованные атомами металлов и кислотными остатками
Обновлено: 16.05.2024
Основания являются классом неорганических веществ, применяемым в жизни с давних времен за счет ощущения мылкости. Главное отличие этого класса неорганических веществ от остальных - наличие гидроксогруппы, которая придает особые физические и химические свойства.
Основания бывают растворимыми (щелочи) и нерастворимыми. Растворимые основания мылкие на ощупь. Все основания вступают в реакцию нейтрализации - взаимодействие с кислотой. С развитием химии и изучением физических и химических свойств основания расширили круг своего применения: бытовые моющие средства, промышленные чистящие средства, очистка нефти, строительство, краски, удобрения, батарейки. Также стало широко использоваться одно из химических свойств оснований - взаимодействие с кислотами, которое называется реакцией нейтрализацией. Однако основания таят в себе опасность: с растворами щелочей надо работать аккуратно и осторожно, чтобы не получить химических ожогов.
Определение, номенклатура и классификация оснований
Основания – сложные вещества, в состав которых входят атомы металлов, соединенные с одним или несколькими гидроксогруппами (-ОН).
Гидроксид-ион(гидроксогруппа) – сложный ион, состоящий из кислорода и водорода и имеющий суммарный заряд 1- : О -2 Н +1 . Валентность гидроксогруппы равна 1.
Общая формула оснований : М(ОН)n, где М – металл, n- число групп ОН - и в то же время численное значение заряда иона (степени окисления) металла.
Слово «гидроксид» (им.падеж) + название металла (род.падеж) + указание степени окисления, если она переменная, римскими цифрами в скобках
NaOH – гидроксид натрия
Ca(OH)2 – гидроксид кальция
Fe(OH)2 – гидроксид железа (II) (читается «гидроксид железа два»)
Fe(OH)3 – гидроксид железа (III) (читается «гидроксид железа 3»)
Наличие кислорода;Кислородсодержащие;\(KOH, Sr(OH)_<2>\) ;Бескислородные;\(NH_\) как аммиачная вода Кислотность (число групп \(ОН^\) в составе или число присоединяемых \(Н^\));Однокислотные;\(NaOH, TlOH, NH_\) ;Двухкислотные;\(Ca(OH)_<2>, Mg(OH)_<2>\) ;Трёхкислотные;\(La(OH)_, TI(OH)_\) Растворимость в воде;Растворимые (щелочи);\(NaOH, KOH, Ca(OH)_<2>^\), \(Ba(OH)_<2>\) ;Нерастворимые;\(Cr(OH)_<2>, Mn(OH)_<2>\) Степень электролитической диссоциации;Сильные (α→1);\(Щелочи^ LiOH-CsOH\), \(Ca(OH)_<2>-Ra(OH)_<2>\) , \(TlOH\) ;Слабые (α→0);Нерастворимые основания Летучесть;Летучие;\(NH_∙H_<2>O\) ;Нелетучие;Щелочи, нерастворимые основания Стабильность;Стабильные;\(NaOH, Ba(OH)_<2>\) ;Нестабильные;\(NH_∙H_<2>O→ NH_↑+H_<2>O\)
Ca(OH)2 – в таблице растворимости малорастворим (м), но его относят к растворимым основаниям. К малорастворимым веществам относятся вещества, которые растворяются ограниченно – менее 1 г в 100 г воды. Это означает следующее: если в стакан, содержащий 100 г воды, поместить 10 г кристаллического гидроксида кальция, то 1 г вещества растворится, а остальные 9 г – нет. Прозрачная жидкость над осадком будет представлять собой раствор щелочи – гидроксида кальция Ca(OH)2.
Щелочи – растворимые основания. Их образуют элементы-металлы главной подгруппы первой группы (А-группы) периодической системы, а также элементы главной подгруппы второй группы (A-группы): кальций, барий и стронций. Свойства растворимых и нерастворимых оснований существенно различаются.
Получение оснований
Основания получают разными способами. Выбор способа получения зависит от того, к какой группе данное соединение относится, является щёлочью или нерастворимым основанием.
Взаимодействием щелочных и щелочноземельных металлов с водой . Протекает реакция замещения, в ходе которой кроме щёлочи образуется водород. Активные металлы энергично взаимодействуют с водой при обычных условиях.
М + Н2О = Растворимое основание (Щелочь) + Н2↑
Где М – щелочные и щелочноземельные металлы.
Взаимодействием оксидов щелочных и щелочноземельных металлов с водой . При этом протекает реакция соединения. Именно так получают гидроксид кальция в промышленных условиях.
В промышленности гидроксид натрия и калия получают путём электролиза : пропускают постоянный электрический ток через раствор хлорида натрия или калия.
Действием щелочей на растворимые соли металлов.
Раствор щелочи + раствор соли = нерастворимое основание + соль
Свойства основания
Все неорганические основания – твердые вещества (кроме гидроксида аммония NH4OH), которые характеризуются разной растворимостью в воде.
Гидроксиды щелочных металлов при обычных условиях представляют собой твердые белые кристаллические вещества, гигроскопичные, мылкие на ощупь, очень хорошо растворимы в воде (их растворение идет с выделением тепла), легкоплавки.
Гидроксиды щелочноземельных металлов (Ca(OH)2, Ba(OH)2, Sr(OH)2) – белые порошкообразные вещества, гораздо менее растворимые в воде по сравнению с гидроксидами щелочных металлов.
Нерастворимые в воде основания обычно образуются в виде гелеобразных (студенистых) осадков, разлагающихся при хранении.
Нерастворимые в воде основания могут иметь различную окраску, например: гидроксид железа (III) – бурого цвета, гидроксид алюминия - белого цвета, гидроксид меди (II) – голубого цвета.
что такое кислоты ,соли,оксиды,основание? химия.
Кислоты — сложные вещества, которые состоят из атомов водорода, способных замещаться на атомы металлов, и кислотных остатков. Они получили своё название из-за кислого вкуса большинства кислот. В водных растворах они диссоциируют на катион водорода (протон) и анион кислотного остатка.
Соли — класс химических соединений, к которому относятся вещества, состоящие из катионов металла (или катионов аммония NH4+ ; известны соли фосфония PH4+ или гидроксония H3O+) и анионов кислотного остатка.
Оксид — бинарное соединение химического элемента с кислородом в степени окисления −2, в котором сам кислород связан только с менее электроотрицательным элементом. Химический элемент кислород по электроотрицательности второй после фтора, поэтому к оксидам относятся почти все соединения химических элементов с кислородом. К исключениям относятся, например, дифторид кислорода OF2.
Основания — сложные вещества, которые состоят из атомов металла или иона аммония и гидроксогруппы (-OH). В водном растворе диссоциируют с образованием катионов и анионов ОН−. Название основания обычно состоит из двух слов: «гидроксид металла/аммония» . Хорошо растворимые в воде основания называются щелочами.
Согласно другому определению, основания — один из основных классов химических соединений, вещества, молекулы которых являются акцепторами протонов.
Не ну вы серьезно? думаете если скопировали все из вики такие умные? вот кратко
Кислотами называют сложные вещества, молекулы которых состоят из атомов водорода и кислотного остатка.
Соли это сложные вещества, состоящие из ионов металлов и кислотного остатка
основание это сложные вещества, состоящие из ионов металлов и связанных с ними гидроксид ионов.
Оксид это сложные вещества, состоящие из двух химических элементов, один из которых кислород в степени окисления -2
Урок 25. Соли
В уроке 25 «Соли» из курса «Химия для чайников» узнаем, как правильно называть соли, их состав и научимся составлять химические формулы солей.

Как отмечалось в предыдущем уроке, в реакциях кислот с металлами выделяется простое вещество водород Н2. Кроме водорода, образуются и сложные вещества: ZnCl2, MgSO4 и др. Это представители класса широко распространенных в химии соединений — солей (рис. 102).

Здесь же мы рассмотрим состав солей, научимся составлять их формулы, узнаем, как называть соли.
Cостав солей
Сравним формулы кислот HCl и H2SO4 c формулами солей ZnCl2 и FeSO4. Мы видим, что в этих формулах одинаковые кислотные остатки Cl(I) и SO4(II). Но в молекулах кислот они соединены с атомами водорода Н, а в формульных единицах солей — с атомами цинка Zn и железа Fe. Значит, эти и другие соли можно рассматривать как продукты замещения атомов водорода в молекулах кислот на атомы металлов. Вещества, подобные ZnCl2 и FeSO4, относят к классу солей.
Соли — это сложные вещества, состоящие из атомов металлов и кислотных остатков.
В солях кислотные остатки соединяются с атомами металлов в соответствии с их валентностью. Для составления химической формулы соли необходимо знать валентность атома металла и валентность кислотного остатка. При этом пользуются тем же правилом, что и при составлении формул бинарных соединений. Для солей это правило следующее: сумма единиц валентности всех атомов металла должна быть равна сумме единиц валентности всех кислотных остатков.
Для примера составим формулу соли, в которую входят атомы кальция и кислотный остаток фосфорной кислоты PO4(III). Кальций проявляет постоянную валентность II, а валентность кислотного остатка PO4 равна III.

Названия солей
Соли образованы атомами разных металлов и различными кислотными остатками. Поэтому состав солей самый разнообразный. Давайте научимся давать им правильные названия.
Название соли состоит из названия кислотного остатка и названия металла в родительном падеже. Например, соль состава NaCl называют «хлорид натрия».
Если входящий в формульную единицу соли атом металла имеет переменную валентность, то она указывается римской цифрой в круглых скобках после его названия. Так, соль FeCl3 называют «хлорид железа(III)», а cоль FeCl2 — «хлорид железа(II)».
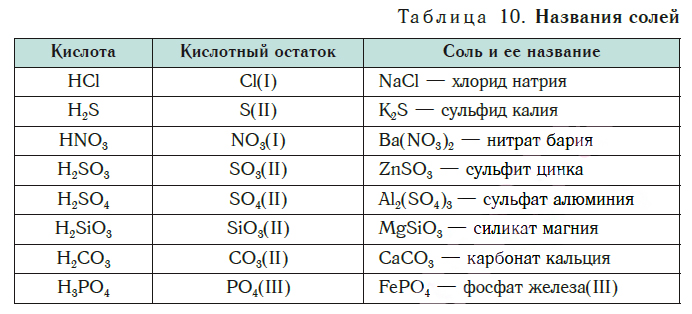
В таблице 10 приведены названия некоторых солей.
Соли — это вещества немолекулярного строения. Поэтому их состав выражают с помощью формульных единиц. В них отражено соотношение атомов металлов и кислотных остатков. Например, в формульной единице NaCl на один атом Na приходится один кислотный остаток Cl.
По химической формуле соли можно вычислить ее относительную формульную массу Mr, а также молярную массу M, например:
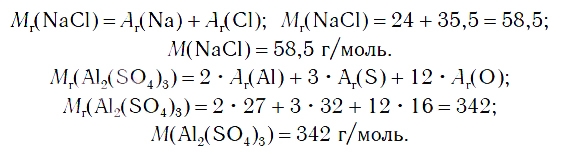
К солям относится не только поваренная соль (NaCl), но и мел, мрамор (СаСО3), сода (Na2CO3), марганцовка (KMnO4) и др.
Краткие выводы урока:
- Соли — сложные вещества, которые состоят из атомов металлов и кислотных остатков.
- Соли образуются при замещении атомов водорода в молекулах кислот на атомы металлов.
- Соли — вещества немолекулярного строения.
Надеюсь урок 25 «Соли» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Урок 23. Понятие о кислотах
В уроке 23 «Понятие о кислотах» из курса «Химия для чайников» познакомимся со сложными веществами — кислотами; узнаем об индикаторах и как они помогают человеку.

В тексте нашего учебника вам уже неоднократно встречалось слово «кислота». Много раз, конечно, вы слышали это слово и в повседневной жизни. При приготовлении пищи используются уксусная и лимонная кислоты, в домашней аптечке есть борная кислота, в аккумуляторы автомашин заливают серную кислоту и т. д. Отметим, что и в быту, и в производственной деятельности людей используются в основном водные растворы кислот. Познакомимся поближе с этими веществами.
Состав кислот
В большинстве случаев в состав молекул кислот входят только атомы неметаллов. На рисунке 97 представлены шаровые модели молекул некоторых кислот и их формулы. Что общего у этих молекул? Ответ прост — в них входят атомы водорода.
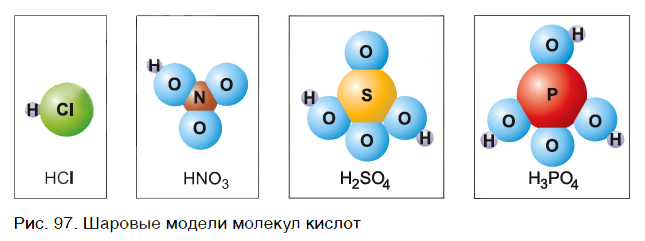
Обратим внимание, что в состав молекулы хлороводорода, кроме атома водорода Н, входит атом хлора Cl, молекулы азотной кислоты — группа атомов NO3, молекулы серной кислоты — SO4, молекулы фосфорной кислоты — PO4.
Атом Cl, группы атомов NO3, SO4, PO4, а также другие атомы и группы атомов в составе кислот называют кислотными остатками.
Кислоты — сложные вещества, в состав которых входят атомы водорода, способные замещаться атомами металлов, и кислотные остатки.
Кислотные остатки в молекулах кислот соединены с атомами водорода в соответствии со своей валентностью. Как можно ее определить? Водород всегда одновалентен. Значит, если кислотный остаток в молекуле кислоты соединен с одним атомом водорода, то его валентность равна единице, если с двумя атомами — двум, а с тремя — трем.
При написании формул кислот сначала пишут атомы водорода, а потом кислотные остатки.
В таблице 8 представлены названия и формулы кислот, с которыми вы будете встречаться при изучении основ химии. Здесь же даны формулы кислотных остатков, которые входят в состав этих кислот, их валентность и названия.
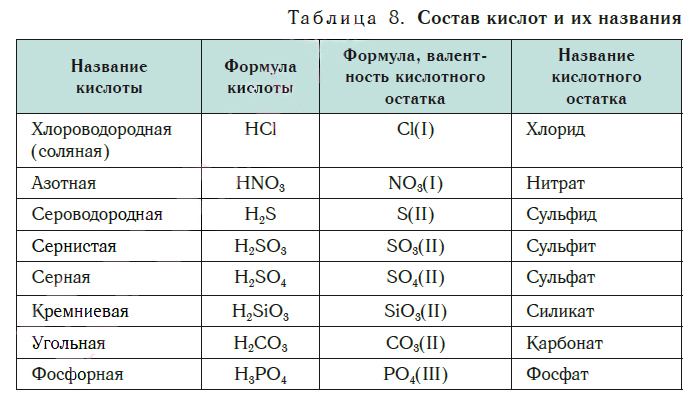
При обычных условиях кислоты существуют в жидком и твердом агрегатных состояниях. Так, фосфорная кислота H3PO4 при комнатной температуре — твердое вещество. При этих же условиях серная кислота H2SO4 — это не имеющая запаха вязкая жидкость. Она почти в 2 раза тяжелее воды. Хлороводородная кислота HCl — раствор газа хлороводорода в воде. Она имеет еще и историческое название «соляная кислота». Раствор этой кислоты имеет характерный запах.
В большинстве случаев кислоты растворяются в воде. Исключение — кремниевая кислота H2SiO3. Водные растворы хлороводородной, серной и фосфорной кислот не имеют окраски. Безводная азотная кислота при хранении желтеет.
Поскольку в состав всех кислот входят атомы водорода, то кислоты обладают общими свойствами: 1) изменяют окраску некоторых органических веществ; 2) имеют кислый вкус (пробовать кислоты на вкус, как и любые другие вещества, запрещается — можно получить ожог полости рта!); 3) оказывают разъедающее действие на кожу человека, ткани, бумагу, древесину и другие материалы.
Есть вещества, которые, как и кислоты, содержат атомы водорода, но кислотными свойствами не обладают, например метан CH4, аммиак NH3, вода H2O и др. Следовательно, не все вещества, содержащие атомы водорода, относят к кислотам.
Меры предосторожности при работе с кислотами
Кислоты — едкие вещества. Попадание кислот на кожу или в глаза может привести к болезненным химическим ожогам. Обращаться с кислотами нужно очень осторожно. При работе с ними следует надевать специальные халаты, перчатки, очки. При попадании кислоты на кожу или в глаза ее необ ходимо немедленно смыть большим количеством воды, а затем пораженный участок промыть раствором питьевой соды. В случае необходимости следует обратиться в медпункт.
Понятие об индикаторах
Некоторые органические вещества изменяют свою окраску в присутствии кислот и ряда других веществ. Такие вещества называют индикаторами, что в переводе с латинского означает «указатель».
Индикаторы — это органические вещества, которые изменяют свою окраску в присутствии кислот и ряда других веществ.
На уроках химии для обнаружения в растворах кислот используют индикаторы лакмус, метиловый оранжевый (метилоранж), а также универсальный индикатор. Это полоска фильтровальной бумаги, пропитанная смесью индикаторов. Окраска индикаторов в воде показана на рисунке 98. Индикаторы изменяют свой цвет, если в растворе есть кислоты (рис. 99).

На заметку: В растворах кислот изменяют цвет сок краснокочанной капусты, вишни, черноплодной рябины, цветки фиалки и др.
- В состав кислот входят атомы водорода и кислотные остатки.
- Индикаторы — органические вещества, изменяющие свою окраску в присутствии кислот и ряда других веществ.
Надеюсь урок 23 «Понятие о кислотах» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Читайте также:
