Соединение кремния с металлами
Обновлено: 05.10.2024
Оксид кремния (IV) является твердым веществом с атомной кристаллической решеткой.
Оксид кремния (IV) или диоксид можно встретить в природе в виде следующих минералов:
- кварц;
- речной песок;
- кремнезем;
- прочие модификации.
+ 14 S i 1 s 2 2 s 2 2 p 6 3 s 2 3 p 2
+ 14 S i * 1 s 2 2 s 2 2 p 6 3 s 1 3 p 3
Физические свойства кремния:
- твердое, тугоплавкое вещество;
- плавится при температуре 1728 °C;
- температура кипения равна 2590 °C;
- атомная кристаллическая решетка.
Оксид кремния относят к типичным кислотным оксидам. Окислительные свойства вещества проявляются в слабой степени.
Будучи кислотным оксидом, диоксид кремния (IV) вступает в химические реакции с растворами и расплавами щелочей, с расплавами основных оксидов. В результате взаимодействия образуются силикаты.
Взаимодействие диоксида кремния и гидроксида калия:
S i O 2 + 2 K O H → K 2 S i O 3 3 + H 2 O
Реакция диоксида кремния с оксидом кальция:
S i O 2 + C a O → C a S i O 3
Оксид кремния (IV) не вступает в химическую реакцию с водой. Это объясняется нерастворимостью кремниевой кислоты.
Оксид кремния (IV) взаимодействует в процессе сплавления с карбонатами щелочных металлов. Данный процесс протекает по правилу, согласно которому при сплавлении происходит вытеснение более летучего оксида (оксида углерода (IV)) из солей менее летучим оксидом (оксидом кремния (IV)).
Взаимодействие оксида кремния (IV) и карбоната калия сопровождается образованием силиката калия и углекислого газа (оксида углерода IV):
S i O 2 + K 2 C O 3 → K 2 S i O 3 + C O 2
Если рассматривать кислоты, то возможна реакция диоксида кремния только с плавиковой кислотой или фтороводородом в газообразном состоянии.
В качестве примера можно записать уравнение реакции:
S i O 2 + 6 H F ( г ) = S i F 4 + H 2 O
S i O 2 + 6 H F ( р - р ) → H 2 [ S i F 6 ] + 2 H 2 O
В условиях нагрева до 1000 °C протекает реакция оксида кремния с активными металлами, что сопровождается образованием кремния.
Взаимодействие оксида кремния и магния приводит к образованию кремния и оксида магния:
S i O 2 + 2 M g → S i + 2 M g O
Если восстановитель имеется в избытке, то реакция приведет к образованию силицидов:
S i O 2 + 4 M g → M g 2 S i + 2 M g O
Оксид кремния (IV) взаимодействует с неметаллами.
Реакция оксида кремния (IV) и водорода в жестких условиях сопровождается проявлением окислительных свойств со стороны оксида кремния:
S i O 2 + 2 Н 2 → S i + 2 Н 2 O
Взаимодействие оксида кремния с углеродом с образованием карборунда и угарного газа:
S i O 2 + 3 С → S i С + 2 С О
В процессе сплавления оксид кремния вступает в химическую реакцию с фосфатом кальция и углем (эта реакция используется в промышленном процессе получения фосфора):
3 S i O 2 + C a 3 ( P O 4 ) 2 + 5 C → 3 C a S i O 3 + 5 C O + 2 P
Получение и применение
Диоксид кремния широко распространен в земной коре, поэтому в промышленности в качестве его источника используют природные минералы.
Для получения аморфного кремния в лабораторных условиях прокаливают смесь из металлического магния и диоксида кремния. Перед постановкой опыта диоксид кремния тщательно измельчают. Когда смесь нагревается, начинает протекать активная химическая реакция. В результате образуется аморфный кремний как один из продуктов этого процесса.
Впервые кремний в свободном состоянии получил Я. Берцелиус в 1822 году. Латинское слово «силиций» является производным от латинского понятия «sileх», значение которого — «кремень».
Еще одним методом синтеза кремния в лабораторных условиях является восстановление с помощью алюминия.
3 S i O 2 + 4 A l → 3 S i + 2 A l 2 O 3
Перечисленные способы получения кремния не являются эффективными в промышленных масштабах. Это связано с высокой ценой на алюминий и магний. По этой причине были разработаны другие способы синтеза вещества.
Вещество восстанавливают из оксида коксом, используя электрические печи. В результате получают кремний, насыщенный примесями карбидов кремния. Данный материал имеет ограниченные сферы применения. К примеру, такой продукт не подходит для производства микросхем.
S i O 2 + 2 C → S i + 2 C O
Получить более чистый материал можно с помощью восстановления тетрахлорида кремния цинком или водородом при нагревании до 1200 °C.
Кремний. Химия кремния и его соединений

Кремний расположен в главной подгруппе IV группы (или в 14 группе в современной форме ПСХЭ) и в третьем периоде периодической системы химических элементов Д.И. Менделеева.
Электронное строение кремния
Электронная конфигурация кремния в основном состоянии :

+14Si 1s 2 2s 2 2p 6 3s 2 3p 2
Электронная конфигурация кремния в возбужденном состоянии :

+14Si * 1s 2 2s 2 2p 6 3s 1 3p 3
Атом кремния содержит на внешнем энергетическом уровне 2 неспаренных электрона и 1 неподеленную электронную пару в основном энергетическом состоянии и 4 неспаренных электрона в возбужденном энергетическом состоянии.
Степени окисления атома кремния — от -4 до +4. Характерные степени окисления -4, 0, +2, +4.
Физические свойства, способы получения и нахождение в природе кремния
Кремний — второй по распространенности элемент на Земле после кислорода. Встречается только в виде соединений. Оксид кремния SiO2 образует большое количество природных веществ – горный хрусталь, кварц, кремнезем.

Простое вещество кремний – атомный кристалл темно-серого цвета с металлическим блеском, довольно хрупок. Температура плавления 1415 °C, плотность 2,33 г/см 3 . Полупроводник.
Качественные реакции
Качественная реакция на силикат-ионы SiO3 2- — взаимодействие солей-силикатов с сильными кислотами . Кремниевая кислота – слабая. Она легко выделяется из растворов солей кремниевой кислоты при действии на них более сильными кислотами.
Например , если к раствору силиката натрия прилить сильно разбавленный раствор соляной кислоты, то кремниевая кислота выделится не в виде осадка, а в виде геля. Раствор помутнеет и «застынет».
Na2SiO3 + 2HCl = H2SiO3 + 2 NaCl

Видеоопыт взаимодействия силиката натрия с соляной кислоты (получение кремниевой кислоты) можно посмотреть здесь.
Соединения кремния
Основные степени окисления кремния +4, 0 и -4.
Наиболее типичные соединения кремния:
Способы получения кремния
В свободном состоянии кремний был получен Берцелиусом в 1822 г. Его латинское название «силиций» произошло от латинского слова « sile х», что означает «кремень». Аморфный кремний в лаборатории можно получить при прокаливании смеси металлического магния с диоксидом кремния. Для опыта диоксид кремния следует тщательно измельчить. При нагревании смеси начинается бурная реакция. Одним из продуктов этой реакции является аморфный кремний.
SiO2 + 2Mg → Si + 2MgO
Видеоопыт взаимодействия оксида кремния (IV) с магнием можно посмотреть здесь.
Еще один способ получения кремния в лаборатории — восстановление из оксида алюминием:
В промышленности использовать дорогие алюминий и магний неэффективно, поэтому используют другие, более дешевые способы:
1. Восстановление из оксида коксом в электрических печах:
SiO2 + 2C → Si + 2CO
Однако в таком процессе образующийся кремний загрязнен примесями карбидов кремния, и для производства, например, микросхем уже не подходит.
2. Наиболее чистый кремний получают восстановлением тетрахлорида кремния водородом при 1200 °С:
SiCl4 +2H2 → Si + 4HCl
или цинком :
SiCl4 + 2Zn → Si + 2ZnCl2
3. Также чистый кремний получается при разложении силана :
Химические свойства
При нормальных условиях кремний существует в виде атомного кристалла, поэтому химическая активность кремния крайне невысокая.
1. Кремний проявляет свойства окислителя (при взаимодействии с элементами, которые расположены ниже и левее в Периодической системе) и свойства восстановителя (при взаимодействии с элементами, расположенными выше и правее). Поэтому кремний реагирует и с металлами , и с неметаллами .
1.1. При обычных условиях кремний реагирует с фтором с образованием фторида кремния (IV):
При нагревании кремний реагирует с хлором, бромом, йодом :
1.2. При сильном нагревании (около 2000 о С) кремний реагирует с углеродом с образованием бинарного соединения карбида кремния (карборунда):
C + Si → SiC
При температуре выше 600°С взаимодействует с серой:
Si + 2S → SiS2
1.3. Кремний не взаимодействует с водородом .
1.4. С азотом кремний реагирует в очень жестких условиях:
1.5. В реакциях с активными металлами кремний проявляет свойства окислителя. При этом образуются силициды:
2Ca + Si → Ca2Si
Si + 2Mg → Mg2Si
1.6. При нагревании выше 400°С кремний взаимодействует с кислородом :
2. Кремний взаимодействует со сложными веществами:
2.1. В водных растворах щелочей кремний растворяется с образованием солей кремниевой кислоты. При этом щелочь окисляет кремний.
2.2. Кремний не взаимодействует с водными растворами кислот , но аморфный кремний растворяется в плавиковой кислоте с образованием гексафторкремниевой кислоты :
При обработке кремния безводным фтороводородом комплекс не образуется:
С хлороводородом кремний реагирует при 300 °С, с бромоводородом – при 500 °С.
2.3. Кремний растворяется в смеси концентрированных азотной и плавиковой кислот :
3Si + 4HNO3 + 12HF → 3SiF4 + 4NO + 8H2O
Бинарные соединения кремния
Силициды металлов
Силициды – это бинарные соединения кремния с металлами, в которых кремний имеет степень окисления -4. Химическая связь в силицидах металлов — ионная.
Силициды, как правило, легко гидролизуются в воде или в кислой среде.
Например , силицид магния разлагается водой на гидроксид магния и силан:
Соляная кислота легко разлагает силицид магния:
Получают силициды сплавлением простых веществ или восстановлением смеси оксидов коксом в электропечах:
2Mg + Si → Mg 2 Si
2MgO + SiO2 + 4C → Mg2Si + 4CO
Силан
Силан – это бинарное соединение кремния с водородом SiH4, ядовитый бесцветный газ.
Если поместить порошок силицида магния в очень слабый раствор соляной кислоты, то на поверхности раствора образуются пузырьки газа. Они лопаются и загораются на воздухе. Это горит силан. Он образуется при взаимодействии кислоты с силицидом магния:

Видеоопыт получения силана из силицида магния можно посмотреть здесь.
На воздухе силан горит с образованием SiO2 и H2O:
Видеоопыт сгорания силана можно посмотреть здесь.
Силан разлагается водой разлагается с выделением водорода:
Силан разлагается (окисляется) щелочами :
Силан при нагревании разлагается :
Карбид кремния
В соединениях кремния с неметаллами — ковалентная связь.
Рассмотрим карбид кремния – карборунд Si +4 C -4 . Это вещество с атомной кристаллической решеткой. Он имеет структуру, подобную структуре алмаза и характеризуется высокой твердостью и температурой плавления, а также высокой химической устойчивостью.
Карборунд окисляется кислородом при высокой температуре:
Карборунд окисляется кислородом в расплаве щелочи :
Галогениды кремния
Хлорид и фторид кремния – галогенангидриды кремниевой кислоты.
SiCl4.
Получают галогениды кремния действием хлора на сплав оксида кремния с углем :
Галогениды кремния разлагаются водой до кремниевой кислоты и хлороводорода:
Хлорид кремния (IV) восстанавливается водородом :
SiCl4 + 2H2 → Si + 4HCl
Оксид кремния (IV)
Физические свойства и нахождение в природе
Оксид кремния (IV) – это твердое вещество с атомной кристаллической решеткой. В природе встречается в виде кварца, речного песка, кремнезема и прочих модификаций:

Химические свойства
Оксид кремния (IV) – типичный кислотный оксид . За счет кремния со степенью окисления +4 проявляет слабые окислительные свойства.
1. Как кислотный оксид, диоксид кремния (IV) взаимодействует с растворами и расплавами щелочей и в расплаве с основными оксидами . При этом образуются силикаты.
Например , диоксид кремния взаимодействует с гидроксидом калия:
Еще пример : диоксид кремния взаимодействует с оксидом кальция.
SiO2 + CaO → CaSiO3
2. Оксид кремния (IV) не взаимодействует с водой , т.к. кремниевая кислота нерастворима .
3. Оксид кремния (IV) реагирует при сплавлении с карбонатами щелочных металлов . При этом работает правило: менее летучий оксид вытесняет более летучий оксид из солей при сплавлении.
Например , оксид кремния (IV) взаимодействует с карбонатом калия. При этом образуется силикат калия и углекислый газ:
4. Из кислот диоксид кремния реагирует только с плавиковой или с газообразным фтороводородом :
5. При температуре выше 1000 °С оксид кремния реагирует с активными металлами, при этом образуется кремний.
Например , оксид кремния взаимодействует с магнием с образованием кремния и оксида магния:
SiO2 + 2Mg → Si + 2MgO
При избытке восстановителя образуются силициды:
SiO2 + 4Mg → Mg2Si + 2MgO
6. Оксид кремния (IV) взаимодействует с неметаллами.
Например , оксид кремния (IV) реагирует с водородом в жестких условиях. При этом оксид кремния проявляет окислительные свойства:
Еще пример : оксид кремния взаимодействует с углеродом. При этом образуется карборунд и угарный газ:
SiO2 + 3С → SiС + 2СО
При сплавлении оксид кремния взаимодействует с фосфатом кальция и углем:
Кремниевая кислота
Строение молекулы и физические свойства
Кремниевые кислоты — очень слабые, малорастворимые в воде соединения общей формулы nSiO2•mH2O. Образует коллоидный раствор в воде.
Метакремниевая H2SiO3 существует в растворе в виде полимера:

Способы получения
Кремниевая кислота образуется при действии сильных кисло т на растворимые силикаты (силикаты щелочных металлов).
Например , при действии соляной кислоты на силикат натрия:
Na 2 SiO 3 + 2 HCl → H 2 SiO 3 + 2 NaCl
Видеоопыт получения кремниевой кислоты из силиката натрия можно посмотреть здесь.
Даже слабая угольная кислота вытесняет кремниевую кислоту из солей:
1. Кремниевая кислота — нерастворимая. Кислотные свойства выражены очень слабо, поэтому кислота реагирует только с сильными основаниями и их оксидами :
Например , кремниевая кислота реагирует с концентрированным гидроксидом калия:
2. При нагревании кремниевая кислота разлагается на оксид и воду :
Силикаты
Силикаты — это соли кремниевой кислоты. Большинство силикатов нерастворимо в воде, кроме силикатов натрия и калия, их называют «жидким стеклом».
Способы получения силикатов:
1 . Растворение кремния, кремниевой кислоты или оксида в щелочи:
2. Сплавление с основными оксидами:
СаО + SiO2 → CaSiO3
3. Взаимодействие растворимых силикатов с солями:
Оконное стекло (натриевое стекло) — силикат натрия и кальция: Na2O·CaO·6SiO2.
Стекло получают при сплавлении в специальных печах смеси соды Na2CO3, известняка CaCO3 и белого песка SiO2:
Для получения специального стекла вводят различные добавки, так стекло содержащее ионы Pb 2+ – хрусталь; Cr 3+ – имеет зеленую окраску, Fe 3+ – коричневое бутылочное стекло, Co 2+ – дает синий цвет, Mn 2+ – красновато-лиловый.
В большинстве реакций Si выступает в роли восстановителя:
При низких температурах кремний химически инертен, при нагревании его реакционная способность резко возрастает.
1. С кислородом взаимодействует при Т выше 400°С:
Si + О2 = SiO2 оксид кремния
2. С фтором реагирует уже при комнатной температуре:
Si + 2F2 = SiF4 тетрафторид кремня
3. С остальными галогенами реакции идут при температуре = 300 - 500°С
4. С парами серы при 600°С образует дисульфид:
5. Реакция с азотом происходит выше 1000°С:
6. При температуре = 1150°С реагирует с углеродом:
SiO2 + 3С = SiС + 2СО
По твердости карборунд близок к алмазу.
7. С водородом кремний непосредственно не реагирует.
8. Кремний стоек к действию кислот. Взаимодействует только со смесью азотной и фтороводородной (плавиковой) кислот:
9. реагирует с растворами щелочей с образованием силикатов и выделением водорода:
10. Восстановительные свойства кремния используют для выделения металлов из их оксидов:
2MgO = Si = 2Mg + SiO2
В реакциях с металлами Si - окислитель:
Кремний образует силициды с s-металлами и большинством d-металлов.
Состав силицидов данного металла может быть различен. (Например, FeSi и FeSi2; Ni2Si и NiSi2.) Один из наиболее известных силицидов - силицид магния, который можно получать прямым взаимодействием простых веществ:
Силан (моносилан) SiH4
Силаны (кремневодороды) SinH2n + 2, (ср. с алканами), где п = 1-8. Силаны - аналоги алканов, отличаются от них неустойчивостью цепей -Si-Si-.
Моносилан SiH4 - бесцветный газ с неприятным запахом; растворяется в этаноле, бензине.
1. Разложение силицида магния соляной кислотой: Mg2Si + 4HCI = 2MgCI2 + SiH4
2. Восстановление галогенидов Si алюмогидридом лития: SiCl4 + LiAlH4 = SiH4↑ + LiCl + AlCl3
Силан - сильный восстановитель.
1.SiH4 окисляется кислородом даже при очень низких температурах:
2. SiH4 легко гидролизуется, особенно в щелочной среде:
Оксид кремния (IV) (кремнезем) SiO2
Кремнезем существует в виде различных форм: кристаллической, аморфной и стеклообразной. Наиболее распространенной кристаллической формой является кварц. При разрушении кварцевых горных пород образуются кварцевые пески. Монокристаллы кварца - прозрачны, бесцветны (горный хрусталь) или окрашены примесями в различные цвета (аметист, агат, яшма и др.).
Аморфный SiO2 встречается в виде минерала опала: искусственно получают силикагель, состоящий из коллоидных частиц SiO2 и являющийся очень хорошим адсорбентом. Стеклообразный SiO2 известен как кварцевое стекло.
Физические свойства
В воде SiO2 растворяется очень незначительно, в органических растворителях также практически не растворяется. Кремнезем является диэлектриком.
Химические свойства
1. SiO2 - кислотный оксид, поэтому аморфный кремнезем медленно растворяется в водных растворах щелочей:
2. SiO2 взаимодействует также при нагревании с основными оксидами:
3. Будучи нелетучим оксидом, SiO2 вытесняет углекислый газ из Na2CO3 (при сплавлении):
4. Кремнезем реагирует с фтороводородной кислотой, образуя кремнефтористоводородную кислоту H2SiF6:
5. При 250 - 400°С SiO2 взаимодействует с газообразным HF и F2, образуя тетрафторсилан (тетрафторид кремния):
Кремниевые кислоты
- ортокремниевая кислота H4SiО4;
- метакремниевая (кремниевая) кислота H2SiO3;
- ди- и поликремниевые кислоты.
Все кремниевые кислоты малорастворимы в воде, легко образуют коллоидные растворы.
Способы по-лучения
1. Осаждение кислотами из растворов силикатов щелочных металлов:
2. Гидролиз хлорсиланов: SiCl4 + 4Н2О = H4SiO4 + 4HCl
Кремниевые кислоты - очень слабые кислоты (слабее угольной кислоты).
При нагревании они дегидратируются с образованием в качестве конечного продукта кремнезема
Силикаты - соли кремниевых кислот
Поскольку кремниевые кислоты чрезвычайно слабые, их соли в водных растворах сильно гидро лизованы:
SiO3 2- + Н2О = HSiO3 - + ОН - (щелочная среда)
По этой же причине при пропускании углекислого газа через растворы силикатов происходит вытеснение из них кремниевой кислоты:
Данную реакцию можно рассматривать как качественную реакцию на силикат-ионы.
Среди силикатов хорошо растворимыми являются только Na2SiO3 и K2SiO3, которые называются растворимым стеклом, а их водные растворы - жидким стеклом.
Стекло
Обычное оконное стекло имеет состав Na2O • СаО • 6SiO2, т. е. является смесью силикатов натрия и кальция. Его получают сплавлением соды Na2CO3, известняка СаСO3 и песка SiO2;
Цемент
Порошкообразный вяжущий материал, образующий при взаимодействии с водой пластичную массу, превращающуюся со временем в твердое камневидное тело; основной строительный материал.
Химический состав наиболее распространенного портланд-цемента (в % по массе) - 20 - 23% SiO2; 62 - 76 % СаО; 4 - 7 % Al2O3; 2-5% Fe2O3; 1- 5% МgО.
Кремний
Кремний - неметаллический элемент IVa группы периодической таблицы Д.И. Менделеева. Второй после кислорода элемент по распространенности в земной коре.
В чистом виде в природе практически отсутствует. Чаще всего встречается в виде кремнезема - SiO2 - песок, песчаник, кварц, глина.

Кремниевая (силиконовая) долина
Регион в штате Калифорния (США), отличающийся большой плотностью высоко технологичных компаний, связанных с производством компьютеров и микропроцессоров.
Кремний является природным полупроводником, используется как основной материал для производства микросхем. Кремний ближе, чем вы думаете: внутри гаджета, которым вы пользуетесь ;)

Основное и возбужденное состояние кремния
При возбуждении атома кремния электроны на s-подуровне распариваются и один из них переходит на p-подуровень.
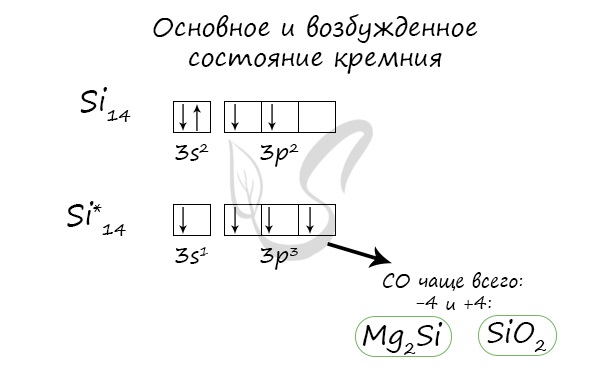
Природные соединения
- SiO2 - кварц, кремнезем, гранит, песчаник, песок, глина
- SiO2 с примесью Fe 3+ - цитрин
- SiO2 с примесью Fe 2+ и Fe 3+ - аметист

Получение
В промышленности кремний получают путем восстановления кремнезема в электрических печах, алюминотермией.
В лабораторных условиях мелкий белый песок прокаливают с магнием:
SiO2 + Mg → (t) MgO + Si
Химические свойства
При обычных условиях без нагревания кремний реагирует только со фтором.
При нагревании кремний вступает в реакции с остальными галогенами (Cl, Br, I), углеродом, кислородом. При очень высоких температурах (1200 °C) кремний с кислородом образует оксид кремния II - несолеобразующий оксид.
Si + O2 → (t = 1200 °C) SiO

В подобных реакциях кремния проявляет свои окислительные способности.
Ca + Si → Ca2Si (силицид кальция)
С целью травления (удаления поверхностного слоя материала) кремниевые изделия можно погружать в раствор щелочи.
Оксид кремния IV - SiO2
Оксид кремния IV имеет атомное строение, обладает высокой прочностью и твердостью. Плавится при температуре +1730 °C градусов.
В промышленности оксид кремния IV получают нагреванием кремния в атмосфере кислорода.
В лабораторных условиях проводят реакция силиката натрия с уксусной кислотой. Кремниевая кислота сразу же распадается на SiO2, который выпадает в осадок, и воду.

- Реакции с кислотами
Химически SiO2 устойчив к действию кислот, однако вступает в реакцию с газообразным фтороводородом (газом) и плавиковой кислотой (жидкостью).
SiO2 является кислотным оксидом, соответствует кремниевой кислоте. Вступая в реакции с основными оксидами и щелочами, образует соли данной кислоты - силикаты.

Так как чаще всего кислотные оксиды с солями не реагируют, тем более необычной кажется реакция оксида кремния IV с карбонатами.
Кремниевая кислота
Слабая, малорастворимая в воде кислота. Ее соли носят название - силикаты.
Поскольку кремниевая кислота малорастворима, то банальной реакцией SiO2 с водой ее не получить. Эту задачу решают в две стадии через ее соли - силикаты.
Кремниевая кислота слабая, нестойкая, легко распадается на воду и оксид кремния IV.

Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Основные сведения о кремнии и его соединениях
Кремний в химии имеет обозначение Si (силициум) от латинского слова silex «кремень». Это типичный неметалл, элемент 14 группы (по прежней классификации — главной подгруппы IV группы) и третьего периода периодической системы Д.И. Менделеева. Атомный номер 14. Атомная масса 28,09.
Рисунок 1. Структура кремния и его внешний вид.
Физические свойства кремния. Аллотропные модификации кремния
Кремний имеет две аллотропные модификации:
- Кристаллический — свойства обусловлены наличием кубической кристаллической решетки. Атомы расположены на вершине и в центре каждой грани, прочно связаны друг с другом ковалентной связью.
- Аморфный — порошок бурого цвета на основе разупорядоченной кристаллической структуры. Гигроскопичный, активнее вступает в реакции.
Таблица 1. Основные физические параметры кристаллического кремния.
Химические свойства Si
Определяются положением кремния в периодической системе Д.И. Менделеева и строением атома: электронная формула 1s2 2s2 2p6 3s2 3p2. Проявляет степени окисления: -4, 0, +2, +4. Валентность: II и IV.
Окислительные свойства кремний проявляет в реакциях с активными металлами:
S i + 2 M g → t ° M g 2 S i - 4 силицид магния;
С водородом не реагирует, но при растворении силицидов в кислотах образуется силан:
M g 2 S i + 4 H C l → 2 M g C l 2 + S i H 4 силан.
Восстановительные свойства кремния.
- +галогены (Cl, Br, J) при нагревании, со фтором при комнатной температуре:
S i + 2 F 2 → S i F 4 тетрафторид кремния;
- при избытке кислорода: S i + O 2 → 600 ° С S i O 2 оксид кремния IV;
- при недостатке кислорода: 2 S i + O 2 → 400 ° С 2 S i O монооксид кремния;
- образование бинарных соединений:
- +сера: S i + S → 600 ° С S i S 2 сульфид кремния;
- +азот: 3 S i + 2 N 2 → 1300 ° С S i 3 N 4 нитрид кремния;
- +углерод: S i + C → 2000 ° С S i C карбид кремния (карборунд);
- +щелочи при кипячении:
- S i + 4 N a O H к о н ц → t ° N a 4 S i O 4 + 2 H 2 ↑ ;
- S i + 2 K O H + H 2 O → t ° K 2 S i O 3 + 2 H 2 ↑ ;
- с кислотами не реагирует. Растворяется только в смеси плавиковой и азотной кислот:
3 S i + 4 H N O 3 + 18 H F → 3 H 2 [ S i F 6 ] + 4 N O + 8 H 2 O .
Нахождение в природе
Кремний в чистом виде (как самородный минерал) встречается крайне редко. Но, соединяясь с кислородом, он образует S i O 2 — кремнезем, входящий в состав многих минералов: песок, кварц, полевой шпат, слюда, некоторые поделочные и полудрагоценные камни: яшма, гранат, турмалин и др., что обуславливает высокое (не менее 26%) содержание кремния в земной коре.
Рисунок 2. Оксид кремния IV в природе.
Содержание кремния в морской воде достигает 3 мг/л, поэтому он накапливается в кремниевых губках, диатомовых водорослях, радиоляриях.
Пищевые продукты, содержащие кремний: овес, огурцы, рис, пшеница, лук, семя льна, авокадо и др.
Технология получения
В лабораторных условиях кремний получают:
- прокаливанием белого песка (оксид кремния IV) с металлическим магнием:
2 M g + S i O 2 → t ° S i ↓ + 2 M g O ;
- восстановлением из оксида кремния IV с помощью алюминия:
2 A l + S i O 2 → t ° S i ↓ + A l 2 O 3 .
Промышленные способы получения кремния:
S i O 2 + 2 C к о к с → t ° 2 C O ↑ + S i ↓ .
Однако, такой кремний имеет примеси карбида кремния и не подходит для производства микросхем.
Продукт со степенью чистоты до 99,9% получают:
- восстановлением водородом или цинком из S i C l 4 :
S i C l 4 + 2 H 2 → 1200 ° С S i ↓ + 4 H C l ;
S i H 4 → t ° S i ↓ + 2 H 2 ↑ .
Важные соединения кремния
Оксид кремния (IV) S i O 2 имеет атомное строение, высокий показатель твердости, тугоплавкий (плавится при температуре 1730 °С). Кислотный оксид, соответствует кремниевой кислоте.
- в промышленности — нагреванием кремния в атмосфере кислорода:
S i + O 2 → 600 ° С S i O 2 .
- в лабораториях — взаимодействие силиката натрия с уксусной кислотой. Кремниевая кислота сразу распадается на воду и S i O 2 , который выпадает в осадок:
- N a 2 S i O 3 + C H 3 C O O H → C H 3 C O O N a + H 2 S i O 3 ↓ ;
- H 2 S i O 3 → S i O 2 ↓ + H 2 O .
Химические свойства SiO2:
- не растворяется в кислотах, реагирует только с плавиковой кислотой и газообразным фтороводородом:
- S i O 2 + 6 H F ж и д → Н 2 [ S i F 6 ] + 2 H 2 O ;
- S i O 2 + 4 H F г а з → S i F 4 + 2 H 2 O ;
- при взаимодействии с основными оксидами и щелочами, а также с карбонатами образуются соли кремниевой кислоты — силикаты:
- C a O + S i O 2 → C a S i O 3 силикат кальция;
- 2 К O H + S i O 2 → K 2 S i O 3 силикат калия + H 2 O ;
- N a 2 C O 3 + S i O 2 → N a 2 S i O 3 силикат натрия + C O 2 ↑ .
На реакции с карбонатами основано получение оконного стекла — смесь из соды, известняка и белого песка прокаливают при температуре, равной 1500 °С:
N a 2 C O 3 + C a C O 3 + 6 S i O 2 → t ° N a 2 O · C a O · 6 S i O 2 + 2 C O 2 ↑ .
Кремниевая кислота и ее соли — силикаты.
Кремниевая кислота H 2 S i O 3 — слабая, малорастворимая. Легко распадается на оксид и воду, при подсыхании превращается в студенистое вещество — силикагель. Получают при взаимодействии кислот (в том числе, угольной) с растворимыми силикатами щелочных металлов:
N a 2 S i O 3 + 2 H C l → 2 N a C l + H 2 S i O 3 ↓ .
Кремниевая кислота реагирует только с сильными основаниями и их оксидами, образуя силикаты:
H 2 S i O 3 + L i O H → L i 2 S i O 3 + 2 H 2 O .
Силикаты, кроме N a 2 S i O 3 и K 2 S i O 3 (их называют жидким стеклом), нерастворимы в воде. Получают следующими методами:
- взаимодействие кремния, оксида кремния или кремниевой кислоты с щелочами:
- S i + 2 N a O H + 2 H 2 O → t ° N a 2 S i O 3 силикат натрия + 2 H 2 ↑ ;
- 2 L i O H + S i O 2 → L i 2 S i O 3 силикат лития + H 2 O ;
- 2 K O H + H 2 S i O 3 → K 2 S i O 3 силикат калия + 2 H 2 O ;
- сплавление оксида кремния с основными оксидами:
M g O + S i O 2 → M g S i O 3 с и л и к а т м а г н и я ;
K 2 S i O 3 + C a C l 2 → C a S i O 3 с и л и к а т к а л ь ц и я + 2 K C l .
Силициды — это бинарные соединения кремния с металлами, в которых кремний имеет степень окисления -4. Тип химической связи — ионная.
Получают при сплавлении простых веществ или восстановлением смеси оксидов коксом в электропечах:
- S i + 2 C a → t ° C a 2 S i - 4 силицид кальция;
- 2 M g O + S i O 2 + 4 C → M g 2 S i силицид магния + 4 C O .
Вступают в реакцию:
- с водой (гидролиз): M g 2 S i + 4 H 2 O → 2 M g ( O H ) 2 + S i H 4 ;
- с кислотами: C a 2 S i + 4 H C l → 2 C a C l 2 + S i H 4 .
Силан — это бинарное соединение кремния с водородом S i H 4 , ядовитый бесцветный газ.
Если к порошку силицида магния добавить разбавленную соляную кислоту, то на поверхности раствора образуются пузырьки силана. Они лопаются и загораются на воздухе.
- M g 2 S i + 4 H C l → 2 M g C l 2 + S i H 4 силан;
- S i H 4 + 2 O 2 → S i O 2 + 2 H 2 O — горение силана.
Химические свойства силана:
- + H 2 O : S i H 4 + 2 H 2 O → S i O 2 + 4 H 2 ;
- +щелочи: 2 S i H 4 + 2 N a O H + H 2 O → N a 2 S i O 3 + 4 H ;
- разложение при нагревании: S i H 4 → S i + 2 H 2 .
5. Карборунд SiC имеет атомный тип кристаллической решетки, сходный с алмазной. Твердый, плавится при температуре 2730 °С.
Получают по схеме:
S i + C → 2000 ° С S i C .
- при высокой температуре: S i C + 2 O 2 → t ° S i O 2 + C O 2 ;
- в расплаве щелочи: S i C + 2 O 2 + 4 N a O H → N a 2 S i O 3 + N a 2 C O 3 + 2 H 2 O .
Применение кремния и его соединений — силикатная промышленность.
Кремний используют в металлургии — добавка к стали и другим сплавам; в электронике — изготовление полупроводниковых приборов, радиодеталей и солнечных батарей.
Кремний необходим для поддержания здоровья кожи, волос и ногтей. Кремний участвует в формировании костей, повышает эластичность и прочность кровеносных сосудов, что используется в профилактике сердечно-сосудистых заболеваний.
Диоксид кремния:
- производство стекла, керамики, бетона и кирпича. Из керамики, помимо посуды и декоративных изделий, производят изоляторы для высоковольтных ЛЭП и другие изделия, используемые в технике и строительстве;
- чистый кварц используется в приборостроении;
- производство косметики: как эмульгатор и компонент против слеживания.
Силициды входят в состав жаропрочных и кислотоустойчивых сплавов и высокотемпературных полупроводниковых материалов.
Карбид кремния используют как абразив при затачивании резцов металлорежущих станков и шлифовки драгоценных камней, а также в качестве имитации алмаза в ювелирном деле.
Читайте также:
