Сущность металлического ионного и ковалентного типов связи
Обновлено: 05.10.2024
В чем сущность металлического, ионного и ковалентного типов связи?
Металлическая связь – тип связи атомов в кристаллических веществах, обладающих металлическими свойствами (металлах, металлидах). М. с. обусловлена большой концентрацией в таких кристаллах квазисвободных электронов (электронов проводимости). Отрицательно заряженный электронный газ «связывает» положительно заряженные ионы друг с другом.
Ковалентная связь – один из видов химической связи между двумя атомами, которая осуществляется общей для них электронной парой (по одному электрону от каждого атома).
К. с. существует как в молекулах (в любых агрегатных состояниях), так и между атомами, образующими решетку кристалла. К. с. может связывать одинаковые атомы (в молекулах H2, Cl2, в кристаллах алмаза) или разные (в молекулах воды, в кристаллах карборунда SiC). Почти все виды основных связей в молекулах органических соединений являются ковалентными (С — С, С — Н, С — N и др.). К. с. очень прочны. Этим объясняется малая химическая активность парафиновых углеводородов. Многие неорганические соединения, кристаллы которых имеют атомную решётку, то есть образуются с помощью К. с., являются тугоплавкими, обладают высокой твёрдостью и износостойкостью. К ним принадлежат некоторые карбиды, силициды, бориды, нитриды (в частности, известный боразон BN), нашедшие применение в новой технике.
Ионная связь – электровалентная связь, гетеровалентная связь, один из видов химической связи, в основе которого лежит электростатическое взаимодействие между противоположно заряженными ионами. Такие связи в сравнительно чистом виде образуются в галогенидах щелочных металлов, например KF, так как атомы щелочных металлов имеют по одному слабо удерживаемому электрону (энергия связи примерно 3-5 эв), а атомы галогенов обладают наибольшим сродством к электрону. Но даже в кристаллах (и тем более в молекулах) этих соединений полной передачи электрона от атома металла атому галогена большей частью все же не происходит.
Распространенные прежде представления об образовании в других случаях двух-, трех- или четырехзарядных ионов Ca2+, C2-, B3+, Si4+ не подтвердились, так как химическая связь образуется в таких случаях более сложным путём. Для оценки степени ионности связи пользуются понятием эффективного заряда иона.
Каким способом можно восстановить пластичность холоднокатанных медных лент? Назначьте режим термической обработки и опишите сущность происходящих процессов.
С увеличением степени холодной деформации свойства, характеризующие сопротивление деформации повышаются, а способность к пластической деформации уменьшается. Это явление получило название наклепа.
Рекристаллизационный отжиг используют в промышленности как первоначальную операцию перед холодной обработкой давлением (для придания материалу наибольшей пластичности), как промежуточный процесс между операциями холодного деформирования (для снятия наклепа) и как окончательную (выходную) термическую обработку (для придания полуфабрикату или изделию необходимых свойств).
При нагреве наклепанного металла не восстанавливается старое зерно, а появляется совершенно новое зерно, размеры которого могут существенно отличаться от исходного. Происходит образование новых, равноосных зерен вместо ориентированной волокнистой структуры деформированного металла.
Температура отжига для достижения рекристаллизации по всему объему и сокращения времени процесса превышает температуру порога рекристаллизации. Температура нагрева связана с температурой плавления: ТН ≈ 0,4 Тпл (для чистых металлов).
Для меди: Тн = 0,4 (1083 + 273) – 273 ≈ 270 °С.

Вычертите диаграмму состояния железо – карбид железа, укажите структурные составляющие во всех областях диаграммы, опишите превращения и постройте кривую охлаждения (с применением правила фаз) для сплава, содержащего 0,2% С. Какова структура этого сплава при комнатной температуре и как такой сплав называется?
Первичная кристаллизация сплавов системы железо-углерод начинается по достижении температур, соответствующих линии ABCD (линии ликвидус), и заканчивается при температурах, образующих линию AHJECF (линию солидус).
При кристаллизации сплавов по линии АВ из жидкого раствора выделяются кристаллы твердого раствора углерода в α-железе (δ-раствор). Процесс кристаллизации сплавов с содержанием углерода до 0,1 % заканчивается по линии АН с образованием α (δ)-твердого раствора. На линии HJB протекает перитектическое превращение, в результате которого образуется твердый раствор углерода в γ-железе, т. е. аустенит. Процесс первичной кристаллизации сталей заканчивается по линии AHJE.
При температурах, соответствующих линии ВС, из жидкого раствора кристаллизуется аустенит. В сплавах, содержащих от 4,3 % до 6,67 % углерода, при температурах, соответствующих линии CD, начинают выделяться кристаллы цементита первичного. Цементит, кристаллизующийся из жидкой фазы, называется первичным. B точке С при температуре 1147°С и концентрации углерода в жидком растворе 4,3 % образуется эвтектика, которая называется ледебуритом. Эвтектическое превращение с образованием ледебурита можно записать формулой ЖР4,3Л[А2,14+Ц6,67]. Процесс первичной кристаллизации чугунов заканчивается по линии ECF образованием ледебурита.
Таким образом, структура чугунов ниже 1147°С будет: доэвтектических – аустенит+ледебурит, эвтектических – ледебурит и заэвтектических – цементит (первичный)+ледебурит.
Превращения, происходящие в твердом состоянии, называются вторичной кристаллизацией. Они связаны с переходом при охлаждении γ-железа в α-железо и распадом аустенита.
Линия GS соответствует температурам начала превращения аустенита в феррит. Ниже линии GS сплавы состоят из феррита и аустенита.
Линия ЕS показывает температуры начала выделения цементита из аустенита вследствие уменьшения растворимости углерода в аустените с понижением температуры. Цементит, выделяющийся из аустенита, называется вторичным цементитом.
В точке S при температуре 727°С и концентрации углерода в аустените 0,8 % образуется эвтектоидная смесь состоящая из феррита и цементита, которая называется перлитом. Перлит получается в результате одновременного выпадения из аустенита частиц феррита и цементита. Процесс превращения аустенита в перлит можно записать формулой А0,8П[Ф0,03+Ц6,67].
Линия PQ показывает на уменьшение растворимости углерода в феррите при охлаждении и выделении цементита, который называется третичным цементитом.
Следовательно, сплавы, содержащие менее 0,008% углерода (точкаQ), являются однофазными и имеют структуру чистого феррита, а сплавы, содержащие углерод от 0,008 до 0,03% – структуру феррит+цементит третичный и называются техническим железом.
Доэвтектоидные стали при температуре ниже 727ºС имеют структуру феррит+перлит и заэвтектоидные – перлит+цементит вторичный в виде сетки по границам зерен.
В доэвтектических чугунах в интервале температур 1147–727ºС при охлаждении из аустенита выделяется цементит вторичный, вследствие уменьшения растворимости углерода(линия ES). По достижении температуры 727ºС (линия PSK) аустенит, обедненный углеродом до 0,8% (точка S), превращаясь в перлит. Таким образом, после окончательного охлаждения структура доэвтектических чугунов состоит из перлита, цементита вторичного и ледебурита превращенного (перлит+цементит).
Структура эвтектических чугунов при температурах ниже 727ºС состоит из ледебурита превращенного. Заэвтектический чугун при температурах ниже 727ºС состоит из ледебурита превращенного и цементита первичного.
Правило фаз устанавливает зависимость между числом степеней свободы, числом компонентов и числом фаз и выражается уравнением:
C = K + 1 – Ф,
где С – число степеней свободы системы;
К – число компонентов, образующих систему;
1 – число внешних факторов (внешним фактором считаем только температуру, так как давление за исключением очень высокого мало влияет на фазовое равновесие сплавов в твердом и жидком состояниях);
Ф – число фаз, находящихся в равновесии.
Сплав железа с углеродом, содержащий 0,2%С, называется доэвтектоидной сталью. Его структура при комнатной температуре – Феррит + Цементит (первичный).
Используя диаграмму состояния железо-цементит, опишите структурные превращения, происходящие при нагреве стали У10. Укажите критические точки и выберите оптимальный режим нагрева этой стали под закалку. Охарактеризуйте процесс закалки, опишите получаемую структуру и свойства стали.
Диаграмма состояния железо-цементит представлена на рисунке 1. При комнатной температуре сталь У10 имеет структуру цементита и перлита. До температуры Аc1 сохраняется исходная структура. При температуре Аc1 происходит превращение перлита в аустенит с содержанием углерода 0,8%. При нагреве выше точки Ас1 происходит растворение цементита в аустените (в соответствии с линией SE). Увеличение температуры выше точки Асm вызывает рост зерна аустенита.
Критические точки для стали У10: Аc1 = 730°С; Аcm = 800°С.
Для закалки заэвтектоидные стали нагревают на 50-70°С выше точки Ас1. Таким образом, температура нагрева под закалку составляет 780-800°С. При этих температурах в стали наряду с аустенитом имеется цементит. Поэтому после закалки в структуре заэвтектоидных сталей будет мартенсит с цементитом и небольшое количество остаточного аустенита. Охлаждающая среда при закалке – индустриальное масло. Твердость поверхности после закалки 62-64 HRC. Для снятия напряжений и стабилизации структуры после закалки изделия подвергают низкому отпуску.
Используя диаграмму состояния железо – карбид железа и кривую изменения твердости в зависимости от температуры отпуска, назначьте для углеродистой стали 40 температуру закалки и температуру отпуска, необходимые для обеспечения твердости 250 НВ. Опишите превращения на всех этапах термической обработки и получаемую структуру.
Закалка доэвтектоидной стали заключается в нагреве стали до температуры выше критической (Ас3), в выдержке и последующем охлаждении со скоростью, превышающей критическую.
Температура точки Ас3 для стали 40 составляет 790°С.
Доэвтектоидные стали для закалки следует нагревать до температуры на 30-50°С выше Ас3. Температура нагрева стали под закалку, таким образом, составляет 820-840°С. Структура стали 40 при температуре нагрева под закалку – аустенит, после охлаждения со скоростью выше критической – мартенсит.
В зависимости от температуры отпуска меняется твердость закаленной стали. Например, при 600°С твердость НВ не более 200 ед., при 400°С – не более 280 ед., а при 200°С – не более 450 ед.
Поэтому для получения твердости 250 НВ закаленную сталь подвергают высокому отпуску при температуре 500-520°С. Структура стали после высокого отпуска – сорбит отпуска. Высокий отпуск создает наилучшее соотношение прочности и вязкости.
Термическая обработка, состоящая из закалки и высокого отпуска, называют улучшением.
Лекция 3. Основные типы химической связи. Ковалентная связь
Ключевые слова: типы химической связи: ионная, металлическая, ковалентная, σ - и - связи, свойства ковалентной связи, механизмы образования связи, валентность.
Под химической связью понимают силы притяжения, удерживающие атомы или (ионы) друг около друга и создающие тем самым достаточно стабильный агрегат атомов (или ионов). По современным представлениям химическая связь имеет электростатическую природу. В ее образовании участвуют валентные электроны внешних и предвнешних подуровней атомов. Выделяют три основных типа химической связи: ковалентная, ионная, металлическая.
Ионная связьосуществляется, как электростатическое притяжение противоположно заряженных ионов (простых или сложных). Принято считать связь ионной, если разность электроотрицательностей элементов больше 1,9. Ионная связь, как правило, образуется между атомами типичных металлов и типичных неметаллов. Ионная связь характеризуется ненаправленностью и ненасыщаемостью. По этой причине посредством ионной связи образуются ионные кристаллы. Состав ионного соединения AnBm отражает только соотношение между числом катионов A m + и анионов B n - .
Металлическая связь возникает в металлах, сплавах, интерметаллических соединениях. Валентные электроны внешних оболочек металла относительно легко удаляются, из атомов образуются катионы металла. Электроны делокализованы и могут свободно перемещаться по всему кристаллу. Оставшиеся катионы металлов притягиваются делокализованным электронным облаком («электронным газом»),заполняющим пространство между ними. Образованную подобным образом химическую связь называют металлической связью. Металлическая связь характеризуется ненаправленностью и ненасыщаемостью. Строение металлических кристаллов наиболее точно описывается «структурами с плотнейшей укладкой шаров».
Для объяснения природы ковалентной связи и механизма ее образования используются два метода – метод валентных связей (ВС) и метод молекулярных орбиталей (МО). В основе метода ВС лежит теория Льюиса об образовании ковалентной связи формированием общей пары электронов между взаимодействующими атомами. В 1927 г. немецкие физики Гейтлер и Лондон провели квантово-механический расчет с использованием уравнения Шредингера для выяснения вопроса – как изменяется энергия в системе из двух атомов водорода при их сближении. Из расчетов были получены следующие выводы: 1. Для образования химической связи атомы должны предоставить в общее пользование электроны с противоположными спинами. 2. Атомные орбитали при образовании химической связи «перекрываются». 3. При образовании химической связи выделяется энергия, называемая энергией связи, что является движущей силой протекания химической реакции. Связь, образованную посредством перекрывания электронных облаков, то есть осуществляемую общей парой электронов с противоположными спинами, называют ковалентной связью. Если электронные облака перекрываются вдоль линии, соединяющей ядра атомов, образуется σ-связь. Если электронные облака перекрываются выше и ниже линии, соединяющей ядра атомов, образуется π-связь. σ-Связь более прочная, вокруг нее возможно вращение без ее разрыва. π-Связь менее прочная и образуется как дополнительная. Порядок (кратность) связи определяется числом общих электронных пар, осуществляющих связь между ядрами атомов. Основные характеристики ковалентной химической связи – длина связи, энергия связи. С увеличением кратности связи уменьшается длина связи и увеличивается суммарная энергия связи. Ковалентной связи присущи следующие особенности – насыщаемость и направленность. Насыщаемостьопределяет стехиометрию молекулярных химических соединений (формульный состав, массовые соотношения элементов) и валентные возможности атомов (способность образовать ограниченное число ковалентных связей). Общая пара связывающих электронов может образоваться в результате объединения взаимодействующими атомами неспаренных электронов с противоположными спинами (обменный механизм). Во многих случаях число связей образованных атомом оказывается больше числа неспаренных электронов в основном состоянии. Это объясняется возможностью образования связей из возбужденного состояния: происходит распаривание одной или нескольких внешних электронных пар с последующим переходом одного электрона от каждой пары на свободную орбиталь более высокого подуровня того же внешнего уровня. Энергия, затраченная на возбуждение атома, с большим избытком компенсируется энергией, выделяемой при образовании связей возбужденным атомом. Например, для бора характерно образование трех связей в соединениях (BF3) в результате перехода в возбужденное состояние с тремя неспаренными электронами: B …2s 2 2p 1 → B*…2s 1 2p 2 .
Как правило, максимальная валентность элемента совпадает с номером группы, в которой он находится, исключение составляют N, O, F и некоторые d - металлы с почти заполненным предвнешним d - подуровнем.
Второй механизм образования ковалентной связи – донорно-акцепторный: один атом (донор) представляет неподеленную пару электронов, а другой (акцептор) свою вакантную орбиталь.
Типы химической связи: ионная, ковалентная (типы ковалентной связи, полярность), координационная, металлическая, водородная.
Электроотрицательность-способность атома притягивать электроны.
Ионная связь — очень прочная химическая связь, образующаяся между атомами с большой разностью (>1,5 по шкале Полинга) электроотрицательностей, при которой общая электронная пара полностью переходит к атому с большей электроотрицательностью.(Электростатическое взаимодействие между ионами).
Если химическая связь образуется между атомами, которые имеют очень большую разность электроотрицательностей (ЭО > 1.7 по Полингу), то общая электронная пара полностью переходит к атому с большей ЭО. Результатом этого является образование соединения противоположно заряженных ионов:
Ковалентная связь (атомная связь, гомеополярная связь) — это самая прочная, самая распространенная хим. связь образуется за счёт обобществления не спаренных электронов, атомов неметаллов в общую электронную пару (в орган.соед.).
A· + ·В → А : В
Между одинаковыми атомами – ковалентная неполярная(F2, H2, N2), между разными – ковалентная полярная(HCI, NaCI).
-Простая ковалентная связь. Для её образования каждый из атомов предоставляет по одному неспаренному электрону. При образовании простой ковалентной связи формальные заряды атомов остаются неизменными.
H • + • H H : H
-Донорно-акцепторная связь. Для образования этого вида ковалентной связи оба электрона предоставляет один из атомов — донор. Второй из атомов, участвующий в образовании связи, называется акцептором. В образовавшейся молекуле формальный заряд донора увеличивается на единицу, а формальный заряд акцептора уменьшается на единицу.
- Семиполярная связь. Её можно рассматривать как полярную донорно-акцепторную связь. Этот вид ковалентной связи образуется между атомом, обладающим неподелённой парой электронов (азот, фосфор, сера, галогены и т. п.) и атомом с двумя неспаренными электронами (кислород, сера).
Координационная(Донорно-акцепторная) связь- частный случай ковалентной связи, при которой донор предоставляет целую электронную пару, акцептор- свободную арбиталь(NH4 + , в комплексных соединениях [ ]).
Металлическая связь — химическая связь, которая обусловлена взаимодействием положительных ионов металлов, составляющих кристаллическую решётку, с электронным газом из валентных электронов.
Водородная связь — электростатическое взаимодействие между положительно поляризованным атомом водорода и другим электроотрицательным атомом(O, S, N, F). Водородные связи могут быть межмолекулярными или внутримолекулярными. Особенностями водородной связи, по которым её выделяют в отдельный вид, является её не очень высокая прочность, её распространенность и важность, особенно в органических соединениях, а также некоторые побочные эффекты, связанные с малыми размерами и отсутствием дополнительных электронов у водорода.
12. Термодинамические системы: изолированные, закрытые, открытые, гомогенные, гетерогенные. Параметры системы.
Под термодинамической системой подразумевают избранную совокупность тел или веществ, состоящую из большого числа структурных единиц (молекул, атомов, ионов) и отделенную от окружающей внешней среды определенной границей или поверхностью раздела.
В зависимости от свойств поверхности раздела, термодинамические системы делятся на изолированные, закрытые и открытые.
Изолированные системы не могут обмениваться с окружающей средой ни веществом, ни энергией. Закрытые системы обмениваются с внешним миром только энергией, а открытые – и веществом, и энергией.
Если между отдельными частями системы не существует физических, т.е. реальных границ раздела, то такие системы называются гомогенными(однородными). Свойства данных систем, находящихся в состоянии равновесия, одинаковы во всех их точках.
Существуют также системы, между отдельными частями которых имеются границы раздела. При переходе через них многие свойства меняются скачкообразно. Такие системы называются гетерогенными.
Физические величины, характеризующие какое-либо свойство системы, называются термодинамическими параметрами. Они могут быть микроскопическими и макроскопическими.
Совокупность значений размеров и масс всех частиц (молекул либо ионов), составляющих систему, их положений в пространстве, скоростей движения и т.д. называется набором микроскопических параметров.
Величины, характеризующие всю систему в целом (давление, объем, температура, масса, плотность и т.д.) называются макроскопическими параметрами.
Некоторые макроскопические параметры системы (масса, внутренняя энергия) могут быть заданы как сумма соответствующих микроскопических параметров.
Экстенсивными называются такие параметры, значения которых для всей системы равны сумме значений этих же параметров для отдельных частей системы (например, масса, объем).
Совокупность численных значений термодинамических параметров системы, характеризующих ее физические и химические свойства (присущие ей в данный момент времени), называется иначе состоянием системы.
Если значения параметров не меняются во времени, такое состояние системы называется равновесным. Такое состояние называется стационарным.
Изменение во времени значений одного или нескольких макроскопических параметров системы называют иначе термодинамическим процессом.
Сумму всех процессов, которые вывели систему из начального состояния, а затем вернули ее в это же состояние, называют круговым процессом или циклом.
Все процессы, встречающиеся в природе, можно разделить на самопроизвольные и несамопроизвольные.
Термодинамические процессы подразделяются также на обратимые и необратимые, равновесные и неравновесные.
Процесс называется термодинамически обратимым, если его можно провести и в прямом, и в обратном направлении.
Реальные процессы, протекающие в природе, являются термодинамически необратимыми и неравновесными.
Функции состояния системы: внутренняя энергия, энтальпия, энтропия, химический потенциал, изобарно- и изохорно-изотермический потенциал. Изобарные, изохорные, изотермические процессы.
Энергетическое состояние химической реакции как системы описывается с использованием следующих характеристик: U-внутренняя энергия,H-энтальпия,S-энтропия,G-энергия Гиббса.Теплота, которую получает система, идет на приращение внутренней энергии и совершение работы: Q=DU+A. Если система не совершает никакой работы, кроме работы расширения, тоQ=DU+pDV. ВеличинаDH=DU+pDVприp=constназываетсяэнтальпией реакции. Т.к. внутреннюю энергию тела измерить невозможно (можно измерить только изменениеDU), то точно так же невозможно измерить энтальпию тела – в расчетах используется изменение энтальпииDH.
Законы термохимии:
Лавуазье-Лапласа: тепловой эффект образования химических соединений равен, но обратен по знаку тепловому эффекту его разложения.
Гесса: тепловой эффект реакции при постоянном давлении или объеме зависит только от начального и конечного состояния системы и не зависит от пути перехода.
Энтропия– количественная мера беспорядка системы. Энтропия зависит от: от числа частиц в системе, от природы вещества, от агрегатного состояния. Для газообразных веществ знак DS определяется по изменению объема. Если объем не изменяется, то знак определить нельзя. В изолированных системах возможны процессы, которые идут с увеличением энтропии. Это означает, что знак DS можно принять за критерий возможного самопроизвольного протекании реакции (только в изолированных системах!).
Химическийпотенциал ini=0 – условие химического равновесия,m-энергия Гиббса 1 моля вещества (для однокомпонентной системы). Значение химического потенциала нельзя измерить, но можно рассчитать исходя из уравнения связывающего химический потенциал с составом:mi=mi o +RTlnK, гдеK=i-парциальное давление,Ci-концентрация,Cmi-массовая доля,Xi-мольная доля> – константа. Для реальных растворов - mi=mi o +RTlnAi.
Суммарное влияние энергетических и энтропийных факторов при постоянном давлении и температуре отражает изменение изотермического потенциала, который называется изменением свободной энергии Гиббса: DG=DH-TDS. Свободной энергией Гиббса называется энергия, складываемая из энергий химических связей. Знак DG есть критерий термодинамической вероятности самопроизвольного протекания процесса в данных условиях (p,T=const). При данных условиях могут самопроизвольно протекать только те процессыDG для которых меньше 0. При низких температурах протекают главным образом экзотермические реакции. При высоких температурах главную роль играет энтропийный член уравнения.
ИЗОХОРНО-ИЗОТЕРМИЧЕСКИЙ ПОТЕНЦИАЛ - свободная энергия, энергияГельмгольца, - один из потенциалов термодинамических, равный F = U - TS, где U, S и Т - внутренняя энергия, энтропия и термодинамическая температура системы. При изотермическом переходе (T=const) системы из состояния 1, в котором её изохорно-изотермический потенциал равен F1, в состояние 2, в котором её изохорно-изотермический потенциал равен F2, система совершает работу А< (F1 - F2), где знак равенства соответствует обратимому процессу, а знак неравенства - необратимому процессу. То есть, изменение изохорно-изотермического потенциала определяет работу, совершаемую системой в обратимом изотермическом процессе.
ИЗОБАРНО-ИЗОТЕРМИЧЕСКИЙ ПОТЕНЦИАЛ Гиббса-энергия, свободная энтальпия, - один из потенциалов термодинамических, равный
G = Н - TS, где Н, S, Т - энтальпия,
энтропия, термодинамическая температура системы. Изобарно-изотермический потенциал пропорционален числу частиц в системе; отнесённый к одной частице он называется химическим потенциалом. Изобарно-изотермический потенциал удобен для описания процессов, в которых возможен обмен веществом с окружающими телами.
Изобарный процесс — процесс изменения состояния термодинамической системы при постоянном давлении ().
Изохорный процесс — процесс изменения состояния термодинамической системы при постоянном объёме ().
Изотермический процесс — процесс изменения состояния термодинамической системы при постоянной температуре ()
Сущность металлического ионного и ковалентного типов связи
Ключевые слова конспекта. Химическая связь: ковалентная (полярная и неполярная), ионная, металлическая.
Силы, которые удерживают атомы в молекулах, называются химическими связями.
Образование химической связи происходит в том случае, если этот процесс сопровождается выигрышем энергии. Эта энергия возникает, если каждый атом, образующий химическую связь, получает устойчивую электронную конфигурацию.
По способу образования и существования химическая связь может быть ковалентной (полярной, неполярной), ионной, металлической.
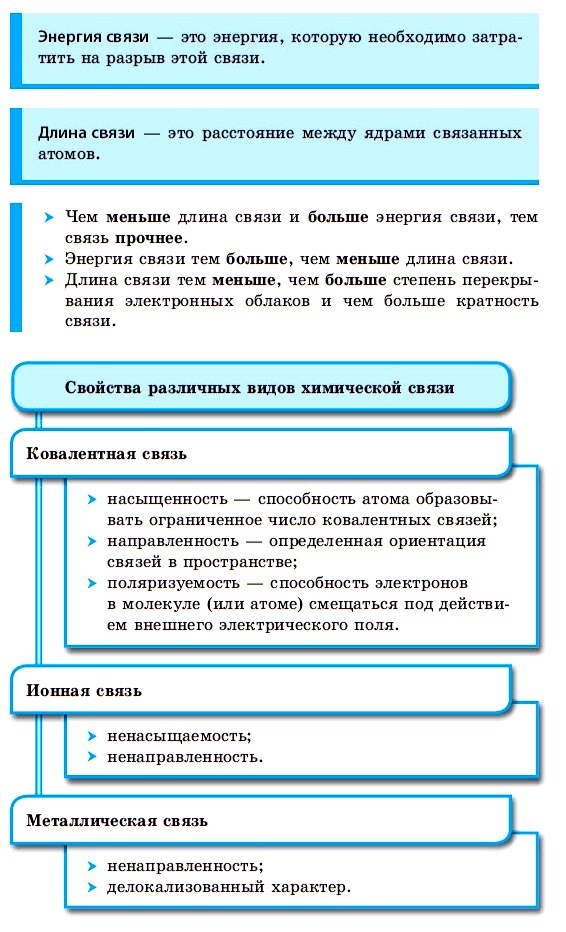
Ковалентная химическая связь
■ Ковалентная химическая связь — это связь, возникающая между атомами путем образования общих электронных пар за счет неспаренных электронов.
Внешние уровни большинства элементов периодической системы (кроме благородных газов) содержат неспаренные электроны, то есть являются незавершенными. В процессе химического взаимодействия атомы стремятся завершить свой внешний электронный уровень.
Например, электронная формула атома водорода: 1s 1 . Ее графический вариант:Таким образом, атом водорода в химических реакциях стремится завершить свой внешний 1 s-уровень одним s-электроном. При сближении двух атомов водорода происходит усиление притяжения электронов одного атома к ядру другого атома. Под действием этой силы расстояния между ядрами атомов сокращаются и в результате их электронные орбитали перекрывают друг друга, создавая общую электронную орбиталь — молекулярную. Электроны каждого из атомов водорода через область перекрывания орбиталей мигрируют от одного атома к другому, то есть образуют общую электронную пару. Ядра будут сближаться до тех пор, пока нарастающие силы отталкивания одноименных зарядов не уравновесят силы притяжения.
Переход электронов с атомной орбитали на молекулярную сопровождается снижением энергии системы (более выгодное энергетическое состояние) и образованием химической связи:

Подобным образом образуются общие электронные пары при взаимодействии атомов р-элементов. Так образуются все двухатомные молекулы простых веществ. При образовании F2 и Cl2 перекрываются по одной р-орбитали от каждого из атомов (образуется одинарная связь), а при взаимодействии атомов азота перекрываются по три р-орбитали от каждого и в молекуле азота N2 образуется тройная связь.

Электронная формула атома хлора: 1s 2 2s 2 2p 6 3s 2 3p 5 . Графическая формула:
Электронная формула атома азота: 1s 2 2s 2 2p 3 . Графическая формула:
Прочность связей в молекуле определяется количеством общих электронных пар у ее атомов. Двойная связь прочнее одинарной, тройная — прочнее двойной.
С увеличением количества связей между атомами сокращается расстояние между ядрами атомов, которое называют длиной связи, и увеличивается количество энергии, необходимое для разрыва связи, которое называется энергией связи. Например, в молекуле фтора связь одинарная, ее длина составляет 1,42 нм (1 нм = 10 –9 м), а в молекуле азота связь тройная, ее длина — 0,11 нм. Энергия связи в молекуле азота в 7 раз превышает энергию связи в молекуле фтора.

При взаимодействии атома водорода с атомом хлора оба атома будут стремиться завершить свои внешние энергетические уровни: водород — 1 s-уровень и хлор — 3р-уровень. В результате их сближения происходит перекрывание 1 s-орбитали атома водорода и 3р-орбитали атома хлора, а из соответствующих неспаренных электронов формируется общая электронная пара:

В молекулах Н2 и HCl область перекрывания орбиталей атомов водорода расположена в одной плоскости — на прямой, соединяющей центры атомных ядер. Такая связь называется σ-связью (сигма-связью):
Однако если в молекуле формируется двойная связь (с участием двух электронных орбиталей), то одна связь будет σ-связью, а вторая будет образована между орбиталями, расположенными параллельно друг другу. Параллельные орбитали перекроются с образованием двух общих участков, расположенных сверху и снизу от линии, соединяющей центры атомов.
При образовании ковалентной связи меду атомами с одинаковой электроотрицательностью (Н2, F2, O2, N2) общая электронная пара будет располагаться на одинаковом расстоянии от атомных ядер. При этом общие электронные пары принадлежат в равной степени обоим атомам одновременно, и ни на одном из атомов не будет избыточного отрицательного заряда, который несут на себе электроны. Такой вид ковалентной связи называется неполярной.
■ Ковалентная неполярная связь — вид химической связи, образующийся между атомами с одинаковой электроотрицательностью.

В случае, когда электроотрицательности элементов, вступающих во взаимодействие, не равны, но близки по значению, общая электронная пара смещается в сторону элемента с большей электроотрицательностью. При этом на нем образуется частичный отрицательный заряд (за счет отрицательно заряженных электронов):
В результате на атомах соединения образуются частичные заряды Н +0,18 и Cl –0,18 ; а в молекуле возникают два полюса — положительный и отрицательный. Такую ковалентную связь называют полярной.
■ Ковалентная полярная связь — вид ковалентной связи, образующейся при взаимодействии атомов, электроотрицательность которых отличается незначительно.
Образовавшийся частичный заряд на атомах в молекуле обозначают греческой буквой 8 (дельта), а направление смещения электронной пары — стрелкой:Ионная химическая связь
В случае химического взаимодействия между атомами, электроотрицательность которых резко отличается (например, между металлами и неметаллами), происходит почти полное смещение электронных облаков к атому с большей электроотрицательностью. При этом, поскольку заряд ядра атома имеет положительное значение, атом, который почти полностью отдал свои валентные электроны, превращается в положительно заряженную частицу — положительный ион, или катион. Атом, получивший электроны, превращается в отрицательно заряженную частицу — отрицательный ион, или анион:Ион — это одноатомная или многоатомная отрицательно либо положительно заряженная частица, в которую превращается атом в результате потери или присоединения электронов.
Между разноименно заряженными ионами при их сближении возникают силы электростатического притяжения — положительно и отрицательно заряженные ионы сближаются, образуя молекулу вещества.
■ Ионная химическая связь — это связь, образующаяся между ионами за счет сил электростатического притяжения.
Процесс присоединения электронов в ходе химических взаимодействий атомами с большей электроотрицательностью называется восстановлением, а процесс отдачи электронов атомами с меньшей электроотрицательностью — окислением.

Схему образования ионной связи между атомами натрия и хлора можно представить следующим образом:
Ионная химическая связь присутствует в оксидах, гидроксидах и гидридах щелочных и щелочноземельных металлов, в солях, а также в соединениях металлов с галогенами.
Ионы могут быть как простыми (одноатомными): Cl – , Н + , Na + , так и сложными (многоатомными): NH4 – . Заряд иона принято записывать вверху после знака химического элемента. Вначале записывается величина заряда, а затем его знак.
Металлическая связь
Между атомами металлов возникает особый вид химической связи, которая называется металлической. Образование этой связи обусловлено тремя особенностями строения атомов металлов:
- на внешнем энергетическом уровне присутствуют 1—3 электрона (исключения: атомы олова и свинца (4 электрона), атомы сурьмы и висмута (5 электронов), атом полония (6 электронов));
- атом имеет сравнительно большой радиус;
- атом имеет большое количество свободных орбиталей (например, у Na один валентный электрон располагается на 3-м энергетическом уровне, который имеет десять орбиталей (одну s-, три р- и пять d-орбиталей).
При сближении атомов металлов происходит перекрытие их свободных орбиталей, и валентные электроны получают возможность перемещаться на близкие по значениям энергии орбитали соседних атомов. Атом, теряющий электрон, превращается в ион. Таким образом, в металле формируется совокупность электронов, свободно перемещающихся между ионами. Притягиваясь к положительным ионам металла, электроны восстанавливают их, а затем снова отрываются, переходя к другим ионам. Такой процесс превращения атомов в ионы и обратно происходит в металлах непрерывно. Частицы, из которых состоят металлы, называют атом-ионами.
■ Металлическая связь — это связь, образующаяся между атом-ионами в металлах и сплавах посредством постоянного перемещения между ними валентных электронов: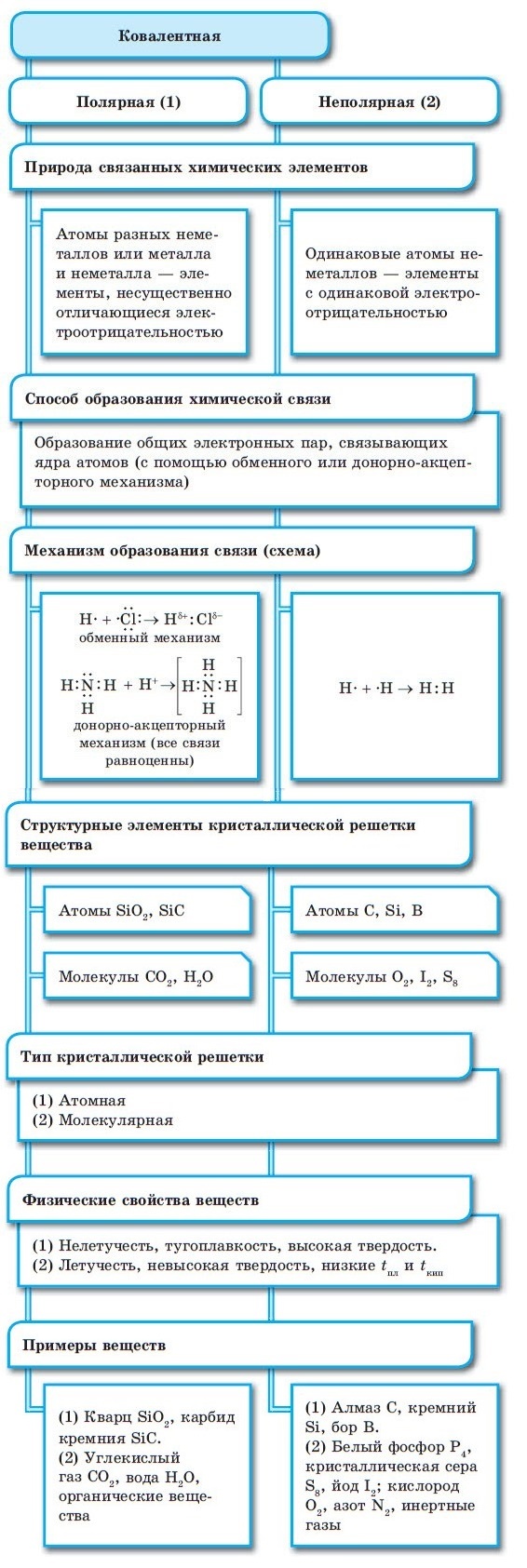
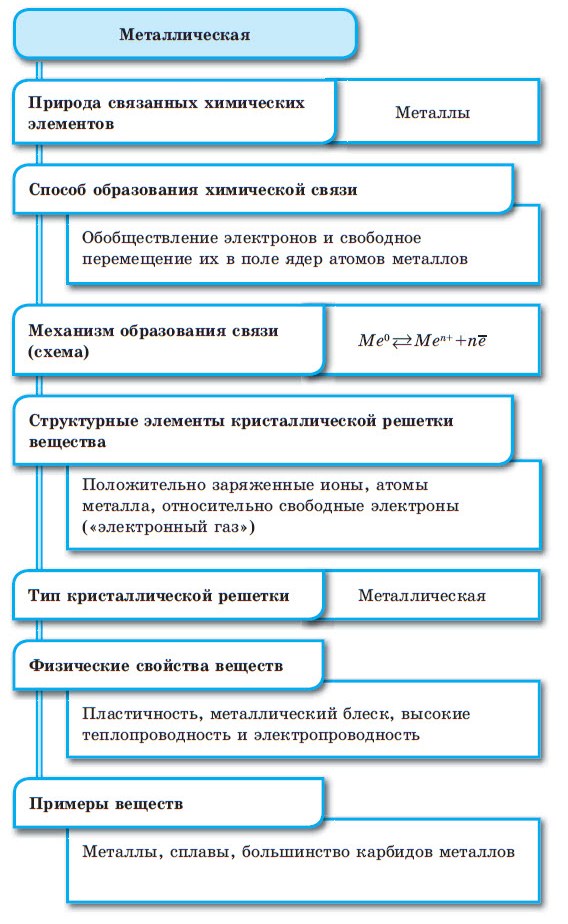

Конспект урока «Химическая связь: ковалентная, ионная, металлическая».
Ионная связь
В этом материале речь пойдет о том, что такое ионная связь и чем она отличается от других видов, которые изучают на уроках химии в 8 классе.
О чем эта статья:
Общие сведения о химических связях
Давайте вспомним, как образуются химические связи. Для этого представим атом: он состоит из ядра с положительным зарядом и набора отрицательно заряженных электронов, которые располагаются на нескольких уровнях. Внешний уровень называется валентным, на нем располагаются валентные электроны. Они могут образовывать пары или быть свободными, т. е. неспаренными.
Во взаимодействии двух атомов участвуют свободные электроны внешней оболочки. Сколько таких электронов имеется у атома — столько химических связей он может образовать.
При этом каждый атом стремится приобрести устойчивую конфигурацию — двух- или восьмиэлектронную внешнюю оболочку, подобную той, что есть у инертного газа. Атом может достичь ее, отдавая или принимая часть электронов, а также образуя общую электронную пару с другим атомом. Если в результате получается два разноименно заряженных иона, говорят об ионном типе связи. Он характерен для взаимодействия атомов металла и неметалла.
Определение ионной связи
Рассмотрим этот тип связи на примере реакции натрия и водорода, в результате которой получается гидрид натрия. У атома натрия Na есть один свободный электрон на внешнем уровне, в то время как атому водорода H не хватает одного электрона, чтобы завершить внешнюю оболочку и принять стабильную форму. Поскольку натрий имеет более низкую электроотрицательность, чем водород, он отдает свой валентный электрон и получает отрицательный заряд. Водород принимает этот электрон и получает положительный заряд. В итоге образуется два иона — катион Na + и анион H - .
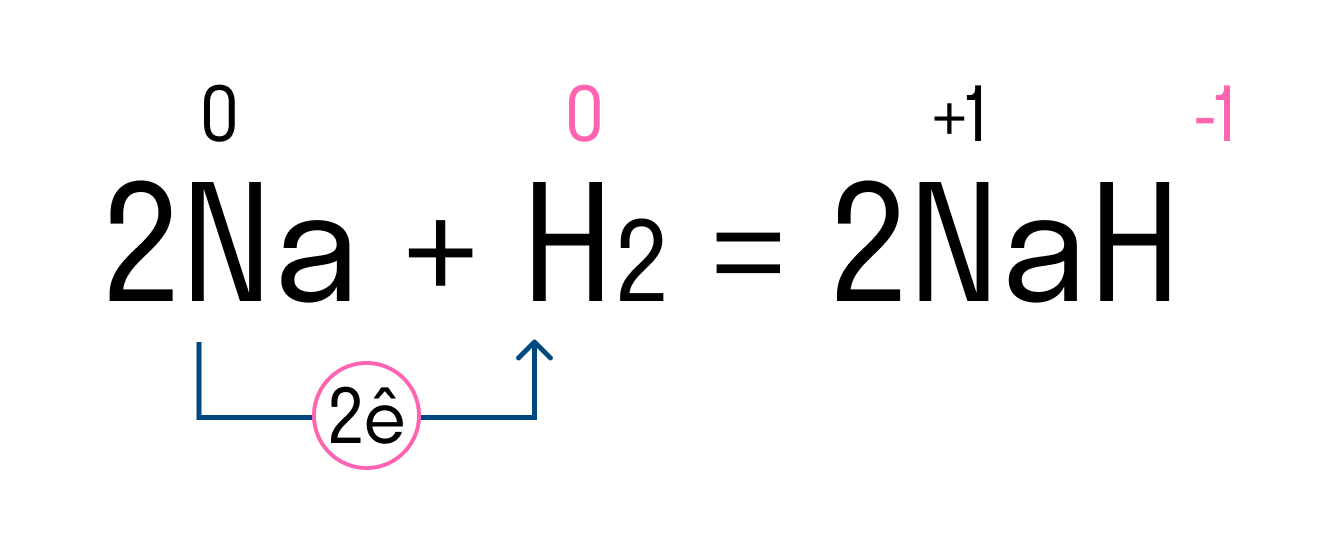
Между положительным ионом Na + и отрицательным H - возникает электростатическое притяжение, которое и удерживает их вместе. Так образуется ионная связь в гидриде натрия.
Ионная связь — это тип химической связи, характерный для разноименно заряженных ионов, которые образовались в результате отдачи и присоединения электронов атомами. В нее вступают элементы с большой разностью электроотрицательности. Обычно так взаимодействуют атомы металла и неметалла.
Чаще всего именно так связаны в соединениях щелочные и щелочноземельные металлы с галогенами. Поскольку у щелочных металлов электроотрицательность ниже, их атомы становятся катионами, а атомы галогенов — анионами.
Механизм образования ионной связи похож на донорно-акцепторный механизм ковалентной связи. Первую даже называют крайним выражением второй.
Соли аммония NH4NO3, NH4Cl, (NH4)2SO4 хоть и не являются соединениями металла и неметалла, но также образованы с помощью ионной связи.
Координационное число
Вернемся к нашему примеру с гидридом натрия и посмотрим на кристаллическую решетку, которую имеет это ионное соединение. Каждый ион Na + контактирует с шестью ионами H - . Это максимально возможное для данного иона число химических связей, оно называется координационным.
Координационное число — это количество ближайших соседей иона в ионной кристаллической решетке. По сути это количество связей, которые образует каждый ион в составе сложного вещества.
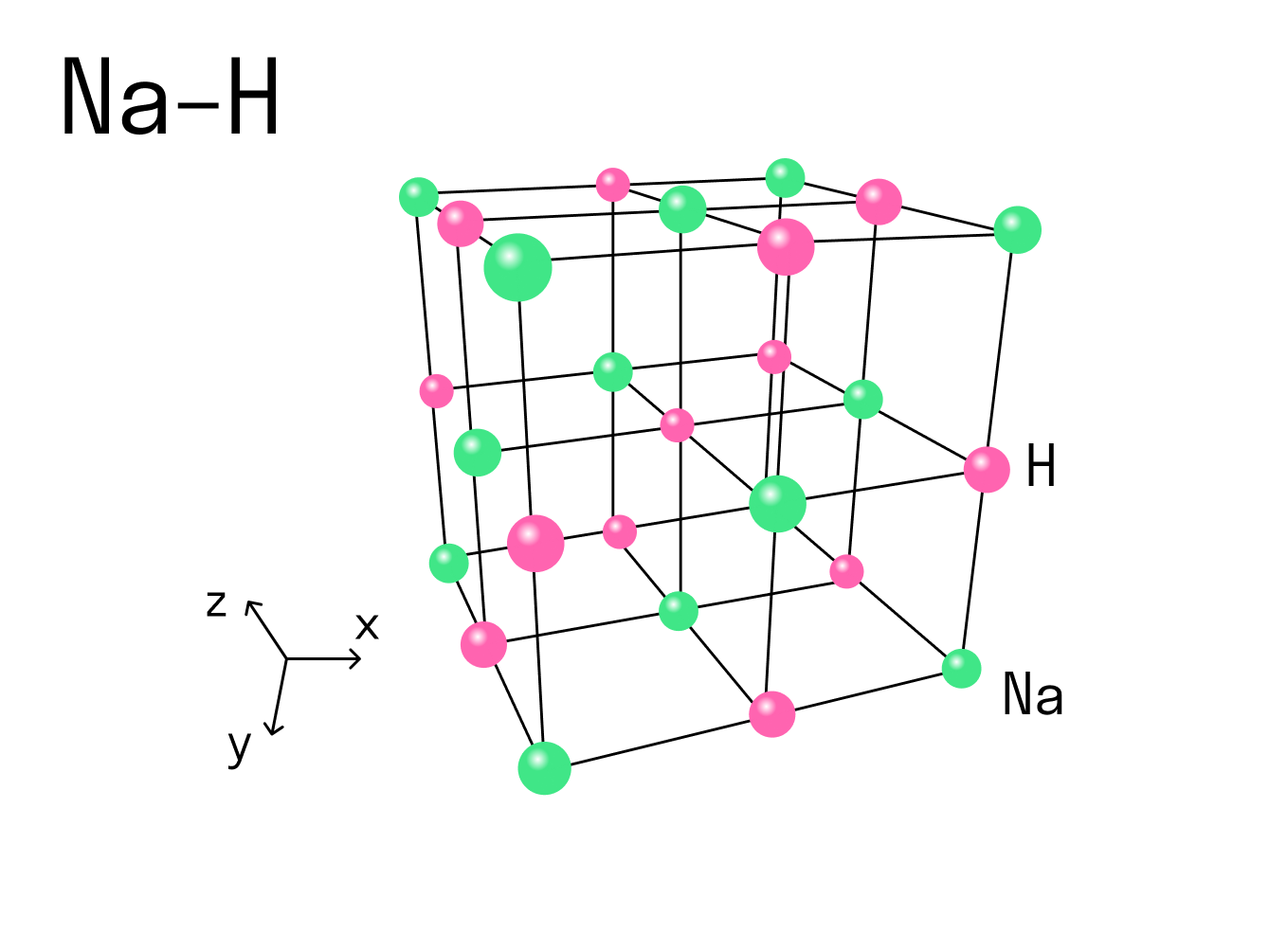
При рассмотрении ковалентной химической связи говорят о валентности — она характеризует, сколько связей есть у конкретного атома с другими атомами. Но к ионным соединениям это понятие не применяют, потому что все ионы в кристаллической решетке взаимодействуют друг с другом. Вместо этого есть координационное число, и оно отражает количество таких взаимодействий.
Примеры веществ с ионной связью
Таким же образом, как в гидриде натрия, ионы образуются и в других подобных ему соединениях. Например, в хлориде натрия NaCl атом натрия имеет один свободный электрон и отдает его атому хлора. В итоге оба завершают свой внешний уровень. Образуется ион натрия с положительным зарядом и отрицательно заряженный ион хлора.
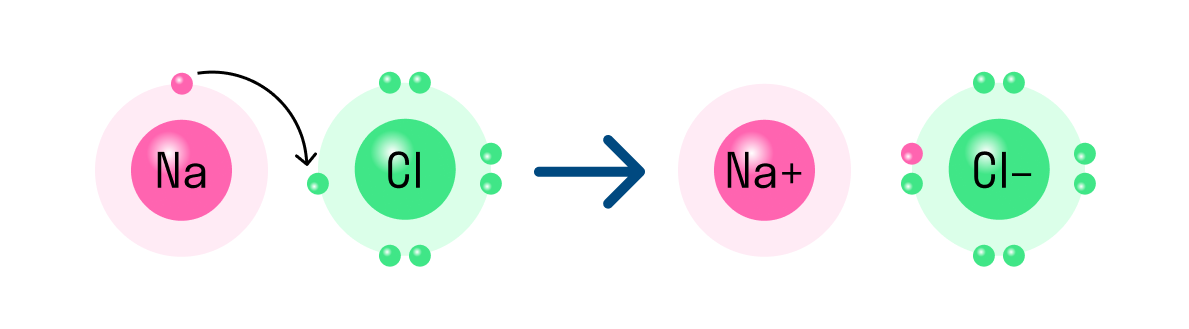
Другой пример ионной химической связи — сульфид натрия Na2S. В данном случае у нас также есть натрий с одним свободным электроном и сера, у которой на внешнем уровне есть 2 свободных электрона из 6. Таким образом, чтобы завершить уровень и обрести стабильную форму, сере нужно 2 электрона. Поэтому в формуле сульфида серы присутствует два атома натрия.
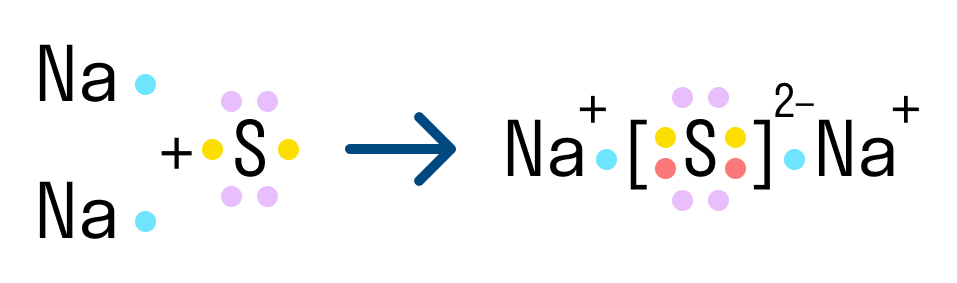
Характеристики ионной связи
Мы узнали, как образуется ионная связь, а теперь поговорим о ее характеристиках. Она существенно отличается от других типов связи между атомами.
не имеет кратности.
Разберемся в каждом пункте и начнем с направленности. Ковалентная полярная связь направлена, потому что она подразумевает смещение общей электронной пары к тому атому, который имеет большую электроотрицательность. В случае с ионами все иначе. Согласно закону Кулона притяжение между отрицательным и положительным ионом идет по прямой, соединяющей эти заряженные частицы. В кристаллической решетке все разноименно заряженные ионы взаимодействуют друг с другом и притяжение распределяется равномерно, поэтому говорят, что ионная связь не направлена.
А как насчет насыщаемости? Эта характеристика указывает на то, что атом может вступить в ограниченное количество химических связей, поскольку имеет ограниченное число неспаренных электронов. Но ионная связь — это не процесс соединения свободных электронов в пары, а взаимное притяжение ионов. Каждый ион может притягивать к себе неограниченное число ближайших соседей, поэтому нет смысла говорить о насыщаемости.
Из вышесказанного понятно, что ионная связь не имеет и кратности. Эта характеристика означает число общих электронных пар у атома, но в данном случае мы рассматриваем притяжение между ионами.

Физические свойства ионной связи
Между ионами в молекуле всегда образуется достаточно сильное притяжение, поэтому вещества с ионной связью в обычных условиях твердые и нелетучие. Такие соединения сложно разрушить при помощи тепловой энергии, что обуславливает высокую температуру кипения и плавления. При этом ионы имеют небольшой радиус взаимодействия — это придает веществам хрупкость.
Свойства ионных соединений:
растворимость в воде,
Типичным веществом с ионными связями можно считать хлорид натрия NaCl или поваренную соль. Ее кристаллы в точности соответствуют всем характеристикам.
Как определить ионную связь
Чтобы быстро понять, является ли нужное нам соединение ионным, выполните следующие действия:
Посмотрите, какие элементы входят в состав соединения. Формула вещества с ионной связью должна включать металл и неметалл. Если это щелочной металл (I группа таблицы Менделеева) и галоген (VII группа), то связь между ними точно ионная.
По шкале Полинга определите электроотрицательности обоих элементов соединения. Если разница между ними больше 1,7 — связь ионная. Это объясняется тем, что такой тип связи характерен для веществ, у которых сильно отличаются показатели электроотрицательности.
Дополнительным способом убедиться в правильности результата может стать оценка физических свойств вещества. Если оно имеет высокую температуру кипения или плавления и проводит электроток — связь скорее всего ионная.
Вопросы для самопроверки:
Опишите, как образуется ионная связь. Какие условия для этого необходимы?
Что такое координационное число элемента в ионном соединении?
Каковы основные физические свойства ионных соединений?
В чем разница между характеристиками ионной и ковалентной связей?
Как можно определить ионную связь, зная электроотрицательность элементов в соединении?
Читайте также:
