Тест 11 класс металлы неметаллы
Обновлено: 21.06.2024
За лето ребенок растерял знания и нахватал плохих оценок? Не беда! Опытные педагоги помогут вспомнить забытое и лучше понять школьную программу. Переходите на сайт и записывайтесь на бесплатный вводный урок с репетитором.
Вводный урок бесплатно, онлайн, 30 минут
Предварительный просмотр:
Контрольная работа «Металлы и Неметаллы».
Тестовые задания с выбором одного правильного ответа из четырех.
1. s-Элементу 4-го периода ПСХЭ соответствует электронная формула:
1) 1s 2 2s 2 2p 6 3s 2 3p 6 3d 3 4s 2 2) 1s 2 2s 2 2p 6 3s 2 3p 6 3d 1 4s 2
3) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 4) 1s 2 2s 2 2p 6 3s 1
2. Электронная формула иона натрия:
1) 1s 2 2s 2 2p 6 3s 2 2) 1s 2 2s 2 2p 6 3) 1s 2 2s 2 2p 6 3s 1 4) 1s 2 2s 2 2p 5
3. Переменную степень окисления в соединениях проявляет:
1) барий 2) медь 3) кальций 4) цезий
4. Простое вещество – железо – может являться:
1) только восстановителем 2) только окислителем
3) и окислителем, и восстановителем
5. Схема превращений Cu +2 →Cu +1 →Cu 0 представляет собой процессы:
1) восстановления 2) окисления
3) окисления (1), восстановления (2) 4) восстановления(1), окисления(2)
6. Восстановительные свойства в ряду химических элементов: Cs – Rb – K – Ca:
1) изменяются периодически 2) не изменяются 3) ослабевают 4) усиливаются
7. Формула вещества Х в уравнении реакции: Cu+2H 2 SO 4 =CuSO 4 +X+2H 2 O:
1) H 2 2) SO 2 3) H 2 S 4) SO 3
8. Формулы продуктов электролиза бромида натрия на инертных электродах:
1) Na, H 2 2) NaOH, Br 2 , H 2 3) Na, Br 2 4) NaOH, H 2
9. Цинк взаимодействует с каждым веществом группы:
1) водород, сульфат меди (II) (раствор), метаналь
2) кислород, муравьиная кислота, сера
3) оксид углерода (IV), оксид кальция, фенол (расплав)
4) глюкоза, этанол, хлор
10. Основные свойства гидроксидов усиливаются в ряду:
1) KOH-NaOH-Be(OH) 2 -LiOH 2) Be(OH) 2 -LiOH-NaOH-KOH
3) LiOH-Be(OH) 2 -NaOH-KOH 4) KOH-NaOH-Be(OH) 2 -LiOH
Задания со свободным ответом.
11. Составьте формулы высшего оксида и гидроксида элемента, в ядре которого содержится 56 протонов. Назовите эти вещества, укажите их характер.
12. Составьте уравнения реакций следующих превращений: Al → X → AlCl 3 → Al(NO 3 ) 3 → X → KAlO 2
13. Дополните фразу: «В периоде с уменьшением заряда ядра атома от галогена к щелочному металлу радиус атомов …».
14. Сравните число атомов в 32 г меди и 12 г магния.
15. Рассчитайте объем, количество вещества и массу газа, полученного при взаимодействии 3,5 г лития с водой, взятой в избытке.
16. Напишите уравнения химических реакций:
а) получения фосфора из фосфата кальция;
б) взаимодействия фосфора с избытком кислорода
в) взаимодействие фосфора с магнием;
г) взаимодействие фосфора с разбавленной азотной кислотой;
д) взаимодействие фосфора с серой.
Для каждой реакции составьте электронные уравнения процессов окисления и восстановления. Укажите окислитель и восстановитель.
Составьте электронную формулу атома фосфора его иона Р 3+ .
- Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: CH 4 1 CO 2 2 CaCO 3 3 Ca(HCO 3 ) 2 4 CaCO 3 5 CaCl 2
Для реакций 1 составьте электронный баланс, для реакции 3, 4 и 5 – ионные уравнения в краткой форме. Назовите полученные вещества.
Тест 11 класс металлы неметаллы
Тесты по химии 11 класс. Тема: "Неметаллы"
Правильный вариант ответа отмечен знаком +
1. Неметаллы – это:
+ химические элементы, которые могут проявлять свойства как окислителя (принимают электроны), так и восстановителя (отдают электроны)
- химические элементы, которые проявляют свойства только окислителя (принимают электроны)
- химические элементы, которые проявляют свойства только восстановителя (отдают электроны)
2. Сколько химических элементов относятся к неметаллам:
3. За счет каких связей образованы простые вещества - неметаллы:
+ ковалентных неполярных связей
- ковалентных полярных связей
4. Неметалл, являющийся газом при нормальных условиях:
5. Неметалл, являющийся летучей жидкостью при нормальных условиях:
6. Неметалл, являющийся твердым веществом при нормальных условиях:
7. К физическим свойствам неметаллов относится:
- наличие металлический блеска
8. При освещении данный неметалл проводит электрический ток в тысячу раз больше, чем в темноте:
9. Какую окраску имеет фтор?
тест 10. Цвет кристаллической серы:
11. Наибольшие окислительные свойства проявляет:
12. Наибольшие восстановительные свойства проявляет:
13. В реакции взаимодействия между металлом и неметаллом последний всегда выполняет роль:
- не выполняет какой-либо роли
14. При взаимодействии неметаллов между собой в роли окислителя выступает тот неметалл, у которого:
15. Степень окисления серы в данной реакции 3 F2 + S = SF6 равно:
16. Степень окисления кислорода в данной реакции O2 + S =SO2 равно:
17. Способны окислять сложные вещества:
18. Азот в реакции с кислород проявляет свойства:
- как окислительные, так и восстановительные
19. Какая соль относится к сильным окислителям:
тест-20. Формулой хлората калия является:
21. К окислительным свойствам неметаллов относится:
- взаимодействие неметаллов друг с другом на примере азота
- восстановление сложных веществ
+ взаимодействие неметаллов с металлами
22. К восстановительным свойствам неметаллов относится:
- окисление неметаллов сложных веществ
- взаимодействие неметаллов с металлами
+ восстановление сложных веществ
23. В каком году получил хлорат калия Клод Луи Бертолле:
24. В каком ряду представлены простые вещества – неметаллы:
+ кислород, озон, азот
- железо, ртуть, хлор
- никель, алмаз, кальций
25. Взаимодействие аммиака с хлороводородом является реакцией:
26. Самым легким газом является:
27. Неметаллы, имеющие наибольшую электроотрицательность находятся:
- в левом нижнем углу в Периодической системе Менделеева
- в левом верхнем углу в Периодической системе Менделеева
+ в правом верхнем углу в Периодической системе Менделеева
28. Валентность фтора в соединениях:
29. В качестве топлива в транспортной промышленности используется:
тест_30. Неметалл, который используют в пищевой промышленности для продления сроков годности:
31. Металлический блеск из неметаллов имеют:
32. К аллотропным модификациям кислорода относится:
33. Специфический запах жженных спичек обусловлен выделением:
34. При взаимодействии Cl2 + KOH в обычных условиях продуктом реакции является:
35. При взаимодействии Cl2 + KOH в условиях нагревания продуктом реакции является:
36. Данным образом выглядит:
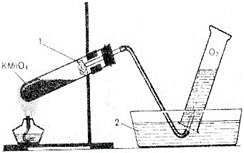
+ установка для получения и сбора кислорода
- установка для окисления перманганата калия
- установка для качественной реакции на кислород
37. На данном изображении представлен:
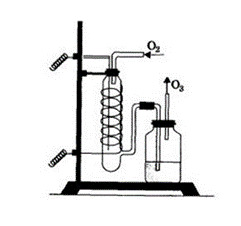
- способ получения кислорода из озона
- окисление озона до кислорода и воды
38. При какой длине волны происходит распад озона?
+ от пятьсот восьмидесяти до шестьсот пятидесяти
- от четырехсот сорока до пятьсот тридцати
- от семьсот девяноста пяти до восемьсот семидесяти
39. Глауберова соль в медицине используется в качестве:
Тесты по химии 11 класс. Тема: "Металлы"
1. В какой группе находится металл полоний:
2. К четвертой группе относится элемент:
3. Как проходит условная граница между между металлическими и неметаллическими элементами:
4. Металлургический процесс включает в себя:
+ восстановление ионов металла
- окисление ионов неметалла
- восстановление ионов неметалла
5. Пирометаллургией является:
+ процесс получения металлов из их соединений при высокой температуре
- процесс получения неметаллов из их соединений при низкой температуре
- процесс получения неметаллов из их соединений при высокой температуре
6. В пирометаллургии используются:
- как восстановители, так и окислители
7. При алюмотермии используют металл:
8. В гидрометаллургии получают:
+ металлы из растворов их соединений
- неметаллы из растворов их соединений
- воду из растворов их соединений
9. В электрометаллургии используется процесс:
- обработка при предельно высокой температуре
- реакция замещения и соединения
тест 10. При электролизе восстановителем является:
11. Чем определяются физические свойства металлов:
+ типом кристаллической решетки
- количеством протонов, электронов, нейтронов
- расположением в определенной группе или подгруппе
12. Отличием атомов металлов от неметаллов можно назвать:
+ содержат небольшое количество электронов на внешнем уровне, большой радиус и низкая электроотрицательность
- содержат большое количество электронов на внешнем энергетическом уровне, маленький радиус и высокая электроотрицательность
- содержат большое количество электронов на внешнем энергетическом уровне, большой радиус и высокая электроотрицательность
13. Металлической является связь:
+ между ионами металлов
- между ионами неметаллов
- между ионами металла и неметалла
14. Для какого агрегатного состояния не характерна металлическая связь:
- для жидкого состояния
- для твердого состояния
15. Чем обусловлена электропроводность металлов?
+ наличием свободных электронов
- наличием свободных нейтронов
- наличием свободных протонов
16. С повышением температуры электропроводность:
- может как повышаться, так и понижаться
17. Электропроводность увеличивается от:
+ ртути к серебру
- алюминия к цинку
18. Максимальной теплопроводностью обладает:
19. Наиболее пластичным металлом называют:
тест-20. Твердым веществом при нормальных условиях не является:
21. Самым твердым металлом является:
- щелочно – земельные металлы
22. Самым тяжелым металлом является:
23. Самым тугоплавким металлом является:
24. К черным металлам можно отнести:
25. Какие степени окисления имеют металлы:
- как положительные, так и отрицательные
26. Металлы в соединениях проявляют свойства:
- окислительно – восстановительные свойства
27. Какая закономерность уменьшения восстановительных свойств металлов:
+ слева направо, снизу-вверх
- справа налево, сверху вниз
28. На данном изображении представлена:
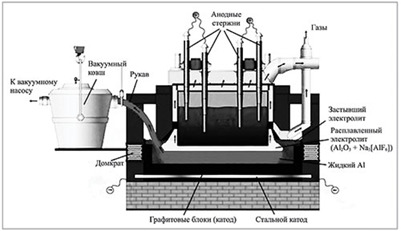
+ схема получения алюминия электролизом
- схема получения железа электролизом
- схема получения гидроксида алюминия электролизом
29. Чем левее находится металл в ряду, тем:
+ больше его восстановительная способность
- меньше его восстановительная способность
- больше его окислительная способность
тест_30. Лантаноиды на внешнем энергетическом уровне содержат по:
31. Сколько примерно имеются металлов в периодической системе Менделеева:
+ более девяти ста
- менее восьми ста
- менее двадцати ста
32. Во сколько раз литий легче осмия:
+ в сорок пять раз
- в шестьдесят раз
- в семьдесят раз
33. Провода высоковольтных изготавливают из:
34. Бронза является сплавом:
- железа и алюминия
- вольфрама и серебра
35. На данном рисунке представлена:
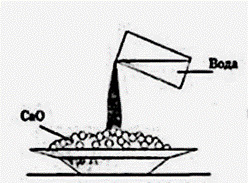
+ реакция гашения извести водой
- реакция соединения калия с хлором
- окисление перманганата калия
36. При взаимодействии с кислородом металлы образуют:
37. При взаимодействии щелочноземельных металлов с водой образуются:
- альдегиды и кетоны
38. Оксидом железа можно назвать:
39. В алюминотермии используется:
тест*40. Взаимодействие металлов с оксидами является реакцией:
Тесты по химии 8 класс. Тема: "Неметаллы. Простые вещества"
1. Какое количество химических элементов является неметаллами?
2. В стандартных условиях твёрдым веществом является:
3. Озон (см. рис.) – это …

- прозрачный бесцветный газ
+ аллотропная модификация О2
- обычный газ в стандартных условиях
4. Какое из суждений ложное?
- О2 – это бесцветный газ
- О3 имеет бледно-фиолетовый цвет
+ О2 имеет голубую окраску
5. Выберите ряд, в котором указаны только простые соединения-неметаллы:
6. Какое вещество является аллотропной формой О2?
7. В каком агрегатном состоянии могут находиться простые вещества-неметаллы в стандартных условиях?
+ все ответы верные
8. Какое место в периодической системе Д.И. Менделеева занимают неметаллы?
- всю периодическую таблицу
+ верхний угол справа
- I, II, III периоды
- нижний угол слева
9. Какому неметаллу присущ металлический блеск?
тест 10. Кристаллическая сера имеет … окраску.
11. Если сравнивать водород с гелием, то последний:
12. Какой показатель относится к физическим свойствам неметаллов?
- высокий показатель электропроводности
13. Какой неметалл наиболее активный?
14. Какие свойства характерны для азота в реакции с кислородом?
- и восстановительные, и окислительные
15. Какой газ используется при рекламном светопреставлении?
16. Какое максимальное количество электронов может размещаться на последнем энергетическом уровне у инертного химического элемента?
17. Аллотропными формами какого элемента являются алмаз и графит?
18. Какой оттенок имеет двухатомный газ F2?
19. У какого простого вещества-неметалла при освещении электропроводность в 1000 раз выше, нежели в темноте?
тест-20. При помощи какого типа химической связи образуются неметаллы?
21. При взаимодействии неметалла с металлом первому всегда принадлежит роль:
- и окислителя, и восстановителя
- не принадлежит никакая роль
22. Чему равно окислительное число S в реакции 3F2 + S = SF6?
23. Какой из газов самый лёгкий?
24. Кто впервые получил изотопы азота и натрия?

25. Какой тип кристаллической решётки характерный для простых веществ-неметаллов?
26. Чему равна валентность F в веществах?
27. Озон (О3) распадается при длине волны:
28. Выберите неметалл s-семейства:
29. Какое вещество-неметалл принято использовать в пищевой промышленности с целью продления сроков хранения?
тест_30. При взаимодействии H2 с Cl2 протекает химическая реакция:
Читайте также:
