Тест общие свойства металлов 11 класс
Обновлено: 04.07.2024
Тестовые задания по теме "Металлы" для подготовки к ЕГЭ (11 класс).
| Вложение | Размер |
|---|---|
| testy_metally_11kl.doc | 46 КБ |
Подтяните оценки и знания с репетитором Учи.ру
За лето ребенок растерял знания и нахватал плохих оценок? Не беда! Опытные педагоги помогут вспомнить забытое и лучше понять школьную программу. Переходите на сайт и записывайтесь на бесплатный вводный урок с репетитором.
Вводный урок бесплатно, онлайн, 30 минут
Предварительный просмотр:
11 класс. Тема Металлы
А1. В атоме хрома электронная конфигурация валентных электронов: А) 3d 2 4s 2 ; Б) 3s 2 3p 4 ;В) 3d 5 4s 1 ;Г) 4s 2 4p 6
А2.Самый большой радиус имеет атом: А) рубидия; Б) цезия; В) меди; Г) лития
А3. Абсолютно верно утверждение: А) только металлы имеют металлический блеск Б) все металлы - твёрдые вещества; В) атомы металлов и металлы - простые вещества; Г) только металлы электропроводны;.
А4. Вещество с металлической связью – это: А) NaCI; Б) CuSO 4 . 5H 2 O; В) HCI; Г) AI
А5. В порядке усиления металлических свойств элементы расположены в ряду: А) Na, Mg, AI, Si, P; Б) K, Na,Be,Ca, Mg; В) Li, Na, K, Rb, Cs; Г) Ba, Sr,Ca, Mg, AI
А6. Ряд, в котором все вещества реагируют с железом: А) HCI, CO 2 , CO; Б) CI 2 , CuCI 2 , HCI; В) H 2 , O 2 , CaO; Г) SiO 2 , HCI, S.
А7. При взаимодействии калия с водой образуются: А) гидроксид калия и водород; Б) оксид калия и водород; В) гидроксид калия и кислород; Г) только гидроксид калия
А8. Как изменяются свойства гидроксидов, образованных металлами II группы главной подгруппы, при увеличении заряда ядра атомов: А) щёлочи→нерастворимые основания→амфотерный гидроксид; Б) амфотерный гидроксид→нерастворимое основание→щёлочь; В) кислота→амфотерный гидроксид→щёлочь; Г) нерастворимое основание→щёлочь→кислота
А9. Что усиливает коррозию металлических деталей, находящихся в воде: А) добавление в воду ингибитора коррозии; Б) применение для соединения деталей заклёпок из более активного металла; В) применение для соединения деталей заклёпок из менее активного металла; Г) окрашивание деталей
А10. Кальций в промышленности получают: А) электролизом раствора CaCI 2 ; Б) электролизом расплава CaCI 2 ; В) реакцией восстановления; Г) действием более активного металла на водные растворы солей
А11. При электролизе раствора хлорида цинка на катоде происходит: А) восстановление катионов цинка; Б) восстановление воды; В) восстановление катионов цинка и воды; Г) окисление атомов хлора
А12. К микроэлементам относится; А) Fe; Б) Ca; В) K; Г) Mg
В1. Укажите порядковые номера элементов III периода, которые образуют соединения с металлической связью. Ответ________(номера запишите в порядке возрастания и без пробелов между цифрами)
В2. В атоме скандия число полностью заполненных подуровней равно_______(ответ запишите цифрами)
С1. Предложите 3 способа получения гидроксида калия. Ответ подтвердите уравнениями реакций.
С2. При электролизе раствора хлорида меди (II) на аноде выделилось 8,96 л. газа. Какое вещество выделилось на катоде? Найдите его массу.
А1.Химический элемент расположен в IV периоде; I группе А. Распределению электронов в атоме этого элемента соответствует: А) 2,8,8,2; Б) 2,8,18,1; В) 2,8,8,1; Г) 2,8,18,2
А2. В порядке уменьшения атомного радиуса химические элементы расположены в ряду: А) Li, Be, B, C; Б) Be, Mg, Ca, Sr; В) Si, AI, Mg, Na; Г) Li, Na, K, Rb
А3. Какие физические свойства не являются общими для всех металлов: А) электропроводность; Б) теплопроводность; В) твёрдое агрегатное состояние при стандартных условиях; Г) металлический блеск
А4. Кристаллическая решётка вещества железа: А) атомная; Б) молекулярная; В) ионная; Г) металлическая.
А5. Восстановительные свойства элементов усиливаются в ряду: А) K, Na, Li;
Б) Na, Mg, AI; В) Na, Be, Mg; Г) Be, Mg, Ca
А6. Кальций реагирует (по отдельности) со всеми веществами набора: А) Mg, H 2 O, Na 2 CO 3 , CO; Б) H 2 , KOH, CO 2 , H 2 O; В) O 2 , HCI, H 2 O, Br 2 ; Г) Br 2 , CaCO 3 , O 2 , CO
А7. Все металлы какого ряда реагируют с соляной кислотой; А) цинк, железо, кобальт; Б) железо, алюминий, платина; В) никель, хром, золото; Г) олово, магний, ртуть
А8. Гидроксид какого металла обладает наименее основными свойствами: А) лития; Б) калия; В) берилия; Г) кальция.
А9. Какой из компонентов загрязнённого воздуха является наиболее коррозионно-активным по отношению к металлам при повышенной влажности воздуха: А) CO 2 ; Б) SO 2 ; В) N 2 ; Г) CO
А10. Какой восстановитель не используют в металлургическом производстве: А) оксид углерода (II); Б) водород; В) алюминий; Г) нет правильного ответа
А11. При электролизе раствора нитрата серебра на катоде выделяется: А) серебро; Б) водород; В) серебро и водород; Г) кислород и водород
А12. Самый распространённый на Земле переходный элемент: А) Cu; Б) Fe; В) AI; Г) Ti
В1. Запишите порядковый номер элемента, у которого электроны внешнего уровня распределены по орбиталям следующим образом: …3s 2 3p 1
В2. Запишите номер периода, в котором нет элементов, образующих вещества с металлической связью. Ответ___________(запишите цифрами)
С1. Предложите 3 способа получения хлорида алюминия. Ответ подтвердите уравнениями реакций
С2. При электролизе раствора нитрата ртути (II) на катоде выделилось 60,3 г. ртути. Какой газ выделился на аноде? Найдите его объём.
Тестовая работа по теме "Металлы" (11 класс)
А) Ca Б) М g В) Sr Г) Fe .
13.Тип связи в простом веществе натрия:
Б) ковалентная неполярная
В) металлическая
Г) ковалентная полярная
14. Наиболее ярко выраженные металлические свойства
проявляет:
А) Mg Б) K В) Al Г) Ca
15. Какую электронную конфигурацию имеет атом наиболее
активного металла?
А) 1 s 2 2 s 2 2 p 11 Б) 1 s 2 2 s 2 2 p 6 3 s 1
В) 1 s 2 2 s 2 Г) 1 s 2 2 s 2 2 p 6 3 s 2 3 p 1
16. Алюмотермия - это
А) восстановление алюминия водородом из его оксида
Б) восстановление металлов из оксидов алюминием
В) шлифовка алюминиевых изделий
Г) получение алюминиевых сплавов
ТЕСТ №2 по теме «Металлы»
1. Какому металлу соответствует электронная формула
1 s 2 2 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 10 ?
А) Mo Б) Zn
В) Ba Г) Fe
2. При взаимодействии железа с разбавленной H 2 SO 4 образуется
3.Какой металл не вытеснит водород из разбавленной H 2 SO 4 ?
А) Fe Б) Cr В) Cu Г) Zn
4.В порядке уменьшения восстановительных свойств металлы расположены в ряду:
А ) Al, Zn, Fe Б ) Al, Na, K
В ) Fe, Zn, Mg Г ) Fe, Zn, Al
5.Оксиды CrO и CrO 3 -
А) основные
Б) основные и кислотные
В) кислотные
Г) кислотные и основные
6.К какому типу элементов относится железо?
А) р - элементам
Б) s -элементам
В) d -элементам
Г) f -элементам
7. На d - подуровне максимально может находиться:
А) 2е Б) 6е В)10е Г) 18е
8. Металлический хром может взаимодействовать с:
А) H 2 О Б) HCl (разб.)
В) HNO 3 (конц.) Г) NaOH (конц.)
9. Для металлов не характерно следующее физическое свойство:
А) теплопроводность
Б) металлический блеск
В) электропроводность
Г) хрупкость
10.Установите соответствии между металлом и способом его получения
А) Na 1. алюмотермия
Б) Fe 2. восстановление углеродом
В) Cr 3 . электролиз расплавов солей
11. С точки зрения типа кристаллической решетки «лишнее» простое вещество среди данных
А) алмаз В) железо
Б) хром Г) кобальт
12.Электронная формула иона Fe +2
А) 1 s 2 2 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 6
Б) 1 s 2 2 s 2 2 p 6 3 s 2 3 p 6 4 s 0 3 d 10
В) 1 s 2 2 s 2 2 p 6 3 s 2 3 p 6 4 s 0 3 d 6
Г) 1 s 2 2 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 10
13. Свойства оксидов металлов побочных подгрупп с уменьшением степени окисления металла изменяются в следующем порядке
А) основные, амфотерные, кислотные
Б) кислотные, амфотерные, основные
В) основные, кислотные, амфотерные
Г) кислотные, основные, амфотерные
14. В схеме превращения
веществами X и Y соответственно являются
В) Fe и HCl
15. В схеме превращения
веществами X 1 , X 2 , X 3 соответственно являются
Тест общие свойства металлов 11 класс
Тесты по химии 11 класс. Тема: "Металлы"
Правильный вариант ответа отмечен знаком +
1. В какой группе находится металл полоний:
2. К четвертой группе относится элемент:
3. Как проходит условная граница между между металлическими и неметаллическими элементами:
4. Металлургический процесс включает в себя:
+ восстановление ионов металла
- окисление ионов неметалла
- восстановление ионов неметалла
5. Пирометаллургией является:
+ процесс получения металлов из их соединений при высокой температуре
- процесс получения неметаллов из их соединений при низкой температуре
- процесс получения неметаллов из их соединений при высокой температуре
6. В пирометаллургии используются:
- как восстановители, так и окислители
7. При алюмотермии используют металл:
8. В гидрометаллургии получают:
+ металлы из растворов их соединений
- неметаллы из растворов их соединений
- воду из растворов их соединений
9. В электрометаллургии используется процесс:
- обработка при предельно высокой температуре
- реакция замещения и соединения
тест 10. При электролизе восстановителем является:
11. Чем определяются физические свойства металлов:
+ типом кристаллической решетки
- количеством протонов, электронов, нейтронов
- расположением в определенной группе или подгруппе
12. Отличием атомов металлов от неметаллов можно назвать:
+ содержат небольшое количество электронов на внешнем уровне, большой радиус и низкая электроотрицательность
- содержат большое количество электронов на внешнем энергетическом уровне, маленький радиус и высокая электроотрицательность
- содержат большое количество электронов на внешнем энергетическом уровне, большой радиус и высокая электроотрицательность
13. Металлической является связь:
+ между ионами металлов
- между ионами неметаллов
- между ионами металла и неметалла
14. Для какого агрегатного состояния не характерна металлическая связь:
- для жидкого состояния
- для твердого состояния
15. Чем обусловлена электропроводность металлов?
+ наличием свободных электронов
- наличием свободных нейтронов
- наличием свободных протонов
16. С повышением температуры электропроводность:
- может как повышаться, так и понижаться
17. Электропроводность увеличивается от:
+ ртути к серебру
- алюминия к цинку
18. Максимальной теплопроводностью обладает:
19. Наиболее пластичным металлом называют:
тест-20. Твердым веществом при нормальных условиях не является:
21. Самым твердым металлом является:
- щелочно – земельные металлы
22. Самым тяжелым металлом является:
23. Самым тугоплавким металлом является:
24. К черным металлам можно отнести:
25. Какие степени окисления имеют металлы:
- как положительные, так и отрицательные
26. Металлы в соединениях проявляют свойства:
- окислительно – восстановительные свойства
27. Какая закономерность уменьшения восстановительных свойств металлов:
+ слева направо, снизу-вверх
- справа налево, сверху вниз
28. На данном изображении представлена:
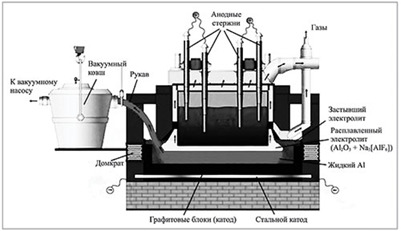
+ схема получения алюминия электролизом
- схема получения железа электролизом
- схема получения гидроксида алюминия электролизом
29. Чем левее находится металл в ряду, тем:
+ больше его восстановительная способность
- меньше его восстановительная способность
- больше его окислительная способность
тест_30. Лантаноиды на внешнем энергетическом уровне содержат по:
31. Сколько примерно имеются металлов в периодической системе Менделеева:
+ более девяти ста
- менее восьми ста
- менее двадцати ста
32. Во сколько раз литий легче осмия:
+ в сорок пять раз
- в шестьдесят раз
- в семьдесят раз
33. Провода высоковольтных изготавливают из:
34. Бронза является сплавом:
- железа и алюминия
- вольфрама и серебра
35. На данном рисунке представлена:
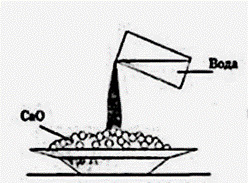
+ реакция гашения извести водой
- реакция соединения калия с хлором
- окисление перманганата калия
36. При взаимодействии с кислородом металлы образуют:
37. При взаимодействии щелочноземельных металлов с водой образуются:
- альдегиды и кетоны
38. Оксидом железа можно назвать:
39. В алюминотермии используется:
тест*40. Взаимодействие металлов с оксидами является реакцией:
Тесты по химии 9 класс. Тема: "Металлы"
3. Как проходит условная граница между металлическими и неметаллическими элементами:
+ слева направо, снизу вверх
28. Легкому окислению поддаются:
35. Кто изображен на данной фотографии:

Тесты по химии 11 класс. Тема: "Неметаллы"
1. Неметаллы – это:
+ химические элементы, которые могут проявлять свойства как окислителя (принимают электроны), так и восстановителя (отдают электроны)
- химические элементы, которые проявляют свойства только окислителя (принимают электроны)
- химические элементы, которые проявляют свойства только восстановителя (отдают электроны)
2. Сколько химических элементов относятся к неметаллам:
3. За счет каких связей образованы простые вещества - неметаллы:
+ ковалентных неполярных связей
- ковалентных полярных связей
4. Неметалл, являющийся газом при нормальных условиях:
5. Неметалл, являющийся летучей жидкостью при нормальных условиях:
6. Неметалл, являющийся твердым веществом при нормальных условиях:
7. К физическим свойствам неметаллов относится:
- наличие металлический блеска
8. При освещении данный неметалл проводит электрический ток в тысячу раз больше, чем в темноте:
9. Какую окраску имеет фтор?
тест 10. Цвет кристаллической серы:
11. Наибольшие окислительные свойства проявляет:
12. Наибольшие восстановительные свойства проявляет:
13. В реакции взаимодействия между металлом и неметаллом последний всегда выполняет роль:
- не выполняет какой-либо роли
14. При взаимодействии неметаллов между собой в роли окислителя выступает тот неметалл, у которого:
15. Степень окисления серы в данной реакции 3 F2 + S = SF6 равно:
16. Степень окисления кислорода в данной реакции O2 + S =SO2 равно:
17. Способны окислять сложные вещества:
18. Азот в реакции с кислород проявляет свойства:
- как окислительные, так и восстановительные
19. Какая соль относится к сильным окислителям:
тест-20. Формулой хлората калия является:
21. К окислительным свойствам неметаллов относится:
- взаимодействие неметаллов друг с другом на примере азота
- восстановление сложных веществ
+ взаимодействие неметаллов с металлами
22. К восстановительным свойствам неметаллов относится:
- окисление неметаллов сложных веществ
- взаимодействие неметаллов с металлами
+ восстановление сложных веществ
23. В каком году получил хлорат калия Клод Луи Бертолле:
24. В каком ряду представлены простые вещества – неметаллы:
+ кислород, озон, азот
- железо, ртуть, хлор
- никель, алмаз, кальций
25. Взаимодействие аммиака с хлороводородом является реакцией:
26. Самым легким газом является:
27. Неметаллы, имеющие наибольшую электроотрицательность находятся:
- в левом нижнем углу в Периодической системе Менделеева
- в левом верхнем углу в Периодической системе Менделеева
+ в правом верхнем углу в Периодической системе Менделеева
28. Валентность фтора в соединениях:
29. В качестве топлива в транспортной промышленности используется:
тест_30. Неметалл, который используют в пищевой промышленности для продления сроков годности:
31. Металлический блеск из неметаллов имеют:
32. К аллотропным модификациям кислорода относится:
33. Специфический запах жженных спичек обусловлен выделением:
34. При взаимодействии Cl2 + KOH в обычных условиях продуктом реакции является:
35. При взаимодействии Cl2 + KOH в условиях нагревания продуктом реакции является:
36. Данным образом выглядит:
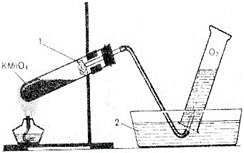
+ установка для получения и сбора кислорода
- установка для окисления перманганата калия
- установка для качественной реакции на кислород
37. На данном изображении представлен:
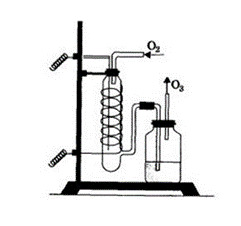
- способ получения кислорода из озона
- окисление озона до кислорода и воды
38. При какой длине волны происходит распад озона?
+ от пятьсот восьмидесяти до шестьсот пятидесяти
- от четырехсот сорока до пятьсот тридцати
- от семьсот девяноста пяти до восемьсот семидесяти
39. Глауберова соль в медицине используется в качестве:
Читайте также:
