Титан это легкий металл или тяжелый
Обновлено: 04.05.2024

Титан – лёгкий прочный металл серебристо-белого цвета. Существует в двух кристаллических модификациях: α-Ti с гексагональной плотноупакованной решёткой, β-Ti с кубической объёмно-центрированной упаковкой, температура полиморфного превращения α↔β 883 °C.Титан и титановые сплавы сочетают легкость, прочность, высокую коррозийную стойкость, низкий коэффициент теплового расширения, возможность работы в широком диапазоне температур.
СТРУКТУРА
Кристаллическая структура кристалла
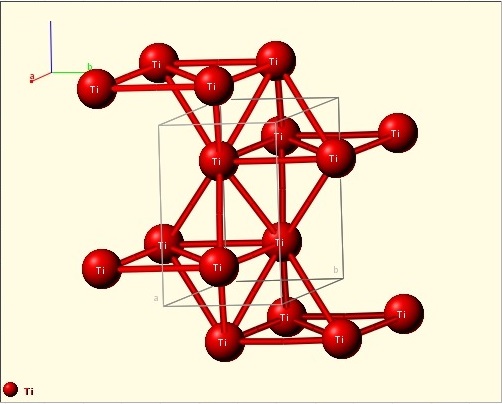
Титан имеет две аллотропические модификации. Низкотемпературная модификация, существующая до 882 °C, имеет гексагональную плотноупакованную решетку с периодами а = 0,296 нм и с = 0,472 нм. Высокотемпературная модификация имеет решетку объемноцентрированного куба с периодом а = 0,332 нм.
Полиморфное превращение (882 °C) при медленном охлаждении происходит по нормальному механизму с образованием равноосных зерен, а при быстром охлаждении – по мартенситному механизму с образованием игольчатой структуры.
Титан обладает высокой коррозионной и химической стойкостью благодаря защитной окисной пленке на его поверхности. Он не корродирует в пресной и морской воде, минеральных кислотах, царской водке и др.
СВОЙСТВА

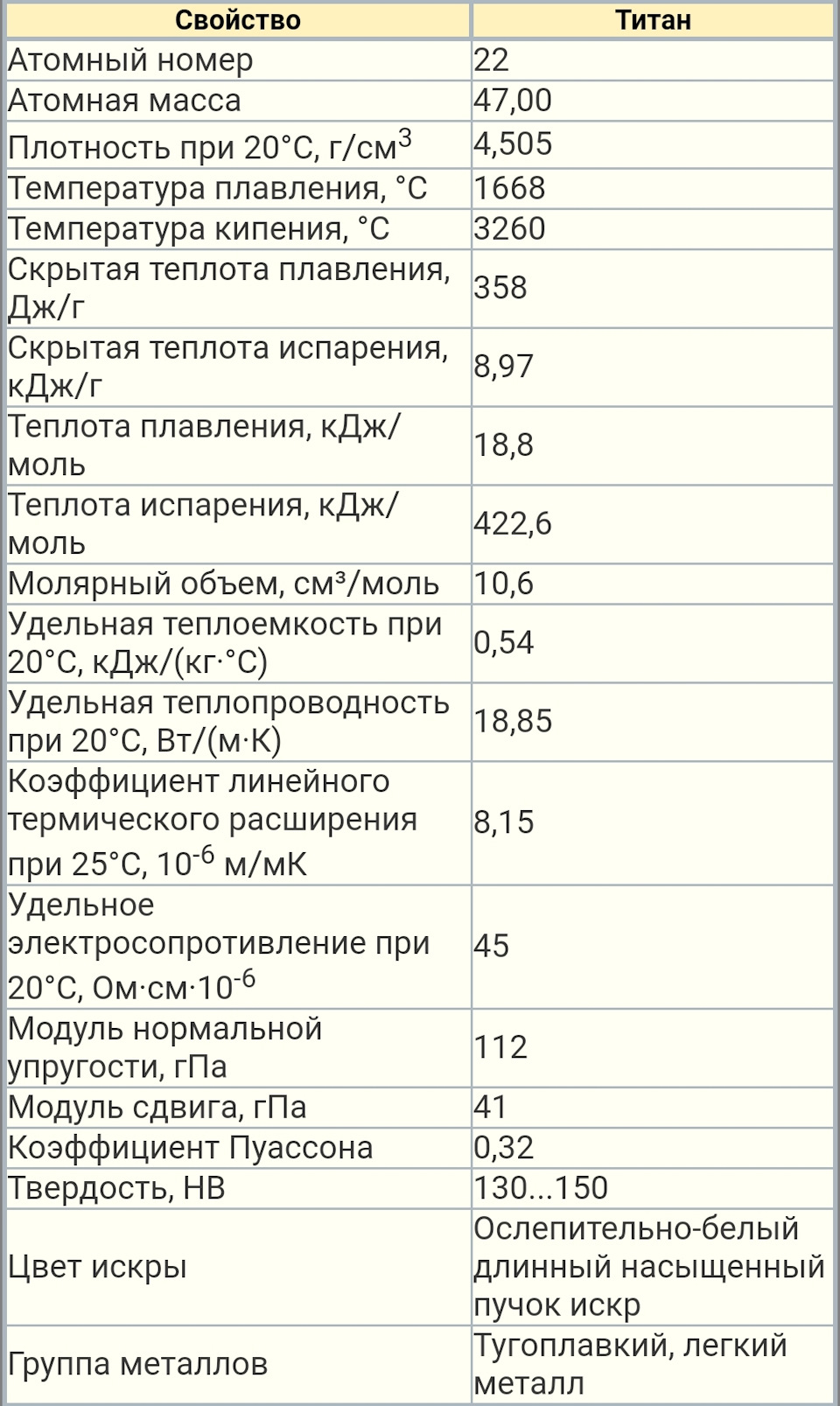
Точка плавления 1671 °C, точка кипения 3260 °C, плотность α-Ti и β-Ti соответственно равна 4,505 (20 °C) и 4,32 (900 °C) г/см³, атомная плотность 5,71×1022 ат/см³. Пластичен, сваривается в инертной атмосфере.
Применяемый в промышленности технический титан содержит примеси кислорода, азота, железа, кремния и углерода, повышающие его прочность, снижающие пластичность и влияющие на температуру полиморфного превращения, которое происходит в интервале 865-920 °С. Для технического Титана марок ВТ1-00 и ВТ1-0 плотность около 4,32 г/см 3 , предел прочности 300-550 Мн/м 2 (30-55кгс/мм 2 ), относительное удлинение не ниже 25%, твердость по Бринеллю 1150-1650 Мн/м 2 (115-165 кгс/мм 2 ). Является парамагнетиком. Конфигурация внешней электронной оболочки атома Ti 3d24s2.
Имеет высокую вязкость, при механической обработке склонен к налипанию на режущий инструмент, и поэтому требуется нанесение специальных покрытий на инструмент, различных смазок.
При обычной температуре покрывается защитной пассивирующей пленкой оксида TiO2, благодаря этому коррозионностоек в большинстве сред (кроме щелочной). Титановая пыль имеет свойство взрываться. Температура вспышки 400 °C.
ЗАПАСЫ И ДОБЫЧА

Основные руды: ильменит (FeTiO3), рутил (TiO2), титанит (CaTiSiO5).
На 2002 год, 90 % добываемого титана использовалось на производство диоксида титана TiO2. Мировое производство диоксида титана составляло 4,5 млн т. в год. Подтвержденные запасы диоксида титана (без России) составляют около 800 млн т. На 2006 год, по оценке Геологической службы США, в пересчёте на диоксид титана и без учёта России, запасы ильменитовых руд составляют 603—673 млн т., а рутиловых — 49.7—52.7 млн т. Таким образом, при нынешних темпах добычи мировых разведанных запасов титана (без учёта России) хватит более чем на 150 лет.
Россия обладает вторыми в мире, после Китая, запасами титана. Минерально-сырьевую базу титана России составляют 20 месторождений (из них 11 коренных и 9 россыпных), достаточно равномерно рассредоточенных по территории страны. Самое крупное из разведанных месторождений находится в 25 км от города Ухта (Республика Коми). Запасы месторождения оцениваются в 2 миллиарда тонн.
Концентрат титановых руд подвергают сернокислотной или пирометаллургической переработке. Продукт сернокислотной обработки — порошок диоксида титана TiO2. Пирометаллургическим методом руду спекают с коксом и обрабатывают хлором, получая пары тетрахлорида титана их при 850 °C восстанавливают магнием.
Полученную титановую «губку» переплавляют и очищают. Ильменитовые концентраты восстанавливают в электродуговых печах с последующим хлорированием возникающих титановых шлаков.
ПРОИСХОЖДЕНИЕ

Титан находится на 10-м месте по распространённости в природе. Содержание в земной коре — 0,57 % по массе, в морской воде — 0,001 мг/л. В ультраосновных породах 300 г/т, в основных — 9 кг/т, в кислых 2,3 кг/т, в глинах и сланцах 4,5 кг/т. В земной коре титан почти всегда четырёхвалентен и присутствует только в кислородных соединениях. В свободном виде не встречается. Титан в условиях выветривания и осаждения имеет геохимическое сродство с Al2O3. Он концентрируется в бокситах коры выветривания и в морских глинистых осадках.
Перенос титана осуществляется в виде механических обломков минералов и в виде коллоидов. До 30 % TiO2 по весу накапливается в некоторых глинах. Минералы титана устойчивы к выветриванию и образуют крупные концентрации в россыпях. Известно более 100 минералов, содержащих титан. Важнейшие из них: рутил TiO2, ильменит FeTiO3, титаномагнетит FeTiO3 + Fe3O4, перовскит CaTiO3, титанит CaTiSiO5. Различают коренные руды титана — ильменит-титаномагнетитовые и россыпные — рутил-ильменит-цирконовые.
Месторождения титана находятся на территории ЮАР, России, Украины, Китая, Японии, Австралии, Индии, Цейлона, Бразилии, Южной Кореи, Казахстана. В странах СНГ ведущее место по разведанным запасам титановых руд занимает РФ (58.5%) и Украина (40.2%).
ПРИМЕНЕНИЕ

Изделия из титана
Титановые сплавы играют большую роль в авиационной технике, где стремятся получить наиболее легкую конструкцию в сочетании с необходимой прочностью. Титан легок по сравнению с другими металлами, но в то же время может работать при высоких температурах. Из титановых сплавов изготовляют обшивку, детали крепления, силовой набор, детали шасси, различные агрегаты. Также данные материалы применяются в конструкциях авиационных реактивных двигателей. Это позволяет уменьшить их массу на 10-25%. Из титановых сплавов производят диски и лопатки компрессора, детали воздухозаборника и направляющего аппарата, крепеж.
Также титан и его сплавы используют в ракетостроении. Ввиду кратковременной работы двигателей и быстрого прохождения плотных слоев атмосферы в ракетостроении в значительной мере снимаются проблемы усталостной прочности, статической выносливости и отчасти ползучести.
Технический титан из-за недостаточно высокой теплопрочности не пригоден для применения в авиации, но благодаря исключительно высокому сопротивлению коррозии в ряде случаев незаменим в химической промышленности и судостроении. Так его применяют при изготовлении компрессоров и насосов для перекачки таких агрессивных сред, как серная и соляная кислота и их соли, трубопроводов, запорной арматуры, автоклав, различного рода емкостей, фильтров и т.п. Только титан обладает коррозионной стойкостью в таких средах, как влажный хлор, водные и кислые растворы хлора, поэтому из данного металла изготовляют оборудование для хлорной промышленности. Из титана делают теплообменники, работающие в коррозионно активных средах, например в азотной кислоте (не дымящей). В судостроении титан используется для изготовления гребных винтов, обшивки морских судов, подводных лодок, торпед и т.д. На титан и его сплавы не налипают ракушки, которые резко повышают сопротивление судна при его движении.
Титановые сплавы перспективны для использования во многих других применениях, но их распространение в технике сдерживается высокой стоимостью и дефицитностью титана.
Титан – полезные свойства и особенности металла
Этот металл – один из самых распространенных на планете. Его значение для человека неоценимо: титан стал «дублером» поврежденных зубов и суставов. У него есть фанаты, стремящиеся заменить все свои кости титановыми.

Что представляет собой
Титан – элемент периодической системы Менделеева №22. Международное обозначение – Titanium (Ti).
Это блестящий серебристый металл. Легок, прочен, устойчив к коррозии.
По составу представляет собой конгломерат пяти стабильных изотопов.
История открытия
История открытия металла связана с именами нескольких ученых:
- В конце 18 века немец Мартин Клапрот и англичанин Уильям Грегор одновременно открыли диоксид вещества.
- Через десять лет их компанию пополнил француз Луи-Николя Воклен.
- К середине 19 века Иенс Берцелиус получил металлический титан.
- Еще через сто лет материал повышенной чистоты выделили голландцы.
Название нового вещества предложил Клапрот: по учрежденной им традиции химик назвал открытый элемент именем персонажа греческой мифологии.
Титаны – это дети главных богов греческого пантеона Зевса и Геи. То есть второе поколение богов.
Физико-химические характеристики
Свойства металла хорошо изучены:
- Легко реагирует с кислотами даже малой концентрации.
- Это тугоплавкий металл: температура плавления – 1670°C. Для вскипания требуется вдвое больше.
- Пластичен, хрупкость обретает на морозе (-80°C).
- На прочность влияет степень очистки, но не температура.
- При комнатной температуре покрывается оксидной пленкой, что делает его устойчивым к коррозии (исключая щелочи).
- При обычном давлении существует два вида титана с разными типами решеток: высоко- и низкотемпературный.
Легкость, почти невесомость – главное свойство, по которому титан легко отличить от других металлов.
| Свойства атома | |
|---|---|
| Название, символ, номер | Тита́н / Titanium (Ti), 22 |
| Атомная масса (молярная масса) | 47,867(1) а. е. м. (г/моль) |
| Электронная конфигурация | [Ar] 3d2 4s2 |
| Радиус атома | 147 пм |
| Химические свойства | |
| Ковалентный радиус | 132 пм |
| Радиус иона | (+4e)68 (+2e)94 пм |
| Электроотрицательность | 1,54 (шкала Полинга) |
| Электродный потенциал | −1,63 |
| Степени окисления | 2, 3, 4 |
| Энергия ионизации (первый электрон) | 657,8 (6,8281) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
| Плотность (при н. у.) | 4,54 г/см³ |
| Температура плавления | 1670 °C 1943 K |
| Температура кипения | 3560 K |
| Уд. теплота плавления | 18,8 кДж/моль |
| Уд. теплота испарения | 422,6 кДж/моль |
| Молярная теплоёмкость | 25,1 Дж/(K·моль) |
| Молярный объём | 10,6 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | гексагональная плотноупакованная (α-Ti) |
| Параметры решётки | a=2,951 с=4,697 (α-Ti) |
| Отношение c/a | 1,587 |
| Температура Дебая | 380 K |
| Прочие характеристики | |
| Теплопроводность | (300 K) 21,9 Вт/(м·К) |
| Номер CAS | 7440-32-6 |
Из-за повышенной вязкости механическая обработка металла затруднена. Этот недостаток устраняют, смазывая инструмент специальными составами.
Технология получения
Технический прогресс частично отразился на способе получения металла.
Сегодня титан получают двумя методами:
- Процесс Кролла. Один из основных, предложен в 1940 году ученым из Люксембурга Гийомом Кроллом. Заключается в восстановлении металлического титана магнием при высоких температурах. Комбинаты, вырабатывающее такое сырье, именуются титано-магниевыми.
- FFC Cambridge. Новацией является электрохимическая технология. Она предполагает прямое восстановление металла из оксида в расплавленной смеси хлорида и оксида кальция. Процесс назван по именам разработчиков, сотрудников Кембриджского университета Фрэя, Фартинга, Чена.
Цена продукта доступна: титан разной степени очистки на мировых биржах торгуют по $5,7 – 6,1 за кг.
Месторождения, добыча
Месторождения равномерно распределены по планете. Российские залежи рассредоточены по всей территории страны (20 рудников). Крупнейшее – на севере, в Республике Коми.
Добыча ведется традиционным способом, но предполагает использование средств защиты от пыли.
Мировые резервы руды оцениваются триллионом тонн. При нынешних темпах добычи титанового сырья хватит на полтора столетия.
Присутствие в природе
В природе титан представлен оксидами разных химических элементов (более ста). В свободном виде не встречается.
Не считается редким металлом: содержание в породах исчисляется килограммами на тонну (от 2,3 до 9).
Это девятый по распространенности элемент земной коры – более полупроцента по массе.
Больше всего его в бокситах и морской осадочной глине.
Породы плохо выветриваются, образуя крупные россыпи.
Где используется
Титан так же прочен, как сталь, но вполовину легче. Он вдвое превосходит по прочности алюминий, но тяжелее всего на 60%. Этими достоинствами обусловлено использование человеком титана как металла.
Промышленность
Титановые сплавы – конструкционный материал номер один для строителей ракет, самолетов, океанских лайнеров. Чаще их выполняют из сплавов с другими металлами (особенно никелем и алюминием).

Заготовка титанового шпангоута истребителя F-15 до и после прессования на штамповочном прессе компании Alcoa усилием 45 тыс. тонн, май 1985
Титан легче других металлов, но способен работать при высоких температурах.
Есть и другие области применения металла:
- Трубы, насосы, другое оборудование для работы с агрессивными жидкостями.
- Военно-промышленный комплекс – бронированные жилеты, корпусы субмарин, детали ракет, самолетов.
- Установки для опреснения воды, очистки воздуха.
- Исходник при производстве целлюлозы, бумаги.
- Детали автомобилей, сельхозтехники, оборудование пищепрома.
- Спортивный инвентарь.

Более половины соединений вещества забирают производители лаков и красок. Это, например, титановые белила.

Все больше продукции из титана припадает на IT-сферу: корпус, начинка мобильных телефонов, других гаджетов.
Медицина
Прочный металл дружелюбен к процессам, протекающим в организме человека. Поэтому его активно задействуют как материал протезов конечностей, зубных имплантов. Медицина ценит его свойство безболезненно сращиваться с костной тканью. Поэтому титан относится к металлам будущего.
Безопасность для тканей организма человека сделала возможным применение металла для пирсинга.
Другие сферы
Из титана изготавливают корпусы часов класса люкс. Это материал ювелирных изделий.

Часы из титанового сплава
Нитридом вещества «золотят» купола храмов, предметы декора. Четырехвалентный хлорид «создает» дымовую завесу и дымчатость стекла.
Пищевая добавка Е171 – это белый диоксид титана (TiO2), пищевой краситель.
Марки и сплавы
Номенклатура титановых сплавов насчитывает десятки позиций.
Самый востребованный – с алюминием и ванадием, 6% и 4% соответственно. На его производство тратится половина добываемого сырья.
Второй по популярности – ферротитан (соотношение титан-железо – 1:3). В черной металлургии это средство для очистки стали от примесей.
Чаще всего выплавляются следующие марки титана:
Это технический материал, без легирующих присадок. В нем минимум примесей: содержание Ti (%) – 99,24+.
Предостережение
Металлическое вещество безопасно. Опасность исходит от титановой пыли: она провоцирует онкологию. Это проблема людей, работающих на добыче руды, и металлургов.
Кроме того, титановая пыль – потенциальное взрывчатое вещество.
ТИТАН — супермен среди металлов
Титаном назвали металл не зря. Имя принадлежит мифологическим древнегреческим божествам, олицетворявшим силу и мощь природы. Герой статьи делится своей силой с человеком.
Кто открыл суперметалл
История открытия рядовая. Химик и священник Грегор обнаружил оксид неизвестного металла, и дал ему название «менакеновая земля».

Чуть позже немецкий химик Клапрот, исследуя минерал рутил, обнаружил в нем новый элемент, который назвал титаном.
Интересно: Клапрот ранее открыл новый элемент, и назвал его ураном. Это имя в греческой мифологии принадлежало отцу титанидов.
Чистый титан удалось получить талантливому исследователю Берцелиусу.
Свойства титана

Титан относится к металлам; в периодической таблице Менделеева имеет № 22; он легкий, прочный, устойчив к коррозии. Внешне (цветом) похож на алюминий или нержавеющую сталь.
- На воздухе образует на поверхности оксидную пленку.
- Имеет высокую химическую и коррозионную стойкость (благодаря защитной оксидной пленке).
- Имеет две аллотропные модификации: низкотемпературная (существует до температуры 882°С) и высокотемпературная.
- Обладает парамагнитными свойствами.
- Титан образует с другими металлами интерметаллические соединений, его добавляют в сплавы.
Титановая пыль взрывается, а его стружка пожароопасна.
Металл образует с карбидами тугоплавкие высокотвердые соединения.
| Свойства атома | |
|---|---|
| Название, символ, номер | Тита́н / Titanium (Ti), 22 |
| Атомная масса (молярная масса) | 47,867(1)[1] а. е. м. (г/моль) |
| Электронная конфигурация | [Ar] 3d2 4s2 |
| Радиус атома | 147 пм |
| Химические свойства | |
| Ковалентный радиус | 132 пм |
| Радиус иона | (+4e)68 (+2e)94 пм |
| Электроотрицательность | 1,54 (шкала Полинга) |
| Электродный потенциал | −1,63 |
| Степени окисления | 2, 3, 4 |
| Энергия ионизации (первый электрон) | 657,8 (6,8281[2]) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
| Плотность (при н. у.) | 4,54 г/см³ |
| Температура плавления | 1670 °C 1943 K |
| Температура кипения | 3560 K |
| Уд. теплота плавления | 18,8 кДж/моль |
| Уд. теплота испарения | 422,6 кДж/моль |
| Молярная теплоёмкость | 25,1[3] Дж/(K·моль) |
| Молярный объём | 10,6 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | гексагональная плотноупакованная (α-Ti) |
| Параметры решётки | a=2,951 с=4,697 (α-Ti) |
| Отношение c/a | 1,587 |
| Температура Дебая | 380 K |
| Прочие характеристики | |
| Теплопроводность | (300 K) 21,9 Вт/(м·К) |
| Номер CAS | 7440-32-6 |
Месторождения
Титан называют редким металлом, что не совсем верно. По запасам титансодержащих руд элемент занимает 10 место.
Известно больше 100 таких руд. Среди них:
- рутил;
- титаномагнетит;
- ильменит;
- титанит.
Месторождения титансодержащих руд:
Добыча и переработка
Титан получают из концентрата титансодержащих руд методами пирометаллургии или сернокислотной переработки.
Концентраты из ильменитовых руд плавят в электродуговых печах.
При необходимости черновой металл рафинируют.
Марки титана и виды изделий
Виды выпускаемых титановых изделий:
Сплавы
Титановые сплавы по областям применения делятся на деформируемые и литейные.
| Марка сплава | Присадки |
| ВТ3-1 | Ti, Al, Cr, Mo, Fe, S |
| ВТ5-1 | Ti-Al-Sn |
| ПТ-7М | Ti-Al-Zr |
| ОТ4-1 | Ti-Al-Mn |
| ВТ18 | Ti-Al-Zr-Mo-Nb-Si |
| ВТ14 | Ti-A1-Мо-V |
Достоинства сплавов — сочетание высокой коррозионной стойкости с жаропрочностью и хорошей удельной прочностью.
Плюсы и минусы металла и его сплавов
Достоинства титановых сплавов:
- Соотношение прочность-плотность у титановых сплавов почти в 2 раза лучше, чем у легированных сталей.
- Высокая механическая прочность.
- Отличная коррозионная стойкость, что позволяет изделиям работать в агрессивных средах.

К недостаткам титановых сплавов можно отнести:
- Высокая цена (титан гораздо дороже многих цветных металлов).
- При обработке металла и его сплавов возникает проблема налипания, что грозит быстрым износом режущих инструментов.
- Сложности при сварке титановых изделий.
Область применения титановых изделий широка, хотя может ограничиваться ценовой составляющей.

Заготовка титанового шпангоута истребителя F-15 до и после прессования на штамповочном прессе компании Alcoa усилием 45 тыс. тонн, май 1985
Есть случаи, когда титановые сплавы — единственные, которые возможно использовать в конкретных условиях.
- Надежность продукции из титана проверялась на гоночных автомобилях.
- Металл и его сплавы незаменимы в ракето- и судостроении, химической, энергетической промышленности.
- Титановые соединения востребованы в производстве конденсаторов турбин, труб для перекачки агрессивных жидкостей, сосудов высокого давления.
- Перспективная область применения титановых сплавов — оборудование для глубокого и сверхглубокого бурения.
- Не обходятся без титановых изделий оборонная и военная промышленности.

Стоимость металла
Цена титана в порошке ПТМ-1 7500 рублей за килограмм (на 25.07.2020).

Мне 42 года и я специалист в области минералогии. Здесь на сайте я делюсь информацией про камни и их свойства — задавайте вопросы и пишите комментарии!
Титан

Титан — химический элемент с атомным номером 22. Принадлежит к 4-й группе периодической таблицы химических элементов (по устаревшей короткой форме периодической системы принадлежит к побочной подгруппе IV группы, или к группе IVB), находится в четвёртом периоде таблицы. Атомная масса элемента 47,867(1) а. е. м . Обозначается символом Ti. Простое вещество титан — лёгкий прочный металл серебристо-белого цвета. Обладает высокой коррозионной стойкостью.
Содержание
- 1 История
- 2 Происхождение названия
- 3 Нахождение в природе
- 4 Месторождения
- 5 Запасы и добыча
- 6 Получение
- 7 Физические свойства
- 7.1 Изотопы
- 9.1 В чистом виде и в виде сплавов
- 9.2 В виде соединений
- 9.3 Анализ рынков потребления
- 9.4 Цены
![Титан]()
История
Открытие диоксида титана (TiO2) сделали практически одновременно и независимо друг от друга англичанин У. Грегор и немецкий химик М. Г. Клапрот. У. Грегор, исследуя состав магнитного железистого песка (Крид, Корнуолл, Англия, 1791), выделил новую «землю» (оксид) неизвестного металла, которую назвал менакеновой. В 1795 году немецкий химик Клапрот открыл в минерале рутиле новый элемент и назвал его титаном. Спустя два года Клапрот установил, что рутил и менакеновая земля — оксиды одного и того же элемента, за которым и осталось название «титан», предложенное Клапротом. Через 10 лет открытие титана состоялось в третий раз: французский учёный Л. Воклен обнаружил титан в анатазе и доказал, что рутил и анатаз — идентичные оксиды титана.
Первый образец металлического титана получил в 1825 году швед Й. Я. Берцелиус. Из-за высокой химической активности титана и сложности его очистки чистый образец Ti получили голландцы А. ван Аркел и И. де Бур в 1925 году термическим разложением паров иодида титана TiI4.
Титан не находил промышленного применения, пока люксембуржец Г. Кролл в 1940 году не запатентовал простой магниетермический метод восстановления металлического титана из тетрахлорида; этот метод процесс Кролла до настоящего времени остаётся одним из основных в промышленном получении титана.
Происхождение названия
Металл получил своё название в честь титанов, персонажей древнегреческой мифологии, детей Геи. Название элементу дал Мартин Клапрот в соответствии со своими взглядами на химическую номенклатуру в противовес французской химической школе, где элемент старались называть по его химическим свойствам. Поскольку немецкий исследователь сам отметил невозможность определения свойств нового элемента только по его оксиду, он подобрал для него имя из мифологии, по аналогии с открытым им ранее ураном.
Нахождение в природе
Титан находится на 10-м месте по распространённости в природе. Содержание в земной коре — 0,57 % по массе, в морской воде — 0,001 мг/л . В ультраосновных породах 300 г/т , в основных — 9 кг/т , в кислых 2,3 кг/т , в глинах и сланцах 4,5 кг/т . В земной коре титан почти всегда четырёхвалентен и присутствует только в кислородных соединениях. В свободном виде не встречается. Титан в условиях выветривания и осаждения имеет геохимическое сродство с Al2O3. Он концентрируется в бокситах коры выветривания и в морских глинистых осадках. Перенос титана осуществляется в виде механических обломков минералов и в виде коллоидов. До 30 % TiO2 по весу накапливается в некоторых глинах. Минералы титана устойчивы к выветриванию и образуют крупные концентрации в россыпях. Известно более 100 минералов, содержащих титан. Важнейшие из них: рутил TiO2, ильменит FeTiO3, титаномагнетит FeTiO3 + Fe3O4, перовскит CaTiO3, титанит (сфен) CaTiSiO5. Различают коренные руды титана — ильменит-титаномагнетитовые и россыпные — рутил-ильменит-цирконовые.
Крупные коренные месторождения титана находятся на территории ЮАР, России, Украины, Канады, США, Китая, Норвегии, Швеции, Египта, Австралии, Индии, Южной Кореи, Казахстана; россыпные месторождения имеются в Бразилии, Индии, США, Сьерра-Леоне, Австралии. В странах СНГ ведущее место по разведанным запасам титановых руд занимает РФ (58,5 %) и Украина (40,2 %). Крупнейшее месторождение в России — Ярегское.
По данным на 2002 год, 90 % добываемого титана использовалось на производство диоксида титана TiO2. Мировое производство диоксида титана составляло 4,5 млн т. в год. Подтверждённые запасы диоксида титана (без России) составляют около 800 млн т. На 2006 год, по оценке Геологической службы США, в пересчёте на диоксид титана и без учёта России, запасы ильменитовых руд составляют 603—673 млн т., а рутиловых — 49,7—52,7 млн т. Таким образом, при нынешних темпах добычи мировых разведанных запасов титана (без учёта России) хватит более чем на 150 лет.
Россия обладает вторыми в мире, после Китая, запасами титана. Минерально-сырьевую базу титана России составляют 20 месторождений (из них 11 коренных и 9 россыпных), достаточно равномерно рассредоточенных по территории страны. Самое крупное из разведанных месторождений (Ярегское) находится в 25 км от города Ухта (Республика Коми). Запасы месторождения оцениваются в 2 миллиарда тонн руды со средним содержанием диоксида титана около 10 %.
Крупнейший в мире производитель титана — российская компания «ВСМПО-АВИСМА».
Получение
![Титан]()
Брусок кристаллического титана (чистота 99,995 %, вес ≈283 г, длина ≈14 см, диаметр ≈25 мм), изготовленный на заводе «Уралредмет» иодидным методом ван Аркеля и де Бура
Как правило, исходным материалом для производства титана и его соединений служит диоксид титана со сравнительно небольшим количеством примесей. В частности, это может быть рутиловый концентрат, получаемый при обогащении титановых руд. Однако запасы рутила в мире весьма ограничены, и чаще применяют так называемый синтетический рутил или титановый шлак, получаемые при переработке ильменитовых концентратов. Для получения титанового шлака ильменитовый концентрат восстанавливают в электродуговой печи, при этом железо отделяется в металлическую фазу (чугун), а невосстановленные оксиды титана и примесей образуют шлаковую фазу. Богатый шлак перерабатывают хлоридным или сернокислотным способом.
Концентрат титановых руд подвергают сернокислотной или пирометаллургической переработке. Продукт сернокислотной обработки — порошок диоксида титана TiO2. Пирометаллургическим методом руду спекают с коксом и обрабатывают хлором, получая пары тетрахлорида титана TiCl4:
Образующиеся пары TiCl4 при 850 °C восстанавливают магнием:
Кроме этого, в настоящее время начинает получать популярность так называемый процесс FFC Cambridge, названный по именам его разработчиков Дерека Фрэя, Тома Фартинга и Джорджа Чена из Кембриджского университета, где он был создан. Этот электрохимический процесс позволяет осуществлять прямое непрерывное восстановление титана из оксида в расплаве смеси хлорида кальция и негашёной извести (оксида кальция). В этом процессе используется электролитическая ванна, наполненная смесью хлорида кальция и извести, с графитовым расходуемым (либо нейтральным) анодом и катодом, изготовленным из подлежащего восстановлению оксида. При пропускании через ванну тока температура быстро достигает ~1000—1100 °C, и расплав оксида кальция разлагается на аноде на кислород и металлический кальций:
Полученный кислород окисляет анод (в случае использования графита), а кальций мигрирует в расплаве к катоду, где и восстанавливает титан из его оксида:
Образующийся оксид кальция вновь диссоциирует на кислород и металлический кальций, и процесс повторяется вплоть до полного преобразования катода в титановую губку либо исчерпания оксида кальция. Хлорид кальция в данном процессе используется как электролит для придания электропроводности расплаву и подвижности активным ионам кальция и кислорода. При использовании инертного анода (например, диоксида олова), вместо углекислого газа на аноде выделяется молекулярный кислород, что меньше загрязняет окружающую среду, однако процесс в таком случае становится менее стабильным, и, кроме того, в некоторых условиях более энергетически выгодным становится разложение хлорида, а не оксида кальция, что приводит к высвобождению молекулярного хлора.
Полученную титановую «губку» переплавляют и очищают. Рафинируют титан йодидным способом или электролизом, выделяя Ti из TiCl4. Для получения титановых слитков применяют дуговую, электронно-лучевую или плазменную переработку.
Физические свойства
Титан — лёгкий серебристо-белый металл. При нормальном давлении существует в двух кристаллических модификациях: низкотемпературный α -Ti с гексагональной плотноупакованной решёткой (гексагональная сингония, пространственная группа C6mmc, параметры ячейки a = 0,2953 нм , c = 0,4729 нм , Z = 2 ) и высокотемпературный β -Ti с кубической объёмно-центрированной упаковкой (кубическая сингония, пространственная группа Im3m, параметры ячейки a = 0,3269 нм , Z = 2 ), температура перехода α↔β 883 °C, теплота перехода ΔH =3,8 кДж/моль (87,4 кДж/кг). Большинство металлов при растворении в титане стабилизируют β -фазу и снижают температуру перехода α↔β . При давлении выше 9 ГПа и температуре выше 900 °C титан переходит в гексагональную фазу ( ω -Ti). Плотность α -Ti и β -Ti соответственно равна 4,505 г/см³ (при 20 °C) и 4,32 г/см³ (при 900 °C). Атомная плотность α-титана 5,67⋅10 22 ат/см³ .
Температура плавления титана при нормальном давлении равна 1670 ± 2 °C, или 1943 ± 2 К (принята в качестве одной из вторичных калибровочных точек температурной шкалы ITS-90. Температура кипения 3287 °C. При достаточно низкой температуре (-80 °C), титан становится довольно хрупким. Молярная теплоёмкость при нормальных условиях Cp = 25,060 кДж/(моль·K) , что соответствует удельной теплоёмкости 0,523 кДж/(кг·K) . Теплота плавления 15 кДж/моль , теплота испарения 410 кДж/моль . Характеристическая дебаевская температура 430 К . Теплопроводность 21,9 Вт/(м·К) при 20 °C. Температурный коэффициент линейного расширения 9,2·10 −6 К −1 в интервале от −120 до +860 °C. Молярная энтропия α -титана S 0 = 30,7 кДж/(моль·К). Для титана в газовой фазе энтальпия формирования ΔH 0
f = 473,0 кДж/моль , энергия Гиббса ΔG 0
f = 428,4 кДж/моль , молярная энтропия S 0 = 180,3 кДж/(моль·К) , теплоёмкость при постоянном давлении Cp = 24,4 кДж/(моль·K)Удельное электрическое сопротивление при 20 °C составляет 0,58 мкОм·м (по другим данным 0,42 мкОм·м), при 800 °C 1,80 мкОм·м. Температурный коэффициент сопротивления 0,003 К −1 в диапазоне 0…20 °C.
Пластичен, сваривается в инертной атмосфере. Прочностные характеристики мало зависят от температуры, однако сильно зависят от чистоты и предварительной обработки. Для технического титана твёрдость по Виккерсу составляет 790—800 МПа , модуль нормальной упругости 103 ГПа , модуль сдвига 39,2 ГПа . У высокочистого предварительно отожжённого в вакууме титана предел текучести 140—170 МПа, относительное удлинение 55—70 %, твёрдость по Бринеллю 716 МПа .
При обычной температуре покрывается защитной пассивирующей плёнкой оксида TiO2, благодаря этому коррозионностоек в большинстве сред (кроме щелочной).
Температура перехода в сверхпроводящее состояние 0,387 К. При температурах выше 73 кельвин титан парамагнитен. Магнитная восприимчивость при 20 °C составляет 3,2·10 −6 . Постоянная Холла α -титана равна +1,82·10 −13 .
Изотопы
Известны изотопы титана с массовыми числами от 38 до 63 (количество протонов 22, нейтронов от 16 до 41), и 2 ядерных изомера.
Природный титан состоит из смеси пяти стабильных изотопов: 46 Ti (изотопная распространенность 7,95 %), 47 Ti (7,75 %), 48 Ti (73,45 %), 49 Ti (5,51 %), 50 Ti (5,34 %).
Среди искусственных изотопов самые долгоживущие 44 Ti (период полураспада 60 лет) и 45 Ti (период полураспада 184 минуты).
Химические свойства
Устойчив к коррозии благодаря оксидной плёнке, но при измельчении в порошок, а также в тонкой стружке или проволоке титан пирофорен. Титановая пыль имеет свойство взрываться. Температура вспышки — 400 °C. Титановая стружка пожароопасна.
Титан устойчив к разбавленным растворам многих кислот и щелочей (кроме HF, H3PO4 и концентрированной H2SO4). Титан устойчив к влажному хлору и водным растворам хлора.
Легко реагирует даже со слабыми кислотами в присутствии комплексообразователей, например, с плавиковой кислотой HF он взаимодействует благодаря образованию комплексного аниона [TiF6] 2− . Титан наиболее подвержен коррозии в органических средах, так как в присутствии воды на поверхности титанового изделия образуется плотная пассивная плёнка из оксидов и гидрида титана. Наиболее заметное повышение коррозионной стойкости титана заметно при повышении содержания воды в агрессивной среде с 0,5 до 8,0 %, что подтверждается электрохимическими исследованиями электродных потенциалов титана в растворах кислот и щелочей в смешанных водно-органических средах.
При нагревании на воздухе до 1200 °C Ti загорается ярким белым пламенем с образованием оксидных фаз переменного состава TiOx. Из растворов солей титана осаждается гидроксид TiO(OH)2·xH2O, осторожным прокаливанием которого получают оксид TiO2. Гидроксид TiO(OH)2·xH2O и диоксид TiO2 амфотерны.
TiO2 взаимодействует с серной кислотой при длительном кипячении. При сплавлении с содой Na2CO3 или поташом K2CO3 оксид TiO2 образует титанаты:
При нагревании Ti взаимодействует с галогенами (например, с хлором — при 550 °C). Тетрахлорид титана TiCl4 при обычных условиях — бесцветная жидкость, сильно дымящая на воздухе, что объясняется гидролизом TiCl4, содержащимися в воздухе парами воды и образованием мельчайших капелек HCl и взвеси гидроксида титана.
Восстановлением TiCl4 водородом, алюминием, кремнием, другими сильными восстановителями, получен трихлорид и дихлорид титана TiCl3 и TiCl2 — твёрдые вещества, обладающие сильными восстановительными свойствами. Ti взаимодействует с Br2 и I2.
С азотом N2 выше 400 °C титан образует нитрид TiNx (x = 0.58—1.00). Титан — единственный элемент, который горит в атмосфере азота.
При взаимодействии титана с углеродом образуется карбид титана TiCx (x = 0.49—1.00).
При нагревании Ti поглощает H2 с образованием соединения переменного состава TiHx (x = 2.00—2.98). При нагревании эти гидриды разлагаются с выделением H2.
Титан образует сплавы и интерметаллические соединения со многими металлами.
📚Всё, что необходимо знать о металле ТИТАН (Ti)…
![]()
-Титан обладает высокой прочностью, хорошей коррозионной стойкостью и при этом имеет сравнительно небольшую массу, что делает его применение незаменимым в областях, где важны хорошие механические свойства изделий одновременно с их массой. На странице представлено описание данного металла: физические, химические свойства, области применения, марки и его сплавов, виды продукции.
Основные сведения:
-Титан — химический элемент с порядковым номером 22, атомный вес 47,88, легкий серебристо-белый металл. Плотность 4,51 г/см3, Tпл=1668+(-)5 °С, Tкип=3260 °С. Данный материал сочетает легкость, прочность, высокую коррозионную стойкость, низкий коэффициент теплового расширения, возможность работы в широком диапазоне температур.История открытия:
-Оксид титана TiO2 впервые был обнаружен в 1789 году английским ученым, специалистом в области минералогии У. Грегором, который при исследовании магнитного железистого песка выделил окись неизвестного металла, назвав ее менакеновой. Первый образец металлического титана получил в 1825 году шведский химик и минераловед Й. Я. Берцелиус.Свойства титана:
-В периодической системе элементов Д. И. Менделеева Ti расположен в IV группе 4-го периода под номером 22. В важнейших и наиболее устойчивых соединениях металл четырехвалентен. По внешнему виду похож на сталь. Титан относится к переходным элементам. Данный металл плавится при довольно высокой температуре (1668±4 °С) и кипит при 3300 °С, скрытая теплота плавления и испарения почти в два раза больше, чем у железа. Известны две аллотропические модификации титана (две разновидности данного металла, имеющие одинаковый химический состав, но различное строение и свойства). Низкотемпературная альфа-модификация, существующая до 882,5 °С и высокотемпературная бетта-модификация, устойчивая от 882,5 °С и до температуры плавления. По плотности и удельной теплоемкости титан занимает промежуточное место между двумя основными конструкционными металлами: алюминием и железом. Стоит также отметить, что его механическая прочность примерно вдвое больше, чем чистого железа, и почти в шесть раз выше, чем алюминия. Но указанный материал может активно поглощать кислород, азот и водород, которые резко снижают пластические свойства металла. С углеродом титан образует тугоплавкие карбиды, обладающие высокой твердостью. Титан обладает низкой теплопроводностью, которая в 13 раз меньше теплопроводности алюминия и в 4 раза — железа. Коэффициент термического расширения при комнатной температуре сравнительно мал, с повышением температуры он возрастает. Модули упругости титана невелики и обнаруживают существенную анизотропию. Модули упругости характеризуют способность материала упруго деформироваться при приложении к нему силы. Анизотропия заключается в различии свойств упругости в зависимости от направления действия силы. С повышением температуры до 350 °С модули упругости уменьшаются почти по линейному закону. Небольшое значение модулей упругости Ti — существенный его недостаток, т.к. в некоторых случаях для получения достаточно жестких конструкций приходится применять большие сечения изделий по сравнению с теми, которые следуют из условий прочности. Титан имеет довольно высокое удельное электросопротивление, которое в зависимости от содержания примесей колеблется в пределах от 42·10-8 до 80·10-6 Ом·см. При температурах ниже 0,45 К он становится сверхпроводником. Титан — парамагнитный металл. Обычно у парамагнитных веществ магнитная восприимчивость при нагревании уменьшается. Магнитная восприимчивость характеризует связь между намагниченностью вещества и магнитным полем в этом веществе. Данный материал составляет исключение из этого правила — его восприимчивость существенно увеличивается с температурой.Физические и механические свойства:
![]()
Химические свойства:
![]()
Достоинства / недостатки:
— Достоинства:
-малая плотность (4500 кг/м3) способствует уменьшению массы выпускаемых изделий;
-высокая механическая прочность. Стоит отметить, что при повышенных температурах (250-500 °С) титановые -сплавы по прочности превосходят высокопрочные сплавы алюминия и магния;
-необычайно высокая коррозионная стойкость, обусловленная способностью Ti образовывать на поверхности -тонкие (5-15 мкм) сплошные пленки оксида ТiO2, прочно связанные с массой металла;
-удельная прочность (отношение прочности и плотности) лучших титановых сплавов достигает 30-35 и более, что почти вдвое превышает удельную прочность легированных сталей.
— Недостатки:
-высокая стоимость производства, Ti значительно дороже железа, алюминия, меди, магния;
-активное взаимодействие при высоких температурах, особенно в жидком состоянии, со всеми газами, -составляющими атмосферу, в результате чего Ti и его сплавы можно плавить лишь в вакууме или в среде инертных газов;
-трудности вовлечения в производство титановых отходов;
-плохие антифрикционные свойства, обусловленные налипанием Ti на многие материалы; титан в паре с титаном вообще не может работать на трение;
-высокая склонность Ti и многих его сплавов к водородной хрупкости и солевой коррозии;
-плохая обрабатываемость резанием, аналогичная обрабатываемости нержавеющих сталей аустенитного класса;
-большая химическая активность, склонность к росту зерна при высокой температуре и фазовые превращения при сварочном цикле вызывают трудности при сварке титана.Области применения:
-Основная часть титана расходуется на нужды авиационной и ракетной техники и морского судостроения. Его, а также ферротитан используют как легирующую добавку к качественным сталям и как раскислитель. Технический титан идет на изготовление емкостей, химических реакторов, трубопроводов, арматуры, насосов, клапанов и других изделий, работающих в агрессивных средах. Из компактного титана изготавливают сетки и другие детали электровакуумных приборов, работающих при высоких температурах. По использованию в качестве конструкционного материала Ti находится на 4-ом месте, уступая лишь Al, Fe и Mg. Алюминиды титана являются очень стойкими к окислению и жаропрочными, что в свою очередь определило их использование в авиации и автомобилестроении в качестве конструкционных материалов. Биологическая безвредность данного металла делает его превосходным материалом для пищевой промышленности и восстановительной хирургии. Титан и его сплавы нашли широкое применение в технике ввиду своей высокой механической прочности, которая сохраняется при высоких температурах, коррозионной стойкости, жаропрочности, удельной прочности, малой плотности и прочих полезных свойств. Высокая стоимость данного металла и материалов на его основе во многих случаях компенсируется их большей работоспособностью, а в некоторых случаях они являются единственным сырьем, из которого можно изготовить оборудование или конструкции, способные работать в данных конкретных условиях. Титановые сплавы играют большую роль в авиационной технике, где стремятся получить наиболее легкую конструкцию в сочетании с необходимой прочностью. Ti легок по сравнению с другими металлами, но в то же время может работать при высоких температурах. Из материалов на основе Ti изготавливают обшивку, детали крепления, силовой набор, детали шасси, различные агрегаты. Также данные материалы применяются в конструкциях авиационных реактивных двигателей. Это позволяет уменьшить их массу на 10-25%. Из титановых сплавов производят диски и лопатки компрессоров, детали воздухозаборников и направляющих в двигателях, различный крепеж. Еще одной областью применения является ракетостроение. Ввиду кратковременной работы двигателей и быстрого прохождения плотных слоев атмосферы в ракетостроении в значительной мере снимаются проблемы усталостной прочности, статической выносливости и отчасти ползучести. Технический титан из-за недостаточно высокой тепловой прочности не пригоден для применения в авиации, но благодаря исключительно высокому сопротивлению коррозии в ряде случаев незаменим в химической промышленности и судостроении. Так его применяют при изготовлении компрессоров и насосов для перекачки таких агрессивных сред, как серная и соляная кислота и их соли, трубопроводов, запорной арматуры, автоклав, различного рода емкостей, фильтров и т. п. Только Ti обладает коррозионной стойкостью в таких средах, как влажный хлор, водные и кислые растворы хлора, поэтому из данного металла изготовляют оборудование для хлорной промышленности. Также из него делают теплообменники, работающие в коррозионно активных средах, например в азотной кислоте (не дымящей). В судостроении титан используется для изготовления гребных винтов, обшивки морских судов, подводных лодок, торпед и т.д. На данный материал не налипают ракушки, которые резко повышают сопротивление судна при его движении. Титановые сплавы перспективны для использования во многих других применениях, но их распространение в технике сдерживается высокой стоимостью и недостаточной распространенностью данного металла. Соединения титана также получили широкое применение в различных отраслях промышленности. Карбид (TiC) обладает высокой твердостью и применяется в производстве режущих инструментов и абразивных материалов. Белый диоксид (TiO2) используется в красках (например, титановые белила), а также при производстве бумаги и пластика. Титанорганические соединения (например, тетрабутоксититан) применяются в качестве катализатора и отвердителя в химической и лакокрасочной промышленности. Неорганические соединения Ti применяются в химической электронной, стекловолоконной промышленности в качестве добавки. Диборид (TiB2)- важный компонент сверхтвердых материалов для обработки металлов. Нитрид (TiN) применяется для покрытия инструментов.-Удачной Вам эксплуатации и спасибо за внимание! Надеюсь, что помог Вам!
-С уважением DrPavlov.Читайте также: