Тяжелые металлы в реке
Обновлено: 03.07.2024

В природе тяжелые металлы (ТМ) находятся, в основном, в труднорастворимой и труднодоступной для растений форме. Однако, в результате антропогенного вмешательства, резко возрастает содержание ТМ в природных экосистемах — в воздухе, природных водах и почве. Одновременно изменяется и форма нахождения ТМ в природных средах — в составе относительно хорошо растворимых соединений, что позволяет им с легкостью вовлекаться в пищевые цепи [8].
Тяжелые металлы обладают высокой способностью к многообразным химическим, физико-химическим и биологическим реакциям. Многие из них имеют переменную валентность и участвуют в окислительно-восстановительных процессах. Тяжелые металлы и их соединения, как и другие химические соединения, способны перемещаться и перераспределяться в средах жизни, т. е. мигрировать [3].
В ряду тяжелых металлов одни крайне необходимы для жизнеобеспечения человека и других живых организмов и относятся к так называемым биогенным элементам. Другие вызывают противоположный эффект и, попадая в живой организм, приводят к его отравлению или гибели. Эти металлы относят к классу ксенобиотиков, то есть чуждых живому. Специалистами по охране окружающей среды среди металлов-токсикантов выделена приоритетная группа [5]. В нее входят кадмий, медь, мышьяк, никель, ртуть, свинец, цинк и хром как наиболее опасные для здоровья человека и животных. Из них ртуть, свинец и кадмий наиболее токсичны.
Город Сумгаит является вторым по величине промышленным городом Азербайджана. В нем сосредоточены предприятия химической, металлургической промышленности, предприятия оргсинтеза. В настоящее время в Сумгаите имеются приблизительно 3000 стационарных источников атмосферного загрязнения. Отходы этих предприятий содержат тяжелые металлы, органические соединения.
Особую озабоченность вызывают ртутные загрязнения завода по производству хлор-алкилина, различные хлорсодержащие соединения нефтехимических отраслей, фтороводород, содержащийся в выбросах алюминиевого производства, тяжелые металлы — свинец, цинк, кадмий в составе пыли сталелитейного производства и т. д.
Донные отложения вблизи Сумгаита содержат 1–2 г углеводородов, 0,5–1,0 г фенолов и 0,1- 0,6 г ртути на кг. С биологической точки зрения, эти области дна рассматриваются фактически мертвыми, воздействуя на осетра и другую рыбу, которая кормится фауной морского дна [1]. Несмотря на снижение производственных мощностей и сворачивание многих производств, накопленные в окружающей среде токсичные вещества продолжают воздействовать на здоровье населения Сумгаита.
Город Сумгаит находится в бассейне одноименной реки Сумгаитчай, имеющей несколько притоков — Гозлучай, Гуздучай, Чигилчай, Ченгичай и Кендачай. Сумгаитчай относится к «временным» рекам, так как в летний период из-за отсутствия атмосферных осадков практически полностью пересыхает. Ее длина составляет 198 км, площадь бассейна — 1751 км 2 . Она на 90 % питается дождевыми водами [7]. Впадает непосредственно в Каспийское море недалеко от Сумгаита.
С целью экологического оценивания нами исследовано содержание тяжелых металлов — Cd(II), Hg(II), Pb(II) в морской воде и донных отложениях Каспийского моря вблизи Сумгаита, а также в пробах речной воды Сумгаитчая и всех его притоков методом ААС [2]. Исследования проводились на ААС ZEEnit 700 P.
Для исследования были взяты пробы промышленных и бытовых сточных вод, выбрасываемых в море, а также пробы морской воды и донных отложений вблизи Сумгаита. Результаты анализа проб промышленных и бытовых сточных вод представлены в таблице 1.
Содержание тяжелых металлов впробах промышленных источных вод Сумгаита, мкг/л
Определение тяжелых металлов в пробах воды, взятых из реки Араз

Река Араз — является 2-й магистральной артерией Азербайджана, длина — 1072 км, площадь бассейна 102 тыс. км 2 , берёт начало с 2990 м высоты Бингёлького хребта Турции, в основном питается подземными водами (46 %), снеговыми (38 %) и дождевыми (16 %) осадками. На территории Сабирабада Араз сливаясь с Курой впадает в Каспийское море. К Аразу на территории Нахичеванской АР примешиваются воды рек Нахичевань, Джахри, Арна, Элинджа, Ордубад и Гилан, а на юго- восточных склонах Малых Кавказских гор примешиваются воды рек Хекери, Бергушад, Кёнделен, Охчучай и Гуручай.
Река Араз на протяжении 600 км составляет государственную границу между Турцией, Азербайджаном и Ираном. Начиная от гидроузла Бахрамтапа до устья реки, она течет по территории Азербайджана. Слева в реку Араз присоединяется Ахурчай, Зангичай, Арпачай, Нахчиванчай, Алинджачай, Охчучай, Акаричай, (Баргушадчай), Кендаланчай и др., справа — больше 100 маленьких рек, а в долине Кура Аракса на протяжении 100 км в реку Араз не впадает ни одна река. Река Араз имеет большое экономическое значение. Река используется для обеспечения водой населения, в оросительных целях, для получения энергии, в расширении рыбного промысла. С целью эффективного её использования на реке построен гидроузел Араз (Нахичеванское водохранилище), Миль-Муганский и Бахрамтапинский гидроузлы.
Воды Араза постоянно загрязняются, при протекании через территорию Армении. В последнее время выявлено, что отбросы ртути, радиоактивные отходы Армянской АЭС и залежи полезных ископаемых, чрезвычайно опасные для человеческого здоровья, умышленно вливаются в Араз.
В 2005-м году была создана региональная лаборатория с целью контроля уровня транспограничного в Бейлаганском районе (для Араза). Сильному антропогенному воздействию подвергается река Араз и ее притоки, протекающие по территории Армении. В водах реки Араз наблюдается превышение в сто раз нормы по меди, молибдену и прочим тяжелым металлам. В результате этого в водах реки микрофлора и фауна исчезает, процесс самоочищения остановлен, речной бассейн превратился в «мертвую зону». Если учесть, что 80 % населения использует в питьевых и сельскохозяйственных целях загрязненную речную воду, то можно представить, какая опасность возникает для здоровья людей и экологической системы в целом. Большая часть населения проживает в Кура-Аразской низменности и получает воду из Куры и Араза.
Результаты проб воды, взятые в реке Охчучай, впадающей в Араз, выявили высокое содержание в ней тяжелых металлов — меди, молибдена, марганца, железа, цинка, хрома. По данным мониторинга, проведенного в январе-марте этого года, содержание никеля в этих реках было в 7 раз выше нормы, железа — в 4 раза, а медно-молибденового соединения — в 2 раза. Высокое содержание тяжелых металлов губит не только речную фауну, но и крайне опасно для здоровья человека. Использование такой воды может иметь пагубные последствия — от расстройств ЖКТ, деструктивных процессов в почках и костной ткани до расстройств сердечно-сосудистой, нервной и кроветворной систем организма [1–3].
Основная цель исследования — определить количество тяжелых металлов в пробах естественной речной воды, взятой из реки Араз (Ордубад и Джульфа), проходящей через Нахчыванскую Автономную Республику, и провести сравнительный анализ. Определение тяжелых металлов в пробах природной воды из реки Араз было проведено с помощью прибора Agilent 7500 Series ICP-MS. На рис. показаны градуировочные графики определения тяжелых металлов масс-спектрометрическим методом.
Результаты анализа обработаны методом математической статистики. Как видно из градуировочных графиков, содержание тяжелых металлов было определено с высокой точностью. Результаты проведенных исследований показаны в таблице 1.
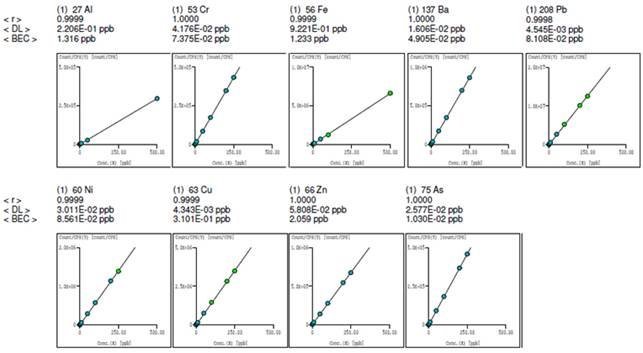
Рис. 1. Градуировочные графики определения тяжелых металлов
Количество тяжелых металлов в пробах воды, взятых из Ордубадского и Джульфинского районов реки Араз
Анализ особенностей накопления и распределения тяжелых металлов в организме рыб (обзор литературы)

В статье рассмотрен обзор литературы, касающейся содержания тяжелых металлов (ТМ) в организме рыб разных видов. Приведен анализ химико-экологической ситуации водоемов, места обитания гидробионтов.
Ключевые слова: рыба, тяжелые металлы, организм, органы, ткани.
К числу важнейших факторов, влияющих на устойчивость биоценозов, относится антропогенное химическое загрязнение поверхностных вод ТМ, которые попадают в водоемы со стоками и смывами с территорий промышленных предприятий, сельхозугодий, городов и мелких населенных пунктов [2, 18].
ТМ представляют серьезную опасность в качестве загрязнителей водных экосистем и относятся к консервативным загрязняющим веществам, которые не разлагаются в природных водах, а только изменяют формы своего существования, перераспределяясь между биотическими и абиотическими звеньями. Также они являются неотъемлемой составной частью организма, но индивидуальная потребность гидробионтов в металлах очень мала, и содержание металлов, превышающее индивидуальные потребности организмов, способно вызывать нарушения различных функций гидробионтов, накапливаться в их органах, превышая нормируемые величины [4, 8, 9].
Рыбы, занимая в биоценозах водных экосистем верхний трофический уровень, обладают способностью, аккумулировать ТМ, степень накопления которых зависит, как от биотических (половая принадлежность, вид, возраст, занимаемая экологическая ниша), так и абиотических (фоновое содержание ТМ в природных водах, рН, карбонатная жесткость) факторов [1, 6, 7].
Изучение биологических систем различного уровня организации в условиях, как их естественной среды обитания, так и изменения под воздействием антропогенного фактора позволяет непосредственно выявить эффекты, обусловленные воздействием всего комплекса загрязняющих веществ и естественных абиотических факторов за продолжительный период времени, определить пороговые уровни нагрузок и дать наиболее реалистичный прогноз ее развития. Особо острой проблемой является загрязнение природных пресных вод тяжелыми металлами, для которых в воде не существует надежных механизмов самоочищения: они лишь перераспределяются в экосистемах, взаимодействуя с организмами разных трофических уровней и оставляя видимые или невидимые последствия [10, 11, 12, 13, 14, 16].
Среди поллютантов ТМ представляют наиболее приоритетный интерес не только из-за высокой токсичности для водных организмов, но и способности к аккумуляции и трансформации внутрибиоценоза водоёма [11, 14, 17].
Рядом ученых были проведены исследования органов и тканей рыб на наличие в них общих закономерностей распределения ТМ. В частности, И. А. Глазуновой (2005) установлено, что металлы аккумулируются в организме рыб в количествах, во много раз превышающих их содержание в воде. Автор указывает, что данный факт приводит к снижению продуктивности водоемов верховьев Оби и к потенциальной опасности для человека. При этом отмечена видовая специфичность в накоплении металлов рыбами в зависимости от типа их питания: лещ концентрирует медь, судак — цинк, свинец [7]. Кинетика аккумуляции ТМ в рыбах Байкальского региона исследуемых С. В. Гомбоевой (2003) показала неравномерное распределение металлов в организме рыб, однако все исследуемые металлы аккумулировались в основном в печени. В наиболее высоких концентрациях в органах и тканях рыб отмечался цинк, содержание свинца и кадмия в органах оказалось сравнительно невелико. Примечательно, что наибольшее содержание элементов выявлено летом, наименьшее — зимой, у старшевозрастных и хищных видов рыб содержание металлов оказалось выше [5]. Такое же исследование проводила Ваганов А. С. на промысловых видах рыб различных экологических групп Куйбышевского водохранилища (2012). Установила особенности накопления и распределения ТМ в печени и жабрах рыб [3]. Превышение предельно допустимых концентраций в органах и паразитах рыб Ладожского озера установлено С. А. Салтыковой (2006), при этом распределение металлов в организме рыб характеризовалось неоднородностью [15]. Кашулин Н. А. (2000) разработал научные основы и методы биоиндикации техногенного загрязнения водоемов Арктики и Субарктики ТМ. На основе исследования в популяциях рыб наблюдается сокращение числа возрастных групп, свидетельствующее о снижении продолжительности жизни [9]. При исследрвании заливов Набиль, Ныйский, Чайво и Пильтун Бедрицкая И. Н. (2000) выявила невысокое содержание ТМ [2].
Заключение. Загрязнение окружающей среды тяжелыми металлами является одной из глобальных проблем современности. Это указывает на необходимости проведения экологического мониторинга содержания тяжелых металлов в воздухе, воде, почве. В частности, проведение санитарно-гигиенического мониторинга пищевого сырья и продуктов питания, изучение цепей миграции тяжелых металлов от их источника до человека являеться важной состовляющей в оценке безопасности и качества сырья и продукции.
- Батоян В. В., Сорокин В. Н. Микроэлементы в рыбах Куйбышевского водохранилища // Экология, 1989. № 6. — С. 81–83.
- Бедрицкая И. Н. Влияние тяжелых металлов на организм рыб, выращиваемых на сбросных водах электростанций Диссертация и автореферат по ВАК 03.00.10 Троицк 2000 — с. 185.
- Ваганов А. С. Накопление тяжелых металлов тканями и органами промысловых видов рыб различных экологических групп Куйбышевского водохранилища Диссертация и автореферат по ВАК 03.02.08 Ульяновск 2012 — с. 120.
- Гомбоева С. В., Пронин Н. М., Цыренов В. Ж. Оценка качества воды озера Гусиное и озера Байкал. Современные проблемы гидробиологии Сибири: Тез. докл. всерос. конф./ Томск, 2001. — С. 110–1112.
- Гомбоева С. В. Экологические особенности распределения тяжелых металлов в рыбах Байкальского региона Диссертация и автореферат по ВАК 03.00.16 Улан-Удэ 2003 — с. 150.
- Горден Ю. В. Содержание и методы прогноза изменения тяжелых металлов в органах и тканях севрюги (Acipenser Stellatus Pallas) разного возраста в речной период жизни Диссертация и автореферат по ВАК 03.00.13 Ставрополь 2001 — с. 190.
- Глазунова И. А. Содержание и особенности распределения тяжелых металлов в рыбах верховьев Оби Диссертация и автореферат по ВАК 03.00.16 Барнаул 2005 — с. 103.
- Грубинко В. В., Смольский A. C., Коновец И. Н., Арсан О. М. Гемоглобин рыб при действии аммиака и солей тяжелых металлов // Гидробиологический журнал. — 1995. Т. 31, № 4. — С. 82–87.
- Кашулин Н. А. Ихтиологические основы биоиндикации загрязнения среды тяжелыми металлами Диссертация и автореферат по ВАК 03.00.10 Апатиты 2000 — с. 381.
- Кузнецов В. А. Признаки дестабилизации в рыбном сообществе Куйбышевского водохранилища // Актуальные экологические проблемы республики Татарстан. Казань: «Новое знание», 2000. С. 60.
- Линник П. Н., Набиванец Б. И. Формы миграции металлов в пресных поверхностных водах. // Гидрометеоиздат, 1986. — с.272.
- Моисеенко Т. И. Оценка экологической опасности в условиях загрязнения вод металлами // Водные ресурсы. 1999. — Т. 26, № 2. — С 186–197.
- Перевозников М. А., Богданова Е.А Тяжелые металлы в пресноводных экосистемах. — С.-Петербург, 1999. — с.227.
- Пономаренко A. M. Эколого-рыбохозяйственные аспекты ртутного загрязнения водохранилищ: Дис. канд. биол. наук. Казань, 2006. — с.116.
- Салтыкова С. А. Сравнительный анализ особенностей накопления тяжелых металлов в рыбах и их паразитах:на примере экосистемы Ладожского озера Диссертация и автореферат по ВАК 03.00.16 Петрозаводск 2006 — с. 109.
- Степанова Н. Ю., Яковлев В. А., Латыпова В. З. Зообентос как индикатор экотоксикологической обстановки в Куйбышевском водохранилище // Вестник РУДН: серия «Экология и безопасность жизнедеятельности», 2007. № 2. — С. 50–56.
- Степанова Н. Ю., Латыпова В. З., Мухаметшин A. M. Уровень содержания металлов в тканях, органах рыб и воде Куйбышевского водохранилища // Вестник ТО РЭА, 2005. № 4. — С.44–49.
- Gomboeva S. V., Т syren о v V, Zh„ Pro n in N. M. Distribution of heavy metals in fish organs and tissues with different type of nutrition in the Baikal coastal and bay zoes // Ecologically equivalent and exotic aquatic species in Great and large lakes of the world: The second internat. Symposium / SB RAS. — Ulan-Ude, 2002. — P.29–30.
Основные термины (генерируются автоматически): организм рыб, металл, вод, орган, рыба, содержание металлов.
Тяжелые и благородные металлы в водах ледниковой реки Черек

Кабардино-Балкарский государственный высокогорный природный заповедник — красивейший уголок Кавказа. Эта уникальная территория, свободная от антропогенного загрязнения, идеально подходит для проведения наблюдений за распространением загрязняющих веществ. Заповедник расположен между 42°47′ и 43°20′ с. ш., 42°40′ и 43°35′ в. д. Здесь находится Безенгийское ущелье — единственное в своем роде по высоте замыкающих его вершин Большого Кавказа. Все эти гранитные великаны — Дых-Тау (5204), Коштан-Тау (5152), Шхара (5201), Кышкара (5068), пик Пушкина (5033), Джанги-Тау (5058), Гестола (4859) и Катын-Тау (4858,8) — превышают знаменитый Монблан. Безенгийская ледяная стена — классический район для альпинистов всех стран мира. Отсюда берут начало вскипающие, мощные, наполненные силой природы потоки р. Черека Безенгийского — левой составляющей р. Черека. Относится он к бассейну Терека — одной из крупнейших рек Кавказа [1].
Бассейн Черека Безенгийского располагается на северном склоне Центрального Кавказа и граничит на западе с бассейном р. Чегема, на востоке — с Череком Балкарским, а на юге — с Ингури. Протяженность Черека Безенгийского (до слияния с правым истоком — Череком Балкарским) составляет 51 км, площадь его водосбора 627 км 2 при среднем уклоне реки 60% и средней высоте водосбора 2480 м. В верхней части, где река пересекает Боковой хребет, ширина долины не превышает 1–2 км. Между Боковым и Скалистым хребтами она расширяется в Северной депрессии до 5–10 км. Прорезая Скалистый хребет, река протекает в узком каньонообразном Хуламском ущелье. Его глубина достигает 450 м, а ширина 50–200 м.
Ледник Безенги площадью 36,2 км 2 и наибольшей длиной 17,6 км (по восточному потоку от горы Башхааузбаши) — крупнейший ледник не только Кавказа, но и Европы. По морфологическому типу он сложный долинный, северо-восточной экспозиции [2].
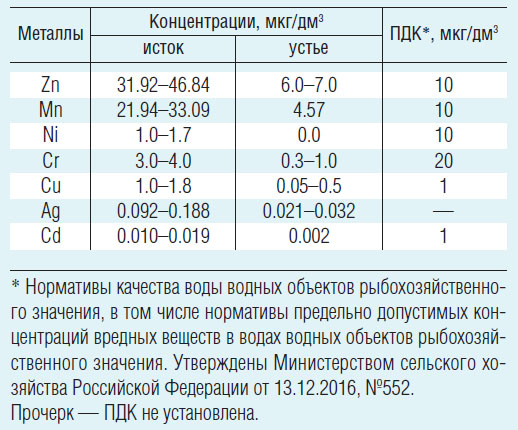
Практически все ледники находятся в верховьях рек, а наибольшее их количество расположено в верховьях Черека Безенгийского. Это типично горная река с ледниково-снежным питанием. В ее бассейне встречаются обширные снеговые поля и ледники. В результате наших исследований установлено, что воды реки относятся к нейтральным или слабощелочным. Величина рН в летних образцах проб речной воды изменяется в пределах 6,80–7,80, а максимальная сумма растворенных ионов достигает 148,74 мг/л. Преобладающие анионы — гидрокарбонаты (до 44%), а катион — кальций (от 32 до 42%). Гидрологический режим Черека Безенгийского характеризуется зимней меженью, летними дождевыми паводками и ледниковым половодьем, которые напрямую зависят от высоты его протекания и метеорологических особенностей года. В результате взаимодействия с горными породами природные воды обогащаются различными микроэлементами. Их средние содержания в литосфере очень малы [3–4]. Предельно допустимые концентрации (ПДК) металлов в поверхностных водах приведены в таблице.
Таблица. Концентрации тяжелых металлов в воде Черека и их ПДК
Научными сотрудниками Высокогорного геофизического института осуществляется многолетний мониторинг рек Центрального Кавказа, берущих начало высоко в горах. В ранее опубликованных работах [5–6] приводятся факторы формирования химического состава речных вод, гидрохимические показатели в разные фазы гидрологического режима рек и результаты измерений концентраций тяжелых металлов в водах высокогорной зоны Безенгийского ущелья.

Картосхема отбора проб воды в р. Черек. 1 — Черек Безенгийский, 2 — Черек Балкарский, 3 — предгорная зона (74 км от истока), 4 — равнинная зона (110 км от истока)
Цель данной работы — определение уровня концентрации тяжелых (Zn, Mn, Ni, Cr, Pb, Cu, Cd) и благородных (Ag) металлов в высокогорном Череке в период летнего половодья. В это время значительно меняется соотношение источников питания и отмечается существенное изменение расхода воды, обусловленное интенсивным таянием ледников и снежников.
Отбор проб воды проводили по длине реки, от левого истока (Черека Безенгийского, ледника Уллу-Чиран) до выхода в устьевую зону. Измерения концентраций металлов осуществлялись методом атомно-абсорбционной спектрометрии с термической атомизацией МГА-915 * . Последние два створа были выбраны для сравнения определяемых металлов в водах высокогорной зоны с данными анализа в предгорной (74 км) и равнинной (110 км) территориях, чтобы проследить, как меняются концентрации тяжелых металлов от истока к устью.
В водах высокогорной зоны, в истоке Черека Безенгийского, среди представленных микроэлементов наиболее высокие концентрации у Zn и Mn, в водах же равнинной зоны они гораздо меньше. Далее, вниз по течению реки в устьевую зону, концентрации Zn и Mn убывали в пять-семь раз. На выходе реки в устье также уменьшались концентрации Ni, Cr и Cu (см. табл.).
По сравнению с другими микроэлементами выделялось поведение Ag и Cd. Концентрация Ag изменялась в небольшом интервале в верхнем течении и к замыкающему створу варьировала в пределах 0,021–0,032 мкг/дм 3 . Концентрация Cd в верхнем и нижнем течениях отличалась от Ag на порядок, а от содержания других микроэлементов — более чем на два (см. табл.). Схематично концентрации элементов можно расположить следующим образом: Zn > Mn > Cr > Pb > Cu > Ni > Ag > Cd.
Неоднозначно вел себя и Pb. Этот элемент имеет высокий геохимический фон, но, в отличие от других микроэлементов, его содержание периодически увеличивалось, что, возможно, связано с впадением правого истока (Черека Балкарского). Концентрация Pb сначала возрастала, а затем на равнине уменьшилась почти в два раза, как и концентрации других элементов.
Таким образом, в водах р. Черека в среднем течении (74 км) и в устье (110 км) концентрации микроэлементов значительно ниже, чем в верхнем течении. По экологическим классам качества поверхностных вод суши воды исследуемой реки квалифицируются как чистые и очень чистые [7], а по классификации А. М. Никанорова они относятся к I типу [8]. Загрязняющим элементом реки от истока до устья остается Zn, при этом в высокогорной зоне воды по нему считаются сильно загрязненными (6-й класс), а на равнине, где концентрация Zn составляет всего 6,0–7,0 мкг/дм 3 , — незначительно загрязненными (4-й класс).
Наши работы показали, что загрязнение речных вод тяжелыми металлами в верховье носит природный геохимический характер, связанный с вымыванием их из горообразующих пород. При выходе водотока на равнину концентрации микроэлементов уменьшаются и становятся значительно ниже ПДК.
Реки, берущие начало от ледников, питают равнинные реки республики. Они представляют собой важное и ценное «сырье». В третьем тысячелетии запасы чистой воды есть и будут в дальнейшем надежным капиталом в экономике нашего региона и страны в целом.
Литература
1. Ефремов Ю. В., Панов В. Д., Лурье П. М. и др. Орография, оледенение, климат Большого Кавказа: опыт комплексной характеристики и взаимосвязей. Краснодар, 2007.
2. Лурье П. М. Водные ресурсы и водный баланс Кавказа. СПб., 2002; 114–116.
3. Войткевич Г. В., Кокин А. В., Мирошников А. Е., Прохоров В. Г. Справочник по геохимии. М., 1990.
4. Разумов В. В., Курданов Х. А., Разумова Л. А. и др. Экосистемы гор Центрального Кавказа и здоровье человека. М.; Ставрополь, 2003.
5. Воробьева Т. И., Гущина Л. П., Жинжакова Л. З. и др. Формирование микроэлементного состава в речных водах Центрального Кавказа // Материалы научно-практической конференции «Современные фундаментальные проблемы гидрохимии и мониторинга качества поверхностных вод России». Азов. 8–10 июня 2009. Азов, 2009; 39–42.
6. Воробьева Т. И., Жинжакова Л. З., Чередник Е. А., Отарова А. С. Оценка фонового уровня содержания микропримесей в речных водах на территории Центрального Кавказа // Геолого-геофизические исследования глубинного строения Кавказа: Геология и геофизика Кавказа: современные вызовы и методы исследований. Коллективная монография. Владикавказ, 2017; 535–542.
7. Нежиховский Р. А. Гидролого-экологические основы водного хозяйства. Л., 1990.
8. Никаноров А. М. Гидрохимия. СПб., 2001; 154–162.
* ПНД Ф 14.1:2.253-09 Количественный химический анализ вод. Методика выполнения измерений массовых концентраций Al, Ba, Be, V, Fe, Cd, Co, Li, Mn, Cu, Mo, As, Ni, Sn, Pb, Se, Sr, Ti, Cr, Zn в природных и сточных водах методом атомно-абсорбционной спектроскопии с использованием атомно-абсорбционного спектрометра с электротермической атомизацией «МГА-915». М., 2009.
Читайте также:
