Тяжелый и хрупкий металл
Обновлено: 11.05.2024
Термин «металл» происходит от греческого слова «metalléuō», что означает выкапываю или добываю из земли. Наша планета содержит много металла. На самом деле из 118 элементов периодической системы порядка 95 являются металлами.
Это число не является точным, потому что граница между металлами и неметаллами довольно расплывчата: нет стандартного определения металлоида, как нет и полного согласия относительно элементов, соответствующим образом классифицированных как таковые.
Сегодня мы используем различные виды металлов, даже не замечая их. Начиная с зажимов в сантехнике и заканчивая устройством, которое вы используете для чтения этой статьи, все они сделаны из определенных металлов. Фактически, некоторые металлические элементы необходимы для биологических функций, таких как приток кислорода и передача нервных импульсов. Некоторые из них также широко используются в медицине в виде антацидов.
Все металлы в периодической таблице можно классифицировать по их химическим или физическим свойствам. Ниже мы перечислили некоторые различные типы металлов вместе с их реальным применением.
Классификация металла по физическим свойствам
Легкие металлы

Сплав титана 6AL-4V
Примеры: Алюминий, титан, магний
Легкие металлы имеют относительно низкую плотность. Формального определения или критериев для идентификации этих металлов нет, но твердые элементы с плотностью ниже 5 г/см³ обычно считаются легкими металлами.
Металлургия легких металлов была впервые развита в середине 19 века. Хотя большинство из них происходит естественным путем, значительная их часть образуется при электротермии и электролизе плавленых солей.
Их сплавы широко используются в авиационной промышленности благодаря их низкой плотности и достаточным механическим свойствам. Например, сплав титана 6AL-4V составляет почти 50 процентов всех сплавов, используемых в авиастроении. Он используется для изготовления роторов, лопастей компрессоров, мотогондол, компонентов гидравлических систем.
Тяжелые металлы

Окисленные свинцовые конкреции и кубик размером 1 см3
Примеры: железо, медь, кобальт, галлий, олово, золото, платина.
Тяжелые металлы - это элементы с относительно высокой плотностью (обычно более 5 г/см³ ) и атомным весом. Они, как правило, менее реактивны и содержат гораздо меньше растворимых сульфидов и гидроксидов, чем более легкие металлы.
Эти металлы редки в земной коре, но они присутствуют в различных аспектах современной жизни. Они используются в солнечных батареях, сотовых телефонах, транспортных средствах, антисептиках и ускорителях частиц.
Тяжелые металлы часто смешиваются в окружающей среде из-за промышленной деятельности, ухудшая качество почвы, воды и воздуха, а затем вызывая проблемы со здоровьем у животных и растений. Выбросы транспортных средств, горнодобывающие и промышленные отходы, удобрения, свинцово-кислотные батареи и микропластики, плавающие в океанах, являются одними из наиболее распространенных источников тяжелых металлов в этом контексте.
Белый металл

Подшипники из белого металла
Примеры: Обычно изготавливается из олова, свинца, висмута, сурьмы, кадмия, цинка.
Белые металлы - это различные светлые сплавы, используемые в качестве основы для украшений или изделий из серебра. Например, многие сплавы на основе олова или свинца используются в ювелирных изделиях и подшипниках.
Белый металлический сплав изготавливается путем объединения определенных металлов в фиксированных пропорциях в соответствии с требованиями конечного продукта. Основной металл для ювелирных изделий, например, формуется, охлаждается, экстрагируется, а затем полируется, чтобы придать ему точную форму и блестящий вид.
Они также используются для изготовления тяжелых подшипников общего назначения, подшипников внутреннего сгорания среднего размера и электрических машин.
Хрупкий металл

Хрупкое разрушение чугуна
Примеры: сплавы углеродистой стали, чугуна и инструментальной стали.
Металл считается хрупким, если он твердый, но не может противостоять ударам или вибрации под нагрузкой. Такие металлы под воздействием напряжения ломаются без заметной пластической деформации. Они имеют низкую прочность на разрыв и часто издают щелкающий звук при поломке.
Многие стальные сплавы становятся хрупкими при низких температурах, в зависимости от их обработки и состава. Чугун, например, твердый, но хрупкий из-за высокого содержания углерода. Напротив, керамика и стекло гораздо более хрупки, чем металлы, из-за их ионных связей.
Галлий, висмут, хром, марганец и бериллий также хрупки. Они часто используются в различных гражданских и военных целях, связанных с высокими деформационными нагрузками. Чугун, устойчивый к повреждениям в результате окисления, используется в машинах, трубах и деталях автомобильной промышленности, таких как корпуса коробок передач и головки цилиндров.
Тугоплавкий металл
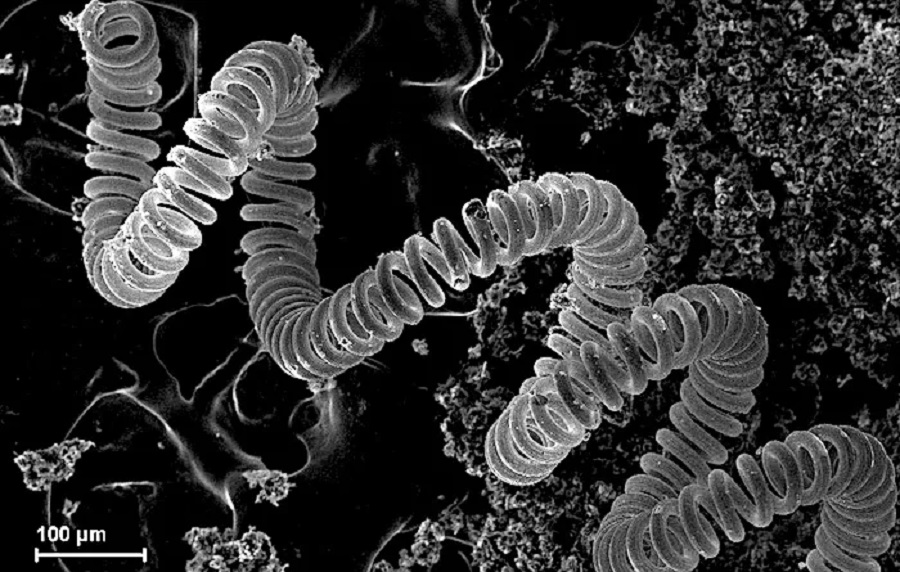
Микроскопическое изображение вольфрамовой нити в лампе накаливания
Примеры: молибден, вольфрам, тантал, рений, ниобий.
Тугоплавкие металлы имеют чрезвычайно высокие температуры плавления (более 2000 °С) и устойчивы к износу, деформации и коррозии. Они являются хорошими проводниками тепла и электричества и имеют высокую плотность.
Другой ключевой характеристикой является их термостойкость: они не расширяются и не растрескиваются при многократном нагревании и охлаждении. Однако они могут деформироваться при высоких нагрузках и окисляться при высоких температурах.
Благодаря своей прочности и твердости они идеально подходят для сверления и резки. Карбиды и сплавы тугоплавких металлов используются почти во всех отраслях промышленности, включая горнодобывающую, автомобильную, аэрокосмическую, химическую и ядерную.
Металлический вольфрам, например, используется в ламповых нитях. Сплавы рения используются в гироскопах и ядерных реакторах. А ниобиевые сплавы используются для форсунок жидкостных ракетных двигателей.
Черные и цветные металлы

Валы-шестерни из (черной) нержавеющей стали
- Черные металлы: Сталь, чугун, сплавы железа.
- Цветные металлы: Медь, алюминий, свинец, цинк, серебро, золото.
Термин "железо" происходит от латинского слова "Ferrum", что переводится как «железо». Таким образом, термин «черный металл» обычно означает "содержащий железо", тогда как "цветной металл" означает металлы и сплавы, которые не содержат достаточного количества железа.
Поскольку черные металлы могут иметь широкий спектр легирующих элементов, которые значительно изменяют их характеристики, очень трудно поместить свойства всех черных металлов под один зонт. Тем не менее некоторые обобщения могут быть сделаны, например, большинство черных металлов являются твердыми и магнитными.
Черные металлы используются для применения с высокой нагрузкой и низкой скоростью, в то время как цветные металлы предпочтительны для применения с высокой скоростью и нулевой нагрузкой для применения с низкой нагрузкой.
Сталь является наиболее распространенным черным металлом. Она составляет около 80% всего металлического материала благодаря своей доступности, высокой прочности, низкой стоимости, простоте изготовления и широкому спектру свойств. Она широко используется в строительстве и обрабатывающей промышленности. Фактически, рост производства стали показывает общее развитие промышленного мира.
Цветные и благородные металлы

Ассортимент благородных металлов
- Цветные металлы: медь, алюминий, олово, никель, цинк
- Благородные металлы: родий, ртуть, серебро, рутений, осмий, иридий
Цветные металлы - это обычные и недорогие металлы, которые корродируют, окисляются или тускнеют быстрее, чем другие металлы, когда подвергаются воздействию воздуха или влаги. Они в изобилии встречаются в природе и легко добываются.
Они широко используются в промышленных и коммерческих целях и имеют неоценимое значение для мировой экономики благодаря своей полезности и повсеместности. Некоторые цветные металлы обладают отличительными характеристиками, которые не могут быть продублированы другими металлами. Например, цинк используется для гальванизации стали, чтобы защитить ее от коррозии, а никель - для изготовления нержавеющей стали.
Благородные металлы, с другой стороны, устойчивы к окислению и коррозии во влажном воздухе. Согласно атомной физике, благородные металлы имеют заполненный электрон d-диапазона. В соответствии с этим строгим определением, медь, серебро и золото являются благородными металлами.
Они находят применение в таких областях, как орнамент, металлургия и высокие технологии. Их точное использование варьируется от одного элемента к другому. Некоторые благородные металлы, такие как родий, используются в качестве катализаторов в химической и автомобильной промышленности.
Драгоценные металлы

Родий: 1 грамм порошка, 1 грамм прессованного цилиндра и 1 г аргонодуговой переплавленной гранулы
Примеры: палладий, золото, платина, серебро, родий.
Драгоценные металлы считаются редкими и имеют высокую экономическую ценность. Химически они менее реакционноспособны, чем большинство элементов (включая благородные металлы). Они также пластичны и имеют высокий блеск.
Несколько веков назад эти металлы использовались в качестве валюты. Но сейчас они в основном рассматриваются как промышленные товары и инвестиции. Многие инвесторы покупают драгоценные металлы (в основном золото), чтобы диверсифицировать свои портфели или победить инфляцию.
Серебро - второй по популярности драгоценный металл для ювелирных изделий (после золота). Однако его значение выходит далеко за рамки красоты. Оно обладает исключительно высокой тепло- и электропроводностью и чрезвычайно низким контактным сопротивлением. Именно поэтому серебро широко используется в электронике, батареях и противомикробных препаратах. Классификация по химическим свойствам
Щелочные металлы

Твердый металлический натрий
Примеры: натрий, калий, рубидий, литий, цезий и франций. Щелочь относится к основной природе гидроксидов металлов. Когда эти металлы реагируют с водой, они образуют сильные основания, которые легко нейтрализуют кислоты.
Они настолько реактивны, что обычно встречаются в природе в слиянии с другими веществами. Карналлит (хлорид калия-магния) и сильвин (хлорид калия), например, растворимы в воде и, таким образом, легко извлекаются и очищаются. Нерастворимые в воде щелочи, такие как фторид лития, также существуют в земной коре.
Одно из самых популярных применений щелочных металлов - использование цезия и рубидия в атомных часах, наиболее точных из известных эталонов времени и частоты. Литий используется в качестве анода в литиевых батареях, композиты калия используются в качестве удобрений, а ионы рубидия используются в фиолетовых фейерверках. Чистый металлический натрий широко используется в натриевых лампах, которые очень эффективно излучают свет.
Щелочноземельные металлы

Изумрудный кристалл, основной минерал бериллия.
Примеры: бериллий, кальций, магний, барий, стронций и радий.
Щелочноземельные металлы в стандартных условиях мягкие и серебристо-белые. Они имеют низкую плотность, температуру кипения и температуру плавления. Хотя они не так реакционноспособны, как щелочные металлы, они очень легко образуют связи с элементами. Как правило, они вступают в реакцию с галогенами, образуя галогениды щелочноземельных металлов.
Все они встречаются в земной коре, кроме радия, который является радиоактивным элементом. Радий уже распадался в ранней истории Земли из-за относительно короткого периода полураспада (1600 лет). Современные образцы поступают из цепочки распада урана и тория.
Щелочноземельные металлы имеют широкий спектр применения. Бериллий, например, используется в полупроводниках, теплопроводниках, электрических изоляторах и в военных целях. Магний часто сплавляют с цинком или алюминием для получения материалов со специфическими свойствами. Кальций в основном используется в качестве восстановителя, а барий используется в вакуумных трубках для удаления газов.
Переходные металлы
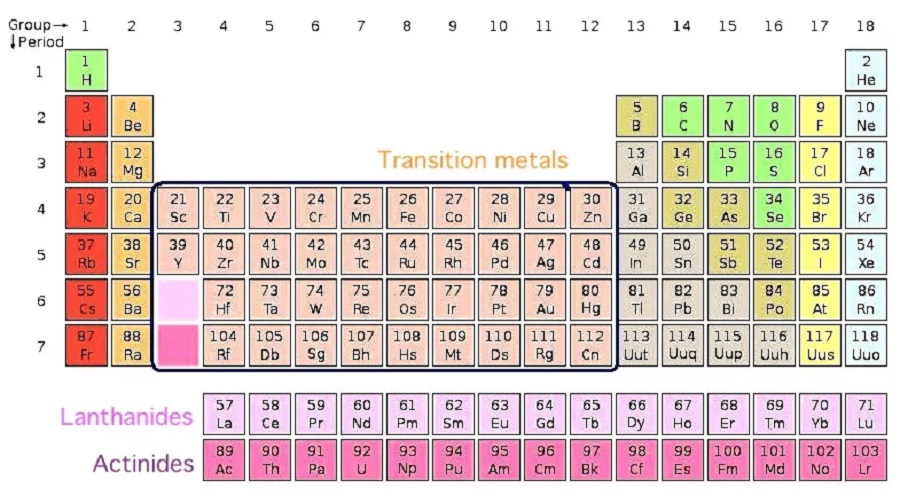
Примеры: титан, ванадий, хром, никель, серебро, вольфрам, платина, кобальт.
Большинство элементов используют электроны из своей внешней оболочки для связи с другими элементами. Переходные металлы, однако, могут использовать две крайние оболочки для соединения с другими элементами. Это химическая особенность, которая позволяет им связываться со многими различными элементами в различных формах.
Они занимают среднюю часть таблицы Менделеева, служа мостом между (или переходом) между двумя сторонами таблицы. Более конкретно, есть 38 переходных металлов в группах с 3 по 12 периодической таблицы. Все они являются пластичными, податливыми и хорошими проводниками тепла и электричества.
Многие из этих металлов, такие как медь, никель, железо и титан, используются в конструкциях и в электронике. Большинство из них образуют полезные сплавы друг с другом и с другими металлическими веществами. Некоторые из них, включая золото, серебро и платину, называются благородными металлами, потому что они крайне инертны и устойчивы к кислотам.
Постпереходные металлы

Висмут в виде синтетических кристаллов
Примеры: алюминий, галлий, олово, свинец, таллий, индий, висмут.
Постпереходные металлы в периодической таблице - это элементы, расположенные справа от переходных металлов и слева от металлоидов. Из-за своих свойств они также называются "бедными" или "другими" металлами.
Физически они хрупки (или мягки) и имеют более низкую температуру плавления и механическую прочность, чем переходные металлы. Их кристаллическая структура довольно сложна: они проявляют ковалентные или направленные эффекты связи.
Различные металлы этого семейства имеют различное применение. Алюминий, например, используется для изготовления оконных рам, кухонной посуды, банок, фольги, деталей автомобилей. Оловянные сплавы используются в мягких припоях, оловянных и сверхпроводящих магнитах.
Индиевые сплавы используются для изготовления плоских дисплеев и сенсорных экранов, а галлий - в топливных элементах и полупроводниках.
Лантаноиды

1-сантиметровый кусок чистого лантана
Примеры: лантан, церий, прометий, гадолиний, тербий, иттербий, лютеций.
Лантаноиды - это редкоземельные металлы с атомными номерами от 57 до 71. Впервые они были обнаружены в 1787 году в необычном черном минерале (гадолините), обнаруженном в Иттербю, Швеция. Позже минерал был разделен на различные элементы лантаноидов.
Лантаноиды - это металлы с высокой плотностью, плотность которых колеблется от 6,1 до 9,8 г/см³, и они, как правило, имеют очень высокие температуры кипения (1200-3500 °C) и очень высокие температуры плавления (800-1600 °C).
Сплавы лантаноидов используются в металлургии из-за их сильных восстановительных способностей. Около 15 000 тонн лантаноидов ежегодно расходуется в качестве катализаторов и при производстве стекол. Они также широко используются в лазерах и оптических усилителях.
Некоторые исследования показывают, что лантаноиды могут быть использованы в качестве противораковых средств. Лантан и церий, в частности, могут подавлять пролиферацию раковых клеток и способствовать цитотоксичности.
Актиниды

Металлический уран, высокообогащенный ураном-235
Примеры: актиний, уран, торий, плутоний, фермий, нобелий, лоренций Подобно лантаноидам, актиниды образуют семейство редкоземельных элементов с аналогичными свойствами. Они представляют собой серию из 15 последовательных химических элементов в периодической системе от атомных номеров 89 до 103.
Все они радиоактивны по своей природе. Синтетически произведенный плутоний, а также природные уран и торий являются наиболее распространенными актинидами на Земле. Первым актинидом, который был открыт в 1789 году, был уран. И большая часть существующих продуктов актинидов была произведена в 20 веке.
Их свойства, такие как излучение радиоактивности, пирофорность, токсичность и ядерная критичность, делают их опасными для обращения. Сегодня значительная часть (кратковременных) актинидов производится ускорителями частиц в исследовательских целях.
Некоторые актиниды нашли применение в повседневной жизни, например, газовые баллоны (торий) и детекторы дыма (америций), большинство из них используются в качестве топлива в ядерных реакторах и для изготовления ядерного оружия. Уран-235 является наиболее важным изотопом для применения в ядерной энергетике, который широко используется в тепловых реакторах.
14 различных типов металлов

Термин "металл" происходит от греческого слова "metalléuō", что означает выкапываю или добываю из земли. Наша планета содержит много металла. На самом деле из 118 элементов периодической системы порядка 95 являются металлами.
Это число не является точным, потому что граница между металлами и неметаллами довольно расплывчата: нет стандартного определения металлоида, как нет и полного согласия относительно элементов, соответствующим образом классифицированных как таковые.
Сегодня мы используем различные виды металлов, даже не замечая их. Начиная с зажимов в сантехнике и заканчивая устройством, которое вы используете для чтения этой статьи, все они сделаны из определенных металлов. Фактически, некоторые металлические элементы необходимы для биологических функций, таких как приток кислорода и передача нервных импульсов. Некоторые из них также широко используются в медицине в виде антацидов.
Все металлы в периодической таблице можно классифицировать по их химическим или физическим свойствам. Ниже мы перечислили некоторые различные типы металлов вместе с их реальным применением.
Классификация по физическим свойствам
14. Легкие металлы

Сплав титана 6AL-4V
Примеры: Алюминий, титан, магний
Легкие металлы имеют относительно низкую плотность. Формального определения или критериев для идентификации этих металлов нет, но твердые элементы с плотностью ниже 5 г/см³ обычно считаются легкими металлами.
Металлургия легких металлов была впервые развита в середине 19 века. Хотя большинство из них происходит естественным путем, значительная их часть образуется при электротермии и электролизе плавленых солей.
Их сплавы широко используются в авиационной промышленности благодаря их низкой плотности и достаточным механическим свойствам. Например, сплав титана 6AL-4V составляет почти 50 процентов всех сплавов, используемых в авиастроении. Он используется для изготовления роторов, лопастей компрессоров, мотогондол, компонентов гидравлических систем.
13. Тяжелые металлы

Окисленные свинцовые конкреции и кубик размером 1 см3
Примеры: железо, медь, кобальт, галлий, олово, золото, платина.
Тяжелые металлы - это элементы с относительно высокой плотностью (обычно более 5 г/см³) и атомным весом. Они, как правило, менее реактивны и содержат гораздо меньше растворимых сульфидов и гидроксидов, чем более легкие металлы.
Эти металлы редки в земной коре, но они присутствуют в различных аспектах современной жизни. Они используются в солнечных батареях, сотовых телефонах, транспортных средствах, антисептиках и ускорителях частиц.
Тяжелые металлы часто смешиваются в окружающей среде из-за промышленной деятельности, ухудшая качество почвы, воды и воздуха, а затем вызывая проблемы со здоровьем у животных и растений. Выбросы транспортных средств, горнодобывающие и промышленные отходы, удобрения, свинцово-кислотные батареи и микропластики, плавающие в океанах, являются одними из наиболее распространенных источников тяжелых металлов в этом контексте.
12. Белый металл

Подшипники из белого металла
Примеры: Обычно изготавливается из олова, свинца, висмута, сурьмы, кадмия, цинка.
Белые металлы - это различные светлые сплавы, используемые в качестве основы для украшений или изделий из серебра. Например, многие сплавы на основе олова или свинца используются в ювелирных изделиях и подшипниках.
Белый металлический сплав изготавливается путем объединения определенных металлов в фиксированных пропорциях в соответствии с требованиями конечного продукта. Основной металл для ювелирных изделий, например, формуется, охлаждается, экстрагируется, а затем полируется, чтобы придать ему точную форму и блестящий вид.
Они также используются для изготовления тяжелых подшипников общего назначения, подшипников внутреннего сгорания среднего размера и электрических машин.
11. Хрупкий металл

Хрупкое разрушение чугуна
Примеры: сплавы углеродистой стали, чугуна и инструментальной стали.
Металл считается хрупким, если он твердый, но не может противостоять ударам или вибрации под нагрузкой. Такие металлы под воздействием напряжения ломаются без заметной пластической деформации. Они имеют низкую прочность на разрыв и часто издают щелкающий звук при поломке.
Многие стальные сплавы становятся хрупкими при низких температурах, в зависимости от их обработки и состава. Чугун, например, твердый, но хрупкий из-за высокого содержания углерода. Напротив, керамика и стекло гораздо более хрупки, чем металлы, из-за их ионных связей.
Галлий, висмут, хром, марганец и бериллий также хрупки. Они часто используются в различных гражданских и военных целях, связанных с высокими деформационными нагрузками. Чугун, устойчивый к повреждениям в результате окисления, используется в машинах, трубах и деталях автомобильной промышленности, таких как корпуса коробок передач и головки цилиндров.
10. Тугоплавкий металл
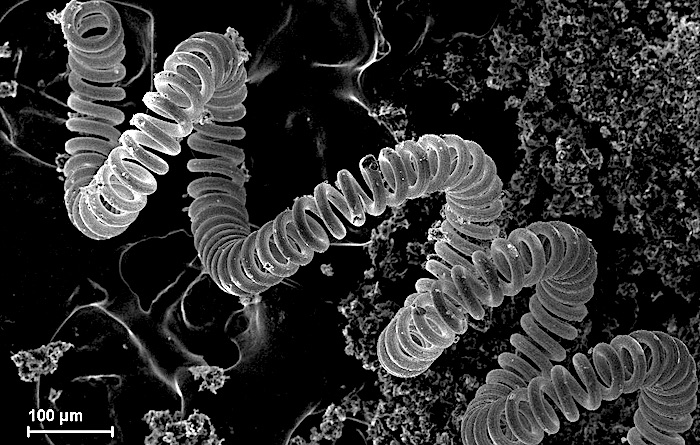
Микроскопическое изображение вольфрамовой нити в лампе накаливания
Примеры: молибден, вольфрам, тантал, рений, ниобий.
Тугоплавкие металлы имеют чрезвычайно высокие температуры плавления (более 2000 °С) и устойчивы к износу, деформации и коррозии. Они являются хорошими проводниками тепла и электричества и имеют высокую плотность.
Другой ключевой характеристикой является их термостойкость: они не расширяются и не растрескиваются при многократном нагревании и охлаждении. Однако они могут деформироваться при высоких нагрузках и окисляться при высоких температурах.
Благодаря своей прочности и твердости они идеально подходят для сверления и резки. Карбиды и сплавы тугоплавких металлов используются почти во всех отраслях промышленности, включая горнодобывающую, автомобильную, аэрокосмическую, химическую и ядерную.
Металлический вольфрам, например, используется в ламповых нитях. Сплавы рения используются в гироскопах и ядерных реакторах. А ниобиевые сплавы используются для форсунок жидкостных ракетных двигателей.
9. Черные и цветные металлы

Валы-шестерни из (черной) нержавеющей стали
Черные металлы: Сталь, чугун, сплавы железа.
Цветные металлы: Медь, алюминий, свинец, цинк, серебро, золото.
Термин "железо" происходит от латинского слова "Ferrum", что переводится как "железо". Таким образом, термин "черный металл" обычно означает "содержащий железо", тогда как "цветной металл" означает металлы и сплавы, которые не содержат достаточного количества железа.
Поскольку черные металлы могут иметь широкий спектр легирующих элементов, которые значительно изменяют их характеристики, очень трудно поместить свойства всех черных металлов под один зонт. Тем не менее некоторые обобщения могут быть сделаны, например, большинство черных металлов являются твердыми и магнитными.
Черные металлы используются для применения с высокой нагрузкой и низкой скоростью, в то время как цветные металлы предпочтительны для применения с высокой скоростью и нулевой нагрузкой для применения с низкой нагрузкой.
Сталь является наиболее распространенным черным металлом. Она составляет около 80% всего металлического материала благодаря своей доступности, высокой прочности, низкой стоимости, простоте изготовления и широкому спектру свойств. Она широко используется в строительстве и обрабатывающей промышленности. Фактически, рост производства стали показывает общее развитие промышленного мира.
8. Цветные и благородные металлы

Ассортимент благородных металлов
Цветные металлы: медь, алюминий, олово, никель, цинк
Благородные металлы: родий, ртуть, серебро, рутений, осмий, иридий
Цветные металлы - это обычные и недорогие металлы, которые корродируют, окисляются или тускнеют быстрее, чем другие металлы, когда подвергаются воздействию воздуха или влаги. Они в изобилии встречаются в природе и легко добываются.
Они широко используются в промышленных и коммерческих целях и имеют неоценимое значение для мировой экономики благодаря своей полезности и повсеместности. Некоторые цветные металлы обладают отличительными характеристиками, которые не могут быть продублированы другими металлами. Например, цинк используется для гальванизации стали, чтобы защитить ее от коррозии, а никель - для изготовления нержавеющей стали.
Благородные металлы, с другой стороны, устойчивы к окислению и коррозии во влажном воздухе. Согласно атомной физике, благородные металлы имеют заполненный электрон d-диапазона. В соответствии с этим строгим определением, медь, серебро и золото являются благородными металлами.
Они находят применение в таких областях, как орнамент, металлургия и высокие технологии. Их точное использование варьируется от одного элемента к другому. Некоторые благородные металлы, такие как родий, используются в качестве катализаторов в химической и автомобильной промышленности.
7. Драгоценные металлы

Родий: 1 грамм порошка, 1 грамм прессованного цилиндра и 1 г аргонодуговой переплавленной гранулы
Примеры: палладий, золото, платина, серебро, родий.
Драгоценные металлы считаются редкими и имеют высокую экономическую ценность. Химически они менее реакционноспособны, чем большинство элементов (включая благородные металлы). Они также пластичны и имеют высокий блеск.
Несколько веков назад эти металлы использовались в качестве валюты. Но сейчас они в основном рассматриваются как промышленные товары и инвестиции. Многие инвесторы покупают драгоценные металлы (в основном золото), чтобы диверсифицировать свои портфели или победить инфляцию.
Серебро - второй по популярности драгоценный металл для ювелирных изделий (после золота). Однако его значение выходит далеко за рамки красоты. Оно обладает исключительно высокой тепло- и электропроводностью и чрезвычайно низким контактным сопротивлением. Именно поэтому серебро широко используется в электронике, батареях и противомикробных препаратах.
Классификация по химическим свойствам
6. Щелочные металлы

Твердый металлический натрий
Примеры: натрий, калий, рубидий, литий, цезий и франций.
Щелочь относится к основной природе гидроксидов металлов. Когда эти металлы реагируют с водой, они образуют сильные основания, которые легко нейтрализуют кислоты.
Они настолько реактивны, что обычно встречаются в природе в слиянии с другими веществами. Карналлит (хлорид калия-магния) и сильвин (хлорид калия), например, растворимы в воде и, таким образом, легко извлекаются и очищаются. Нерастворимые в воде щелочи, такие, как фторид лития, также существуют в земной коре.
Одно из самых популярных применений щелочных металлов - использование цезия и рубидия в атомных часах, наиболее точных из известных эталонов времени и частоты. Литий используется в качестве анода в литиевых батареях, композиты калия используются в качестве удобрений, а ионы рубидия используются в фиолетовых фейерверках. Чистый металлический натрий широко используется в натриевых лампах, которые очень эффективно излучают свет.
5. Щелочноземельные металлы

Изумрудный кристалл, основной минерал бериллия.
Примеры: бериллий, кальций, магний, барий, стронций и радий.
Щелочноземельные металлы в стандартных условиях мягкие и серебристо-белые. Они имеют низкую плотность, температуру кипения и температуру плавления. Хотя они не так реакционноспособны, как щелочные металлы, они очень легко образуют связи с элементами. Как правило, они вступают в реакцию с галогенами, образуя галогениды щелочноземельных металлов.
Все они встречаются в земной коре, кроме радия, который является радиоактивным элементом. Радий уже распадался в ранней истории Земли из-за относительно короткого периода полураспада (1600 лет). Современные образцы поступают из цепочки распада урана и тория.
Щелочноземельные металлы имеют широкий спектр применения. Бериллий, например, используется в полупроводниках, теплопроводниках, электрических изоляторах и в военных целях. Магний часто сплавляют с цинком или алюминием для получения материалов со специфическими свойствами. Кальций в основном используется в качестве восстановителя, а барий используется в вакуумных трубках для удаления газов.
4. Переходные металлы
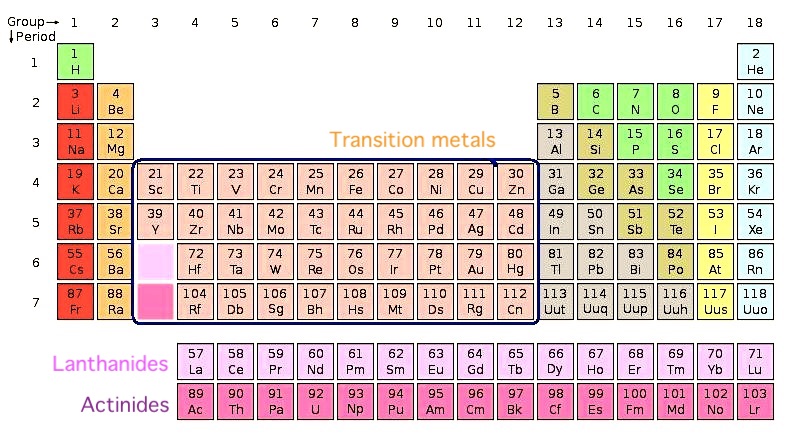
Примеры: титан, ванадий, хром, никель, серебро, вольфрам, платина, кобальт.
Большинство элементов используют электроны из своей внешней оболочки для связи с другими элементами. Переходные металлы, однако, могут использовать две крайние оболочки для соединения с другими элементами. Это химическая особенность, которая позволяет им связываться со многими различными элементами в различных формах.
Они занимают среднюю часть таблицы Менделеева, служа мостом между (или переходом) между двумя сторонами таблицы. Более конкретно, есть 38 переходных металлов в группах с 3 по 12 периодической таблицы. Все они являются пластичными, податливыми и хорошими проводниками тепла и электричества.
Многие из этих металлов, такие как медь, никель, железо и титан, используются в конструкциях и в электронике. Большинство из них образуют полезные сплавы друг с другом и с другими металлическими веществами. Некоторые из них, включая золото, серебро и платину, называются благородными металлами, потому что они крайне инертны и устойчивы к кислотам.
3. Постпереходные металлы

Висмут в виде синтетических кристаллов
Примеры: алюминий, галлий, олово, свинец, таллий, индий, висмут.
Постпереходные металлы в периодической таблице - это элементы, расположенные справа от переходных металлов и слева от металлоидов. Из-за своих свойств они также называются "бедными" или "другими" металлами.
Физически они хрупки (или мягки) и имеют более низкую температуру плавления и механическую прочность, чем переходные металлы. Их кристаллическая структура довольно сложна: они проявляют ковалентные или направленные эффекты связи.
Различные металлы этого семейства имеют различное применение. Алюминий, например, используется для изготовления оконных рам, кухонной посуды, банок, фольги, деталей автомобилей. Оловянные сплавы используются в мягких припоях, оловянных и сверхпроводящих магнитах.
Индиевые сплавы используются для изготовления плоских дисплеев и сенсорных экранов, а галлий - в топливных элементах и полупроводниках.
2. Лантаноиды

1-сантиметровый кусок чистого лантана
Примеры: лантан, церий, прометий, гадолиний, тербий, иттербий, лютеций.
Лантаноиды - это редкоземельные металлы с атомными номерами от 57 до 71. Впервые они были обнаружены в 1787 году в необычном черном минерале (гадолините), обнаруженном в Иттербю, Швеция. Позже минерал был разделен на различные элементы лантаноидов.
Лантаноиды - это металлы с высокой плотностью, плотность которых колеблется от 6,1 до 9,8 г/см³, и они, как правило, имеют очень высокие температуры кипения (1200-3500 °C) и очень высокие температуры плавления (800-1600 °C).
Сплавы лантаноидов используются в металлургии из-за их сильных восстановительных способностей. Около 15 000 тонн лантаноидов ежегодно расходуется в качестве катализаторов и при производстве стекол. Они также широко используются в лазерах и оптических усилителях.
Некоторые исследования показывают, что лантаноиды могут быть использованы в качестве противораковых средств. Лантан и церий, в частности, могут подавлять пролиферацию раковых клеток и способствовать цитотоксичности.
1. Актиниды

Металлический уран, высокообогащенный ураном-235
Примеры: актиний, уран, торий, плутоний, фермий, нобелий, лоренций
Подобно лантаноидам, актиниды образуют семейство редкоземельных элементов с аналогичными свойствами. Они представляют собой серию из 15 последовательных химических элементов в периодической системе от атомных номеров 89 до 103.
Все они радиоактивны по своей природе. Синтетически произведенный плутоний, а также природные уран и торий являются наиболее распространенными актинидами на Земле. Первым актинидом, который был открыт в 1789 году, был уран. И большая часть существующих продуктов актинидов была произведена в 20 веке.
Их свойства, такие как излучение радиоактивности, пирофорность, токсичность и ядерная критичность, делают их опасными для обращения. Сегодня значительная часть (кратковременных) актинидов производится ускорителями частиц в исследовательских целях.
Некоторые актиниды нашли применение в повседневной жизни, например, газовые баллоны (торий) и детекторы дыма (америций), большинство из них используются в качестве топлива в ядерных реакторах и для изготовления ядерного оружия. Уран-235 является наиболее важным изотопом для применения в ядерной энергетике, который широко используется в тепловых реакторах.
Хрупкие металлы – перечень, особенности обработки и использования
Металл ассоциируется с надежностью, прочностью, твердостью. Хрупкость – это атрибут стекла и подобных материалов. Однако и в металлическом сегменте есть «стекло».
Хрупкими могут стать изначально пластичные элементы.

Что представляют собой
Хрупкость – антипод пластичности. Это свойство вещества разрушаться без визуально различимых деформаций. То есть на изломе, например, цинковой проволоки цвет, блеск, структура не изменятся.
Хрупкие металлы подразделяются на две группы:
- Наделенные этим свойством от природы.
- Ставшие таковыми в результате обработки.
Ко второй группе причисляются также сплавы.
Причины уязвимости
Склонность к разрушению у металлов, других простых веществ, сплавов обусловлена следующими причинами:
- Структура. Например, у сурьмы это крупные зерна. У стали – доминирование в структуре а-фазы.
Переход металла в хрупкое состояние происходит при разных температурах.
- Скорость нагрузки. Чем быстрее возрастает нагрузка на материал, тем быстрее он разрушится. Резкие удары способны погубить даже пластичные структуры (малоуглеродистую сталь).
Сплавы становятся хрупкими из-за примесей:
- Самый «вредный» химический элемент – углерод. Он делает сплавы железа (чугун, сталь) хрупче в разы.
- Сталь с фосфором обретает хладноломкость.
- При малейшем «загрязнении» пластичный хром становится неподатливым к обработке.
«Стеклянными» сплавы делают фосфор, сера, мышьяк, сурьма, вольфрам.
Этот изъян не устранили даже создатели материалов поколения 2.0. Например, «супервещества» алюминид титана. Этот титаново-алюминиевый серебристый конгломерат термо-, коррозиестоек, но перед кувалдой бессилен.
Список
К металлам с изначальной хрупкостью относятся природные и технологичные материалы.
- Щелочноземельные – бериллий.
- Легкоплавкие – олово, висмут.
- Тяжелые элементы – цинк, марганец, хром, сурьма, кобальт.
В списке присутствуют уникумы:
- Вольфрам. Самый прочный на растяжение среди металлов. . Твердый хрупкий платиноид голубовато-серебристого цвета, второй по плотности среди простых веществ, тугоплавкий. . Мягкий хрупкий белый металл.
Самый хрупкий металл – сурьма. Ее легко сделать порошком вручную.
Материалы, полученные в результате технологических процессов: бронза, белый чугун, сталь с высоким содержанием углерода.
Особенности обработки
Материалы, наделенные хрупкостью, разрушаются при попытке их удлинить даже на пару процентов.
Поэтому их обработка специфична:
- Перед работой материал подогревают, чтобы нейтрализовать хладноломкость.
- Исключено воздействие давлением. Например, чугун (нагретый либо холодный) после такой операции сохранит форму, но внутренне разрушится.
- Болванки из хрупких сплавов (чугунные, бронзовые) рубят от края к центру.
Неоднозначно воздействие закалки. В отличие от подогрева, при такой обработке кратно увеличивается прочность стали, других материалов, но в ущерб пластичности. То есть порог хрупкости понижается.
Хрупкие металлы легче разрушить растяжением, чем сжатием.
Где используются
Малопластичные вещества используют там, где исключено резкое механическое воздействие:
- Производство катализаторов.
- Электроника.
- Лаки, краски.
- Аптечные препараты.
- Косметические средства.
Алюминид титана задействуют в космических технологиях и медицине.
Тяжелые металлы – перечень, свойства и риски элементов
Официально такой группы химических элементов не существует. Однако металлурги, аграрии, особенно экологи, оперируют понятием «тяжелые металлы». Этот сегмент привлекает повышенное внимание.

Что представляют собой
Термин «тяжелые металлы» еще двести лет назад пытался ввести в научный оборот немецкий химик Лео Гмелин.
Однако в номенклатуре Международного союза, курирующего вопросы теории и практики химии (IUPAC), такое подразделение отсутствует.
Промышленность
В академических и промышленных кругах циркулирует четыре десятка критериев, по которым металл признается тяжелым.
Самые популярные основания:
- Атомный номер выше 50.
- Плотность 5+ г/см3.
На практике чаще востребован второй критерий.
То есть к тяжелым металлам относятся элементы с плотностью, превышающей 5 г/см3.
В соответствии с ним таковыми считаются:
- Традиционные: железо, медь, хром, марганец, кобальт, олово, свинец, никель, цинк.
- Менее известные: кадмий, молибден, вольфрам, сурьма. Плюс экзотика – галлий, теллур.
- И самые коварные – ртуть, таллий, висмут.
На бытовом уровне они считаются токсичными элементами. Подобное отождествление некорректно.
Не каждый тяжелый металл токсичен, но таким способно стать при благоприятных условиях безобидное вещество.
Экология, медицина
У экологов и врачей свои подходы. Для них тяжелыми металлами являются особо значимые (полезные либо опасные) для биологических организмов элементы.
Суровее критерии Организации Объединенных наций (ООН). В соответствии с ее экологической доктриной, тяжелыми считаются стабильные металлы либо металлоиды, их соединения (особенно соли тяжелых металлов) с плотностью более 4,5 г/см3.
Критерий действует с 1998 года.
Классификация
Кроме плотности, маркером принадлежности к группе служат температура плавления, степень использования, другие свойства.
На основании этого выделяют следующие виды тяжелых металлов:
- – цинк, медь, олово, свинец, никель. – железо.
- Редкие – галлий, висмут, таллий, кадмий. – молибден, вольфрам, хром. – кадмий, кобальт, свинец, ртуть, олово, галлий, таллий, висмут.
Самый тяжелый металл планеты – иридий. Кубик с ребром в 1 см весит 22,6 грамма. Но вещество попадает на Землю только с метеоритами.

Иридий
В сегменте обычных земных «тяжеловесов» лидирует вольфрам – он на три грамма легче. Это восьмая позиция среди металлов.
Откуда берутся
Естественных поставщиков тяжелых металлов четыре:
- Горное сырье. Чаще это магматические либо осадочные породы.
- Породообразующие минералы. У меди, например, это малахит и другие минералы.
- Вулканы. Частицы вещества извергаются попутно с вулканическими продуктами (газами, гейзерами).
Еще один источник – Вселенная. Вещество заносится в стратосферу метеоритами либо облаками космической пыли.
Получение продукта
На большинстве металлургических комбинатах сырье плавят в доменных и мартеновских печах. Это оборудование из позапрошлого века делает процесс тяжелым, опасным для экологии и человека.
Внедрение « зеленых » технологий продвигается медленно, поскольку требует инвестиций.
Результат недостаточной очистки отходов производства – высокое содержание вредных компонентов. Следствие – загрязнение почвы, воды, воздуха.
Влияние на экологию
Особо опасные загрязнители биосферы – именно тяжелые металлы. Самая вредная форма соединений – соли.
Пути поступления
Загрязнение биосферы происходит следующими способами:
- Металлургия. Выбросы в процессе плавки, обжига. Вымывание тяжелых веществ из отвалов месторождений либо меткомбинатов водой, выветривание.
- Агросектор. Полив плантаций, удобрение полей илом бытовых стоков либо пестицидами.
- Быт. Использование как топлива торфа, угля, другого сырья.
- Автобаны. Свинцом, цинком, кадмием насыщены обочины автострад.
Свинец пропитывает почву минимум на 100 м по обе стороны дороги.

Свинец
Способы очищения
Почва очищается от такого груза десятилетиями, иногда столетиями.
Концентрация цинка уменьшается наполовину спустя столетие, кадмию требуется вдвое меньше.
Медь исчезает через три столетия, свинец – через десять:
- Токсичные соединения растворяются в воде.
- В почве процесс активируют влажность и растительность.
Флора вытягивает «свои» металлы. Так, лишайники «кушают» цинк, никель, медь.

Самородная медь
Токсичность тяжелых металлов возрастает с увеличением атомного номера.
Воздействие на человека
Влияние большинства таких веществ двояко:
- Микродозы цинка, железа, меди задействованы в биологических процессах. Например, поддержании уровня гемоглобина в крови.
- Превышение микродоз опасно: тормозится работа нервной системы, сердца, почек, других органов. Разрушается скелет, идет разбалансировка жизненных процессов.
- Токсичны бесполезные свинец, ртуть.
Отравление организма внешне проявляется как тошнота, рвота, головная боль, нарушение координации движений. Плюс более тяжелые последствия, до летального исхода.
В зоне риска следующие категории:
- Работники меткомбинатов.
- Жители мегаполисов, окрестностей автострад.
- Потребители продуктов со стихийных рынков (не прошедших санитарный контроль).
Уровень загрязненности территории экологи определяют благодаря местным животным.
Чуткие «индикаторы» загрязненности на европейской части – лоси, мышь-полевка, кроты, бурый мишка.
10 самых-самых металлов планеты

Миллионы лет назад наши далекие предки изготавливали себе инструменты из дерева и камней, но спустя тысячелетия они научились пользоваться металлами. С этого момента человечество начало развиваться немыслимыми темпами, и всё дошло до того, что большинство окружающих нас объектов сделано из железа, алюминия и других разновидностей этого материала.
Практически все металлы хорошо проводят электричество и тепло, при определенных условиях они пластичны и отлично подходят для изготовления различных деталей для электроники, а также обладают характерным металлическим блеском. Но в периодической таблице Менделеева есть металлы, которые обладают уникальными свойствами, которыми не могут похвастаться все остальные. Они по-своему удивительны, и когда-то давно этим металлам присваивали чуть ли не волшебные качества. Итак, давайте перечислим их, а также узнаем о свойствах и других интересных особенностях.
Самый жидкий металл

Ртуть считается самым жидким металлом и, в то же время, одним из самых опасных для человеческого организма. Он практически всегда пребывает в жидком состоянии, потому что температура его плавления равна -38 градусам Цельсия. Именно поэтому этот металл используется в градусниках — при увеличении температуры, жидкость расширяется. Поскольку градусник сделан в виде стеклянной трубочки, расширяться она может только в одном направлении. Чтобы на показатели градусника не влияли другие условия вроде атмосферного давления, из трубочки выкачан воздух.
В средневековье считалось, что при смешивании ртути, серы и загадочного «философского камня» можно получить чистое золото. Поэтому внимания этому металлу уделялось очень много. С средние века получить из ртути золота никому не удалось, но это стало под силу ученым в 1947 году — они поместили 100 миллиграмм ртути в атомный реактор и получили 35 микрограмм золота. Вот и второе удивительное свойство ртути — его можно превратить в золото, но это слишком дорогой процесс.
Третья особенность ртути заключается в том, что при вдыхании его паров человек получает сильное отравление — опасные вещества оседают в легких. Симптомы отравления включают в себя слабость, понижение аппетита, боль при глотании, набухание десен и сильная боль в животе. Из-за своей ядовитости, ртуть входит в десятку химических веществ, представляющих опасность для общественного здоровья.
Самый тугоплавкий металл

А теперь давайте поговорим о полной противоположности ртути — металле, именуемом как вольфрам. В то время как ртуть может расплавиться на человеческой ладони, для расплавления вольфрама необходима температура на уровне 3422 градусов Цельсия.
Сам по себе вольфрам не опасен, но изделия, в котором он используется, могут убить. Этот металл часто используется как наконечник патронов, которые могут пробить даже бронежилет. Только его добавляют совсем чуть-чуть, потому что вольфрам — очень тяжелый металл.
Из-за своей тугоплавкости вольфрам трудно поддается деформации, поэтому в чистом виде его используют очень редко. Как правило, изделия из вольфрама имеют и другие примеси — они делают его более податливым и значительно уменьшают вес.
Самый твердый металл

Самым твердым и при этом легким металлом на нашей планете считается титан. Благодаря своим свойствам он активно используется в авиации и кораблестроении — материал отлично подходит для изготовления корпусов самолетов и кораблей. К тому же, благодаря прочности и легкости, из титана изготавливают бронежилеты. Этот металл безопасен для человеческого организма, поэтому часто применяется в медицине для изготовления инструментов и даже протезов — искусственных частей тела.
При нагревании титан начинает поглощать кислород, хлор, азот и другие газы. Благодаря этому удивительному свойству, металл используется в различных фильтрах — пропуская различные газы через нагретые до 600 градусов Цельсия титановые трубки, можно очистить их от примесей. Таким же образом можно очистить воду от кислорода, что особенно полезно в пищевой промышленности. Считается, что содержащийся в воде кислород ухудшает качество некоторых продуктов — как минимум, он может сократить срок годности пива.
Самый радиоактивный металл
Единственным металлом, который может использоваться в качестве топлива в ядерных реакторах, является уран. Многие люди считают его очень опасным из-за высокой радиоактивности. Однако природный уран безопасен для здоровья человека, а опасность представляет его разновидность под названием U-235 — именно она используется в ядерных реакторах.

Когда-то давно из природного урана даже изготавливали посуду. Например, осколки желтого стекла с содержанием урана были найдены на территории итальянского города Неаполь — по расчетам ученых, стекло было изготовлено в 79 году нашей эры. Он был безопасен для людей и никаких намеков на радиацию вроде свечения не наблюдалось.
Природного урана U-235, пригодного для использования в ядерных реакторах, сегодня в природе очень мало — на протяжении долгих лет он просто улетучился. Зато миллиарды лет назад его было очень много, и ядерные реакции могли запускаться прямо на природе, без участия человека. Так, на территории африканской страны Габон, около 1,8 миллиарда лет назад происходила естественная реакция деления ядер урана. Уран горел на протяжении сотен лет, но в итоге реакция прекратилась из-за истощения запасов металла.
Самый тяжелый металл

Самым тяжелым металлом из всей таблицы Менделеева считается осмий. Его удивительным свойством является то, что будучи самым тяжелым, на воздухе он становится летучим, ядовитым веществом. Название «осмий» с древнегреческого языка можно перевести как «запах». Такое наименование металлу было дано неспроста — в 1803 году английский химик Смитсон Теннант (Smithson Tennant) на собственном опыте ощутил, что металл пахнет хлором и неприятен настолько, что раздражает горло.
Благодаря своей твердости, осмий часто используется в механизмах, а именно в местах, где происходит сильное трение. Также он используется в изготовлении нитей для ламп накаливания. Ядовитые свойства возникают только на открытом воздухе — металл превращается в токсичное вещество тетраоксид осмия, которое вызывает раздражение глаз, поражение верхних дыхательных путей и даже воспаление почек.
Самый стойкий металл
Самым стойким металлом считается иридий — его невозможно растворить ни в одной кислоте. Из-за стойкости, этот металл используется в Международном бюро мер и весов — из него создан эталон килограмма. Этот цилиндр из иридия необходим для того, чтобы у всех стран было единое представление о том, сколько именно должен весить килограмм. Это важно, потому что любое отклонение может стать причиной неисправности в самолётах и кораблях и, впоследствии, серьезной катастрофы.

Также иридий используется при изготовлении денег. Например, в африканской стране Руанде была выпущена иридиевая монета номиналом 10 руандийских франков. Можно сказать, что это самая устойчивая к химическому воздействию монета. Повредить ее можно разве что кину в сосуд со фтором — сильнейшим окислителем. Но разрушительная реакция начнется только при нагревании до 450 градусов Цельсия.
Самый дорогой металл

Многие люди инвестируют в металлы и одним из самых дорогих сегодня является золото. По курсу за июнь 2020 года, грамм золота стоит около 4000 рублей, тогда как цена той же массы платины еле достигает 2000 рублей. Чуть выше мы уже выяснили, что добывать золото из ртути — это очень дорогой процесс. Поэтому получением золота занимаются работники аффинажных заводов — грубо говоря, они извлекают золота из смесей других металлов.
Так как персонал работает с очень дорогим металлом, в заводах действует строгий контроль. Если у человека, например, есть золотой зуб — охрана всегда проверяет, находится ли он на месте. А то вдруг человек избавится от золотого зуба и решит пронести кусочек драгоценного металла, поместив его в освободившемся пространстве между зубами? В некоторых аффинажных заводах работники проходят внутрь голыми и облачаются в рабочую одежду внутри.
Самый редкий металл

Франций — самый редкий металл. По расчетам ученых, в земной коре его концентрация равна всего лишь 340 граммам.
Франций очень радиоактивен, поэтому на данный момент он практически нигде не используется. Однако иногда ученые все же используют разновидности франция в ходе научных исследований. Также предпринимались попытки диагностики рака с использованием технологий, где франций тоже был задействован.
Самый легкий металл
Звание самого легкого металла по праву достается литию. Он окрашен в серебристо-белый цвет и настолько мягок, что легко режется ножом. Так как он является самым легким металлом в таблице Менделеева, при попадании в воду он всплывает на поверхность.
Читайте также:
