Вытеснение металлов из растворов солей другими металлами
Обновлено: 08.05.2024
Металлы в химических реакциях всегда восстановители. Восстановительную активность металла отображает его положение в электрохимическом ряду напряжений.
На основании ряда можно сделать следующие выводы:
1. Чем левее стоит металл в этом ряду, тем более сильным восстановителем он является.
2. Каждый металл способен вытеснять из солей в растворе те металлы, которые стоят правее
3. Металлы, находящиеся в ряду напряжений левее водорода способны вытеснять его из кислот.
Zn + 2HCl → ZnCl2 + H2
4. Металлы, являющиеся самыми сильными восстановителями (щелочные и щелочноземельные) в любых водных растворах прежде сего реагируют с водой.
Восстановительная способность металла, определённая по электрохимическому ряду не всегда соответствует его положению в периодической системе т.к в ряду напряжений учитывается не только радиус атома, но и энергия отрыва электронов.
Альдегиды, их строение и свойства. Получение, применение муравьиного и уксусного альдегидов.
Альдегиды – это органические соединения, в состав молекулы которых входит карбонильная группа, соединённая с водородом и углеводородным радикалом.
Физические свойства
Метаналь – газообразное вещество, водный раствор – формалинь
Химические свойства
Реактивом на альдегиды является Cu(OH)2
Применение
Наибольшее применение имеют метаналь и этаналь. Большое количество метаналя используется для получения фенолформальдегидной смолы, которую получают при взаимодействии метаналя с фенолом. Эта смола необходима для производства различных пластмасс. Пластмассы изготовлены для из фенолформальдегидной смолы в сочетании с различными наполнителями, называются фенопластами. При растворении фенолформальдегидной смолы в ацетоне или спирту получают различные лаки. При взаимодействии метаналя с карбамидом CO(NH2)2 получают карбидную смолу, а из нее – аминопласты. Из этих пластмасс изготавливают микропористые материалы для нужд электротехники.Метаналь идёт так же на производство некоторых лекарственных веществ и красителей. Широко применяется водный раствор, содержащий в массовых долях 40% метаналя. Он называетсяформалином. Его использование основано на свойстве свёртывать белок.
Получение
Альдегиды получают окислением алканов и спиртов. Этаналь получают гидротациейэтина и окислением этена.
Билет №12
Высшие оксиды химических элементов третьего периода. Закономерности в измерении их свойств в связи с положением химических элементов в периодической системе. Характерные химические свойства оксидов: основных, амфотерных, кислотных.
Оксиды – это сложные вещества, состоящие из двух химических элементов, один из которых является кислород со степенью окисления «-2»
С увеличением степени окисления элементов, увеличиваются кислотные свойства оксидов.
Na2O, MgO – основные оксиды
Al2O3 – амфотерный оксид
Основные оксиды реагируют с кислотами с образованием соли и воды.
Оксиды щелочных и щелочноземельных металлов реагируют с водой с образованием щёлочи.
Na2O + HOH → 2NaOH
Основные оксиды реагируют с кислотными оксидами с образованием соли.
Na2O + SO2 → Na2SO3
Кислотные оксиды реагируют со щелочами с образованием соли и воды
Реагирует с водой, с образованием кислоты
Амфотерные оксиды реагируют с кислотами и щелочами
Жиры, их свойства и состав. Жиры в природе, превращение жиров в организме. Продукты технической переработки жиров, понятие о синтетических моющих средствах. Защита природы от загрязнения СМС.
Жиры – это сложные эфиры глицерина и карбоновых кислот.
Общая формула жиров:
Твёрдые жиры образованы преимущественно высщими предельными карбоновыми кислотами – стеариновой C17H35COOH, пальмитиновой C15H31COOH и некоторыми другими. Жидкие жиры образованы главным образом высшими непредельными карбоновыми кислотами – олеиновойC17H33COOH, ленолевойC17H31COOH
Жиры наряду с углеводородами и белками входят в состав организмов животных и растений. Они являются важной составной частью пищи человека и животных. При окислении жиров в организме выделяется энергия. Когда в органы пищеварения поступают жиры, то под влиянием ферментов они гидролизуются на глицерин и соответствующие кислоты.
Продукты гидролиза всасываются ворсинками кишечника, а затем синтезируется жир, но уже свойственный организм. Потоком крови жиры переносятся в другие органы и ткани организма, где накапливаются или снова гидролизуются и постепенно окисляются до оксида углерода (IV) и воды.
Физические свойства.
Животные жиры в большинстве случаев твёрдые вещества, но встречаются и жидкие (рыбий жир). Растительные жиры чаше всего жидкие вещества – масла; известны и твёрдые растительные жиры – кокосовое масло.
Химические свойства.
Жиры в животных организмах в присутствии ферментов гидролизуются. Кроме реакций с водой, жиры взаимодействуют со щелочами.
В состав растительных масел входят сложные эфиры непредельных карбоновых кислот, то их можно подвергнуть гидрированию. Они превращаются в предельные соединения
Пример: Из растительного масла в промышленности получают маргарин.
Применение.
Жиры в основном применяют в качестве пищевого продукта. Раньше жиры использовали для получения мыла
Синтетические моющие средства.
Синтетические моющие средства оказывают вредное действие на окружающую среду, т.к. они устойчивы и с трудом подвергаются разрушению.
Металлы их положение в периодической системе химических элементов Д.И.Менделеева, строение их атомов, металлическая связь. Общие химические свойства металлов.
Известно, что от периода к периоду число металлов, составляющих главные подгруппы, увеличивается. Это связано с тем, что от периода к периоду радиус атома, как правило, увеличивается, поэтому внешние электроны становятся более свободными. Это в значительной степени и определяет, будет элемент металлом или нет. Например, во втором периоде имеется только два металла – литий и бериллий; в состав третьего периода входят три металла – натрий, магний и алюминий. Эту закономерность среди элементов главных подгрупп можно продолжить.
Кроме того, все элементы побочных подгрупп – металлы, они имеют на внешнем слое, как правило, 1-2 электрона, это во многом определяет их свойства.
У металлов главных подгрупп, как правило, на внешнем слое может быть от одного до трёх электронов, однако некоторые из них могут иметь существенно большее число электронов. Например, элемент полоний на внешнем слое имеет шесть электронов. Но этот элемент принадлежит (IV) периоду. Поэтому свойства простого вещества полония сильно отличаются от свойств, например, кислорода или серы, хотя они представители одной подгруппы.
Лёгкость выхода внешних электронов из атомов металлов определяет их свойства как восстановителей. Восстановители – это элементы, повышающие свою степень окисления в процессе реакции. Это происходит, в следствие отдачи электронов окислителям.
Восстановительные свойства металлов проявляются в следующих реакциях:
а) с неметаллами
в данной реакции металл Fe восстановитель, а катион Cu 2+ окислитель.
Электрохимический ряд напряжения металлов. Вытеснение металлов из растворов солей другими металлами.
- Общие свойства металлов как восстановителей.
- Характеристика активности металлов.
- Вытеснение металлов из растворов солей.
Общим свойством металлов является их способность к окислению: Ме 0 -ne - →Me n + . Способность отдавать электроны у металлов проявляется по-разному: наиболее активные щелочные металлы и кальций, они восстанавливают водород даже из воды:
К 0 -1е - →К +1 восстановитель
2Н +1 +2е - →Н2 0 окислитель
Менее активные восстановители – магний, алюминий, цинк и др., ещё менее активны железо, свинец: эти металлы восстанавливают водород из водных растворов кислот, а из растворов солей менее активных металлов – металл.
Zn 0 -2e - →Zn +2 восстановитель
Fe 0 -3e - →Fe +3 восстановитель.
Русский химик Н.Н.Бекетов расположил металлы в порядке убывания их восстановительной активности в водных растворах и назвал его электрохимический ряд напряжения металлов (приложение 5). При этом следует помнить следующее правила: каждый левее стоящий металл может вытеснять все последующие из водных растворов их солей, а сам вытесняется предыдущими металлами. В этом ряде следует обратить внимание на водород как единственный неметалл, имеющий с металлами общее свойство – способность образовывать положительно заряженные ионы. Поэтому водород может замещать некоторые металлы и сам замещаться активными металлами из водных растворов кислот и воды.
Вытеснение менее активных металлов из растворов их солей более активными металлами происходит в соответствии с рядом напряжения. Можно привести дополнительные примеры взаимодействия щелочных металлов с водой.
Разделение и осаждение металлов, получение конечных продуктов
Наиболее распространенные методы разделения и выделения металлов и их соединений из растворов — осаждение (электролиз, цементация, перевод в нерастворимые соединения, кристаллизация), сорбция, экстракция. Выбор наиболее рационального метода должен производиться в каждом отдельном случае с учетом ряда факторов, из которых первостепенное значение имеют состав поступающего на осаждение раствора и требования, предъявляемые к чистоте конечной продукции. Например, в медной промышленности применяют электролиз для переработки богатых растворов и цементацию меди — для осаждения меди при концентрации менее 15 г/л [20, 76].
Осаждение металлов производят электролизом, цементацией, восстановлением соединений до металла водородом, разложением комплексных солей.
Электролиз используют для извлечения металлов из очищенных растворов после выщелачивания (электроосаждение) и для получения чистых металлов из черновых продуктов (электрорафинирование). Этот метод получил широкое применение в гидрометаллургии меди, цинка, кадмия и марганца.
При цементации вытеснение ионов одного металла из растворов его солей производя ионами другого металла, расположенного выше в ряду напряжений (более электроотрицательного). Медь цементируют железом; или чугунной стружкой, железным скрапом губчатым железом, обезоловяненными консервными банками; золото — цинковой стружкой, цинковой и алюминиевой пылью; кадмий — цинковой пылью, никель —
кобальтовым порошком. Цементацию металлов производят в различных. аппаратах периодического или непрерывного действия (конусах барабанах, желобах, чанах, ваннах, аппаратах кипящего слоя).
Кроме того, никель, кобальт и медь осаждают из аммиачных растворов восстановлением их до металла водородом под давлением 3,5—5 МПа.
Осаждение меди или никеля из аммиачных растворов производят также разложением образовавшихся при выщелачивании комплексных углеаммониевых солей этих металлов. Медь осаждается в виде черной окиси меди, а никель — в виде карбоната. В результате дистилляции получают газообразный амиак и углекислоту, которые улавливают и вновь используют в процессе.
Часто металлы осаждаются в виде нерастворимых соединений: гидроокисей, сульфидов, ксантогенатов, карбонатов, вольфраматов, молибдатов и др. При оптимальном рН среды можно практически полностью отделить молибден от вольфрама в виде сульфида из растворов, содержащих вольфрамат натрия тиосоединения молибдена. Большое распространение в гидрометаллургических процeccax получил гидролиз, при котором возможно селективное осаждение некоторых металлов в виде гидроокисей иди основных шей.
При кристаллизации значительная часть извлекаемого металла осаждается в результате упарки и охлаждения раствора или изменения рН среды. Таким образом выделяют из раствора сульфат натрия при хлорирующем обжиге пиритных огарков и сульфат марганца при сернокислотном выщелачивании марганцевых руд. В вольфрамовой и молибденовой промышленности кристаллизацию применяют для получения чистых вольфрамата и молибдата аммония, содержание вредных примесей в которых не должно превышать тысячных долей процента.
В некоторых случаях, особенно при получении полупроводниковых соединений редких металлов, требуется, чтобы суммарное содержание всех примесей не превышало 0,05—0,1%. Поэтому полученные соединения перечищают (растворяют или разлагают их, затем повторно осаждают, часто завершающей стадией осаждения является электролиз, кристаллизация или восстановление до металла водородом).
Сорбционные и экстракционные методы извлечения металлов из растворов для значительного повышения концентрации их и очистки от вредных примесей получили широкое распространение в технологии урановых, золотосодержащих, вольфрамовых, молибденовых, медных и редко-метальных руд [20, 46, 92].
В качестве сорбентов применяют иониты— вещества, способные к обмену ионами с окружающим раствором и практически не растворимые в применяемых в гидрометаллургии растворителях. В зависимости от характера обмениваемых ионов эти вещества делят на катиониты и аниониты.
Наибольшее распространение получила сорбция осветленных растворов в колонках с неподвижным слоем ионита. Однако в урановой и золотодобывающей промышленности успешно внедрена сорбция металла ионитами из жидкой фазы пульпы — бесфильтрационная сорбция. Возможность применения такого способа определяется значительной разницей в крупности ионита и выщелачиваемого материала, что позволяет отделить ионит пропусканием пульпы через сито с отверстиями соответствующего размера. При осуществлении такого варианта ионообменного процесса значительно упрощается и делается более экономичной технологическая схема вследствие исключения операций предварительного фильтрования пульпы. Весьма эффективно совмещение йоннообменной сорбции с выщелачиванием из руды полезных компонентов (ионообменное выщелачивание), позволяющее значительно повысить технико-экономические показатели гидрометаллургического процесса.
Для последующей десорбции металлов из ионитов (элюирование) применяют растворы различных реагентов — нитрата аммоний или натрия, хлористого натрия, аммиака, едкого натра, углекислого натрия, минеральных кислот и др.
Во многих случаях сорбция металлов характеризуется высокими технологическими показателями. Так, емкость анионита по урану составляет 30—50 кг/м 3 смолы в набухшем состоянии, извлечение металла из раствора достигает 98—99,8 %, На 1 м 3 загруженной смолы сорбируется 12—23 кг урана в сутки. Еще более высокая емкость получена по вольфраму и молибдену — до 160 кг/м 3 анионита.
Продолжительность использования ионообменных сорбентов во многих случаях определяется постепенным снижением их емкости вследствие частичного «отравления» ионитов, образования инертных пленок и разрушения обменных групп. Кроме того, неизбежны механические потери ионитов. Например, после двух лет работы опытной установки, на которой уран извлекался непосредственно из пульпы, общие потери ионита вследствие истирания составили 23 %, а емкость уменьшилась на 10 %. Скорость поглощения и элюирования осталась прежней.
В качестве сорбента применяют также активированный уголь, главным образом для сорбции золота и серебра из цианистых растворов.
Очистка растворов от мышьяка и сурьмы, коллоидальной серы и некоторых других вредных примесей осуществляется сорбцией их гидратом окиси железа.
Все большее значение в гидрометаллургии приобретают экстракционные процессы, при которых водный раствор солей металлов вступает в контакт с несмешивающейся с водой органической жидкостью, извлекающей определенные металлы из исходного раствора в виде комплексных соединений. Эффективность экстракционного процесса количественно характеризуется коэффициентом распределения извлекаемого металла
где Y — концентрация металла в органической фазе; X — то же, в водной фазе.
Практически процесс экстракции может быть реализован при коэффициенте распределения металла не менее 0,3—0,5. Высокое извлечение или практически полное разделение металлов достигается при условии противоточного осуществления процесса, когда операция экстракции повторяется многократно.
В ряде случаев при экстракции достигается высокая селекция металлов из растворов, позволяющая осуществить разделение весьма близких по химическим свойствам элементов.
В качестве экстрагентов используют амины, кетоны, карбоновые кислоты, спирты, эфиры, фосфорсодержащие соединения.. В качестве растворителей экстрагентов (разбавителей) применяют углеводороды и их хлорпроизводные.
После отделения органической фазы от водной производится реэкстракцкя металла обработкой органической фазы щелочным или кислым раствором, а иногда только водой. В реэкстракте можно получить концентрацию извлекаемых элементов во много раз выше, чем в исходном растворе.
Экстракцию широко применяют в урановой промышленности. В настоящее время значительные успехи по экстракции достигнуты также в технологии извлечения и очистки многих редких и некоторых цветных металлов — меди, никеля, кобальта, тантала, ниобия, вольфрама, молибдена, рения, индия, германия, гафния и др.
В промышленности для экстракции применяют смесители, отстойники, колонны с насадкой, тарельчатые колонны с пульсацией, центробежные экстракторы и т. д.
Химические свойства металлов

Свойства металлов начинают изучать на уроках химии в 8–9 классе. В этом материале мы подробно разберем химические свойства этой группы элементов, а в конце статьи вы найдете удобную таблицу-шпаргалку для запоминания.
О чем эта статья:
8 класс, 9 класс, ЕГЭ/ОГЭ
Металлы — это химические элементы, атомы которых способны отдавать электроны с внешнего энергетического уровня, превращаясь в положительные ионы (катионы) и проявляя восстановительные свойства.
В окислительно-восстановительных реакциях металлы способны только отдавать электроны, являясь сильными восстановителями. В роли окислителей выступают простые вещества — неметаллы (кислород, фосфор) и сложные вещества (кислоты, соли и т. д.).
Металлы в природе встречаются в виде простых веществ и соединений. Активность металла в химических реакциях определяют, используя электрохимический ряд, который предложил русский ученый Н. Н. Бекетов. По химической активности выделяют три группы металлов.
Ряд активности металлов
Металлы средней активности
Общие химические свойства металлов
Взаимодействие с неметаллами
Щелочные металлы сравнительно легко реагируют с кислородом, но каждый металл проявляет свою индивидуальность:
оксид образует только литий
натрий образует пероксид
калий, рубидий и цезий — надпероксид
Остальные металлы с кислородом образуют оксиды:
2Zn + O2 = 2ZnO (при нагревании)
Металлы, которые в ряду активности расположены левее водорода, при контакте с кислородом воздуха образуют ржавчину. Например, так делает железо:
С галогенами металлы образуют галогениды:
Медный порошок реагирует с хлором и бромом (в эфире):
При взаимодействии с водородом образуются гидриды:
Взаимодействие с серой приводит к образованию сульфидов (реакции протекают при нагревании):
Реакции с фосфором протекают до образования фосфидов (при нагревании):
Основной продукт взаимодействия металла с углеродом — карбид (реакции протекают при нагревании).
Из щелочноземельных металлов с углеродом карбиды образуют литий и натрий:
Калий, рубидий и цезий карбиды не образуют, могут образовывать соединения включения с графитом:
С азотом из металлов IA группы легко реагирует только литий. Реакция протекает при комнатной температуре с образованием нитрида лития:
Взаимодействие с водой
Все металлы I A и IIA группы реагируют с водой, в результате образуются растворимые основания и выделяется H2. Литий реагирует спокойно, держась на поверхности воды, натрий часто воспламеняется, а калий, рубидий и цезий реагируют со взрывом:
Металлы средней активности реагируют с водой только при условии, что металл нагрет до высоких температур. Результат данной реакции — образование оксида.
Неактивные металлы с водой не взаимодействуют.
Взаимодействие с кислотами
Если металл расположен в ряду активности левее водорода, то происходит вытеснение водорода из разбавленных кислот. Данное правило работает в том случае, если в реакции с кислотой образуется растворимая соль.
2Na + 2HCl = 2NaCl + H2
При взаимодействии с кислотами-окислителями, например, азотной, образуется продукт восстановления кислоты, хотя протекание реакции также неоднозначно.
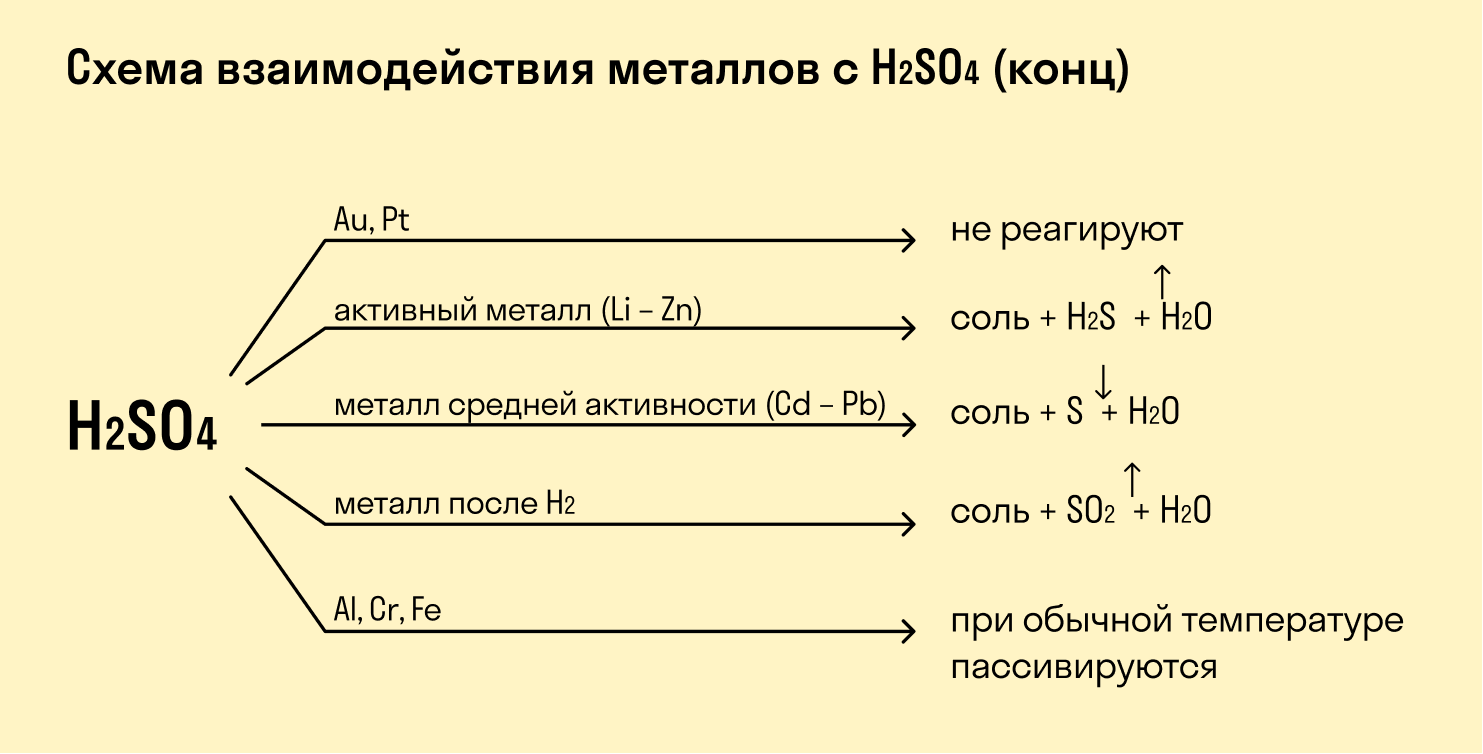
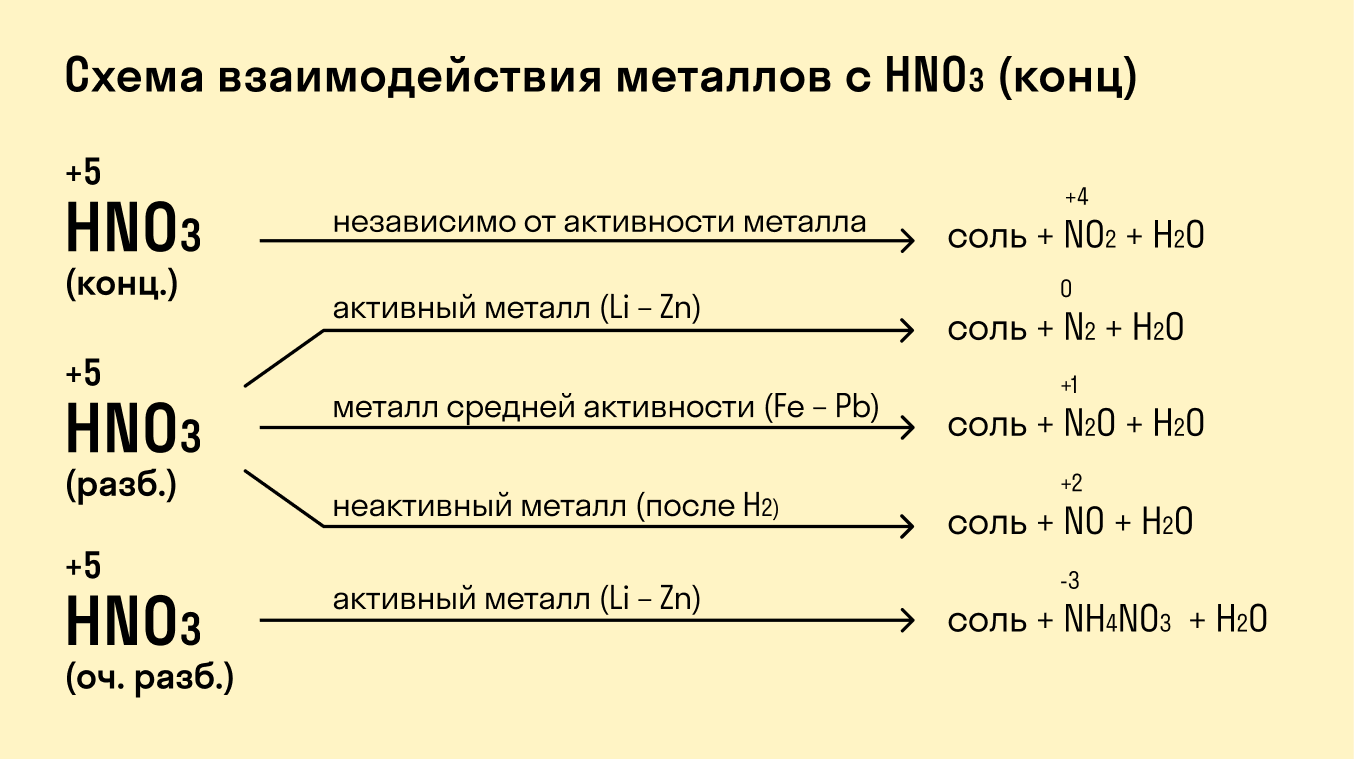
Металлы IА группы:
Металлы IIА группы
Такие металлы, как железо, хром, никель, кобальт на холоде не взаимодействуют с серной кислотой, но при нагревании реакция возможна.
Взаимодействие с солями
Металлы способны вытеснять из растворов солей другие металлы, стоящие в ряду напряжений правее, и могут быть вытеснены металлами, расположенными левее:
Zn + CuSO4 = ZnSO4 + Cu
На металлы IА и IIА группы это правило не распространяется, так как они реагируют с водой.
Реакция между металлом и солью менее активного металла возможна в том случае, если соли — как вступающие в реакцию, так и образующиеся в результате — растворимы в воде.
Взаимодействие с аммиаком
Щелочные металлы реагируют с аммиаком с образованием амида натрия:
Взаимодействие с органическими веществами
Металлы IА группы реагируют со спиртами и фенолами, которые проявляют в данном случае кислотные свойства:
Также они могут вступать в реакции с галогеналканами, галогенпроизводными аренов и другими органическими веществами.
Взаимодействие металлов с оксидами
Для металлов при высокой температуре характерно восстановление неметаллов или менее активных металлов из их оксидов.
3Са + Cr2O3 = 3СаО + 2Cr (кальциетермия)
Вопросы для самоконтроля
С чем реагируют неактивные металлы?
С чем связаны восстановительные свойства металлов?
Верно ли утверждение, что щелочные и щелочноземельные металлы легко реагируют с водой, образуя щелочи?
Методом электронного баланса расставьте коэффициенты в уравнении реакции по схеме:
Mg + HNO3 → Mg(NO3)2 + NH4NO3 + Н2O
Как металлы реагируют с кислотами?
Подведем итоги
От активности металлов зависит их химические свойства. Простые вещества — металлы в окислительно-восстановительных реакциях являются восстановителями. По положению металла в электрохимическом ряду можно судить о том, насколько активно он способен вступать в химические реакции (т. е. насколько сильно у металла проявляются восстановительные свойства).
Напоследок поделимся таблицей, которая поможет запомнить, с чем реагируют металлы, и подготовиться к контрольной работе по химии.
Таблица «Химические свойства металлов»
Mg, Al, Mn, Zn, Cr, Fe, Ni, Sn, Pb
Cu, Hg, Ag, Pt, Au
Восстановительная способность металлов в свободном состоянии
Возрастает справа налево
Взаимодействие металлов с кислородом
Быстро окисляются при обычной температуре
Медленно окисляются при обычной температуре или при нагревании
Взаимодействие с водой
Выделяется водород и образуется гидроксид
При нагревании выделяется водород и образуются оксиды
Водород из воды не вытесняют
Взаимодействие с кислотами
Вытесняют водород из разбавленных кислот (кроме HNO3)
Не вытесняют водород из разбавленных кислот
Реагируют с концентрированными азотной и серной кислотами
С кислотами не реагируют, растворяются в царской водке
Взаимодействие с солями
Не могут вытеснять металлы из солей
Более активные металлы (кроме щелочных и щелочноземельных) вытесняют менее активные из их солей
Взаимодействие с оксидами
Для металлов (при высокой температуре) характерно восстановление неметаллов или менее активных металлов из их оксидов
Химические свойства солей

Впервые школьники знакомятся с химическими свойствами солей в 8 классе, и для понимания дальнейшего материала без этой темы никуда. Наша статья поможет освежить знания перед контрольной или экзаменом: вспомним, какие бывают соли и как они образуются, рассмотрим типичные реакции с ними.
Соли — это сложные вещества, в состав которых входят катионы металла и анионы кислотного остатка. Иногда в состав солей входят водород или гидроксид-ион.
Классификация и номенклатура солей
Так как соли — это продукт полного или частичного замещения металлом атома водорода в кислоте, по составу их можно классифицировать следующим образом.
Кислые соли
Образованы неполным замещением атомов водорода на металл в кислоте.
В наименованиях кислых солей указывают количество водорода приставками «гидро-» или «дигидро-», название кислотного остатка и название металла. Если металл имеет переменную валентность, то в скобках указывают валентность.
Примеры кислых солей и их наименования:
LiHCO3 — гидрокарбонат лития,
NaHSO4 — гидросульфат натрия,
NaH2PO4 — дигидрофосфат натрия.
Средние соли
Образованы полным замещением атомов водорода в кислоте на металл.
Наименования средних солей складываются из названий кислотного остатка и металла. При необходимости указывают валентность.
Примеры средних солей с названиями:
CuSO4 — сульфат меди (II),
CaCl2 — хлорид кальция.
Основные соли
Продукт неполного замещения гидроксогрупп на кислотный остаток.
В наименованиях основных солей указывают количество гидроксид-ионов приставкой «гидроксо-» или «дигидроксо-», название кислотного остатка и название металла с указанием валентности.
Пример: Mg(OH)Cl — гидроксохлорид магния.
Двойные соли
В состав входят два разных металла и один кислотный остаток.
Наименование складывается из названия аниона кислотного остатка и названий металлов с указанием валентности (если металл имеет переменную валентность).
Примеры двойных солей и их наименования:
KNaSO4 — сульфат калия-натрия,
Смешанные соли
Содержат один металл и два разных кислотных остатка.
Наименования смешанных солей складываются из названия кислотных остатков (по усложнению) и названия металла с указанием валентности (при необходимости).
Примеры смешанных солей с наименованиями:
CaClOCl — хлорид-гиполхорит кальция,
PbFCl — фторид-хлорид свинца (II).
Комплексные соли
Образованы комплексным катионом или анионом, связанным с несколькими лигандами.
Называют комплексные соли по схеме: координационное число + лиганд с окончанием «-о» + комплексообразователь с окончанием «-ат» и указанием валентности + внешняя сфера, простой ион в родительном падеже.
Пример: K[Al(OH)4] — тетрагидроксоалюминат калия.
Гидратные соли
В состав входит молекула кристаллизационной воды.
Число молекул воды указывают численной приставкой к слову «гидрат» и добавляют название соли.
Пример: СuSO4∙5H2O — пентагидрат сульфата меди (II).
Получение солей
Получение средних солей
Средние соли можно образовать в ходе следующих реакций:
Так получают только соли бескислородных кислот.
Металл, стоящий левее H2 в ряду активности, с раствором кислоты:
Mg + 2HCl = MgCl2 + H2
Металл с раствором соли менее активного металла:
Основный оксид + кислотный оксид:
Основный оксид и кислота:
Основание с кислотным оксидом:
Основание с кислотой (реакция нейтрализации):
Взаимодействие соли с кислотой:
Взаимодействие возможно, если одним из продуктов реакции будет нерастворимая соль, вода или газ.
Реакция раствора основания с раствором соли:
Взаимодействие растворов двух солей с образованием новых солей:
Получение кислых солей
Кислые соли образуются при взаимодействии:
Кислот с металлами:
Кислот с оксидами металлов:
Гидроксидов металлов с кислотами:
Кислот с солями:
Аммиака с кислотами:
Получение кислых солей возможно, если кислота в избытке.
Также кислые соли образуются в ходе реакции основания с избытком кислотного оксида:
Получение основных солей
Взаимодействие кислоты с избытком основания:
Добавление (по каплям) небольших количеств щелочей к растворам средних солей металлов:
Взаимодействие солей слабых кислот со средними солями:
Получение комплексных солей
Реакции солей с лигандами:
Получение двойных солей
Двойные соли получают совместной кристаллизацией двух солей:
Химические свойства средних солей
Растворимые соли являются электролитами, следовательно, могут распадаться на ионы. Средние соли диссоциируют сразу:
Нитраты разлагаются в зависимости от активности металла соли:
| Металл | Левее Mg, кроме Li | От Mg до Cu | Правее Cu |
| Продукты | MeNO3 + O2 | MexOy + NO2 + O2 | Me + NO2 + O2 |
| Пример | 2NaNO3 = 2NaNO2 + O2 | 2Cu(NO3)2 = 2CuO + 4NO2 + O2 | 2AgNO3= 2Ag + 2NO2 + O2 |
Соли аммония разлагаются с выделением азота или оксида азота (I), если в составе анион, проявляет окислительные свойства. В остальных случаях разложение солей аммония сопровождается выделением аммиака:
Взаимодействие солей с металлами:
Более активные металлы вытесняют менее активные металлы из растворов солей.
Некоторые соли подвержены гидролизу:
Обменные реакции соли и кислоты, соли с основаниями и взаимодействие солей с солями:
Окислительно-восстановительные реакции, обусловленные свойствами катиона или аниона:
Химические свойства кислых солей
Диссоциация. Кислые соли диссоциируют ступенчато:
Термическое разложение с образованием средней соли:
Взаимодействие солей со щелочью. В результате образуется средняя соль:
Химические свойства основных солей
Реакции солей с кислотами — образование средней соли:
Диссоциация — так же как и кислые соли, основные соли диссоциируют ступенчато.
Химические свойства комплексных солей
Избыток сильной кислоты приводит к разрушению комплекса и образованию двух средних солей и воды:
Недостаток сильной кислоты приводит к образованию средней соли активного металла, амфотерного гидроксида и воды:
Взаимодействие слабой кислоты с солью образует кислую соль активного металла, амфотерный гидроксид и воду:
При действии углекислого или сернистого газа получаются кислая соль активного металла и амфотерный гидроксид:
Реакция солей, образованных сильными кислотами с катионами Fe3+, Al3+ и Cr3+, приводит к взаимному усилению гидролиза. Продукты реакции — два амфотерных гидроксида и соль активного металла:
Разлагаются при нагревании:
Вопросы для самопроверки
С чем взаимодействуют средние соли?
Назовите типичные реакции солей.
Из предложенного списка солей выберите те, которые не реагируют с цинком: нитрит калия, бромид железа, карбонат цезия, сульфат меди.
Читайте также:
