Взаимодействие металлов с оксидами металлов
Обновлено: 06.05.2024
Атомы металлов легко отдают электроны внешнего (а некоторые – и предвнешнего) электронного слоя, превращаясь в положительные ионы.
Возможные степени окисления Ме
5. ВЗАИМОДЕЙСТВИЕ С ФОСФОРОМ И АЗОТОМ протекает при нагревании (исключение: литий с азотом при нормальных условиях) :
с фосфором – фосфиды: 3Ca + 2P =Са3P2,
С азотом – нитриды 6Li + N2 = 3Li2N (нитрид лития) (н.у.)
3Mg + N2 = Mg3N2 (нитрид магния)
6. ВЗАИМОДЕЙСТВИЕ С УГЛЕРОДОМ И КРЕМНИЕМ протекает при нагревании:
С углеродом образуются карбиды
С углеродом реагируют только наиболее активные металлы.
Из щелочных металлов карбиды образуют литий и натрий, калий, рубидий, цезий не взаимодействуют с углеродом :
Металлы – d-элементы образуют с углеродом соединения нестехиометрического состава типа твердых растворов: WC, ZnC, TiC – используются для получения сверхтвёрдых сталей.
с кремнием – силициды: 4Cs + Si = Cs4Si,
2. ВЗАИМОДЕЙСТВИЕ МЕТАЛЛОВ С ВОДОЙ:
С водой реагируют металлы, стоящие до водорода в электрохимическом ряду напряжений
Щелочные и щелочноземельные металлы реагируют с водой без нагревания , образуя растворимые гидроксиды( щелочи ) и водород, алюминий (после разрушения оксидной пленки - амальгирование),
магний при нагревании, образуют нерастворимые основания и водород.
2Na + 2HOH = 2NaOH + H2↑
Сa + 2HOH = Ca(OH)2 + H2↑
2Аl + 6Н2O = 2Аl(ОН)3 + ЗН2↑
Остальные металлы реагируют с водой только в раскаленном состоянии , образуя оксиды (железо – железную окалину)
Zn + Н2O = ZnO + H2 ↑ 3Fe + 4HOH = Fe3O4 + 4H2↑
2Cr + 3H₂O = Cr₂O₃ + 3H₂↑

ВЗАИМОДЕЙСТВИЕ МЕТАЛЛОВ С КИСЛОРОДОМ И ВОДОЙ
На воздухе железо и хром легко окисляется в присутствии влаги (ржавление):
4Fe + 3O2 + 6H2O = 4Fe(OH)3
4Cr + 3O2 + 6H2O = 4Cr(OH)3
ВЗАИМОДЕЙСТВИЕ МЕТАЛЛОВ С ОКСИДАМИ
(оксидами неметаллов и менее активных металлов)
Металлы (Al, Mg,Са ), восстанавливают при высокой температуре неметаллы или менее активные металлы из их оксидов → неметалл или малоактивный металл и оксид (кальцийтермия, магнийтермия, алюминотермия)
2Al + Cr2O3 = 2Cr + Al2O3
ЗСа + Cr₂O₃ = ЗСаО + 2Cr (800 °C)
8Al+3Fe3O4 = 4Al2O3+9Fe (термит)
2Mg + CО2 = 2MgO + С Mg + N2O = MgO + N2↑
Zn + CО2 = ZnO+ CO 2Cu + 2NO = 2CuO + N2
3Zn + SО2 = ZnS + 2ZnO
Металлы железо и хром реагируют со оксидами, уменьшая степень окисления
Cr + Cr2⁺³O3 = 3Cr⁺²O
5. ВЗАИМОДЕЙСТВИЕ С КИСЛОТАМИ (КРОМЕ HNO3 и Н2SО4 (конц.)
Металлы, стоящие в электрохимическом ряду напряжений металлов левее водорода, вытесняют его из разбавленных кислот → соль и водород.
Мg + 2НС1 = МgСl2 + Н2↑
Al + 2НС1 = Al⁺³Сl₃ + Н2↑
С концентрированной серной и азотной любой концентрации реакции идет по другому механизму
Металл + HNO₃ → соль + H₂O + …
Запомни! Азотная кислота никогда не выделяет водород при взаимодействии с металлами.
В качестве продуктов могут образовываться оксиды азота в разных степенях окисления, молекулярный азот, аммиак и соли аммония.
Металлы платиновой группы - золото, платина и тантал инертны к азотной кислоте во всём диапазоне концентраций, остальные металлы реагируют с ней, ход реакции при этом определяется концентрацией кислоты.
Общая закономерность при взаимодействии азотной кислоты с металлами: чем более разбавленная кислота и чем активнее металл, тем глубже восстанавливается азот:
←увеличение концентрации кислоты
→ увеличение активности металла
Пассивация: с холодной конц. серной кислотой не реагируют: Al, Cr, Fe, Be, Co
При нагревании пассивирующие пленки растворяются, и взаимодействие с кислотой протекает интенсивно.
Взаимодействие металлов с кислотами
Целью данной работы является рассмотрение связи физико-химических свойств металлов с ЭЛЕКТРОННЫМ строением атомов, строением кристаллической структуры, изучение химических свойств металлов (взаимодействие с простыми и сложными окислителями; водой, кислотами, щелочами, их смесями) для понимания физико-химических процессов при химических методах обработки металлов и сплавов.
Основные понятия темы
Металлы - простые вещества, обладающие характерными свойствами; высокой электропроводностью и теплопроводностью, отрицательным температурным коэффициентом электропроводности, способностью хорошо отражать электромагнитные волны (блеск и непрозрачность), пластичностью.
По химическим свойствам металлы - восстановители, так как легко отдаю: свои валентные электроны:
Металлы - это элементы, атомы которых имеют минимальное количество электронов на внешнем энергетическом уровне. Степень окисления определяется числом неспаренных электронов в нормальном и возбужденном состояниях.
Восстановительную активность атома элемента определяют потенциалом ионизации валентных электронов. Химическая активность металла как простого вещества, имеющего кристаллическое строение, характеризуется термодинамическими величинами (знтальпией ΔН и энергией Гиббса ΔG). Для суждения о возможности реакции металла с водой, кислотами, щелочами необходимо также определение величины ΔG химической реакции, Так как эти реакции являются окислительно-восстановительными, где металл выступает в качестве восстановителя, а ион водорода H + (гидроксоний H2O) либо анион кислоты в виде окислителя.
При условии, что φокисл > φвост, реакция между металлом и водой, кислотой, щелочью, растворами солей возможна
Взаимодействие металлов с простыми окислителями
Простые окислители - это кислород О:, галогены. Наиболее часто встречается реакция окисления металлов кислородом воздуха:
Возможность данной реакции при нормальных условиях определяется
величиной ΔG 0 298 реакции.
При окисления металлов кислородом образуются оксиды. Для металлов, имеющих большое число степеней окисления, низшие оксиды металлов обладают основными свойствами (если степень окисления от 1 до 2), высшие оксиды (оксиды с максимальными степенями окисления) -кислотными (степень окисления > 4), Оксиды, где степень окисления +3, +4 - амфотерны.
7.1.2. Взаимодействие металлов с водой
Металлы взаимодействуют с водой по реакции
Так как эта реакция является окислительно-восстановительной, то возможность данной реакции определяется по величине энергии Гиббса.
Наряду с термодинамическим расчетом необходимо учитывать, что многие металлы покрыты оксидными пленками.
Взаимодействие металлов с кислотами
Для очистки металлов от поверхностных слоев перед нанесением покрытий всегда, когда нужно иметь дело с чистой поверхностью металла, используют кислотное травление. Травление бывает технологическое и структурное
Технологическое травление используют для обработки и изменения формы поверхности металла, структурное травление - для выявления структуры поверхности кристаллических материалов,
Химическое фрезерование проводится для получения нужного рисунка - придания профиля поверхности детали, Согласно чертежу, на отдельные участки поверхности заносится химически стойкий слой, а свободные участка травятся при воздействии смесей кислот.
Химическое травление используется для выявления дефектов в кристаллах: малоугловых и двойниковых границ, дислокаций и дефектов упаковки
Для металлов, химическое травление которых затруднено (Ti, Mo, W, жаропрочные сплавы), используется электрохимическое травление.
Кислоты - вещества, содержащие водород и диссоциирующие с образованием Н + .
Различают бескислородные и кислородсодержащие кислоты.
Бескислородные кислоты - растворы галогеноводородов в воде: соляная (НС1), плавиковая (HF), бромоводородная (НВг), йодоводородная (HI), сероводородная (H-S),
Кислородсодержащие кислоты: азотная, серная, фосфорная, хлорная и другие.
План выполнения эксперимента
Запишите предполагаемое уравнение реакции взаимодействия исследуемого металла с раствором электролита. По уравнениям (7.6-7.9; 7.22-7.24), значениям электродных потенциалов и перенапряжений определите термодинамическую вероятность протекания этих реакций. Для взаимодействия типа Me +
Опустите в пробирки стружки металла и прилейте 1 -2 мл электролита С концентрированными растворами работайте в вытяжном шкафу. Опишите характер протекания реакции, окраску, запах выделяющихся продуктов. Если реакция не идет при комнатной температуре, нагревайте раствор на спиртовке
В отчете приведите уравнения химических реакций, расчет термодинамической вероятности протекания реакции, экспериментальные наблюдения и сопоставьте данные расчета и эксперимента.
Реакция взаимодействия с водой
Положили в пробирку кусочек цинка, налили воды и подогрели на спиртовке. Довели воду до кипения. Наглядных проявлений хода реакции не наблюдалось.
Zn 0 – 2e → Zn 2+ φвост(Zn 2+ /Zn) = -0.763 В φокисл (2H2O/2OH 2- H2) = -0.414 В
E = φокисл – φвост = -0,414 + 0,763 = 0,349 В
ΔG = -zFE = -2*26.8*0.349 = -18.706
Реакция взаимодействия с азотной кислотой.
Положили в пробирку кусочек цинка, налили азотной кислоты. Наблюдалось повышение температуры, появление оранжевой окраски, выделение газа. Реакция прошла.
Zn 0 - 2e → Zn 2+ (восстановитель)
NO3 - + H + + 3e → NO + H2O (окислитель)
уравняем левую и правую части
3 Zn 0 - 2e → Zn 2+ (восстановитель)
2 NO3 - + 4H + + 3e → NO + 2H2O (окислитель)
3Zn 0 + 8H + → 3Zn 2+ + 2NO +4H2O
φвост(Zn 2+ /Zn) = -0.763 В φокисл (NO3 - /NO) = 0.96 В
E = φокисл – φвост = 0,96 + 0,763 = 1,723 В
ΔG = -zFE = -2*26,8*1,723 = -92,35 , т. к. ΔG
Реакция взаимодействия с серной кислотой.
Положили в пробирку кусочек цинка, налили серной кислоты и подогрели на спиртовке. Довели серную кислоту до кипения. Наблюдается появление белого осадка. Реакция прошла.
φвост(Zn 2+ /Zn) = -0.763 В φокисл = +0.351 В
E = φокисл – φвост = 0.351 +0.763 = 1.114 В
Реакция взаимодействия с соляной кислотой.
Положили в пробирку кусочек цинка, налили соляной кислоты. Наблюдается повышение температуры, выделение газа. Реакция прошла.
2H + + 2e → H2 (окислитель)
φвост(Zn 2+ /Zn) = -0.763 В φокисл = 0, т. к. Ph соляной кислоты = 0
E = φокисл – φвост = 0 + 0,763 = 0,763 В
Реакция взаимодействия со щёлочью.
Положили в пробирку кусочек цинка, налили гидроксида натрия. Наблюдается выделение газа. Реакция прошла.
2H2O + 2e → 2OH - + H2 (окислитель)
φвост(Zn 2+ /Zn) = -0.763 В φокисл = -0.82 В
E = φокисл – φвост = -0,82 + 0,763 = -0,057 В
ΔG = zFE = -2*26,8*0,057 = -3,05 , т. к. ΔG
Вывод: Мы рассмотрели связи физико-химических свойств металлов с ЭЛЕКТРОННЫМ строением атомов, строением кристаллической структуры, изучили химические свойства металлов (взаимодействие с простыми и сложными окислителями; водой, кислотами, щелочами, их смесями) для понимания физико-химических процессов при химических методах обработки металлов и сплавов.
Как оформить тьютора для ребенка законодательно: Условием успешного процесса адаптации ребенка может стать.
История государства Древнего Египта: Одним из основных аспектов изучения истории государств и права этих стран является.
Образцы сочинений-рассуждений по русскому языку: Я думаю, что счастье – это чувство и состояние полного.
Поиск по сайту
Взаимодействие оксидов с солями
С кислотами реагируют основные и амфотерные оксиды. При этом образуются соли и вода:
Несолеобразующие оксиды не реагируют с кислотами вообще, а кислотные оксиды не реагируют с кислотами в большинстве случаев.
Когда все-таки кислотный оксид реагирует с кислотой?
Решая часть ЕГЭ с вариантами ответа, вы должны условно считать, что кислотные оксиды не реагируют ни с кислотными оксидами, ни с кислотами, за исключением следующих случаев:
1) диоксид кремния, будучи кислотным оксидом, реагирует с плавиковой кислотой, растворяясь в ней. В частности, благодаря этой реакции в плавиковой кислоте можно растворить стекло. В случае избытка HF уравнение реакции имеет вид:
а в случае недостатка HF:
2) SO2, будучи кислотным оксидом, легко реагирует с сероводородной кислотой H2S по типу сопропорционирования:
S +4 O2+ 2H2S -2 = 3S 0 + 2H2O
3) Оксид фосфора (III) P2O3 может реагировать с кислотами-окислителями, к которым относятся концентрированная серная кислота и азотная кислота любой концентрации. При этом степень окисления фосфора повышается от значения +3 до +5:
| P2O3 | + | 2H2SO4 | + | H2O | =t o => | 2SO2 | + | 2H3PO4 |
| (конц.) | ||||||||
| 3P2O3 | + | 4HNO3 | + | 7H2O | =t o => | 4NO↑ | + | 6H3PO4 |
| (разб.) |
| P2O3 | + | 4HNO3 | + | H2O | =t o => | 2H3PO4 | + | 4NO2↑ |
| (конц.) |
4) Оксид серы (IV) SO2 может быть окислен азотной кислотой, взятой в любой концентрации. При этом степень окисления серы повышается с +4 до +6.
| 2HNO3 | + | SO2 | =t o => | H2SO4 | + | 2NO2↑ | ||
| (конц.) | ||||||||
| 2HNO3 | + | 3SO2 | + | 2H2O | =t o => | 3H2SO4 | + | 2NO↑ |
| (разб.) |
Взаимодействие оксидов с гидроксидами металлов
С гидроксидами металлов как основными, так и амфотерными реагируют кислотные оксиды. При этом образуется соль, состоящая из катиона металла (из исходного гидроксида металла) и кислотного остатка кислоты, соответствующей кислотному оксиду.
Кислотные оксиды, которым соответствуют слабые кислоты или кислоты средней силы, с щелочами могут образовывать как нормальные, так и кислые соли:
«Привередливые» оксиды CO2 и SO2, активности которых, как уже было сказано, не хватает для протекания их реакции с малоактивными основными и амфотерными оксидами, тем не менее, реагируют с большей частью соответствующих им гидроксидов металлов. Точнее, углекислый и сернистый газы взаимодействуют с нерастворимыми гидроксидами в виде их суспензии в воде. При этом образуются только основные соли, называемые гидроксокарбонатами и гидроксосульфитами, а образование средних (нормальных) солей невозможно:
Однако с гидроксидами металлов в степени окисления +3, например, такими, как Al(OH)3, Cr(OH)3, Fe(OH)3 и т.д., углекислый и сернистый газ не реагируют вовсе.
Следует отметить также особую инертность диоксида кремния (SiO2), в природе наиболее часто встречаемого в виде обычного песка. Данный оксид является кислотным, однако из гидроксидов металлов способен реагировать только с концентрированными (50-60%) растворами щелочей, а также с чистыми (твердыми) щелочами при сплавлении. При этом образуются силикаты:
2NaOH + SiO2=t o => Na2SiO3+ H2O
Амфотерные оксиды из гидроксидов металлов реагируют только со щелочами (гидроксидами щелочных и щелочноземельных металлов). При этом при проведении реакции в водных растворах образуются растворимые комплексные соли:
ZnO + 2NaOH + H2O = Na2[Zn(OH)4] — тетрагидроксоцинкат натрия
BeO + 2NaOH + H2O = Na2[Be(OH)4] — тетрагидроксобериллат натрия
Al2O3 + 2NaOH + 3H2O = 2Na[Al(OH)4] — тетрагидроксоалюминат натрия
Cr2O3 + 6NaOH + 3H2O = 2Na3[Cr(OH)6] — гексагидроксохромат (III) натрия
А при сплавлении этих же амфотерных оксидов со щелочами получаются соли, состоящие из катиона щелочного или щелочноземельного металла и аниона вида MeO2 x— , где x = 2 в случае амфотерного оксида типа Me +2 O и x = 1 для амфотерного оксида вида Me2 +2 O3:
ZnO + 2NaOH =t o => Na2ZnO2+ H2O
BeO + 2NaOH =t o => Na2BeO2+ H2O
Al2O3 + 2NaOH =t o => 2NaAlO2 + H2O
Cr2O3 + 2NaOH =t o => 2NaCrO2 + H2O
Fe2O3 + 2NaOH =t o => 2NaFeO2 + H2O
Следует отметить, что соли, получаемые сплавлением амфотерных оксидов с твердыми щелочами, могут быть легко получены из растворов соответствующих комплексных солей их упариванием и последующим прокаливанием:
Na[Al(OH)4] =t o => NaAlO2+ 2H2O
Взаимодействие оксидов с солями
Чаще всего соли с оксидами не реагируют.
Однако следует выучить следующие исключения из данного правила, часто встречающиеся на экзамене.
Одним из таких исключений является то, что амфотерные оксиды, а также диоксид кремния (SiO2) при их сплавлении с сульфитами и карбонатами вытесняют из последних сернистый (SO2) и углекислый (CO2) газы соответственно. Например:
Также к реакциям оксидов с солями можно условно отнести взаимодействие сернистого и углекислого газов с водными растворами или взвесями соответствующих солей — сульфитов и карбонатов, приводящее к образованию кислых солей:
Также сернистый газ при пропускании его через водные растворы или взвеси карбонатов вытесняет из них углекислый газ благодаря тому, что сернистая кислота является более сильной и устойчивой кислотой, чем угольная:
ОВР с участием оксидов
Обряды и обрядовый фольклор: составляли словесно-музыкальные, драматические, игровые, хореографические жанры, которые.
Химические свойства металлов

Свойства металлов начинают изучать на уроках химии в 8–9 классе. В этом материале мы подробно разберем химические свойства этой группы элементов, а в конце статьи вы найдете удобную таблицу-шпаргалку для запоминания.
О чем эта статья:
8 класс, 9 класс, ЕГЭ/ОГЭ
Металлы — это химические элементы, атомы которых способны отдавать электроны с внешнего энергетического уровня, превращаясь в положительные ионы (катионы) и проявляя восстановительные свойства.
В окислительно-восстановительных реакциях металлы способны только отдавать электроны, являясь сильными восстановителями. В роли окислителей выступают простые вещества — неметаллы (кислород, фосфор) и сложные вещества (кислоты, соли и т. д.).
Металлы в природе встречаются в виде простых веществ и соединений. Активность металла в химических реакциях определяют, используя электрохимический ряд, который предложил русский ученый Н. Н. Бекетов. По химической активности выделяют три группы металлов.
Ряд активности металлов
Металлы средней активности
Общие химические свойства металлов
Взаимодействие с неметаллами
Щелочные металлы сравнительно легко реагируют с кислородом, но каждый металл проявляет свою индивидуальность:
оксид образует только литий
натрий образует пероксид
калий, рубидий и цезий — надпероксид
Остальные металлы с кислородом образуют оксиды:
2Zn + O2 = 2ZnO (при нагревании)
Металлы, которые в ряду активности расположены левее водорода, при контакте с кислородом воздуха образуют ржавчину. Например, так делает железо:
С галогенами металлы образуют галогениды:
Медный порошок реагирует с хлором и бромом (в эфире):
При взаимодействии с водородом образуются гидриды:
Взаимодействие с серой приводит к образованию сульфидов (реакции протекают при нагревании):
Реакции с фосфором протекают до образования фосфидов (при нагревании):
Основной продукт взаимодействия металла с углеродом — карбид (реакции протекают при нагревании).
Из щелочноземельных металлов с углеродом карбиды образуют литий и натрий:
Калий, рубидий и цезий карбиды не образуют, могут образовывать соединения включения с графитом:
С азотом из металлов IA группы легко реагирует только литий. Реакция протекает при комнатной температуре с образованием нитрида лития:
Взаимодействие с водой
Все металлы I A и IIA группы реагируют с водой, в результате образуются растворимые основания и выделяется H2. Литий реагирует спокойно, держась на поверхности воды, натрий часто воспламеняется, а калий, рубидий и цезий реагируют со взрывом:
Металлы средней активности реагируют с водой только при условии, что металл нагрет до высоких температур. Результат данной реакции — образование оксида.
Неактивные металлы с водой не взаимодействуют.
Взаимодействие с кислотами
Если металл расположен в ряду активности левее водорода, то происходит вытеснение водорода из разбавленных кислот. Данное правило работает в том случае, если в реакции с кислотой образуется растворимая соль.
2Na + 2HCl = 2NaCl + H2
При взаимодействии с кислотами-окислителями, например, азотной, образуется продукт восстановления кислоты, хотя протекание реакции также неоднозначно.
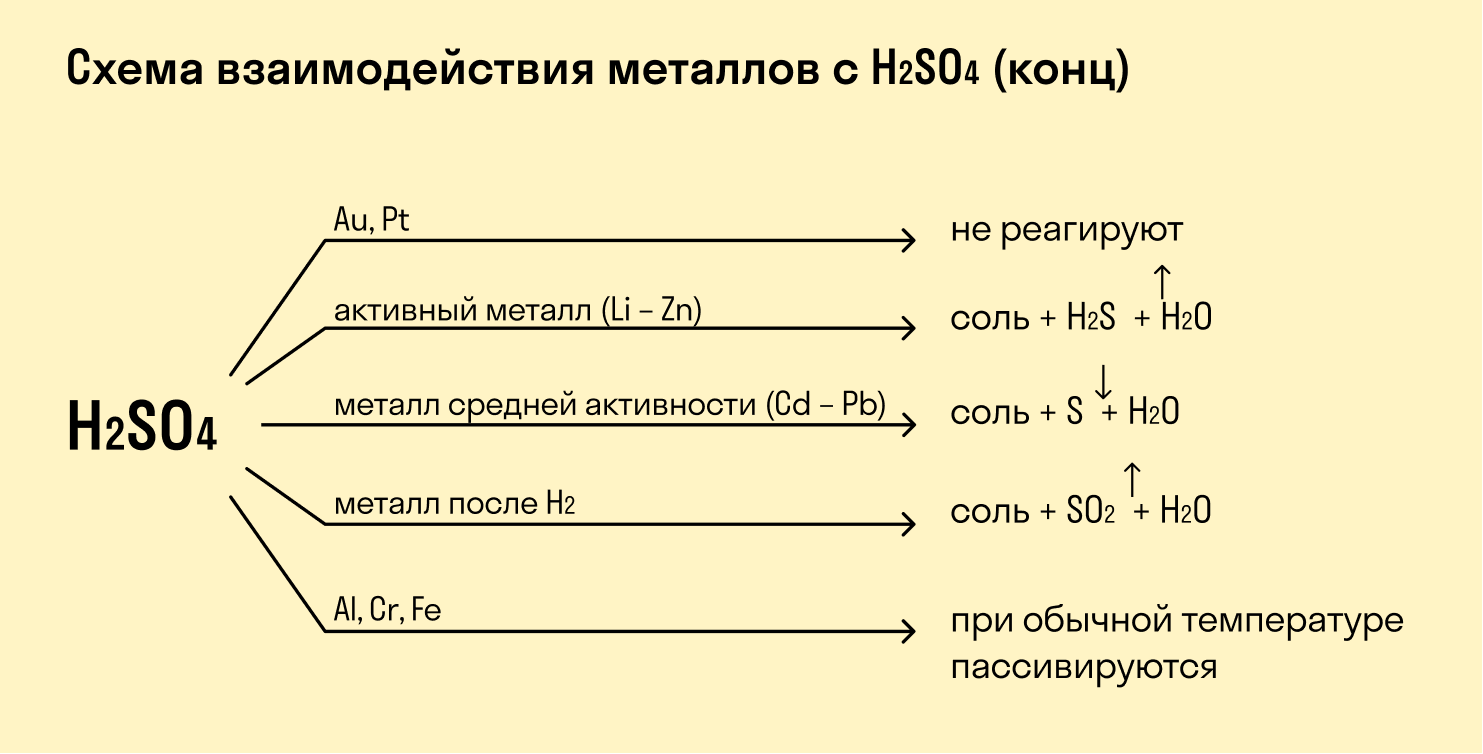
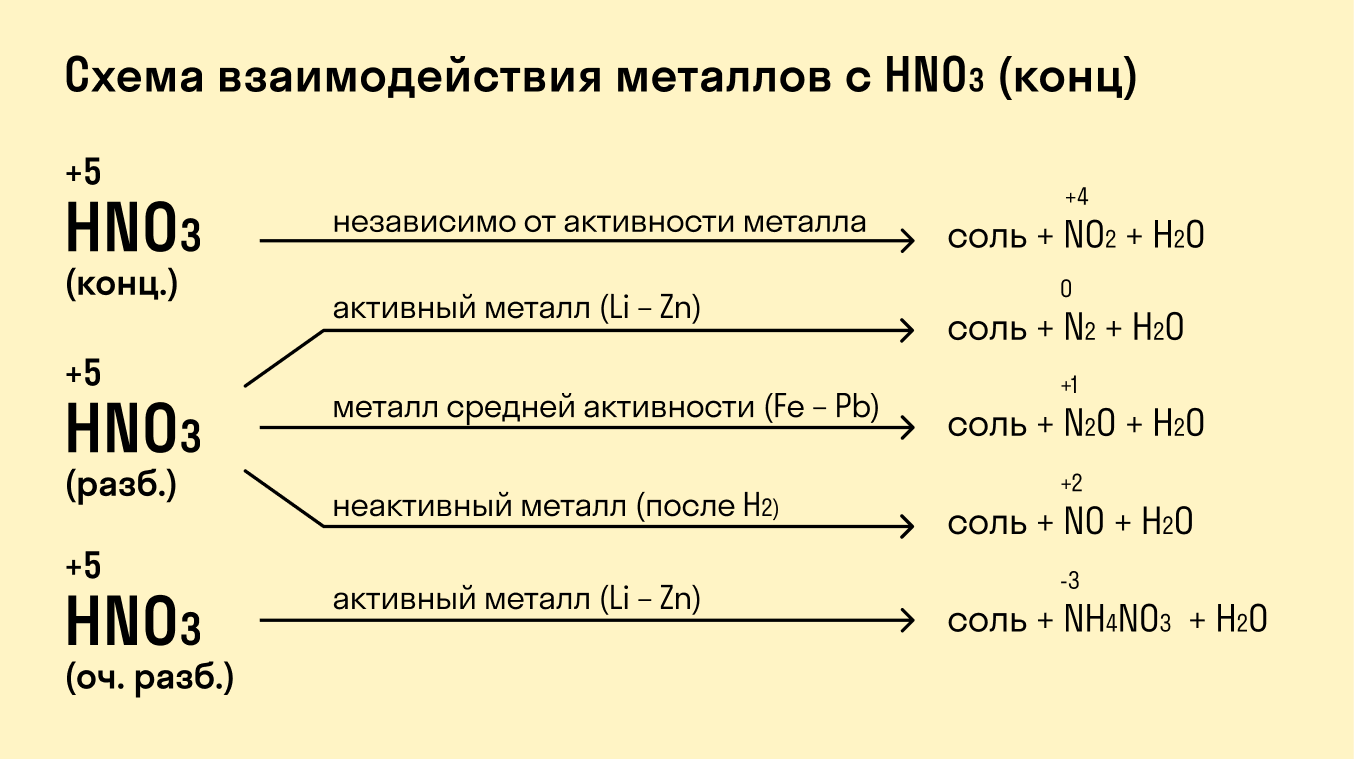
Металлы IА группы:
Металлы IIА группы
Такие металлы, как железо, хром, никель, кобальт на холоде не взаимодействуют с серной кислотой, но при нагревании реакция возможна.
Взаимодействие с солями
Металлы способны вытеснять из растворов солей другие металлы, стоящие в ряду напряжений правее, и могут быть вытеснены металлами, расположенными левее:
Zn + CuSO4 = ZnSO4 + Cu
На металлы IА и IIА группы это правило не распространяется, так как они реагируют с водой.
Реакция между металлом и солью менее активного металла возможна в том случае, если соли — как вступающие в реакцию, так и образующиеся в результате — растворимы в воде.
Взаимодействие с аммиаком
Щелочные металлы реагируют с аммиаком с образованием амида натрия:
Взаимодействие с органическими веществами
Металлы IА группы реагируют со спиртами и фенолами, которые проявляют в данном случае кислотные свойства:
Также они могут вступать в реакции с галогеналканами, галогенпроизводными аренов и другими органическими веществами.
Взаимодействие металлов с оксидами
Для металлов при высокой температуре характерно восстановление неметаллов или менее активных металлов из их оксидов.
3Са + Cr2O3 = 3СаО + 2Cr (кальциетермия)
Вопросы для самоконтроля
С чем реагируют неактивные металлы?
С чем связаны восстановительные свойства металлов?
Верно ли утверждение, что щелочные и щелочноземельные металлы легко реагируют с водой, образуя щелочи?
Методом электронного баланса расставьте коэффициенты в уравнении реакции по схеме:
Mg + HNO3 → Mg(NO3)2 + NH4NO3 + Н2O
Как металлы реагируют с кислотами?
Подведем итоги
От активности металлов зависит их химические свойства. Простые вещества — металлы в окислительно-восстановительных реакциях являются восстановителями. По положению металла в электрохимическом ряду можно судить о том, насколько активно он способен вступать в химические реакции (т. е. насколько сильно у металла проявляются восстановительные свойства).
Напоследок поделимся таблицей, которая поможет запомнить, с чем реагируют металлы, и подготовиться к контрольной работе по химии.
Таблица «Химические свойства металлов»
Mg, Al, Mn, Zn, Cr, Fe, Ni, Sn, Pb
Cu, Hg, Ag, Pt, Au
Восстановительная способность металлов в свободном состоянии
Возрастает справа налево
Взаимодействие металлов с кислородом
Быстро окисляются при обычной температуре
Медленно окисляются при обычной температуре или при нагревании
Взаимодействие с водой
Выделяется водород и образуется гидроксид
При нагревании выделяется водород и образуются оксиды
Водород из воды не вытесняют
Взаимодействие с кислотами
Вытесняют водород из разбавленных кислот (кроме HNO3)
Не вытесняют водород из разбавленных кислот
Реагируют с концентрированными азотной и серной кислотами
С кислотами не реагируют, растворяются в царской водке
Взаимодействие с солями
Не могут вытеснять металлы из солей
Более активные металлы (кроме щелочных и щелочноземельных) вытесняют менее активные из их солей
Взаимодействие с оксидами
Для металлов (при высокой температуре) характерно восстановление неметаллов или менее активных металлов из их оксидов
Оксиды

Знакомство с оксидами обычно начинается на уроках химии в 8 классе. Из этой статьи вы узнаете, что такое оксиды в химии, их классификацию и свойства, а также способы получения.
Определение оксидов
Оксиды — это сложные вещества, состоящие из двух химических элементов (т. е. бинарные соединения), один из которых — кислород в степени окисления −2.
Общая формула оксидов: ЭxOy, где Э – химический элемент, а x и y — индексы, определяемые степенью окисления химических элементов.
Виды оксидов
Все оксиды делятся на солеобразующие и несолеобразующие.
Несолеобразующие оксиды — это оксиды, которые не взаимодействуют с кислотами и щелочами, то есть не способны образовать соли.
К несолеобразующим оксидам относят: CO, SiO, N2O, NO.
Солеобразующие оксиды — это оксиды, которые взаимодействуют с кислотами и щелочами с образованием солей.
Солеобразующие оксиды делятся на три группы:
Основные оксиды — это оксиды, образованные металлами со степенью окисления +1 или +2.
Примеры основных оксидов: Na +1 2O, Ca +2 O, Ba +2 O.
Амфотерные оксиды — оксиды, образованные металлами со степенью окисления +3 или +4.
К амфотерным оксидам относят также: ZnO, BeO, PbO, SnO.
Несмотря на то, что эти металлы проявляют степень окисления +2 в данных соединениях, их оксиды проявляют амфотерные свойства.
Примеры амфотерных оксидов: Al +3 2O3, Fe2 +3 O3.
Кислотные оксиды — оксиды, образованные металлами с валентностью V и более или неметаллами с любой валентностью (за исключением несолеобразующих оксидов, то есть CO, SiO, N2O, NO).
Если один и тот же химический элемент образовывает несколько оксидов, то с увеличением степени окисления основные свойства оксидов ослабевают и усиливаются кислотные.
CrO (оксид хрома (II)) — проявляет основные свойства;
Cr2O3 (оксид хрома (III)) — проявляет амфотерные свойства;
CrO3 (оксид хрома (VI)) — проявляет кислотные свойства.
Закрепим знания о типах оксидов, изучив схему:
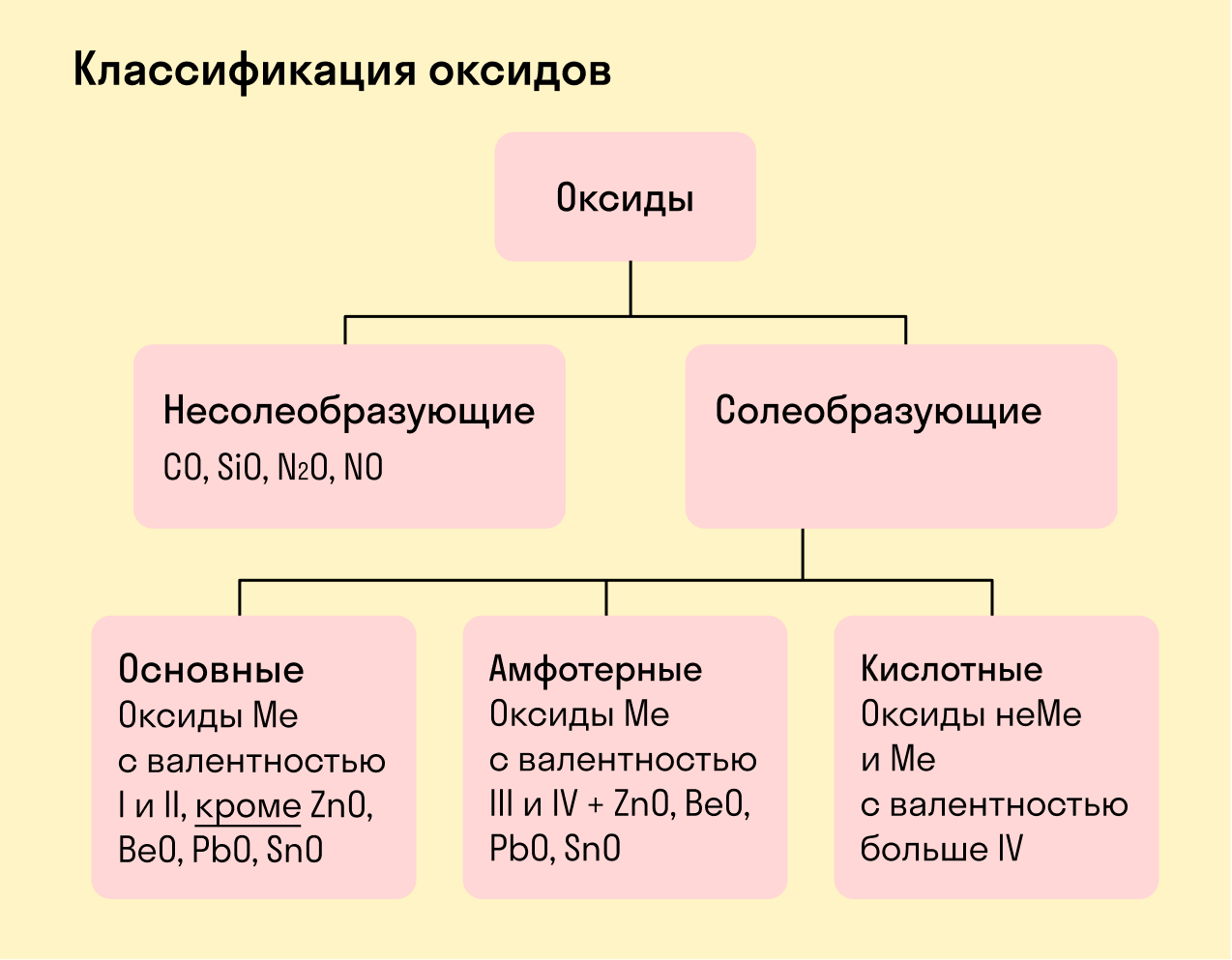
Номенклатура оксидов
Названия оксидов строятся по систематической номенклатуре следующим образом:
Пишем слово «оксид».
Указываем название второго химического элемента в родительном падеже.
Если этот элемент имеет переменную валентность, то указываем валентность элемента в этом соединении в скобках римской цифрой.
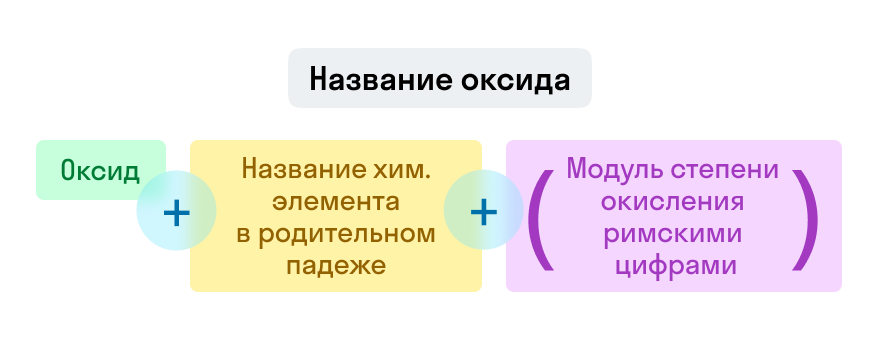
Примеры названий оксидов:
Fe2O3 — оксид железа (III). Читается: феррум два о три.
Na2O — оксид натрия. Читается: натрия два о.
SO3 — оксид серы (VI). Читается: эс о три.
До появления систематической номенклатуры вещества называли по присущим им специфическим свойства (цвету, запаху и т. д.). Такой способ названия веществ — тривиальная номенклатура. Некоторые названия используются и сейчас.
Названия некоторых оксидов: таблица
Химическая формула оксида
Бытовое (тривиальное название)
Возможное научное название
Химические свойства основных оксидов
1. Взаимодействие с водой
С водой способны реагировать оксиды тех металлов, которым соответствуют растворимые гидроксиды. То есть с водой реагируют только оксиды щелочных и щелочноземельных металлов.
Основный оксид + вода = основание
Оксид магния взаимодействует с водой только при нагревании.
2. Взаимодействие с кислотными оксидами и кислотами
Основные оксиды, соответствующие щелочам, взаимодействуют со всеми кислотными оксидами и кислотами. Оксиды неактивных металлов взаимодействуют только с кислотными оксидами, соответствующими сильным кислотам, или с сильными кислотами.
Основный оксид + кислотный оксид = соль
Основный оксид + кислота = соль + вода
3. Взаимодействие с амфотерными оксидами
В эту реакцию могут вступать только основные оксиды щелочных или щелочноземельных металлов. При сплавлении двух оксидов образуется соль.
Основный оксид + амфотерный оксид = соль
Как составлять такие соли: металл в этой соли берем из основного оксида, а кислотный остаток из амфотерного оксида (они проявляют более кислотные свойства).
Химические свойства кислотных оксидов
Кислотные оксиды взаимодействуют с водой с образованием соответствующих кислот. За исключением SiO2, которому соответствует нерастворимая кремниевая кислота.
Кислотный оксид + вода = кислота
2. Взаимодействие с основными оксидами и щелочами
Кислотные оксиды сильных кислот способны взаимодействовать с любыми основными оксидами или основаниями.
Кислотный оксид + основный оксид = соль
Кислотный оксид + основание = соль + вода
Кислотные оксиды, соответствующие слабым кислотам (такие как CO2, SO2), способны взаимодействовать с основными оксидами, соответствующим щелочам, а также с щелочами.
3. Взаимодействие с амфотерными оксидами и гидроксидами
С амфотерными оксидами в реакцию вступают кислотные оксиды — как правило, сильных кислот.
Кислотный оксид + амфотерный оксид = соль
Кислотный оксид + амфотерный оксид = соль + вода
Химические свойства амфотерных оксидов
Амфотерные оксиды не взаимодействуют с водой — даже при нагревании!
Амфотерный оксид + вода ≠
2. Взаимодействие с кислотными оксидами и кислотой
Амфотерные оксиды взаимодействуют только с сильными и средними кислотами и их оксидами.
Амфотерный оксид + кислотный оксид = соль
Амфотерный оксид + кислота = соль + вода
3. Взаимодействие с основными оксидами
Амфотерные оксиды взаимодействуют только с теми оксидами, которые соответствуют щелочам. Реакция протекает только в расплаве, так как в растворе такие оксиды взаимодействуют преимущественно с водой с образованием щелочей.
Амфотерный оксид + основный оксид (расплав) = соль
4. Взаимодействие со щелочами
Продукты взаимодействия амфотерных оксидов со щелочами зависят от условий проведения реакции. В растворе образуются комплексные соли, а при сплавлении – средние соли.
Амфотерный оксид + щелочь (раствор) + вода = комплексная соль
Амфотерный оксид + щелочь (расплав) = средняя соль + вода
Получение оксидов
1. Окисление металлов
Почти все металлы окисляются кислородом до устойчивых степеней окисления.
Металлы с переменной степенью окисления, как правило, образуют соединения в степени окисления +3:
При взаимодействии щелочных металлов (элемента IA группы) образуются пероксиды Me2O2 или надпероксиды MeO2, где Ме — щелочной металл.
2. Окисление простых веществ — неметаллов
При окислении неметаллов в избытке кислорода, как правило, образуются высшие оксиды (это оксиды, в которых неметалл проявляют высшую степень окисления):
При недостаточном количестве кислорода образуются оксиды неметаллов в промежуточной степени окисления:
Существуют и исключения. Например, сера окисляется лишь до оксида серы (IV) даже в избытке кислорода:
Или азот, который взаимодействует с кислородом только при температуре 2 000̊С или под действием электрического разряда с образованием оксида азота (II):
Галогены (элементы VIIA группы) вовсе не взаимодействуют с кислородом, так же как и инертные газы (элементы VIIIA группы).
3. Разложение гидроксидов
Некоторые кислоты и гидроксиды неустойчивы и самопроизвольно разлагаются по схеме:
Гидроксид (кислота) = оксид + вода
Оксиды тяжелых металлов (нерастворимые гидроксиды) и кремниевая кислота разлагаются при нагревании по той же самой схеме.
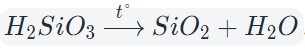
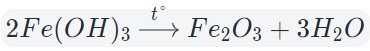
4. Окисление сложных веществ
Сложные бинарные (состоящие из двух химических элементов) соединения окисляются с образованием двух оксидов этих элементов в устойчивых степенях окисления.
Также оксиды получают разложением солей, например, карбонатов, нитратов сульфатов и т. д.
Мы узнали, какие вещества в химии называют оксидами, какие бывают оксиды, а также разобрали свойства каждого вида. Осталось подкрепить теорию практикой — а сделать это можно на курсах по химии в онлайн-школе Skysmart!
Читайте также:
