Вживление в тело металла
Обновлено: 06.07.2024
Выполнены 4 серии экспериментов на взрослых беспородных собаках. Изучена температурная реакция тканей в области имплантации разного типа титановых накостных пластин (без отверстий и с отверстиями) с гидроксиапатитным покрытием, изготовленных методом 3D печати. в зависимости от серии эксперимента, биоактивное покрытие было нанесено методом микродугового оксидирования (МДО) или высокочастотного магнетронного распыления (КФ ВЧМР). в течение первых двух недель после имплантации температура тканей повышалась, что не зависело от типа изделия и способа нанесения биоактивного покрытия. Через 3 недели эксперимента динамика температурной реакции зависела от типа имплантата, а способ нанесения покрытия не оказывал значимого влияния. Через 4 недели после имплантации значения изучаемого показателя во всех сериях нормализовались. Полученные данные будут использованы при оценке особенностей кровообращения в тканях области имплантации тестируемых изделий и учтены при анализе результатов гистологического исследования. Это позволит определить оптимальную пористость и топографию поверхности для накостных и внутрикостных имплантатов с биоактивным гидроксиапатитным покрытием, изготовленных из титановых сплавов с помощью аддитивных технологий.

1. Ахтямов И.Ф. Исследование взаимодействия биосовместимого покрытия из смеси нитридов металлов IV группы с тканями живого организма / И.Ф. Ахтямов, Э.Б. Гатина, Ф.Ф. Кадыров, М.Ф. Шаехов, Ф.В. Шакирова // Вестник Казанского технологического университета. – 2012. – Т.15(20). – С. 176–178.
2. Карлов А.В., Шахов В.П. Системы внешней фиксации и регуляторные механизмы оптимальной биомеханики. – Томск: СТТ, 2001. – C. 480.
3. Кобызев А.Е., Кононович Н.А., Краснов В.В. Температурная реакция тканей при сколиотической деформации поясничного отдела позвоночника и в условиях ее коррекции (экспериментальное исследование) // Успехи современного естествознания. – 2015. – № 9–3. – С. 429–433.
4. Некоторые аспекты применения термографии при реабилитации пациентов с нарушением функций опорно-двигательной и нервной систем / В.И. Виноградов, И.С. Веретенов, В.Н. Слезко, г. И. Пугач, В.А. Ланда, г. И. Большакова // Функциональная диагностика. – 2005. – № 3. – С. 72–78.
5. Попков А.В., Попков Д.А., Кононович Н.А., Горбач Е.Н., Твердохлебов С.И. Возможности остеогенной активности интрамедуллярных имплантатов в зависимости от технологии нанесения кальций-фосфатного покрытия (экспериментальное исследование) // Успехи современного естествознания. – 2015. – № 5. – С. 142–145.
6. Твердохлебов С.И., Игнатов В.П., Степанов И.Б., Сивин Д.О., Петлин Д.Г. Гибридный метод формирования биокомпозитов на поверхности имплантатов из нержавеющей стали // Биотехносфера. – 2012. – № 5–6 (23–24). – C. 63–69.
7. Barrere F., van der Valk C.M., Dalmeijer R.A. et al. Osteogenecity of octacalcium phosphate coatings applied on porous metal implants // J. Biomed. Mater. Res. – 2003. – Vol. 66A. – P. 779–788.
8. Helfet D.L. tt al. AO philosophy and principles of fracture managmentits evolution and evaluatijn. J. Bone Joint Surg. Am. 85– A:1156, 2003.
9. Tverdokhlebov S.I., Bolbasov E.N., Shesterikov E.V., Malchikhina A.I., Novikov V.A., Anissimov Y.G. Research of the surface properties of the thermoplastic copolymer of Vinilidene Fluoride and Tetrafluoroethylene modified with radio-frequency magnetron sputtering for medical application // Applied surface science – 2012 – Vol. 263 – pp. 187–194.
10. Yuan H., Van den Doel M., Li S.H. et al. A comparison of the osteoinductive potential of two calcium phosphate ceramics implanted intramuscularly in goats // J. Mater. Sci. Mater. Med. – 2002. – Vol. 13. – P. 1271–1275.
В настоящее время в медицине одним из актуальных направлений помощи больным с повреждениями и заболеваниями опорнодвигательного аппарата является поиск новых технологий, основанных на использовании имплантатов с биоактивным покрытием. Их основная цель – не только гарантировать успех лечения, но и осуществить это в очень короткие сроки [1, 2, 8].
Остеоиндуктивные и остеокондуктивные свойства используемых материалов зависят от химического состава поверхности (наличие биоактивных элементов), ее топографии и архитектоники (шероховатость, размер пор) [10].
Доказано, что металлические имплантаты, поверхность которых покрыта наночастицам фосфатов кальция, стимулируют остеогенную активность. при этом степень последней может зависеть от способа нанесения биоактивного слоя [5–7, 9].
Одним из критериев обоснования использования новых видов имплантационных материалов и изделий медицинского назначения являются результаты доклинических испытаний. Основная цель данного вида исследований заключается в определении биологического действия и местной реакции тканей на имплантацию.
В этом плане, одним из информативных является методов оценки местной температурной реакции, что косвенно может отражать особенности локального кровообращения, интенсивность воспалительной реакции и активность процессов костеобразования в целом. в клинической практике этот метод может использоваться в качестве дополнительного при диагностике, прогнозе течения и оценки качества проводимого лечения различных патологических состояний опорно-двигательной системы [3, 4].
Целью настоящего исследования являлось определение температурной реакции тканей в области имплантации накостных титановых пластин с биоактивным покрытием, нанесенным разными способами.
Материалы и методы исследования
Проведено пилотное исследование на взрослых (старше 1 года) беспородных собаках обоего пола. Животные были разделены на 4 серии в зависимости от вида имплантируемого изделия и способа нанесения биоактивного покрытия.
Во всех случаях в условиях операционной с медиальной поверхности диафиза большеберцовых костей моделировали повреждение надкостницы. Для этого выполняли продольный разрез параоссальных мягких тканей протяженностью 2,5 см. Надкостницу разрезали так же в продольном направлении и при помощи шпателя отслаивали от компактной кости. После этого на корковую пластинку устанавливали титановые накостные имплантаты, выполненные в виде пластин шириной 1,0 см, длиной 2,0 см и толщиной 1 мм. при этом пластины имели изгиб, повторяющий рельеф кости. Затем на надкостницу и мягкие ткани накладывали узловые швы. Все изделия были изготовлены с использованием аддитивных технологий (методом 3D печати).
Во всех сериях на поверхности имплантатов был слой биоактивного покрытия на основе гидроксиапатита.
В серии 1 использовали пластины без отверстий (n=3), а в качестве способа нанесения покрытия был применен метод микродугового оксидирования (КФ МДО). Данная технология позволяет формировать покрытия с развитой пористой поверхностью.
В серии 2 на пластины без отверстий (n=3) было нанесено покрытие методом высокочастотного магнетронного распыления (КФ ВЧМР). Оно позволяет формировать тонкие плотные, эластичные кальций-фосфатные покрытия с высокими адгезионными свойствами.
В серии 3 и 4 использовали пластины с отверстиями с покрытием нанесенным методом КФ МДО (n=3) и КФ ВЧМР (n=3) соответственно.
Температурную реакцию покровных тканей в области расположения имплантата регистрировали в периоды: перед операцией, через 7, 14, 21 и 28 суток после выполнения оперативного вмешательства. Для этого использовали реограф-полианализатор РГПА-6/12 «РЕАН-ПОЛИ» (НПКФ «МЕДИКОМ-МТД», Россия) и входящий в комплект принадлежностей, контактный температурный датчик термисторного типа – ДТ-3. Показания снимали с участков, освобожденных от шерстного покрова. в качестве физиологической нормы, которую принимали за 100%, использовали результаты, полученные перед операцией, а так же данные от 15 клинически здоровых (интактных) животных соответствующего возраста.
Дополнительно выполняли визуальную оценку состояния мягких тканей в проекции имплантации.
Исследования проводили в утренние часы перед первым кормлением. Температура воздуха в помещении во время проведения обследования составляла 28,6 ± 0,1°С.
При выборе основных периодов обследования руководствовались регламентирующими стандартами, относящимися к времени кратковременной имплантации биостабильных материалов, которое в норме составляет от 1 до 4 недель (по «ГОСТ Р ИСО 10993–6–2009. Национальный стандарт Российской Федерации. Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 6. Исследования местного действия после имплантации»).
Анализ количественных данных проводили методами описательной статистики. Результаты исследований обрабатывали методами непараметрической статистики (критерий Вилкоксона для независимых выборок). Различия показателей считали достоверными при р ? 0,05.
Эксперименты выполнены на базе вивария ФГБУ «РНЦ «ВТО» им. акад. Г.А. Илизарова» Минздрава России. Животные содержались в индивидуальных боксах (по одному). Получали одинаковые стандартные, сбалансированные по питательным веществам, корма и чистую питьевую воду.
До начала исследований было получено одобрение Комитета по этике ФГБУ «РНЦ «ВТО» им. акад. Г.А. Илизарова» на их выполнение.
Результаты исследования и их обсуждение
При визуальной оценке состояния мягких тканей в проекции имплантации тестируемых материалов определили, что процессы эпителизации раневых поверхностей в области швов протекали без особенностей. Признаков острого воспаления, гематомы и очагов некроза выявлено не было. Швы были сняты в общепринятые сроки (через 7–10 суток после оперативного вмешательства).
При изучении температурных данных выявили, что эти значения у интактных животных и экспериментальных собак в области планируемого оперативного вмешательства варьировали в диапазоне 30,06–33,76°С и в среднем составляли 31,43±1,1°С.
Во всех сериях опытов через 7 суток после операции регистрировали однонаправленные изменения локальной температуры тела в сторону увеличения, значения которой между собой достоверных различий не имели (р=0,8). Разница показателей по отношению к нормальным значениям составляла в среднем 2,78±0,5°С (p=0,002). Следует отметить, что в сериях 1 и 3, когда применяли накостные пластины с покрытием, нанесенным методом КФ МДО, температура тканей в зоне расположения имплантатов была выше на 0,75°С в сравнении с аналогичными значениями при использовании пластин покрытых методом КФ ВЧМР (серии 2 и 4).
К 14 суткам эксперимента температура тканей продолжала равномерно увеличиваться во всех сериях. Ее значения были достоверно выше нормы на 3,69±0,3°С (p=0,002) и составляли 35,12±0,3°С. в этот период, не смотря на отсутствие достоверных различий между сериями, температура тканей в сериях 1 и 2 (пластины без отверстий) была выше на 0,42°С чем в случаях, когда использовали имплантаты с отверстиями.
Через 21 сутки поле операции регистрировали наиболее выраженные различия изучаемого показателя между сериями в зависимости от типа изделия. Так, в сериях с пластинами без отверстий (1 и 2) температура в области расположения имплантата продолжала увеличиваться и составляла в среднем 35,29±0,3°С. Тогда как в сериях 3 и 4 – происходило ее резкое достоверное понижение до верхней границы нормы. у этих животных разница по отношению к предыдущему сроку обследования была в среднем 2,0°С.
Динамика локальной температуры тканей в периоде эксперимента представлена на рисунке.
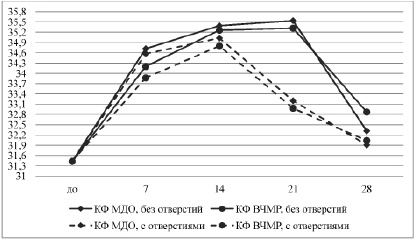
Динамика температурной реакции тканей в области расположения накостных имплантатов с биоактивным покрытием, изготовленных из титановых сплавов по аддитивным технологиям
Таким образом, в результате выполненного исследования была определена местная температурная реакция тканей на материалы, имплантируемые под поврежденную надкостницу большеберцовой кости собаки в периоды 1–4 недели эксперимента. в качестве тестируемых образцов использовали накостные пластины без отверстий и с отверстиями, изготовленные из титана по аддитивной технологии, методом 3D печати. Каждая из пластин была покрыта слоем гидроксиапатита, нанесенного по технологии микродугового оксидирования, либо высокочастотного магнетронного распыления.
Анализ полученных результатов показал, что в течение первых двух недель после операции температура тканей в области расположения имплантатов резко повышалась и ее динамика особо не зависела от типа тестируемого изделия, а также способа нанесения биоактивного покрытия. не смотря на то, что в этот период при использовании накостных пластин с покрытием, нанесенным методом КФ МДО, температурные значения были несколько выше, чем у изделий с покрытием КФ ВЧМР, мы считаем, что подобный эффект мог быть обусловлен в большей степени самой процедурой хирургического вмешательства.
Заключение
Полученные данные в последующем будут использованы как дополнительные, при оценке особенностей кровообращения в тканях области имплантации тестируемых изделий. Будут учитываться при анализе результатов гистологических исследований. Подобный комплексный подход позволит определить оптимальную пористость и топографию поверхности для накостных и внутрикостных имплантатов с биоактивным покрытием на основе гидроксиапатита, изготовленных из титановых сплавов с помощью аддитивных технологий.
Данное исследование выполнено при финансовой поддержке гранта РНФ «Установление закономерностей остеоинтеграции медицинских имплантатов на основе аддитивного производства с биоактивным покрытием», соглашение № 16–17–00176, в рамках задачи по выявлению оптимальной пористости и топографии поверхности для адгезии биоактивного покрытия на основе гидроксиапатита.
Эволюция остеосинтеза: от металла до ультразвука
Насколько серьезными будут последствия перелома, во многом зависит от правильной фиксации отломков костей. Стандартным решением вопроса является наложение гипса, который и обеспечивает иммобилизацию поврежденного участка. Но всегда ли этого метода достаточно? Может ли он помочь при сложных переломах? Когда решить проблему с помощью гипса невозможно, травматологи используют остеосинтез — хирургическую процедуру, при которой обломки фиксируются с помощью различных конструкций, например, штифтов, спиц, пластин, винтов и прочего.
Одним из наиболее известных разработчиков методов остеосинтеза был советский хирург Гавриил Абрамович Илизаров. В честь дня его рождения, который мы отмечаем 15 июня, MedAboutMe расскажет, что дает остеосинтез, где применяется и какие новые методики сегодня используются.
Особенности остеосинтеза при травмах костей
Преимуществ у остеосинтеза немало. Методика позволяет фиксировать поврежденные участки костей на длительное время, а иногда имплантаты остаются у пациента на всю жизнь. Это критически важно для людей пожилого возраста, у которых кости срастаются крайне медленно даже при неосложненных переломах. Также различные фиксационные системы незаменимы при множественных повреждениях кости — они обеспечивают правильную позицию осколков, дают участкам срастись правильно. Помогает технология без осложнений восстановить поврежденные лучевые кости при нестабильных переломах.
Показаниями к остеосинтезу также являются:
- Переломы, которые не срастаются без фиксации.
- Внутрисуставные повреждения костей.
- Тяжелые переломы у пожилых людей, например, переломы шейки бедра.
- Переломы с острыми отломками, которые могут повредить мягкие ткани или нервы.
- Отстроченные операции — при неправильном сращении костей, смещении обломков, возникновении ложных суставов.
Остеосинтез противопоказан при наличии инфекции, в частности, загрязненной раны на месте перелома. Не ставятся фиксирующие системы на открытые переломы, если зона повреждения достаточно большая, и в том случае если у пациента в анамнезе есть выраженный остеопороз.
В современной практике перед проведением операции обязательно проведение 3D-томографии. Диагностика помогает максимально точно определить объем повреждений и правильно установить конструкцию.
Погружной остеосинтез: применение штифтов
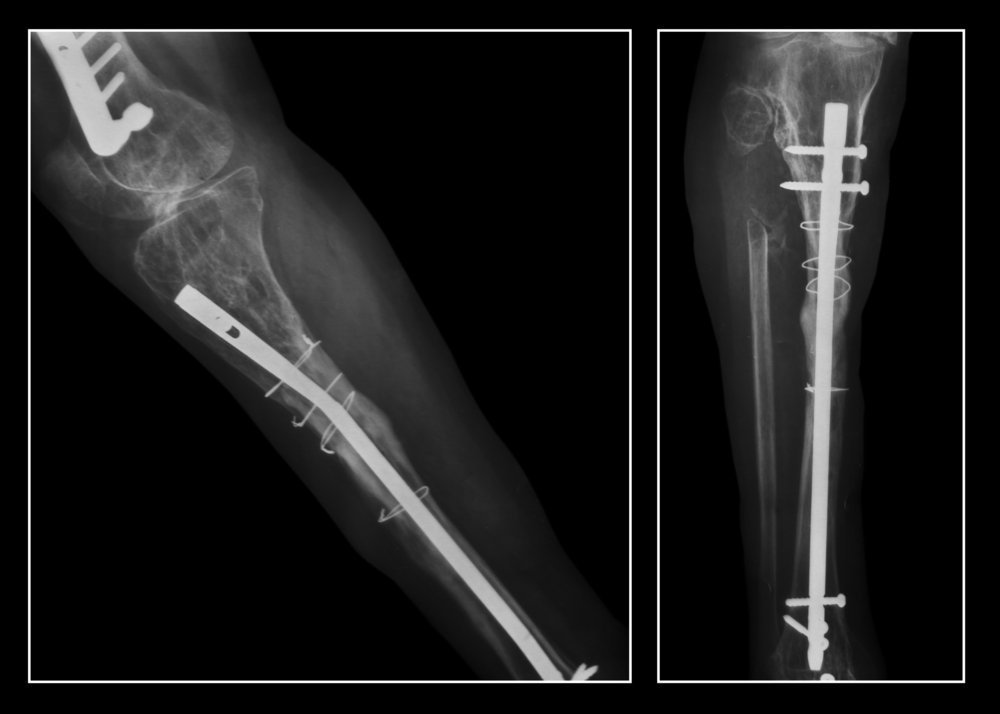
Погружным остеосинтезом называют методы, при которых фиксирующие элементы устанавливаются внутрь кости. Например, золотым стандартом лечения переломов трубчатых костей в зоне диафиза (центрального отдела кости) является блокированный интрамедуллярный остеосинтез (БИОС). В этом случае штифт через разрез не более 5 см вводится непосредственно в костномозговую полость и фиксируется поперечными крепежами. У такого метода сразу несколько преимуществ перед гипсом:
- Надежная фиксация, при которой исключается смещение осколков, поскольку кость, по сути, закреплена на стержне.
- Минимальные повреждения кожи. В зоне самого перелома мягкие ткани вообще не затрагиваются, это помогает сохранить сосуды, которые питают поврежденные участки кости, а значит, ускорить их заживление.
- Уже через день-два после операции пациент может нагружать конечность. Более того, травматологи отмечают, что активность стимулирует рост кости и переломы срастаются быстрее.
Продольные штифты могут использоваться не только для лечения переломов. Например, с их помощью создается каркас для искривленного позвоночника. Основная проблема с такими операциями — использование изогнутых стрежней, которые раньше для каждого пациента гнулись индивидуально в операционной. В 2013 году эта проблема была решена французской компанией Medicrea, создавшей устройство UNiD, которое на основе рентгеновских снимков помогает изготавливать штифт уже с нужным для пациента изгибом. Это сокращает время операции и при этом помогает избежать возможных ошибок.
Погружной остеосинтез: пластины

Другим распространенным методом фиксации различных поврежденных участков кости является накостный метод — наложение пластины поверх кости. Такой остеосинтез может с успехом применяться при лечении сложных переломов, в том числе и суставных. Недостатком метода является необходимость открывать большой участок кости. Такая операция достаточно травматична и сама по себе может спровоцировать ряд осложнений. В том числе воспалительный процесс, вплоть до остеомиелита.
Однако в современной травматологии используются пластины с угловой стабильностью, которые приподнимаются над костью, а значит, позволяют проводить малоинвазивные операции — с минимальным количеством разрезов. Новейшая технология — использование полиаксиальных винтов (LCP), которые при необходимости могут устанавливаться не перпендикулярно, а с наклоном. Это дает возможность не только приподнимать пластину, но и фиксировать ее максимально точно. При этом операции могут проводиться даже людям с остеопорозом, поэтому система подходит для лечения суставных и других сложных переломов у пожилых людей, например, повреждения шейки бедра или проксимального отдела плеча.
Операция по установке современных пластин занимает в среднем 30 минут, поэтому пациенту требуется меньше наркоза. После процедуры поврежденный участок можно нагружать, возвращается подвижность, а это значит, что после сращения костей человеку не потребуется длительный период реабилитации с разработкой суставов.
Особая область применения пластин — фиксация ребер при множественных травмах. Это один из самых тяжелых видов переломов, которые сложно заживают, часто приводят к образованию ложных суставов, смещению костей и прочему. Установка пластины в этом случае не только уже через сутки возвращает человека к привычной жизни, но и помогает избежать отсроченных осложнений. При реберном остеосинтезе имплантаты чаще всего ставятся на всю жизнь и не удаляются после сращивания костей. Сегодня такие операции проводятся и в России, в частности, успешная операция по восстановлению грудной клетки при множественных переломах ребер была проведена в Томске.
Наружный остеосинтез: внешняя фиксация перелома
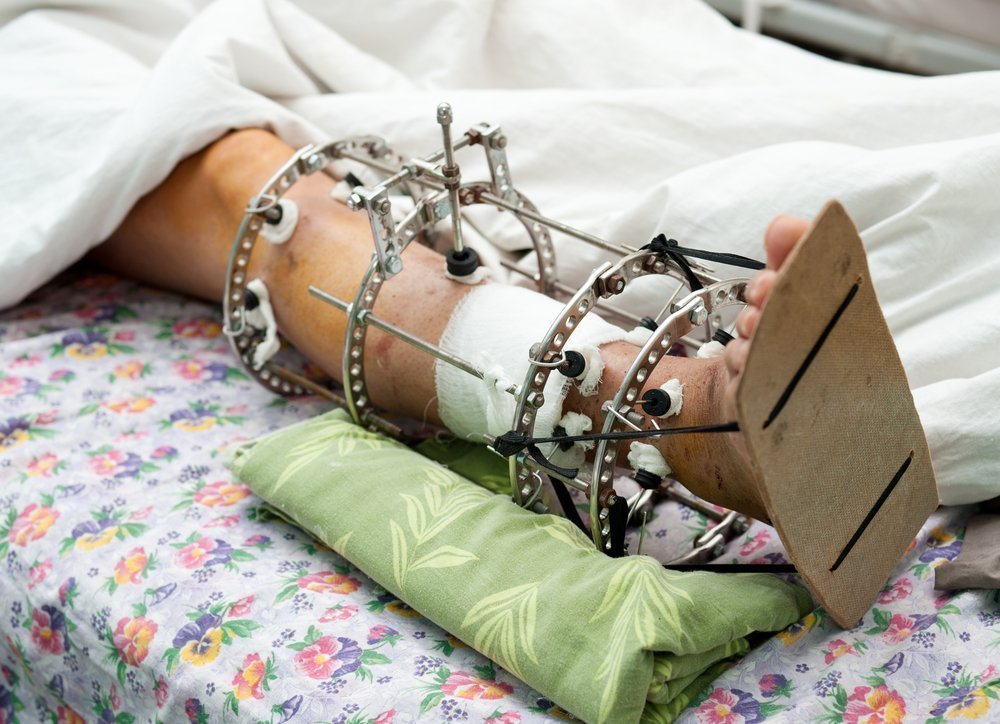
Наружный остеосинтез предполагает установку фиксационной системы над поверхностью кожи. Сами же спицы, которые удерживают кость в правильном положении, проходят поперек нее, а не вдоль, как при интрамедуллярном методе. Для такой иммобилизации разработано множество специальных компрессионно-дистракционных аппаратов, в том числе аппарат Илизарова, Ткаченко, Волкова-Оганесяна и другие.
Основное преимущество чрескостного внешнего остеосинтеза — минимальные повреждения мягких тканей. По сути, врачу нужно сделать лишь несколько точных проколов, через которые вводятся спицы. Сегодня установка конструкций контролируется помощью рентгена, поэтому ошибки практически исключены.
Наружный остеосинтез незаменим при политравме, когда страдает не только скелет, но и мягкие ткани, а сами кости сильно раздроблены. Зафиксировать такие переломы с помощью внутренних конструкций бывает достаточно сложно, а вот внешняя фиксация справляется с этим хорошо.
Как и при внутренних фиксациях, конечность с аппаратом можно нагружать уже через несколько дней. Но после сращения костей спицы обязательно снимаются. Такой метод не подходит при медленно заживающих переломах или же в случае, когда имплантат необходим пожизненно. По этой причине конструкции крайне редко устанавливаются пожилым людям. А вот для молодых пациентов наружный остеосинтез применяется повсеместно.
Ультразвуковой остеосинтез
Ультразвуковой остеосинтез — принципиально новый метод фиксации, при котором не используются заготовленные титановые штифты, пластины, спицы и прочее. Костные фрагменты соединяются с помощью полимерного конгломерата. Перед процедурой в поврежденный участок помещается специальный наполнитель, который под действием ультразвуковой вибрации заполняет трещины и твердеет. Именно поэтому метод еще называют ультразвуковой сваркой костей.
Ультразвуковой остеосинтез уникален тем, что может использоваться при осколочном переломе, раздроблении кости. «Сварка» успешно справляется с фиксацией даже небольших фрагментов и возвращает прочность поврежденному участку. В отличие от внешних конструкций такой имплантат остается в теле на всю жизнь.
Ультразвуковой остеосинтез может применяться и тогда, когда требуется наращивание кости. Например, такой имплантат ставится в том случае, если часть кости была удалена в ходе операции.
Риск остеопороза постепенно повышается, начиная с 40-45 лет, особенно среди женщин, что связано с климактерическими изменениями гормонального фона. Помочь в оценке рисков этого обменного нарушения вам поможет наш тест.
Противопоказания к МРТ

Магнитно-резонансная томография в клинической практике используется более 30 лет, и за этот срок апробации не было выявленного ни одного случая негативного воздействия МРТ на здоровье человека. Также, как и УЗИ, этот метод считается абсолютно безопасным, но для данного вида диагностики существует ряд абсолютных (выполнять исследование нельзя) и относительных (исследование возможно, если польза превосходит риск) противопоказаний. Весь список противопоказаний условно можно разделить на противопоказания, связанные с физикой работы магнитно-резонансного томографа, и ограничениями, связанными с введением контрастного препарата.
ЗАПИСЬ НА ПРИЕМ
Абсолютные противопоказания
Абсолютные противопоказания к томографии определяются особенностями получения изображений на МРТ аппарате. Принцип работы томографической установки строится на явлении ядерного магнитного резонанса. Когда тело пациента попадает внутрь сканера, вокруг него образуется сильное магнитное поле и радиочастотные волны. Под этим воздействием атомы водорода в клетках организма начинают совершать колебательные движения. Этот резонанс улавливает компьютер установки, оцифровывает сигналы и переводит их в трёхмерные изображения. Следует помнить, что магнитно-резонансный томограф – это очень сильный магнит. Как и любой магнит, он имеет свойство притягивать металл и выводить из строя любые электронные устройства. Поэтому абсолютные противопоказания к МРТ включают в себя:
- вживленные в тело металлические импланты (стальные пластины, протезы, скобы, скрепы). Под действием магнитного поля томографа металл нагревается, может произойти расширение и движение, что приведет к внутреннему кровотечению или ожогу.
- внедренные в тело стимуляторы (кардиостимулятор, ушной имплант, инсулиновая помпы). Под воздействием магнитного поля электроустройства могут выйти из строя и сломаться.
Однако не любые импланты станут абсолютным противопоказанием к МРТ. В первую очередь, важно узнать, из какого металла они изготовлены. Если металл имеет ферромагнитные свойства, проводить МРТ обследование нельзя. В современной медицине уже практически не используются магнито-чувствительные компоненты. Большинство имплантов сделаны из титана или медицинского пластика, и проходить томографию с ними можно.
Если у пациента есть в теле осколки, пули или другие металлические инклюзии, и он не знает, из какого металла они сделаны, чтобы решить вопрос о возможности проведения МРТ, нужно будет сделать обычную рентгенографию. Рентген четко покажет наличие металла в составе инородных объектов в организме.
Ещё 10 лет назад наличие кардиостимулятора было абсолютным противопоказанием к МРТ. На данный момент в медицине используются сердечные водители ритма, которые совместимы с магнитным полем. Поэтому, чтобы уточнить, можно ли с вашим водителем ритма сделать МРТ, врач попросит предъявить паспорт изделия. Если в нём стоит отметка о совместимость с МРТ, делать томографию можно.
Относительные противопоказания
Относительные противопоказания к МРТ включают в себя следующие случаи:
- полные и габаритные пациенты. Большая часть аппаратов производится с ограничением по весу 120 кг и максимальным обхватом окружности тела 120 см. В Санкт-Петербурге есть ряд клиник, оборудованных установками с грузоподъемностью 200 кг и максимальным обхватом 140 см. Пациентам с большими объемами в качестве альтернативы могут быть предложены УЗИ или рентген.
- на кожных покровах пациента присутствуют татуировки с металлическими вкраплениями. В этих местах на высокопольных аппарата мощностью 1.5 Тесла и выше может происходит нагрев тела, что может привести к ожогу.
- клаустрофобия. Для лиц, страдающих паническими атаками в замкнутом пространстве, есть возможность пройти исследование на открытом томографе, либо можно сделать МРТ под наркозом или седацией.
МРТ с контрастом - противопоказания
Если вам назначили сделать томографию с контрастом, следует учесть дополнительное ограничение. При введении контраста противопоказанием является:
- беременность на всем сроке вынашивания;
- почечная недостаточность;
- наличие аллергии на препараты гадолиния.
При томографии с контрастом пациенту дополнительно вводится контрастный состав на базе солей гадолиния. Это вещество быстрого распада. Оно выводится мочевыделительной системой в течение 10-24 часов. Но при процедуре контрастирования возникает дополнительная нагрузка на почки. Они могут не выдержать ее, если пациент страдает почечной недостаточностью. Поэтому таких больных попросят сдать анализ крови на креатинин, чтобы оценить риск развития нефропатии.
Кормление грудью не является противопоказания к МРТ с контрастом. Женщине просто необходимо воздержаться от кормления грудью на двое суток. За это время контрастный состав полностью выйдет из организма, и не будет угрозы попадание его остатков через молоко матери в организм младенца.
Противопоказания к МРТ головного мозга
Когда назначают сделать МРТ головного мозга, обычно у пациентов возникает вопрос о возможных дополнительных противопоказаний, например:
- наличие брекетов, зубных имплантов, штифтов и коронок;
- наличие сосудистых клипс на сосудах головного мозга.
Делать томографию головы с зубными имплантами можно. В современной стоматологии уже давно используются композитные материалы, у которых нет металломагнитных сплавов в свойстве. Ваши зубные коронки и штифты не могут повредить сканированию. Само магнитное поле никакого негативного воздействия на них тоже не оказывает.
Ситуация с брекетами более сложная. В большинстве случаев пройти МРТ головного мозга, когда у пациента во рту есть несъемные брекет-системы, можно. Однако некоторые брекеты могут давать артефакты засвета на снимках, тем самым ухудшает качество изображения. Если эти артефакты будут слишком сильными, рентгенолог остановит диагностику и предложит альтернативные методы сканирования.
Сосудистые клипсы, которые были установлены в ходе аневризма-корректирующей операции является противопоказанием к МРТ в первые шесть месяцев после хирургического вмешательства. По истечении этого срока осуществлять магнитно-резонансную томографию можно, однако о наличии сосудистых клипсов нужно обязательно предупредить врачам и принести с собой на диагностику описание модели сосудистой клеммы.



Противопоказания к МРТ позвоночника
Основная сложность при проведении МРТ позвоночника заключается в необходимости соблюдать полную неподвижность в ходе обследования на протяжении 15–20 минут. Иногда болевой синдром в спине не позволяет пациенту вылежать сессию сканирования. Поэтому, при сильно выраженных болям в позвоночнике, томографию лучше всего сделать после того, как вы примете обезболивающие, или вам проведут процедуру медикаментозной блокады.
Противопоказания к МРТ суставов
Большинство суставных протезов совместимы с МРТ, например, титановые эндопротезы тазобедренных суставов. Исключения составляют лишь стальные протезы, которые были на вооружении у советских медиков 30-40 лет назад. Если в состав вашего импланта входит стальной сплав, делать МРТ нельзя. Альтернативным методам обследования в такой ситуации станет КТ и ультразвуковая диагностика на аппарате экспертного класса.
Противопоказания после МРТ
Магнитно-резонансная томография не имеет противопоказаний после процедуры. Пациент может вернуться к обычному образу жизни сразу после диагностики. Никакого реабилитационного периода не предполагается. Исключение составляют лишь редкие случаи, когда томографию проводили под наркозом. Из-за остаточного действия седации после МРТ под наркозом нельзя в течение суток управлять транспортным средством.
Противопоказания к МРТ брюшной полости
МРТ брюшной полости иногда трудно сделать пациентам с сердечными проблемами и хроническими заболеваниями легких. Дело в том, что в ходе томографии брюшной полости пациенту нужно будет несколько раз на 20 секунд задерживать дыхание. Это сложная задача для больных с нарушениями сердечного ритма, астмой и легочной недостаточностью.
Ещё одним ограничением к томографии органов брюшной полости может быть плохая подготовка пациента. Если больной не выполнил требования по диете перед обследованием, излишнее газообразование в кишечнике может привести к тому, что снимки будут низкого качества, и рентгенолог не сможет сделать качественное описание результатов диагностики.
Противопоказания к МРТ органов малого таза
При проведении МРТ малого таза у женщин противопоказанием является менструация. В период месячных делать томографию нецелесообразно, поскольку рентгенолог не сможет увидеть состояние яичников. Беременность не является противопоказанием к МРТ, однако это сканирование проводится беременным женщинам по направлению врача.
Противопоказания при МРТ ребенку
Магнитно-резонансную томографию можно делать детям любого возраста, включая новорожденных и грудничков. Сложность диагностики маленьких пациентов заключается в том, что от них трудно добиться полной неподвижности. Поэтому детям до 3 лет томографию проводит под наркозом. Введение анестезиологического пособия накладывает дополнительные ограничения на процедуру. Чтобы врач мог убедиться, что сердце и легкие ребёнка выдержат фармакологического нагрузку, необходимо будет сдать ряд анализов мочи и крови, сделать ЭКГ и принести заключение невролога.
Частые вопросы от пациентов

Являются ли противопоказанием при МРТ зубные импланты
Зубные импланты не является противопоказанием к МРТ, даже если они сделаны из золота или стальных сплавов. Однако об их присутствии в ротовой полости нужно обязательно предупредить врача, если вы делаете МРТ головного мозга, МРТ гипофиза, МРТ сосудов головного мозга и МРТ височно-нижнечелюстного сустава. Стальные импланты и коронки могут давать сильный артефакт засвета на томограммах. Чтобы врач по ошибке не принял их за признаки патологии, он должен знать обо всех имплантах во рту. Кроме того, зная о зубных протезах, оператор МРТ может выстроить программу таким образом, чтобы подавить негативные эффекты от металл-артефактов и максимально улучшить качество снимков.
Являются ли противопоказанием при МРТ зубные коронки и штифты
Зубные коронки, протезы и штифты не являются противопоказанием к магнитно-резонансной томографии, но о них нужно предупредить врача, если вы собрались делать томографию головы. Тогда врач сможет выставить специальную артефакт-подавляющую программу и максимально улучшить качество изображения. Магнитное поле томографа никоим образом не влияет на состояние ваших зубных имплантов. Они не могут никуда сдвинуться, поломаться или получить дефект покрытия.
Является ли МРТ противопоказанием для беременности
Беременность не является абсолютным противопоказанием к МРТ. Более того, современные пренатальные диагностики активно использует томографию для того, чтобы выявить патологии центральной нервной системы у плода на этапе вынашивания. На информационных сайтах о медицине можно встретить фразу о том, что МРТ не проводится женщинам в первый триместр беременности. Связано такое ограничение с тем, что врачи хотят перестраховаться и оградить женский организм от легкого теплового воздействия, когда тело пациентки находится внутри аппарата. Начиная со второго триместра беременности МРТ, как и УЗИ, считается безопасным методом диагностики. Однако большинство медцентров беременным женщинам делает сканирование по направлению врача.
МРТ с контрастом не проводится беременным женщинам на протяжении всего срока вынашивания. Дело в том, что действие гадолиний-содержащего препарата на формирование и развитие центральной нервной системы ребенка до конца не изучены. Поэтому томографию с контрастом во время беременности делают в крайнем случае, когда стоит вопрос угрозы жизни матери.
Топ-5 рискованных модификаций тела: от пирсинга до «языка змеи»

Модификация тела – излюбленное занятие человечества. Серьги в ушах давно стали нормой и уже никого не удивляют. Реже люди занимаются и другими украшательствами, модифицируя внешний облик в соответствии со своими вкусами и фантазиями. Иногда это смотрится дико, иногда – удивительно, а бывает, что и завораживающе. Но надо понимать, что люди, решившиеся по доброй воле модифицировать свой внешний вид, немало рискуют. Даже с учетом развитой медицины и возможности заниматься модификациями в клиниках пластической хирургии.
MedAboutMe разбирался, какие опасности несут в себе процедуры пирсинга, нанесения тату, скарификации и др.
Пирсинг

Эксперты из American Academy of Dermatology определяют пирсинг как процедуру создания отверстий в теле человека для вставки драгоценностей и иных украшений. Это самая популярная разновидность модификации тела человека. Отверстия люди делают везде, где только можно: в ушах, носу, бровях, языке, губах, сосках и наружных половых органах.
По данным опроса 2017 года, проведенного в США, 32% граждан имеют одно отверстие «под украшения» на теле, 34% – 2-3 отверстия, у 18% – уже 4-5 таких дырок. 1% участников опроса заявил о более чем 20 проколах.
Россияне к пирсингу относятся с некоторым негативом. В 2014 году, согласно результатам опроса, проведенного Левада-центром, 53% россиян резко отрицательно относятся к пирсингу, а скорее положительно и полностью одобряют – 11% и 2%, соответственно. Правда, тут может играть роль вопрос формулировок, ведь серьги – это тоже пирсинг, но уха, а в нашей стране под этим словом чаще подразумевают проколы в других частях тела.
Чем рискуют люди, которые делают себе пирсинг?
- Местная инфекция. Это самое распространенное осложнение процедуры. Чаще всего возникает при прокалывании уха или пупка.
- Боль. Неудачный прокол может быть болезненным сам по себе, а может впоследствии вызывать постоянную боль.
- Контактный дерматит. Это поражение кожи, которое развивается при контакте с украшением, вставленным в прокол. Чаще всего это реакция на никель. Более того, среди людей с пирсингом аллергия на никель встречается в 3 раза чаще, чем среди тех, кто никогда не увлекался «отверстиями в теле»: 20,8% против 6,4%.
- Отек. Может быть признаком аллергической реакции или воспаления. Если не проходит через день-два и даже увеличивается, надо срочно обратиться к врачу, так как скорее всего в рану попала инфекция.
- Аргирия. Изменение цвета кожи до синевато-серого под действием серебра. При этом частицы металла осаждаются в мембране кожных желез и стимулируют меланоциты – клетки, которые вырабатывают пигмент меланин. Солнечный свет, попадая на кожу, кроме того, приводит к восстановлению серебра в коже до сульфида и селенида серебра в виде черно-коричневых гранул. Это редкая патология, тем не менее вполне реальная.
- Келоидные рубцы. Это разрастание тканей, которое выглядит как куполообразное блестящее розово-красное образование, может появляться через некоторое время после прокола. Они могут быть большими по размеру, болеть и зудеть. Чаще всего образуются на мочке уха, груди, спине и плечах.
- Системные инфекции, то есть, распространяющиеся на другие части тела. Среди инфекций, которые можно подхватить в салоне, где не соблюдаются правила гигиены и асептики – сепсис, ВИЧ, гепатиты В и С, столбняка, стафилококковые и стрептококковые патогенные микроорганизмы.

Кожные импланты (пирсинг кожи)

Кожные импланты подразумевают размещение инородные тел в целях боди-арта подкожно (подкожные импланты) или трансдермально. В последнем случае под кожу имплантируется фиксатор (база, основание) для самого ювелирного изделия или арт-элемента, который вставляется или накручивается на резьбу в базе.
Это не самая опасная для организма процедура, осложнения при ее проведении минимальны, если конечно речь идет о стерильных условиях и пластическом хирурге. Тем не менее могут возникнуть следующие негативные эффекты:
- Отторжение импланта.
- Инфекция. Стандартный набор – ВИЧ, гепатиты, стафилококковые инфекции и др.
- Образование язв на месте внедрения импланта и долгое сложное заживление.
- Повреждение нервов и мышц на месте внедрения импланта.
- Аллергические реакции на материал импланта.
- Хроническая боль.

Скарификация
Процедуру скарификации также называют шрамированием. Собственно суть ее проста: создание рисунка на коже из шрамов. Кожу разрезают под определенным углом, чтобы шрам получился выпуклым. Другой вариант – истирание или вырезание верхнего слоя кожи, чтобы на месте повреждения получилось углубление на теле. Также скарификация может быть химической (выжигание на коже при помощи едких веществ), ожоговой (по сути – клеймение при помощи раскаленных предметов или вымораживающего кожу жидкого азота) или при помощи лазера. Иногда в рану добавляют пепел, сажу или цветные пигменты для получения более яркого рисунка.
С какими осложнениями может столкнуться человек, решившийся на процедуру скарификации?
- Инфекция. В этом случае чаще всего речь идет о системной инфекции – гепатиты, ВИЧ, и др.
- Образование некротических язв с черными струпьями или неглубоких язв с желтой коркой как осложнения клеймения раскаленным металлом.
- Септический шок, тромбоз кавернозного синуса, абсцесс селезенки – это довольно редкие, но очень тяжелые осложнения, которые могут привести к смерти человека. Указанные случаи описывают в своей статье за 2009 год в журнале Journal of Medical Case Reports ученые из США, Пакистана и ОАЭ, отмечая, что все пациенты с такими осложнениями до процедуры клеймения имели ряд хронических заболеваний.
- Отек, который может держаться довольно долго, причиняя страдания пациенту.
- Келоидные рубцы, которые будут выглядеть совсем не так, как планировал пациент.
- Язва Марджолина – агрессивный плоскоклеточный рак, развивающийся в области поражения.
«Язык змеи»
«Язык змеи» (сплит языка) – так называется модификация, при которой кончик языка разделяют пополам по средней линии. Это результат хирургической процедуры, которую выполняют скальпелем или лазером.
Умельцы также для раздваивания языка используют метод связывания. При этом сначала выполняется прокол в центре языка, туда вводится леска и туго завязывается так, чтобы она врезалась в язык, постепенно его рассекая. Леску следует постоянно подтягивать. От страдальца, который решил разрезать язык таким способом, требуется довольно долго переносить сильную боль в языке и опухшие гланды. Все это мешает есть, пить и говорить.
Сразу уточним: как и все остальные процедуры модификации, разрезание языка следует доверить специалистам. В данном случае речь идет уже не о салоне, а о клинике пластической хирургии, где специалисты позаботятся о том, чтобы осложнений не наступило.
Итак, чем чревато разрезание языка пополам, выполненное вне стен клиники непрофессионалами?
- Сильное кровотечение.
- Инфекция. Гепатит, ВИЧ, сепсис и др.
- Повреждение нервов и разрушение желез, расположенных на языке. Все это может привести к изменению вкуса, потере чувствительности и нарушению речи.
- Отек языка. При сильном отеке язык может перекрыть дыхательные пути.
Татуировки

Татуировка – это тоже разновидность модификации тела. При этом в кожу вводятся чернила, которые поглощаются клетками иммунной системы макрофагами. Это клетки-мусорщики, они заняты сбором и поеданием остатков отмерших клеток, бактерий, чужеродных для организма частиц. Чернила как раз относятся к таковым. Большая часть макрофагов, сожравших частицы чернил, остаются на том же месте, становясь частью рисунка. Когда эти макрофаги погибают, чернильные частицы поедаются следующим поколением и т.д.
В 2018 году французские ученые из Aix Marseille Université разработали метод удаления татуировок. Они предложили временно блокировать процесс обновления макрофагов, чтобы частицы краски успевали вымываться с места рисунка по лимфатическим сосудам.
Каких негативных последствий можно ожидать от процедуры нанесения татуировки?
Осложнения дентальной имплантации: причины и новые исследования

Имплантация зубов — серьезная операция по восстановлению прикуса, которая связана с длительным периодом подготовки и лечения. Но, несмотря на знания стоматологов и наличие высокотехнологического оборудования, осложнения дентальной имплантации все же могут возникать. Что это за осложнения и каковы их причины? Об этом расскажет MedAboutMe.

На каких этапах дентальной имплантации могут формироваться осложнения?
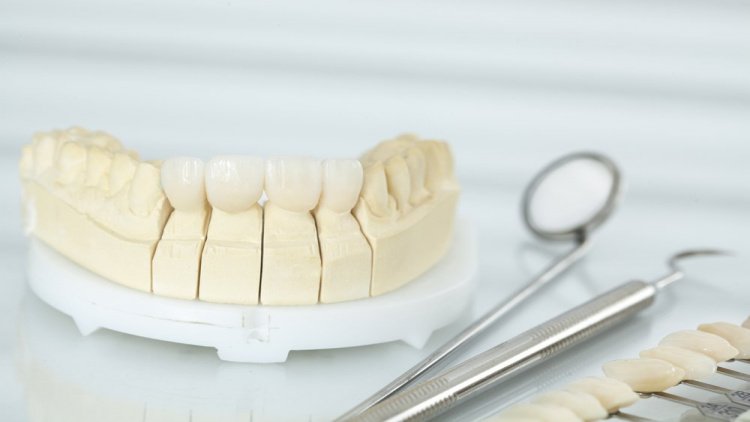
Имплантация проходит в несколько этапов и практически на каждом из них могут возникать те или иные осложнения. Стоматологи выделяют следующие этапы имплантации:
- непосредственно при установке имланта;
- во время ремплантации, когда имплант приживается;
- при установке абаптена (штырь, на который устанавливается коронка зуба);
- уже после имплантации.
Осложнения во время установки импланта
Первые осложнения могут формироваться еще в процессе оперативного лечения. И чаще всего они связаны с особенностями организма, например, аллергические реакции, кровотечение. Во время оперативного вмешательства не исключен и человеческий фактор.
При препарировании бором может развиваться перегрев костных тканей. Такие осложнения могут стать причиной некроза костной ткани и ухудшения качества имплантации. Современные технологии и визуальный контроль на каждом этапе выполнения операции помогут избежать осложнений и сведут их риски к нулю.
Кровотечение — также нередкое осложнение, которое возникает при имплантации. Причины могут быть различными:
- повреждение кровеносных сосудов при подготовке операционного ложа, когда случайно задеваются мягкие ткани лица и лицевой артерии;
- нарушения свертываемости крови. Поэтому перед началом лечения и в период подготовки к имплантации, докторами проводится полный спектр исследования для выяснения свертывающей и противосвертывающей системы крови и наличия болезней, влияющих на эти процессы.
Перфорация костной ткани может заканчиваться тем, что имплант может проникать в полости гайморовой пазухи. Во избежание этих последствий перед имплантацией следует длительный период подготовки и полноценного исследования: КТ черепа, выяснение высоты альвеолярного отростка, и состояние костной ткани. При недостаточном количестве костной ткани могут проводиться дополнительные операции по восстановлению костной ткани.
Также перед операцией докторами изучается анатомия тройничного нерва, при имплантации в некоторые области может происходить затрагивание его ветвей, с соответствующими симптомами: невралгия, боль, онемение, нарушение проводимости и движений.
Воспаление и другие осложнения при приживлении импланта
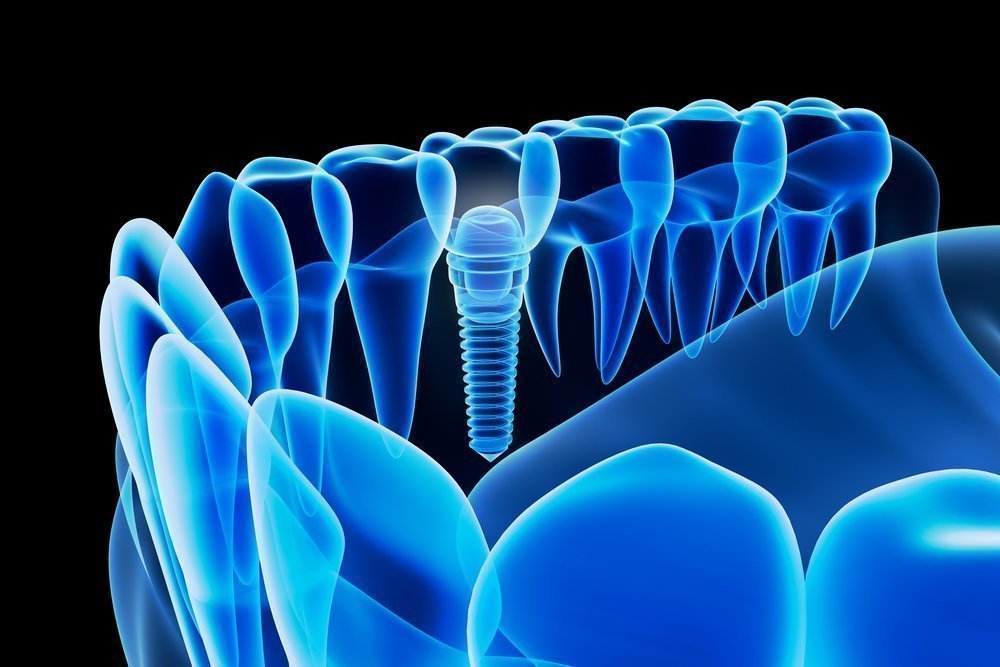
На этапе приживления имплантов, дентальная имплантация может осложниться. Осложнения, которые заслуживают особого внимания — отторжение или воспаление тканей после протезирования.
Воспаление вокруг тканей импланта, к сожалению, может встречаться довольно часто. Оно может формироваться по нескольким причинам. Опытные доктора только по месту кровотечения понимают его причину.
Если воспаление сформировалось над заглушкой импланта, то причина чаще всего скрывается в причине образования кровяного сгустка. При имплантации воспаление может перейти в гнойные формы.
Воспаление развивается и по другим причинам, например, при несоблюдении правил септики и антисептики или при нарушении техники зашивания операционной раны.
Для того чтобы свести все риски отторжения и воспаления к минимуму, перед операцией необходимо проведение подготовительных мероприятий. В первую очередь, санирование полости рта: залечиваются все кариозные зубы, лечится воспаление десен — все очаги хронической инфекции в организме должны быть излечены.
Осложнения имплантации после операции
Осложнения дентальной имплантации иногда возникают буквально сразу после операции или же спустя несколько лет после. Причины осложнений имплантации могут развиваться по разным причинам: технические огрехи или же несоблюдение правил и всех рекомендаций доктора.
Самыми распространенными осложнениями после дентальной имплантации являются боль, кровоизлияние и воспаление в месте имплантации. После имплантации, если появились вышеперечисленные симптомы, необходимо незамедлительно обратиться за помощью к специалистам, чтобы своевременно устранить осложнения.
Любое из перечисленных осложнений, на любом этапе нередко становится причиной удаления импланта.
Как храп влияет на имплантацию?

В 2017 году было опубликовано исследование, показывающее, что у лиц с синдромом обструктивного апноэ сна (храп) выше шансы развития осложнений дентальной имплантации.
Существует множество исследований, доказывающих научным путем связь храпа с кратковременным полным или частичным отсутствием дыхания во сне или бруксизмом.
Доказана тесная взаимосвязь храпа и дентальной имплантации. В исследование было вовлечено 67 пациентов, у 16 были диагностированы осложнения дентальной имплантации и, что самое интересное, у 13 был диагностирован храп.
По мнению большинства стоматологов, храп имеет взаимосвязь с некоторыми стоматологическими заболеваниями, особенно часто осложнения проявляются при протезировании, в том числе, на имплантах.
Пациенты должны понимать, что сегодня дентальная имплантация находится на новом уровне. Осложнения, даже самые незначительные, встречаются крайне редко. Тем более, при соблюдении всех правил постановки имплантов. Отторжение имплантов — так и вовсе нонсенс.
Читайте также:
