Желтый цвет пламени какой металл
Обновлено: 29.04.2024
Эти металлы — очень активные! Именно их кидают в ванны с водой, в результате чего происходят мощщные взрывы.
Щелочные металлы
IA группа называется главной подгруппой первой группы, в которую входят щелочные металлы: литий Li, натрий Na, калий K, рубидий Rb, цезий Cs и франций Fr.
Щелочные металлы — серебристо-белые металлы с высокой электро- и теплопроводностью, обладают ковкостью, пластичностью и металлическим блеском.
Главная особенность строения атомов химических элементов IA группы заключается в том, что они содержат один электрон на внешнем энергетическом уровне — их электронная конфигурация ns 1 .
Из этого следует, что атомам щелочных металлов энергетически выгодно отдать электрон и приобрести конфигурацию инертного газа, приобретая при этом степень окисления +1.
Основным способом получения таких металлов является электролиз расплавов солей.
Химические свойства
Их химические свойства крайне логичны:
- как типичные металлы они будут вступать в реакции со своими противоположностями — неметаллами;
- как восстановители — реагировать с окислителями (в том числе восстанавливать металлы и неметаллы из их оксидов);
- как металлы, стоящие в ряду активности до водорода — вступать в реакции вытеснения с водой, кислотами-неокислителями и солями менее активных металлов.
- Реакции с неметаллами
Как типичные восстановители, щелочные металлы могут взаимодействовать со своими противоположностями — неметаллами.
| Гидриды металлов подвергаются необратимому гидролизу |
В реакциях с щелочными металлами кислород образует ряд веществ:
- литий («кандидат от народа»), как и подавляющее большинство металлов, образует оксид;
4Li + O2 = 2Li2O - натрий образует пероксид;
2Na + O2 = Na2O2 - калий и все нижестоящие металлы — надпероксиды/супероксиды.
K + O2 = KO2
- Реакции с водой
В ряду активности щелочные металлы находятся до водорода, поэтому они способны вытеснять водород из воды:
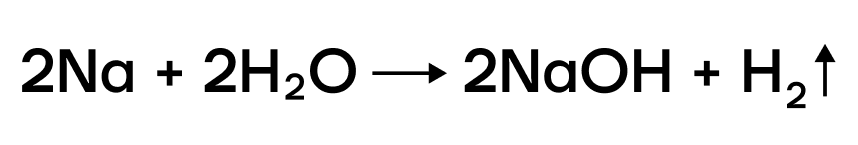
Можно представить воду как HOH, тогда металл (например, натрий) будет замещать один из атомов водорода с образованием NaOH.
За счет крайне низких значений электроотрицательности металлы очень слабо притягивают к себе электроны, а следовательно, у них «легко их украсть». Делаем вывод: в ОВР щелочные металлы проявляют ярко выраженные восстановительные свойства, повышая в реакциях степени окисления.
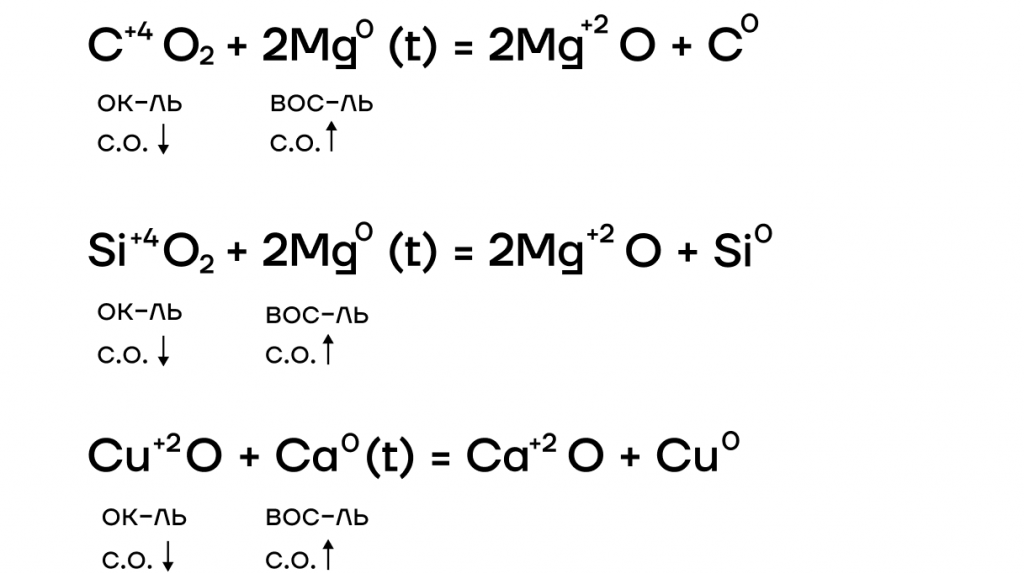
Оксиды щелочных металлов
По физическим свойствам это — бесцветные кристаллические вещества, хорошо растворимые в воде.
Они являются основными оксидами, поэтому:

- вступают в основно-кислотные взаимодействия со своими противоположностями, обладающими кислотными свойствами: кислотами, кислотными оксидами, амфотерными оксидами и гидроксидами:
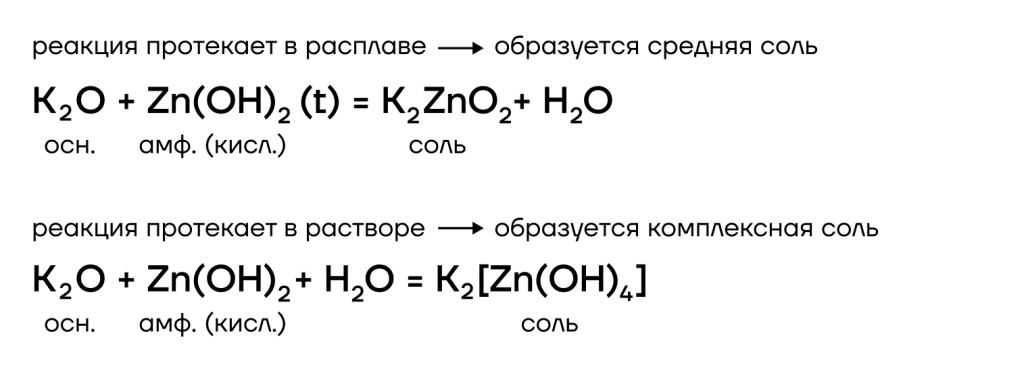
Гидроксиды щелочных металлов
Что же это такое? По-другому их называют щелочами. Они представляют собой бесцветные кристаллические вещества, хорошо растворимые в воде.
По химическим свойствам они являются типичными сильными основаниями, то есть:
- диссоциируют в растворах с образованием гидроксид-анионов. создавая в растворах щелочную среду:
- вступают в основно-кислотные взаимодействия со своими противоположностями (кислотами и кислотными оксидами + амфотерные оксиды и гидроксиды), образуя соли;
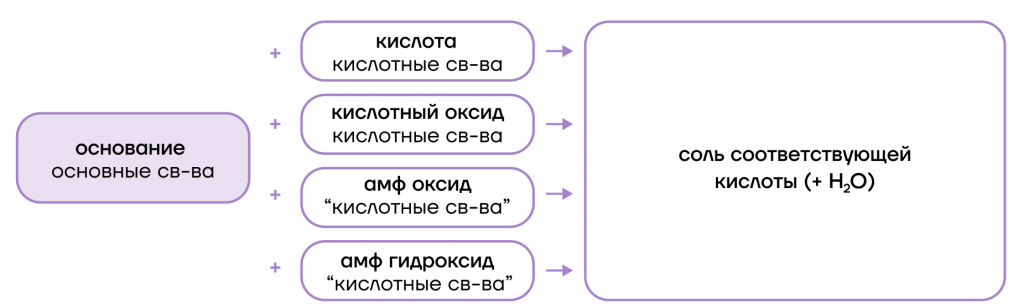
- вступают в реакции ионного обмена с кислотами и солями:
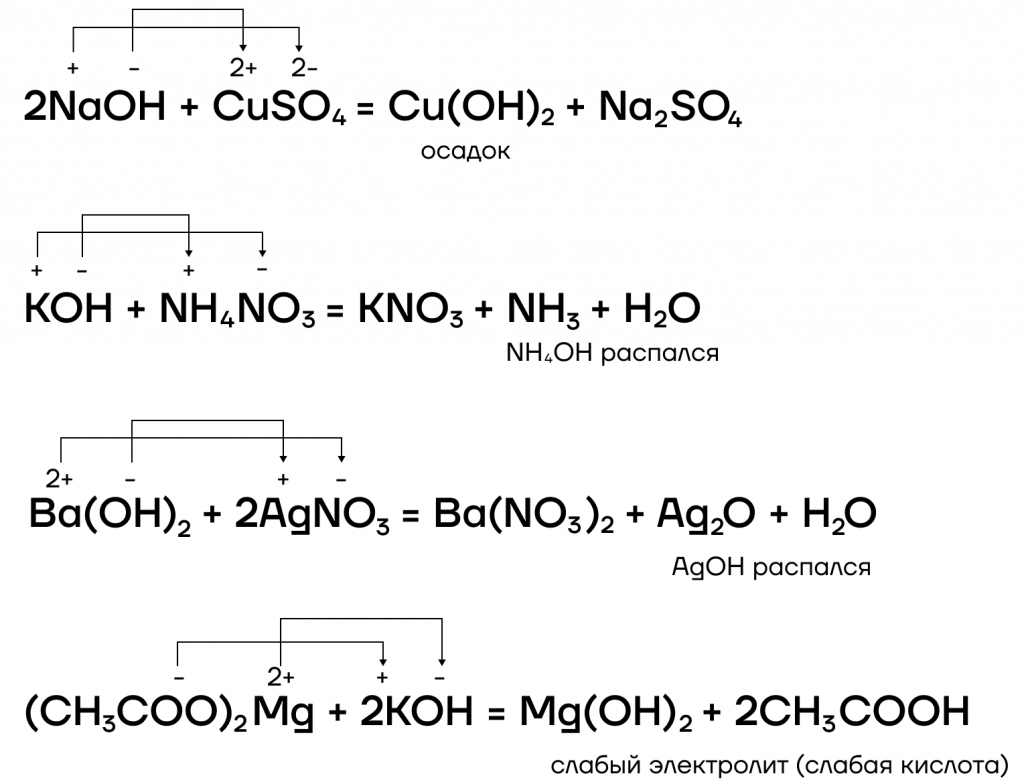
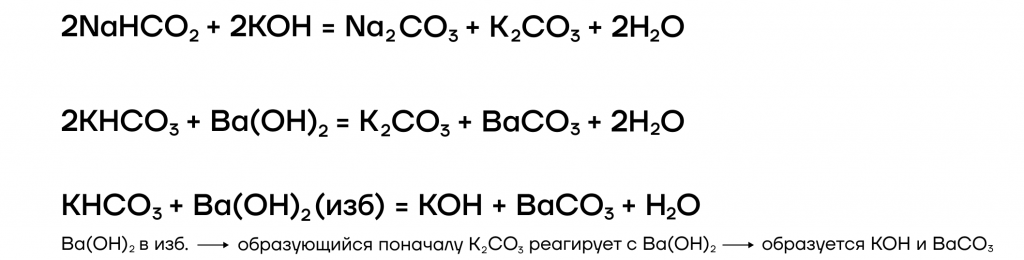
Какие же специфические свойства щелочей существуют? Рассмотрим некоторые из них:
- Окислительно-восстановительные реакции с металлами
Из металлов со щелочами напрямую взаимодействуют только амфотерные бериллий Be, цинк Zn, алюминий Al.
| Эти металлы можно запомнить по аббревиатуре BeZnAl |
А какие соли тогда будут образовываться? В растворе образуются комплексные соли, а в расплаве (t) — средние. В качестве еще одного продукта реакции выделяется газообразный водород.
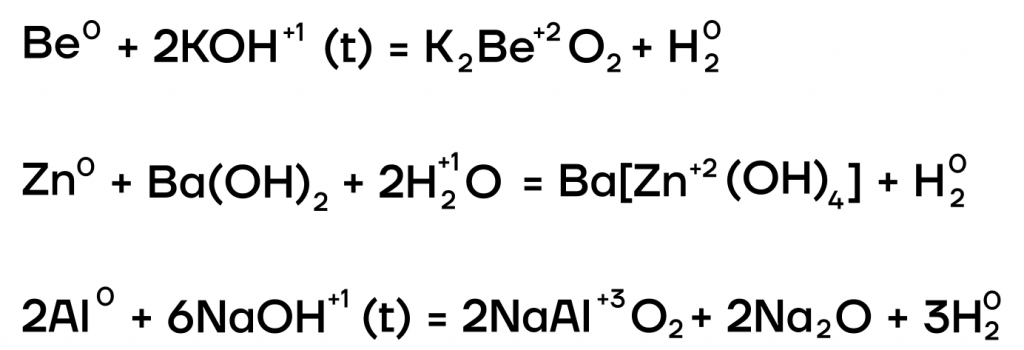
- Окислительно-восстановительные реакции с неметаллами
Неметаллы, которые могут реагировать со щелочами, можно запомнить по «крестообразному» расположению в таблице Менделеева:

Пероксиды щелочных металлов
Что же такое пероксиды? Пероксиды — сложные вещества, которые содержат группу —О—О—, где кислород имеет степень окисления −1.
Фактчек
- Металлы IA группы называются щелочными металлами, которые представлены литием, натрием, калием, рубидием, цезием и францием.
- Постоянная валентность щелочных металлов I, постоянная степень окисления — +1.
- Основной способ получения щелочных металлов — электролиз расплавов солей.
- Щелочные металлы — чрезвычайно активные металлы, могут реагировать с большим рядом простых веществ, с водой.
Проверь себя
Задание 1.
Какой из щелочных металлов имеет самое большое число электронов?
Задание 2.
Щелочные металлы имеют постоянную степень окисления:
Задание 3.
Щелочные металлы образуют с серой соединения, называемые:
- Сульфиты;
- Сульфиды;
- Сульфаты;
- Сульфонаты.
Задание 4.
При реакции калия с кислородом образуется:
- Оксид калия;
- Пероксид калия;
- Супероксид калия;
- Озонид калия
Задание 5.
При внесении солей натрия в пламя оно приобретает окраску:
- Фиолетовую;
- Желтую;
- Небесно-голубую;
- Малиновую
Ответы: 1. — 6; 2. — 1; 3. — 2; 4. — 3; 5. — 2.
Цвет пламени при горении соединений, содержащих металлы - стронций, литий, кальций, натрий, железо, молибден, барий, медь, бор, теллур, таллий, селен, мышьяк, индий, цезий, рубидий, калий, свинец, сурьма, цинк. Цвет пламени спирта.
Цвет пламени при горении соединений, содержащих металлы - стронций, литий, кальций, натрий, железо, молибден, барий, медь, бор, теллур, таллий, селен, мышьяк, индий, цезий, рубидий, калий, свинец, сурьма, цинк. Цвет пламени спирта.
Про спирт: хотя чистый этиловый спирт горит синим пламенем, а метиловый спирт горит зелёным пламенем - технические присадки поменяют цвет в соответствии с таблицей ниже, что не позволяет достоверно отличить метиловый спирт от этилового по цвету пламени, да и остальные способы малонадежны. Не пейте неизвестно какой спирт - вероятность умереть, если это метанол, выше 80%.
| Металл, входящий в соединение | Цвет пламени |  |
| Стронций Sr | Темно-красный | |
| Литий Li | Малиновый | |
| Кальций Ca | Кирпично-красный | |
| Натрий Na | Желтый | |
| Железо Fe | Светло-желтый | |
| Молибден Mb | Желто-зеленоватый | |
| Барий Ba | Желтовато-зеленый | |
| Медь Cu | Ярко-зеленый или сине-зеленый | |
| Бор B | Бледно-зеленый | |
| Теллур Te | Зеленый | |
| Таллий Tl | Изумрудный | |
| Селен Se | Голубой | |
| Мышьяк As | Бледно-синий | |
| Индий in | Сине-фиолетовый | |
| Цезий Cs | Розово-фиолетовый | |
| Рубидий Rb | Красно-фиолетовый | |
| Калий K | Фиолетовый | |
| Свинец Pb | Голубой | |
| Сурьма Sb | Зелено-синий | |
| Цинк Zn | Бледно сине-зеленый |
Дополнительная информация от Инженерного cправочника DPVA, а именно - другие подразделы данного раздела:
Если Вы не обнаружили себя в списке поставщиков, заметили ошибку, или у Вас есть дополнительные численные данные для коллег по теме, сообщите , пожалуйста.
Вложите в письмо ссылку на страницу с ошибкой, пожалуйста.
Опыты: Цветное пламя
Очень красивый научный эксперимент от профессора Николя "Цветное пламя" позволяет получить пламя четырех разных цветов, используя для этого законы химии.

Набор интереснейший, мы действительно на пламя насмотрелись, удивительное зрелище! Интересно всем: и взрослым, и детям, так что очень рекомендую! Плюс в том, что этот опыт с огнём можно провести и дома, не обязательно выходить на улицу. В наборе есть чашки-плошки, в которых горит таблетка сухого горючего, всё безопасно, и на деревянном полу (или столе) можно поставить. Из серии опытов профессора Николя.
Лучше, конечно, под присмотром взрослых опыт проводить. Даже если дети уже немаленькие. Огонь всё же - штука опасная, но при этом . жутко (тут именно это слово подходит очень точно!) интересная!

Фото упаковки набора смотрите в галерее в конце статьи.
Набор 'Цветное пламя' содержит все необходимое для проведения эксперимента. В набор входят:
- иодид калия,
- хлорид кальция,
- раствор соляной кислоты 10%,
- сульфат меди,
- нихромовая проволока,
- медная проволока,
- хлорид натрия,
- сухое горючее, чашка для выпаривания.

Единственное, есть у меня некоторые претензии к производителю - я ожидала найти в коробочке мини-брошюру с описанием химического процесса, который мы здесь наблюдаем, и объяснение, почему пламя становится цветным. Такого описания здесь не оказалось, так что придётся обратиться к энциклопедии по химии (обзор книг по химии здесь). Если, конечно, будет такое желание. А желание у старших детей, конечно, возникает! Младшим детям, конечно, никакие объяснения не нужны: им просто очень интересно смотреть, как меняется цвет пламени.
На обратной стороне коробки-упаковки написано, что нужно делать, чтобы пламя стало цветным. Сначала делали по инструкции, а потом стали просто пламя разными порошками из баночек посыпать (когда убедились, что всё безопасно) - эффект потрясающий. Всполохи красного пламени в жёлтом, ярко-салатовое пламя, зелёное, фиолетовое. зрелище просто завораживает.

Очень здорово покупать на какой-нибудь праздник, это гораздо интереснее любой петарды. И на новый год будет очень здорово. Мы жгли днём, в темноте было бы ещё эффектнее.
Реактивы у нас после сжигания одной таблетки ещё остались, так что, если взять другую таблетку (купить отдельно), можно повторить опыт. Глиняная чашка отмылась довольно хорошо, так что её на много опытов хватит. А если вы на даче, то порошок можно посыпать и на огонь в костре - он тогда, конечно, быстро кончится, но зрелище будет фантастическое!
Добавляю краткую информацию о реактивах, которые идут в комплекте с опытом. Для любознательных детишек, которым интересно узнать больше.
Окрашивание пламени

Стандартный способ окрашивания слабосветящегося газового пламени - введение в него соединений металлов в форме легколетучих солей (обычно, нитратов или хлоридов):
желтое - натрия,
красное - стронция, кальция,
зеленое - цезия (или бора, в виде борноэтилового или борнометилового эфира),
голубое - меди (в виде хлорида).
В синий окрашивает пламя селен, а в сине-зеленый - бор.
Температура внутри пламени различна и с течение времени она меняется (зависит от притока кислорода и горючего вещества). Синий цвет означает что температура очень высокая до 1400 С, желтый - температура чуть меньше, чем когда синее пламя. Цвет пламени может меняться в зависимости от химических примесей.
Цвет пламени определяется только его температурой, если не учитывать его химический (точнее, элементный) состав. Некоторые химические элементы способны окрашивать пламя в характерный для этого элемента цвет.

В лабораторных условиях можно добиться совершенно бесцветного огня, который можно определить лишь по колебанию воздуха в области горения. Бытовой же огонь всегда "цветной". Цвет огня определяется температурой пламени и тем, какие химические вещества в нём сгорают. Высокая температура пламени дает возможность атомам перескакивать на некоторое время в более высокое энергетическое состояние. Когда атомы возвращаются в исходное состояние, они излучают свет с определённой длиной волны. Она соответствует структуре электронных оболочек данного элемента.
Голубой огонек, например, который можно видеть при горении природного газа, обусловлен угарным газом, который и придаёт пламени этот оттенок. Угарный газ, молекула которого состоит из одного атома кислорода и одного атома углерода, является побочным продуктом горения природного газа.
Калий - фиолетовое пламя

Калий (нем. Kalium, франц. и англ. Potassium) — один из важнейших представителей группы щелочных металлов.
Калий — металл наиболее электроположительный после рубидия и цезия. В чистом сухом воздухе при обыкновенной температуре он не изменяется, в обычном — покрывается слоем едкого калия и углекислой его соли; в свежем разрезе в темноте светится, а в тонких пластинках окисляется столь быстро, что может загореться; расплавленный и нагретый, он также горит; пламя его обладает фиолетовым цветом. Вследствие такой склонности к окислению и является необходимым сохранять его под нефтью.
Открывают присутствие калия по фиолетовой окраске газового беcцветного пламени, которая получается при внесении в пламя его соединений, особенно галоидных, на ушке платиновой проволоки (вот почему в опыте нужно вносить калий в пламя на проволоке - эффект изменения цвета пламени тогда заметнее); в присутствии солей натрия окраску наблюдают через синее кобальтовое стекло или через раствор индиго, помещенный в призматический стеклянный сосуд. Спектр пламени характеризуется двумя линиями - красной и фиолетовой.
Кальций хлористый - красное пламя

При нагревании на воздухе или в кислороде кальций воспламеняется и горит красным пламенем с оранжевым оттенком. С менее активными неметаллами (водородом, бором, углеродом, кремнием, азотом, фосфором и другими) кальций вступает во взаимодействие при нагревании.
При внесении в пламя растворимых солей кальция пламя окрашивается в кирпично-красный цвет.
При нагревании в кислороде и на воздухе кальций воспламеняется, сгорая ярко-красным пламенем, при этом образуется основной оксид СаО, который представляет собой белое, весьма огнестойкое вещество, температура плавления которого примерно 2 600 °C. Оксид кальция также известен в технике как негашеная или жженая известь.
Соляная кислота и медь - зелёное пламя
Медь придает пламени зеленый оттенок. При высоком содержании меди в сгораемом веществе пламя имеет яркий зеленый цвет, практически идентичный белому. В зеленый цвет пламя окрашивает борная кислота или медная (латунная) проволока, смоченная в соляной кислоте.
При смачивании соляной кислотой пламя окрашивается в голубой цвет с зеленоватым оттенком.

1) В зеленый цвет пламя окрашивает борная кислота или медная (латунная) проволока, смоченная в соляной кислоте.
2) В красный цвет пламя окрашивает мел, смоченный в той же соляной кислоте.
При сильном прокаливании в тонких осколках Ва-содержащие (Барий-содержащие) минералы окрашивают пламя в желто-зеленый цвет. Окрашивание пламени можно усилить, если после предварительного прокаливания смачивать минерал в крепкой соляной кислоте.
Окислы меди (в опыте для зелёного пламени используются соляная кислота и кристаллики меди) дают изумрудно-зеленое окрашивание. Прокаленные Cu-содержащие соединения, смоченные НС1, окрашивают пламя в лазурно-голубой цвет CuС12). Реакция очень чувствительна.
Зеленый цвет и его оттенки огню придают также барий, молибден, фосфор, сурьма.
Азотнокислый и солянокислый растворы меди имеют голубой или зеленый цвет; при прибавлении аммиака цвет раствора изменяется в темно-синий.
Жёлтое пламя - соль

Для желтого пламени требуется добавка поваренной соли, нитрата натрия или хромата натрия.
Попробуйте посыпать на конфорку газовой плиты с прозрачно-голубым пламенем чуть-чуть поваренныой соли - в пламени появятся жёлтые язычки. Такое жёлто-оранжевое пламя дают соли натрия (а поваренная соль, напомним, это хлорид натрия).
Жёлтый цвет - это цвет натрия в пламени. Натрий есть в любом природном органическом материале, поэтому пламя мы обычно и видим жёлтым. А желтый цвет способен заглушить другие цвета - такова особенность человеческого зрения.
Желтые язычки пламени появляются при распадении солей натрия. Такими солями очень богата древесина, поэтому обычный лесной костер или бытовые спички горят желтым пламенем.
Секреты сумасшедшего профессора Николя
Цветное пламя
Фото упаковки - сбоку. Набор для экспериментов.

Серия химических опытов с профессором Николя.
Цветное пламя - состав набора.

Обратная сторона упаковки - как добиться цветного пламени.
Весь состав набора - чашки (глиняная и стеклянная, потом и для других опытов пригодятся), проволока, реактивы.
Рядом с куклой ростом 18 см для размера.
Химические реактивы для опыта Цветное пламя - на каждой коробочке подписано, что это такое.
Химия пламени

Первые попытки понять механизм горения связаны с именами англичанина Роберта Бойля, француза Антуана Лорана Лавуазье и русского Михаила Васильевича Ломоносова. Оказалось, что при горении вещество никуда не «исчезает», как наивно полагали когда-то, а превращается в другие вещества, в основном газообразные и потому невидимые. Лавуазье в 1774 году впервые показал, что при горении из воздуха уходит примерно пятая его часть. В течение XIX века ученые подробно исследовали физические и химические процессы, сопровождающие горение. Необходимость таких работ была вызвана прежде всего пожарами и взрывами в шахтах.
Но только в последней четверти ХХ века были выявлены основные химические реакции, сопровождающие горение, и по сей день в химии пламени осталось немало темных пятен. Их исследуют самыми современными методами во многих лабораториях. У этих исследований несколько целей. С одной стороны, надо оптимизировать процессы горения в топках ТЭЦ и в цилиндрах двигателей внутреннего сгорания, предотвратить взрывное горение (детонацию) при сжатии в цилиндре автомобиля воздушно-бензиновой смеси. С другой стороны, необходимо уменьшить количество вредных веществ, образующихся в процессе горения, и одновременно — искать более эффективные средства тушения огня.
Существуют два вида пламени. Топливо и окислитель (чаще всего кислород) могут принудительно или самопроизвольно подводиться к зоне горения порознь и смешиваться уже в пламени. А могут смешиваться заранее — такие смеси способны гореть или даже взрываться в отсутствие воздуха, как, например, пороха, пиротехнические смеси для фейерверков, ракетные топлива. Горение может происходить как с участием кислорода, поступающего в зону горения с воздухом, так и при помощи кислорода, заключенного в веществе-окислителе. Одно из таких веществ — бертолетова соль (хлорат калия KClO3); это вещество легко отдает кислород. Сильный окислитель — азотная кислота HNO3: в чистом виде она воспламеняет многие органические вещества. Нитраты, соли азотной кислоты (например, в виде удобрения — калийной или аммиачной селитры), легко воспламеняются, если смешаны с горючими веществами. Еще один мощный окислитель, тетраоксид азота N2O4 — компонент ракетных топлив. Кислород могут заменить и такие сильные окислители, как, например, хлор, в котором горят многие вещества, или фтор. Чистый фтор — один из самых сильных окислителей, в его струе горит вода.
Цепные реакции
Основы теории горения и распространения пламени были заложены в конце 20-х годов прошлого столетия. В результате этих исследований были открыты разветвленные цепные реакции. За это открытие отечественный физикохимик Николай Николаевич Семенов и английский исследователь Сирил Хиншельвуд были в 1956 году удостоены Нобелевской премии по химии. Более простые неразветвленные цепные реакции открыл еще в 1913 году немецкий химик Макс Боденштейн на примере реакции водорода с хлором. Суммарно реакция выражается простым уравнением H2 + Cl2 = 2HCl. На самом деле она идет с участием очень активных осколков молекул — так называемых свободных радикалов. Под действием света в ультрафиолетовой и синей областях спектра или при высокой температуре молекулы хлора распадаются на атомы, которые и начинают длинную (иногда до миллиона звеньев) цепочку превращений; каждое из этих превращений называется элементарной реакцией:
Cl + H2 → HCl + H,
H + Cl2 → HCl + Cl и т. д.
На каждой стадии (звене реакции) происходит исчезновение одного активного центра (атома водорода или хлора) и одновременно появляется новый активный центр, продолжающий цепь. Цепи обрываются, когда встречаются две активные частицы, например Cl + Cl → Cl2. Каждая цепь распространяется очень быстро, поэтому, если генерировать «первоначальные» активные частицы с высокой скоростью, реакция пойдет так быстро, что может привести к взрыву.
Н. Н. Семенов и Хиншельвуд обнаружили, что реакции горения паров фосфора и водорода идут иначе: малейшая искра или открытое пламя могут вызвать взрыв даже при комнатной температуре. Эти реакции — разветвленно-цепные: активные частицы в ходе реакции «размножаются», то есть при исчезновении одной активной частицы появляются две или три. Например, в смеси водорода и кислорода, которая может спокойно храниться сотни лет, если нет внешних воздействий, появление по той или иной причине активных атомов водорода запускает такой процесс:

Возможность взрыва смеси кислорода (или воздуха) со многими горючими газами — водородом, угарным газом, метаном, ацетиленом — зависит от условий, в основном от температуры, состава и давления смеси. Так, если в результате утечки бытового газа на кухне (он состоит в основном из метана) его содержание в воздухе превысит 5%, то смесь взорвется от пламени спички или зажигалки и даже от маленькой искры, проскочившей в выключателе при зажигании света. Взрыва не будет, если цепи обрываются быстрее, чем успевают разветвляться. Именно поэтому была безопасной лампа для шахтеров, которую английский химик Хэмфри Дэви разработал в 1816 году, ничего не зная о химии пламени. В этой лампе открытый огонь был отгорожен от внешней атмосферы (которая могла оказаться взрывоопасной) частой металлической сеткой. На поверхности металла активные частицы эффективно исчезают, превращаясь в стабильные молекулы, и потому не могут проникнуть во внешнюю среду.
Полный механизм разветвленно-цепных реакций очень сложен и может включать более сотни элементарных реакций. К разветвленно-цепным относятся многие реакции окисления и горения неорганических и органических соединений. Таковой же будет и реакция деления ядер тяжелых элементов, например плутония или урана, под воздействием нейтронов, которые выступают аналогами активных частиц в химических реакциях. Проникая в ядро тяжелого элемента, нейтроны вызывают его деление, что сопровождается выделением очень большой энергии; одновременно из ядра вылетают новые нейтроны, которые вызывают деление соседних ядер. Химические и ядерные разветвленно-цепные процессы описываются сходными математическими моделями.
Что надо для начала
Чтобы началось горение, нужно выполнить ряд условий. Прежде всего, температура горючего вещества должна превышать некое предельное значение, которое называется температурой воспламенения. Знаменитый роман Рэя Брэдбери «451 градус по Фаренгейту» назван так потому, что примерно при этой температуре (233°C) загорается бумага. Это «температура воспламенения», выше которой твердое топливо выделяет горючие пары или газообразные продукты разложения в количестве, достаточном для их устойчивого горения. Примерно такая же температура воспламенения и у сухой сосновой древесины.

Самодельные зажигалки времен Великой Отечественной (Одна сделана из патрона от авиационной пушки). Изображение: «Химия и жизнь»
Температура пламени зависит от природы горючего вещества и от условий горения. Так, температура в пламени метана на воздухе достигает 1900°C, а при горении в кислороде — 2700°C. Еще более горячее пламя дают при сгорании в чистом кислороде водород (2800°C) и ацетилен (3000°C). Недаром пламя ацетиленовой горелки легко режет почти любой металл. Самую же высокую температуру, около 5000°C (она зафиксирована в Книге рекордов Гиннесса), дает при сгорании в кислороде легкокипящая жидкость — субнитрид углерода С4N2 (это вещество имеет строение дицианоацетилена NC–C=C–CN). А по некоторым сведениям, при горении его в атмосфере озона температура может доходить до 5700°C. Если же эту жидкость поджечь на воздухе, она сгорит красным коптящим пламенем с зелено-фиолетовой каймой. С другой стороны, известны и холодные пламена. Так, например, горят при низких давлениях пары фосфора. Сравнительно холодное пламя получается и при окислении в определенных условиях сероуглерода и легких углеводородов; например, пропан дает холодное пламя при пониженном давлении и температуре от 260–320°C.
Только в последней четверти ХХ века стал проясняться механизм процессов, происходящих в пламени многих горючих веществ. Механизм этот очень сложен. Исходные молекулы обычно слишком велики, чтобы, реагируя с кислородом, непосредственно превратиться в продукты реакции. Так, например, горение октана, одного из компонентов бензина, выражается уравнением 2С8Н18 + 25О2 = 16СО2 + 18Н2О. Однако все 8 атомов углерода и 18 атомов водорода в молекуле октана никак не могут одновременно соединиться с 50 атомами кислорода: для этого должно разорваться множество химических связей и образоваться множество новых. Реакция горения происходит многостадийно — так, чтобы на каждой стадии разрывалось и образовывалось лишь небольшое число химических связей, и процесс состоит из множества последовательно протекающих элементарных реакций, совокупность которых и представляется наблюдателю как пламя. Изучать элементарные реакции сложно прежде всего потому, что концентрации реакционно-способных промежуточных частиц в пламени крайне малы.
Внутри пламени
Оптическое зондирование разных участков пламени с помощью лазеров позволило установить качественный и количественный состав присутствующих там активных частиц — осколков молекул горючего вещества. Оказалось, что даже в простой с виду реакции горения водорода в кислороде 2Н2 + О2 = 2Н2О происходит более 20 элементарных реакций с участием молекул О2, Н2, О3, Н2О2, Н2О, активных частиц Н, О, ОН, НО2. Вот, например, что написал об этой реакции английский химик Кеннет Бэйли в 1937 году: «Уравнение реакции соединения водорода с кислородом — первое уравнение, с которым знакомится большинство начинающих изучать химию. Реакция эта кажется им очень простой. Но даже профессиональные химики бывают несколько поражены, увидев книгу в сотню страниц под названием «Реакция кислорода с водородом», опубликованную Хиншельвудом и Уильямсоном в 1934 году». К этому можно добавить, что в 1948 году была опубликована значительно большая по объему монография А. Б. Налбандяна и В. В. Воеводского под названием «Механизм окисления и горения водорода».
Современные методы исследования позволили изучить отдельные стадии подобных процессов, измерить скорость, с которой различные активные частицы реагируют друг с другом и со стабильными молекулами при разных температурах. Зная механизм отдельных стадий процесса, можно «собрать» и весь процесс, то есть смоделировать пламя. Сложность такого моделирования заключается не только в изучении всего комплекса элементарных химических реакций, но и в необходимости учитывать процессы диффузии частиц, теплопереноса и конвекционных потоков в пламени (именно последние устраивают завораживающую игру языков горящего костра).
Откуда все берется
Основное топливо современной промышленности — углеводороды, начиная от простейшего, метана, и кончая тяжелыми углеводородами, которые содержатся в мазуте. Пламя даже простейшего углеводорода — метана может включать до ста элементарных реакций. При этом далеко не все из них изучены достаточно подробно. Когда горят тяжелые углеводороды, например те, что содержатся в парафине, их молекулы не могут достичь зоны горения, оставаясь целыми. Еще на подходе к пламени они из-за высокой температуры расщепляются на осколки. При этом от молекул обычно отщепляются группы, содержащие два атома углерода, например С8Н18 → С2Н5 + С6Н13. Активные частицы с нечетным числом атомов углерода могут отщеплять атомы водорода, образуя соединения с двойными С=С и тройными С≡С связями. Было обнаружено, что в пламени такие соединения могут вступать в реакции, которые не были ранее известны химикам, поскольку вне пламени они не идут, например С2Н2 + О → СН2 + СО, СН2 + О2 → СО2 + Н + Н.
Постепенная потеря водорода исходными молекулами приводит к увеличению в них доли углерода, пока не образуются частицы С2Н2, С2Н, С2. Зона сине-голубого пламени обусловлена свечением в этой зоне возбужденных частиц С2 и СН. Если доступ кислорода в зону горения ограничен, то эти частицы не окисляются, а собираются в агрегаты — полимеризуются по схеме С2Н + С2Н2 → С4Н2 + Н, С2Н + С4Н2 → С6Н2 + Н и т. д.
В результате образуются частицы сажи, состоящие почти исключительно из атомов углерода. Они имеют форму крошечных шариков диаметром до 0,1 микрометра, которые содержат примерно миллион атомов углерода. Такие частицы при высокой температуре дают хорошо светящееся пламя желтого цвета. В верхней части пламени свечи эти частицы сгорают, поэтому свеча не дымит. Если же происходит дальнейшее слипание этих аэрозольных частиц, то образуются более крупные частицы сажи. В результате пламя (например, горящей резины) дает черный дым. Такой дым появляется, если в исходном топливе повышена доля углерода относительно водорода. Примером могут служить скипидар — смесь углеводородов состава С10Н16 (CnH2n–4), бензол С6Н6 (CnH2n–6), другие горючие жидкости с недостатком водорода — все они при горении коптят. Коптящее и ярко светящее пламя дает горящий на воздухе ацетилен С2Н2 (CnH2n–2); когда-то такое пламя использовали в ацетиленовых фонарях, установленных на велосипедах и автомобилях, в шахтерских лампах. И наоборот: углеводороды с высоким содержанием водорода — метан СН4, этан С2Н6, пропан С3Н8, бутан С4Н10 (общая формула CnH2n+2) — горят при достаточном доступе воздуха почти бесцветным пламенем. Смесь пропана и бутана в виде жидкости под небольшим давлением находится в зажигалках, а также в баллонах, которые используют дачники и туристы; такие же баллоны установлены в автомобилях, работающих на газе. Сравнительно недавно было обнаружено, что в копоти часто присутствуют шарообразные молекулы, состоящие из 60 атомов углерода; их назвали фуллеренами, а открытие этой новой формы углерода было ознаменовано присуждением в 1996 году Нобелевской премии по химии.
К щелочным металлам относят химические элементы: одновалентные металлы, составляющие Ia группу: литий, натрий, калий, рубидий, цезий и франций.
Эти металлы очень активны, быстро окисляются на воздухе и бурно реагируют с водой. Их хранят под слоем керосина из-за их сильной реакционной способности.

Общая характеристика
От Li к Fr (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств, реакционной способности. Уменьшается электроотрицательность, энергия ионизации, сродство к электрону.

- Li - 2s 1
- Na - 3s 1
- K - 4s 1
- Rb - 5s 1
- Cs - 6s 1
- Fr - 7s 1
Природные соединения
- NaCl - галит (каменная соль)
- KCl - сильвин
- NaCl*KCl - сильвинит

Получение
Получить такие активные металлы электролизом водного раствора - невозможно. Для их получения применяют электролиз расплавов при высоких температурах (естественно - безводных):
NaCl → Na + Cl2↑ (электролиз расплава каменной соли)
Химические свойства
Одной из особенностей щелочных металлов является их реакция с кислородом. Литий в такой реакции преимущественно образует оксид, натрий - пероксид, калий, рубидий и цезий - супероксиды.
K + O2 → KO2 (супероксид калия)
Помните, что металлы никогда не принимают отрицательных степеней окисления. Щелочные металлы одновалентны, и проявляют постоянную степень окисления +1 в различных соединениях: гидриды, галогениды (фториды, хлориды, бромиды и йодиды), нитриды, сульфиды и т.д.
Li + H2 → LiH (в гидридах водород -1)
Na + F2 → NaF (в фторидах фтор -1)
Na + S → Na2S (в сульфидах сера -2)
K + N2 → K3N (в нитридах азот -3)
Щелочные металлы бурно взаимодействуют с водой, при этом часто происходит воспламенение, а иногда - взрыв.
Na + H2O → NaOH + H2↑ (воду можно представить в виде HOH - натрий вытесняет водород)
Иногда в задачах может проскользнуть фраза такого плана: ". в ходе реакции выделился металл, окрашивающий пламя горелки в желтый цвет". Тут вы сразу должны догадаться: речь, скорее всего, про натрий.
Щелочные металлы по-разному окрашивают пламя. Литий окрашивает в алый цвет, натрий - в желтый, калий - в фиолетовый, рубидий - синевато-красный, цезий - синий.

Оксиды щелочных металлов
Имеют общую формулу R2O, например: Na2O, K2O.
Получение оксидов щелочных металлов возможно в ходе реакции с кислородом. Для лития все совсем несложно:
В подобных реакциях у натрия и калия получается соответственно пероксид и супероксид, что приводит к затруднениям. Как из пероксида, так и из супероксида, при желании можно получить оксид:
По свойствам эти оксиды являются основными. Они хорошо реагируют c водой, кислотными оксидами и кислотами:
Li2O + H2O → LiOH (осн. оксид + вода = основание - реакция идет, только если основание растворимо)
Na2O + SO2 → Na2SO3 (обратите внимание - мы сохраняем СО серы +4)
Гидроксиды щелочных металлов
Относятся к щелочам - растворимым основаниям. Наиболее известные представители: NaOH - едкий натр, KOH - едкое кали.
Гидроксиды щелочных металлов получаются в ходе электролиза водных растворов их солей, в реакциях обмена, в реакции щелочных металлов и их оксидов с водой:
KCl + H2O → (электролиз!) KOH + H2 + Cl2 (на катоде выделяется водород, на аноде - хлор)

Проявляют основные свойства. Хорошо реагируют с кислотами, кислотными оксидами и солями, если в ходе реакции выпадает осадок, выделяется газ или образуется слабый электролит (вода).
LiOH + H2SO4 → LiHSO4 + H2O (соотношение 1:1, кислота в избытке - получается кислая соль)
2LiOH + H2SO4 → Li2SO4 + 2H2O (соотношение 2:1, основание в избытке - получается средняя соль)
KOH + SO2 → KHSO3 (соотношение 1:1 - получается кислая соль)
2KOH + SO2 → K2SO3 + H2O (соотношение 2:1 - получается средняя соль)
С амфотерными гидроксидами реакции протекают с образованием комплексных солей (в водном растворе) или с образованием окиселов - смешанных оксидов (при высоких температурах - прокаливании).
NaOH + Al(OH)3 → Na[Al(OH)4] (в водном растворе образуются комплексные соли)
NaOH + Al(OH)3 → NaAlO2 + H2O (при прокаливании образуется окисел - смесь двух оксидов: Al2O3 и Na2O, вода испаряется)
Реакции щелочей с галогенами заслуживают особого внимания. Без нагревания они идут по одной схеме, а при нагревании эта схема меняется:
NaOH + Cl2 → NaClO + NaCl + H2O (без нагревания хлор переходит в СО +1 и -1)
NaOH + Cl2 → NaClO3 + NaCl + H2O (с нагреванием хлор переходит в СО +5 и -1)
В реакциях щелочей с йодом образуется исключительно иодат, так как гипоиодит неустойчив даже при комнатной температуре, не говоря о нагревании. С серой реакция протекает схожим образом:
NaOH + I2 → NaIO3 + NaI + H2O (с нагреванием)

NaOH + S → Na2S + Na2SO3 + H2O (сера переходит в СО -2 и +4)
Уникальным является также взаимодействие щелочей с кислотным оксидом NO2, который соответствует сразу двум кислотам - и азотной, и азотистой.
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Читайте также:
