Алюминий и сталь коррозия
Обновлено: 24.04.2024
Стандарт EN 1999, который еще называют «Еврокод 9», применяется в странах Европейского Союза при проектировании конструкций из алюминиевых сплавов для зданий и гражданских сооружений. Этот стандарт соответствует принципам и требованиям по безопасности и эксплуатационной пригодности конструкций, исходным данным для их проектирования и проверкам, которые указаны в более общем строительном стандарте EN 1990 — Основы проектирования строительных конструкций.
Стандарт EN 1999-1-1 – первая часть стандарта EN 1999 – определяет основные правила для проектирования конструкций из деформируемых алюминиевых сплавов, а также, в ограниченном объеме, по применению в строительстве алюминиевых отливок.
Ниже представлен обзор рекомендаций Еврокода 9 по защите алюминиевых строительных конструкций от коррозии, которая возникает в соединениях алюминия с другими металлами: щелевой и гальванической. В строительстве такими «металлами» являются в основном:
- различные сплавы самого алюминия,
- оцинкованная сталь,
- окрашенная сталь и
- нержавеющая сталь.
Коррозия алюминия в соединениях
При проектировании алюминиевых строительных конструкций необходимо отдельно рассматривать вопросы коррозии алюминия в следующих условиях:
- все контакты алюминия в соединениях с различными материалами с образованием щелей для предотвращения щелевой коррозии;
- все контакты алюминия в соединениях с металлическими материалами или с металлическими шайбами, в результате которых между ними может происходить электрохимическое взаимодействие – гальваническая коррозия.
Защита контактов от щелевой и гальванической коррозии
Контактные поверхности и соединения алюминия с алюминием или с другими металлами требуют дополнительной защиты от коррозии в дополнение к общей защите алюминиевых конструкций от коррозии. Степень общей защиты алюминиевых конструкций от коррозии зависит от климатических условий их эксплуатации. Это относится также к контактным поверхностям в соединениях, выполненных на болтах, заклепках, сварке и с использованием высокопрочных фрикционных болтовых зажимах.
Рекомендации по такой дополнительной защите от щелевой и гальванической коррозии в алюминиевых строительных конструкциях в различных климатических условиях эксплуатации изложены ниже в таблицах 1-3:
- таблица 1 – для не морской атмосферы различной загрязненности;
- таблица 2 – для морской атмосферы различной загрязненности и
- таблица 3 – для конструкций, которые работают в условиях погружения в воду, пресную или морскую.
Если осуществляется сборка строительных компонентов, которые были подвергнуты предварительному окрашиванию или защите от коррозии, то в строительной технической документации необходимо предусмотреть дополнительную изоляцию для контактирующих поверхностей, включая тип и процедуру такой изоляции. Эти меры должны учитывать предполагаемый срок эксплуатации алюминиевой конструкции, воздействие внешних факторов и степень защиты таких предварительно защищенных компонентов.
Защита от коррозии соединений в конструкциях
Поверхность соединений
Метод 0
Обычно нет необходимости в какой-либо обработке для защиты от коррозии.
Метод 0/Х
Необходимость обработки для защиты от коррозии зависит от особенностей конструкции. Небольшие контактирующие поверхности, а также поверхности, которые быстро и естественным образом высыхают от влаги можно монтировать без какой-либо герметизации (см. метод Х)
Метод Х
Обе контактирующие поверхности должны быть собраны таким образом, чтобы не оставалось щелей, в которые может проникнуть вода. Обе контактирующие поверхности, включая отверстия под болты и заклепки, перед монтажом конструкции должны быть очищены, предварительно обработаны и на них должен быть нанесен один слой грунтовки, как это указано в EN 1090-3, или герметик, так чтобы он выступал за пределы контактирующей поверхности. Поверхности должны быть соединены вместе, пока слой грунтовки еще влажный.
Если собираются предварительно окрашенные или компоненты с защитой от коррозии, то герметизация контактирующих поверхностей может быть необязательной, в зависимости от состава краски или примененного способа защиты от коррозии, а также предполагаемого срока эксплуатации конструкции и особенностей окружающей среды.
Метод Y
Полная электрическая изоляция между двумя металлами и всеми крепежными деталями. Обеспечивается за счет установки неабсорбирующих и неэлектропроводящих пленок, шайб и прокладок, чтобы предотвратить металлический контакт между материалами. Может потребоваться применение дополнительного покрытия или герметиков.
Метод Z
Если требуется применение метода Y, а нагрузка передается через точечный контакт, и это препятствует применению изолирующих материалов, то соединение должно быть собрано без использования изолирующих материалов, но с выполнением полной внешней изоляции всего сборочного узла, чтобы предотвратить проникновение влаги к элементам соединения. Способы такой изоляции должны быть установлены по согласованию между заинтересованными сторонами.
Болты и заклепки
Как правило, никакой дополнительной обработки не требуется.
Метод 1
Между головками болтов, гайками, шайбами и соединяемыми материалами должны быть установлены прокладки из инертного материала или герметики, чтобы герметизировать соединение и предотвратить попадание влаги на поверхность контакта между строительными компонентами и крепежными деталями.
Необходимо принять меры для того, чтобы применяемые прокладки и герметики в соединении не оказывали отрицательного влияния на передачу нагрузки через это соединение.
Метод 2
- (1) В случае, если поверхности соединения не имеют слоя краски или другого покрытия, то головки болтов, гайки и заклепки, а также близлежащие участки соединяемых материалов, должны быть защищены, по крайней мере, одним слоем грунтовки (см. EN 1090-3). Особое внимание следует уделить герметизации всех щелей.
- (2) В случае применения оцинкованных болтов, защита соединения со стороны алюминия не требуется.
- (3) В случае применения алюминиевых болтов или заклепок, защита соединения со стороны алюминия не требуется.
- (4) В случае применения болтов из нержавеющей стали для соединения алюминиевых или оцинкованных стальных деталей, близлежащая оцинкованная область соединения должна иметь аналогичную защиту (т. е. защищена хотя бы одним слоем грунтовки).
Дополнительная защита от коррозии
Процедура а
В тех случаях, когда в области соединения может скапливаться грязь или удерживаться влага, а прилегающие к соединению металлические детали не были окрашены по каким-либо причинам, то может потребоваться их защита с помощью подходящего лакокрасочного покрытия
Процедура z
Может потребоваться дополнительная защита оцинкованных строительных деталей в целом.
Защита контактов “металл-металл” от щелевой и гальванической коррозии
Обозначения в таблицах 1-3:
- M – металл (metal), В – болт (bolt), R – заклепка (rivet)
- Методы защиты от коррозии металлов 0, 0/Х, Х, Y и Z – см. раздел 4.1
- Методы защиты болтов и заклепок 0, 1 и 2 – см. раздел 4.2
- Дополнительные методы защиты a и z – см. раздел 4.3
- При назначении методов защиты в скобках ( ) необходимо принять во внимание особые условия для общей коррозионной защиты (см. Общая защита от коррозии алюминиевых конструкций, раздел 5)
Щелевая и гальваническая коррозия в обычной атмосфере

Таблица 1 – Методы защиты соединений металл-металл от щелевой и гальванической коррозии в условиях обычной (не морской) атмосферы – сельской и промышленной
Щелевая и гальваническая коррозия в морской атмосфере

Таблица 2 – Методы защиты соединений металл-металл от щелевой и гальванической коррозии в условиях морской атмосферы – сельской и промышленной
Щелевая и гальваническая коррозии в воде – пресной и морской

Таблица 3 – Методы защиты соединений металл-металл от щелевой и гальванической коррозии в условиях эксплуатации в воде – пресной и морской
Совместимость металлов или как избежать гальванической коррозии?

Контактная коррозия происходит при непосредственном контакте двух разнородных металлов. Нельзя, к примеру, соединять алюминиевые листы медной заклепкой, так как при определенных условиях они образуют сильную гальваническую пару.
Разные металлы имеют разные электродные потенциалы. В присутствии электролита один из них играет роль катода, а другой анода. В результате химической реакции, протекающей между ними, начнется коррозионный процесс, в котором медь (катод) будет беспощадно разрушать алюминий (анод).
Почти все пары разнородных металлов, находящиеся в контакте между собой, подвержены коррозии, так как даже влага из воздуха может выступить в роли электролита и активировать их электродный потенциал. Но одни пары уязвимы в большей степени, а другие – в меньшей.
Например, алюминий отлично контактирует с оцинкованной сталью, хромом и цинком, а латунь совершенно не «дружит» со сталью, алюминием и цинком. Чтобы узнать, какие металлы совместимы, а какие нет, обратимся к основам химии.
В ряду электрохимической активности металлы стоят в следующей последовательности:

Электрохимический ряд напряжения металлов
Для примера рассмотрим пару алюминий – медь. Алюминий стоит в ряду слева от водорода и имеет электроотрицательный потенциал равный -1.7В, а медь находится справа и имеет положительный потенциал +0.4В. Большая разница потенциалов приводит к разрушению более активного алюминия. Медь сильнее всех, впереди стоящих элементов, поэтому в паре с любым из них она выйдет победителем. Чем дальше друг от друга в ряду стоят элементы, тем выше их несовместимость и вероятность протекания гальванической коррозии.
Данные о совместимости некоторых металлов представлены в таблице:
| Алюминий | Латунь | Бронза | Медь | Оцинкованная сталь | Железо | Свинец | Нержавеющая сталь | Цинк | |
| Алюминий | Д | Н | Н | Н | Д | О | О | Д | Д |
| Медь | Н | О | О | Д | О | Н | О | Н | Н |
| Оцинкованная сталь | Д | О | О | О | Д | О | Д | О | Д |
| Свинец | О | О | О | О | Д | Д | Д | О | Д |
| Нержавеющая сталь | Д | Н | Н | Н | О | О | О | Д | Н |
| Цинк | Д | Н | Н | Н | Д | Н | Д | Н | Д |
Д – абсолютно допустимые контакты (низкий риск ГК);
О – ограничено допустимые контакты (средний риск ГК);
Н – недопустимые контакты (высокий риск ГК).
Приведенная таблица может служить кратким справочником для определения совместимости некоторых конструкционных металлов. Допустимость и недопустимость контактов разнородных в электрохимическом отношении металлов устанавливает ГОСТ 9.005-72.
Пример недопустимых гальванических пар:

Гальваническое действие может возникнуть, если строительную конструкцию из нержавеющей стали скреплять оцинкованными болтами. В этой нежелательной паре пострадает высоко анодный крепеж, поскольку его электроны будут перемещаться в направлении катодной нержавеющей стали. Поэтому, крепежные детали должны быть изготовлены из менее гальванически активного металла, чем материал металлоконструкции.

На скорость течения гальванокоррозии оказывает влияние площадь поверхности анода и катода. Если большой по размеру анод соединить с маленьким катодом, то анод будет ржаветь медленно, а если сделать наоборот, то быстро. Например, используйте болты из нержавеющей стали для крепления алюминия, но не наоборот.
Степень интенсивности протекания контактной коррозии зависит и от условий эксплуатации соединения. В обычных атмосферных условиях процесс будет протекать менее быстро и возрастает в агрессивной электропроводной среде, например, растворах кислот и щелочей. Присутствие в воде других веществ увеличивает проводимость электролита и скорость коррозии. Поэтому при проектировании конструкций важна оценка окружающей среды.
Как защитить конструкцию или узел от контактной коррозии?
Если по конструктивным соображениям невозможно избежать нежелательного контакта разнородных металлов, то можно попытаться уменьшить гальваническую коррозию с помощью следующих методов:
- окраска поверхностей в районе их стыка;
- нанесение совместимых металлических покрытий;
- изоляция соединения от внешней среды;
- электрическая изоляция;
- установка неметаллических прокладок, вставок, шайб в болтовых соединениях.
Практика показывает, что в тех случаях, когда пренебрегают требованиями к допустимости контактов разных металлов, приходится дорого за это расплачиваться. Неправильная компоновка контактных пар выводит из строя узлы крепления, металлоконструкции и может стоять человеческой жизни.
Сталь и алюминий защитим, оцинковку вылечим

Те, кто следит за нашими антикоррозионными публикациями, хорошо знают препарат Dinitrol 479. Когда-то мы с компанией ЮВК назвали его «три в одном»: он и днище от коррозии защищает, и арки колесные от гравия оберегает, и дорожный шум в салоне уменьшает.
Потом слоган «Dinitrol 479 – три в одном» стал интернет-мемом и разошелся по множеству сайтов. Как водится, без всяких ссылок на «АБС-авто» и ЮВК. Пусть это останется на совести копипастеров, тем более что воровать сегодня модно, а работать они не умеют.
Итак, «три в одном». Иными словами, Dinitrol 479 совмещает функции классического антикоррозионного материала для днища, антигравийного покрытия и шумоизоляции. Однако его назначение производитель формулирует иначе: «шумоизоляционный материал с антикорозионными и антигравийными свойствами».
Но прогресс не стоит на месте. Сегодня у знаменитого 479-го появилось альтернативное решение – препарат Dinitrol 650 BD.
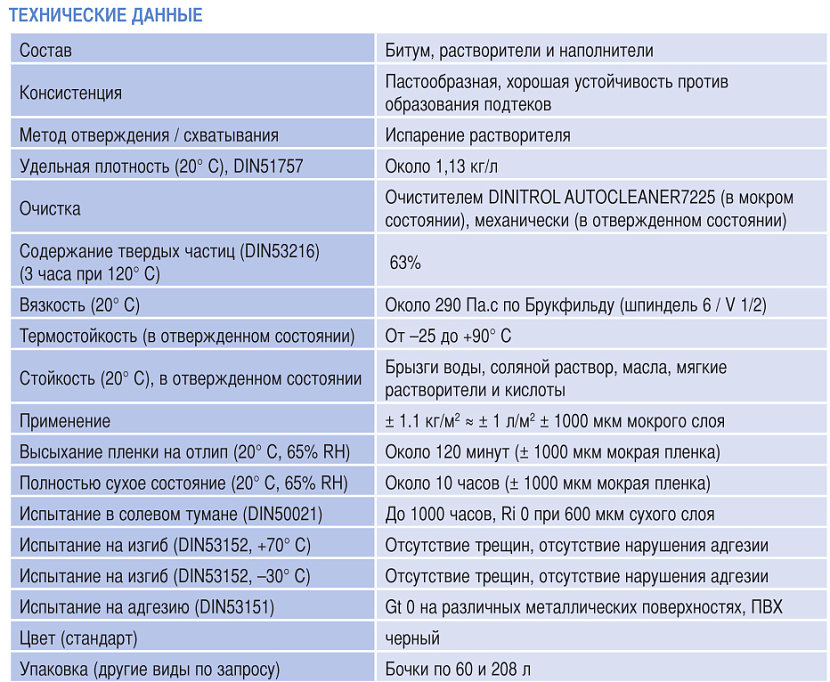
Это состав черного цвета, износостойкий и прочный. Создан на основе битума, содержит специальные наполнители и минимум мягкого растворителя, что вызвано экологическими требованиями. Поэтому материал безопасен для здоровья и не вредит лакокрасочному покрытию кузова, а также пластиковым и резиновым деталям – здесь все как у предшественника Dinitrol 479.
И разумеется, Dinitrol 650 BD не боится холода и жары – температурный диапазон, в котором твердая пленка сохраняет эксплуатационные характеристики, составляет от –25 до +90° C. А при нанесении материал не стекает с вертикальной поверхности благодаря тиксотропности.
А в чем же отличие, спросите вы? Все перечисленное мы уже видели у 479-го… А вот в чем.
Первое. Dinitrol 650 BD можно наносить на поверхность, загрунтованную жидким антикором Dinitrol ML. Такое грунтование необходимо, когда днище или арка поражены коррозией. Dinitrol ML пропитывает ржавчину и останавливает процесс разрушения стали благодаря эффективным ингибиторам коррозии.
Так вот, новый состав Dinitrol 650 BD, нанесенный через 2–4 часа после ML-препарата, обеспечивает отличную адгезию к металлу. И тут же включает в работу собственные ингибиторы.
Второе. Новый материал можно наносить профессиональным оборудованием безвоздушным способом. Применяемые насосы – 26:1 или 65:1, сопло 0,018 дюйма. Материал может наноситься толстыми слоями, а оптимальное расстояние при распылении составляет примерно 30 см.
Преимущества такого способа очевидны: экономичный расход препарата и чистота антикоррозионного участка. Ведь воздушное распыление неизбежно выбрасывает часть материала в окружающую среду в виде тумана.
Пример обработки колесных арок Toyota Yaris 2007 г. в. Слева – незащищенная арка. Поверхность необходимо загруновать жидким антикоррозионным препаратом типа Dinitrol ML. А потом нанести слой Dinitrol 650 BD. Результат показан на правой фотографии Пример обработки днища Toyota Yaris 2007 г. в. Поверхность со следами ржавчины следует загруновать жидким антикоррозионным препаратом типа Dinitrol ML. А потом нанести слой Dinitrol 650 BD – все, как в случае с арками. Результат показан справа
В итоге мы получаем прочную пленку, защищающую от коррозии, летящего дорожного гравия и соли, а также снижающую шум. Таким образом, автомобиль становится более комфортным, а путешествие на нем – более приятным.
Завершим эту главу формальным перечислением областей, где можно применять Dinitrol 650 BD. Это шасси, днище и колесные арки легковых и коммерческих автомобилей, а также автобусов. Защищать эти транспортные средства можно всегда и везде: в процессе производства, при эксплуатации и обслуживании в автопарках и на СТОА, в гаражах и частных мастерских.
А производитель Dinitrol 650 BD указывает и другие отрасли – например, судостроение. И хотя это не наша тема, все равно интересно – как покажет себя новый материал в морской воде? Наверное, не подведет.
Спасти алюминий
Современное автомобилестроение немыслимо без использования алюминиевых материалов. Далее мы будем использовать термин «алюминий», подразумевая не чистый металл, а конструкционные сплавы на его основе.
Первые автомобили Land Rover имели алюминиевые кузова, а множество Defender со стальной рамой и алюминиевыми панелями и сейчас колесит по дорогам всего мира. Многие модели Audi, Jaguar, Volvo, BMW, пикапы Mazda и других авто имеют детали из алюминия. И уж конечно, системы охлаждения двигателя и кондиционирования без алюминия немыслимы.
«Алюминий не ржавеет» – эту фразу мы помним со школы. А еще нам говорили, что на воздухе изделия из алюминиевых сплавов самопроизвольно покрываются тончайшей оксидной пленкой Al2O3 – она-то и предохраняет их от дальнейших коррозионных атак. Поэтому хозяйки пользуются алюминиевой посудой десятилетиями.

Авиационные материалы для защиты алюминиевых деталей, прототипы Dinitrol 713 IQ
Все верно. Но в машиностроении картина гораздо сложнее. Вибрации, перепады температур, влажная и химически агрессивная среда (вспомним хотя бы солевые растворы на дорогах) – эти и другие факторы повреждают «природную» защитную пленку и препятствуют ее восстановлению.
В местах контакта алюминиевого сплава со сталью (а в большинстве конструкций это неизбежно) возникают гальванические пары. Поскольку алюминий более активный металл, чем железо, электрохимическая коррозия разъедает именно его. Так что алюминиевая трубка со стальным штуцером не такая уж безобидная вещь. Гальванические пары образуются и в зонах сварных швов. А вслед за электрохимической коррозией приходит межкристаллитная, разрушающая границы зерен металла.

Dinitrol 713 IQ создает легкую прозрачную пленку толщиной всего 15 мкм, которая прекрасно пропускает тепло, не снижая эффективности теплообменника
Главная опасность межкристаллитной коррозии в том, что она существенно снижает прочность и другие механические характеристики изделия при неизменном внешнем виде. А нагрузи деталь чуть сильнее – рассыплется в порошок.
К сожалению, в данном случае практика подтверждает теорию. Ежегодно дилерские сервисы меняют множество теплообменников, изготовленных из «крылатого металла».
Препараты для защиты авиационных сплавов маркируются индексом AV, например, AV‑15. В Швеции их применяли для антикоррозионной защиты радиаторов автомобилей Mercedes. Так сугубо авиационный состав приобрел автомобильный опыт. Защита оказалась настолько эффективной, что на основе AV‑15 был создан препарат Dinitrol 713 IQ – специальный антикор для автомобильных узлов и деталей из алюминия. Впрочем, он умеет защищать и медь, и бронзу, и латунь, и нержавеющую сталь, которая на самом деле тоже не вечна.
«Семьсот тринадцатый» перенял все достоинства «летающего брата» AV‑15, а именно:
– уникальную способность беречь алюминиевые сплавы (авиация!), что достигается за счет особых ингибиторов;
– создавать на поверхности очень легкую (снова авиация!) и тонкую прозрачную пленку – ее толщина всего 15 мкм, и, кстати, она прекрасно пропускает тепло, не снижая эффективности защищаемого теплообменника;
– технологичность нанесения (опять же авиация!).
Говоря о технологичности, подчеркнем, что материал Dinitrol 713 IQ – так называемый одношаговый, не требующий предварительного грунтования. Он «сам себе режиссер»: проникает во все щели и прочие труднодоступные участки конструкции и обеспечивает собственную адгезию. Наносится с помощью кисти, распылением из пистолета или же окунанием.
При необходимости ремонта системы кондиционирования пленка Dinitrol 713 IQ смывается горячей водой под давлением – для этого достаточно обычного моечного аппарата. А при эксплуатации автомобиля защитную пленку рекомендуется регулярно обновлять, например, перед каждой зимой.
Теперь слово за мастерами станций технического обслуживания. Если они вооружатся Dinitrol 713 IQ, число поломок кондиционеров пойдет на убыль. А народ быстро сообразит, что лучше заплатить за обработку, чем менять дорогущие узлы кондиционера.
О «холодном цинковании»
В народе до сих пор живет легенда: дескать, кузов «Победы» был покрыт оловом, и никакая коррозия его не брала. Известны ее корни: мастера, ремонтирующие аварийные машины, использовали местный нагрев. И вдруг из-под пламени горелки начинало литься олово – много олова! Отсюда и пошла молва: кузов, дескать, весь облужен…
На самом деле все гораздо прозаичнее. Штамповая оснастка тех лет была несовершенной, и заводские технологии предусматривали рихтовку кузовных деталей. Остающиеся неровности заливали припоем – вот и все. Особенно много его было вблизи рамки ветрового стекла.
Так ли хорошо покрытие кузова оловом, как считают некоторые? Давайте разбираться. Коррозия всегда возникает на поверхности металла, а облуженная деталь ведет себя так, будто она изготовлена из олова. А оно само по себе очень стойко и практически не корродирует. Значит, и сталь под слоем олова находится в полной безопасности.
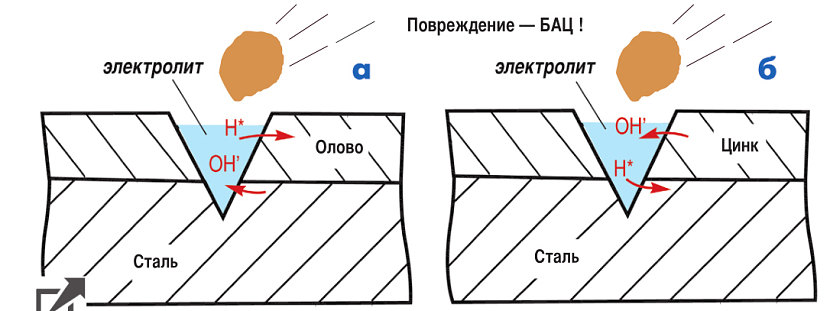
а) Схема коррозии луженой стали. При повреждении покрытия электрохимическая коррозия разрушает сталь. б) Схема коррозии оцинкованной стали. При повреждении покрытия электрохимическая коррозия разрушает цинк
Но когда защитный слой получает повреждение, картина меняется. Между сталью (железом) и оловом мгновенно возникает гальваническая пара. А поскольку олово является менее активным металлом, сталь под воздействием гальванического тока начинает разрушаться.
Вспомним судьбу консервных банок, изготовленных из луженой жести. Все бывает хорошо, пока банку не поцарапаешь. А уж коль случилось такое, «всей птичке пропасть»: луженая сталь в месте повреждения ржавеет гораздо быстрее нелуженой. Поэтому не будем говорить о «вечных луженых кузовах» – может выйти неловко.
Все мы знаем, что кузовные панели многих автомобилей оцинковывают на заводах. Покрытие толщиной от 2 до 10 мкм обеспечивает прекрасную защиту от возникновения и распространения коррозионных поражений.
Электрохимический ряд напряжений металлов. Тот, кто выше, защищает того, кто ниже
Применительно к оцинковке можно сказать, что человечество борется с электрохимической коррозией под лозунгом «бей врага его же оружием». Защищающий металл (цинк) в ряду напряжений расположен левее железа. Следовательно, и коррозия в поврежденном месте протекает иначе, чем в случае с оловом. Гальваническая пара, само собой, тоже возникает, но разрушается уже не сталь, а цинк.
Почему же тогда цинковый щит не исчезает, не тает со временем? Исчезает и тает, но очень-очень медленно. Здесь есть особенность: цинк начинает активно разрушаться лишь при повышенных температурах. Вот почему в оцинкованных ведрах не рекомендуют кипятить воду. И тогда эти ведра живут долго – десятилетиями. И оцинкованные крыши тоже.
Но вернемся к автомобилям. Промышленные методы оцинковки, будь то горячее окунание или гальваностегия, не применимы в сервисных и гаражных условиях. Поэтому появление так называемых «препаратов холодного цинкования» оказалось для ремонтников весьма кстати.
Наносимые подобно грунтовке или краске, эти материалы образуют двойную защиту стальной поверхности: активную, как у горячей оцинковки, и пассивную, как у лакокрасочного слоя. Давайте познакомимся с ними на примере шведских препаратов Dinitrol 443 и Dinitrol 444.

Они представляют собой готовые к применению жидкие однокомпонентные составы, содержащие технически чистый гальванический цинк. «Технически чистый» означает 99,995% Zn, что является очень высоким показателем для промышленного продукта. И вот такого, практически не содержащего примесей цинка, в препаратах Dinitrol 443 и Dinitrol 444 ни много ни мало – 95%. Остальные 5% приходятся на синтетические смолы, безопасный растворитель и некоторые специальные добавки.
Очень важна роль синтетической каучуковой смолы, входящей в рецептуру препарата. Благодаря ей слой Dinitrol 443 или 444 обладает отменной адгезией. Но это еще не все: при высыхании он сохраняет эластичность, без проблем выдерживая механические и тепловые деформации.
А как обстоят дела с термостойкостью? А вот как: пленка препарата выдерживает температуры от –40 до +150° С без потери эксплуатационных свойств. Так что, добро пожаловать и в Сибирь, и в окрасочно-сушильную камеру!
Что касается стойкости к химической агрессии, то «шведы» могут находиться в среде с рН от 5 до 10. Для тех, кто химию подзабыл, напомним: дистиллированная вода имеет рН = 7. Значит, Dinitrol 443 и 444 выдерживает как щелочную, так и кислотную «баню».
«Холодный цинк» марки Dinitrol может наноситься методом распыления, кистью, валиком или окунанием. При толщине пленки 40 мкм расход составит 0,25 кг/м2. Высыхание длится 48 часов при комнатной температуре (на отлип – 10 мин). Для ускорения сушки деталь можно поместить в камеру и выдержать 30–60 мин при 60° С. Повторный слой материала наносится через час. Полученную пленку можно окрашивать практически всеми видами ЛКМ.
Алюминий на железе – зло? или познавательная коррозия.

С чего обычно начинаются работы по добавлению функционала наших машин? Правильно – с посещения сайтов и форумов, чтобы посмотреть, как другие реализовали подобные идеи, подчерпнуть что-то интересное и не совершать чужих ошибок. Но всегда ли стоит верить тому, что написано на форумах? Чужой опыт не всегда является истиной и редко описывается человеком, достигшим Дзен в данном вопросе. Вспоминаю свои первые посты – такую ерунду писал, да еще и отстаивал свою правоту, да так убедительно. А ведь кто-то может этим воспользоваться. Так же помню читал раньше, где уже не помню, о том, что ни в коем случае нельзя выполнять отделку кузова алюминием. Звучало это приблизительно так: «Ребята, да Вы что, совсем физику не учили?! При контакте алюминия и железа Вы создаете гальваническую пару и у Вас кузов за полгода сгниет весь, растворится! Головой-то надо думать хоть иногда!». Гальваническая пара создается, да, но будет ли таким плачевным результат? Об этом далее.
По моей новой профессии отправили меня учится на повышение квалификации в Уфимский Государственный Нефтяной Технический Университет, где в течении двух недель кандидаты технических наук рассказывали мне о коррозии металла и как с ней бороться. Эта статья не будет научно-публицистической, дабы не забивать Вам голову, постараюсь все рассказать на примере яблок, образно.
Итак, по механизму протекания коррозия делится на химическую и электрохимическую. Химическая коррозия протекает в неэлектролитической среде при высокой температуре. Так как мы рассматриваем кузов автомобиля, то данный тип коррозии не применим. Нас интересует электрохимическая коррозия, электролитом в которой выступает влага. Из курса физики и химии мы все помним, что все металлы имеют кристаллическую решетку, в которой электроны свободно двигаются и называется такая решетка металлосвязью. Эта связь атомов не очень крепкая и ее свойства позволяют активно использовать данные материалы в нашей жизни.
Но тот факт, что она не крепкая доставляет нам проблемы. Например, диполи воды (а вода, в силу своего строения, является довольно агрессивной средой) разбивают металлосвязь и наиболее активно это происходит в местах, где количество электронов недостаточно, вытягивая молекулы металла и создавая с ними более стабильное соединение. Эти места являются очагами коррозии. Как же возникают участки металла с малым количеством электронов? Связано это как раз со способностью электронов свободно перемещаться в кристаллической решетке металла. Все металлы имеют естественный потенциал (электростатический), отличный от нуля. Железо в естественных условиях имеет потенциал, равный приблизительно -0,44 Вольта, цинк -0, 76 В, алюминий -1, 67 В, магний -2,3 В. Но даже металл одной природы, например, лист железа, в разных своих частях имеет отличающиеся потенциалы. Незначительно, но отличаются. Это связано с различными причинами, в том числе с механическими напряжениями в структуре металла, различными вкраплениями, острыми краями, заусенцами, царапинами, наклёпами, сварочными швами и т.д. Такие места имеют более отрицательный потенциал по отношению к другим частям и они являются анодными зонами, т.е. анодами (остальные части соответственно являются катодами).
При протекании электрохимической коррозии в электролите анод насыщает электронами через проводник катод, тем самым теряя силу молекулярной связи и разрушается под действием агрессивной среды.
Вспомните места, где наиболее часто гниет кузов – это сгибы кузова, швы, соединения различных частей и т.д., т.е. в местах, где присутствует влага и есть дополнительные факторы, создающие анодные зоны. Те же полики на наших машинах не гниют равномерно по всей площади. Очаги начинают развиваться в углах и на сгибах. Каждый из Вас может в качестве подтверждения провести один небольшой и не сложный опыт: Возьмите два одинаковых гвоздя. Один из них согните на 90 градусов. Затем обезжирьте оба и не касаясь пальцами (можно брать их бумажкой) положите в раствор поваренной соли (NaCl). Коррозия будет протекать наиболее интенсивно на согнутом гвозде в месте изгиба. На прямом гвозде она будет протекать более равномерно по всей площади и менее интенсивно. Кому доводилось разбирать деревянные постройки, в которых ржавые гвозди, могут вспомнить, что согнутые гвозди в местах сгибов очень легко ломаются и практически все место слома ржавое насквозь.
От действия коррозии кузов защищает изоляция, в роли которой выступают краска и грунтовка. Но тут есть один момент – в местах нарушения изоляции коррозия будет развиваться более интенсивно, нежели бы весь металл был голым, без изоляции.
Так какое же все-таки влияние оказывает алюминий на железо в местах контакта? Металлы с более отрицательным естественным потенциалом при соприкосновении с железом выступают в роли анода, т.е. защищают металл от коррозии. К таким металлам относятся цинк, алюминий и магний. Т.е. при отделке кузова алюминием при наличии электролита между ними в качестве анода будет выступать алюминий и именно он будет разрушаться. Процесс этот длительный, а при условии, что алюминий редко несет серьезные механические нагрузки – еще и безболезненный. На данном принципе построена протекторная защита металлоконструкций от коррозии, например, нефтепроводов.
Конечно, никто Вам гарантий того, что уложив лист алюминия на полик Вы полностью защите кузов от коррозии, здесь не дает. На этот процесс влияет много факторов, в том числе токи, протекающие по кузову от электроприемников, различные агрессивные среды, разлитые масла, химические жидкости и т.д. Но хуже алюминием Вы не сделаете, даже наоборот.
Здесь еще стоит отметить, что в местах контакта кузова с металлами, имеющими меньший естественный потенциал по отношению к железу, железо уже не будет катодом, а станет анодом, как следствие процесс коррозии будет протекать более интенсивно. К таким металлам относятся никель, олово, свинец, медь. Серебро и золото тоже, но они думаю у вас в машинах не валяются.
Вот собственно и все о коррозии и с чем ее едят, не сильно кратко, но и не очень заумно) Надеюсь, что статья оказалась для Вас полезной!
Гальваническая коррозия алюминия
Следует подчеркнуть, что стойкость алюминия и алюминиевых сплавов к нормальным условиях окружающей среды является очень высокой. Главным источником защиты от коррозии является прочная, самовосстанавливающаяся оксидная пленка, которая всегда присутствует на алюминии в условиях окружающей воздушной атмосферы (рисунок 1).

Рисунок 1 – Естественная защита алюминия от коррозии – поверхностная оксидная пленка [4]
Основные типы коррозии алюминия
Для коррозии алюминия характерны следующие основные типы [4]:
- Общая коррозия
- Щелевая коррозия
- Фреттиниг-коррозия
- Коррозия под напряжением
- Гальваническая коррозия
- Точечная (питтинговая) коррозия
- Межзеренная коррозия
- Подповерхностная коррозия

Рисунок 2 – Общая коррозия алюминия: растворение естественной оксидной пленки
растворами сильных щелочей и некоторых кислот [4]

Рисунок 3 – Щелевая коррозия алюминия [4]

Рисунок 4 – Фреттинг-коррозия алюминия: взаимное трение двух алюминиевых компонентов
в условиях шероховатого контакта [4]

Рисунок 5 – Коррозия алюминиевых сплавов под напряжением: при некоторых условиях
в сплавах Al-Cu, Al-Mg, Al-Zn-Mg [4]

Рисунок 6 – Гальваническая коррозия алюминиевого сплава
происходит в условиях его мокрого или влажного контакта
с другим, более “благородным” металлом, таким как медь [4]

Рисунок 7 – Питтинговая (точечная) коррозия алюминия
под воздействием хлоридных ионов [4]

Рисунок 8 – Межзеренная коррозия и подповерхностная коррозия [4]
В зависимости от условий окружающей среды, нагружения и функционального назначения детали любой из видов коррозии может явиться причиной преждевременного разрушения. Кроме того, неправильное применение алюминиевых деталей и изделий может усугублять коррозионные процессы.
Наиболее частые ошибки проектирования алюминиевых конструкций связаны с гальванической коррозией. Гальваническая или электрохимическая коррозия происходит, когда два разнородных металла образуют электрическую цепь, замыкаемую жидким или пленочным электролитом или коррозионной средой. В этих условиях разность потенциалов между разнородными металлами создает электрический ток, проходящий через электролит, который (ток) и приводит к коррозии в первую очередь анода или менее благородного металла из этой пары.
Сущность гальванической коррозии
Когда два различных металла находятся в прямом контакте с электропроводящей жидкостью, то опыт показывает, что один из них может корродировать, то есть подвергаться коррозии. Это называют гальванической коррозией.
Другой металл не будет корродировать, наоборот, он будет защищен от этого вида коррозии.
Этот вид коррозии отличается от тех видов коррозии, которые могли бы возникнуть, если бы оба эти металлы были помещены раздельно в ту же самую жидкость. Гальваническая коррозия может случиться с любым металлом, как только два различных металла будут находиться в контакте в электропроводящей жидкости.
Внешний вид гальванической коррозии
Внешний вид гальванической коррозии является очень характерным. Эта коррозия не раскидывается по всей поверхности изделия, как это бывает с точечной – питтинговой – коррозий. Гальваническая коррозия плотно локализована в зоне контакта алюминия с другим металлом. Коррозионное воздействие на алюминий имеет равномерный характер, он развивается в глубь в виде кратеров, которые имеют более или менее округлую форму [3[.
Все алюминиевые сплавы подвергаются идентичной гальванической коррозии [3].
Принцип батареи
Гальваническая коррозия работает как батарея, которая состоит из двух электродов:
- катода, где происходит реакция восстановления
- анода, где происходит реакция окисления.
Эти два электрода погружены в проводящую жидкость, которая называется электролитом. Электролит – это обычно разбавленный кислотный раствор, например, серной кислоты, или соляной раствор, например, сульфат меди. Эти два электрода соединены снаружи электрической цепью, которая обеспечивает циркуляцию электронов. Внутри жидкости передача электрического тока происходит путем перемещения ионов. Жидкость, таким образом, обеспечивает ионное электрическое соединение (рисунок 9).

Рисунок 9 – Принцип гальванической ячейки [3]
Рисунок 1 показывает ячейку, в которой электролитом является раствор серной кислоты. Серная кислота полностью диссоциирована в воде (поскольку является сильной кислотой) путем образования ионов Н + , которые определяют кислотность среды. Происходит следующая электрохимическая реакция [3]:
на медном катоде восстанавливаются протоны Н + :
Полная реакция имеет вид:
Эта ячейка производит электричество за счет потребления цинка, который выделяется в виде гидроксида цинка Zn(OH)2.
Для работы ячейки необходимо одновременное выполнение трех условий:
- два различных металла, которые образуют два электрода;
- присутствие электролита;
- непрерывность всей электрической цепочки.
Если хотя бы одно из этих условий не выполняется, например, если нарушается электрический контакт, то ячейка не будет производить электричество, и окисления на аноде не будет происходить (также как и восстановления на катоде).
Условия для гальванической коррозии
Гальваническая коррозия основана на том же самом принципе и для того, чтобы она происходила необходимо одновременное выполнение следующих трех условий [3]:
- различные типы металлов;
- присутствие электролита;
- электрический контакт между двумя металлами.
Различные типы металлов
Для любых металлов, которые относятся к различным их типам, гальваническая коррозия является возможной. Металл с электроотрицательным потенциалом (или более электроотрицательный металл, если они оба электроотрицательные) действует как анод.
Тенденцию различных металлов образовывать гальванические пары и направленность электрохимического действия в различных коррозионных средах (морской воде, тропическом климате, промышленной атмосфере и т.д.) показывают в так называемых гальванических рядах. Чем далее удалены друг от друга металлы в этих рядах, тем более серьезной может быть электрохимическая коррозия. В разных коррозионных средах эти последовательности металлов могут быть разными (рисунок 10).
Присутствие электролита
Область контакта должна быть смочена водным раствором, чтобы обеспечивать ионную электропроводимость. В противном случае отсутствует возможность для гальванической коррозии.
Электрический контакт между металлами
Электрический контакт между металлами может происходить или путем прямого контакта между двумя металлами, или через крепежное соединение, например, болт.
Как видно из графиков рисунка 10 алюминий и его сплавы становятся анодами в гальванических ячейках с большинством металлов, и алюминий корродирует, как говорят, жертвенно и защищает от коррозии другой металл гальванической пары.
Только магний и цинк, включая и оцинкованную сталь, являются более анодными и поэтому, сами подвергаясь коррозии, защищают от нее алюминий.
Алюминий и кадмий вообще имеют почти одинаковые электродные потенциалы и поэтому ни алюминий, ни кадмий не подвергаются гальванической коррозии. К сожалению, кадмий признан весьма токсичным и все реже применяется, а во многих странах просто запрещен, как антикоррозионная защита.
Гальванические пары
Относительное расположение двух металлов или сплавов в гальваническом ряду указывает только возможность гальванической коррозии, если различие их гальванических потенциалов является достаточно большим. Больше этот ряд ничего не говорит, и особенно ничего – о скорости или интенсивности гальванической коррозии. Она может быть нулевой или несущественной или даже незаметной. Ее интенсивность зависит от типов металлов, которые входят в контакт – гальванической пары.
Пара: алюминий – нелегированная сталь
В строительных конструкциях алюминиевые детали, которые открыты для воздействия климатических и погодных воздействий, могут соединяться винтами из обычной стали. Опыт показывает, что алюминий в контакте со стальными винтами подвергается только очень поверхностной коррозии. Возникающая ржавчина, которая не оказывает никакого влияния на алюминий, полностью пропитывает слой оксида алюминия и образует на поверхности пятна. Фактически, для алюминиевой конструкции в контакте с незащищенной сталью важнее будет ее влияние на внешний вид и декоративные качества, а не способность сопротивляться коррозии.
Это явление имеет следующее объяснение:
- на поверхностях контакта образуются пленки с продуктами коррозии – ржавчины на стали и оксида алюминия на алюминии, которые и замедляют электрохимические реакции.
Пара: алюминий – оцинкованная сталь
Судя по гальваническому ряду, цинк является более электроотрицательным, чем алюминий. Крепеж из оцинкованной стали может, поэтому, применяться для соединения и сборки конструкций из алюминиевых сплавов. Надо помнить, что когда цинковое покрытие станет слишком изношенным, чтобы защищать сталь и алюминий, наступает предыдущий сценарий контакта между алюминием и голой сталью [3] .
Пара: алюминий – нержавеющая сталь
Хотя и существует большая разность потенциалов между нержавеющей сталью и алюминиевыми сплавами – около 650 мВ, очень редко можно увидеть гальваническую коррозию на алюминии в контакте с нержавеющей сталью. Поэтому алюминиевые конструкции очень часто собираются с применением болтов и винтов из нержавеющей стали [3].
Пара: алюминий – медь
Контакт между алюминиевыми сплавами и медью, а также медными сплавами (бронза, латунь) приводит к совершенно незначительной гальванической коррозии алюминия под воздействием атмосферных условий. Тем не менее, рекомендуется обеспечивать электрическую изоляцию между этими двумя металлами, чтобы локализовать коррозию алюминия.
Необходимо отметить, что продуктом коррозии меди является, так называемая, патина. Эта патина – голубовато-зеленый налет на меди, который состоит в основном из карбоната меди. Эта патина химически воздействует на алюминий и может восстанавливаться с образованием малых частиц меди. Эти медные частицы, в свою очередь, могут вызывать локальную питтинговую коррозию алюминия [3].
Ближе к контакту – больше коррозия
Ускоренная гальваническая коррозия обычно наиболее интенсивна вблизи мест соединения двух металлов; с удалением от мест соединения ее интенсивность уменьшается. Существенное влияние на скорость коррозии оказывает величина отношения площади поверхности катода, контактирующей с электролитом, к площади незащищенной поверхности анода. Желательно иметь малое отношение площади катода к площади анода.
Читайте также:
