Сталь и алюминий окисление
Обновлено: 23.04.2024
Исследования электрических параметров не дают полной характеристики биметаллических сварных Соединений. И поэтому наряду с измерением токов, потенциалов и поляризаций большое значение для практических целей представляют и исследования коррозионной стойкости в условиях постоянного и переменного погружения в морскую воду, в условиях морской атмосферы и др.
Исследованиями было выявлено влияние меди, цинка и железа на коррозию алюминия, находящегося с ними в контакте. Испытания проводились в камерах с различными средами: во влажной атмосфере, в морской атмосфере, в атмосфере влажных промышленных газов (С02 й S02). При испытаниях алюминий соединяли с другими металлами с помощью алюминиевых болтов, выдерживая при закреплении одинаковые давления. Как показал автор, контакт алюминия с цинк — алюминием, углеродистой сталью» ’и фералюминием во всех средах дает уменьшение коррозии алюминия или только незначительное увеличение ее.
Бельчук Г. А. определил, что коррозионная стойкость сварных композитных соединений из алюминиевого сплава и оцинкованной стали в синтетической морской воде достаточно высокая.
В. П. Ситалов, Раздуй Ф. И. [35] исследовали стойкость сварных соединений АМгб — Ст4, сваренных через биметаллические вставки, и сделали вывод, что коррозионная стойкость соединений вполне удовлетворительна. Сварные швы как со стороны стали, так и со стороны алюминиевого сплава не уступают по коррозионной стойкости основному металлу; алюминий подвергается большей коррозии по сравнению со сталью. Механические испытания образцов показали неизменность прочностных свойств до и после коррозионных исследований. На основании исследований была предложена следующая схема лакокрасочных покрытий для защиты конструкций от коррозионных разрушений: грунт ВЛ —- 02— один слой, краска ЗП— 71 — четыре слоя, сварные швы и биметаллические вставки покрывались герметиком
В лабораторных условиях было проведено исследование коррозионной стойкости в синтетической морской воде сварных соединений алюминий — сталь с эмалевыми покрытиями. Перед сваркой на кромки пластин СтЗ наносили двойное гальваническое покрытие — слой меди толщиной 5— 6 мкм, затем слой цинка толщиной 30—40 мкм. Сварку между стальными пластинами и пластинами сплава АМгЗ производили аргонодуговым методом с применением присадочной проволоки АДО. На поверхность сварных образцов наносилось пять видов покрытий, основой которых были грунты BJI-02, АГ-10С и ФЛ-03, а также эмали ПХВ-бЭА, ЭП-51. Торцы образцов защищали бакелитовым лаком. Образцы испытывали в аппарате переменного погружения и влажной камере. Наилучшими из опробованных покрытий оказалось покрытие на основе грунта ВЛ-02 — первый слой, второй слой-— грунт АГ-10С, третий слой — грунт АГ ЮС + 2% алюминиевой пудры и затем два слоя эмали ПХВ - бЭА. Осмотр после испытаний показал, что более жесткими являются испытания при переменном погружении. Покрытия на образцах после выдержки во влажной камере сохранились лучше.
В г. Севастополе коррозионная стойкость сварных соединений сплавов АМц и АМгб со сталями марок СтЗ и ХЮН ЮТ исследовалась в течение года. Ряд соединений для повышения механических свойств был выполнен при помощи присадочных проволок, дополнительно легирующих сварной шов кремнием, цинком и бериллием. Электрохимическая гетерогенность поверхности сварных соединений в известной мере уравнивалась применением для сварки проволоки АДО и покрытием поверхности стали марки СтЗ цинком, сталь Х18Н10Т — алитировалась. Часть образцов перед испытанием была покрыта лако-красочными покрытиями. Коррозионные испытания проводились при полном и переменном погружении в море и в морской атмосфере.
Оценку степени коррозионного воздействия морской воды на соединения проводили по результатам механических исследований, проведенных до и после испытаний, визуальному осмотру и по глубине имеющихся коррозионных разрушений.
Соединения АМц + СтЗ после испытаний при постоянном и переменном погружении в море и в морской атмосфере показали хорошую коррозионную стойкость. Поверхность сплава АМц слегка потемнела, коррозионные разрушения отсутствовали, поверхность оцинкованной стали СтЗ в отдельных местах была покрыта продуктами коррозии.
Металлографические исследования показали, что меж - кристаллитная коррозия в отдельных местах после годичных испытаний наблюдается только на сплаве АМц; по линии сплавления, шву и по стали разрушений не обнаружено.
Испытания окрашенных (грунт ВЛ-02 — первый слой, краска ПФ-64 — второй слой) сварных образцов соединения АМц + СтЗ в морской атмосфере показало, что лакокрасочное покрытие имеет хорошую стойкость; покрытие сохранилось на всей поверхности. Однако в условиях полного и переменного погружения данный вид покрытия неприменим.
Соединения АМгб + СтЗ при испытаниях в условиях переменного погружения имели редкие точечные продукты коррозии, под которыми поверхность более светлая. На сплаве АМгб наблюдаются точечные разрушения (6—8 на 1 см2, глубина их не превышает 0,3 мм), на сварных швах имеются единичные точечные продукты коррозии.
При полном погружении образцы характеризуются недостаточной стойкостью. Металлографическими исследованиями сварных соединений после обеих видов испытаний не было обнаружено межкристаллитной коррозии.
Сварные соединения АМгб + СтЗ, сваренные проволоками, легированными кремнием, цинком, бериллием, показали
недостаточную коррозионную стойкость при полном погружении в море, интенсивное разрушение шва и наличие меж- кристаллитной коррозии по краю образцов и по линии сплавления,
Соединения АМгб + Х18Н10Т при испытании в условиях постоянного погружения в море склонны к щелевой коррозии, так как швы на сплаве АМгб располагаются у мест крепления образцов к кассете, под краской и резиной.
При переменном погружении описанное явление не наблюдали, отмечены редкие точечные продукты коррозии, под которыми поверхность более светлая.
При обоих методах испытания коррозионные разрушения наблюдали со стороны алюминия, по краям и по шву, Со стороны стали — отдельные места с общими коррозионными разрушениями.
Определение зависимости электродного потенциала от времени производили на образцах сталей, алюминиевых сплавов и их сварных соединений, находящихся в условиях полного погружения в морскую воду. После восьми месяцев испытаний наиболее положительным потенциалом обладает сварное соединение АМгб + X18Н10Т и АМгб + СтЗ, При введении в шов легирующих элементов потенциал резко сдвигается в отрицательную сторону. Сварное соединение АМц + СтЗ характеризуется более отрицательным потенциалом, чем соединение СтЗ + АМгб.
В табл. 36 приведены механические свойства сварных соединений после испытаний в морской воде, Сварные соединения АМц + СтЗ показали наибольшую коррозионную стойкость в атмосферных условиях, сварные соединения АМгб + Х18Н10Т ■— в условиях переменного погружения в море. Дополнительные легирования металла шва сварных соединений АМгб + СтЗ при испытании в морской воде показали значительное ухудшение механических и коррозионных свойств, что связано с ухудшением свойств образующейся на шве защитной пленки.
Предел прочности соединений на разрыв, 10 7 Н/м2, образцов после натурных испытаний
Совместимость металлов или как избежать гальванической коррозии?

Контактная коррозия происходит при непосредственном контакте двух разнородных металлов. Нельзя, к примеру, соединять алюминиевые листы медной заклепкой, так как при определенных условиях они образуют сильную гальваническую пару.
Разные металлы имеют разные электродные потенциалы. В присутствии электролита один из них играет роль катода, а другой анода. В результате химической реакции, протекающей между ними, начнется коррозионный процесс, в котором медь (катод) будет беспощадно разрушать алюминий (анод).
Почти все пары разнородных металлов, находящиеся в контакте между собой, подвержены коррозии, так как даже влага из воздуха может выступить в роли электролита и активировать их электродный потенциал. Но одни пары уязвимы в большей степени, а другие – в меньшей.
Например, алюминий отлично контактирует с оцинкованной сталью, хромом и цинком, а латунь совершенно не «дружит» со сталью, алюминием и цинком. Чтобы узнать, какие металлы совместимы, а какие нет, обратимся к основам химии.
В ряду электрохимической активности металлы стоят в следующей последовательности:

Электрохимический ряд напряжения металлов
Для примера рассмотрим пару алюминий – медь. Алюминий стоит в ряду слева от водорода и имеет электроотрицательный потенциал равный -1.7В, а медь находится справа и имеет положительный потенциал +0.4В. Большая разница потенциалов приводит к разрушению более активного алюминия. Медь сильнее всех, впереди стоящих элементов, поэтому в паре с любым из них она выйдет победителем. Чем дальше друг от друга в ряду стоят элементы, тем выше их несовместимость и вероятность протекания гальванической коррозии.
Данные о совместимости некоторых металлов представлены в таблице:
| Алюминий | Латунь | Бронза | Медь | Оцинкованная сталь | Железо | Свинец | Нержавеющая сталь | Цинк | |
| Алюминий | Д | Н | Н | Н | Д | О | О | Д | Д |
| Медь | Н | О | О | Д | О | Н | О | Н | Н |
| Оцинкованная сталь | Д | О | О | О | Д | О | Д | О | Д |
| Свинец | О | О | О | О | Д | Д | Д | О | Д |
| Нержавеющая сталь | Д | Н | Н | Н | О | О | О | Д | Н |
| Цинк | Д | Н | Н | Н | Д | Н | Д | Н | Д |
Д – абсолютно допустимые контакты (низкий риск ГК);
О – ограничено допустимые контакты (средний риск ГК);
Н – недопустимые контакты (высокий риск ГК).
Приведенная таблица может служить кратким справочником для определения совместимости некоторых конструкционных металлов. Допустимость и недопустимость контактов разнородных в электрохимическом отношении металлов устанавливает ГОСТ 9.005-72.
Пример недопустимых гальванических пар:

Гальваническое действие может возникнуть, если строительную конструкцию из нержавеющей стали скреплять оцинкованными болтами. В этой нежелательной паре пострадает высоко анодный крепеж, поскольку его электроны будут перемещаться в направлении катодной нержавеющей стали. Поэтому, крепежные детали должны быть изготовлены из менее гальванически активного металла, чем материал металлоконструкции.

На скорость течения гальванокоррозии оказывает влияние площадь поверхности анода и катода. Если большой по размеру анод соединить с маленьким катодом, то анод будет ржаветь медленно, а если сделать наоборот, то быстро. Например, используйте болты из нержавеющей стали для крепления алюминия, но не наоборот.
Степень интенсивности протекания контактной коррозии зависит и от условий эксплуатации соединения. В обычных атмосферных условиях процесс будет протекать менее быстро и возрастает в агрессивной электропроводной среде, например, растворах кислот и щелочей. Присутствие в воде других веществ увеличивает проводимость электролита и скорость коррозии. Поэтому при проектировании конструкций важна оценка окружающей среды.
Как защитить конструкцию или узел от контактной коррозии?
Если по конструктивным соображениям невозможно избежать нежелательного контакта разнородных металлов, то можно попытаться уменьшить гальваническую коррозию с помощью следующих методов:
- окраска поверхностей в районе их стыка;
- нанесение совместимых металлических покрытий;
- изоляция соединения от внешней среды;
- электрическая изоляция;
- установка неметаллических прокладок, вставок, шайб в болтовых соединениях.
Практика показывает, что в тех случаях, когда пренебрегают требованиями к допустимости контактов разных металлов, приходится дорого за это расплачиваться. Неправильная компоновка контактных пар выводит из строя узлы крепления, металлоконструкции и может стоять человеческой жизни.
Алюминий на железе – зло? или познавательная коррозия.

С чего обычно начинаются работы по добавлению функционала наших машин? Правильно – с посещения сайтов и форумов, чтобы посмотреть, как другие реализовали подобные идеи, подчерпнуть что-то интересное и не совершать чужих ошибок. Но всегда ли стоит верить тому, что написано на форумах? Чужой опыт не всегда является истиной и редко описывается человеком, достигшим Дзен в данном вопросе. Вспоминаю свои первые посты – такую ерунду писал, да еще и отстаивал свою правоту, да так убедительно. А ведь кто-то может этим воспользоваться. Так же помню читал раньше, где уже не помню, о том, что ни в коем случае нельзя выполнять отделку кузова алюминием. Звучало это приблизительно так: «Ребята, да Вы что, совсем физику не учили?! При контакте алюминия и железа Вы создаете гальваническую пару и у Вас кузов за полгода сгниет весь, растворится! Головой-то надо думать хоть иногда!». Гальваническая пара создается, да, но будет ли таким плачевным результат? Об этом далее.
По моей новой профессии отправили меня учится на повышение квалификации в Уфимский Государственный Нефтяной Технический Университет, где в течении двух недель кандидаты технических наук рассказывали мне о коррозии металла и как с ней бороться. Эта статья не будет научно-публицистической, дабы не забивать Вам голову, постараюсь все рассказать на примере яблок, образно.
Итак, по механизму протекания коррозия делится на химическую и электрохимическую. Химическая коррозия протекает в неэлектролитической среде при высокой температуре. Так как мы рассматриваем кузов автомобиля, то данный тип коррозии не применим. Нас интересует электрохимическая коррозия, электролитом в которой выступает влага. Из курса физики и химии мы все помним, что все металлы имеют кристаллическую решетку, в которой электроны свободно двигаются и называется такая решетка металлосвязью. Эта связь атомов не очень крепкая и ее свойства позволяют активно использовать данные материалы в нашей жизни.
Но тот факт, что она не крепкая доставляет нам проблемы. Например, диполи воды (а вода, в силу своего строения, является довольно агрессивной средой) разбивают металлосвязь и наиболее активно это происходит в местах, где количество электронов недостаточно, вытягивая молекулы металла и создавая с ними более стабильное соединение. Эти места являются очагами коррозии. Как же возникают участки металла с малым количеством электронов? Связано это как раз со способностью электронов свободно перемещаться в кристаллической решетке металла. Все металлы имеют естественный потенциал (электростатический), отличный от нуля. Железо в естественных условиях имеет потенциал, равный приблизительно -0,44 Вольта, цинк -0, 76 В, алюминий -1, 67 В, магний -2,3 В. Но даже металл одной природы, например, лист железа, в разных своих частях имеет отличающиеся потенциалы. Незначительно, но отличаются. Это связано с различными причинами, в том числе с механическими напряжениями в структуре металла, различными вкраплениями, острыми краями, заусенцами, царапинами, наклёпами, сварочными швами и т.д. Такие места имеют более отрицательный потенциал по отношению к другим частям и они являются анодными зонами, т.е. анодами (остальные части соответственно являются катодами).
При протекании электрохимической коррозии в электролите анод насыщает электронами через проводник катод, тем самым теряя силу молекулярной связи и разрушается под действием агрессивной среды.
Вспомните места, где наиболее часто гниет кузов – это сгибы кузова, швы, соединения различных частей и т.д., т.е. в местах, где присутствует влага и есть дополнительные факторы, создающие анодные зоны. Те же полики на наших машинах не гниют равномерно по всей площади. Очаги начинают развиваться в углах и на сгибах. Каждый из Вас может в качестве подтверждения провести один небольшой и не сложный опыт: Возьмите два одинаковых гвоздя. Один из них согните на 90 градусов. Затем обезжирьте оба и не касаясь пальцами (можно брать их бумажкой) положите в раствор поваренной соли (NaCl). Коррозия будет протекать наиболее интенсивно на согнутом гвозде в месте изгиба. На прямом гвозде она будет протекать более равномерно по всей площади и менее интенсивно. Кому доводилось разбирать деревянные постройки, в которых ржавые гвозди, могут вспомнить, что согнутые гвозди в местах сгибов очень легко ломаются и практически все место слома ржавое насквозь.
От действия коррозии кузов защищает изоляция, в роли которой выступают краска и грунтовка. Но тут есть один момент – в местах нарушения изоляции коррозия будет развиваться более интенсивно, нежели бы весь металл был голым, без изоляции.
Так какое же все-таки влияние оказывает алюминий на железо в местах контакта? Металлы с более отрицательным естественным потенциалом при соприкосновении с железом выступают в роли анода, т.е. защищают металл от коррозии. К таким металлам относятся цинк, алюминий и магний. Т.е. при отделке кузова алюминием при наличии электролита между ними в качестве анода будет выступать алюминий и именно он будет разрушаться. Процесс этот длительный, а при условии, что алюминий редко несет серьезные механические нагрузки – еще и безболезненный. На данном принципе построена протекторная защита металлоконструкций от коррозии, например, нефтепроводов.
Конечно, никто Вам гарантий того, что уложив лист алюминия на полик Вы полностью защите кузов от коррозии, здесь не дает. На этот процесс влияет много факторов, в том числе токи, протекающие по кузову от электроприемников, различные агрессивные среды, разлитые масла, химические жидкости и т.д. Но хуже алюминием Вы не сделаете, даже наоборот.
Здесь еще стоит отметить, что в местах контакта кузова с металлами, имеющими меньший естественный потенциал по отношению к железу, железо уже не будет катодом, а станет анодом, как следствие процесс коррозии будет протекать более интенсивно. К таким металлам относятся никель, олово, свинец, медь. Серебро и золото тоже, но они думаю у вас в машинах не валяются.
Вот собственно и все о коррозии и с чем ее едят, не сильно кратко, но и не очень заумно) Надеюсь, что статья оказалась для Вас полезной!
Сталь + алюминий = гальванопара = проблемы

Итакс, понадобилось мне снять продолный рычаг №3, для замены сайлента №11.
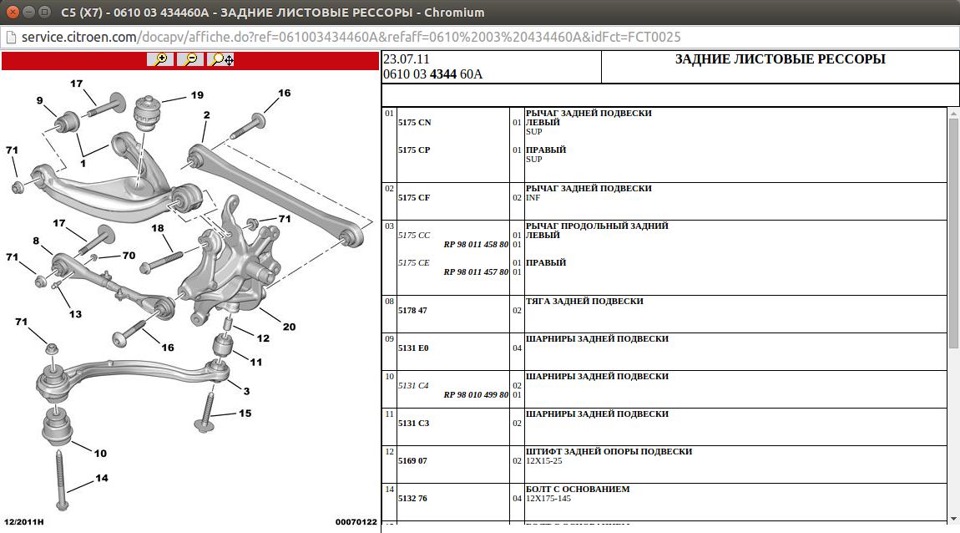
С правой стороны все открутилось без проблем, а вот с левой болт №15 законтачил с алюминиевой цапфой, да так сильно, что труба еле с ним справлялась.
Сделав один недополуоборот с трубой, я понял, что просто так болт выкручиваться не будет, начал его замачвать тормозухой и крутить в раскачку с переодическим постукиванием. После нескольких оборотов взору моих пальцев открылось отверстие в цапфе на выходе болта. Отверстие меньше диаметра болта, сделано под конус на конце болта, но это не мешает влаге добираться до резьбы и делать свои страшные делишки.
Потратив почти два часа, болт я все же выкрутил, но приварившийся алюминий на трех витках резьбы болта при выкручивании подпортил резьбу в цапфе — зажать с нужным момнтом не удалось.
Был куплен болт М12 длиной 100мм, (кстати купить болт с шагом резьбы 1,25 не так уж и легко), плашкой прорезана резьба до шляпки, самоконтрящаяся гайка, пару шайб.


Сверлом на 10.5мм досверлено сквозное отверстие, метчиком М12х1,25 обновлена резьба в цапфе. Болт затянут и подконтрен гайкой с обратной стороны.

Скопипащу себе выводы wulin , очень они правильные и я с ними согласен, надеюсь он не против :)
ИТОГИ и ВЫВОДЫ:
1. Проблема с металлическими болтами в алюминии не нова и может быть предотвращена. Никогда не позволяйте мастерам крутить болты подвески пневмоинструментом ударно-вращательного действия — деформирует витки алюминия и потом все это в рассоле и с влагой прикипает к резьбе железных болтов.
2. При закручивании болта в алюминий впрысните в отверстие какой-нибудь анаэробный герметик для резьб с термоослаблением- предотвратить окисление и закипание болтов. Или графитка должна помочь.
3. Тянуть болты не метровым рычагом, а согласно норм или хотя бы с умом.
4. Перед выкручиванием болтов из алюминиевого тела предварительно нагреть горелкой или феном тело, впрыскивая проникающую жидкость — при охлаждении жидкость будет проникать внутрь резьбового соединения. Операцию повторить несколько раз. И только потом аккуратно пытаться выкрутить. Если не идет, то греть-прыскать-охлаждать-потихоньку тянуть с постукиваниями.
Поверьте — лучше потерять 2 часа времени на медленное выкручивание, чем сутки времени и кучу нервов, денег и безопасности при поиске вариантов избавиться от обломка!
5. Если сломали, то сверлить очень хорошим сверлом, сначала тонким, затем больше.
6. Экстракторы надежны при цене не менее 100 руб за набор. Всякие Мариксы, Спидеры, Мудеры, Звери-зубры и т.д. — лопнут и принесут море проблем.
Экстрактор использовать при диаметре отверстия для него не более 1/2 диаметра выкручиваемого болта, иначе он будет распирать болт и клинить еще больше. Глубина отверстия под экстрактор не менее 1,5 диаметра отверстия под него.
7. Можно вытравить железный остаток теплой азотной кислотой (35-50% по разным источникам). Долго, но резьбу поможет сохранить.
Шприцом заливать в отверстие, греть, через полчаса высасывать шприцем взвесь и заливать новую порцию кислоты. Время травления — от 3-х часов до 3-х суток.
8. Если есть возможности — добыть болты из нержавейки. Они-то в соединении с алюминием вообще нейтральны.
Нвблюдение. Вкрученные на заводе болты, даже старые, отворачиваются не нарушая резьбы. А вот после первой же замены, т.е. выкручивания и скручивания, следующий ремонт выходит боком. Похоже кислород и влага при первом же ремонте окисляет моментально алюминий и потом достаточно трех месяцев, чтобы болт прикипел. Почитал советы электриков-они применяют какой-то технический вазелин для соединений-гальванопар. Возможно это достойная замена графитке
Читайте также:
