7а группа это группа металлов
Обновлено: 05.10.2024
В 17 группу входят F, Cl, Br, I, At (табл. 1 и 2). Слово галоген («гало» + «ген») означает «образующий соль». Все элементы — неметаллы. Во внешней оболочке имеют 7 электронов. Из-за высокой электроотрицательности и реакционной способности в свободном виде в природе не встречаются. Благодаря легкому присоединению электрона образуют галогенид-ионы, поэтому существуют в форме двухатомных молекул. Атомы в молекулах связаны ковалентной связью в результате обобществления пары электронов, по одному от атома. Молекулы галогенов удерживаются вместе слабыми вандерваальсовыми силами, что объясняет их высокую летучесть.
Таблица 1 . Некоторые физические и химические свойства металлов 17 группы
Относит, ат. масса
Фтор Fluorine [от лат. fluere — течь]
Хлор Chlorine [от греч. chloros — зеленоватый]
Бром Bromine [от греч. bromos — зловоние]
[Ar]3d 10 4s 2 4p 5
Йод Iodine [от греч. iodes — фиолетовый]
[Kr]4d 10 5s 2 5p 5
Астат Astatine [от греч. Astatos — неустойчивый]
[Xe]4f 14 5d 10 6s 2 6p 5
Все галогены токсичны, имеют характерные резкий запах и окраску, интенсивность которой возрастает к нижней части группы. Эта группа состоит из наиболее реакционноспособных элементов Периодической системы. Атомные и ионные радиусы галогенов, а также длины связи в молекулах возрастают к нижней части группы в Периодической системе. Напротив, энергии диссоциации связи и ее прочность при этом уменьшаются, за исключением фтора.
Галогениды щелочных металлов (1 группа) являются соединениями ионного типа. У галогенидов щелочноземельных металлов (2 группа), кроме ионных, встречаются соединения частично ковалентного типа. При перемещении слева направо вдоль периода галогениды элементов становятся более ковалентными. Ковалентный характер галогенидов возрастает также при перемещении по группе вниз. При этом, если металл может существовать в нескольких состояниях окисления, то его связь с галогенидом в низшем из них имеет ионный характер, а в высшем — ковалентный. Как ионные, так и ковалентные галогениды двухвалентных металлов, как правило, кристаллизуются в слоистые решетки. Исключением является СиСl2, имеющий полимерное строение. Галогенид-ионы являются лигандами во многих комплексных ионах, вытесняя при этом менее сильные лиганды, например, воду.
Галогениды серебра неустойчивы на солнечном свету, разлагаясь на металл и галоген. Это свойство использовано в черно-белой фотографии. Наиболее светочувствительными оказались бромиды Ag. Широкое применение имеют галогеноводороды, являющиеся одними из самых известных сильных кислот. Кислотность их водных растворов увеличивается к нижней части группы. Исключением является фтороводород. Его водный раствор (плавиковая кислота) имеет небольшую кислотность, благодаря прочности связи Н – F и малой константе диссоциации кислоты.
Таблица 2. Содержание в организме, токсическая (ТД) и летальная дозы (ЛД) металлов 17 группы
В человеческом организме
Среднее (при массе тела 70 кг)
ТД - 20 мг, ЛД - 2 г
ТД - 3 г, ЛД - >35 г
ТД - 2 мг, ЛД - 35-350 г
Следы в некоторых минералах
Токсичен из-за радиоактивности
Фтор (F) — по распространенности занимает 13 место среди элементов земной коры, наиболее реакционноспособный элемент, наиболее мощный из промышленно получаемых окислителей. В газообразном виде имеет бледно-желтый цвет. В промышленности используют его органические соединения, полимеры и все соли, особенно CaF2 — в качестве флюса в металлургии, и AlF3 — при производстве Аl. Большие количества F2 производили в атомной промышленности для получения UF6 в процессах обогащения ядерного топлива.
Близкое расположение атомов в молекуле F приводит к сильному отталкиванию между несвязывающими электронами, что объясняет ослабление связи в молекуле. Поэтому фтор в элементном состоянии в форме F2 не встречается, но присутствует в виде фторид-иона в криолите Na3AlF6 и плавиковом шпате (флюорите) CaF2.
F всегда имеет степень окисления -1. Малый ковалентный радиус позволяет ему образовывать соединения с высокими координационными числами; например, SF6 существует, a SJ6 образоваться не может. В ионах фторидов металлов небольшой размер иона F - обусловливает высокие значения энтальпий решетки и термодинамическую стабильность.
После инкубации печени крыс с NaF поглощенный фтор концентрируется в митохондриях и ядрах гепатоцитов. Костной тканью (зубы, кости, хрящи) он поглощается в 3 раза активней, чем кровью. Выводится F в основном почками. Токсическое действие фторид-ионов связано с тем, что они связывают и тем самым инактивируют ионы-активаторы ферментных систем Са 2+ , Mg 2+ с образованием малорастворимых фторидов. Комплексные ионы PF - , BF4 - , SiF6 2- , вследствие прочности ковалентных связей в их молекулах, биологически неактивны. F - ингибирует металлопротеины.
Соединения с O2 (хлорноватистая НСlO, соли «гипохлориты»; хлористая НСlO2, соли «хлориты»; хлорноватая HСlO3, соли «хлораты»; хлорная НСlO4 кислоты, соли «перхлораты», а также их анионы и оксиды) являются окислителями; их применяют в качестве дезинфицирующих средств.
Содержание хлора в тканях млекопитающих близко к его содержанию в морской воде. Хлорид-ионы Сl - почти равномерно распределяются в организме живых существ в заметных количествах (от 70 до 103 ммоль/л). Их выделение осуществляется почками. Жидкий хлор вызывает серьезные ожоги кожи, а газообразный — сильно раздражает глаза и легкие, образуя с тканевой жидкостью соляную и хлорноватистую кислоты. В легких при этом может развиться пневмония.
Бром (Вr) — густая темно-красная жидкость с резким запахом и тяжелыми парами коричневого цвета. Это единственный неметалл, находящийся в жидком состоянии при комнатной температуре. Его используют в составе добавок к топливу, как ингибитор горения в огнестойких материалах, в красках и пестицидах, в фотографии. Биологическая роль изучена слабо, хотя Вr2 ядовит. Соотношение Br/Cl в крови равно примерно 0,01, причем Вr - содержится в основном в плазме. Сопутствует хлору в процессах обмена веществ, выводится с мочой.
Йод (I) — твердый черный блестящий неметалл. Легко возгоняется. Применяется в качестве дезинфицирующего спиртового раствора, в пищевых добавках, красителях, катализаторах, в фотографии. Относится к биологически необходимым («эссенциальным») элементам, входит в состав тиреоид-ных гормонов. Его дефицит считают фактором, предрасполагающим к развитию рака щитовидной и молочной желез.
I избирательно накапливается в щитовидной железе (более 80%). Йодид I - , поступивший в организм, быстро концентрируется в железе, где его концентрация выше, чем в крови, в 25-500 раз. В щитовидной железе йодид окисляется до йода, который под влиянием специфичного фермента йодирует ароматические кольца тирозина в молекулах тиреоглобулина с образованием липофильных гормонов роста — тироксина, йодтиронина, трийодтиронина. Йод в концентрации 5x10 -5 М разобщает окислительное фосфорилирование в митохондриях, легко образует нерастворимые хелаты с двухзарядными ионами металлов, особенно с Mg 2+ и Мп 2+ . Деятельность щитовидной железы активируется йодсодержащим тиреотропным гормоном гипофиза.
Недостаток йода в пище человека приводит к гипотиреозу и базедовой болезни (зобу). Йод в заметных количествах содержится в составе морской капусты (бурых водорослей рода Laminaria) в виде моно- и дийодтирозина, а также моно- и дийодтиронина, что позволяет использовать эти водоросли при заболеваниях щитовидной железы в качестве природного источника готовых предшественников гормона роста.
В биогеохимических провинциях с недостатком йода его соли добавляют в пищевую соль, однако это не приносит положительных результатов. Установлено, что значительно эффективнее с дефицитом йода можно бороться добавлением природных йодсодержащих продуктов, в частности, морской капусты, в пищевые продукты, например, в хлеб. Раньше йод извлекали из золы бурых водорослей, в настоящее время — из нефти и солевых источников. Отметим, что один из ключевых ферментов обмена йода (дейодиназа), обеспечивающий гомеостаз тироксина, относится к селенопротеинам. Следовательно, борьба с йоддефицитом на фоне дефицита Se бессмысленна, а с учетом механизма обратных связей — вредна.
Астат (At) — радиоактивный неметалл, получаемый при нейтронной бомбардировке изотопа 209 Bi. Из-за малого времени полураспада почти не изучен.
7а группа это группа металлов

Общая характеристика некоторых элементов
в связи с их положением в Периодической системе
Элемент ЕГЭ: 1.2.2. Общая характеристика металлов IA-IIIA групп в связи с их положением в Периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов. 1.2.3. Характеристика переходных элементов (меди, цинка, хрома, железа)… 1.2.4. Общая характеристика неметаллов IVA-VIIA групп…
1.2.2. Общая характеристика металлов IA-IIIA групп …
Все элементы IА–IIIА-групп Периодической системы относят к металлам (кроме бора). На внешнем энергетическом уровне эти элементы имеют не более трех электронов, что соответствует номеру группы, в которой они расположены.
Металлы IA-группы называют щелочными, так как при взаимодействии с водой они образуют щелочи. Металлы IIА-группы, за исключением бериллия и магния, называют щелочноземельными.
I группа, главная подгруппа —
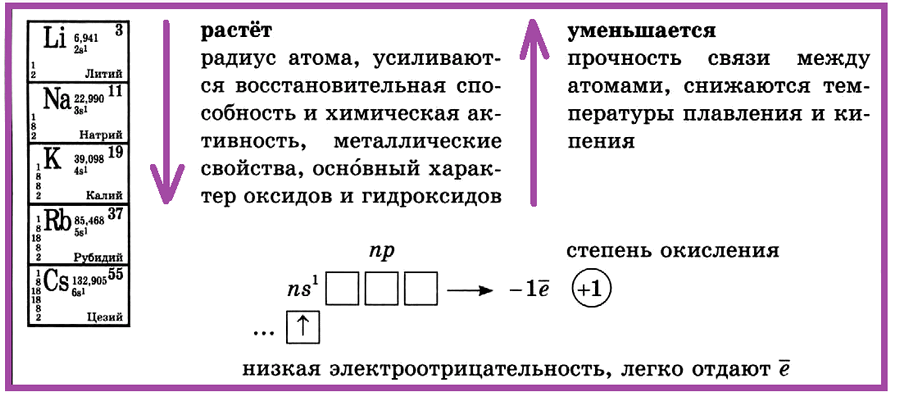
щелочные металлы (литий, натрий, калий, рубидий, цезий).
I группа, главная подгруппа — щелочные металлы: литий, натрий, калий, рубидий, цезий. С увеличением порядкового номера в ПСХЭ растет радиус атома, усиливаются восстановительная способность и химическая активность, металлические свойства, основный характер оксидов и гидроксидов.
II группа, главная подгруппа —
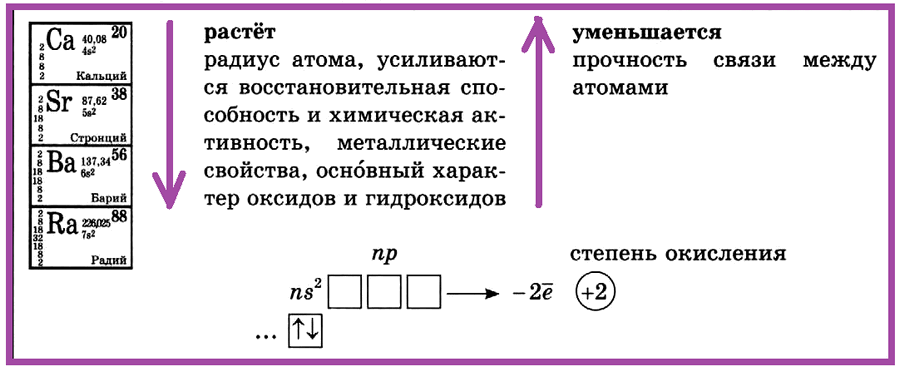
щёлочноземельные металлы (кальций, стронций, барий, радий)
II группа, главная подгруппа — щёлочноземельные металлы: кальций, стронций, барий, радий. С увеличением порядкового номера в ПСХЭ растет радиус атома, усиливаются восстановительная способность и химическая активность, металлические свойства, оснОвный характер оксидов и гидроксидов.
Элементы III группы главной подгруппы
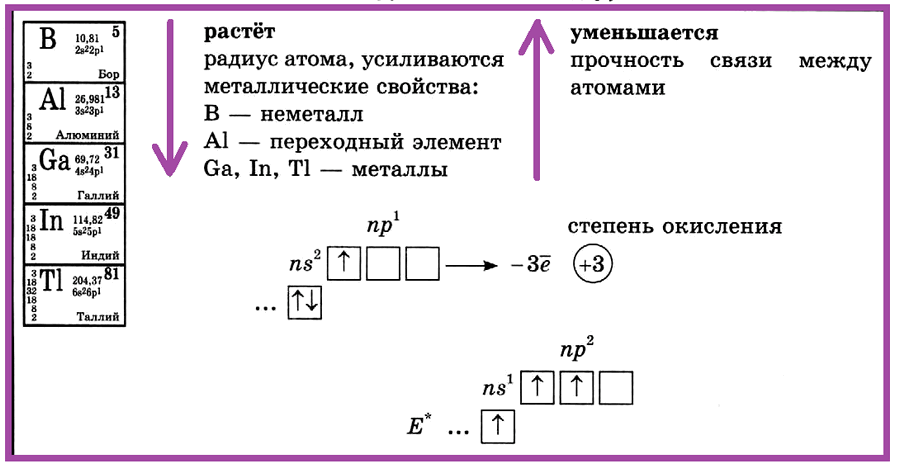
(бор, алюминий, галлий, индий, таллий)
Элементы III группы главной подгруппы: бор, алюминий, галлий, индий, таллий. С увеличением порядкового номера в ПСХЭ растет радиус атома, усиливаются металлические свойства. В — неметалл, Аl — переходный элемент, Ga, In, Тl — металлы.
1.2.3. Характеристика переходных элементов (меди, цинка, хрома, железа) …
Понятие переходный элемент относится к d-элементам, занимающим переходное положение между s- и p-элементами. Они расположены в побочных подгруппах (группах IБ-VIIIБ). Все d-элементы являются металлами, валентные электроны которых расположены на ns- и (n–1)d-подуровнях, т.е. они имеют электронную конфигурацию: (n–1)d 1–10 ns 1–2 .
Щелочные металлы. Элементы IA-группы
Ключевые слова конспекта: щелочные металлы, элементы IA-группы, литий, натрий, цезий, калий, рубидий, надпероксиды, пероксид натрия, щелочи, получение и применение щелочных металлов.
Щелочными металлами называют элементы IA-группы Периодической системы. Групповое название «щелочные» обусловлено тем, что растворимые в воде гидроксиды натрия и калия известны с древних времён, их называли щелочами. Важнейшие параметры этих элементов приведены в таблице.

Вы видите, как меняются свойства элементов в подгруппе: от лития к цезию радиусы атомов увеличиваются, значения энергии ионизации и электроотрицательности уменьшаются, металлические свойства усиливаются.
Электронная конфигурация валентного электронного слоя атомов щелочных металлов ns 1 , где n – номер валентного энергетического уровня. Щелочные металлы являются s-элементами.
В соединениях щелочных металлов преобладает ионный характер связи. В своих соединениях щелочные металлы могут быть только одновалентны. Во всех своих соединениях щелочные металлы имеют степень окисления +1.
Высшими оксидами являются соединения состава Ме2O, они имеют ярко выраженный основный характер. Высшие гидроксиды щелочных металлов МеОН – типичные основания, щёлочи. Водородные соединения щелочных металлов – твёрдые гидриды состава МеН.
ЩЕЛОЧНЫЕ МЕТАЛЛЫ – ПРОСТЫЕ ВЕЩЕСТВА
Щелочные металлы – вещества немолекулярного строения, их кристаллическая решётка металлическая.
При обычных условиях щелочные металлы – твёрдые вещества, имеют металлический блеск на свежем срезе (быстро тускнеют вследствие окисления), лёгкие (литий – самый лёгкий металл, его плотность составляет 0,53 г/см 3 ), легкоплавкие, мягкие (легко режутся ножом).
При внесении щелочных металлов или их соединений в бесцветное пламя оно приобретает характерную окраску:
Элемент
Окраска пламени
Li
Rb
Na
Cs
К
Щелочные металлы являются активными восстановителями. В атмосфере хлора и фтора они воспламеняются при обычных условиях.
Взаимодействие щелочных металлов с жидким бромом сопровождается взрывом.
Нагретые щелочные металлы легко сгорают на воздухе или в кислороде, но только при сгорании лития образуется оксид: При сгорании натрия обычно образуется пероксид (Na2O2):Пероксид натрия Na2O2 – кристаллы светло-жёлтого цвета – можно рассматривать как соль пероксида водорода H2O2.
При сгорании остальных щелочных металлов образуются надпероксиды (например, КO2). Получить оксиды Na2О, К2O, Rb2O, Cs2O можно восстановлением пероксидов и надпероксидов щелочными металлами, например, по реакции: КO2 + 3К = 2К2O
Щелочные металлы взаимодействуют с серой при нагревании.
Литий – единственный металл, который реагирует с азотом с образованием нитрида уже при комнатной температуре:Остальные щелочные металлы с азотом не реагируют (натрий реагирует с азотом при 100 °С, при электрическом разряде).
При нагревании щелочные металлы взаимодействуют с водородом с образованием твёрдых гидридов:
Щелочные металлы активно взаимодействуют с водой с образованием щёлочи и водорода. При этом кусочек лития или натрия с шипением «бегает» по поверхности воды, при взаимодействии калия происходит возгорание выделяющегося водорода (бледно-фиолетовое пламя), рубидий и цезий взаимодействуют со взрывом:
Щелочные металлы активно реагируют с разбавленными кислотами с образованием соли и водорода, но при этом параллельно протекают реакции щелочного металла с водой и образовавшейся щёлочи с кислотой.

Иначе протекают реакции с концентрированными растворами кислот или с самими кислотами – сильными окислителями, например с азотной и серной. В этих реакциях происходит восстановление азота в высшей степени окисления (в HNO3) или серы в высшей степени окисления (в H2SO4). Образуется соль, продукт восстановления азота или серы и вода:
Щелочные металлы активно взаимодействуют с растворами солей, но при этом происходит не замещение металла, входящего в состав соли, щелочным металлом, а прежде всего взаимодействие щелочного металла с водой раствора.
Натрий получают электролизом расплава поваренной соли (с добавками СаCl2 для понижения температуры плавления смеси):Щелочные металлы находят широкое применение в промышленности и в технике:
- литий – в литий-ионных аккумуляторах, в термоядерной энергетике для получения изотопа водорода – трития, а также в качестве теплоносителя в ядерных реакторах;
- натрий используют как теплоноситель в ядерных реакторах, для синтеза некоторых органических соединений (например, как катализатор в синтезе каучука, как активный восстановитель в других реакциях, часто в сплаве с калием), в металлотермии (натрийтермия);
- цезий легко теряет электроны даже под действием света, поэтому он применяется в фотоэлементах.
Наиболее распространёнными соединениями щелочных металлов являются (приведены исторические названия):
NaOH – едкий натр (каустическая сода),
NaCl – поваренная соль,
NaNO3 – чилийская селитра,
Na2SO4 • 10H2O – глауберова соль,
Na2CO3 • 10H2O – сода кристаллическая,
КОН – едкое кали,
КCl – хлорид калия, входит в состав калийной соли (NaCl • КCl + КCl),
KNO3 – индийская селитра,
К2СO3 – поташ.
Конспект урока по химии «Щелочные металлы. Элементы IA-группы». Выберите дальнейшее действие:
1.2.2. Общая характеристика металлов IА–IIIА групп в связи с их положением в Периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов.
В IA группу (главная подгруппа первой группы) таблицы Менделеева входят металлы — литий Li, натрий Na, калий К, рубидий Rb, цезий Cs и франций Fr. Традиционно, данные элементы называют щелочными металлами (ЩМ), так как их простые вещества образуют при взаимодействии с водой едкие щелочи. Последний из известных представителей группы щелочных металлов (Fr) является радиоактивным элементом, в связи с чем его химические свойства изучены недостаточно: период полураспада его наиболее долгоживущего изотопа 223 Fr составляет всего лишь около 22 мин.
Электронные формулы, а также некоторые свойства щелочных металлов представлены в таблице ниже:
| Свойство | Li | Na | К | Rb | Cs | Fr |
| Заряд ядра Z | 3 | 11 | 19 | 37 | 55 | 87 |
| Электронная конфигурация в основном состоянии | [He]2s1 | [Ne]3s1 | [Аr]4s1 | [Kr]5s1 | [Хе]6s1 | [Rn]7s1 |
| Металлический радиус rмет, нм | 0,152 | 0,186 | 0,227 | 0,248 | 0,265 | 0,270 |
| Ионный радиус rион*, нм | 0,074 | 0,102 | 0,138 | 0,149 | 0,170 | 0,180 |
| Радиус гидратированного иона,rион , нм | 0,340 | 0,276 | 0,232 | 0,228 | 0,228 | — |
| Энергия ионизации, кДж/моль: I1 I2 | 520,2 7298 | 495,8 4562 | 418,8 3052 | 403,0 2633 | 375,7 2234 | (380) (2100) |
| Электроотрицательность | 0,98 | 0,93 | 0,82 | 0,82 | 0,79 | 0,70 |
При движении вниз по IA группе возрастает радиус атомов металлов (rмет), что, собственно, характерно для любых элементов всех главных подгрупп. Относительно малое увеличение радиуса при переходе от K к Rb и далее к Cs обусловлено заполнением 3d- и 4d-подуровней соответственно.
Ионные радиусы ЩМ существенно меньше металлических, что связано с потерей единственного валентного электрона. Они также закономерно возрастают от Li + к Cs + . Размеры же гидратированных катионов изменяются в противоположном направлении, что объясняется в рамках простейшей электростатической модели. Наименьший по размеру ион Li + лучше катионов остальных щелочных металлов притягивает к себе полярные молекулы воды, образуя наиболее толстую гидратную оболочку. Исследования показали, что в водном растворе катион лития Li + окружен 26 молекулами воды, из которых только 4 находятся в непосредственном контакте с ионом лития (первой координационной сфере). По этой причине многие соли лития, например, хлорид, перхлорат и сульфат, а также гидроксид выделяются из водных растворов в виде кристаллогидратов. Хлорид LiCl·Н2O теряет воду при температуре 95 °С, LiOH·Н2O — при 110°С, а LiClO4·Н2O — только при температуре выше 150°С. С увеличением ионного радиуса катиона щелочного металла сила его электростатического взаимодействия с молекулами воды ослабевает, что приводит к снижению толщины гидратной оболочки и, как следствие, радиуса гидратированного иона [М(Н2O)n] (где n = 17, 11, 10, 10 для М + = Na + , К + , Rb + , Cs + соответственно).
Внешний энергетический уровень атома ЩМ содержит один единственный электрон, который слабо связан с ядром, о чем говорят низкие значения энергии ионизации I1. Атомы щелочных металлов легко ионизируются с образованием катионов М + , входящих в состав практически всех химических соединений этих элементов. Значения I2 для всех щелочных металлов настолько высоки, что в реально осуществимых условиях ион М 2+ не образуется. Электроотрицательность щелочных элементов мала, их соединения с наиболее электроотрицательными элементами (хлор, кислород, азот)имеют ионное строение, как минимум в кристаллическом состоянии.
Маленький радиус иона Li + и высокая плотность заряда, являются причиной того, что соединения лития оказываются схожими по свойствам аналогичным соединениям магния (диагональное сходство) и в то же время отличаются от соединений остальных ЩМ.
Элементы IIA группы
В IIA группу Периодической системы элементов входят бериллий Ве, магний Мg и четыре щелочноземельных металла (ЩЗМ): кальций Са, стронций Sr, барий Ва и радий Ra, оксиды которых, раньше называемые «землями», при взаимодействии с водой образуют щелочи. Радий — радиоактивный элемент (α-распад, период полураспада примерно 1600 лет).
Электронная конфигурация и некоторые свойства элементов второй группы приведены в таблице ниже:
| Свойство | Be | Mg | Ca | Sr | Ba | Ra |
| Заряд ядра Z | 4 | 12 | 20 | 38 | 56 | 88 |
| Электронная конфигурация в основном состоянии | [He]2s 2 | [Ne]3s 2 | [Ar]4s 2 | [Kr]5s 2 | [Xe]6s 2 | [Rn]7s 2 |
| Металлический радиус rмет, нм | 0,112 | 0,160 | 0,197 | 0,215 | 0,217 | 0,223 |
| Ионный радиус rион*, нм | 0,027 | 0,72 | 0,100 | 0,126 | 0,142 | 0,148 |
| Энергия ионизации, кДж/моль: |
По электронному строению атомов элементы второй группы близки щелочным металлам. Они имеют конфигурацию благородного газа, дополненную двумя s-электронами на внешнем уровне. В то же время от элементов первой группы они отличаются более высокими значениями энергии ионизации, убывающими в ряду Ве—Мg—Са—Sr— Ва. Эта тенденция нарушается при переходе от бария к радию: повышениe П и І, для Rа по сравнению с Ва объясняется эффектом инертной 6s 2 -пары.
Следует отметить, что в то время как для щелочных металлов характерна значительная разница между I1 и I2 для элементов второй группы подобный скачок наблюдается между I2 и I3. Именно поэтому щелочные металлы в сложных веществах проявляют только степень окисления +1, а элементы второй группы +2. Наличие единственной положительной степени окисления и невозможность восстановления ионов M 2+ в водной среде придает большое сходство всем металлам s-блока.
Изменение свойств по группе следует общим закономерностям, рассмотренным на примере щелочных металлов. Элемент второго периода бериллий, подобно элементу первой группы литию, значительно отличается по своим свойствам от других элементов второй группы. Так, ион Be 2+ благодаря чрезвычайно малому ионному радиусу (0,027 нм), высокой плотности заряда, большим значениям энергий атомизации и ионизации оказывается устойчивым лишь в газовой фазе при высоких температурах. Поэтому химическая связь в бинарных соединениях бериллия даже с наиболее электроотрицательными элементами (кислород, фтором) обладает высокой долей ковалентности. Химия водных растворов бериллия также имеет свою специфику: в первой координационной сфере бериллия могут находиться лишь четыре лиганда ([Be(H2O)4] 2+ , (Bе(OH)4] — ), что связано с малым ионным радиусом металла и отсутствием d-орбиталей.
Щелочноземельные металлы (Са, Sr, Ва, Ra) образуют единое семейство элементов, в пределах которого некоторые свойства (энергия гидратации, растворимость и термическая устойчивость солей) меняются монотонно с увеличением ионного радиуса, а многие их соединения являются изоморфными.
Элементы IIIA группы
Элементы IIIA группы: бор В, алюминий Al, галлий Ga, индий In и таллий Tl — имеют мало стабильных изотопов, что характерно для атомов с нечетными порядковыми номерами. Электронная конфигурация внешнего энергетического уровня в основном состоянии ns 2 nр 1 характеризуется наличием одного неспаренного электрона. В возбужденном состоянии элементы IIIA группы содержат три неспаренных электрона, которые, находясь в sp 2 -гибридизации, принимают участие в образовании трех ковалентных связей. При этом у атомов остается одна незанятая орбиталь. Поэтому многие ковалентные соединения элементов IIIA группы являются акцепторами электронной пары (кислоты Льюиса), т.е. могут образовывать четвертую ковалентную связь по донорно-акцепторному механизму, создавая которую, они изменяют геометрию своего окружения — она из плоской становится тетраэдрической (состояние sp 3 -гибридизации). Бор сильно отличается по свойствам от других элементов IIIA группы. Он является единственным неметаллом, химически инертен и образует ковалентные связи со фтором, азотом, углеродом и т.д. Химия бора более близка химии кремния, в этом проявляется Диагональное сходство. У атомов алюминия и его тяжелых аналогов появляются вакантные d-орбитали, возрастает радиус атома. Галлий, индий и таллий расположены в Периодической системе сразу за металлами d-блока, поэтому их часто называют постпереходными элементами. Заполнение d-оболочки сопровождается последовательным сжатием атомов, в 3d-pяду оно оказывается настолько сильным, что нивелирует возрастание радиуса при появлении четвертого энергетического уровня. В результате d-сжатия ионные радиусы алюминия и галлия близки, а атомный радиус галлия даже меньше, чем алюминия.
Для таллия, свинца, висмута и полония наиболее устойчивы соединения со степенью окисления +1, +2, +3, +4 соответственно.
| Свойство | B | Al | Ga | In | Tl |
| Заряд ядра Z | 5 | 13 | 31 | 49 | 81 |
| Электронная конфигурация в основном состоянии | [He]2s 2 2p 1 | [Ne]3s 2 3p 1 | [Ar]3d 10 4s 2 4p 1 | [Kr]4d 10 5s 2 5p 1 | [Xe]4f 14 5d 10 6s 2 6p 1 |
| Атомный радиус, нм | 0,083 | 0,143 | 0,122 | 0,163 | 0,170 |
| Энергия ионизации, кДж/моль: I1 I2 I3 | 801 2427 3660 | 577 1817 2745 | 579 1979 2963 | 558 1821 2704 | 589 1971 2878 |
| Электроотрицательность | 2,04 | 1,61 | 1,81 | 1,78 | 2,04 |
Для соединений элементов IIIA группы наиболее характерна степень окисления +3. В ряду бор-алюминий-галлий-индий-таллий устойчивость таких соединений уменьшается, а устойчивость соединений со степенью окисления +1, напротив, увеличивается. Энергия связи М—Hal в галогенидах последних при переходе от легких к более тяжелым элементам М уменьшаются, амфотерные свойства оксидов и гидроксидов смещаются в сторону большей основности, склонность катионов к гидролизу (взаимодействию с водой) ослабевает.
Химия индия и особенно галлия вообще очень близка химии алюминия. Соединения этих металлов в низших степенях окисления (Ga2O, Ga2S, InCl и др.) в водных растворах диспропорционируют. Для таллия состояние +1, напротив, является наиболее устойчивым из-за инертности электронной пары 6s 2 .
2.2.2. Химические свойства металлов IIA группы.
IIA группа содержит только металлы – Be (бериллий), Mg (магний), Ca (кальций), Sr (стронций), Ba (барий) и Ra (радий). Химические свойства первого представителя этой группы — бериллия — наиболее сильно отличаются от химических свойств остальных элементов данной группы. Его химические свойства во многом даже более схожи с алюминием, чем с остальными металлами IIA группы (так называемое «диагональное сходство»). Магний же по химическим свойствами тоже заметно отличается от Ca, Sr, Ba и Ra, но все же имеет с ними намного больше сходных химических свойств, чем с бериллием. В связи со значительным сходством химических свойств кальция, стронция, бария и радия их объединяют в одно семейство, называемое щелочноземельными металлами.
Все элементы IIA группы относятся к s-элементам, т.е. содержат все свои валентные электроны на s-подуровне. Таким образом, электронная конфигурация внешнего электронного слоя всех химических элементов данной группы имеет вид ns 2 , где n – номер периода, в котором находится элемент.
Вследствие особенностей электронного строения металлов IIA группы, данные элементы, помимо нуля, способны иметь только одну единственную степень окисления, равную +2. Простые вещества, образованные элементами IIA группы, при участии в любых химических реакциях способны только окисляться, т.е. отдавать электроны:
Ме 0 – 2e — → Ме +2
Кальций, стронций, барий и радий обладают крайне высокой химической активностью. Простые вещества, образованные ими, являются очень сильными восстановителями. Также сильным восстановителем является магний. Восстановительная активность металлов подчиняется общим закономерностям периодического закона Д.И. Менделеева и увеличивается вниз по подгруппе.
Взаимодействие с простыми веществами
с кислородом
Без нагревания бериллий и магний не реагируют ни с кислородом воздуха, ни с чистым кислородом ввиду того, что покрыты тонкими защитными пленками, состоящими соответственно из оксидов BeO и MgO. Их хранение не требует каких-либо особых способов защиты от воздуха и влаги, в отличие от щелочноземельных металлов, которые хранят под слоем инертной по отношению к ним жидкости, чаще всего керосина.
Be, Mg, Ca, Sr при горении в кислороде образуют оксиды состава MeO, а Ba – смесь оксида бария (BaO) и пероксида бария (BaO2):
Следует отметить, что при горении щелочноземельных металлов и магния на воздухе побочно протекает также реакция этих металлов с азотом воздуха, в результате которой, помимо соединений металлов с кислородом, образуются также нитриды c общей формулой Me3N2.
с галогенами
Бериллий реагирует с галогенами только при высоких температурах, а остальные металлы IIA группы — уже при комнатной температуре:
с неметаллами IV–VI групп
Все металлы IIA группы реагируют при нагревании со всеми неметаллами IV–VI групп, но в зависимости от положения металла в группе, а также активности неметаллов требуется различная степень нагрева. Поскольку бериллий является среди всех металлов IIA группы наиболее химически инертным, при проведении его реакций с неметаллами требуется существенно большая температура.
Следует отметить, что при реакции металлов с углеродом могут образовываться карбиды разной природы. Различают карбиды, относящиеся к метанидам и условно считающимися производными метана, в котором все атомы водорода замещены на металл. Они так же, как и метан, содержат углерод в степени окисления -4, и при их гидролизе или взаимодействии с кислотами-неокислителями одним из продуктов является метан. Также существует другой тип карбидов – ацетилениды, которые содержат ион C2 2- , фактически являющийся фрагментом молекулы ацетилена. Карбиды типа ацетиленидов при гидролизе или взаимодействии с кислотами-неокислителями образуют ацетилен как один из продуктов реакции. То, какой тип карбида – метанид или ацетиленид — получится при взаимодействии того или иного металла с углеродом, зависит от размера катиона металла. С ионами металлов, обладающих малым значением радиуса, образуются, как правило, метаниды, с ионами более крупного размера – ацетилениды. В случае металлов второй группы метанид получается при взаимодействии бериллия с углеродом:
Остальные металлы II А группы образуют с углеродом ацетилениды:
С кремнием металлы IIA группы образуют силициды — соединения вида Me2Si, с азотом – нитриды (Me3N2), фосфором – фосфиды (Me3P2):
с водородом
Все щелочноземельные металлы реагируют при нагревании с водородом. Для того чтобы магний прореагировал с водородом, одного нагрева, как в случае со щелочноземельными металлами, недостаточно, требуется, помимо высокой температуры, также и повышенное давление водорода. Бериллий не реагирует с водородом ни при каких условиях.
Взаимодействие со сложными веществами
с водой
Все щелочноземельные металлы активно реагируют с водой с образованием щелочей (растворимых гидроксидов металлов) и водорода. Магний реагирует с водой лишь при кипячении вследствие того, что при нагревании в воде растворяется защитная оксидная пленка MgO. В случае бериллия защитная оксидная пленка очень стойкая: с ним вода не реагирует ни при кипячении, ни даже при температуре красного каления:
c кислотами-неокислителями
Все металлы главной подгруппы II группы реагируют с кислотами-неокислителями, поскольку находятся в ряду активности левее водорода. При этом образуются соль соответствующей кислоты и водород. Примеры реакций:
c кислотами-окислителями
− разбавленной азотной кислотой
С разбавленной азотной кислотой реагируют все металлы IIA группы. При этом продуктами восстановления вместо водорода (как в случае кислот-неокислителей) являются оксиды азота, преимущественно оксид азота (I) (N2O), а в случае сильно разбавленной азотной кислоты – нитрат аммония (NH4NO3):
− концентрированной азотной кислотой
Концентрированная азотная кислота при обычной (или низкой) температуре пассивирует бериллий, т.е. в реакцию с ним не вступает. При кипячении реакция возможна и протекает преимущественно в соответствии с уравнением:
Магний и щелочноземельные металлы реагируют с концентрированной азотной кислотой с образованием большого спектра различных продуктов восстановления азота.
− концентрированной серной кислотой
Бериллий пассивируется концентрированной серной кислотой, т.е. не реагирует с ней в обычных условиях, однако реакция протекает при кипячении и приводит к образованию сульфата бериллия, диоксида серы и воды:
Барий также пассивируется концентрированной серной кислотой вследствие образования нерастворимого сульфата бария, но реагирует с ней при нагревании, сульфат бария растворяется при нагревании в концентрированной серной кислоте благодаря его превращению в гидросульфат бария.
Остальные металлы главной IIA группы реагируют с концентрированной серной кислотой при любых условиях, в том числе на холоду. Восстановление серы происходит преимущественно до сероводорода:
с щелочами
Магний и щелочноземельные металлы со щелочами не взаимодействуют, а бериллий легко реагирует как растворами щелочей, так и с безводными щелочами при сплавлении. При этом при осуществлении реакции в водном растворе в реакции участвует также и вода, а продуктами являются тетрагидроксобериллаты щелочных или щелочноземельных металлов и газообразный водород:
При осуществлении реакции с твердой щелочью при сплавлении образуются бериллаты щелочных или щелочноземельных металлов и водород
с оксидами
Щелочноземельные металлы, а также магний могут восстанавливать менее активные металлы и некоторые неметаллы из их оксидов при нагревании, например:
Метод восстановления металлов из их оксидов магнием называют магниетермией.
Читайте также: