Число атомов металла в соли
Обновлено: 07.07.2024
1. Ознакомить студентов с основными химическими законами и единицами массы.
2. С помощью математической обработки подученных студентами экспериментальных данных сделать вывод о названии металла, данного для работы и его положении в периодической таблице Д.И. Менделеева.
ОСНОВНЫЕ ПОНЯТИЯ
Вспомним основные частицы вещества:
Молекула – наименьшая частица вещества, обладающая его химическими свойствами и состоящая из атомов. Атом – наименьшая частица элемента, обладающая его химическими свойствами. Химический элемент можно определить как вид атомов, характеризующийся определенной совокупностью свойств.
Простейшим примером сказанному может служить молекула хлористого водорода ( HCl ). Водород и хлор, вступая в реакцию, теряют свои свойства, характерные для газообразных Н2 и Cl2, поэтому считается, что в состав хлористого водорода входят элементы – водород и хлор.
Масса атомов и молекул выражается в атомных единицах массы (а.е.м.), принятых в 1961 г. За одну атомную единицу массы принимается 1/12 часть массы атома изотопа углерода 12 С. Таким образом, масса атома или молекулы любого вещества представляется относительной величиной, показывающей, во сколько раз масса данного атома (молекулы) тяжелее выбранной атомной единицы массы.
Так, относительная атомная масса цинка (Ar) равна 65.38 а.е.м., относительная молекулярная масса воды (Mr) равна 1,008 ∙ 2 + 15,9994 = 18,0154 а.е.м. и т.д.
Однако при решении задач и в расчетах по уравнениям реакций гораздо чаще пользуются понятием «моль».
Моль – это количество вещества, содержащее столько молекул, атомов, ионов, электронов или других структурных единиц, сколько содержится атомов в 12 граммах изотопа углерода 12 C.
Применяя слово «моль», необходимо в каждом случае точно указывать, какие единицы входят в данное вещество. Существует понятия «моль атомов», «моль молекул» и т.д. Масса одного моля взятого вещества называется его молярной массой. Она выражается в г/моль.
Числовое значение молярной массы вещества в г/моль равно относительной молекулярной массе Mr, если вещество состоит из молекул, или относительной атомной массе Ar, если вещество состоит из атомов. Например, молярная масса атомарного кислорода равна ~16 г/моль, молекулярного кислорода ~32 г/моль.
Моль любого вещества содержит совершенно одинаковое количество структурных единиц. Это число называет числом Авогадро, его значение принимают равным 6,02·10 23 .
Часто в химических расчетах используется понятие эквивалента.
Эквивалентом вещества называется такое его количество, которое соединяется без остатка с 1 молем атомов водорода или замещает то же количество атомов водорода в химических реакциях.
Например, в соединениях HCl, H2S и NH3 эквивалент элементов хлора, серы и азота соответственно равен 1 моль, ½ моля и 1/3 моля. Масса одного эквивалента называется его эквивалентной массой или молярной массой эквивалента.Выражается в г/моль.
Так, в приведенных примерах эквивалентные массы хлора, серы и азота легко подсчитать, используя атомные массы этих элементов, они соответственно равны mэ(Cl) = 35,5 г/моль; mэ(S) = 32:2 = 16 г/моль; mэ(N) = 14:3 = 4,7 г/моль. Из разобранных примеров видно, что эквивалентная масса элемента находится из соотношения
Эквивалентная масса или .
Понятие об эквивалентах и эквивалентных массах распространяется также на сложные вещества. Эквивалентом сложного вещества называется такое его количество, которое взаимодействует без остатка с одним эквивалентом водорода или вообще с одним эквивалентом любого другого вещества.
1. Эквивалентная масса оксида складывается из значений эквивалентных масс, составляющих оксид элементов.
а) Эквивалентные массы металла и кислорода в оксиде ZnO, соответственно, равны половине молярных масс атомов:
б) Валентность серы в оксиде SO3 равна 6, следовательно
2. Эквивалентная масса кислоты равна её молярной массе, деленной на основность кислоты (число атомов водорода в молекуле кислоты).
а) Молярная масса HNO3 равна 63 г/моль. Кислота одноосновная, следовательно .
б) Молярная масса H3PO4 равна 98 г/моль. Основность равна 3.
3. Эквивалентная масса основания равна его молярной массе, деленной на валентность металла, образующего основание.
Молярная масса Mg(OH)2 равна 58 г/моль, валентность цинка 2. .
4. Эквивалентная масса соли равна отношению её молярной массы к произведению валентности металла на число его атомов в молекуле.
а) Молярная масса Na2CO3 равна 106 г/моль. Валентность металла I, число его атомов 2.
5. Эквиваленты одних и тех же сложных веществ и их эквивалентные массы могут иметь различные значения, если их рассматривать не как отдельные вещества, а составные части химических реакций, в которых они участвуют.
| H2CO3 + 2NaOH = Na2CO3 + 2H2O | (1) |
| H2CO3 + NaOH = NaHСO3 + H2O | (2) |
эквивалент H2CO3 и его масса зависит от количества атомов водорода, участвующих в реакции и соответственно равны:
| , – по уравнению (1); | (1) |
| , – по уравнению (2); | (2) |
| Cr(OH)3 + 2HCl = CrOHCl2 + 2H2O; | (3) |
| Cr(OH)3 + 3HCl = CrCl3 + 3H2O; | (4) |
| , – по уравнению (3); | (3) |
т.к. в реакции было замещено только две гидроксидных группы на кислотный остаток.
| , – по уравнению (4); | (4) |
т.к. произошло замещение всех трех гидроксогрупп.
Известно несколько способов определения эквивалента.
I. Прямое или непосредственное определение эквивалента из соединения элементов с водородом или кислородом.
Пример 1. Рассчитать эквивалент железа в его оксиде FeO.
Эквивалент кислорода по определению равен ½ моля атомов, эквивалентная масса кислорода равна 16 : 2 = 8 г/моль. В данном соединении на ½ моля атомов кислорода приходится столько же, т.е. ½ моля атомов железа. Следовательно, эквивалент железа в данном оксиде равен ½ моля, а его эквивалентная масса 56 : 2 = 28 г/моль.
II. Определение эквивалента с помощью закона эквивалентов.
Закон эквивалентов (эквивалентных масс), предложенный в 1803-1814 гг. Дальтоном и Рихтером: Элементы и вещества соединяются друг с другом, а также замещают друг друга, в химических реакциях в строго определенных весовых количествах, прямо пропорциональных их эквивалентам.
Математическая запись закона такова:
где m1 и m2 – массы взаимодействующих элементов или веществ, г;
mЭ1 и mЭ2 – соответственно эквивалентные массы этих веществ, г/моль.
Пример 2. Определить эквивалентную и молярную массы 3-валентного металла, зная, что 0,52 г его при окислении образуют 0,98 г оксида.
Решение. В соответствии с законом эквивалентов
Массу кислорода определим по разности масс оксида и металла
mO = 0,98 – 0,52 = 0,46 г.
Эквивалентная масса кислорода известна, она равна 8 г/моль.
Т.к. валентность металла равна 3, то его молярная масса
Пример 3. Вычислить эквивалентную массу металла, если в его хлориде массовая доля хлора 79,78 %, эквивалентная масса хлора равна 53,45 г/моль.
Решение. Массовая доля w металла в хлориде равна
w = 100 - 79,78 = 20,22 %.
Согласно закону эквивалентов, отношение массы металла и массы хлора в соединении должно быть равно отношению их эквивалентных масс
Пример 4. Определите молярную массу двух валентного металла, если 14,2 г оксида этого металла образуют 30,2 г сульфата металла.
Эквивалентная масса сульфата металла равна .
Согласно закону эквивалентов
Т.к. валентность металла равна 2, то его молярная масса равна:
A = 27,5 · 2 = 55 г/моль.
III. Если в химической реакции одно из участвующих веществ находится в газообразном состоянии, то запись закона эквивалентов выражается формулой
где соответственно m(Me) и mэ(Me) – масса металла и его эквивалентная масса, а V и Vэ - объем вступившего в реакцию газа и объем эквивалентной массы этого газа.
Для расчета объемов реагирующих газов необходимо знание Закона Авогадро и его следствий.
Закон Авогадро (1911): В равных объемах различных газов при постоянных температуре и давлении содержится одинаковое число молекул.
Следствия из закона Авогадро:
1. Один моль любого газа при нормальных условиях (н.у.) –температура 0 ºС и давление 760 мм.рт.ст. занимает один и тот же объем равный 22,4 литра. Этот объем называют – молярным объемом газа VМ = 22,4 л/моль.
2. Один моль любого газа содержит одно и то же число молекул, а именно NA = 6,02 · 10 23 моль -1 .
3. Относительная плотность одного газа по другому равна отношению их молярных (M) или относительных молекулярных масс
На основании этих следствий можно рассчитать количество вещества
Пример 5. Рассчитать массу 3 л хлора, взятого при н.у.
Решение. Т.к. молярная масса хлора (Cl2) равна 35,5 ∙ 2 = 71 г/моль то из соотношения (IV) легко найти массу искомого объема
Пример 6. Сколько молей и сколько молекул содержится в 2,2 г углекислого газа? Какой объем они занимают при н.у.?
Решение. Т.к. молярная масса углекислого газа (СО2) равна 44 г/моль, то
Найдем объем газа при н.у.
Пример 7. Определите массу молекулы газа, если масса 2 л газа (н.у.) равна 0,357 г.
Решение. Исходя из молярного объема газа определим молярную массу газа
Число молекул в 1 моль любого вещества равно постоянной Авогадро. Следовательно, масса молекул газа (m) равна
Первое следствие из закона Авогадро позволяет рассчитать объемы эквивалентных масс различных газов:
Так, если эквивалентная масса водорода равна 1,008 г/моль, то её объем равен
Подобным образом находится объем эквивалентной массы кислорода, который оказывается равным
Пример 8. При растворении 0,506 г металла в серной кислоте выделилось 100,8 мл водорода, измеренного при н.у. Определить эквивалентную массу металла.
Задачу можно решить двумя способами:
а) прямой подстановкой данных в формулу (II).
б) используя формулу (I), откуда
, где mэ(H) = 1,008 г/ моль.
Для решения задачи в этом случае надо найти m(H2). Согласно следствию из закона Авогадро
Теперь найденное значение m(H2) подставим в формулу (I)
Значения эквивалентных масс позволяют определить атомную массу металлов по формуле:
A = тэ · В, (V)
где В – валентность металла
А – его атомная масса, в г/моль.
Если же валентность металла неизвестна, то атомную массу можно определить через удельную теплоемкость. В данных расчетах используется правило Дюлонга и Пти: Произведение удельной теплоемкости простого твердого вещества на его атомную массу для большинства элементов приблизительно одинаково. Полученная величина имеет среднее значение, равное 26,8 Дж/моль·К (6,3 кал/моль·град). Она носит название атомной теплоемкости металлов (СА) и представляет собой количество тепла, необходимого для нагревания 1 моля атомов металла на один Кельвин. Математически это правило имеет вид
| СА = А · С ~ 26,8 Дж/моль·К | (VI) |
где С – удельная теплоемкость металла, Дж/г·К;
А – атомная масса взятого металла, г/моль.
Под удельной теплоемкостью понимается то количество тепла, которое необходимо затратить для нагревания 1 г вещества на 1 Кельвин.
Пример 9. При окислении 0,16 г металла образовалось 0,223 г оксида. Вычислить точную атомную массу металла, зная, что удельная теплоемкость 0,635 Дж/г·К.
Решение. По правилу Дюлонга и Пти найдем приближенное значение атомной массы данного металла
По формуле (1) найдем эквивалентную массу этого металла. Масса кислорода 0,223 г. – 0,16 г. = 0,063 г.
Зная приближенную атомную массу металла и его эквивалентнуюмассу, можно найти валентность этого металла.
Способы определения молекулярной формулы соли, если известна степень окисления металла
Задача 114.
В 20 г сульфата некоторого металла содержится 4,5 г атомов серы. Определите формулу соли, если известно, что металл проявляет в этом соединении степень окисления (+1).
Дано: масса образца сульфата некоторого металла: m(соли) = 20 г; масса серы в образце: m(S) = 4,5 г; степень окисления неизвестного металла: +1.
Найти: формулу сульфата.
Решение:
Для идентификации металла необходимо определить его молярную массу. Здесь возможны 2 способа решения.
I способ (последовательно-разветвленный алгоритм).
Схематично алгоритм данного способа можно записать следующим образом:
Применим предложенный алгоритм.
1) m(S) → m (SО 4 ) 2–
По степени окисления металла в сульфате определяем общую формулу искомого вещества Ме 2+ (SO4) 2– . В кислотном остатке серной кислоты (SО4) 2– соотношение атомов строго определено уже известными индексами. Поэтому мы легко сможем определить массу кислотного остатка в 20 г сульфата металла по массе серы:
М(SО4) 2– = М(S) . 1 + М(О) . 4 = 32 . 1 + 16 . 4 = 96 г/моль.
Масса 1 моль кислотного остатка (SО 4 ) 2– составляет 96 г 1 .
вклад серы в 96 г ионов (SО 4 ) 2– составляет 32 г (по молярной массе)
вклад серы в х г ионов (SО 4 ) 2– составляет 4,5 г (по условию)
2) m (SО 4 ) 2– → n (SО 4 ) 2–
Находим количество вещества ионов (SО 4 ) 2–
3) n (SО 4 ) 2– → n(Me + )
Находим количество вещества ионов Ме + , соответствующее содержанию ионов кислотного остатка n (SО 4 ) 2– = 0,141 моль. Используя формулу Ме2 + (SО 4 ) 2– , составим пропорцию:
на 2 моль ионов Ме + приходится 1 моль ионов (SО 4 ) 2– (по индексам в формуле)
на х моль ионов Ме + , приходится 0,141 моль ионов (SО 4 ) 2– (по условию)
4) m (SО 4 ) 2– → m(Me) +
Находим массу металла в 20 г соли Ме2SО4.
m(Ме + ) = m Ме2 + (SО 4 ) 2– – m (SО 4 ) 2– = 20 – 13,5 = 6,5 г.
5) Находим молярную массу атомов металла
В данном случае молярную массу ионов металла можно приравнять к молярной массе незаряженных атомов:
М(Ме + ) = М(Ме) = 23 г/моль.
По таблице Д.И. Менделеева находим элемент, имеющий молярную массу 23г/моль. Подходит натрий. Этот элемент действительно проявляет степень окисления (+1) и образует сульфат Nа2SО4.
II способ (встречный алгоритм).
Применим данный алгоритм.
1) По степени окисления металла в сульфате определяем общую формулу искомого вещества Ме2 + (SО 4 ) 2–
2) По массе серы в образце определяем ее количество вещества:
3) По записи формулы сульфата Ме2 + моль ионов Ме + содержится в 20 г соли Ме2SO4 видно, что количество вещества серы равно количеству вещества соли:
n(S) = nМе2 + (SО 4 ) 2– . = 0,141 моль.
4) По значениям количества вещества и массы образца сульфата определяем значение молярной массы соли:
5) Записываем выражение для определения молярной массы для сульфата металла, исходя из значений молярных масс элементов:
М(Ме2 + (SО 4 ) 2– ) = М(Ме) . 2 + М(S) . 1 + М(О) . 4 =
= М(Ме) . 2 + 32 . 1 + 16 . 4 = [М(Ме) . 2 + 96] г/моль.
6) Приравниваем полученное выражение к значению молярной массы соли, полученному в четвертом действии:
М(Ме) . 2 + 96 = 142.
Получили одно математическое уравнение с одним неизвестным. Его решение дает нам молярную массу искомого металла: М(Ме) = 23 г/моль.
По таблице Д. И. Менделеева находим элемент, имеющий молярную массу 23 г/моль. Подходит натрий. Этот элемент действительно проявляет степень окисления (+1) и образует сульфат Nа2SО4.
III способ (встречный алгоритм).
Графический алгоритм данного способа будет следующим:
1) По степени окисления металла в сульфате определяем общую формулу искомого вещества Ме2+ (SО 4 ) 2– . Записываем значение молярной массы для этого вещества:
М(Ме2+ (SО 4 ) 2– ) = М(Ме) . 2 + М(S) . 1 + М(О) . 4 =
= М(Ме) . 2 + 32 . 1 + 64 . 4 = (М(Ме) . 2 + 96) г/моль.
Вклад серы в общую массу 1 моль Ме2 + (SО 4 ) 2– составляет:
М(S) . 1 = 32 . 1 = 32 г.
Выбираем в качестве образца массу 1 моль Ме2 + (SО 4 ) 2– :
M(Ме2 + (SО 4 ) 2– ) = (М(Ме) . 2 + 96) г
Масса серы в этом выбранном образце: m(S) = 32 г.
2) Составляем пропорцию:
(М(Ме) . 2 + 96) г Ме2 + (SО 4 ) 2– содержит 32 г (S) (по молярной массе)
20 г Ме2+ (SО 4 ) 2– содержит 4,5 г (S) (по условию)
3) Из пропорции получаем уравнение с одним неизвестным:
(M(Ме) . 2 + 96) . 4,5 = 20 . 32
4) Решая уравнение, получаем значение молярной массы искомого металла:
По таблице Д.И. Менделеева находим элемент, имеющий молярную массу 23,1 г/моль. Подходит натрий. Этот элемент действительно проявляет степень окисления (+1) и образует сульфат Nа2SО4.
Ответ: Nа2SО4.
Комментарии:
1 Молярную массу любых ионов можно считать точно так, как и молярную массу нейтральных частиц. Молярная масса любого иона отличается от молярной массы такой же незаряженной частицы на массу нескольких электронов. Если заряд иона «+n», то М(иона) < М(незаряженной частицы) на массу n электронов, если заряд иона «-n», то M(иона) > М(незаряженной частицы) на массу n электронов. Так как масса электрона значительно меньше (в 1840 раз) массы даже самого легкого атома водорода, не говоря уже о более тяжелых атомах других металлов, то массой электронов при подсчете молярной массы можно пренебречь и считать условно, что M(иона) = М(незаряженной частицы).
Закон эквивалентов – для молекулярных соединений количество составляющих элементов пропорционально их химическим эквивалентам
1. Все вещества состоят из молекул. Молекула – наименьшая частица вещества, обладающая его химическими свойствами.
2. Молекулы состоят из атомов. Атом – наименьшая частица элемента в химических соединениях. Разным элементам соответствуют разные атомы.
3. Молекулы и атомы находятся в непрерывном движении.
4. При химических реакциях молекулы одних веществ превращаются в молекулы других веществ. Атомы при химических реакциях не изменяются.
Развитие методов химического анализа позволило определять соотношение элементов в соединениях.
Закон постоянства состава: все соединения содержат элементы в строго определенных весовых пропорциях, независимо от способа получения (Ж. Пруст, 1801-1808 гг.). Так, например, сернистый газ, полученный сжиганием серы, или действием кислот на сульфиты, или любым другим способом, всегда содержит 1 весовую часть серы и 1 весовую часть кислорода.
Эквивалент (Э)– частица вещества, которая в данной кислотно-основной реакции эквивалентна одному иону водорода или в данной окислительно-восстановительной реакции одному электрону.
Э = 1 / z (моль)
где z – степень окисления или число электронов, перешедших от восстановителя к окислителю.
Так, в Н2О и NН3 с 1 моль атомов водорода соединяется соответственно ½ моль атомов кислорода и ⅓ моль атомов азота, и следовательно эквивалент кислорода и азота равны ½ и ⅓ моля.
Масса 1 моля эквивалента вещества называется молярной массой эквивалента или эквивалентной массой (mЭ)и равна мольной массе его атомов (М), деленной на валентность элемента (В) в данном соединении:
mЭ = М ∙ Э или mЭ = М / В (г/моль)
Так, эквивалентная масса кислорода и азота в Н2О и NН3, соответственно, вычисляются исходя из молярных масс элементов: кислорода 16∙½ = 8 г/моль и азота 14∙⅓ = 4,67 г/моль.
Эквивалент кислоты = 1 / основность (число атомов водорода);
Эквивалент основания = 1 / кислотность (число гидроксильных групп);
Эквивалент соли = 1 / валентность металла в соли · число атомов металла.
Эквивалент оксида = 1 / валентность металла · число атомов металла;
Эквивалентная масса кислоты = М (кислоты) / основность (кислоты);
Эквивалентная масса основания = М (основания) / кислотность (основания);
Эквивалентная масса оксида = М (оксида) / валентность металла · число атомов металла;
Эквивалентная масса соли = М (соли) / валентность металла в соли · число атомов металла.
Согласно закону эквивалентов: массы (объемы) реагирующих веществ пропорциональны их эквивалентным массам (объемам):
Закон кратных отношений: весовые доли любого из элементов в соединениях относятся друг к другу как небольшие целые числа (Д. Дальтон, 1808 г.) Из этого закона следует,что атомыэлементов соединяются в молекулы, причем молекулы содержат небольшое число атомов.
Важнейшим открытием атомно-молекулярной теории стал закон сохранения массы, который был сформулирован великим ученым М.В. Ломоносовым (1748 г.), подтвержден экспериментально им самим (1756 г.) и позже А.‑Л. Лавуазье (1789 г.).
Закон сохранения массы: масса всех веществ, вступающих в химическую реакцию, равна массе всех продуктов реакции.
Данный закон подтвердил, что атомы являются неделимыми и при химических реакциях не изменяются. Молекулы при реакции обмениваются атомами, но общее число атомов каждого вида не изменяется, и поэтому общая масса веществ в процессе реакции сохраняется.
Закон сохранения массы является частным случаем общего закона природы – закона сохранения энергии: энергия изолированной системы постоянна. Энергия – это мера движения и взаимодействия различных видов материи. При любых процессах в изолированной системе энергия не производится и не уничтожается, она может только переходить из одной формы в другую.
Одной из форм энергии является так называемая энергия покоя, которая связана с массой соотношением Эйнштейна: Е0 = m0 ∙ с 2 ,где с – скорость света в вакууме (с = 3∙10 8 м/с). Это соотношение показывает, что масса может переходить в энергию и наоборот. Именно это и происходит во всех ядерных реакциях, и поэтому закон сохранения массы в ядерных процессах нарушается. Однако, закон сохранения энергии остается справедливым и в этом случае, если учитывать энергию покоя.
В химических реакциях изменение массы, вызванное выделением или поглощением энергии, очень мало и изменение массы невозможно зарегистрировать экспериментально, поэтому можно утверждать, что в химических реакциях закон сохранения массы выполняется практически точно.
Металлы в растворе собственной соли.
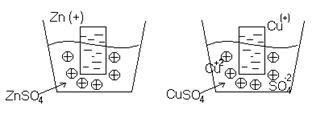
Количество ионов, которые будут взаимодействовать с раствором соли, будет меньше, т.к. соль уже содержит некоторое количество ионов этого металла.
Т.е. имеет большое значение какой металл и какая концентрация металла в соли, поведение металла.
Например: медь из раствора соли перейдет в электрод, т.е. имеются в виду положительные ионы.
Гальванический элемент – любое устройство, позволяющее получать электрический ток, за счет протекания химических реакций.
Гальваническая цепь – последовательная совокупность скачков потенциала на границе раздела фаз.
Максимальная разность потенциалов, отвечающая обратимому протеканию химической реакции – ЭДС (Е)
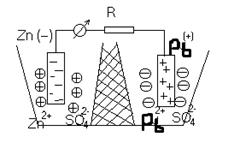 |
Каждые два металла, будучи погруженными в растворы их солей, которые сообщаются между собой посредством сифона, заполненного электролитом, образуют гальванический элемент. Пластинки металлов, погруженные в растворы, называются электродами элемента.
Если соединить наружные концы электродов (полюсы элемента) проволокой, то от металла, у которого величина потенциала меньше, начинают перемещаться электроны к металлу, у которого она больше (например, от Zn к Pb). Уход электронов нарушает равновесие, существующее между металлом и его ионами в растворе, и вызывает переход в раствор нового количества ионов – металл постепенно растворяется. В то же время электроны, переходящие к другому металлу, разряжают у его поверхности находящиеся в растворе ионы - металл выделяется из раствора.
Электрод, на котором протекает окисление, называется анодом. Электрод, на котором протекает восстановление, называется катодом.
В свинцово-цинковом элементе цинковый электрод является анодом, а свинцовый – катодом.
Таким образом, в замкнутом гальваническом элементе происходит взаимодействие между металлом и раствором соли другого металла, не соприкасающимися непосредственно друг с другом. Атомы первого металла, отдавая электроны, превращаются в ионы, а ионы второго металла, присоединяя электроны, превращаются в атомы. Первый металл вытесняет второй из раствора его соли. Например, при работе гальванического элемента, составленного из цинка и свинца, погруженных соответственно в растворы Zn(NO3)2 и Pb(NO3)2 у электродов происходят следующие процессы:
Суммируя оба процесса, получаем уравнение Zn + Pb 2+ ↔ Pb + Zn 2+ , выражающее происходящую в элементе реакцию в ионной форме. Молекулярное уравнение той же реакции будет иметь вид:
Электродвижущая сила гальванического элемента равна разности потенциалов двух его электродов. При определении его всегда вычитают из большего потенциала меньший. Например, электродвижущая сила (Э.д.с.) рассмотренного элемента равна:
| Э.д.с. = | -0,13 | – | (-0,76) | = 0,63 v |
| EPb | EZn |
Такую величину она будет иметь при условии, что металлы погружены в растворы, в которых концентрация ионов равна 1 г-ион/л. При других концентрациях растворов величины электродных потенциалов будут несколько иные. Их можно вычислить по формуле:
E = E 0 + (0,058 / n) • lgC уравнение Нернста
или E = E 0 + • lgC
где E - искомый потенциал металла (в вольтах)
E 0 - его нормальный потенциал
n - валентность металла (зарядность иона)
С - концентрация ионов в растворе (г-ион/л)
F – число Фарадея
R – универсальная газовая постоянная
Т – температура по абсолютной шкале
Пример:
Найти электродвижущую силу элемента (э. д. с.) образованного цинковым электродом, опущенным в 0,1 М раствор Zn(NO3)2 и свинцовым электродом, опущенным в 2 М раствор Pb(NO3)2.
Решение:
Вычисляем потенциал цинкового электрода:
EZn = -0,76 + (0,058 / 2) lg 0,1 = -0,76 + 0,029 • (-1) = -0,79 v
Вычисляем потенциал свинцового электрода:
EPb = -0,13 + (0,058 / 2) lg 2 = -0,13 + 0,029 • 0,3010 = -0,12 v
Находим электродвижущую силу элемента:
Э. д. с. = -0,12 – (-0,79) = 0,67 v
Электролиз
Совокупность окислительно-восстановительных реакций, которые протекают на электродах в растворах или расплавах электролитов при пропускании через них электрического тока, называют электролизом.
Сущность электролиза заключается в том, что при пропускании тока через раствор электролита (или расплавленный электролит) положительно заряженные ионы перемещаются к катоду, а отрицательно заряженные – к аноду. Достигнув электродов, ионы разряжаются, в результате чего у электродов выделяются составные части растворенного электролита или водород и кислород из воды.
Для перевода различных ионов в нейтральные атомы или группы атомов требуется различное напряжение электрического тока. Одни ионы легче теряют свои заряды, другие труднее. Степень легкости, с которой разряжаются (присоединяют электроны) ионы металлов, определяется положением металлов в ряду напряжений.
На катоде источника тока происходит процесс передачи электронов катионам из раствора или расплава, поэтому катод является “восстановителем”. На аноде происходит отдача электронов анионами, поэтому анод является “окислителем”.
При электролизе как на аноде, так и на катоде могут происходить конкурирующие процессы.
При проведении электролиза с использованием инертного (нерасходуемого) анода (например, графита или платины), как правило, конкурирующими являются два окислительных и два восстановительных процесса:
на аноде — окисление анионов и гидроксид-ионов,
на катоде — восстановление катионов и ионов водорода.
При проведении электролиза с использованием активного (расходуемого) анода процесс усложняется и конкурирующими реакциями на электродах являются:
на аноде — окисление анионов и гидроксид-ионов, анодное растворение металла — материала анода;
на катоде — восстановление катиона соли и ионов водорода, восстановление катионов металла, полученных при растворении анода.
При выборе наиболее вероятного процесса на аноде и катоде следует исходить из положения, что будет протекать та реакция, для которой требуется наименьшая затрата энергии. При использовании инертных электродов используют следующие правила:
1. На аноде могут образовываться следующие продукты:
а) при электролизе растворов, содержащих в своем составе анионы F - , SO4 2- , NО3 - , РО4 3- (если электролизу подвергается соль кислородсодержащей кислоты или сама кислота, то разряжаются гидроксильные ионы, а не ионы кислородных остатков), а также растворов щелочей выделяется кислород Образующиеся при разряде гидроксильных ионов нейтральные группы ОН - тотчас же разлагаются по уравнению:
4OH- ® 2H2O + O2В результате у анода выделяется кислород.
б) при окислении анионов Сl - , Вr - , I - выделяются соответственно хлор, бром, иод;
в) при окислении анионов органических кислот происходит процесс:
2. При электролизе растворов солей, содержащих ионы, расположенные в ряду напряжений левее Аl 3+ , на катоде выделяется водород; если ион расположен в ряду напряжений правее водорода, то на катоде выделяется металл. Чем левее стоит металл в ряду напряжений, чем больше его отрицательный потенциал (или меньше положительный потенциал), тем труднее при прочих равных условиях разряжаются его ионы (легче всего разряжаются ионы Аu 3+ , Ag + ; труднее всегоLi + , Rb + , K + ).
Если в растворе одновременно находятся ионы нескольких металлов, то в первую очередь разряжаются ионы того металла, у которого отрицательный потенциал меньше (или положительный – больше). Например, из раствора, содержащего ионы Zn 2+ и Cu 2+ , сперва выделяется металлическая медь. Но величина потенциала металла зависит также и от концентрации его ионов в растворе; точно также изменяется и легкость разряда ионов каждого металла в зависимости от их концентрации: увеличение концентрации облегчает разряд ионов, уменьшение – затрудняет. Поэтому при электролизе раствора, содержащего ионы нескольких металлов может случиться, что выделение более активного металла будет происходить раньше, чем выделение менее активного (если концентрация ионов первого металла значительна, а второго – очень мала).
3. При электролизе растворов солей, содержащих ионы, расположенные в ряду напряжений между Al + и Н + , на катоде могут протекать конкурирующие процессы как восстановления катионов, так и выделения водорода. Только при электролизе солей натрия, кальция и других металлов до алюминия включительно разряжаются ионы водорода и выделяется водород.
Рассмотрим в качестве примера электролиз водного раствора хлорида меди на инертных электродах. В растворе находятся ионы Сu 2+ и 2Сl - , которые под действием электрического тока направляются к соответствующим электродам:
На катоде выделяется металлическая медь, на аноде — газообразный хлор.
Если в рассмотренном примере электролиза раствора CuCl2 в качестве анода взять медную пластинку, то на катоде выделяется медь, а на аноде, где происходят процессы окисления, вместо разрядки ионов Сl - и выделения хлора протекает окисление анода (меди). В этом случае происходит растворение самого анода, и в виде ионов Си он переходит в раствор. Электролиз CuCl2 с растворимым анодом можно записать так:
Электролиз растворов солей с растворимым анодом сводится к окислению материала анода (его растворению) и сопровождается переносом металла с анода на катод. Это свойство широко используется при рафинировании (очистке) металлов от загрязнений.
Электролиз раствора хлорида никеля NiCl2
Раствор содержит ионы Ni 2+ и Cl - , а также в ничтожной концентрации ионы Н + и ОН - . При пропускании тока ионы Ni 2+ перемещаются к катоду, а ионы Cl - – к аноду. Принимая от катода по два электрона, ионы Ni 2+ превращаются в нейтральные атомы, выделяющиеся из раствора. Катод постепенно покрывается никелем.
Ионы хлора,достигая анода, отдают ему электроны и превращаются в атомы хлора, которые, соединяясь попарно, образуют молекулы хлора. У анода выделяется хлор.
Таким образом, у катода происходит процесс восстановления, у анода – процесс окисления.
Читайте также:
