Число электронов на внешнем электронном уровне атома металла
Обновлено: 25.06.2024
На этом уроке вы узнаете, как устроена электронная оболочка атома, и сможете объяснить явление периодичности. Познакомитесь с моделями строения электронных оболочек атомов, с помощью которых можно предсказать и объяснить свойства химических элементов и их соединений.
I. Состояние электронов в атоме
Выдающийся датский физик Нильс Бор (Рис. 1) предположил, что электроны в атоме могут двигаться не по любым, а по строго определенным орбитам.
При этом электроны в атоме различаются своей энергией. Как показывают опыты, одни из них притягиваются к ядру сильнее, другие – слабее. Главная причина этого заключается в разном удалении электронов от ядра атома. Чем ближе электроны к ядру, тем они прочнее связаны с ним и их труднее вырвать из электронной оболочки. Таким образом, по мере удаления от ядра атома запас энергии электрона увеличивается.
Электроны, движущиеся вблизи ядра, как бы загораживают (экранируют) ядро от других электронов, которые притягиваются к ядру слабее и движутся на большем удалении от него. Так образуются электронные слои.
Каждый электронный слой состоит из электронов.
Электрон вращается вокруг ядра атома с невообразимой скоростью. Так, за 1 секунду он делает столько оборотов вокруг ядра атома, сколько оборотов делает пропеллер самолета вокруг оси за 5–5,5 лет непрерывной работы двигателя. Пропеллер самолета образует «облако», находящееся в одной плоскости, а электрон образует объемное облако –электронное облако, форма и размер которого зависят от энергии электрона.
Если обозначить точками все вероятные места нахождения электрона в атомном пространстве за некоторое время, то совокупность этих точек будет представлять собойэлектронное облако.
II. Электронное облако
Электронное облако – это модель, которая описывает состояние (движение) электрона в атоме.
Электронное облако не имеет строго очерченных границ и плотность его неравномерна.
Часть атомного пространства, в котором вероятность нахождения электрона наибольшая (~90%), называется орбиталью.
Виды электронных орбиталей
Форма орбитали в пространстве
Количество орбиталей в атоме.
Условное обозначение орбитали – клетка:
(электронное облако s – электрона)
Электронное облако такой формы может занимать в атоме одно положение
(электронное облако p – электрона)
Электронное облако такой формы может занимать в атоме три положения вдоль осей координат пространства x, y и z.
(электронное облако d – электрона)
Все d-орбитали (а их может быть уже пять) одинаковы по энергии, но по-разному расположены в пространстве. Да и по форме, напоминающей перевязанную лентами подушечку, одинаковы только четыре.
А пятая - вроде гантели, продетой в бублик
(электронное облако f – электрона)
Электронное облако такой формы может занимать в атоме семь положений.
Условное обозначение электрона – стрелка , направленная вверх↑ (электрон вращается вокруг собственной оси по часовой стрелке) или стрелка, направленная вниз↓ (электрон вращается вокруг собственной оси против часовой стрелки).
Число электронов в атоме определяют по порядковому номеру
О – 8 электронов, S – 16 электронов.
На одной орбитали могут находиться только ДВА электрона, которые вращаются вокруг своей оси в противоположных направлениях (по часовой стрелке и против часовой стрелке) – электроны с противоположными спинами:
Cледовательно, на s – орбитали максимально может разместиться два электрона (s 2 ); на p – орбитали максимально может разместиться шесть электронов (p 6 ) на d – орбитали максимально может разместиться десять электронов (d 10 ); f – четырнадцать электронов (f 14 ).
Располагаясь на различных расстояниях от ядра, электроны образуют электронные слои (энергетические уровни) – каждому слою соответствует определённый уровень энергии.
Условное обозначение уровня - скобка: )
Число энергетических уровней определяют по номеру периода, в котором находится химический элемент
О – 2 уровня, S – три уровня.

Для элементов главных подгрупп (А) число электронов на внешнем уровне = номеру группы.
+15P – V группа (А) – на внешнем уровне 5 электронов
Для элементов побочных подгрупп (В) число электронов на внешнем уровне = двум.
Исключения (один электрон) – хром, медь, серебро, золото и некоторые другие.
III. Формулы отражающие строение атомов первого и второго периодов
– схема строения атома, отображает распределение электронов по энергоуровням.
+1 Н 1s 1
– электронная формула, отображает число электронов по орбиталям.
- электронно-графическая формула – показывает распределение электронов по орбиталям и отображает спин электрона.


У элементов второго периода начинается заполнение второго энергетического уровня — он включает восемь электронов (n = 2, N = 8). Второй период содержит восемь элементов. У неона, элемента, завершающего второй период, первый и второй энергетические уровни оказываются целиком заполненными.

Американский химик Гилберт Льюис дал объяснение этому и выдвинул правило октета, в соответствии с которым устойчивым является восьмиэлектронный слой (за исключением 1 слоя: т. к. на нем может находиться не более 2 электронов, устойчивым для него будет двухэлектронное состояние).
IV. Распределение электронов по энергетическим уровням элементов третьего и четвертого периодов ПСХЭ
1. Порядок заполнения уровней и подуровней электронами
Электронные формулы атомов химических элементов составляют в следующем порядке:
- Сначала по номеру элемента в таблице Д. И. Менделеева определяют общее число электронов в атоме;
- Затем по номеру периода, в котором расположен элемент, определяют число энергетических уровней;
- Уровни разбивают на подуровни и орбитали, и заполняют их электронами в соответствии Принципом наименьшей энергии
- Для удобства электроны можно распределить по энергетическим уровням, воспользовавшись формулой N=2n2 и с учётом того, что:
- У элементов главных подгрупп (s-;p-элементы) число электронов на внешнем уровне равно номеру группы.
- У элементов побочных подгрупп на внешнем уровне обычно дваэлектрона (исключение составляют атомы Cu,Ag,Au,Cr,Nb,Mo,Ru,Rh, у которых на внешнем уровне один электрон, у Pd на внешнем уровне нольэлектронов);
- Число электронов на предпоследнем уровне равно общему числу электронов в атоме минус число электронов на всех остальных уровнях.
Порядок заполнения электронами атомных орбиталей определяется :
Принципом наименьшей энергии
Шкала энергий:

2. Семейства химических элементов
Элементы, в атомах которых происходит заполнение электронами s-подуровня внешнего энергетического уровня, называются s-элементами. Это первые 2 элемента каждого периода, составляющие главные подгруппы I и II групп.
Элементы, в атомах которых электронами заполняется p-подуровень внешнего энергетического уровня, называются p-элементами. Это последние 6 элементов каждого периода (за исключением I и VII), составляющие главные подгруппы III-VIII групп.
Элементы, в которых заполняется d-подуровень второго снаружи уровня, называются d-элементами. Это элементы вставных декад IV, V, VI периодов.
Элементы, в которых заполняется f-подуровень третьего снаружи уровня, называются f-элементами. К f-элементам относятся лантаноиды и актиноиды.
В третьем периоде происходит заполнение третьего энергетического уровня. Третий уровень (n = 3) может максимально вмещать 18 электронов. Однако элементов в третьем периоде всего восемь. К концу третьего периода (у аргона) полностью заполняются 3s- и 3p-подуровни, а 3d-подуровень остается пустым, поэтому третий уровень не заполняется до конца.

В четвертом периоде у первых двух элементов (калия и кальция) электроны идут на четвертый энергетический уровень (4s-подуровень), а затем у последующих десяти элементов (от скандия до цинка) завершается заполнение третьего энергетического уровня (3d-подуровня).

«Проскок» или «провал» электрона
У атомов Cr, Cu, Nb, Mo, Ru, Rh, Pd, Ag, Pt, Au имеет место «провал» электрона с s-подуровня внешнего слоя на d-подуровень предыдущего слоя, что приводит к энергетически более устойчивому состоянию атома. Например, электронная формула атома меди, исходя из вышенаписанного, должна иметь вид: Cu 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 9 . Однако в действительности один из двух 4s-электронов «проваливается» на 3d-подуровень, и атом меди имеет следующую конфигурацию: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 3d 10 .
Для элементов IБ-подгруппы характерна конфигурация внешнего слоя: ns 1 (n−1)d 10 .
Для элементов Cr и Mo характерна конфигурация внешнего слоя: ns 1 (n−1)d 5 .
Особо следует отметить палладий, у которого «проваливаются» два электрона:
Pd1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 0 4d 10
V. Тест
Решите тестовые задания (один верный вариант ответа).
1. Заряд ядра атома фосфора равен
2. Количество энергоуровней в атоме равно
а) порядковому номеру элемента;
б) номеру группы;
в) заряду ядра атома;
г) номеру периода
3. Число нейтронов в атоме цинка равно
4. В ряду элементов Na, Mg, Al, Cl металлические свойства
в) не изменяются;
г) сначала убывают, а затем возрастают
5. Формула высшего оксида RO2 характерна для
6. Электронная формула строения атома меди, это-
а) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 ;
б) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 9 ;
в) 1s 2 2s 2 2p 6 3s 1 3p 6 4s 2 3d 10 ;
г) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 11 .
7. Заряд ядра атома кальция равен
8. Число электронов на внешнем энергоуровне для элементов главных подгрупп равно
а) номеру периода;
в) порядковому номеру элемента;
г) атомной массе.
9. Число нейтронов в атоме железа равно
10. В ряду элементов C, Si, Ge, Sn способность отдавать валентные электроны
б) не изменяется;
г) сначала увеличивается, а затем уменьшается.
11. Формула летучего водородного соединения для элемента с электронным строением атома 1s22s22p2 – это
Строение атома. Строение электронных оболочек атомов первых 20 элементов Периодической системы Д.И. Менделеева

Атом — электронейтральная частица, состоящая из положительно заряженного ядра и отрицательно заряженных электронов. В центре атома находится положительно заряженное ядро. Оно занимает ничтожную часть пространства внутри атома, в нём сосредоточены весь положительный заряд и почти вся масса атома.
Ядро состоит из элементарных частиц — протона и нейтрона; вокруг атомного ядра по замкнутым орбиталям движутся электроны.
Протон (р) — элементарная частица с относительной массой 1,00728 атомной единицы массы и зарядом +1 условную единицу. Число протонов в атомном ядре равно порядковому номеру элемента в Периодической системе Д.И. Менделеева.
Нейтрон (n) — элементарная нейтральная частица с относительной массой 1,00866 атомной единицы массы (а. е. м.).
Число нейтронов в ядре N определяют по формуле:
где А — массовое число, Z — заряд ядра, равный числу протонов (порядковому номеру).
Обычно параметры ядра атома записывают следующим образом: слева внизу от символа элемента ставят заряд ядра, а вверху — массовое число, например:
Эта запись показывает, что заряд ядра (следовательно, и число протонов) для атома фосфора равен 15, массовое число равно 31, а число нейтронов равно 31 – 15 = 16. Так как массы протона и нейтрона очень мало отличаются друг от друга, то массовое число приблизительно равно относительной атомной массе ядра.
Электрон ( е – ) — элементарная частица с массой 0,00055 а. е. м. и условным зарядом –1. Число электронов в атоме равно заряду ядра атома (порядковому номеру элемента в Периодической системе Д.И. Менделеева).
Электроны движутся вокруг ядра по строго определённым орбиталям, образуя так называемое электронное облако.
Область пространства вокруг атомного ядра, где наиболее (90 и более %) вероятно нахождение электрона, определяет форму электронного облака.
Электронное облако s-электрона имеет сферическую форму; на s-энергетическом подуровне может максимально находиться два электрона.
Электронное облако p-электрона имеет гантелеобразную форму; на трёх p-орбиталях максимально может находиться шесть электронов.
Орбитали изображают в виде квадрата, сверху или снизу которого пишут значения главного и побочного квантовых чисел, описывающих данную орбиталь. Такую запись называют графической электронной формулой, например:
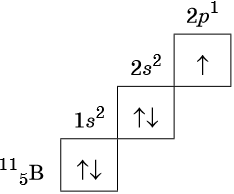
В этой формуле стрелками обозначают электрон, а направление стрелки соответствует направлению спина — собственного магнитного момента электрона. Электроны с противоположными спинами ↑↓ называют спаренными.
Электронные конфигурации атомов элементов можно представить в виде электронных формул, в которых указывают символы подуровня, коэффициент перед символом подуровня показывает его принадлежность к данному уровню, а степень у символа — число электронов данного подуровня.
В таблице 1 приведено строение электронных оболочек атомов первых 20 элементов Периодической системы химических элементов Д.И. Менделеева.
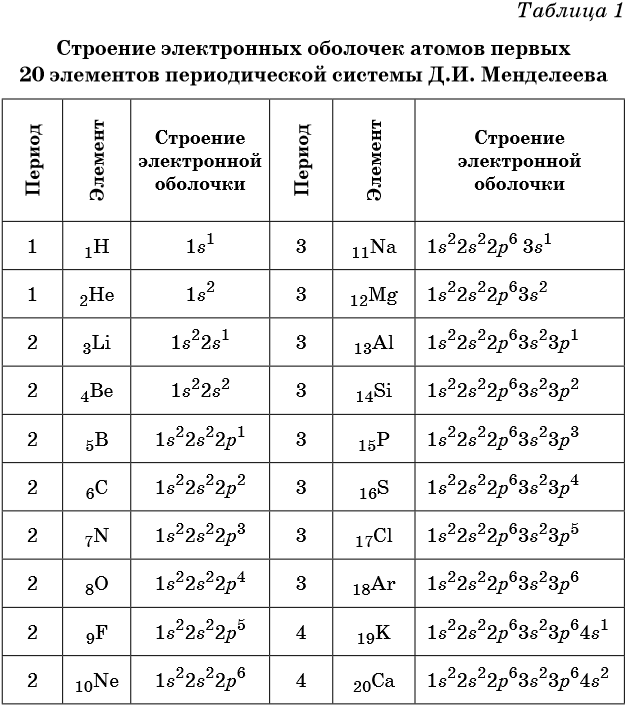
Химические элементы, в атомах которых s-подуровень внешнего уровня пополняется одним или двумя электронами, называют s-элементами. Химические элементы, в атомах которых заполняется p-подуровень (от одного до шести электронов), называют p-элементами.
Число электронных слоёв в атоме химического элемента равно номеру периода.
В соответствии с правилом Хунда электроны располагаются на однотипных орбиталях одного энергетического уровня таким образом, чтобы суммарный спин был максимален. Следовательно, при заполнении энергетического подуровня каждый электрон прежде всего занимает отдельную ячейку, а только после этого начинается их спаривание. Например, у атома азота все p-электроны будут находиться в отдельных ячейках, а у кислорода начнётся их спаривание, которое полностью закончится у неона.
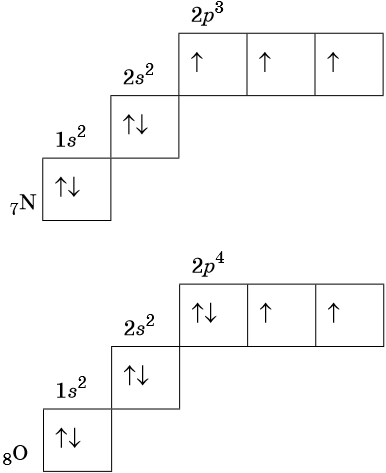
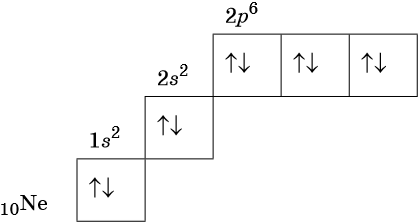
Изотопами называют атомы одного и того же элемента, содержащие в своих ядрах одинаковое число протонов, но различное число нейтронов.
Изотопы известны для всех элементов. Поэтому атомные массы элементов в периодической системе являются средним значением из массовых чисел природных смесей изотопов и отличаются от целочисленных значений. Таким образом, атомная масса природной смеси изотопов не может служить главной характеристикой атома, а следовательно, и элемента. Такой характеристикой атома является заряд ядра, определяющий число электронов в электронной оболочке атома и её строение.
Рассмотрим несколько типовых заданий по этому разделу.
Пример 1. Атом какого элемента имеет электронную конфигурацию 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 ?
На внешнем энергетическом уровне у данного элемента находится один 4s-электрон. Следовательно, этот химический элемент находится в четвёртом периоде первой группе главной подгруппе. Этот элемент — калий.
К этому ответу можно прийти по-другому. Сложив общее количество всех электронов, получим 19. Общее число электронов равно порядковому номеру элемента. Под номером 19 в периодической системе находится калий.
Пример 2. Химическому элементу соответствует высший оксид RO2. Электронной конфигурации внешнего энергетического уровня атома этого элемента соответствует электронная формула:
- ns 2 np 4
- ns 2 np 2
- ns 2 np 3
- ns 2 np 6
По формуле высшего оксида (смотрите на формулы высших оксидов в Периодической системе) устанавливаем, что этот химический элемент находится в четвёртой группе главной подгруппы. У этих элементов на внешнем энергетическом уровне находятся четыре электрона — два s и два p. Следовательно, правильный ответ 2.
Тренировочные задания
1. Общее число s-электронов в атоме кальция равно
2. Число спаренных p-электронов в атоме азота равно
3. Число неспаренных s-электронов в атоме азота равно
4. Число электронов на внешнем энергетическом уровне атома аргона равно
5. Число протонов, нейтронов и электронов в атоме 9 4Be равно
1) 9, 4, 5
2) 4, 5, 4
3) 4, 4, 5
4) 9, 5, 9
6. Распределение электронов по электронным слоям 2; 8; 4 — соответствует атому, расположенному в(во)
1) 3-м периоде, IА группе
2) 2-м периоде, IVА группе
3) 3-м периоде, IVА группе
4) 3-м периоде, VА группе
7. Химическому элементу, расположенному в 3-м периоде VA группе соответствует схема электронного строения атома
1) 2, 8, 6
2) 2, 6, 4
3) 2, 8, 5
4) 2, 8, 2
8. Химический элемент с электронной конфигурацией 1s 2 2s 2 2p 4 образует летучее водородное соединение, формула которого
9. Число электронных слоёв в атоме химического элемента равно
1) его порядковому номеру
2) номеру группы
3) числу нейтронов в ядре
4) номеру периода
10. Число внешних электронов в атомах химических элементов главных подгрупп равно
1) порядковому номеру элемента
2) номеру группы
3) числу нейтронов в ядре
4) номеру периода
11. Два электрона находятся во внешнем электронном слое атомов каждого из химических элементов в ряду
1) He, Be, Ba
2) Mg, Si, O
3) C, Mg, Ca
4) Ba, Sr, B
12. Химический элемент, электронная формула которого 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 , образует оксид состава
13. Число электронных слоев и число p-электронов в атоме серы равно
1) 2, 6
2) 3, 4
3) 3, 16
4) 3, 10
14. Электронная конфигурация ns 2 np 4 соответствует атому
1) хлора
2) серы
3) магния
4) кремния
15. Валентные электроны атома натрия в основном состоянии находятся на энергетическом подуровне
1) 2s
2) 2p
3) 3s
4) 3p
16. Атомы азота и фосфора имеют
1) одинаковое число нейтронов
2) одинаковое число протонов
3) одинаковую конфигурацию внешнего электронного слоя
4) одинаковое число электронов
17. Одинаковое число валентных электронов имеют атомы кальция и
1) калия
2) алюминия
3) бериллия
4) бора
18. Атомы углерода и фтора имеют
1) одинаковое число нейтронов
2) одинаковое число протонов
3) одинаковое число электронных слоёв
4) одинаковое число электронов
19. У атома углерода в основном состоянии число неспаренных электронов равно
20. В атоме кислорода в основном состоянии число спаренных электронов равно
Построение структурно-электронной формулы элементов B-подгрупп
Элементы побочной подгруппы еще называют d-элементами или переходными металлами. Они отличаются тем, что их валентные электроны расположены не только на s-подуровне внешнего энергетического слоя, но и на d-подуровне предвнешнего слоя. Валентными электронами называют те, что способны участвовать в образовании химической связи.
Что бы построить модель атома такого элемента, нам необходимо знать одно важное отличие этих элементов от элементов А-подгрупп: если у элементов главных (А) подгрупп количество электронов на внешнем уровне определяется по номеру группы (например, у лития один электрон на внешнем слое, у бериллия – два, у бора – три и так далее), то у элементов побочных подгрупп это количество не зависит от номера группы.
Для определения количества электронов на внешнем уровне, легче всего просто запомнить несколько распространённых примеров (они выделены красным):
Количество электронов на внешнем уровне
Cu, Ag, Au, Nb, Cr, Mo, Ru, Rh, Pt, Ds
Все остальные элементы B-подгрупп, кроме палладия.
Остальные правила работают как с элементами А-подгрупп, так и с элементами Б-подгрупп. Например, заряд ядра определяется по порядковому номеру элемента, количество энергетических уровней по расположению в определенном периоде.
Рассмотрим конфигурацию нескольких элементов побочных подгрупп:
На рисунке показано, что несмотря на положение элементов в определенных подгруппах, количество электронов у них не равно этой группе.
Для сравнения изучим еще один рисунок, на котором мы можем сравнить элементы А- и Б-подгрупп одной и той же группы:
На этом рисунке мы снова можем убедиться, что элементы, находящиеся в одной и той же группе. В одном и том же периоде, но в разных подгруппах имеют разное строение.
Что бы разобраться, почему эти элементы называются d-элементами, разберем структурно-электронные формулы некоторых из них, например, хрома, железа и марганца, строение которых описывалось выше. Как уже было сказано, у этих элементов валентными являются не только внешний. Но и предвнешний уровень.
3s 2 3p 6 3d 5 4s 1
3s 2 3p 6 3d 6 4s 2
3s 2 3p 6 3d 5 4s 2
d-орбиталь содержит неспаренные электроны, которые могут вступать в химическую связь. Поэтому высшая валентность хрома равна не двум (по количеству электронов на внешнем уровне), а шести – по общему количеству электронов внешнего энергетического уровня и d-электронов предвнешнего уровня.
Вы можете встретить немного измененный порядок заполнения орбиталей, например, у марганца: 3s 2 3p 6 4s 2 3d 5 . s- и d-подуровень поменялись местами, в таких формулах учтен уровень энергии орбиталей: чем меньшей энергией обладает орбиталь, тем быстрее она будет заполняться электронами.
Правильнее будет заполнять электроны в следующем порядке:
1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p…
Тренировочные задания ЕГЭ
Задание 1.
Для выполнения заданий 1 – 3 используйте следующий ряд химических элементов:
Ответом в заданиях 1 – 3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
Определите, атомы каких из указанных элементов имеют электронную конфигурацию внешнего энергетического уровня ns 2 (n-1) d 10
Решение задания:
Для начала разберемся со страшной формулой ns 2 (n-1) d 10 . Попробуем заменить переменную n на любое число, например, на 4, тогда мы получим 4s 2 (4-1)d 10 или 4s 2 3d 10 . Эта формула отображает порядок распределения электронов согласно их энергии. Если для нас такой порядок непривычен, то мы можем поменять его местами, тогда получим 3d 10 4s 2 . Получившаяся формула приблизительна, вместо нее может быть 4d 10 5s 2 или 5d 10 6s 2 , но по этой формуле мы понимаем, что должны искать элемент с двумя электронами на внешнем энергетическом уровне (это приводит к тому, что медь выбывает из списка претендентов на правильный ответ), и элемент должен иметь d-орбиталь на внешнем уровне (кальций и стронций выпадают)
Верный ответ: 23
Задание 2.
Определите, атомы каких из указанных в ряду элементов не имеют на внешнем энергетическом уровне неспаренных электронов.
Решение: построим электронные конфигурации данных атомов.
Сурьма – Sb, элемент главной подгруппы пятой группы (А), у таких элементов валентные электроны находятся только на внешнем слое: 5s 2 5p 3 , что соответствует структурно-электронной формуле:
Элемент имеет три неспаренных p-электрона.
Последовательность расположения электронов на энергетических уровнях выражается следующим рядом чисел:
Распределение электронов по подуровням. Разбор первого задания ЕГЭ.
Напомню, что любой энергетический уровень можно разделить на орбитали (подуровни) – области вокруг ядра, в которых с наибольшей вероятностью встречаются определенные электроны. Их распределение не случайно, а согласованно с их энергией.
Для начала, определим максимальное количество электронов на подуровнях:
Каждый уровень начинается с s-подуровня, далее, если количество электронов достаточно большое, заполняется p-подуровень, затем d- и f-орбитали.
Для лучшего понимания распределения электронов начните с построения планетарной модели атома. Рассмотрим на примере брома.
Начинаем запись структуры электронной оболочки атома с обозначения номера уровня, к которому принадлежат электроны (на рисунке обозначено красной стрелкой).
Затем называем подуровень (s, p, d, f).
Определяем количество электронов на этом уровне (зеленая стрелка на рисунке).
На первом уровне всего два электрона, оба поместились на s-подуровне, раз больше электронов на внутренней оболочке нет, может приступить с следующим уровням по тому же алгоритму:
Электронно-структурная формула брома может быть записана двумя распространенными методами
Способ 1. Каждый последующий уровень имеет большую энергию и записывается выше:
Способ 2. Более компактный, заключается в записи электронов каждого уровня с новой строки:
По электронно-структурной формуле легко понять, что у брома на внешнем уровне есть один неспаренный р-электрон и ему, до завершения внешнего энергетического уровня, не хватает одного электрона.
Попробуем применить полученные знания в решении первых заданий ЕГЭ по химии:
Задание 1: определите, атомы каких из указанных в ряду элементов имеют три неспаренных электрона в основном состоянии.
Решение: у элементов А-подгрупп неспаренные электроны могут находиться только на внешнем уровне, поэтому далее будем рассматривать только его.
Верный ответ: 14
Обратите внимание на электронно-структурную формулу фтора и мышьяка. Их внешний энергетический уровень можно было записать и другим, к сожалению, неверным способом:
Всё, потому что есть еще одно правило, которым нужно пользоваться при построении структуры атома – правило Гунда (Хунда), которое определяет порядок заполнения электронами внутри орбитали таким образом, чтобы было заполнено как можно больше ячеек.
Рассмотрим еще одно задание:
Задание 2: определите, атомам каких из указанных элементов до завершения внешнего энергетического уровня не хватает одного электрона.
Решение: для решения данного задания нет необходимости составлять структурные формулы, достаточно знать, что большинства элементов на внешнем уровне наиболее выгодным количеством электронов будет восемь (легко запомнить, так как количество электронов на внешнем уровне определяется по номеру группы, всего групп в ПС восемь, значит, максимум электронов на внешнем слое тоже восемь).
Таким образом, калий, находящийся в первой группе, имеет всего один электрон на внешнем уровне, до завершения внешней электронной оболочки ему не хватает целых семь электронов.
Фтор – элемент седьмой подгруппы, у него семь электронов на внешнем уровне, до «идеальной» оболочки ему не хватает одного электрона. Это первый правильный ответ.
Литий, как и калий относится к первой группе. Ему не хватает целых семь электронов.
Хлор, как же как и фтор, относится к седьмой группе, ему не хватает одного электрона до восьмиэлектронного внешнего энергетического уровня. Это наш второй верный ответ.
Алюминий – элемент третьей группы. До завершения внешнего слоя ему не хватает пять электронов.
Верный ответ: 24
Таким образом всем элементам IА-подгруппы не хватает семи электронов, IIА – шести, IIIА – пяти, IVА – четырех и так далее. Это может вам заметно сэкономить время на экзамене.
Решение задания ЕГЭ химия
Задание 3: определите, атомам каких из указанных элементов до завершения внешнего энергетического уровня не хватает трёх электронов.
Решение: исходя из вышенаписанного, трех электронов до завершения внешнего энергетического уровня может не хватать элементам пятой группы Периодической системы. Это мышьяк и висмут.
Число электронов на внешнем электронном уровне атома металла
I. Периодическая система химических элементов Д. И. Менделеева
Основные понятия:
1. Порядковый номер химического элемента - номер, данный элементу при его нумерации. Показывает общее число электронов в атоме и число протонов в ядре, определяет заряд ядра атома данного химического элемента.
2. Период – химические элементы, расположенные в строчку (периодов всего 7). Период определяет количество энергетических уровней в атоме.
Малые периоды (1 – 3) включают только s- и p- элементы (элементы главных подгрупп) и состоят из одной строчки; большие (4 – 7) включают не только s- и p- элементы (элементы главных подгрупп), но и d- и f- элементы (элементы побочных подгрупп) и состоят из двух строчек.
3. Группы – химические элементы, расположенные в столбик (групп всего 8). Группа определяет количество электронов внешнего уровня для элементов главных подгрупп, а так же число валентных электронов в атоме химического элемента.
Главная подгруппа (А) – включает элементы больших и малых периодов (только s- и p- элементы).
Побочная подгруппа (В) – включает элементы только больших периодов (только d- или f- элементы).
4. Относительная атомная масса (Ar) – показывает, во сколько раз данный атом тяжелее 1/12 части атома 12 С, это безразмерная величина (для расчётов берут округлённое значение).
5. Изотопы – разновидность атомов одного и того же химического элемента, отличающиеся друг от друга только своей массой, с одинаковым порядковым номером.
II. Строение атома
1. Электронное облако – это модель квантовой механики, описывающая движение электрона в атоме.
2. Орбиталь (s, p, d, f) – часть атомного пространства, в котором вероятность нахождения данного электрона наибольшая (~ 90%).
3. Энергетический уровень – это энергетический слой с определённым уровнем энергии находящихся на нём электронов.
Число энергетических уровней в атоме химического элемента равно номеру периода, в котором этот элемент расположен.
4. Максимально возможное число электронов на данном энергетическом уровне определяется по формуле:
N = 2n 2 , где n – номер периода
5. Распределение орбиталей по уровням представлено схемой:

6. Химический элемент – это вид атомов с определённым зарядом ядра.
Частица
Заряд
Масса
8. Состав атомного ядра:
В состав ядра входят элементарные частицы – протоны (p) и нейтроны (n).
Т.к. практически вся масса атома сосредоточена в ядре, то округлённое значение Arхимического элемента равно сумме протонов и нейтронов в ядре.
9. Общее число электронов в электронной оболочке атома равно числу протонов в ядре и порядковому номеру химического элемента.
Порядок заполнения уровней и подуровней электронами
1. Электронные формулы атомов химических элементов составляют в следующем порядке:
- Сначала по номеру элемента в таблице Д. И. Менделеева определяют общее число электронов в атоме;
- Затем по номеру периода, в котором расположен элемент, определяют число энергетических уровней;
- Уровни разбивают на подуровни и орбитали, и заполняют их электронами в соответствии Принципом наименьшей энергии
- Для удобства электроны можно распределить по энергетическим уровням, воспользовавшись формулой N=2n 2 и с учётом того, что:
- у элементов главных подгрупп (s-;p-элементы) число электронов на внешнем уровне равно номеру группы.
- у элементов побочных подгрупп на внешнем уровне обычно два электрона (исключение составляют атомы Cu, Ag, Au, Cr, Nb, Mo, Ru, Rh, у которых на внешнем уровне один электрон, у Pd на внешнем уровне ноль электронов);
- число электронов на предпоследнем уровне равно общему числу электронов в атоме минус число электронов на всех остальных уровнях.
2. Порядок заполнения электронами атомных орбиталей определяется :
1.Принципом наименьшей энергии
Шкала энергий:
2. Состояние атома с полностью или наполовину заполненным подуровнем (т. е. когда на каждой орбитали имеется по одному неспаренному электрону) является более устойчивым.
Этим объясняется «провал» электрона. Так, устойчивому состоянию атома хрома соответствует следующее распределение электронов:
Cr: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 3d 5 , ане 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 4 ,
т. е. происходит «провал» электрона с 4s-подуровня на 3d-подуровень.
3. Семейства химических элементов.
- Элементы, в атомах которых происходит заполнение электронами s-подуровня внешнего энергетического уровня, называются s-элементами. Это первые 2 элемента каждого периода, составляющие главные подгруппы I иII групп.
- Элементы, в атомах которых электронами заполняется p-подуровень внешнего энергетического уровня, называются p-элементами. Это последние 6 элементов каждого периода (за исключением Iи VII), составляющие главные подгруппы III-VIII групп.
- Элементы, в которых заполняется d-подуровень второго снаружи уровня, называются d-элементами. Это элементы вставных декад IV, V, VI периодов.
- Элементы, в которых заполняется f-подуровень третьего снаружи уровня, называются f-элементами. К f-элементам относятся лантаноиды и актиноиды.
III. Периодический закон Д. И. Менделеева
1 марта 1869г. Формулировка периодического закона Д.И. Менделеева.
Свойства простых веществ, а также формы и свойства соединений элементов находятся в периодической зависимости от величины атомных весов элементов.
Современная формулировка периодического закона.
Свойства химических элементов и их соединений находятся в периодической зависимости от величины заряда ядер их атомов, выражающейся в периодической повторяемости структуры внешней валентной электронной оболочки.
Основные положения
1. В периоде слева направо:
1) Относительная атомная масса – увеличивается
2) Заряд ядра – увеличивается
3) Количество энергоуровней – постоянно
4) Количество электронов на внешнем уровне - увеличивается
5) Радиус атомов – уменьшается
6) Электроотрицательность – увеличивается
Следовательно, внешние электроны удерживаются сильнее, и металлические (восстановительные) свойства ослабевают, а неметаллические (окислительные) усиливаются.
2. В группе, в главной подгруппе сверху вниз:
2) Число электронов на внешнем уровне – постоянно
3) Заряд ядра – увеличивается
4) Количество энергоуровней – увеличивается
5) Радиус атомов - увеличивается
6) Электроотрицательность – уменьшается.
Следовательно, внешние электроны удерживаются слабее, и металлические (восстановительные) свойства элементов усиливаются, неметаллические (окислительные) - ослабевают.
3. Изменение свойств летучих водородных соединений:
1) В группах главных подгруппах с ростом заряда ядра прочность летучих водородных соединений уменьшается, а кислотные свойства их водных растворов усиливаются (основные свойства уменьшаются).
2) В периодах слева направо кислотные свойства летучих водородных соединений в водных растворах усиливаются (основные уменьшаются), а прочность уменьшается.
3) В группах с ростом заряда ядра в главных подгруппах валентность элемента в летучих водородных соединениях не изменяется, в периодах слева направо уменьшается от IV до I.
4. Изменение свойств высших оксидов и соответствующих им гидроксидов (кислородсодержащие кислоты неметаллов и основания металлов):
1) В периодах слева направо свойства высших оксидов и соответствующих им гидроксидов изменяются от основных через амфотерные к кислотным.
2) Кислотные свойства высших оксидов и соответствующих им гидроксидов с ростом заряда ядра в периоде усиливаются, основные уменьшаются, прочность уменьшается;
3) В группах главных подгруппах у высших оксидов и соответствующих им гидроксидов с ростом заряда ядра прочность растёт, кислотные свойства уменьшаются, основные усиливаются;
4) В группах с ростом заряда ядра в главных подгруппах валентность элемента в высших оксидах не изменяется, в периодах слева направо увеличивается от I до VIII.
5. Завершенность внешнего уровня – если на внешнем уровне атома 8 электронов (для водорода и гелия 2 электрона)
6. Металлические свойства – способность атома отдавать электроны до завершения внешнего уровня.
7. Неметаллические свойства - способность атома принимать электроны до завершения внешнего уровня.
8. Электроотрицательность – способность атома в молекуле притягивать к себе электроны
9. Семейства элементов:
10. Радиус атома – расстояние от ядра атома до внешнего уровня
IV. Задания для закрепления
№1. Решите задания теста
1. Чему равен заряд ядра атома натрия?
1) 0; 2) +11; 3) +1; 4) +23.
2. Сколько электронов в атоме азота?
1) 0; 2) 1; 3) 7; 4) 14.
3. Сколько нейтронов в атоме углерода C?
1) 0; 2) 12; 3) 6; 4) 7.
4. Укажите атом, в котором больше всего электронов:
1) H; 2) Al; 3) Ar; 4) K.
5. Сколько электронов содержится в молекуле CO2?
1) 6; 2) 12; 3) 8; 4) 22.
6. На внешнем энергитическом уровне элементов главных подгрупп число электронов:
2) равно номеру периода;
3) равно номеру группы;
7. Элементу 2-го периода до завершения внешнего уровня не хватает 3 электронов. Это элемент-…
1) бор; 2) углерод; 3) азот; 4) фосфор.
1) 3d 7 ; 2) 2s 2 2p 5 ; 3) 3s 2 3p 5 ; 4) 3s 2 4d 5 .
9. Формула высшего оксида некоторого элемента – ЭО3. Какую конфигурацию валентных электронов может иметь этот элемент в основном состоянии?
1) 4d 6 ; 2) 2s 2 2p 4 ; 3) 3s 2 3p 4 ; 4) 3s 1 3d 5 .
10. Строение внешнего и предвнешнего электронных слоёв атома меди
1) 3s 2 3p 6 3d 9 4s 2 ;
2) 3s 2 3p 6 3d 10 4s 0 ;
3) 3s 2 3p 6 4s 1 3d 10 ;
4) 3s 2 3p 6 3d 11 .
11. Относительная атомная масса хлора
1) 36; 2) 35; 3) 35,5; 4) 35,4
12. Менее яркие чем у кальция металлические свойства выражены у
1) калия; 2) радия; 3) франция; 4) алюминия
13. В ряду Al - Si - Cl увеличиваются
1) Металлические свойства,
2) Неметаллические свойства,
4) Способность отдавать электроны
Задание №2:
Используя таблицу, изучите закономерности изменения свойств элементов в периоде.
Читайте также:
