Что тяжелее стекло или металл
Обновлено: 21.09.2024
Смотря какое железо. Химически чистое железо мягкий металл, не оставляющий царапин на стекле. А вот легированное примесями железо может быть и тверже стекла.
Обычно стекло тверже железа, но оно слишком хрупкое.
Конечно стекло! Железо можно железным гвоздем поцарапать, а вот со стеклом такого не выйдет. Стеклорез потребуется.
Вспомните фильм - "Хозяин Красных гор" -- Вот нож. Сам ковал из руды. Стекло режет! - Да не смеши! - Смотри. (и порезал стекло на столе).
Ну, гвоздем выцарапать свои инициалы на окне вам вряд ли удастся. А вот осколком бутылки на дверце соседской машины - запросто. Так что.
Тут вопрос плотности и толщины изделия. В одной ситуации может быть твёрже стекло, в другой - железо.
Стекло лишь в очень незначительной степени пропускает ультрафиолетовые лучи. Солнечного света, проходящего через оконные стекла, достаточно для роста растений, но недостаточно для того, чтобы человек загорел. Поэтому для того, чтобы загореть, рекомендуется открывать окна, чтобы солнышко светило прямо на кожу человека.
Сейчас, ранней весной, я иногда загораю таким образом. У меня окна выходят на юго-восточную сторону, поэтому днем, ближе к обеду, я иногда открываю окно, чтобы хоть немного загорели лицо, руки и ноги. Даже если кожа и не успеет загореть, то свою порцию ультрафиолета для стимулирования синтеза витамина D в организме она уж точно получит. Когда станет теплее, можно и в купальнике загорать таким образом, но сейчас в комнате прохладно становится, если полностью открыть окно.
Со стекла морилка легко удаляется обычной тёплой водой.
Можно добавить в воду немного нашатырного спирта или аммиака. Морилка, это не краска, она даже при высыхании водорастворимая, если конечно не покрыта лаком сверху.
Можно попробовать водой с уксусом, тоже как вариант рассматривается.

Паста зелёного цвета "ГОИ" была разработана специально для полировки стеклянных поверхностей в Государственном Оптическом Институте, поэтому и получила такое название. Этой пастой техники полируют глазные протезы из стекла, когда глазное яблоко удалено. Поэтому для удаления мелких повреждений на стекле она отлично подходит.
Абразивом в этой пасте является трёхвалентный оксид хрома, который и придаёт ей зелёный цвет. Кроме этого в ней содержатся органические связующие, активирующие и интенсифицирующие добавки. В зависимости от % содержания этого оксида выпускается бледно - зелёная паста, самая грубая, дающая на стекле матовую поверхность, зелёная - средней грубости, тёмно - зелёная и чёрная, имеющая зеленоватый отлив, которой делают тонкую доводку и придают стеклу зеркальный блеск.
Паста подходит также для обработки металлов - стали, золота, керамики, полимеров и пластмассы.
И та и другая хороша в своей, если так выразиться, области. Нержавейка не вредит здоровью - стекло тоже. Но, допустим, нержавейку в микроволновку не поставишь. Результат - здесь лучше для использования стекло. Но стекло довольно хрупко, и не всегда подходит для готовки на той же плите. Здесь явное преимущество нержавейки, как металла.
Бывает, в Китае все бывает и даже стеклянный мост.)
Его называют "Воздушная тропа", находится в провинции Хунань, он соединяет две горы Тянь-Шань и Тянь-Мэнь. Полностью стеклянный, что пол, что боковины.
Расположен на высоте 1430 метров, длина его 61 метр, а ширина 1.5 метра. Стекло естественно очень крепкое, выдерживает до тонны на квадратный метр.
Что удивительно, посетителей пускают на него только в бахилах.
Говорят, что на него приезжал Камерон перед съемками "Аватара", так что вот откуда Пандора.)
Ещё в Китае есть мост в долине Пиньян. Он находится на высоте 180 метров, его длина 300 метров. Пол в три слоя прочного стекла 36 мм. Выдерживает диапазон температур до 60°C и ветер скоростью до 220км/ч.

Ещё есть стеклянный мост в Тбилиси ( Грузия).
Мост через Куру, его длина 156 метров. Сделан по итальянскому проекту. Он пешеходный. Назвали его "Мост Мира". В нем смонтировано 30000 лампочек.
14 различных типов металлов

Термин "металл" происходит от греческого слова "metalléuō", что означает выкапываю или добываю из земли. Наша планета содержит много металла. На самом деле из 118 элементов периодической системы порядка 95 являются металлами.
Это число не является точным, потому что граница между металлами и неметаллами довольно расплывчата: нет стандартного определения металлоида, как нет и полного согласия относительно элементов, соответствующим образом классифицированных как таковые.
Сегодня мы используем различные виды металлов, даже не замечая их. Начиная с зажимов в сантехнике и заканчивая устройством, которое вы используете для чтения этой статьи, все они сделаны из определенных металлов. Фактически, некоторые металлические элементы необходимы для биологических функций, таких как приток кислорода и передача нервных импульсов. Некоторые из них также широко используются в медицине в виде антацидов.
Все металлы в периодической таблице можно классифицировать по их химическим или физическим свойствам. Ниже мы перечислили некоторые различные типы металлов вместе с их реальным применением.
Классификация по физическим свойствам
14. Легкие металлы

Сплав титана 6AL-4V
Примеры: Алюминий, титан, магний
Легкие металлы имеют относительно низкую плотность. Формального определения или критериев для идентификации этих металлов нет, но твердые элементы с плотностью ниже 5 г/см³ обычно считаются легкими металлами.
Металлургия легких металлов была впервые развита в середине 19 века. Хотя большинство из них происходит естественным путем, значительная их часть образуется при электротермии и электролизе плавленых солей.
Их сплавы широко используются в авиационной промышленности благодаря их низкой плотности и достаточным механическим свойствам. Например, сплав титана 6AL-4V составляет почти 50 процентов всех сплавов, используемых в авиастроении. Он используется для изготовления роторов, лопастей компрессоров, мотогондол, компонентов гидравлических систем.
13. Тяжелые металлы

Окисленные свинцовые конкреции и кубик размером 1 см3
Примеры: железо, медь, кобальт, галлий, олово, золото, платина.
Тяжелые металлы - это элементы с относительно высокой плотностью (обычно более 5 г/см³) и атомным весом. Они, как правило, менее реактивны и содержат гораздо меньше растворимых сульфидов и гидроксидов, чем более легкие металлы.
Эти металлы редки в земной коре, но они присутствуют в различных аспектах современной жизни. Они используются в солнечных батареях, сотовых телефонах, транспортных средствах, антисептиках и ускорителях частиц.
Тяжелые металлы часто смешиваются в окружающей среде из-за промышленной деятельности, ухудшая качество почвы, воды и воздуха, а затем вызывая проблемы со здоровьем у животных и растений. Выбросы транспортных средств, горнодобывающие и промышленные отходы, удобрения, свинцово-кислотные батареи и микропластики, плавающие в океанах, являются одними из наиболее распространенных источников тяжелых металлов в этом контексте.
12. Белый металл

Подшипники из белого металла
Примеры: Обычно изготавливается из олова, свинца, висмута, сурьмы, кадмия, цинка.
Белые металлы - это различные светлые сплавы, используемые в качестве основы для украшений или изделий из серебра. Например, многие сплавы на основе олова или свинца используются в ювелирных изделиях и подшипниках.
Белый металлический сплав изготавливается путем объединения определенных металлов в фиксированных пропорциях в соответствии с требованиями конечного продукта. Основной металл для ювелирных изделий, например, формуется, охлаждается, экстрагируется, а затем полируется, чтобы придать ему точную форму и блестящий вид.
Они также используются для изготовления тяжелых подшипников общего назначения, подшипников внутреннего сгорания среднего размера и электрических машин.
11. Хрупкий металл

Хрупкое разрушение чугуна
Примеры: сплавы углеродистой стали, чугуна и инструментальной стали.
Металл считается хрупким, если он твердый, но не может противостоять ударам или вибрации под нагрузкой. Такие металлы под воздействием напряжения ломаются без заметной пластической деформации. Они имеют низкую прочность на разрыв и часто издают щелкающий звук при поломке.
Многие стальные сплавы становятся хрупкими при низких температурах, в зависимости от их обработки и состава. Чугун, например, твердый, но хрупкий из-за высокого содержания углерода. Напротив, керамика и стекло гораздо более хрупки, чем металлы, из-за их ионных связей.
Галлий, висмут, хром, марганец и бериллий также хрупки. Они часто используются в различных гражданских и военных целях, связанных с высокими деформационными нагрузками. Чугун, устойчивый к повреждениям в результате окисления, используется в машинах, трубах и деталях автомобильной промышленности, таких как корпуса коробок передач и головки цилиндров.
10. Тугоплавкий металл
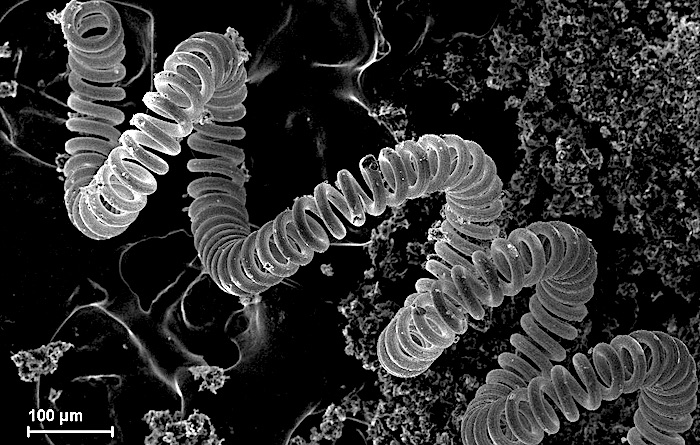
Микроскопическое изображение вольфрамовой нити в лампе накаливания
Примеры: молибден, вольфрам, тантал, рений, ниобий.
Тугоплавкие металлы имеют чрезвычайно высокие температуры плавления (более 2000 °С) и устойчивы к износу, деформации и коррозии. Они являются хорошими проводниками тепла и электричества и имеют высокую плотность.
Другой ключевой характеристикой является их термостойкость: они не расширяются и не растрескиваются при многократном нагревании и охлаждении. Однако они могут деформироваться при высоких нагрузках и окисляться при высоких температурах.
Благодаря своей прочности и твердости они идеально подходят для сверления и резки. Карбиды и сплавы тугоплавких металлов используются почти во всех отраслях промышленности, включая горнодобывающую, автомобильную, аэрокосмическую, химическую и ядерную.
Металлический вольфрам, например, используется в ламповых нитях. Сплавы рения используются в гироскопах и ядерных реакторах. А ниобиевые сплавы используются для форсунок жидкостных ракетных двигателей.
9. Черные и цветные металлы

Валы-шестерни из (черной) нержавеющей стали
Черные металлы: Сталь, чугун, сплавы железа.
Цветные металлы: Медь, алюминий, свинец, цинк, серебро, золото.
Термин "железо" происходит от латинского слова "Ferrum", что переводится как "железо". Таким образом, термин "черный металл" обычно означает "содержащий железо", тогда как "цветной металл" означает металлы и сплавы, которые не содержат достаточного количества железа.
Поскольку черные металлы могут иметь широкий спектр легирующих элементов, которые значительно изменяют их характеристики, очень трудно поместить свойства всех черных металлов под один зонт. Тем не менее некоторые обобщения могут быть сделаны, например, большинство черных металлов являются твердыми и магнитными.
Черные металлы используются для применения с высокой нагрузкой и низкой скоростью, в то время как цветные металлы предпочтительны для применения с высокой скоростью и нулевой нагрузкой для применения с низкой нагрузкой.
Сталь является наиболее распространенным черным металлом. Она составляет около 80% всего металлического материала благодаря своей доступности, высокой прочности, низкой стоимости, простоте изготовления и широкому спектру свойств. Она широко используется в строительстве и обрабатывающей промышленности. Фактически, рост производства стали показывает общее развитие промышленного мира.
8. Цветные и благородные металлы

Ассортимент благородных металлов
Цветные металлы: медь, алюминий, олово, никель, цинк
Благородные металлы: родий, ртуть, серебро, рутений, осмий, иридий
Цветные металлы - это обычные и недорогие металлы, которые корродируют, окисляются или тускнеют быстрее, чем другие металлы, когда подвергаются воздействию воздуха или влаги. Они в изобилии встречаются в природе и легко добываются.
Они широко используются в промышленных и коммерческих целях и имеют неоценимое значение для мировой экономики благодаря своей полезности и повсеместности. Некоторые цветные металлы обладают отличительными характеристиками, которые не могут быть продублированы другими металлами. Например, цинк используется для гальванизации стали, чтобы защитить ее от коррозии, а никель - для изготовления нержавеющей стали.
Благородные металлы, с другой стороны, устойчивы к окислению и коррозии во влажном воздухе. Согласно атомной физике, благородные металлы имеют заполненный электрон d-диапазона. В соответствии с этим строгим определением, медь, серебро и золото являются благородными металлами.
Они находят применение в таких областях, как орнамент, металлургия и высокие технологии. Их точное использование варьируется от одного элемента к другому. Некоторые благородные металлы, такие как родий, используются в качестве катализаторов в химической и автомобильной промышленности.
7. Драгоценные металлы

Родий: 1 грамм порошка, 1 грамм прессованного цилиндра и 1 г аргонодуговой переплавленной гранулы
Примеры: палладий, золото, платина, серебро, родий.
Драгоценные металлы считаются редкими и имеют высокую экономическую ценность. Химически они менее реакционноспособны, чем большинство элементов (включая благородные металлы). Они также пластичны и имеют высокий блеск.
Несколько веков назад эти металлы использовались в качестве валюты. Но сейчас они в основном рассматриваются как промышленные товары и инвестиции. Многие инвесторы покупают драгоценные металлы (в основном золото), чтобы диверсифицировать свои портфели или победить инфляцию.
Серебро - второй по популярности драгоценный металл для ювелирных изделий (после золота). Однако его значение выходит далеко за рамки красоты. Оно обладает исключительно высокой тепло- и электропроводностью и чрезвычайно низким контактным сопротивлением. Именно поэтому серебро широко используется в электронике, батареях и противомикробных препаратах.
Классификация по химическим свойствам
6. Щелочные металлы

Твердый металлический натрий
Примеры: натрий, калий, рубидий, литий, цезий и франций.
Щелочь относится к основной природе гидроксидов металлов. Когда эти металлы реагируют с водой, они образуют сильные основания, которые легко нейтрализуют кислоты.
Они настолько реактивны, что обычно встречаются в природе в слиянии с другими веществами. Карналлит (хлорид калия-магния) и сильвин (хлорид калия), например, растворимы в воде и, таким образом, легко извлекаются и очищаются. Нерастворимые в воде щелочи, такие, как фторид лития, также существуют в земной коре.
Одно из самых популярных применений щелочных металлов - использование цезия и рубидия в атомных часах, наиболее точных из известных эталонов времени и частоты. Литий используется в качестве анода в литиевых батареях, композиты калия используются в качестве удобрений, а ионы рубидия используются в фиолетовых фейерверках. Чистый металлический натрий широко используется в натриевых лампах, которые очень эффективно излучают свет.
5. Щелочноземельные металлы

Изумрудный кристалл, основной минерал бериллия.
Примеры: бериллий, кальций, магний, барий, стронций и радий.
Щелочноземельные металлы в стандартных условиях мягкие и серебристо-белые. Они имеют низкую плотность, температуру кипения и температуру плавления. Хотя они не так реакционноспособны, как щелочные металлы, они очень легко образуют связи с элементами. Как правило, они вступают в реакцию с галогенами, образуя галогениды щелочноземельных металлов.
Все они встречаются в земной коре, кроме радия, который является радиоактивным элементом. Радий уже распадался в ранней истории Земли из-за относительно короткого периода полураспада (1600 лет). Современные образцы поступают из цепочки распада урана и тория.
Щелочноземельные металлы имеют широкий спектр применения. Бериллий, например, используется в полупроводниках, теплопроводниках, электрических изоляторах и в военных целях. Магний часто сплавляют с цинком или алюминием для получения материалов со специфическими свойствами. Кальций в основном используется в качестве восстановителя, а барий используется в вакуумных трубках для удаления газов.
4. Переходные металлы
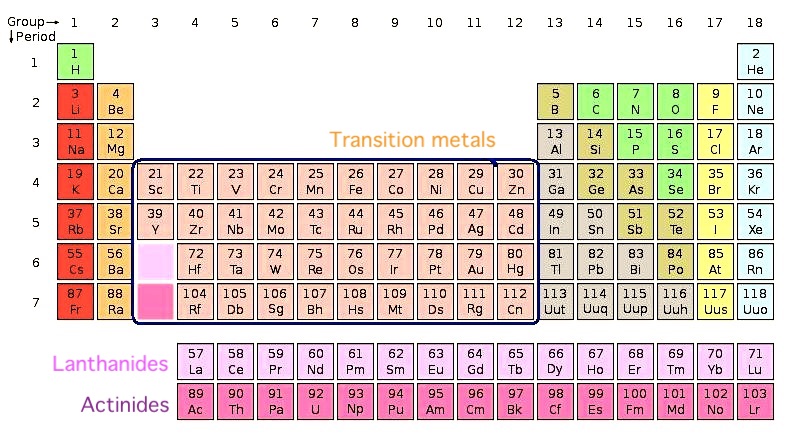
Примеры: титан, ванадий, хром, никель, серебро, вольфрам, платина, кобальт.
Большинство элементов используют электроны из своей внешней оболочки для связи с другими элементами. Переходные металлы, однако, могут использовать две крайние оболочки для соединения с другими элементами. Это химическая особенность, которая позволяет им связываться со многими различными элементами в различных формах.
Они занимают среднюю часть таблицы Менделеева, служа мостом между (или переходом) между двумя сторонами таблицы. Более конкретно, есть 38 переходных металлов в группах с 3 по 12 периодической таблицы. Все они являются пластичными, податливыми и хорошими проводниками тепла и электричества.
Многие из этих металлов, такие как медь, никель, железо и титан, используются в конструкциях и в электронике. Большинство из них образуют полезные сплавы друг с другом и с другими металлическими веществами. Некоторые из них, включая золото, серебро и платину, называются благородными металлами, потому что они крайне инертны и устойчивы к кислотам.
3. Постпереходные металлы

Висмут в виде синтетических кристаллов
Примеры: алюминий, галлий, олово, свинец, таллий, индий, висмут.
Постпереходные металлы в периодической таблице - это элементы, расположенные справа от переходных металлов и слева от металлоидов. Из-за своих свойств они также называются "бедными" или "другими" металлами.
Физически они хрупки (или мягки) и имеют более низкую температуру плавления и механическую прочность, чем переходные металлы. Их кристаллическая структура довольно сложна: они проявляют ковалентные или направленные эффекты связи.
Различные металлы этого семейства имеют различное применение. Алюминий, например, используется для изготовления оконных рам, кухонной посуды, банок, фольги, деталей автомобилей. Оловянные сплавы используются в мягких припоях, оловянных и сверхпроводящих магнитах.
Индиевые сплавы используются для изготовления плоских дисплеев и сенсорных экранов, а галлий - в топливных элементах и полупроводниках.
2. Лантаноиды

1-сантиметровый кусок чистого лантана
Примеры: лантан, церий, прометий, гадолиний, тербий, иттербий, лютеций.
Лантаноиды - это редкоземельные металлы с атомными номерами от 57 до 71. Впервые они были обнаружены в 1787 году в необычном черном минерале (гадолините), обнаруженном в Иттербю, Швеция. Позже минерал был разделен на различные элементы лантаноидов.
Лантаноиды - это металлы с высокой плотностью, плотность которых колеблется от 6,1 до 9,8 г/см³, и они, как правило, имеют очень высокие температуры кипения (1200-3500 °C) и очень высокие температуры плавления (800-1600 °C).
Сплавы лантаноидов используются в металлургии из-за их сильных восстановительных способностей. Около 15 000 тонн лантаноидов ежегодно расходуется в качестве катализаторов и при производстве стекол. Они также широко используются в лазерах и оптических усилителях.
Некоторые исследования показывают, что лантаноиды могут быть использованы в качестве противораковых средств. Лантан и церий, в частности, могут подавлять пролиферацию раковых клеток и способствовать цитотоксичности.
1. Актиниды

Металлический уран, высокообогащенный ураном-235
Примеры: актиний, уран, торий, плутоний, фермий, нобелий, лоренций
Подобно лантаноидам, актиниды образуют семейство редкоземельных элементов с аналогичными свойствами. Они представляют собой серию из 15 последовательных химических элементов в периодической системе от атомных номеров 89 до 103.
Все они радиоактивны по своей природе. Синтетически произведенный плутоний, а также природные уран и торий являются наиболее распространенными актинидами на Земле. Первым актинидом, который был открыт в 1789 году, был уран. И большая часть существующих продуктов актинидов была произведена в 20 веке.
Их свойства, такие как излучение радиоактивности, пирофорность, токсичность и ядерная критичность, делают их опасными для обращения. Сегодня значительная часть (кратковременных) актинидов производится ускорителями частиц в исследовательских целях.
Некоторые актиниды нашли применение в повседневной жизни, например, газовые баллоны (торий) и детекторы дыма (америций), большинство из них используются в качестве топлива в ядерных реакторах и для изготовления ядерного оружия. Уран-235 является наиболее важным изотопом для применения в ядерной энергетике, который широко используется в тепловых реакторах.
Стеклянный vs каменный — лучше, хуже или равно?
Тема со стеклом в петербургском «Лахта центре» весьма любопытна, хотя бы потому, что стекло выполняет в башне функцию стен. Значит, должно защищать от внешней среды и быть устойчивым к деструктивному воздействию как минимум не хуже, чем традиционные материалы. Но можно ли сказать, что за фасадом «Лахта центра» — как за каменной стеной?

Вопрос не праздный. Ведь все мы с детства знаем, как печально заканчиваются истории про домики, где стены сделаны из неправильных материалов…
Разберемся!
Архитекторы небоскребов часто делают выбор в пользу стеклянных фасадов. Потому что это:
B. Фасад из стекла легче, чем из традиционных материалов. Хотя вес сопоставимых объемов стекла и тяжелого бетона примерно равен, стеклянного материала нужно меньше для возведения стен одной квадратуры.
С. Стекло отвечает всем необходимым требованиям, предъявляемым к стенам – по прочности, теплоизоляции, защите от разнообразных внешних воздействий. Об этом и поговорим ниже. Итак,
Нужно ли быть крепким орешком, чтобы разбить фасад башни
В прошлом посте была отдельная дискуссия относительно прочности стеклянного фасада небоскреба. Где-то на интуитивном уровне понятно, что фасады в башне должны быть надежны, но жизненный опыт одновременно подсказывает, что стекло – все же непрочный материал. Даже лобовое на автомобиле может повредиться из-за разности температур или попадания камня. Чего уж говорить про стеклянную стену – к ней просто страшно прислониться, особенно – где-нибудь на 87 этаже.

Визуализация панорамы с верхнего этажа «Лахта центра». Вы бы подошли вплотную к стеклу?
Тем не менее, обсуждаемый случай – как раз тот, когда жизненный опыт ошибочен. Подобно тому, что земля все же круглая, самолет летает, не размахивая при этом крыльями, современное фасадное стекло с достоинством выдерживает попадание в него камня, температурный шок и при повреждении не дает осколков, нарушая тем самым привычное, добытое путем опытных наблюдений, представление о мире.
Более того — сегодня инженеры используют стекло как конструктивный элемент, то есть, в качестве несущих структур. Первое здание с конструктивом из стекла было построено еще в прошлом веке — в 1951. Сейчас светопрозрачные крыши со стеклянными балками и арками имеют здание Народного банка в Ганновере, столовая Технологического университета в Дрездене, стеклянные колонны, каждая из которых обладает несущей способностью в 6 тонн — под крышей внутреннего двора здания городского управления в Сен-Жермен-ан-Ле.

Крыша со стеклянными арками — здание Volksbank (Ганновер) Фото отсюда. Пять арок с шагом в 2,5 м, склеены из 3 листов стекла. Стальные полосы — «страховка» от обрушения в случае отказа балки. Подробнее почитать о стеклянном конструктиве можно, например, тут
В качестве еще одного наглядного доказательства надежности стекла приведу пример вот такого страшного, но безопасного аттракциона:

Обзорная площадка на 103 этаже Willis Tower, Чикаго. Выполнена полностью из стекла. За посетительницу можно не переживать – пол под ней имеет толщину почти 4 см., балкон выдерживает нагрузку в 5 тонн.
Фасадное стекло в петербургском «Лахта центре» даже немного толще – 4,15 см. Расчетная нагрузка на фасады – 400 кг. на кв. м. Это примерно так:
Смог бы разбить его Брюс Уиллис?
Скорее всего, нет. А вот Майк Тайссон, с ударом в 800 кг вполне бы справился.

Если вы – не Майк, то можете не только смело прислоняться к такому фасаду, но даже слегка постучать по нему стулом — как в кино не получится.
Майк разбил стекло. Что дальше?
Ничего страшного не произойдет.
Во-первых, стеклянный фасад хоть и является стеной, несущей «роли» не играет. Можно разбить сколько угодно стекол — это никак не отразится на устойчивости конструкций башни, где несущие нагрузки распределены между железобетонным ядром и колоннами.
Во-вторых, стекло, предназначенное для фасадов «Лахта центра» (и для фасадов других небоскребов), является безопасным – при повреждении оно не дает крупных или острых осколков. Оно вообще не дает осколков – вместо этого на нем образуются вмятины или трещины. Поврежденный стеклопакет в таком «помятом», но механически целостном виде дожидается своей замены.
Так происходит потому, что стекло состоит из слоев, одним из которых является пленка.
Эта технология называется Triplex и, думаем, известна читателям. Например, она применяется для изготовления лобовых автомобильных стекол.

След от попадания камня на стекле Triplex
Формула стекла и альтернативная реальность
Стекла для фасадов «Лахта центра» изготовлены по многослойной формуле: стекло 8мм + 1,5 мм пленка + 8мм стекло + 16мм аргона + 8 мм стекло, итого — 4,15 см толщины.

Толщину стекол можно оценить по реберной части листов
Особенность внешнего слоя стекла — термоотражающие свойства. Для защиты от избытка солнечной радиации (пусть такое допущение странно звучит для климатических условий Северной столицы), на стекло нанесено специальное напыление. Оно, кстати, и придает фасадному покрытию «металлический», холодный серо-голубой оттенок.

Внутренний слой стекла — каленый. Каленое стекло — это второй вид особо прочного и, при этом, безопасного стекла, которое не дает острых или крупных осколков при повреждении.
Аргоновая прослойка применяется в целях повышения энергоэффективности.
Теплопроводность этого газа приблизительно в 1,5 раза ниже, чем у воздуха (0,68 от теплопроводности воздуха). Хотя цифра не столь велика, но она становится весьма существенной в масштабах площади остекления здания – 72, 5 тыс. кв.м.
Есть и другие приятные «мелочи» — например, большая вязкость благородного газа, уменьшающие скорость конвекции, а, следовательно, теплообмена между слоями стекла.
Благодаря многослойности и аргоновой прослойке, пакет в «Лахта центре» однокамерный и нитка остекления одиночная, за исключением некоторых особых участков, о которых будет рассказано позже. Вес стеклянной части фасада составляет около 13 тыс. тонн. В случае многокамерных стеклопакетных решений вес бы существенно увеличился. Это, в свою очередь, повлияло бы на конструктивные параметры – вероятно, мы бы не увидели башню такой, какой она строится сейчас.

Подопытный
Испытания герметичности фасадов — на площадке компании Gartner (Германия). С помощью различных приборов испытатели будут имитировать разные типы сильного дождя и их воздействие на стеклопакеты.

Лабораторный участок, где проводилась проливка. Обратите внимание на легкие металлические леса. За ними расположен натурный макет фасада — несколько стеклопакетов в форме параллелограмма.

Тестирование началось. Стеклопакет поливают струей воды под сильным давлением. Вода поступает из вот таких спринклеров:

Спринклер не одиночный. То, что выглядело как леса, на самом деле — многочисленные ряды спринклеров:

В ходе эксперимента выявлен побочный эффект — радуга):
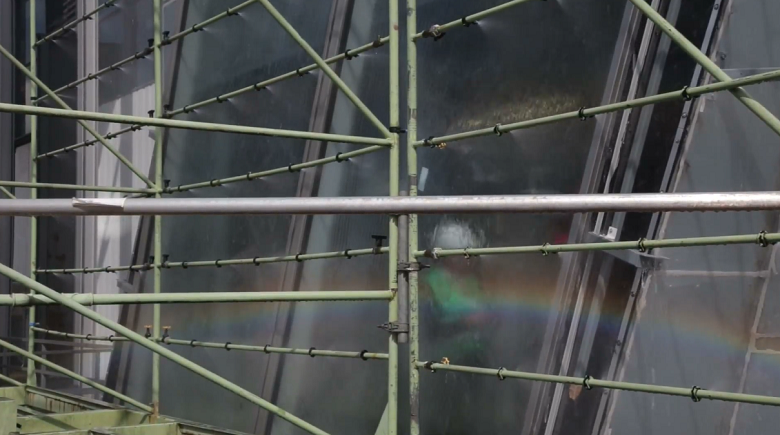
По эту сторону стекла — просто потоп:

Но этого мало. Ведь что такое «дождь» без «ветра»? В бой идет вот такая установка:

Она добавит ураганного ветра:

Теперь за фасадом бушует целый шторм:

С противоположной стороны испытатели, сухие до нитки, в отличие от их коллег снаружи, собирают показатели и фиксируют реакцию фасада на разные «погодные» условия, устойчивость стеклопакета к различным типам дождя, герметичность «обшивки» натурной модели.

А вот другая серия испытаний — огнем. Тут стеклопакет будут поджигать. Натурные огневые испытания проводятся в поверхностном бетонном бункере, одна из стен которого заменена подопытным стеклом, на котором закреплены датчики:

В ходе первой части будут тестировать реакцию стекла на пожар при работающей системе пожаротушения. Внутри помещения все готово к поджогу:

Защищать фасад будут вот эти спринклеры:


Уже через несколько минут внутри бетонной кабины бушует огонь…

И вода… Спринклеры работают — на фото можно увидеть скопление влаги на раме:


Вторая часть испытаний — для подтверждения предела термостойкости стекол. Тут систему пожаротушения выключают и фиксируют максимальные температуры, при которых стекло сохраняет свою целостность, а также — другие свойства без необратимых изменений:

Свыше 600 градусов — хороший показатель. Примерно такой же — у специализированного каминного стекла.
Наконец, еще одно натурное моделирование было проведено для того чтобы оценить эстетические свойства фасада. Сегодня на площадке для моделирования, которая расположена рядом со стройкой, не протолкнуться — там и сетки, и образцы тротуарных покрытий, и варианты оболочки планетария… Но вот этот макет:

… появился на площадке самым первым, почти полтора года назад. В него вставлялись и менялись разные образцы стекол. Группа проектировщиков наблюдала за тем, как выглядит стекло и как оно себя ведет в разных погодных условиях, в разные сезоны и время суток — и днем, и ночью.
Благодаря напылению и тому, что стекло на фасадах — «просветленное», т.е. с минимально возможным содержание «желтящего» оксида железа (менее 0,015 против обычных 0,6-0,8), башня при разном освещении выглядит в холодной гамме. Оттенки зависят от освещенности. Например, днем при ярком солнце и отражении неба — стекла синие:

В пасмурную погоду грани фасада могут выглядеть как серые и бронзовые:

На расцвете и закате в ясную малооблачную погоду наблюдатели могут застать еще один необычный оттенок — красно-фиолетовый:

И все же большую часть времени башня — серо-синего цвета, органично сливающегося с нашим северным небом и гладью холодного Финского залива.
Все эти серии испытаний — на огонь, воду и красоту, подтвердили соответствие фасадных конструкций заданным проектным параметрам.
Как видите, стеклянные фасады могут быть прочными, безопасными, теплыми и красивыми стенами. Наше мнение — лучше камня.

В следующем посте расскажем о том, как достигается эстетический эффект остекления без граней, и как монтируют фасады башни.
7 самых тяжелых элементов на Земле | По атомной массе

Мы должны быть более конкретными, когда говорим о том, насколько тяжелый элемент. Есть два возможных способа определения «самых тяжелых» элементов - на основе их плотности или атомной массы.
Самый тяжелый элемент с точки зрения плотности можно определить как массу на единицу объема, которая обычно измеряется в граммах на кубический сантиметр или килограммах на кубический метр.
Самым плотным природным элементом на Земле является осмий. Это блестящее вещество имеет плотность 22,59 г / см3, чуть больше, чем у иридия.
Другой способ взглянуть на тяжесть - это атомный вес, средняя масса атомов элемента. Стандартная единица атомной массы составляет одну двенадцатую от массы одного атома углерода-12.
Это фундаментальное понятие в химии, потому что большинство химических реакций происходит в соответствии с простыми числовыми соотношениями между атомами. Ниже мы перечислили 7 самых тяжелых элементов, найденных на Земле в соответствии с их атомными массами.
Примечание: мы не упомянули элементы, свойства которых неизвестны или еще не подтверждены, такие, как московия, флеровия, нихония и мейтнерия.
7. Резерфордий

Атомная масса: 267
Резерфордий (Rf) был первым сверхтяжелым элементом, который был обнаружен [в 1964 году]. Он очень радиоактивен, и его самый стабильный изотоп 267Rf имеет период полураспада около 78 минут.
Ожидается, что этот элемент будет твердым при нормальных условиях и предположительно будет иметь химические свойства, подобные гафнию. Он был создан только в незначительных количествах и используется только для научных исследований.
6. Дубний

Атомная масса: 268
Дубний (Db) - радиоактивный элемент, впервые синтезированный в 1968 году в Объединенном институте ядерных исследований, Россия. Он имеет семь признанных изотопов, из которых наиболее стабильным является 268Db с периодом полураспада 32 часа.
Дубний можно получить бомбардировкой калифорния-249 азотом или америция-243 неоном. Ограниченный анализ химии Дубния подтвердил, что этот элемент ведет себя больше как ниобий, а не тантал, нарушая периодические тенденции.
Поскольку элемент не найден в природе свободным и не создан в больших количествах в лаборатории, у него нет других применений, кроме научных исследований.
5. Сиборгиум

Атомная масса: 269
Seaborgium (Sg) был впервые синтезирован в 1974 году в лаборатории Лоуренса в Беркли, штат Калифорния. Исследовательская группа подвергла бомбардировке калифорний-249 ядрами кислорода-18 для получения сиборгия-263.
Это радиоактивный элемент, чей самый стабильный изотоп (269Sg) имеет период полураспада около 14 минут. Только несколько атомов сиборгия когда-либо были произведены, и его использование исключительно для научных исследований.
Небольшое исследование, проведенное на этом синтетическом химическом элементе, указывает на то, что сиборгий является плотным тяжелым металлом в нормальных условиях.
В 2014 году японские исследователи впервые установили химическую связь между атомом углерода и сиборгием, открывая новые двери для анализа влияния относительности Эйнштейна на структуру периодической таблицы.
4. Борий

Атомная масса: 270
Bohrium (Bh) - это искусственно созданный радиоактивный элемент, названный в честь известного физика Нильса Бора. Он синтезируется путем бомбардировки висмута ионами хрома.
Поскольку он очень быстро разлагается за счет испускания альфа-частиц (период полураспада 270Bh составляет 61 секунду), изучать этот элемент очень сложно.
Борий не встречается в природе, и только несколько атомов были получены до настоящего времени. Возможно, он никогда не будет изолирован в наблюдаемых количествах.
3. Хассий
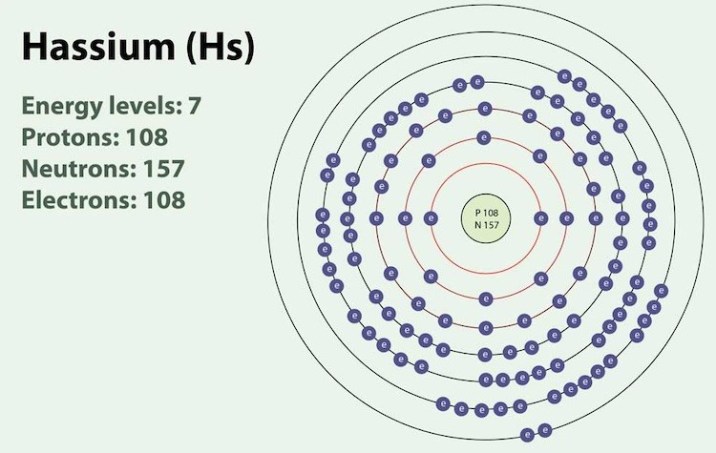
Атомная масса: 270
Обнаруженный немецкими физиками в 1984 году, калий (Hs) является одним из самых тяжелых и плотных элементов периодической таблицы. Все 9 изотопов элемента имеют очень короткие периоды полураспада: самый стабильный (270Hs) имеет период полураспада 10 секунд.
Пока что получено всего несколько атомов хасция. Таким образом, его свойства еще не известны. Хотя точная температура плавления, температура кипения и плотность не подтверждены, элемент считается твердым при комнатной температуре.
Этот радиоактивный переходный металл может реагировать с другими элементами [своей группы], если он производится в больших количествах. На данный момент он не имеет коммерческого использования, кроме научных исследований.
2. Tennessine

Атомная масса: 294
Tennessine (Ts) является вторым наиболее тяжелым известным элементом, обнаруженным российско-американским коллаборацией в 2010 году. Это радиоактивный, искусственно произведенный элемент. Хотя его классификация неизвестна, ожидается, что он будет надежным.
Теннессин был получен реакцией синтеза кальция-48 с берклием-249. Во всех проведенных экспериментах его атомы длились десятки и сотни миллисекунд.
Использование tennessine ограничено исследовательскими целями из-за его незначительного производства. Его самый стабильный изотоп (294Ts) имеет период полураспада около 80 миллисекунд, который распадается из-за альфа-распада.
1. Оганесон

Впервые синтезированный в 2002 году, Oganesson (Og) - самый тяжелый элемент периодической таблицы. Этот высокорадиоактивный элемент является членом группы благородных газов. Удивительно, но это первый благородный газ, который химически реактивен.
С 2005 года было идентифицировано только 6 атомов Oganesson. Он проявляет очень необычные физические и химические свойства, большинство из которых еще недостаточно изучены.
Поскольку Oganesson очень нестабилен (с периодом полураспада около 0,89 миллисекунд) и не происходит естественным путем, почти нет причин для рассмотрения его опасности для здоровья.
Тяжелый элемент природного происхождения: Уран

Урановое стекло светится под ультрафиолетовым светом | Предоставлено: Wikimedia Commons.
Атомная масса: 238,0289
На протяжении более 6 десятилетий уран (U) использовался в качестве богатого источника концентрированной энергии. Это самый тяжелый элемент в земной коре, он встречается в 500 раз чаще, чем золото, и в 40 раз чаще, чем серебро.
Хотя уран является радиоактивным элементом, скорость его распада значительно ниже, чем у других элементов, связанных с радиоактивностью. Его наиболее естественная форма (уран-238) имеет период полураспада около 4,5 миллиарда лет.
Уран в основном используется в качестве ядерного топлива для производства электроэнергии на атомных электростанциях. Один килограмм урана-235 может генерировать около 80 тераджоулей энергии, что эквивалентно энергии, генерируемой 3000 тонн угля.
Это чрезвычайно токсичный элемент: прием соединений шестивалентного урана может привести к повреждению иммунной системы и врожденным дефектам.
Читайте также:
